SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Ilmu Farmasi
Oleh :
Rocha Ifahyana Siagian NIM : 068114106
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
ii SKRIPSI
Presented as partitial fulfilment of the requirement To obtain Sarjana Farmasi (S.Farm)
In Faculty of Pharmacy
By :
Rocha Ifahyana Siagian NIM : 068114106
FACULTY OF PHARMACY SANATA DHARMA UNIVERSITY
v
”Ketika kumohon kekuatan, Allah memberiku
kesulitan agar aku menjadi kuat”
”Ketika kumohon kebijaksanaan,
Allah memberiku masalah untuk kupecahkan”
”Ketika kumohon kesejahteraan, Allah memberikan
aku akal untuk berpikir”
”Ketika kumohon keberanian, Allah memberiku
kondisi bahaya untuk kuatasi”
”K etika kumohon sebuah cinta, A llah memberiku orang-orang bermasalah untuk kutolong”
”Ketika kumohon bantuan,
Allah memberiku kesempatan”
” Aku tidak pernah menerima apa yang kupinta, tetapi aku menerima
segala yang kubutuhkan” (Mazmur)
Kupersembahkan karyaku ini untuk : Tuhan Yesusku, Bapa yang selalu menopangku saat ku tak mampu dan mengangkatku saat kuterjatuh serta memberiku kekuatan. Papi dan mamiku untuk segala doa, cinta dan perhatiannya. Kakak-kakakku dan adikku yang selalu memberikan semangat.
vii
kepada penulis, sehingga penulis dapat menyelesaikan skripsi yang berjudul ”Ketoksikan Akut Sari Wortel (Daucus carota L.) Kajian terhadap Histologi Ginjal dan Kadar Kreatinin serta Ureum Serum pada Tikus Betina Galur Wistar” sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi (S. Farm) di Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
Kesuksesan penyusunan ini tidak lepas dari dukungan dan bantuan dari banyak pihak, baik berupa materiil, moral, tenaga, maupun doa. Penulis mengucapkan terima kasih kepada :
1. Bapak Yosef Wijoyo, M.Si., Apt. selaku dosen pembimbing yang telah menyediakan waktu dan tenaga untuk memberikan bimbingan, masukan, dan perhatiannya yang besar serta saran dalam penyusunan skripsi ini.
2. Ibu Phebe Hendra, Msi., PhD., Apt. selaku dosen penguji skripsi yang telah menyediakan waktu untuk memberikan saran dan masukan demi kesempurnaan skripsi ini.
3. Bapak Ipang Djunarko, S.Si., Apt. selaku dosen penguji skripsi yang telah menyediakan waktu untuk memberikan saran dan masukan demi kesempurnaan skripsi ini.
viii
6. Ibu Prof. Drh. Kurniasih, MVSc., PhD. selaku dosen yang mengamati hasil pemeriksaan histopatologi organ ginjal dari penelitian ini.
7. Para karyawan dan laboran Laboratorium Farmakologi-Toksikologi (Pak Heru, Pak Parjiman, dan Mas Kayat), yang telah banyak membantu selama penelitian ini.
8. Kedua orang tuaku yaitu Bapak Haden Siagian dan Ibu Murniati Sitorus yang telah memberikan kasih sayang yang besar dan memberikan dukungan dalam doa dan perhatian sehingga skripsi ini dapat terselesaikan.
9. Saudara-saudara kandungku yaitu kakak Yenny, abang Denny, kakak Putri, adikku Nina, dan adikku Indra, serta seluruh keluarga besarku atas semua perhatian, dukungan, serta doa yang tiada hentinya selama penelitian dan penyusunan skripsi ini.
10. Abang Renyus, sebagai kekasih saya yang turut memberikan dukungan dan perhatian, sehingga saya dapat menyelesaikan penelitian ini dengan baik. 11. Kakak mitra yang memberikan semangat setiap hari melalui alat komunikasi
sehingga saya dapat menyelesaikan skripsi ini.
12. Abang Kris yang memberikan dukungan dengan meminjamkan printer sehingga dapat terselesaikan skripsi ini.
xi
tertentu, yang terjadi dalam waktu 24 jam setelah pemberiannya pada dosis tunggal. Penelitian ini bertujuan untuk menetapkan potensi toksisitas akut berdasarkan harga LD50, menilai gejala toksik, spektrum efek toksik yang timbul,
dan pengaruh dosis pemberian sari wortel (Daucus carota L.) terhadap wujud efek toksik yang ditimbulkan ditinjau dari histologi ginjal dan parameter biokimia seperti kadar kreatinin dan ureum serum.
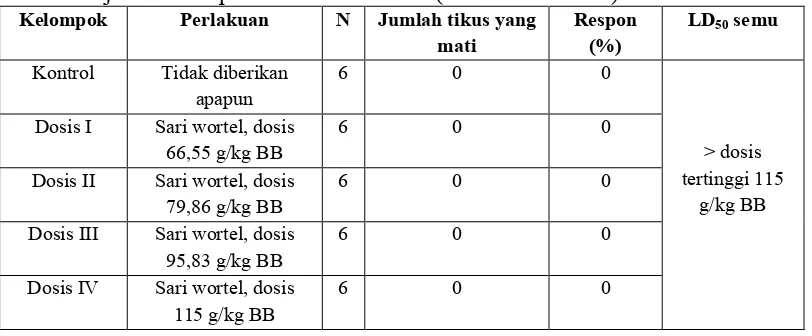
Penelitian ini merupakan jenis penelitian eksperimental murni acak lengkap pola searah. Penelitian ini menggunakan 30 subyek uji. Hewan uji dibagi dalam 5 kelompok yang terdiri dari kelompok kontrol dan kelompok perlakuan. Tiap kelompok terdiri atas 6 ekor hewan uji. Kelompok I adalah kelompok kontrol yang tidak diberikan perlakuan apapun, kelompok II sampai V adalah kelompok yang diberikan sari wortel sekali pemejanan dengan dosis masing-masing 66,55 g/kg BB; 79,86 g/kgBB; 95,83 g/kg BB; 115 g/kg BB. Analisis statistik menggunakan Shapiro-Wilk, Uji One-Way ANOVA, General Linear Model
Multivariate, serta Paired T-Test.
Berdasarkan hasil yang diperoleh menunjukkan bahwa pemberian sari wortel tidak menunjukkan gejala efek toksik. Potensi ketoksikan akut sari wortel pada tikus betina galur Wistar yang diperoleh berupa harga LD50 semu yaitu >115
g/kg BB. Berdasarkan analisis histopatologi organ ginjal menunjukkan bahwa tidak ada kerusakan jaringan ginjal. Selain itu, berdasarkan analisis statistik menunjukkan tidak ada pengaruh pemberian sari wortel terhadap kadar kreatinin dan ureum serum pada waktu 24 jam dan hari ke-14 setelah pemberian sari wortel mulai dari dosis 66,55 g/kg BB hingga 115 g/kg BB.
xii
animal, that happens in 24 for hours after the giving on a sole dosage. This research aims to establish acute toxical potency based on LD50 value, to estimate
toxic symptom, emerged toxical effect spectrum, and the dosage effect of giving carrot juice (Daucus carota L.) to the emerged toxical effect shape, observed from kidney histology and biochemistry parameter i.e. kreatinin degree and ureum serum.
This is such a same-direction system complete random pure experimental research, that uses 30 experimental subjects. The experiment animals are divided into 5 groups, consisted of control group and treatment group. Every group consists of 6 experimental animals. The first group is the group in which no treatment is given, while the second until the fifth group are the groups given carrot juice for every exposure with 66,55 g/kg BB; 79,86 g/kg BB; 95,83 g/kg BB; 115 g/kg BB dosage per each. The statistical analysis uses Shapiro-Wilk,
One-Way ANOVA examination, General Linear Model Multivariate, and Paired
T-Test.
Based on result retrieved, it is shown that the giving of carrot juice does not point out the toxic effect symptom. The potential gotten of the carrot juice acute toxicant of strain Wistar female rats is mien LD50, i.e. >115 g/kg BB. By
reffering to the kidney organ histopatology analysis, it is shown that there is no kidney network damage. Besides, based on the analysis, the statistic shows that there is no effect of the giving the carrot juice of kreatinin and serum ureum degree in 24 hours and the 14th day after carrot juice is exposured starting from 66,55 g/kg BB to 115 g/kg BB dosage.
xiii
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN ... iv
HALAMAN PERSEMBAHAN ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI ... vi
PRAKATA ... vii
PERNYATAAN KEASLIAN PENELITIAN ... x
INTISARI ... xi
ABSTRACT... xii
DAFTAR ISI ... xiii
DAFTAR TABEL ... xviii
DAFTAR GAMBAR ... xxi
DAFTAR LAMPIRAN ... xxiv
BAB I. PENGANTAR A. Latar Belakang ... 1
1. Permasalahan ... 3
2. Keaslian penelitian ... 4
3. Manfaat penelitian ... 7
B. Tujuan Penelitian ... 8
1. Tujuan umum ... 8
xiv
2. Morfologi ... 10
3. Kandungan kimia ... 11
4. Kegunaan di masyarakat ... 12
B. Beta Karoten ... 12
C. Toksikologi ... 15
1. Definisi toksikologi ... 15
2. Asas umum toksikologi ... 16
a. Kondisi efek toksik ... 16
b. Mekanisme efek toksik ... 17
c. Wujud efek toksik ... 18
d. Sifat efek toksik ... 19
3. Jenis uji toksikologi ... 20
a. Uji ketoksikan tak khas ... 20
b. Uji ketoksikan khas ... 21
D. Uji Toksisitas Akut ... 21
E. Median Lethal Dosage(LD50) ... 23
xv
3. Nefropati tubulus distal ... 29
H. Kreatinin dan Ureum Serum ... 29
1. Kreatinin serum ... 29
2. Ureum serum ... 30
I. Landasan Teori ... 31
J. Hipotesis ... 32
BAB III. METODE PENELITIAN A. Jenis dan Rancangan Penelitian ... 33
B. Variabel dan Definisi Operasional ... 33
1. Variabel utama ... 33
2. Variabel pengacau ... 34
3. Definisi Operasional ... 35
C. Alat dan Bahan Penelitian ... 36
1. Alat ... 36
2. Bahan ... 36
D. Tata Cara Penelitian ... 37
1. Penyiapan hewan uji ... 37
2. Pengelompokkan hewan uji ... 37
3. Pengumpulan bahan ... 38
xvi
8. Uji toksisitas ... 41
9. Pengambilan darah dan pemeriksaan kadar kreatinin dan ureum serum ... 42
a. Pengambilan darah sebelum pemejanan sari wortel ... 42
b. Pengambilan darah setelah pemejanan sari wortel ... 43
10. Pembuatan dan pemeriksaan preparat histopatologi ... 43
E. Tata Cara Analisis Hasil ... 44
BAB IV. HASIL DAN PEMBAHASAN A. Determinasi Tanaman ... 46
B. Jalan Penelitian ... 46
C. Uji Toksisitas Akut ... 48
D. Pengamatan Makroskopis dan Mikroskopis Organ Ginjal ... 50
E. Pemeriksaan Kadar Kreatinin dan Ureum Serum ... 58
1. Pemeriksaan kadar kreatinin serum ... 60
2. Pemeriksaan kadar ureum serum ... 66
F. Analisis Berat Organ Ginjal Relatif ... 73
G. Analisis Berat Badan ... 77
xvii
DAFTAR PUSTAKA ... 89
LAMPIRAN ... 94
xviii
Tabel II. Hasil pengamatan secara kualitatif gejala-gejala efek toksik
tikus betina galur Wistar pada kelompok kontrol dan
kelompok perlakuan pemberian sari wortel selama waktu
pengamatan mulai dari 3 jam setelah pemberian sari wortel
hingga hari ke-14 ... 48
Tabel III. Jumlah kematian tikus betina galur Wistar pada waktu
pengamatan 24 jam setelah pemberian sari wortel (Daucus
carota L.) ... 49
Tabel IV. Hasil pemeriksaan histopatologi organ ginjal tikus betina
galur Wistarakibat pemberian sari wortel 1x dengan waktu
pengamatan 24 jam setelah pemejanan ... 52
Tabel V. Hasil pemeriksaan histopatologi organ ginjal tikus betina
galur Wistarakibat pemberian sari wortel 1x dengan waktu
pengamatan pada hari ke-14 setelah pemejanan ... 54
Tabel VI. Purata kadar kreatinin serum ± SE tikus betina galur Wistar
sebelum pemberian sari wortel (Daucus carotaL.) ... 61
Tabel VII. Purata kadar kreatinin serum ± SE tikus betina galur Wistar
pada waktu 24 jam setelah pemberian sari wortel (Daucus
xix
Tabel IX. Purata kadar kreatinin serum ± SE tikus betina galur Wistar
pada waktu pengamatan hari ke-14 setelah pemejanan sari
wortel (Daucus carotaL.) ... 64
Tabel X. Purata kadar kreatinin serum ± SE pada tikus betina galur
Wistar sebelum pemberian sari wortel dan hari ke-14
setelah pemberian sari wortel (Daucus carotaL.) ... 65
Tabel XI. Purata kadar ureum serum ± SE pada tikus betina galur
Wistar pada waktu sebelum pemberian sari wortel (Daucus
carotaL.) ... 67
Tabel XII. Purata kadar ureum serum ± SE tikus betina galur Wistar
pada waktu 24 jam setelah pemberian sari wortel (Daucus
carotaL.) ... 67
Tabel XIII. Purata kadar ureum serum ± SE pada tikus betina galur
Wistar sebelum pemberian sari wortel dan 24 jam setelah
pemberian sari wortel (Daucus carotaL.) ... 69
Tabel XIV. Purata kadar ureum serum ± SE tikus betina galur Wistar
pada hari ke-14 setelah pemberian sari wortel (Daucus
xx
Tabel XVI. Rata-rata berat organ ginjal relatif akibat 1x pemberian sari
wortel pada pengamatan 24 jam setelah pemejanan ... 75
Tabel XVII. Rata-rata berat organ ginjal relatif akibat 1x pemberian sari
wortel pada pengamatan hari ke-14 setelah pemejanan ... 75
Tabel XVIII. Rata-rata berat badan hari ke-0, ke-7, dan ke-14 tikus betina
galur Wistar akibat 1x pemberian sari wortel (Daucus
xxi
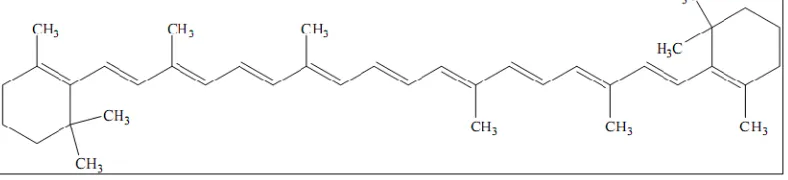
Gambar 1. Struktur kimia beta karoten ... ...13
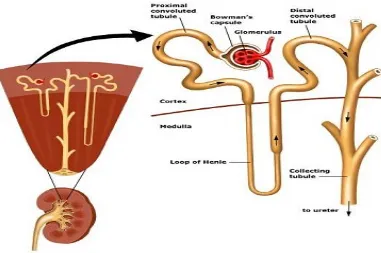
Gambar 2. Anatomi ginjal ... ...26
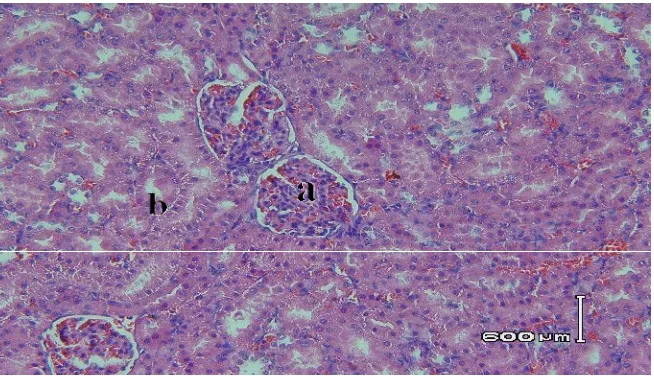
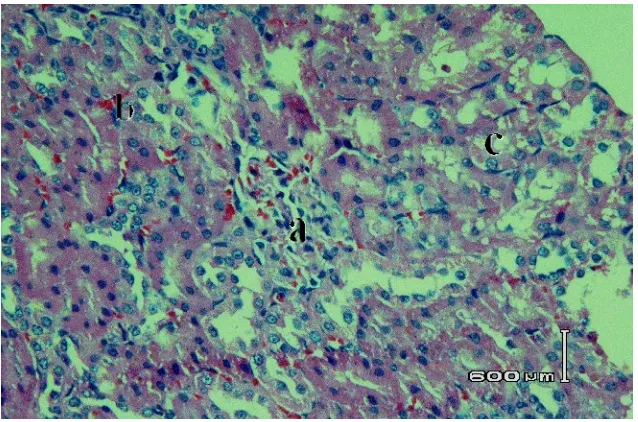
Gambar 3. Irisan melintang jaringan organ ginjal tikus betina galur
Wistar pada kelompok kontrol (tidak diberikan perlakuan
apapun) dengan perbesaran 200x menggunakan
pengecatan hematoksilin-eosin ...53
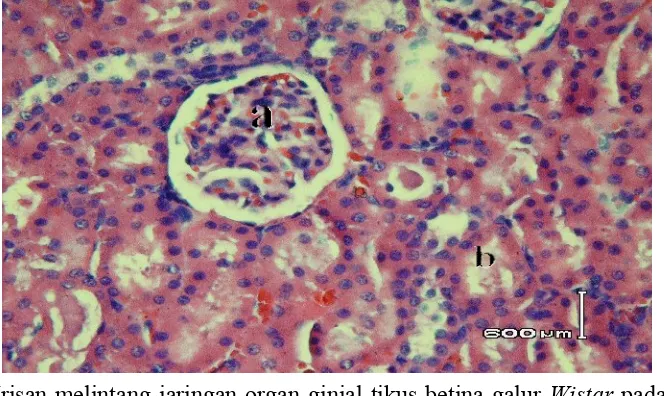
Gambar 4. Irisan melintang jaringan organ ginjal tikus betina galur
Wistar pada kelompok perlakuan yang diberikan sari
wortel (dosis 66,55 g/kg sampai 115 g/kg BB) dengan
perbesaran 200x menggunakan pengecatan
hematoksilin-eosin...53
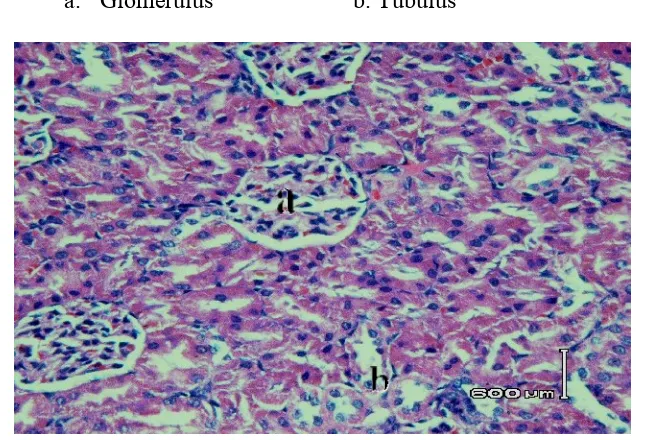
Gambar 5. Irisan melintang jaringan organ ginjal tikus betina galur
Wistar pada kelompok kontrol (tidak diberikan apapun)
dengan perbesaran 400x menggunakan pengecatan
hematoksilin-eosin...54
Gambar 6. Irisan melintang jaringan organ ginjal tikus betina galur
Wistar akibat pemberian sari wortel dosis 66,55 g/kg BB
dengan perbesaran 400x menggunakan pengecatan
xxii
hematoksilin-Eosin ...55
Gambar 8. Irisan melintang jaringan organ ginjal tikus betina galur
Wistar akibat pemberian sari wortel dosis 95,83 g/kg BB
dengan perbesaran 400x menggunakan pengecatan
hematoksilin-Eosin ...56
Gambar 9. Irisan melintang jaringan organ ginjal tikus betina galur
Wistar akibat pemberian sari wortel dosis 115 g/kg BB
dengan perbesaran 400x menggunakan pengecatan
hematoksilin-Eosin ...56
Gambar 10. Diagram batang purata kadar kreatinin serum sebelum
pemberian sari wortel dan 24 jam setelah pemberian sari
wortel (Daucus carotaL.) pada tikus betina galur Wistar...63
Gambar 11. Diagram batang purata kadar kreatinin serum sebelum
pemberian sari wortel dan hari ke-14 setelah pemberian
sari wortel (Daucus carota L.) pada tikus betina galur
Wistar...65
Gambar 12. Diagram batang purata kadar ureum serum sebelum
pemberian sari wortel dan 24 jam setelah pemberian sari
xxiii
Wistar...71
Gambar 14. Diagram persentase purata berat organ ginjal pada tikus
betina galur Wistar pada waktu 24 jam setelah pemberian
sari wortel (Daucus carota L.) ...75
Gambar 15. Diagram persentase purata berat organ ginjal pada tikus
betina galur Wistarpada hari ke-14 setelah pemberian sari
wortel (Daucus carotaL.) ... 76
Gambar 16. Grafik purata berat badan tikus betina galur Wistar pada
hari ke-0, 7, dan 14 hari setelah pembe-rian sari wortel
xxiv
Lampiran 2. Surat pembelian tikus putih betina galur Wistar sebanyak
30 ekor di LPPT, Universitas Gadjah Mada ... 95
Lampiran 3. Hasil pemeriksaan histopatolgi organ ginjal tikus betina
galur Wistar pada pengamatan 24 jam setelah pemberian
sari wortel ... 97
Lampiran 4. Hasil pemeriksaan histopatolgi organ ginjal tikus betina
galur Wistar pada pengamatan hari ke-14 setelah
pemberian sari wortel ... 98
Lampiran 5. Surat hasil pemeriksaan kadar kreatinin dan ureum serum
sebelum pemberian sari wortel yang dilakukan oleh
LPPT-UGM ... 99
Lampiran 6. Surat hasil pemeriksaan kadar kreatinin dan ureum serum
24 jam setelah pemberian sari wortel yang dilakukan oleh
LPPT-UGM ... 101
Lampiran 7. Surat hasil pemeriksaan kadar kreatinin dan ureum serum
14 hari setelah pemberian sari wortel yang dilakukan oleh
LPPT-UGM ... 102
Lampiran 8. Data penimbangan berat organ ginjal relatif tikus betina
xxv
Lampiran 11. Gambar umbi wortel ... 104
Lampiran 12. GambarJuice Extractor... 104
Lampiran 13. Tikus putih betina galurWistardan foto timbangan ... 104
Lampiran 14. Sari wortel yang diperoleh dengan menggunakan Juice
Extractor... 105
Lampiran 15. Sari wortel disaring menggunakan saringan teh biasa
(penyaringan 1) ... 105
Lampiran 16. Penyaringan sari wortel menggunakan kertas saring
(penyaringan 2) ... 106
Lampiran 17. Sari wortel yang diperoleh dari hasil penyaringan ke-2 ... 106
Lampiran 18. Pemberian sari wortel pada tikus betina galur Wistar... 107
Lampiran 19. Gambar makroskopis organ ginjal pada kelompok kontrol
dan perlakuan... 107
Lampiran 20. Data berat organ ginjal relatif ... 108
Lampiran 21. Data berat badan pada hari ke-0, ke-7, dan ke-14 ... 114
Lampiran 22. Data kadar kreatinin serum... 118
Lampiran 23. Data kadar ureum serum... 125
Lampiran 24. Perhitungan LD50sari wortel ke manusia ... 130
xxvi
kelompok perlakuan (dosis 66,55 g/kgBB sampai 115
1
A. Latar Belakang
Obat tradisional merupakan obat yang dibuat dari bahan atau paduan bahan-bahan yang diperoleh dari tanaman, hewan atau yang belum berupa zat murni dan digunakan secara turun-temurun (Soesilo, 1992). Pemanfaatan tanaman obat sebagai sumber obat tradisional telah banyak digunakan dan diupayakan adanya pemeliharaan atau peningkatan taraf kesehatan. Hal ini diduga karena bahan alami yang digunakan lebih aman dibandingkan obat-obat kimia atau sintetik. Selain itu, obat tradisional juga memiliki berbagai kelebihan yaitu mudah diperoleh, harga relatif murah karena bisa ditanam sendiri dan relatif tanpa efek samping (Muhlisah, 2003).
tradisional dibandingkan obat-obat kimia. Namun, tetap perlu hati-hati dalam menggunakan obat-obat tradisional karena penggunaan secara berlebihan (dosis berlebih) dapat bersifat toksik di dalam tubuh (Koeman, 1987). Dalam wortel terkandung senyawa beta karoten yang akan dikonversi oleh tubuh menjadi vitamin A (Rukmana, 1995). Vitamin A yang ditemukan dalam wortel dinamakan karotenoid provitamin A. Bila mengkonsumsi karotenoid provitamin A dalam dosis tinggi dapat menyebabkan hiperavitaminosis A yang dapat berlangsung akut maupun kronis (Pitojo, 2004). Selain itu, beta karoten dapat berperan sebagai prooksidan, dimana bila aktivitas prooksidan terjadi dalam sel normal maka dapat menyebabkan kerusakan oksidatif yang menekan integritas sel dan menginduksi transformasi neoplastik (Masotti, Casali, and Galeotti, 1988). Dengan demikian, perlu dilakukan uji praklinik pada obat-obat tradisional untuk dapat menentukan keamanan melalui uji toksisitas dan uji farmakologi (Anonim, 2000). Karena penelitian mengenai keamanan penggunaan wortel masih kurang terkait dengan uji toksisitas wortel, maka perlu dilakukan penelitian mengenai ketoksikan akut sari wortel (Daucus carota L.).
2006), sehingga peneliti tertarik ingin meneliti apakah sari wortel bersifat toksik terhadap organ ginjal dengan melihat adanya perubahan struktural (histopatologi) yang dilakukan secara mikroskopis, serta melakukan pemeriksaan terhadap kadar kreatinin dan ureum serum yang merupakan parameter biokimia untuk melihat adanya perubahan biokimia dalam tubuh setelah diberikan sari wortel. Dari hal diatas, maka peneliti melakukan penelitian tentang ketoksikan akut sari wortel (Daucus carotaL.) kajian terhadap histologi organ ginjal dan kadar kreatinin serta ureum serum pada tikus betina galur Wistar. Sepanjang pengetahuan peneliti, penelitian ini belum pernah dilakukan sebelumnya.
1. Permasalahan
Berdasarkan latar belakang di atas dapat dirumuskan permasalahan sebagai berikut:
a. Apa saja gejala ketoksikan yang timbul akibat pemejanan akut sari wortel (Daucus carota L.) pada tikus betina galur Wistar?
b. Berapa besar potensi ketoksikan akut sari wortel (Daucus carota L.) pada tikus betina galurWistaryang dinyatakan dengan Median Lethal Dosage(LD50)?
c. Apakah pemberian sari wortel (Daucus carota L.) dapat menyebabkan efek toksik ditinjau dari histopatologi organ ginjal?
2. Keaslian penelitian
Beberapa penelitian mengenai khasiat dan keamanan tanaman wortel adalah sebagai berikut :
a. The Potential Role of Daucus carota L. Aqueous and Methanolic Extracts on Inflammation and Gastric Ulcers in Rats (Wehbe, dkk., 2009).
Ekstrak aquadest dan metanol dari Daucus carota L. memberikan aktivitas antiinflamasi pada dosis dari 400 dan 140 mg/kgBB dengan masing-masing sebesar 90,9 dan 58,6%. Sedangkan pada inflamasi kronis, menunjukkan bahwa dengan dosis 400 dan 140 mg/kgBB memberikan aktivitas antiinflamasi sebesar 58 dan 44,1%. Ekstrak aquadest dan metanol Daucus carotaL. signifikan menunjukkan perlindungan terhadap ulkus lambung yang diinduksi etanol dengan rasio masing-masing 46,8 kuratif dan 68,7% dengan dosis 250 mg/kgBB.
b. Efek Analgesik Air Perasan Umbi Wortel (Daucus carotaL.) pada Mencit Putih Betina Galur Wistar(Putra, 2003).
c. Efek Hepatoprotektif Air Perasan Umbi Wortel (Daucus carota L.) Terhadap Mencit Jantan Terinduksi CCl4(Nuraeni, 2003).
Air perasan umbi wortel (Daucus carota L.) mempunyai efek hepatoprotektif terhadap mencit jantan terinduksi CCl4 dosis 3,92 ml/kgBB. Efek hepatoprotektif ditandai dengan menurunnya aktivitas GPT-serum dan menurunnya derajat kerusakan sel hati mencit akibat hepatotoksikan CCl4. Efek hepatoprotektif air perasan umbi wortel dosis 0,14; 0,392; 1,162; 3,50; 10,50 dan 31,50 ml/kgBB berturut-turut sebesar 10,53%; 12,83%; 18,87%; 28,26%; 35,70%; dan 77,12%. Dosis efektif (ED50) air perasan umbi wortel pada mencit 20 gram terinduksi CCl4 sebesar 12,189 ml/kgBB.
d. Purple Carrot (Daucus carota L.) Polyacetylenes Decrease Lipopolysaccharide-Induced Expression of Inflammatory Proteins in Macrophage and Endothelial Cells (Metzger, Barnes, dan Reed, 2008). Kandungan poliasetilen yang terdapat dalam wortel memiliki efek antiinflamasi yang tinggi yang ditunjukkan dengan sekresi protein IL-6 dan TNF- R turun menjadi 77 and 66% dalam sel endotelial dengan dosis pemberian 6,6 and 13,3 µg/mL dari fraksi LH-20. Poliasetilen diisolasi dan menurunkan NO dalam sel makrofag sebanyak 65% tanpa sitotoksik. e. Pengaruh Pemberian Wortel (Daucus carota L.) terhadap Jumlah Sel
limfosit meningkat secara signifikan (p=0,000, uji Posthoc) pada kelompok yang dipapar asap rokok (sel limfosit = 609 ± 30,65942 sel) dibanding kontrol negatif (sel limfosit 61,75 ± 6,60177 sel), dan menurun secara bermakna pada kelompok 250 mg/hari (p=0,011 dengan sel limfosit= 499,25 ± 40,72162 sel), kelompok 500 mg/hari (p=0,000 dengan sel limfosit = 237 ± 59,40258 sel, serta kelompok 750 mg/hari (p = 0,037 dengan sel limfosit = 440,75 ± 43,78261 sel) dibandingkan dengan kelompok kontrol positif.
f. Toksisitas Akut Sari Wortel (Daucus carota L.) Kajian terhadap Organ Lambung, Ginjal, Hati pada Mencit Putih Betina Galur Balb/c (Karlina, 2009).
LD50 semu yang diperoleh >16,7 ml/kgBB. Pemberian sari wortel menyebabkan perubahan sikap, beringas, dan takikardi. Hasil histopatologi menunjukkan radang pada organ lambung, dan ginjal yang bersifat terbalikkan, serta nekrosis pada organ hati (24 jam setelah pemberian). Peningkatan aktivitas SGPT terjadi secara bermakna melalui uji statistik dengan tingkat kepercayaan 95%, tetapi tidak menyebabkan peningkatan kadar kreatinin serum secara signifikan.
g. Pengaruh Pemberian Akut Jus Wortel (Daucus carota L.) pada Tikus Jantan Wistar : Kajian terhadap Organ Ginjal dan Kadar Kreatinin Serum (Thejo, 2009).
yang mati (LD50 semu > 8,750 g/kgBB). Efek toksik bersifat terbalikkan. Tidak ada perbedaan signifikan antara kadar kreatinin serum perlakuan jus wortel dengan kontrol negatif. Kadar kreatinin serum pada penelitian ini tidak berkorelasi dengan kondisi ginjal.
h. Pengaruh Pemberian Akut Jus Wortel (Daucus carota L.) pada Tikus Jantan Wistar : Kajian terhadap Organ Hati dan Kadar SGPT (Novianti, 2009).
Jus wortel tidak menyebabkan kematian hewan uji (LD50 semu > 8,750 g/kgBB). Pemberian jus wortel tidak menimbulkan gejala toksik. Pengamatan histopatologi menunjukkan bahwa jus wortel menyebabkan perubahan struktural sel hati seperti hemorrhage, nekrosis, degenerasi hidrofik, dan pembentukan jaringan fibroblast yang bersifat terbalikkan. Jus wortel tidak mempengaruhi aktivitas SGPT.
Sejauh ini, penelitian tentang ketoksikan akut sari wortel (Daucus carota L.) kajian histologi organ ginjal dan kadar kreatinin serta ureum serum pada tikus betina galur Wistarbelum pernah dilakukan.
3. Manfaat penelitian
Penelitian ketoksikan akut sari wortel (Daucus carota L.) kajian histologi organ ginjal dan kadar kreatinin serta ureum serum pada tikus betina galur Wistar, diharapkan mempunyai manfaat :
a. Manfaat teoritis
carota L.) pada tikus betina galur Wistar serta melihat pengaruh ketoksikan pada fungsi organ ginjal. Selain itu dapat juga bermanfaat bagi pengembangan penelitian toksikologi terhadap tanaman/bahan alam.
b. Manfaat praktis
Memberikan informasi kepada masyarakat tentang toksisitas akut sari wortel dan pengaruh ketoksikan akut sari wortel terhadap fungsi organ ginjal.
B. Tujuan Penelitian
1. Tujuan umum :
a. Mengetahui gejala ketoksikan yang timbul akibat pemejanan tunggal sari wortel (Daucus carota L.) pada tikus betina galur Wistar.
b. Mengetahui besar potensi ketoksikan akut sari wortel (Daucus carota L.) pada tikus betina galur Wistar yang dinyatakan dengan Median Lethal Dosage(LD50).
c. Mengetahui pemberian sari wortel (Daucus carota L.) dapat menyebabkan
efek toksik ditinjau dari histopatologi organ ginjal.
2. Tujuan khusus :
1. Mengetahui hubungan antara dosis sari wortel dengan gambaran histopatologi organ ginjal pada tikus betina galur Wistar setelah pemejanan sari wortel.
2. Mengetahui hubungan antara dosis pemberian sediaan uji dengan kadar kreatinin dan ureum serum.
3. Mengetahui hubungan antara hasil histopatologi organ ginjal dengan kadar kreatinin dan ureum serum.
10
A. Sistematika Tanaman
1. Taksonomi tanaman
Divisio : Spermatophyta Sub-divisio : Angiospermae Classis : Dicotyledonae Ordo : Umbelliferales Familia : Apiaceae Genus : Daucus
Spesies : Daucus carotaL. (Backer and Van Den Brink, 1968)
2. Morfologi
Wortel termasuk jenis tanaman sayuran umbi semusim, berbentuk semak (perdu) yang tumbuh tegak dengan ketinggian antara 30-100 cm atau lebih, tergantung jenis atau varietasnya. Tanaman wortel berumur pendek yaitu berkisar antara 70-120 hari, tergantung dari varietasnya (Cahyono, 2002).
batangnya berbentuk umbi yang dikonsumsi oleh manusia. Bentuk umbi wortel bermacam-macam dan bervariasi, tergantung varietas dan kultivarnya. Bentuk umbi wortel yang dikenal ada 3 macam, yaitu berbentuk bulat panjang dengan ujung runcing, bulat panjang dengan ujung tumpul, dan bentuk kombinasi dari keduanya. Selain itu ada juga yang berbentuk percabangan. Umbi wortel berwarna kuning atau jingga (Cahyono, 2002).
Akar umbi wortel adalah akar tunggang yang berubah fungsinya sebagai tempat penyimpanan cadangan makanan (misalnya karbohidrat, protein, lemak, vitamin, mineral, dan air). Kulit umbi wortel adalah tipis dan berwarna kuning kemerahan atau jingga karena kandungan karoten yang tinggi. Daging umbi wortel bertekstur renyah, serta rasanya manis (Cahyono, 2002).
3. Kandungan kimia
4. Kegunaan di masyarakat
Bagian dari wortel yang dikonsumsi oleh masyarakat di dunia ini adalah bagian umbinya. Masyarakat menggunakan umbi wortel sebagai pengobatan dan bahan makanan. Hal ini karena dalam wortel terkandung
vitamin A yang berasal dari -karoten. Di dalam tubuh, -karoten diubah
menjadi vitamin A. Sebagai pengobatan, umbi wortel digunakan untuk penyakit seperti diuretik, busung lapar, penyakit gagal ginjal, diare kronik, disentri kronik, nutrisi makanan, obat kuat, gangguan pencernaan, karminatif dan sedatif untuk semua organ (Perry and Metzger, 1980). Selain itu, khasiat wortel juga dimanfaatkan untuk mengobati kejang jantung, eksim, cacing kremi, mata minus, tekanan darah tinggi, dan radang lambung (Pitojo, 2004). Umbi wortel juga dapat digunakan sebagai pencegahan rabun senja, antibakteri dalam rongga mulut, mencegah pembentukan asam urat dengan mengunyah umbi yang telah dikupas atau hasil perasannya (Rukmana, 1995).
Menurut hasil penelitian National Cancer Institutetahun 1991, wortel mengandung senyawa beta-karoten. Senyawa ini dapat mencegah benzopiren penyebab kanker paru-paru (Rukmana, 1995).
B. Beta Karoten
jenis karoten yang berbeda, antara lain: karoten, lutein, dan lycopen. Beta karoten yang terdapat pada wortel, pepaya, sayur mayur yang berwarna kemerahan dan minyak kelapa sawit berpotensi sebagai antioksidan (Anonim, 2003).
Beta karoten berkhasiat sebagai antioksidan spesifik untuk menetralkan oksigen singlet reaktif dan mencegah pembentukan radikal peroxyl akibat peroksidasi lipida (Tjay dan Rahardja, 2002). Beta karoten menghambat proses peroksidasi lipid dalam membran, tetapi hanya pada konsentrasi singlet oxygen yang rendah. Beta karoten biasanya digunakan sebagai suplemen nutrisi maupun prekursor vitamin A. Namun, beta karoten lebih berperan sebagai detoksifikasi berbagai bentuk oksigen (Krinsky, 1989).
Gambar 1. Struktur kimia beta karoten (Anonim, 1979).
oksigen tersebut sangat meningkat atau ketika kadar antioksidan menurun. Keadaan ini dinamakan ”stress oksidatif” dan dapat mengakibatkan kerusakan sel yang berat jika stress tersebut masif atau berlangsung lama (Tjay dan Rahardja, 2002).
Ketika aktivitas prooksidan terjadi dalam sel yang telah mengalami transformasi (perubahan), senyawa tersebut akan berpotensi sebagai antioksidan. Namun, ketika aktivitas prooksidan beta karoten terjadi dalam sel normal, maka akan dihasilkan kerusakan oksidatif yang menekan integritas sel dan menginduksi transformasi neoplastik (Masotti, dkk., 1988).
Beta karoten pada kadar oksigen yang tinggi dapat mengalami autooksidasi (Null, 2000). Menurut Murata dan Kawanishi (2000), anion radikal superoksida yang dibentuk akibat proses autooksidasi beta karoten yang kemudian didismutasi dengan H2O2 yang dapat merusak DNA. Dengan terjadinya kerusakan DNA maka terjadi gangguan dalam biosintesis protein. Bila tidak segera dinetralkan oleh tokoferol (vitamin E) dan asam askorbat (viatmin C), dapat menginisiasi kerusakan sel seperti neoplasma. Salah satu produk oksidasi dari beta karoten adalah beta apo-8’-karotenal (Null, 2000).
Beta karoten yang berperan sebagai prooksidan akan dimodulasi oleh Fe dalam jaringan. Pada penelitian yang dilakukan oleh Garcia (1998), pemberian beta karoten pada tikus yang telah diberi canthacanthin (suplemen yang mengandung Fe) dapat menyebabkan penyerapan Fe meningkat sehingga akan menyebabkan pembentukan kompleks karotenoid dengan Fe yang dapat larut dalam lumen usus, kemudian mencegah efek penghambatan polifenol pada absorpsi Fe. Ada keuntungan yang diperoleh dari sifat beta karoten sebagai agen oksidatif yang selektif terhadap sel tumor (Null, 2000).
C. Toksikologi
1. Definisi toksikologi
toksisitas adalah kapasitas suatu zat kimia atau bahan beracun untuk menimbulkan efek toksik tertentu pada makhluk hidup (Priyanto, 2007).
Timbulnya efek toksik dalam suatu organisme dapat disebabkan karena adanya pengaruh dari suatu zat yang tergantung pada banyaknya zat tersebut terakumulasi di dalam tubuh organisme tersebut. Banyaknya zat tersebut berkaitan dengan seberapa besar ukuran keracunan dari suatu zat. Menurut Koeman (1987) ukuran keracunan ditentukan oleh dosis pada waktu tejadi keracunan. Paracelcus (1443-1541) juga menyatakan bahwa pada dasarnya antara obat dan racun adalah sama, namun yang membedakannya adalah dosis. Sehingga yang menjadi perhatian adalah pengaruh kuantitatif zat kimia atas sistem biologis, yang pusat perhatiannya terletak pada aksi berbahaya zat kimia itu (Donatus, 2001).
Dari pernyataan tersebut dapat diartikan bahwa dengan adanya racun potensial pada organisme belum tentu menimbulkan keracunan (Mutschler, 2000) dan ketoksikan suatu zat kimia ditentukan oleh dosis senyawa tersebut.
Berdasarkan atas alur timbulnya efek toksik suatu senyawa maka ada empat asas utama yang perlu dipahami dalam toksikologi yaitu meliputi kondisi pemejanan dan kondisi makhluk hidup, mekanisme aksi, wujud, dan sifat efek toksik atau pengaruh racun berbahaya (Donatus, 2001).
2. Asas umum toksikologi a. Kondisi efek toksik
toksisitasnya atau keefektifan antaraksinya dengan sel sasaran disebut kondisi efek toksik. Kondisi efek toksik antara lain kondisi pemejanan yang meliputi jenis pemejanan (akut, subkronis, kronis), jalur pemejanan (intravaskular dan ekstravaskular), lama dan kekerapan pemejanan, saat pemejanan, dan takaran atau dosis pemejanan (Loomis, 1978).
Kondisi makhluk hidup meliputi keadaan normal (misalnya berat badan, umur, suhu tubuh, kecepatan pengosongan lambung, kecepatan aliran darah, status gizi, kehamilan, genetika, jenis kelamin, ritme sirkadian, ritme diurenal) dan keadaan tak normal (misalnya penyakit saluran cerna, kardiovaskuler, hati, dan ginjal) (Donatus, 2001).
b. Mekanisme efek toksik
Berdasarkan sifat dan tempat kejadiannya, mekanisme aksi efek toksik zat kimia dibagi menjadi dua yaitu mekanisme luka intrasel dan mekanisme luka ekstrasel. Mekanisme luka intrasel adalah luka sel yang diawali oleh aksi racun pada tempat aksi di dalam sel sasaran. Mekanisme ini sering disebut mekanisme langsung atau primer. Pada mekanisme luka intrasel, racun mungkin berada dalam bentuk zat kimia induk atau metabolit reaktif (produk metabolisme), sebelum berada di sel sasaran (Glaister, 1986).
intrasel pada dasarnya sebagai perubahan atau kekacauan biokimia, fungsional, atau struktural (Glaister, 1986).
Sedangkan luka ekstrasel adalah luka sel yang terjadi secara tidak langsung, dimana aksi racun dari suatu zat terjadi di lingkungan luar sel. Mekanisme ini sering disebut mekanisme tak langsung atau sekunder (Donatus, 1990). Bila racun berada di lingkungan ekstrasel, maka akan mengganggu sistem mekanisme metabolik dan pengaturan aktivitas sel sehingga menimbulkan perubahan struktur atau fungsi sel (Glaister, 1986).
c. Wujud efek toksik
Perubahan biokimia, fungsional, dan struktur pada dasarnya merupakan wujud efek toksik. Namun tidak berarti bahwa efek toksik zat beracun sepenuhnya dapat terpisah dengan tegas ke dalam tiga jenis wujud dasar efek toksik itu, melainkan sering merupakan campuran, karena ketiganya merupakan proses yang saling berkaitan (Donatus, 2001).
Jenis efek toksik berdasarkan perubahan biokimiawi, meliputi jenis wujud efek toksik yang berkaitan dengan respon dan perubahan atau kekacauan biokimia terhadap luka sel, akibat antaraksi antara zat beracun dan tempat aksi tertentu, yang sifatnya terbalikkan. Termasuk dalam jenis wujud efek toksik ini antara lain penghambatan respirasi sel, perubahan keseimbangan cairan dan elektrolit, dan gangguan pasok energi (Donatus, 2001).
homeostatis tertentu. Jenis wujud efek toksik ini diantaranya anoksia, gangguan pernafasan, gangguan sistem saraf pusat, hipertensi, atau hipotensi, hiperglikemia atau hipoglikemia, perubahan keseimbangan cairan atau elektrolit, perubahan kontraksi atau relaksasi otot dan hipotermi atau hipertermi (Loomis, 1978).
Efek toksik berdasarkan perubahan struktural, meliputi jenis wujud efek toksik yang berkaitan dengan perubahan morfologi sel yang akhirnya terwujud sebagai kekacauan struktural. Sehubungan dengan masalah ini, terdapat respon histopatologi dasar sebagai tanggapan terhadap adanya luka sel, yakni degenerasi, proliferasi, dan inflamasi atau perbaikan. Jenis wujud efek toksik ini berkaitan dengan respon dan perubahan atau kekacauan biokimia terhadap luka sel, akibat antaraksi zat racun dan sel sasaran yang sifatnya terbalikkan (Glaister, 1986).
d. Sifat efek toksik
Pada dasarnya hanya terdapat dua jenis sifat efek toksik zat beracun, yaitu terbalikkan dan tak terbalikkan. Ciri khas dari wujud efek toksik yang terbalikkan antara lain bila kadar racun yang ada dalam tempat aksi atau reseptor tertentu telah habis, maka reseptor tersebut akan kembali ke kedudukan semula; efek tokik yang ditimbulkan akan cepat kembali ke kedudukan semula; efek toksik yang ditimbulkan akan kembali normal; dan ketoksikan beracun tergantung pada takaran serta kecepatan absorpsi, distribusi, dan eliminasi racunnya (Lu, 1995).
dalam jangka panjang akan menimbulkan efek toksik yang seefektif dengan yang ditimbulkan oleh pemejanan racun dengan takaran besar dalam jangka pendek (Donatus, 2001).
3. Jenis uji toksikologi
Pada umumnya, jenis uji toksikologi dapat dibagi menjadi 2 golongan, yaitu uji ketoksikan tak khas dan uji ketoksikan khas.
a. Uji ketoksikan tak khas, yaitu uji toksikologi yang dirancang untuk mengevaluasi keseluruhan atau spektrum efek toksik suatu senyawa pada aneka ragam jenis hewan uji. Termasuk dalam uji ini adalah : (1) uji ketoksikan akut; (2) uji ketoksikan subkronis; (3) uji ketoksikan kronis (Donatus, 2001).
1) Uji toksisitas akut, dilakukan dengan memberikan zat kimia yang sedang diuji sebanyak satu kali, atau beberapa kali dalam jangka waktu 24 jam (Lu, 1995).
2) Uji toksisitas jangka panjang, (juga dikenal dengan uji subakut atau uji subkronis) dilakukan dengan memberikan bahan tersebut berulang-ulang, biasanya setiap hari atau lima kali seminggu, selama jangka waktu kurang lebih 10 % dari masa hidup hewan, yaitu tiga bulan untuk tikus dan satu atau dua tahun untuk anjing (Lu, 1995).
mencit, 24 bulan untuk tikus, dan 7-10 tahun untuk anjing dan monyet (Lu, 1995).
b. Uji ketoksikan khas, yaitu uji toksikologi yang dirancang untuk mengevaluasi secara rinci efek yang khas suatu senyawa pada aneka ragam jenis hewan uji (Donatus, 2001). Termasuk dalam uji ketoksikan khas adalah: uji potensiasi, kekarsinogenikan, kemutagenikan, keratogenitikan, reproduksi, kulit dan mata, serta perilaku (Loomis, 1978).
D. Uji Toksisitas Akut
Uji toksisitas akut merupakan uji yang termasuk dalam uji ketoksikan tak khas, dimana uji ini merupakan uji ketoksikan suatu senyawa yang dilakukan pertama kali dalam rangkaian uji toksikologi. Salah satu definsi uji toksisitas akut yang didefinsikan oleh Donatus (2001) sebagai suatu uji yang dirancang untuk menentukan efek toksik dari suatu senyawa yang akan terjadi dalam jangka waktu 24 jam setelah pemejanan dalam takaran (dosis/konsentrasi) tertentu. Jangka waktu pengamatan harus cukup panjang sehingga efek yang muncul lambat termasuk kematian, tidak luput dari pengamatan. Jangka waktu pengamatan biasanya dilakukan 7 sampai 14 hari (Donatus, 2001).
Untuk pengamatan dilakukan selama 24 jam, kecuali kasus tertentu selama 7-14 hari, dimana pengamatan dilakukan terhadap gejala-gejala klinis, jumlah hewan yang mati dan histopatologi organ (Donatus, 2001).
Dari uji toksisitas akut akan diperoleh data kualitatif dan kuantitatif. Data kualitatif yaitu penampakan klinis dan morfologi efek toksik senyawa uji yang dapat digunakan untuk menentukan potensi ketoksikan akut senyawa relatif terhadap senyawa lain dan data kuantitatifnya digunakan untuk memperkirakan dosis pada uji lain.
Hodgson dan Lewi (2000), menyatakan bahwa dalam uji ketoksikan akut senyawa yang diberikan dapat diabsorpsi dengan cepat sehingga menghasilkan efek toksik segera tetapi dapat juga menghasilkan efek toksik yang tertunda. Efek toksik segera ini ditunjukkan dari pengamatan 24 jam dari saat pemejanan sedangkan untuk efek toksik tertunda ditunjukkan setelah hari ke-14.
berdasarkan jenis kelamin yaitu tikus putih jantan dan betina maka sebaiknya dilakukan evaluasi terpisah karena respon dari keduanya berbeda.
Setelah suatu senyawa yang bersifat toksik diberikan, maka dilakukan penilaian terhadap jumlah hewan uji yang mati dan dilakukan juga pengamatan terhadap waktu kematiannya untuk dapat memperkirakan Median Lethal Dosage (LD50). LD50 yang diperoleh adalah sebagai data kuantitatif. Sedangkan data kualitatifnya berupa spektrum efek toksik yaitu dengan mengamati gejala-gejala efek toksik setelah pemejanan dari suatu senyawa.
E. Median Lethal Dosage(LD50)
Seperti penjelasan sebelumnya, telah dikatakan bahwa dalam mengukur tingkat ketoksikan dari hasil uji toksikologi akut, maka dapat diukur secara kualitatif (berdasarkan spektrum efek toksik) dan kuantitatif (berdasarkan LD50).
atau lebih dengan harapan bahwa sekurang-kurangnya tiga diantaranya akan berada dalam rentang dosis yang dikehendaki (Lu, 2006).
LD50 akan lebih tepat bila digunakan lebih banyak hewan untuk tiap dosis dan bila rasio antara dosis yang berurutan lebih kecil. Banyak peneliti menggunakan 40-50 hewan per LD50 dan memilih rasio 1,2-1,5. Lu mengatakan bahwa kadang untuk menentukan LD50 yang lebih tepat, maka rasio antara dosis-dosis yang berurutan harus lebih kecil. Untuk dapat menunjukkan tiadanya variasi yang berarti dan tiadanya perbedaan yang besar dalam toksisitas (Lu, 2006).
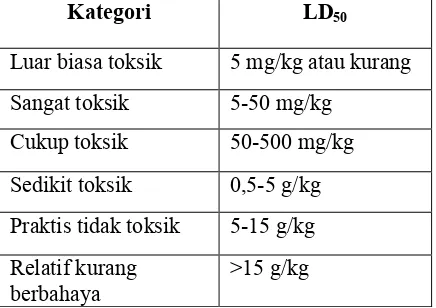
Tabel. I. Klasifikasi potensi ketoksikan suatu senyawa (Loomis, 1978)
Kategori LD50
Luar biasa toksik 5 mg/kg atau kurang Sangat toksik 5-50 mg/kg
Cukup toksik 50-500 mg/kg Sedikit toksik 0,5-5 g/kg Praktis tidak toksik 5-15 g/kg Relatif kurang
berbahaya
>15 g/kg
F. Anatomi dan Fisiologi Ginjal
Ginjal berfungsi untuk mengekskresi cairan (termasuk xenobiotik yang larut dan konjugatnya) dari darah melalui urin dan meregulasi air dan garam dalam tubuh seperti kalium dan natrium. Disamping itu, hormon dan enzim yang diproduksi oleh ginjal penting dalam mengatur tekanan darah, pH, metabolisme kalsium, dan produksi sel darah merah (Stine and Brown, 1996).
dibagian luar dan medula dibagian dalam. Medula ginjal terbagi menjadi beberapa massa jaringan yang disebut piramida ginjal (Guyton and Hall, 1997).
Gambar 2. Anatomi ginjal (Sukmarini, 2008)
lengkung Henle yang mengosongkan diri ke duktus koligen (Price dan Wilson, 1985). Tiap nefron terdiri atas glomerulus dan serangkaian tubulus. Glomerulus didarahi oleh sistem kapiler bertekanan tinggi yang menghasilkan ultrafiltrat dari plasma. Filtrat yang terkumpul dalam kapsul Bowman mengalir melalui tubulus berkelok proksimal, ansa Henle, dan tubulus distal, dan kemudian mengalir lewat kumpulan tubulus ke dalam piala ginjal dan dibuang sebagai urin (Lu, 1995).
Selain fungsi ginjal di atas, ginjal juga dapat berperan penting dalam mempertahankan homeostasis air dan elektrolit dalam tubuh. Ginjal dikenal juga sebagai pembuang bahan-bahan sampah tubuh dari hasil pencernaan atau yang diproduksi oleh metabolik, serta sebagai pengontrol volume dan komposisi cairan tubuh, air, serta semua elektrolit dalam tubuh. Keseimbangan antara asupan (akibat pencernaan atau produksi metabolik) dan keluaran (akibat ekskresi atau konsumsi metabolik) sebagian besar dipertahankan oleh ginjal (Stine and Brown, 1996).
G. Nefropati Toksik
1. Glumerulonefropati
Glumerulus merupakan organ target yang jarang dipengaruhi oleh bahan beracun. Organ ini dapat dipengaruhi oleh bahan beracun baik secara langsung maupun tidak langsung. Salah satu perubahan glumerulus adalah perubahan permeabilitasnya terhadap protein-protein plasma (Glaister, 1986). Perubahan yang ditunjukkan dengan meningkatkan permeabilitas glumerulus yang disebabkan oleh protein uria, kebocoran glumerulus karena protein-protein yang bermolekul besar, sampai ke urin. Hal ini disebut protein-proteinuria. Beberapa toksikan juga dapat menurunkan fungsi membran glumerulus dan dapat mengeluarkan anion-anion yang banyak (Stine and Brown, 1996).
2. Nefropati tubulus proksimal
3. Nefropati tubulus distal
Efek toksik yang sering ditemui pada tubulus distal adalah kristaluria, dan nekrosis papila ginjal. Hal tersebut berhubungan dengan fungsi tubulus distal dalam mengatur keseimbangan air, elektrolit, dan asam-basa (Glaister, 1986).
H. Kreatinin dan Ureum Serum
Kreatinin dan ureum serum merupakan beberapa tes fungsi ginjal yang digunakan untuk menggambarkan adanya gangguan fungsi ginjal. Menurut Baron (1990), tes fungsi ginjal memiliki dua tujuan utama yaitu dapat mendeteksi kemungkinan terjadinya kerusakan ginjal dan menentukan derajat kerusakan fungsi ginjal. Sekali kerusakan ginjal terdeteksi, maka tes-tes fungsi ginjal memperlihatkan kelainan, dan kegagalan ginjal berkembang bila ada ketidakmampuan ginjal dalam mempertahankan keseimbangan. Tes fungsi ginjal yang dilakukan dapat melalui uji diagnostik yang digunakan untuk dapat mendeteksi adanya penyakit ginjal karena banyak penyakit ginjal serius yang tidak menimbulkan gejala sampai fungsi ginjal sudah terganggu. Kedua pemeriksaan ini hanyalah sebagian kecil dari tes pemeriksaan fungsi ginjal lainnya sebagai indikasi adanya gangguan fungsi pada organ ginjal (Baron, 1990). 1. Kreatinin serum
memerlukan energi (Widmann, 1995). Kreatinin disintesis di hati dan ditemukan juga dalam otot rangka dan darah, dan diekskresikan dalam urin (Sutedjo, 2006).
Jumlah kreatinin dalam darah dapat digunakan untuk mendiagnosis adanya kegagalan ginjal yaitu dengan mengukur laju filtrasi glomerolus (Glomerular filtration rate=GFR). Peningkatan kreatinin dalam darah tidak dipengaruhi diet dan masukan cairan. Peningkatan kreatinin dalam darah menunjukkan adanya penurunan fungsi ginjal dan penyusutan massa otot rangka. Peningkatan kadar kreatinin darah cenderung tetap / tidak banyak berubah dibandingkan kadar ureum (Sutedjo, 2006).
Dalam mengukur nilai GFR juga dipengaruhi oleh nilai kreatinin, ureum, dan volume urin 24 jam. Bila GFR turun, maka kreatinin plasma meningkat. Kreatinin plasma merupakan indeks GFR yang lebih cermat karena kecepatan produksinya terutama merupakan fungsi dari massa otot yang sedikit sekali mengalami perubahan. Konsentrasi kreatinin plasma normal besarnya 0,7 sampai 1,5 mg per 100 ml (Price and Wilson, 2006). Sedangkan menurut Cockroft and Gault (1976), kreatinin plasma normal berkisar antara 0,7 sampai 1,2 mg/dl.
2. Ureum serum
dapat menggambarkan semua jalur metabolisme protein yang banyak ragamnya. Bila mekanisme ekskresi ginjal terganggu, maka penetapan kadar ureum yang meningkat dalam darah lebih mudah dilakukan daripada mengukur turunnya ekskresi ureum. Meningkatnya kadar ureum dalam darah dinamai uremia. Keadaan itu paling sering disebabkan oleh ekskresi ureum yang terhambat oleh kegagalan fungsi ginjal.
I. Landasan Teori
Umbi wortel telah digunakan sebagai diuretik, pengobatan busung lapar, penyakit gagal ginjal, diare kronik, nutrisi makanan, obat kuat, gangguan pencernaan, karminatif, dan sedatif untuk semua organ tubuh (Perry dan Metzger, 1980), kejang-kejang, jantung, eksim, cacing kremi, mata minus, tekanan darah tinggi, dan radang lambung (Pitojo, 2004). Selain itu, umbi wortel dapat juga digunakan sebagai pencegahan rabun senja, antibakteri dalam rongga mulut mencegah pembentukan asam urat dengan mengunyah umbi yang telah dikupas atau hasil perasaannya (Rukmana, 1995).
ureum serum yang merupakan parameter biokimia yang digunakan untuk mengetahui adanya gangguan fungsi ginjal. Sekali kerusakan ginjal terdeteksi, maka tes-tes fungsi ginjal memperlihatkan kelainan, dan kegagalan ginjal berkembang bila ada ketidakmampuan ginjal dalam mempertahankan keseimbangan (Baron, 1990). Peningkatan kreatinin dalam darah menunjukkan adanya penurunan fungsi ginjal dan penyusutan massa otot rangka. Peningkatan kadar kreatinin darah cenderung tetap / tidak banyak berubah dibandingkan kadar ureum (Sutedjo, 2006). Bila mekanisme ekskresi ginjal terganggu, maka penetapan kadar ureum yang meningkat dalam darah lebih mudah dilakukan daripada mengukur turunnya ekskresi ureum. Meningkatnya kadar ureum dalam darah dinamai uremia. Keadaan itu paling sering disebabkan oleh ekskresi ureum yang terhambat oleh kegagalan fungsi ginjal (Widmann, 1995).
J. Hipotesis
33
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk penelitian eksperimental murni dengan
menggunakan rancangan acak lengkap pola searah. Pada penelitian ini subjek uji
berjumlah 30 ekor yang terbagi dalam 5 kelompok yang terdiri dari 1 kontrol dan
4 perlakuan yang diberi sari wortel (Daucus carota L.) menurut peringkat dosis
yang ditentukan dari hasil orientasi. Tiap kelompok masing-masing terdiri dari 6
ekor hewan uji.
B. Variabel dan Definisi Operasional
1. Variabel utama
a. Variabel bebas
Dosis sari wortel merupakan sejumlah (gram) sari wortel tiap satuan kg
berat badan subyek uji. Dosis sari wortel terbagi dalam 4 peringkat dosis.
Peringkat dosis sari wortel yang dibuat dalam 4 peringkat dosis yaitu :
1) Peringkat dosis I : 66,55 g/kg BB
2) Peringkat dosis II : 79,86 g/kg BB
3) Peringkat dosis III : 95,83 g/kg BB
b. Variabel tergantung : jumlah kematian hewan uji (LD50), gejala efek toksik,
sifat efek toksik, wujud efek toksik, dan perubahan fungsi ginjal (ditunjukkan
dengan hasil pemeriksaan kadar kreatinin dan ureum dalam darah).
2. Variabel pengacau
a. Variabel pengacau terkendali
1) Bahan uji : umbi wortel yang diperoleh dari warung sayur-sayuran dekat
Instiper dimana warung tersebut memperolehnya dari daerah
Tawangmangu pada tanggal 4 September 2009.
2) Hewan uji : tikus putih yang berjumlah 30 ekor.
3) Berat badan hewan uji: 150-200 gram (dengan variasi yang
diperbolehkan sebesar kurang lebih 10%) yang diadaptasikan selama 1
minggu.
4) Jenis kelamin: Betina.
5) Galur hewan uji: Wistar.
6) Umur hewan uji : 2 – 3 bulan.
7) Zat gizi dalam pakan : hewan uji diberikan makanan 10% dari berat
badannya.
8) Kualitas udara : hewan uji dibuat dengan kondisi yang sama mulai dari
pemeliharaan sampai pada percobaan penelitian dengan suhu ruangan
yang sama yaitu 28oC.
b. Variabel pengacau tak terkendali
Kondisi patologis tikus : meski keadaan fisik berstatus sehat, belum dapat
3. Definisi operasional
a. Sari wortel adalah sejumlah cairan yang diperoleh dari umbi wortel dengan
menggunakan juice extractor yang kemudian disaring dengan penyaring
biasa untuk memisahkan sari dan ampas kasar (berukuran besar), kemudian
dilanjutkan dengan menggunakan kertas saring untuk memisahkan sari dari
ampas (berukuran kecil) agar tidak menyumbat di dalam syringedan mudah
diinjeksikan secara oral ke hewan uji.
b. Uji toksisitas akut adalah tingkat efek toksik suatu senyawa yang terjadi
dalam waktu 24 jam setelah pemberian sari wortel dengan dosis tunggal
pada tikus betina galur Wistar yang bertujuan untuk menetapkan potensi
toksisitas akut melalui Median Lethal Dosage (LD50), menilai gejala toksik,
wujud efek toksik, spektrum efek toksik yang timbul akibat pemberian sari
wortel (Daucus carota L.).
c. Harga Median Lethal Dosage (LD50) adalah dosis tunggal yang dapat
menyebabkan 50 % kematian hewan uji akibat pemberian akut sari wortel
(Daucus carota L.).
d. Pemeriksaan kadar kreatinin dan ureum dalam darah merupakan dua dari
beberapa parameter biokimia yang digunakan untuk mengetahui terjadinya
gangguan fungsi ginjal setelah pemberian akut sari wortel (Daucus carota
C. Alat dan Bahan Penelitian
1. Alat
a. Alat-alat gelas seperti : labu ukur, pipet tetes, corong pisah, gelas ukur
b. Microtube
c. Juice extractor
d. Kamera Hp
e. Kandang tikus (menggunakan ember yang sedang)
f. Kertas saring
g. Mikropipet
h. Pot unguenta
i. Seperangkat alat bedah (gunting, jarum pentul, pinset)
j. Spuit injeksi oral
k. Stop watch
l. Timbangan (analyitical balance)
m. Timbangan tikus
2. Bahan
a. Subyek uji yang digunakan adalah tikus putih betina galur Wistar dengan
berat badan 150-200 gram, umur berkisar antara 2-3 bulan, dan berjumlah
30 ekor yang diperoleh dari Fakultas Kedokteran Hewan LPPT Universitas
Gadjah Mada, Yogyakarta.
b. Umbi wortel segar diperoleh dari warung sayur di daerah Instiper,
Maguwoharjo, Yogyakarta, dimana warung tersebut memperolehnya dari
c. NaCl 0,9% fisiologis, digunakan untuk membilas organ ginjal sebelum
dilakukan penimbangan organ ginjal. NaCl diperoleh dari Laboratorium
Biofarmasetika Universitas Sanata Dharma, Yogyakarta.
d. Pakan merk AD 5 dan minum merk Agua.
e. Formalin 10%, yang digunakan untuk mengawetkan organ ginjal yang
diperoleh dari Laboratorium Biofarmasetika Univeritas Sanata Dharma,
Yogyakarta.
D. Tata Cara Penelitian
1. Penyiapan hewan uji
Hewan uji yang digunakan berjumlah 30 ekor tikus putih betina galur
Wistar. Sebelum perlakukan, tikus tersebut diadaptasikan atau dikarantinakan
sesuai dengan lingkungan Laboratorium Imono selama 10 hari. Selama adaptasi
tersebut tikus diberi pakan pelet dan diberi minum ad libitium. Pakan yang
diberikan disesuaikan dengan berat badan dari tikus yaitu 10% BB per hari.
Sedangkan minum yang diberikan adalah aqua galon sebanyak 240 ml per hari.
2. Pengelompokkan hewan uji
Penelitian ini menggunakan hewan uji berjumlah 30 ekor tikus betina yang
akan dikelompokkan ke dalam lima kelompok secara random. Pengelompokan
hewan uji dilakukan secara random menggunakan proses penomoran pada hewan
uji, kemudian dilanjutkan dengan pengundian. Masing–masing tikus diberi kode
nomor uji, dan pada sangkar diberi etiket. Pada proses ini hewan uji dibagi ke
perlakuan apapun) dan empat kelompok yang lain sebagai kelompok perlakuan
yang diberikan sari wortel menurut peringkat dosis. Tiap kelompok
masing terdiri dari 6 ekor hewan uji. Perwakilan satu hewan uji dari
masing-masing kelompok dipelihara dalam satu kandang. Pada penelitian ini dilakukan
replikasi sebanyak 3 kali untuk masing-masing kelompok pada pengamatan yaitu
3 kali replikasi pada waktu pengamatan 24 jam setelah pemberian sari wortel dan
3 kali replikasi pada hari ke-14 setelah pemberian sari wortel.
3. Pengumpulan bahan
Bahan uji yang digunakan adalah umbi wortel yang diambil sarinya. Umbi
wortel (Daucus carota L.) diperoleh dari warung sayur didekat Instiper,
Maguwoharjo, Yogyakarta, dimana warung tersebut memperoleh wortel dari
daerah Tawangmangu pada tanggal 4 September 2009. Wortel tersebut dipilih
dengan melihat warna yang orange, segar, bersih, dan tidak busuk.
4. Determinasi tanaman
Tanaman Wortel (Daucus carota L.) yang akan digunakan dalam
penelitian ini dideterminasi di bagian Biologi Farmasi Universitas Gadjah Mada,
Yogyakarta.
5. Pembuatan larutan sampel
Umbi wortel dipilih tanpa adanya luka pada umbinya, dikupas, ditimbang
beratnya sebanyak 400,4 g dan dicuci bersih kemudian dipotong agak kecil.
Setelah itu potongan wortel dimasukkan ke dalam juice extractor dan hasilnya
sari dari ampas kasar yang berukuran besar, kemudian dilanjutkan dengan
menggunakan kertas saring untuk memisahkan sari dari ampas yang berukuran
kecil, sehingga akan diperoleh sari wortel (sari wortel yang diperoleh adalah 174
ml). sari wortel yang diperoleh diharapkan tidak menyumbat di syringedan dapat
diberikan pada hewan uji secara oral. Pembuatan sari wortel harus selalu dibuat
baru.
Skema kerja:
Umbi wortel dikupas
Ditimbang, cuci bersih
Dipotong agak kecil, masukkan dalam juice extractor
Ambil sarinya, saring dengan penyaringan biasa kemudian dilanjutkan
dengan menggunakan kertas saring
Sari wortel (siap diberikan pada hewan uji)
6. Penentuan dosis
Pada orientasi digunakan dosis tertinggi yang secara teknis masih bisa
diberikan dan tidak melebihi volume maksimum yang masih boleh diberikan
kepada hewan uji (5,0 ml/100g BB). Dari hasil orientasi didapatkan dosis
tertingginya yaitu: 115 g/kg BB dan diharapkan mematikan seluruh hewan uji.
Dari dosis tertinggi kemudian dibuat peringkat dosis dengan faktor perkalian tetap
yaitu 1,2. Maka dari faktor perkalian tersebut peringkat dosisi yang akan
peringkat dosis II yaitu 79,86 g/kg BB, peringkat dosis III yaitu 95,83 g/kg BB,
peringkat dosis IV yaitu 115 g/kg BB, dan kelompok kontrol tidak diberikan
perlakuan apapun. Berikut adalah data perhitungan dosis.
Penimbangan Wortel = 400,4 g
Sari yang diperoleh = 174 ml
Csari wortel = 2,3 g/ml
= 2300 mg/ml
Volume maksimum pemberian pada tikus = 5 ml/100 g BB
C1 x V = BB x D
2300 mg/ml x 5 ml = 100 g x D
D = 115 mg/g BB
D = 115 g/kg BB (sebagai peringkat dosis IV)
Faktor pengali yang digunakan sebesar 1,2, maka:
Peringkat dosis III =115 g/kg
1,2 = 95,83 g/kg BB
Peringkat dosis II =95,83 g/kg
1,2 = 79,86 g/kg BB
Peringkat dosis I =79,86 g/kg
1,2 = 66,55 g/kg BB
7. Pengamatan
Pengamatan yang dilakukan pada penelitian ini meliputi :
a. Pengamatan fisik terhadap gejala–gejala toksik, wujud efek toksik, serta
pemberian sediaan uji, 24 jam pertama setelah pemberian sediaan uji
dan sekali sehari selama pengamatan sampai hari ke-14.
b. Kematian hewan uji pada masing – masing kelompok yang diamati 3
jam pertama sampai pada waktu 24 jam setelah pemberian sari wortel.
c. Pemeriksaan histopatologi organ ginjal yang dilakukan pada waktu 24
jam dan 14 hari setelah pemberian sari wortel.
d. Penimbangan berat badan dilakukan mulai hari ke-0 (saat pemejanan
sari wortel) hingga hari ke-14.
e. Penimbangan berat organ ginjal dilakukan setelah hewan uji dibedah
pada waktu pengamatan 24 jam dan hari ke-14 setelah pemberian sari
wortel.
f. Pemeriksaan kadar kreatinin dan ureum serum dengan mengambil darah
pada hewan uji dilakukan 3 hari sebelum pemberian sari wortel (Daucus
carotaL.), 24 jam dan hari ke-14 setelah pemberian sari wortel.
8. Uji toksisitas
Sari wortel yang telah disiapkan, diinjeksikan secara oral kepada tikus, dan
kemudian dilakukan pengamatan terhadap perilaku tikus selama 3 jam pertama
(dengan membandingkan antara perilaku tikus yang mendapatkan perlakuan sari
wortel dengan perilaku tikus sebagai kontrol), dan dicatat pada blanko data.
Pengamatan fisik gejala-gejala pada seluruh tikus betina tiap kelompok
dilakukan terus menerus selama 3 jam pertama serta sesering mungkin selama 24
jam pertama setelah pemberian sari wortel. Apabila saat pengamatan langsung
pengambilan organ ginjal dari masing-masing tikus betina. Apabila tidak ada
hewan uji yang mati pada masa akhir 24 jam setelah pemberian sari wortel, hewan
uji dikorbankan secara fisik dengan dislokasi leher, kemudian dilakukan
pembedahan pada bagian perut secara melintang dari 3 ekor tikus betina dari
masing-masing tingkatan dosis, dan kontrol. Kemudian sisa tikus betina lainnya
yang masih hidup pada masing-masing kelompok dibiarkan sampai 14 hari.
Dalam rentang waktu 14 hari tersebut tetap dilakukan pengamatan dan
penimbangan berat badan.
9. Pengambilan darah dan pemeriksaan kadar kreatinin dan ureum serum
a. Pengambilan darah sebelum pemejanan sari wortel
Pengambilan darah sebelum pemejanan dilakukan tiga hari sebelum
pemejanan, dimana semua hewan uji diambil sampel darahnya melalui vena
orbitalis. Kemudian sampel darah segera diukur agar tidak terjadi lisis.
Sebelum pengambilan darah, seluruh hewan uji terlebih dahulu dipuasakan
sehari sebelumnya. Pengambilan darah pada waktu sebelum pemberian sari
wortel diasumsikan sebagai nilai normal kadar kreatinin dan ureum serum
yang akan dibandingkan dengan kadar kreatinin dan ureum serum setelah
pemejanan sari wortel. Hal ini dikarenakan tidak ditemukan literature yang
jelas yang digunakan sebagai acuan nilai normal kadar kreatinin dan ureum
serum pada tikus betina galur Wistar. Pemeriksaan kadar kreatinin dan ureum
dalam darah digunakan sebagai parameter biokimia untuk menentukan
adanya gangguan fungsi ginjal. Pemeriksaan kadar kreatinin dan ureum
b. Pengambilan darah setelah pemejanan sari wortel
Setelah 24 jam pemejanan sari wortel, tiga ekor hewan uji dari tiap
kelompok perlakuan dan kontrol diambil sampel darahnya melalui vena
orbitalis. Kemudian darah segera diukur untuk mencegah terjadinya lisis. Sisa
hewan uji lainnya akan diambil sampel darahnya setelah hari ke-14 dengan
perlakuan yang sama. Pemeriksaan kadar kreatinin dan ureum dalam darah
pada waktu 24 jam dan hari ke-14, dianalisis di LPPT Unit I Universitas
Gadjah Mada, Yogyakarta.
10. Pembuatan dan pemeriksaan preparat histopatologi
Setelah hewan uji diambil darahnya, kemudian hewan uji dinekropsi lalu
dibedah untuk mengambil organ tubuhnya. Pada penelitian ini, hewan uji dibedah
dengan menggunakan seperangkat alat-alat bedah untuk mengambil organ ginjal
dari tiap masing-masing kelompok perlakuan dan kontrol. Organ ginjal yang telah
diambil, diamati secara makroskopis. Setelah itu, dicuci dengan NaCl fisiologis,
kemudian ditimbang dan difiksasi menggunakan formalin 10% untuk diawetkan.
Pada proses ini juga dilakukan hal yang sama terhadap tikus betina yang masih
hidup sampai pada hari ke-14 setelah pemberian sari wortel yang akan dibedah.
Pembuatan preparat histopatologi organ ginjal dilakukan di Laboratorium Patologi
Anatomi Fakultas Kedokteran Umum Universitas Gadjah Mada, Yogyakarta
dengan pengecatan Hematoksilin–Eosin. Sedangkan untuk pemeriksaan preparat
histopatologi organ ginjal diinterpretasikan oleh Prof. drh. Kurniasih, MVSc.,
Pemeriksaan dilakukan dengan cara membandingkan antara kelompok perlakuan
dan kontrol di bawah mikroskop cahaya.
E. Tata Cara Analisis Hasil
Data yang didapat dari penelitian yaitu LD50, spektrum efek toksik, data
histopatologi dan kadar kreatinin dan ureum serum.
1. Data kematian hewan uji digunakan untuk mengetahui harga LD50 yang
kemudian dapat ditentukan potensi ketoksikannya. Harga LD50 dihitung dari jumlah hewan uji yang mati pada masing–masing kelompok, menggunakan
metode kertas grafik logaritma Miller dan Tainter dan secara kuantitatif
digunakan untuk menentukan potensi ketoksikan akut mengikuti ketentuan
Loomis (1978). Jika sampai batas volume maksimal yang boleh diberikan
tidak menimbulkan kematian hewan uji, maka peringkat dosis tertinggi
sebagai LD50semu.
2. Gejala ketoksikan dapat dilakukan dengan mengamati tingkah laku hewan uji
selama percobaan, lalu membandingkan tingkah laku kelompok kontrol
dengan kelompok perlakuan yang dipejankan sari wortel. Pengamatan tingkah
laku hewan uji yang dilakukan dapat dilihat pada lampiran 9.
3. Histopatologi dilakukan dengan membandingkan histopatologi organ ginjal
pada kelompok kontrol dengan kelompok perlakuan dari masing–masing
peringkat dosis sari wortel pada waktu 24 jam dan hari ke-14 setelah
pemejanan sari wortel.
4. Dilakukan uji distribusi normal terlebih dulu dengan menggunakan Shapiro
uji distribusi normal dilakukan menggunakan Kolmogorrov-Smirnov. Data
dikatakan terdistribsui normal bila p>0,05 (menggunakan taraf kepercayaan
95%).
5. Kadar kreatinin dan ureum serum dianalisis dengan analisis statistik yaitu One
Way ANOVA (bila data berdistribusi normal) atau Uji Friedmann (bila data
tidak berdistribusi normal) digunakan untuk melihat ada tidaknya perbedaan
pada setiap waktu pemeriksaan darah dan bila ada perbedaan (p<0,05) maka
dilanjutkan denganPost Hoc Test, Scheffe untuk melihat perbedaannya antar
kelompok perlakuan terhadap kontrol. Setelah itu, dilanjutkan dengan uji
Paired T-Test untuk melihat adanya perbedaan antar kelompok perlakuan dan
kontrol dengan membandingkan antara kadar kreatinin dan ureum serum pada
waktu sebelum perlakuan dengan setelah perlakuan untuk mengetahui ada
tidaknya perubahan selama perlakuan (syaratnya subyek uji yang digunakan
sama).
6. Berat badan hewan uji dari hari ke-0, hari ke-7, dan hari ke-14 dianalisis
dengan General Linear Model, Multivariate, kemudian dilanjutkan dengan uji
Post Hoc Tets, Scheffe.
7. Berat organ ginjal relatif dari masing–masing kelompok perlakuan dianalisis