Asam, Basa, dan Garam
Asam, Basa, dan Garam
Kelas VII.C
Kelas VII.C
Kelompok Kation :
Kelompok Kation :
Jauhar Zainal Arifin
Jauhar Zainal Arifin
Wahidah Koswulan Sari
Wahidah Koswulan Sari
Ega Oktaviane
Ega Oktaviane
Kezia Tamariska Seraf
Kezia Tamariska Seraf
Friska Dayanti Nadeak
Friska Dayanti Nadeak
Sekolah Menengah Pertama Negeri 6 Kota
Sekolah Menengah Pertama Negeri 6 Kota
Bogor
Bogor
Jl. Dr. Sumeru-Gang Kelor No.4
Asam, Basa, dan Garam
Asam, Basa, dan Garam
Kelas VII.C
Kelas VII.C
Kelompok Kation :
Kelompok Kation :
Jauhar Zainal Arifin
Jauhar Zainal Arifin
Wahidah Koswulan Sari
Wahidah Koswulan Sari
Ega Oktaviane
Ega Oktaviane
Kezia Tamariska Seraf
Kezia Tamariska Seraf
Friska Dayanti Nadeak
Friska Dayanti Nadeak
Sekolah Menengah Pertama Negeri 6 Kota
Sekolah Menengah Pertama Negeri 6 Kota Bogor
Bogor
Jl. Dr. Sumeru-Gang Kelor No.4
ii ii
Puji dan syukur panjatkan kehadirat Tuhan YME atas
Puji dan syukur panjatkan kehadirat Tuhan YME atas
limpahan rahmat dan karunia-Nya, sehingga kami dapat
limpahan rahmat dan karunia-Nya, sehingga kami dapat
menyelesaikan laporan yang berjudul “Asam, Basa,
menyelesaikan laporan yang berjudul “Asam, Basa, dan
dan
Garam
Garam” ini dengan lancar. Penulisan laporan ini bertujuan
” ini dengan lancar. Penulisan laporan ini bertujuan
untuk memenuhi salah satu tugas yang diberikan oleh Dra.
untuk memenuhi salah satu tugas yang diberikan oleh Dra.
Rini Sri Wilujeng mata pelajaran Biolog
Rini Sri Wilujeng mata pelajaran Biologi & Kimia.
i & Kimia.
Laporan ini ditulis dari hasil
Laporan ini ditulis dari hasil penyusunan data-data, hasil
penyusunan data-data, hasil
pengamatan dan hasil praktikum yang berkaitan dengan
pengamatan dan hasil praktikum yang berkaitan dengan
Biologi & Kimia, serta alat-alat praktikum seperti pengunaan
Biologi & Kimia, serta alat-alat praktikum seperti pengunaan
lakmus,
lakmus, indikator
indikator universal,
universal, indikator
indikator alami,
alami, dan
dan sifat-sifat
sifat-sifat
asam, basa,
asam, basa, garam
garam tidak lupa
tidak lupa kami mengucapkan
kami mengucapkan terima kasih
terima kasih
kepada pengajar mata pelajaran Biologi & Kimia atas
kepada pengajar mata pelajaran Biologi & Kimia atas
bimbingan dan arahan dalam penulisan laporan ini. Juga
bimbingan dan arahan dalam penulisan laporan ini. Juga
kepada teman-teman yang telah mendukung sehingga dapat
kepada teman-teman yang telah mendukung sehingga dapat
diselesaika
diselesaikannya laporan ini.
nnya laporan ini.
Kami harap, dengan membaca laporan ini dapat
Kami harap, dengan membaca laporan ini dapat
memberi manfaat bagi kita semua, dalam hal ini dapat
memberi manfaat bagi kita semua, dalam hal ini dapat
menambah wawasan kita mengenai pembelajaran Asam Basa
menambah wawasan kita mengenai pembelajaran Asam Basa
Garam, khususnya bagi kami selaku penulis. Memang laporan
Garam, khususnya bagi kami selaku penulis. Memang laporan
ini
ini masih jauh
masih jauh dari
dari sempurna, maka
sempurna, maka kami
kami mengharapkan kritik
mengharapkan kritik
dan saran dari pembaca demi perbaikan menuju arah yang
dan saran dari pembaca demi perbaikan menuju arah yang
lebih baik.
lebih baik.
Bogor, 27 Oktober 2012
Bogor, 27 Oktober 2012
Kelompok Kation
Kelompok Kation
KATA PENGANTAR
KATA PENGANTAR
iii iii
Asam dan basa merupakan dua golongan zat kimia yang sangat penting. Selain Asam dan basa merupakan dua golongan zat kimia yang sangat penting. Selain kedua zat tersebut, kamu juga dapat menemukan zat lain di sekitarmu, yaitu garam. kedua zat tersebut, kamu juga dapat menemukan zat lain di sekitarmu, yaitu garam. Asam, basa, dan garam telah dikenal sebagai zat-zat yang
Asam, basa, dan garam telah dikenal sebagai zat-zat yang menarik untuk dipelajari sejakmenarik untuk dipelajari sejak zaman alkimia. Kimia asam-basa berperan penting dalam banyak proses yang terjadi zaman alkimia. Kimia asam-basa berperan penting dalam banyak proses yang terjadi dalam tubuhmu. Sebagai contoh peran asam dalam tubuhmu selama berolahraga. dalam tubuhmu. Sebagai contoh peran asam dalam tubuhmu selama berolahraga. Ketika kamu berolahraga, asam laktat akan dihasilkan sebagai hasil samping Ketika kamu berolahraga, asam laktat akan dihasilkan sebagai hasil samping proses-proses di dalam sel. Bila kita berolah lebih giat, akan lebih banyak asam laktat yang proses di dalam sel. Bila kita berolah lebih giat, akan lebih banyak asam laktat yang dihasilkan daripada yang dapat dikeluarkan melalui sistem sirkulasi. Secara sedehana dihasilkan daripada yang dapat dikeluarkan melalui sistem sirkulasi. Secara sedehana sifat-sifat yang teramati juga mampu membedakan asam, basa, dan garam seperti sifat-sifat yang teramati juga mampu membedakan asam, basa, dan garam seperti berikut ini.
berikut ini. A.
A. AsamAsam
Kata “asam” berasal dari bahasa latin, yaitu acidus yang berarti masam. Secara kimia, Kata “asam” berasal dari bahasa latin, yaitu acidus yang berarti masam. Secara kimia,
asam merupakan suatu zat yang dalam pelarut air dapan menghasilkan ion hidrogen asam merupakan suatu zat yang dalam pelarut air dapan menghasilkan ion hidrogen (H+). Senyawa asam banyak ditemukan dikehidupan sehari-hari, seperti pada makanan (H+). Senyawa asam banyak ditemukan dikehidupan sehari-hari, seperti pada makanan dan minuman. Selain iu, senyawa asam juga dapat ditemukan dalam lambung, yaitu dan minuman. Selain iu, senyawa asam juga dapat ditemukan dalam lambung, yaitu asam klorida yang ber
asam klorida yang berfungsi membunuh kuman. fungsi membunuh kuman. Beberapa senyaBeberapa senyawa asam: asam sitratwa asam: asam sitrat contohnya
contohnya jeruk, jeruk, asam asam tartat tartat contohnya contohnya anggur, anggur, asam asam malat malat contohnya contohnya apel, apel, asamasam klorida
klorida contohnya contohnya lambung, lambung, asam asam nitrat nitrat pupuk pupuk tanaman.tanaman. 1. Sifat-sifat asam:
1. Sifat-sifat asam: a.
a. rasa masamrasa masam b.
b. mengubah lakmus biru menjadi merahmengubah lakmus biru menjadi merah c.
c. menghantarkan arus listrikmenghantarkan arus listrik d.
d. bereaksi dengan logam menghasilkan gas hidrogenbereaksi dengan logam menghasilkan gas hidrogen 2. Kekuatan asam
2. Kekuatan asam
Berdasarkan kekuatannya, asam dibagi menjadi dua , yaitu asam kuat dan asam lemah. Berdasarkan kekuatannya, asam dibagi menjadi dua , yaitu asam kuat dan asam lemah. Kuat lemahnya asam ditentukan oleh jumlah ion hidrogen yang terionisasi dalam Kuat lemahnya asam ditentukan oleh jumlah ion hidrogen yang terionisasi dalam larutan. Asam kuat adalaah asam yang banyak menghasilkan ion dalam larutannya larutan. Asam kuat adalaah asam yang banyak menghasilkan ion dalam larutannya (terionisasi sempurna), sedangkan asam lemah adalah asam yang sedikit menghasilkan (terionisasi sempurna), sedangkan asam lemah adalah asam yang sedikit menghasilkan ion dalam larutannya (terionisasi sebagian).
ion dalam larutannya (terionisasi sebagian). 3.Peranan asam dalam kehidupan
3.Peranan asam dalam kehidupan
Asam merupakan salah satu senyawa yang mempunyai peranan penting dalam Asam merupakan salah satu senyawa yang mempunyai peranan penting dalam kehidupan. Dalam bidang industri, asam bnyak digunakan dalam proses pembuatan kehidupan. Dalam bidang industri, asam bnyak digunakan dalam proses pembuatan pupuk, obat-obatan, bahan peledak, plastik, dan pembersih permukaan logam.
pupuk, obat-obatan, bahan peledak, plastik, dan pembersih permukaan logam. Selain ituSelain itu terdapat beberapa asam yang digunakan sebagai pengawet makanan, seperti asam terdapat beberapa asam yang digunakan sebagai pengawet makanan, seperti asam benzoat, asam asetat, dan asam askorbat. Meskipun asam merupakan senyawa yang benzoat, asam asetat, dan asam askorbat. Meskipun asam merupakan senyawa yang sangat bermanfaat, tetapi asam juga dapat menyebabkan berbagai kerusakan karena sangat bermanfaat, tetapi asam juga dapat menyebabkan berbagai kerusakan karena sifatnya yang korosif. Salah satunya adalah peristiwa hujan asam yang akhir-akhir ini sifatnya yang korosif. Salah satunya adalah peristiwa hujan asam yang akhir-akhir ini menimbulkan masalah lingkungan yang serius.
menimbulkan masalah lingkungan yang serius.
PENDAHULUAN
PENDAHULUAN
iv iv
B.
B. BasaBasa
Secara kimia, basa merupakan senyawa yang menghasilkan ion hidroksida (OH-) ketika Secara kimia, basa merupakan senyawa yang menghasilkan ion hidroksida (OH-) ketika larut dalam pelarut air. Adanya gugus OH- inilah yang menyebabkan senyawa basa larut dalam pelarut air. Adanya gugus OH- inilah yang menyebabkan senyawa basa memiliki sifat-sifat khas sebagai suatu basa.
memiliki sifat-sifat khas sebagai suatu basa. 1. Sifat-sifat basa:
1. Sifat-sifat basa: a.
a. pahit dan terasa licin di kulitpahit dan terasa licin di kulit b.
b. mengubah lakmus merah menjadi birumengubah lakmus merah menjadi biru c.
c. menghantarkan arus listrikmenghantarkan arus listrik d.
d. menetralkan sifat asammenetralkan sifat asam 2. Kekuatan basa
2. Kekuatan basa
Kekuatan basa sangat bergantung pada kemampuan basa tersebut melepaskan Kekuatan basa sangat bergantung pada kemampuan basa tersebut melepaskan OH-dalam larutan dan konse
dalam larutan dan konsentrasi basa tersebut. Berdntrasi basa tersebut. Berdasarkan asarkan hal tersebut, senyawa hal tersebut, senyawa basabasa dibagi menjadi dua basa kuat dan basa lemah. Semakin banyak ion OH- yang dilepaskan, dibagi menjadi dua basa kuat dan basa lemah. Semakin banyak ion OH- yang dilepaskan, maka kekuatan akan bertambah. Basa kuat bersifat korosif, sehingga peru berhati-hati maka kekuatan akan bertambah. Basa kuat bersifat korosif, sehingga peru berhati-hati dalam mengunakan zat tersebut. Contoh senyawa yang tergolong basa kuat adalah dalam mengunakan zat tersebut. Contoh senyawa yang tergolong basa kuat adalah natrium hidroksida (NaOH), kalium hidroksida (KOH), kalsium hidroksida natrium hidroksida (NaOH), kalium hidroksida (KOH), kalsium hidroksida (Ca(OH)2)sedangk
(Ca(OH)2)sedangkan an amonia (NH3) termaamonia (NH3) termasuk basa lemah.suk basa lemah. 3. Peranan Basa dalam kehidupan
3. Peranan Basa dalam kehidupan
Senyawa basa banyak digunakan dalam rumah tangga maupun di industri. Senyawa Senyawa basa banyak digunakan dalam rumah tangga maupun di industri. Senyawa basa dapat digunakan sebagai pembersih. Pemmbersih alat-alat dapur yang ada di basa dapat digunakan sebagai pembersih. Pemmbersih alat-alat dapur yang ada di pasaran mengandung natrium hidroksida yang berfungsi membersihkan noda minyak pasaran mengandung natrium hidroksida yang berfungsi membersihkan noda minyak atau mentega.pembersih lantai mengandung amonia yang daoat membersihkan debu. atau mentega.pembersih lantai mengandung amonia yang daoat membersihkan debu.
C.
C. GaramGaram
Garam merupakan senyawa yang terbentuk dari reaksi antara asam dengan basa. Selain Garam merupakan senyawa yang terbentuk dari reaksi antara asam dengan basa. Selain itu, garam juga dapat terbentuk dari reaksi antara logam dengan asam kuat encer.
itu, garam juga dapat terbentuk dari reaksi antara logam dengan asam kuat encer. Asam + Basa ---> Garam +
Asam + Basa ---> Garam + airair D.
D. pH dan IndicatorpH dan Indicator a). pH
a). pH
Sifat keasaman / kebasaan suatu
Sifat keasaman / kebasaan suatu zat dapat diketahui dengan menentukan pH zatzat dapat diketahui dengan menentukan pH zat tersebut. Skala pH (power of hydrogen) berkisar 0 sampai 14. Suatu asam
tersebut. Skala pH (power of hydrogen) berkisar 0 sampai 14. Suatu asam mempunyai pH yng lebih kecil dri
mempunyai pH yng lebih kecil dri 7 (pH <7).7 (pH <7).
b). Indicator b). Indicator
1. Indikator Universal 1. Indikator Universal
Indikator universal merupakan campuran dari bermacam-macam indikator yang
Indikator universal merupakan campuran dari bermacam-macam indikator yang
dapat menunjukkan pH suatu larutan
dapat menunjukkan pH suatu larutan dari perubahan warnanya.dari perubahan warnanya.
2. Indikator Kertas
2. Indikator Kertas
Indikator kertas berupa kertas serap dan tiap kotak kemasan indikator jenis ini
Indikator kertas berupa kertas serap dan tiap kotak kemasan indikator jenis ini
dilengkapi dengan peta warna.
v v
3. Indikator Larutan
3. Indikator Larutan
Salah satu contoh indikator universal jenis larutan adalah larutan metil jingga
Salah satu contoh indikator universal jenis larutan adalah larutan metil jingga
(Metil
(Metil Orange Orange = = MO). MO). Pada Pada pH pH kurang kurang dari dari 6 6 larutan ilarutan ini ni berwarna jingga,berwarna jingga,
sedangkan pada pH lebih dari 7 warnanya menjadi kuning.
vi vi
Kata Kata Pengantar ....Pengantar ... ... iiii
Pendahuluan Pendahuluan ... ... iiiiii
Daftar Daftar Isi Isi ... ... vivi
Asam, Asam, Basa, Basa, & & Garam Garam ... ... 11
a.
a. Sifat-sifat Sifat-sifat Asam, Asam, Basa, Basa, & & Garam Garam ... ... 22
b.
b. Identifikasi Identifikasi Asam, Asam, Basa, Basa, & & Garam Garam ... ... 88
c.
c. Penentuan Penentuan Skala Skala Keasaman Keasaman & & Kebasaan Kebasaan ... ... 1212
Laporan Laporan Praktikum Praktikum ... ... 1515
a.
a. Kertas Kertas Lakmus Lakmus Sebagai Sebagai Penentu Penentu Asam Asam Basa Basa ... ... 1717
b.
b. Indicator Indicator Universal Universal (pH) (pH) Sebagai Sebagai Penentu Penentu Asam Asam Basa Basa ... ... 1919
c.
c. Indicator Alami (Bunga Sepatu & Kol Ungu)Indicator Alami (Bunga Sepatu & Kol Ungu) Sebagai Penentu Asam Basa
Sebagai Penentu Asam Basa ... ... 2020
Kritik Kritik & & Saran Saran Dari Dari Kami Kami ... ... 2121
a.
a. Jauhar Jauhar Zainal Zainal Arifin Arifin ... .... 2222
b.
b. Wahidah Wahidah Koswulan Koswulan Sari Sari ...
c.
c. Ega Ega Oktaviane Oktaviane ...
d.
d. Kezia Kezia Tamariska Tamariska Seraf Seraf ...
e.
e. Friska Friska Dayanti Dayanti Nadeak Nadeak ...
Daftar Isi
Daftar Isi
Tahukah kamu bahwa sebagian
Tahukah kamu bahwa sebagian
besar
bahan
makanan
dan
besar
bahan
makanan
dan
minuman
minuman
yang
yang
kita
kita
konsumsi
konsumsi
sehari-hari bersifat asam, basa,
sehari-hari bersifat asam, basa,
atau garam? Pernahkah kamu
atau garam? Pernahkah kamu
makan semangkuk baso atau soto
makan semangkuk baso atau soto
yang
telah
diberi
cuka?
yang
telah
diberi
cuka?
Bagaimanakah rasanya? Apakah
Bagaimanakah rasanya? Apakah
cuka tersebut tergolong larutan asam? Apa ciri-ciri larutan
cuka tersebut tergolong larutan asam? Apa ciri-ciri larutan
yang bersifat asam, basa, atau garam? Bagaimana cara
yang bersifat asam, basa, atau garam? Bagaimana cara
menguji
menguji
suatu
suatu
larutan
larutan
itu
itu
tergolong
tergolong
asam,
asam,
basa
basa
atau
atau
garam? Mari kita pelajari bersama.
garam? Mari kita pelajari bersama.
ASAM, BASA,
ASAM, BASA,
& GARAM
& GARAM
“
“Selamat membaca!Selamat membaca!””
Tujuan pembelajaran
Tujuan pembelajaran
Setelahmempelajaribabini, Setelahmempelajaribabini, kamudiharapkandapat: kamudiharapkandapat: 1.mengelompokkansifatlaru 1.mengelompokkansifatlaru tanasam,larutanbasa,dan tanasam,larutanbasa,dan larutangarammelalui larutangarammelalui alatdanindikatoryang alatdanindikatoryang tepat; tepat; 2.melakukanpercobaansed 2.melakukanpercobaansed erhanadenganbahan-bahan erhanadenganbahan-bahan yangdiperolehdalam yangdiperolehdalam kehidupansehari-hari. kehidupansehari-hari. 1 1Materi: Asam, Basa, dan Garam
Materi: Asam, Basa, dan Garam
2
2
Bagaimana rasa permen vitamin C atau kuah bakso yang diberi
Bagaimana rasa permen vitamin C atau kuah bakso yang diberi
cuka? Tentu kamu akan menjawab rasanya masam. Pernahkah kamu mencicipi garam?
cuka? Tentu kamu akan menjawab rasanya masam. Pernahkah kamu mencicipi garam?
Bagaimana rasanya? Bagaimanakah rasa jamu? Rasanya pahit atau manis? Rasa
Bagaimana rasanya? Bagaimanakah rasa jamu? Rasanya pahit atau manis? Rasa
pahit merupakan salah satu sifat zat yang bersifat basa. Memang, sejak zaman
pahit merupakan salah satu sifat zat yang bersifat basa. Memang, sejak zaman
d
daahhuullu u aassaamm, , bbaassaa, , ddaan n ggaarraam m ssuuddaah h ddiikkeennaall, , kkaarreenna a bbaannyyaak k bbaahhaann
m
maakkaannaan n aattaau u mmiinnuummaan n yyaanng g ddiigguunnaakkaan n ddaallaam m kkeehhiidduuppaan n sseehhaarrii--hhaarrii
bersifat asam, basa atau garam. Coba kamu sebutkan contoh bahan makanan
bersifat asam, basa atau garam. Coba kamu sebutkan contoh bahan makanan
atau minuman yang bersifat asam.
atau minuman yang bersifat asam.
Istilah asam
Istilah asam (acid )(acid ) berasal dari bahasa Latin berasal dari bahasa Latin acetumacetum yang berarti cuka. yang berarti cuka.
Seperti diketahui, zat utama dalam cuka adalah asam asetat. Basa
Seperti diketahui, zat utama dalam cuka adalah asam asetat. Basa (alkali)(alkali)
berasal dari bahasa Arab yang berarti abu. Apakah sifat asam, basa, dan garam itu?
berasal dari bahasa Arab yang berarti abu. Apakah sifat asam, basa, dan garam itu?
Coba kamu perhatikan larutan pembersih porselin atau keramik. Apa yang terjadi jika
Coba kamu perhatikan larutan pembersih porselin atau keramik. Apa yang terjadi jika
larutan pembersih tersebut terkena lantai keramik? Coba kamu simpulkan
larutan pembersih tersebut terkena lantai keramik? Coba kamu simpulkan
sifat-sifat
sifat asam!. Pernahkah asam!. Pernahkah kamu mencuci kamu mencuci dengan deterdengan deterjen atau jen atau sabun? Apa sabun? Apa yangyang
kamu rasakan pada tanganmu itu? Apakah licin dan terasa panas? Seperti
kamu rasakan pada tanganmu itu? Apakah licin dan terasa panas? Seperti
halnya dengan sabun, basa bersifat kaustik (licin),selain itu basa juga bersifat
halnya dengan sabun, basa bersifat kaustik (licin),selain itu basa juga bersifat
alkali (bereaksi
alkali (bereaksi dengan protein dengan protein di dalam di dalam kulit kulit sehingga sel-sel sehingga sel-sel kulit akankulit akan
mengalami
mengalami pergantian). Kita pergantian). Kita dapat mengenali dapat mengenali asam asam dan basa dan basa dari rasanya.dari rasanya.
Namun, kita dilarang mengenali asam dan basa dengan cara mencicipi karena
Namun, kita dilarang mengenali asam dan basa dengan cara mencicipi karena
cara tersebut bukan merupakan cara yang aman. Bagaimanakah cara
cara tersebut bukan merupakan cara yang aman. Bagaimanakah cara mengidentifikasimengidentifikasi
asam dan basa
asam dan basa yang baik dan aman? yang baik dan aman? Kamu dapat mengenali asam Kamu dapat mengenali asam dan dan basabasa
dengan menggunakan indikator. Indikator yaitu suatu bahan yang dapat
dengan menggunakan indikator. Indikator yaitu suatu bahan yang dapat
bereaksi dengan asam, basa, atau garam sehingga akan menimbulkan
bereaksi dengan asam, basa, atau garam sehingga akan menimbulkan
perubahan warna.
perubahan warna.
gambar 1.1 Svante August A
gambar 1.1 Svante August Arrheniusrrhenius
1. Asam
1. Asam
Kamu sudah mengetahui jika asam merupakan salah satu penyusun dari
Kamu sudah mengetahui jika asam merupakan salah satu penyusun dari
berbagai bahan makanan dan minuman, misalnya cuka, keju,dan buah-buahan.
berbagai bahan makanan dan minuman, misalnya cuka, keju,dan buah-buahan.
Menurut Arrhenius, asam adalah zat yang dalam air akan melepaskan ion H
Menurut Arrhenius, asam adalah zat yang dalam air akan melepaskan ion H++..
Jadi, pembawa sifat asam adalah ion H
Jadi, pembawa sifat asam adalah ion H++(ion hidrogen), sehingga rumus kimia asam(ion hidrogen), sehingga rumus kimia asam
selalu mengandung
selalu mengandung atom hidrogen. atom hidrogen. Tahukah kamTahukah kamu perbedaan anu perbedaan antara tara ion, kation, ion, kation, dandan
an
anioion? n? IoIon adalah n adalah atom atom atau atau sekelosekelompok mpok atom atom yang yang bermuatbermuatan lian listrik. strik. KationKation
adalah ion yang bermuatan listrik positif. Adapun anion adalah ion yang
adalah ion yang bermuatan listrik positif. Adapun anion adalah ion yang
bermuatan listrik negatif. Sifat khas lain dari asam adalah dapat bereaksi
bermuatan listrik negatif. Sifat khas lain dari asam adalah dapat bereaksi
Svante August Arrhenius
Svante August Arrhenius
Svante August Arrhenius (19 Februari 1859
Svante August Arrhenius (19 Februari 1859 — —2 Oktober 1927) ialah2 Oktober 1927) ialah
seorang ilmuwan Swedia yang merupakan salah satu penggagas kimia fisik.
seorang ilmuwan Swedia yang merupakan salah satu penggagas kimia fisik.
Ia mendapat Penghargaan Nobel dalam Kimia atas karyanya mengenai
Ia mendapat Penghargaan Nobel dalam Kimia atas karyanya mengenai
ionisasi pada tahun 1903. Ia mengemukakan bahwa senyawa dalam larutan
ionisasi pada tahun 1903. Ia mengemukakan bahwa senyawa dalam larutan
dapat teru
dapat terurai menjadi rai menjadi ion-ionnya, ion-ionnya, dan dan kekuatan asam kekuatan asam dalam larutdalam larutan aquaan aqua
tergantung pada konsentrasi ion-ion hidrogen di dalamnya.
tergantung pada konsentrasi ion-ion hidrogen di dalamnya.
Tokoh IPA Tokoh IPA
Materi: Asam, Basa, dan Garam
Materi: Asam, Basa, dan Garam
3
3
dengan berbagai bahan seperti logam, marmer, dan keramik. Reaksi antara
dengan berbagai bahan seperti logam, marmer, dan keramik. Reaksi antara
asam dengan logam bersifat korosif. Contohnya, logam besi dapat bereaksi
asam dengan logam bersifat korosif. Contohnya, logam besi dapat bereaksi
cepat dengan asam klorida (HC
cepat dengan asam klorida (HCℓℓ) ) membemembentuk ntuk Besi Besi (II)(II)klklororidida (a (FeFeCCℓℓ22).).
Asam-asam apa
Asam-asam apa
sajakah
sajakah
yang
yang
ada
ada
dalam
dalam
kehidupan sehari-hari
kehidupan sehari-hari
kita? Mari kita cermati tabel berikut.
kita? Mari kita cermati tabel berikut.
Tabel 1.1 Beberapa asam yang dikenal
Tabel 1.1 Beberapa asam yang dikenal
Nama Asam
Nama Asam
Rumus Kimia
Rumus Kimia
Terdapat dalam
Terdapat dalam
Asam
Asam
Assetat
Assetat
CH
CH
22COOH
COOH
Larutan
Larutan
Cuka
Cuka
Asam
Asam
Askorbat
Askorbat
C
C
66H
H
88O
O
66Jeruk,
Jeruk,
tomat,
tomat,
sayuran
sayuran
Asam
Asam
Sitrat
Sitrat
C
C
66H
H
88O
O
77Jeruk
Jeruk
Asam
Asam
Borat
Borat
H
H
33BO
BO
33Larutan
Larutan
pencuci
pencuci
mata
mata
Asam
Asam
Karbonat
Karbonat
H
H
22CO
CO
33Minuman
Minuman
berkarbonasi
berkarbonasi
Asam
Asam
Klorida
Klorida
HC
HC
ℓℓ
Asam
Asam
lambung
lambung
Asam
Asam
Nitrat
Nitrat
HNO
HNO
33Pupuk,
Pupuk,
peledak
peledak
TNT
TNT
Asam
Asam
Fosfat
Fosfat
H
H
33PO
PO
44Deterjen,
Deterjen,
pupuk
pupuk
Asam
Asam
Tartrat
Tartrat
C
C
44H
H
66O
O
66Anggur
Anggur
Asam
Asam
Malat
Malat
C
C
44H
H
66O
O
55Apel
Apel
Asam
Asam
Formiat
Formiat
HCOOH
HCOOH
Sengatan
Sengatan
lebah
lebah
Asam
Asam
Laktat
Laktat
C
C
33H
H
66O
O
33Keju
Keju
Asam Benzoat
Asam Benzoat
Asam Sulfat
Asam Sulfat
Asam Brominda
Asam Brominda
Asam Sianida
Asam Sianida
C
C
66H
H
55COOH
COOH
H
H
22SO
SO
44HBr
HBr
HCN
HCN
Bahan pengawet makanan
Bahan pengawet makanan
Aki mobil
Aki mobil
Indikator terjadinya suatu reaksi kimia
Indikator terjadinya suatu reaksi kimia
Umbi-umbian, misalnya gadung
Umbi-umbian, misalnya gadung
Berdasarkan asalnya, asam dikelompokkan dalam 2 golongan,yaitu asam
Berdasarkan asalnya, asam dikelompokkan dalam 2 golongan,yaitu asam
org
organianik dan k dan asam anasam anorgorganikanik. Tahuk. Tahukah kamu aah kamu apa bedpa bedanyaanya?As?Asam am ororgaganinik k umumumumnynyaa
bersifat
bersifat asam asam lemah, lemah, korosif, korosif, dan dan banyak banyak terdapat terdapat di di alam. alam. AsamAsam
anorganik umumnya bersifat asam kuat dan korosif. Karena sifat-sifatnya itulah,
anorganik umumnya bersifat asam kuat dan korosif. Karena sifat-sifatnya itulah,
maka asam-asam anorganik banyak digunakan di berbagai kebutuhan manusia.
maka asam-asam anorganik banyak digunakan di berbagai kebutuhan manusia.
gambar 1.2 Jeruk purut dan keju sebagai contoh
gambar 1.2 Jeruk purut dan keju sebagai contoh dari asamdari asam
Asam
Asam sitrat sitrat terdapat terdapat pada pada berbagai berbagai jenis jenis buah buah dan dan sayuran. sayuran. AsamAsam
sitrat yang konsentrasi tinggi, mencapai 8% bobot kering, terdapat pada jeruk
sitrat yang konsentrasi tinggi, mencapai 8% bobot kering, terdapat pada jeruk
lemon dan limau (misalnya jeruk nipis dan jeruk purut).Rumus kimia asam
lemon dan limau (misalnya jeruk nipis dan jeruk purut).Rumus kimia asam
sitrat adalah C
Materi: Asam, Basa, dan Garam
Materi: Asam, Basa, dan Garam
4
4
2. Basa
2. Basa
Jika kamu mencuci tangan dengan sabun, apa yang kamu rasakan pada
Jika kamu mencuci tangan dengan sabun, apa yang kamu rasakan pada
tanganmu? Dalam keadaan murni, basa umumnya berupa kristal padat dan
tanganmu? Dalam keadaan murni, basa umumnya berupa kristal padat dan
bersifat kaustik. Beberapa produk rumah tangga seperti deodoran, obat maag
bersifat kaustik. Beberapa produk rumah tangga seperti deodoran, obat maag
(antacid) , sabun ,serta deterjen mengandung basa. Basa adalah suatu
(antacid) , sabun ,serta deterjen mengandung basa. Basa adalah suatu
senyawa yang jika dilarutkan dalam air(larutan) dapat melepaskan ion
senyawa yang jika dilarutkan dalam air(larutan) dapat melepaskan ion
hidroksida (OH
hidroksida (OH--). Oleh karena itu,semua rumus kimia basa umumnya). Oleh karena itu,semua rumus kimia basa umumnya
mengandung gugus OH. Jika diketahui rumus kimia suatu basa, maka untuk
mengandung gugus OH. Jika diketahui rumus kimia suatu basa, maka untuk
memberi nama
memberi nama basa, basa, cukup cukup dengan menyebut dengan menyebut nama nama logam logam dan dan diikuti katadiikuti kata
hidroksida.
hidroksida.
Tahukah kamu, basa apa yang ada di sekitar kita? Mari kita cermati tabel
Tahukah kamu, basa apa yang ada di sekitar kita? Mari kita cermati tabel
berikut ini.
berikut ini.
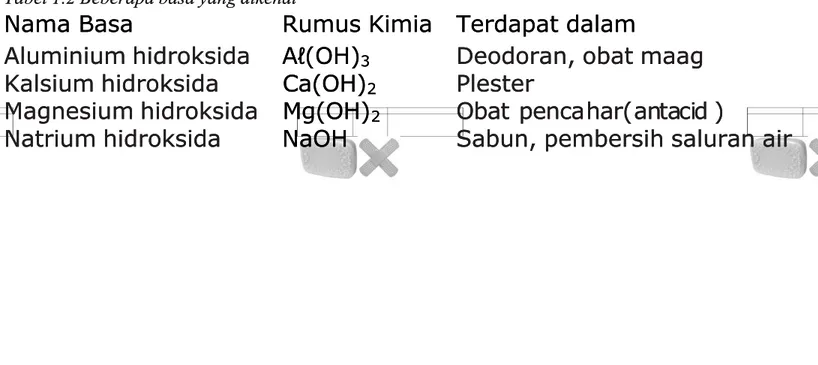
Tabel 1.2 Beberapa basa yang dikenal
Tabel 1.2 Beberapa basa yang dikenal
Nama
Nama Basa
Basa
Rumus
Rumus Kimia
Kimia Terdapat
Terdapat dalam
dalam
Aluminium hidroksida
Aluminium hidroksida
A
Aℓℓ(OH)
(OH)
33Deodoran, obat maag
Deodoran, obat maag
Kalsium hidroksida
Kalsium hidroksida
Ca(OH)
Ca(OH)
22Plester
Plester
Magnesium hidroksida
Magnesium hidroksida
Mg(OH)
Mg(OH)
22Obat
Obat
penca
penca
har(
har(
an
an
ta
ta
ci
ci
d )
d )
Natrium hidroksida
Natrium hidroksida
NaOH
NaOH
Sabun, pembersih saluran air
Sabun, pembersih saluran air
Gambar 1.3 sabun dan plester sebagai contoh dari
Gambar 1.3 sabun dan plester sebagai contoh dari basabasa
3. Garam
3. Garam
Jika mendengar kata ”garam”, pastilah
Jika mendengar kata ”garam”, pastilahyang terbyang terbayang pada benaayang pada benak k mu amu adadalalahh
garam dapur. Garam dapur memang merupakan salah s
garam dapur. Garam dapur memang merupakan salah satu contoh garam.atu contoh garam.
Dalam kehidupan sehari-hari pernahkah kamu melihat orang yang sakit
Dalam kehidupan sehari-hari pernahkah kamu melihat orang yang sakit
perut(maag dan sejenisnya)? Tahukah kamu mengapa orang yang sakit maag
perut(maag dan sejenisnya)? Tahukah kamu mengapa orang yang sakit maag
minum obat sakit maag atau
minum obat sakit maag atau antacid? Apakah antacid itu? Orang mengalamiantacid? Apakah antacid itu? Orang mengalami
sakit
sakit perut perut disebabkan disebabkan asam asam lambung lambung yang yang meningkat. meningkat. Untuk Untuk menetralkanmenetralkan
asam lambung (HCℓ) digunakan
asam lambung (HCℓ) digunakan antacid . Antacid mengandung basa yang dapatantacid . Antacid mengandung basa yang dapat
menetralkan kelebihan asam lambung (HCℓ).
menetralkan kelebihan asam lambung (HCℓ).
Umumnya zat-zat dengan sifat yang berlawanan, seperti asam dan basa
Umumnya zat-zat dengan sifat yang berlawanan, seperti asam dan basa
cenderung bereaksi membentuk zat baru. Bila larutan asam direaksikan
cenderung bereaksi membentuk zat baru. Bila larutan asam direaksikan
dengan larutan basa, maka ion H
dengan larutan basa, maka ion H++ dari asam akan bereaksi dengan ion OHdari asam akan bereaksi dengan ion OH-- daridari
basa membentuk molekul air.
basa membentuk molekul air.
H
H
++(aq)
(aq)
+
+
OH
OH
--(aq)
(aq)
H
H
22O
O
(ℓ)
(ℓ)
Asam
Materi: Asam, Basa, dan Garam
Materi: Asam, Basa, dan Garam
5
5
Karena air bersifat netral, maka reaksi asam dengan basa disebut
Karena air bersifat netral, maka reaksi asam dengan basa disebut
reaksi penetralan(netralisasi).
reaksi penetralan(netralisasi).
Apak
Apakah terah terjadi rjadi reakseaksi antai antara ion ra ion neganegatif datif dari asam ri asam dan iodan ion posin positif tif lologagam m dadari ri babasasa??
Ion-ion ini akan bergabung membentuk senyawa ion yang disebut garam. Bila
Ion-ion ini akan bergabung membentuk senyawa ion yang disebut garam. Bila
garam yang terbentuk ini mudah larut dalam air, maka ion-ionnya akan tetap
garam yang terbentuk ini mudah larut dalam air, maka ion-ionnya akan tetap
ada
ada di di dalam dalam larutan. larutan. Tetapi Tetapi jika jika garam garam itu itu sukar sukar larut larut dalam dalam air, air, maka maka ion-
ion-ionnya akan bergabung membentuk suatu endapan.
ionnya akan bergabung membentuk suatu endapan. Jadi, reaksi asam denganJadi, reaksi asam dengan basa disebut juga reaksi penggaraman karena membentuk senyawa garam. Mari basa disebut juga reaksi penggaraman karena membentuk senyawa garam. Mari kita simak contoh reaksi pembentukan garam berikut!
kita simak contoh reaksi pembentukan garam berikut!
Asam
Asam +
+ Basa
Basa
Garam
Garam +
+ Air
Air
Asam
Asam klorida
klorida +
+ Natrium
Natrium hidroksida
hidroksida
Natrium
Natrium klorida
klorida +
+ Air
Air
HCℓ(aq) + NaOH(aq)
HCℓ(aq) + NaOH(aq)
NaCℓ(aq)
NaCℓ(aq) +
+ H
H
22O(ℓ)
O(ℓ)
Asam
Asam
Basa
Basa
Garam
Garam
Air
Air
Walaupun reaksi asam dengan basa disebut reaksi penetralan, tetapi hasil Walaupun reaksi asam dengan basa disebut reaksi penetralan, tetapi hasil reaksi(garam) tidak selalu bersifat netral. Sifat asam basa dari larutan garam reaksi(garam) tidak selalu bersifat netral. Sifat asam basa dari larutan garam bergantung pada kekuatan asam dan basa penyusunnya.
bergantung pada kekuatan asam dan basa penyusunnya.
Garam yang berasal dari asam kuat dan
Garam yang berasal dari asam kuat dan
basa
basa kuat kuat bersifat bersifat netral, netral, disebut disebut garamgaram
normal, contohnya NaC
normal, contohnya NaCℓℓ dan dan KNOKNO33. Garam yang. Garam yang
berasal
berasal dari dari asam asam kuat kuat dan dan basa basa lemah lemah bersifatbersifat
asam dan disebut garam asam, contohnya adalah
asam dan disebut garam asam, contohnya adalah
NH
NH44CCℓℓ. Garam yang berasal dari asam lemah dan. Garam yang berasal dari asam lemah dan
basa kuat bersifat basa dan disebut garam basa,
basa kuat bersifat basa dan disebut garam basa,
contohnya adalah CH
contohnya adalah CH33COONa. Contoh asam kuatCOONa. Contoh asam kuat
adalah HC
adalah HCℓℓ, HNO, HNO33,, HH22SOSO44. Adapun KOH, NaOH, Ca(OH). Adapun KOH, NaOH, Ca(OH)2.2.
gambar 1.4 garam
gambar 1.4 garam
Simaklah be
Simaklah beberapa garberapa garam yang am yang telah telah dikenal dikenal dalam kehidupan dalam kehidupan sehari-
sehari-hari pada tabel berikut. Apa sajakah garam yang ada dalam kehidupan kita?
hari pada tabel berikut. Apa sajakah garam yang ada dalam kehidupan kita?
Tabel 1.3 Beberapa garam yang dikenal
Tabel 1.3 Beberapa garam yang dikenal
Nama
Nama Garam
Garam
Rumus
Rumus Kimia
Kimia Nama
Nama Dagang
Dagang Kegunaan
Kegunaan
Natrium klorida
Natrium klorida
NaCℓ
NaCℓ
Garam
Garam dapur
dapur
Penambah
Penambah rasa
rasa
Kalsium
Kalsium karbonat
karbonat
CaCO
CaCO
33Kalsit
Kalsit
Bahan cat
Bahan
cat
Kalium
Kalium nitrat
nitrat
KNO
KNO
33Salpeter
Salpeter
Pupuk
Pupuk
Kalium
Kalium karbonat
karbonat
K
K
22CO
CO
33Potas
Potas
Bahan
Bahan sabun
sabun
Natrium
Natrium fosfat
fosfat
Na
Na
33PO
PO
44TSP
TSP
Bahan
Bahan deterjen
deterjen
Amonium klorida
Amonium klorida
Magnesium Sulfat
Magnesium Sulfat
Natrium bikarbonat
Natrium bikarbonat
Kalium sianida
Kalium sianida
Monosodium glutamat Monosodium glutamatNH
NH
44Cℓ
Cℓ
MgSO
MgSO
44NaHCO
NaHCO
33KCN
KCN
MSG
MSG
Salmoniak
Salmoniak
Garam inggris
Garam inggris
Soda kue
Soda kue
Potas
Potas
Penyedap rasa
Penyedap rasa
Bahan baterai
Bahan baterai
Obat pencahar
Obat pencahar
Pengembang kue
Pengembang kue
Potas
Potas
Penyedap rasa
Penyedap rasa
Materi: Asam, Basa, dan Garam
Materi: Asam, Basa, dan Garam
6
6
4.
4.
Larutan
Larutan
Asam,
Asam,
Basa,
Basa,
dan
dan
Garam
Garam
Bersifat Elektrolit
Bersifat Elektrolit
Pernahkah kamu melihat seseorang mencari ikan dengan menggunakan
Pernahkah kamu melihat seseorang mencari ikan dengan menggunakan
”setrum”
”setrum” atau aliran listrik yang berasal dari aki? Apa yang terjadi setelah atau aliran listrik yang berasal dari aki? Apa yang terjadi setelah
beberapa saat ujung alat yang telah dialiri arus listrik itu dicelupkan ke dalam air
beberapa saat ujung alat yang telah dialiri arus listrik itu dicelupkan ke dalam air
sungai? Ternyata ikan yang berada disekitar ujung alat itu terkena aliran listrik
sungai? Ternyata ikan yang berada disekitar ujung alat itu terkena aliran listrik
dan pingsan atau mati. Apakah
dan pingsan atau mati. Apakah air dapat menghantarkan listrik?air dapat menghantarkan listrik?
Sebenarnya air murni adalah penghantar listrik yang buruk. Akan tetapi bila
Sebenarnya air murni adalah penghantar listrik yang buruk. Akan tetapi bila
dilarutkan asam, basa, atau garam ke dalam air maka larutan ini dapat menghantarkan
dilarutkan asam, basa, atau garam ke dalam air maka larutan ini dapat menghantarkan
arus listrik. Zat-zat yang larut dalam air dan dapat membentuk suatu larutan
arus listrik. Zat-zat yang larut dalam air dan dapat membentuk suatu larutan
yang menghantarkan arus listrik dinamakan larutan elektrolit. Contohnya adalah
yang menghantarkan arus listrik dinamakan larutan elektrolit. Contohnya adalah
larutan garam dapur dan larutan asam klorida. Zat yang tidak menghantarkan
larutan garam dapur dan larutan asam klorida. Zat yang tidak menghantarkan
arus listrik dinamakan larutan non elektrolit. Contohnya adalah larutan gula dan
arus listrik dinamakan larutan non elektrolit. Contohnya adalah larutan gula dan
larutan urea.
larutan urea.
Untuk mengetahui suatu larutan dapat menghantarkan arus listrik atau
Untuk mengetahui suatu larutan dapat menghantarkan arus listrik atau
tidak, dapat diuji dengan alat penguji elektrolit. Alat penguji elektrolit sederhana terdiri
tidak, dapat diuji dengan alat penguji elektrolit. Alat penguji elektrolit sederhana terdiri
dari dua elektroda yang dihubungkan dengan sumber arus listrik searah dan
dari dua elektroda yang dihubungkan dengan sumber arus listrik searah dan
dilengkapi dengan lampu ,serta bejana yang berisi larutan yang akan diuji. Mari
dilengkapi dengan lampu ,serta bejana yang berisi larutan yang akan diuji. Mari
kita lakukan kegiatan berikut untuk mengetahui apakah asam, basa, dan garam
kita lakukan kegiatan berikut untuk mengetahui apakah asam, basa, dan garam
dapat menghantarkan arus listrik.
dapat menghantarkan arus listrik.
Kegiatan Ilmiah .1
Kegiatan Ilmiah .1
Uji Larutan Berdasarkan Daya Hantar Listrik
Uji Larutan Berdasarkan Daya Hantar Listrik
Tujuan
Tujuan
Menguji larutan berdasarkan daya hantar listriknya
Menguji larutan berdasarkan daya hantar listriknya
A
Allaat t ddaan n BBaahhaann
1.
1. Gelas Gelas kimia kimia 5. 5. Larutan Larutan NaCNaC
ℓℓ
2.
2. Elektroda Elektroda karbon karbon 6. 6. Larutan Larutan asam asam cukacuka
3.
3. Baterai Baterai 7. 7. Larutan Larutan NaOHNaOH
4.
4. Bola Bola lampu lampu 8. 8. Larutan Larutan gulagula
Petunjuk Kerja
Petunjuk Kerja
1. Rangkailah alat uji elektrolit seperti tampak pada gambar di atas.
1. Rangkailah alat uji elektrolit seperti tampak pada gambar di atas.
2. Isilah gelas dengan larutan asam
2. Isilah gelas dengan larutan asam asetat.asetat.
3. Celupkan elektroda ke dalam larutan
3. Celupkan elektroda ke dalam larutan asam asetat.asam asetat.
4. Amatilah bola lampu,
Materi: Asam, Basa, dan Garam
Materi: Asam, Basa, dan Garam
7
7
5. Ulangi kegiatan di atas
5. Ulangi kegiatan di atas dengan mengganti larutan asam asetat dengan larutandengan mengganti larutan asam asetat dengan larutan
NaOH ,larutan NaC
NaOH ,larutan NaC
ℓℓ
, dan larutan gula , dan larutan gula secara bergantian.secara bergantian.6. Catat hasil pengamatan dalam tabel.
6. Catat hasil pengamatan dalam tabel.
7. Buatlah kesimpulan dari hasil kegiatan dan diskusikan bersama teman satu kelompok.
7. Buatlah kesimpulan dari hasil kegiatan dan diskusikan bersama teman satu kelompok.
Tabel 1.4 Hasil pengamatan uji larutan elektrolit dan
Tabel 1.4 Hasil pengamatan uji larutan elektrolit dan non elektrolitnon elektrolit
No.
Larutan
No.
Larutan
Nyala
Nyala
Lampu
Lampu
Gelembung
Gelembung
gas
gas
Terang
Terang
Redup
Redup
Padam
Padam
Ada
Ada
Tidak
Tidak
ada
ada
Pertanyaan
Pertanyaan
1. Apa yang disebut dengan larutan?
1. Apa yang disebut dengan larutan?
2. Apa yang disebut dengan larutan elektrolit kuat, larutan elektrolit lemah, dan
2. Apa yang disebut dengan larutan elektrolit kuat, larutan elektrolit lemah, dan
larut-an non elektrolit?
an non elektrolit?
3. Berdasarkan kegiatan yang kamu lakukan, berilah contoh larutan elektrolit
3. Berdasarkan kegiatan yang kamu lakukan, berilah contoh larutan elektrolit lemah,lemah,
kuat,dan non elektrolit.
Materi: Asam, Basa, dan Garam
Materi: Asam, Basa, dan Garam
8
8
B a n y a k s e k a l i l a r u t a n d i s e k i t a r k i t a , b a i k y a n g b e r s i f a t
B a n y a k s e k a l i l a r u t a n d i s e k i t a r k i t a , b a i k y a n g b e r s i f a t
a
assaamm, , basa, basa, maupun maupun netranetral. Tl. Tahukah ahukah kamu kamu bagaimbagaimana ana cara cara menemenentukan ntukan sisifafatt
asam dan basa larutan secara tepat? Indikator yang dapat digunakan
asam dan basa larutan secara tepat? Indikator yang dapat digunakan
adalah indikator asam basa. Indikator adalah zat-zat yang
adalah indikator asam basa. Indikator adalah zat-zat yang
menunjukkan indikasi berbeda dalam larutan asam, basa, dan garam.
menunjukkan indikasi berbeda dalam larutan asam, basa, dan garam.
Cara menentukan senyawa bersifat asam, basa, atau netral dapat menggunakan
Cara menentukan senyawa bersifat asam, basa, atau netral dapat menggunakan
kertas lakmus dan larutan indikator atau indikator alami. Berikut adalah
kertas lakmus dan larutan indikator atau indikator alami. Berikut adalah
beberapa cara menguji sifat larutan.
beberapa cara menguji sifat larutan.
1.
1.
Identitif
Identitif
ikasi
ikasi
Larutan
Larutan
Asam
Asam
dan
dan
Larutan
Larutan
Basa
Basa
Menggunakan Kertas Lakmus
Menggunakan Kertas Lakmus
Warna kertas
Warna kertas lakmus lakmus dalam larutan dalam larutan asam, larutan asam, larutan basa basa dan larutandan larutan
bersifat netral berbeda. Ada dua macam kertas lakmus, yaitu lakmus merah dan
bersifat netral berbeda. Ada dua macam kertas lakmus, yaitu lakmus merah dan
lakmus biru. Sifat
lakmus biru. Sifat dari masing-masing kertas dari masing-masing kertas lakmus lakmus tersebut adalah sebagaitersebut adalah sebagai
berikut.
berikut.
a. Lakmus merah dalam larutan asam berwarna merah dan dalam larutan basa
a. Lakmus merah dalam larutan asam berwarna merah dan dalam larutan basa
berwarna biru.
berwarna biru.
b. Lakmus biru dalam larutan asam berwarna merah dan dalam larutan basa
b. Lakmus biru dalam larutan asam berwarna merah dan dalam larutan basa
berwarna biru.\
berwarna biru.\
c. Lakmus merah maupun bir
c. Lakmus merah maupun biru dalam larutan netrau dalam larutan netral tidak berubah wal tidak berubah warnrnaa
Agar kamu lebih paham mengenai materi ini, mari k
Agar kamu lebih paham mengenai materi ini, mari kita lakukan kegiatanita lakukan kegiatan
berikut.
berikut.
Kegiatan Ilmiah .2
Kegiatan Ilmiah .2
Identi
Identi
fi
fi
kasi Larutan Asam, Basa,dan Garam
kasi Larutan Asam, Basa,dan Garam
Menggunakan Kertas Lakmus
Menggunakan Kertas Lakmus
Tujuan
Tujuan
Mengidentifikasi larutan asam, basa, dan
Mengidentifikasi larutan asam, basa, dan garam menggunakan kertas lakmusgaram menggunakan kertas lakmus..
Alat dan Bahan
Alat dan Bahan
gambar 1.5 kertas lak
gambar 1.5 kertas lakmus merah dalam lmus merah dalam larutan basa berwarna biru, daarutan basa berwarna biru, dan kertas lakmus biru daln kertas lakmus biru dalam larutanam larutan asam berwarna merah
Materi: Asam, Basa, dan Garam
Materi: Asam, Basa, dan Garam
9
9
1. Gelas plastik/gelas kimia
1. Gelas plastik/gelas kimia
2. Pelat tetes 2. Pelat tetes 3. Pipet tetes 3. Pipet tetes 4. Kertas lakmus 4. Kertas lakmus
5. Bahan-bahan kimia dalam kehidupan sehari-hari, seperti
5. Bahan-bahan kimia dalam kehidupan sehari-hari, seperti
cuka, air aki, teh, sabun, kapur,air sumur, garam, dan air jeruk.
cuka, air aki, teh, sabun, kapur,air sumur, garam, dan air jeruk.
Petunjuk Kerja
Petunjuk Kerja
1. Kumpulkan bahan-bahan kimia dalam
1. Kumpulkan bahan-bahan kimia dalam kehidupan sehari-kehidupan
sehari-hari yang berupa bahan padatatau larutan.
hari yang berupa bahan padatatau larutan.
2. Larutkan bahan-bahan yang padat tersebut ke dalam air.
2. Larutkan bahan-bahan yang padat tersebut ke dalam air.
3. Masukkan atau celupkan kertas lakmus ke dalam cekungan-cekungan pelat tetes.
3. Masukkan atau celupkan kertas lakmus ke dalam cekungan-cekungan pelat tetes.
4. Teteskan dengan pipet tetes asam, basa, dan
4. Teteskan dengan pipet tetes asam, basa, dan netral dari bahan-netral dari
bahan-bahan tersebut padalakmus yang terdapat di dalam cekungan pelat tetes.
bahan tersebut padalakmus yang terdapat di dalam cekungan pelat tetes.
5. Catat hasil pengamatan dalam tabel
5. Catat hasil pengamatan dalam tabel dandanklasifikasikan bahanklasifikasikan bahan-bahan tersebut-bahan tersebut
berdasar-kan sifatnya.
berdasar-kan sifatnya.
6. Buatlah kesimpulan dari hasil kegiatan dan
6. Buatlah kesimpulan dari hasil kegiatan dan susunlah laporannya.susunlah laporannya.
Tabel 1.5 Hasil pengamatan identifikasi larutan dengan kertas lakmus
Tabel 1.5 Hasil pengamatan identifikasi larutan dengan kertas lakmus
No. Bahan-bahan
No. Bahan-bahan Hasil pengamatanHasil pengamatan
menggunakan lakmus
menggunakan lakmus Asam Asam Basa Basa NetralNetral
1.
1. Larutan Larutan cukacuka
2.
2. Air Air jerukjeruk
3.
3. Air Air akiaki
4.
4. Larutan Larutan gulagula
5.
5. Larutan Larutan sabunsabun
6.
6. Larutan Larutan kapurkapur
7.
7. Air Air tehteh
8.
8. Air Air sumursumur
9.
9. Larutan Larutan garam garam dapurdapur
Pertanyaan
Pertanyaan
1. Apa yang terjadi pada kertas lakmus jika ditetesi dengan larutan asam, basa, atau larutan
1. Apa yang terjadi pada kertas lakmus jika ditetesi dengan larutan asam, basa, atau larutan
netral?
netral?
2. Mengapa larutan yang netraltidak dapat menunjukkan perubahan warna pada
2. Mengapa larutan yang netraltidak dapat menunjukkan perubahan warna pada
lak-mus?
mus?
2. Identitifikasi Larutan Asam dan Larutan Basa
2. Identitifikasi Larutan Asam dan Larutan Basa
Menggunakan Indikator Alami
Menggunakan Indikator Alami
Percobaan yang telah kamu lakukan adalah mengidentifikasi suatu larutan
Percobaan yang telah kamu lakukan adalah mengidentifikasi suatu larutan
bersifat asam, basa atau netral dengan menggunakan kertas lakmus. Adakah
bersifat asam, basa atau netral dengan menggunakan kertas lakmus. Adakah
cara lain untuk
cara lain untuk mengidentimengidentififikasi suatu larutan? Ada beberapa cara yangkasi suatu larutan? Ada beberapa cara yang
dapat kamu lakukan sendiri di rumah,yaitu dengan menggunakan indikator
dapat kamu lakukan sendiri di rumah,yaitu dengan menggunakan indikator
alami. Berbagai bunga yang berwarna atau tumbuhan, seperti daun, mahkota
alami. Berbagai bunga yang berwarna atau tumbuhan, seperti daun, mahkota
bunga, kunyit, kulit manggis, dan kubis ungu dapat digunakan sebagai indikator
Materi: Asam, Basa, dan Garam
Materi: Asam, Basa, dan Garam
10
10
asam basa. Ekstrak atau sari dari bahan-bahan ini dapat menunjukkan warna
asam basa. Ekstrak atau sari dari bahan-bahan ini dapat menunjukkan warna
yang berbeda dalam larutan asam basa.
yang berbeda dalam larutan asam basa.
Sebagai contoh, ambillah kulit manggis, tumbuklah sampai halus dan
Sebagai contoh, ambillah kulit manggis, tumbuklah sampai halus dan
campur dengan sedikit air. Warna kulit manggis adalah ungu (dalam keadaan
campur dengan sedikit air. Warna kulit manggis adalah ungu (dalam keadaan
netral). Jika
netral). Jika ekstrak ekstrak kulit manggis kulit manggis dibagi dua dibagi dua dan masing-masing dan masing-masing diteteskanditeteskan
larutan asam dan basa, maka dalam larutan asam terjadi perubahan warna dari
larutan asam dan basa, maka dalam larutan asam terjadi perubahan warna dari
ungu menjadi cokelat kemerahan. Larutan basa yang diteteskan akan mengubah
ungu menjadi cokelat kemerahan. Larutan basa yang diteteskan akan mengubah
warna dari ungu menjadi biru kehitaman.
warna dari ungu menjadi biru kehitaman.
Agar kamu lebih paham dengan pokok bahasan ini, mari kita lakukan
Agar kamu lebih paham dengan pokok bahasan ini, mari kita lakukan
kegiatan berikut.
kegiatan berikut.
Kegiatan Ilmiah .3
Kegiatan Ilmiah .3
Identi
Identi
fi
fi
kasi Larutan Asam, Basa, dan Garam
kasi Larutan Asam, Basa, dan Garam
Menggunakan Indikator Alami
Menggunakan Indikator Alami
Tujuan
Tujuan
Mengidentifikasi larutan
Mengidentifikasi larutan asam, basa, asam, basa, dan dan garam dengan garam dengan menggunakan indikatormenggunakan indikator
alami
alami
Alat dan Bahan
Alat dan Bahan
1.
1. Lumpang Lumpang dan dan alu alu 7. 7. Air Air kapurkapur
2.
2. Corong Corong 8. 8. Air Air sulingsuling
3.
3. Tabung Tabung reaksi reaksi 9. 9. Larutan Larutan NaOHNaOH
4.
4. Pipet Pipet tetes tetes 10. 10. Larutan Larutan HCHC
ℓℓ
5.
5. Gelas Gelas ukur ukur 11. 11. Larutan Larutan garam garam dapurdapur
6.
6. Bunga Bunga berwarna berwarna atau atau bahan bahan alam alam 12. 12. Larutan Larutan cukacuka
Petunjuk Kerja
Petunjuk Kerja
1. Siapkan berbagaimacam bunga berwarna atau bahan alam (misalnya bunga sepa
1. Siapkan berbagaimacam bunga berwarna atau bahan alam (misalnya bunga sepa
-tu, bunga mawar, kunyit,
-tu, bunga mawar, kunyit, bougenvilebougenvile, dan bunga kana)., dan bunga kana).
2. Siapkan lumpang dan alu.
2. Siapkan lumpang dan alu.
3.
3. Tumbuklah Tumbuklah bahan-bahan bahan-bahan tersebut tersebut dengan dengan menggerusnya menggerusnya dan dan tambahkan tambahkan airair
± 5ml. Kemudian, amati
± 5ml. Kemudian, amati indikator warnanya.indikator warnanya.
4. Siapkan 5 tabung reaksi yang berisi
4. Siapkan 5 tabung reaksi yang berisi larutan yang akan diuji.larutan yang akan diuji.
5. Masukkan masing-masing 1 ml ekstrak ke dalam
5. Masukkan masing-masing 1 ml ekstrak ke dalam 5 tabung reaksi.5 tabung reaksi.
6. Masukkan masingmasing 5 tetes larutan cuka ke
6. Masukkan masingmasing 5 tetes larutan cuka ke dalam tabung reaksi 1, larutandalam tabung reaksi 1, larutan
natrium klorida ke dalam tabung 2, dan larutan natrium hidroksida ke dalam tabung
natrium klorida ke dalam tabung 2, dan larutan natrium hidroksida ke dalam tabung
3. Amati perubahan warna indikator dalam l
3. Amati perubahan warna indikator dalam larutan.arutan.
gambar 1.6 indikator alami :
Materi: Asam, Basa, dan Garam
Materi: Asam, Basa, dan Garam
11
11
7. Lakukan dengan cara yang sama untuk ektrak bahan lain
7. Lakukan dengan cara yang sama untuk ektrak bahan lain dan dalam larutan lainndan dalam larutan lainn
ya.
ya.
8. Catat perubahan warna indikator alami
8. Catat perubahan warna indikator alami tersebut ke dalam tabel.tersebut ke dalam tabel.
9. Buatlah kesimpulan dari hasil kegiatan, kemudian diskusikan dengan teman satu
9. Buatlah kesimpulan dari hasil kegiatan, kemudian diskusikan dengan teman satu
kelompok.
kelompok.
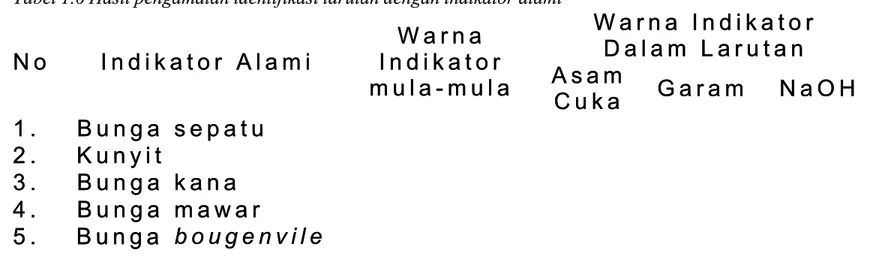
Tabel 1.6 Hasil pengamatan identifikasi larutan dengan indikator alami
Tabel 1.6 Hasil pengamatan identifikasi larutan dengan indikator alami
N o N o I n d i k a t o r A l a m iI n d i k a t o r A l a m i W a r n a W a r n a I n d i k a t o r I n d i k a t o r m u l a - m u l a m u l a - m u l a W a r n a I n d i k a t o r W a r n a I n d i k a t o r D a l a m L a r u t a n D a l a m L a r u t a n A A ss aa mm C u k a C u k a G a r a m G a r a m N a O HN a O H 1 . 1 . B u n g a B u n g a s e p a t us e p a t u 2 . K u n y i t 2 . K u n y i t 3 . 3 . B u n g a B u n g a k a n ak a n a 4 . 4 . B u n g a B u n g a m a w a rm a w a r 5 . B u n g a 5 . B u n g a b o u g e n v i l eb o u g e n v i l e Pertanyaan Pertanyaan
1. Perubahan warna apa yang terjadi
1. Perubahan warna apa yang terjadi pada ekstrak yang ditetesi dengan larutanpada ekstrak yang ditetesi dengan larutan
asam, basa atau larutan netral?
asam, basa atau larutan netral?
2 . M e n g a p a l a r u t a n y a n g n e t r a l t i d a k d a p a t
2 . M e n g a p a l a r u t a n y a n g n e t r a l t i d a k d a p a t
m e n u n j u k k a n p e r u b a h a n w a r n a p a d a e k s t r a k ?
Materi: Asam, Basa, dan Garam
Materi: Asam, Basa, dan Garam
12
12
1. Kekuatan Asam & Basa
1. Kekuatan Asam & Basa
Masih ingatkah kamu dengan sifat asam dan basa? Misalnya bebe-rapa jenis
Masih ingatkah kamu dengan sifat asam dan basa? Misalnya bebe-rapa jenis
asa
asam m dapdapat at dimdiminum inum ataatau u dikdikonsonsumsumsi, i, sebsebalikaliknya nya ada ada bebebeberarapa apa asasam yam yangng
berbahaya bila kena kulit, karena dapat merusak jaringan. Asam juga dapat merusak
berbahaya bila kena kulit, karena dapat merusak jaringan. Asam juga dapat merusak
logam dan keramik.
logam dan keramik.
Apakah asam dan basa mempunyai kekuatan yang sama?
Apakah asam dan basa mempunyai kekuatan yang sama?
Kekuatan suatu asam atau basa tergantung bagaimana senyawa tersebut dapat
Kekuatan suatu asam atau basa tergantung bagaimana senyawa tersebut dapat
diuraikan menjadi ion-ion dalam air. Peristiwa terurainya suatu zat menjadi
diuraikan menjadi ion-ion dalam air. Peristiwa terurainya suatu zat menjadi
ion-ionnya dalam air disebut ionisasi. Asam atau basa yang terionisasi
ion-ionnya dalam air disebut ionisasi. Asam atau basa yang terionisasi
secara sempurna dalam larutan merupakan asam kuat atau basa kuat.
secara sempurna dalam larutan merupakan asam kuat atau basa kuat.
Sebaliknya asam atau basa yang hanya terionisasi sebagian merupakan asam
Sebaliknya asam atau basa yang hanya terionisasi sebagian merupakan asam
lemah atau basa lemah.
lemah atau basa lemah.
Jika ingin mengetahui kekuatan asam dan basa kamu dapat melakukan
Jika ingin mengetahui kekuatan asam dan basa kamu dapat melakukan
percobaan sederhana. Perhatikan nyala lampu saat mengadakan
percobaan sederhana. Perhatikan nyala lampu saat mengadakan
percobaan uji larutan elektrolit. Bila nyala lampu redup berarti larutan
percobaan uji larutan elektrolit. Bila nyala lampu redup berarti larutan
tergolong asam atau basa lemah, sebaliknya apabila nyala lampu terang berarti
tergolong asam atau basa lemah, sebaliknya apabila nyala lampu terang berarti
larutan tersebut tergolong asam atau basa kuat.
larutan tersebut tergolong asam atau basa kuat.
Asam kuat atau asam lemah pada konsentrasi yang sama
Asam kuat atau asam lemah pada konsentrasi yang sama
menghantarkan listrik yang berbeda. Nyala lampu pada gambar a
menghantarkan listrik yang berbeda. Nyala lampu pada gambar a
tampak reup. Ini bearti larutan yang diuji berupa asam lemah atau
tampak reup. Ini bearti larutan yang diuji berupa asam lemah atau
basa lemah. Adapun pada gambar b lampu menyala terang
basa lemah. Adapun pada gambar b lampu menyala terang
menandakan larutan yang diuji berupa asam kuat atau
menandakan larutan yang diuji berupa asam kuat atau basa kuat.basa kuat.
2. Derajat Keasaman & Kebasaan
2. Derajat Keasaman & Kebasaan
Mungkin kamu pernah mendengar istilah pH suatu larutan. Apakah pH itu? Pada
Mungkin kamu pernah mendengar istilah pH suatu larutan. Apakah pH itu? Pada
dasarnya derajat/tingkat keasaman suatu larutan (pH =
dasarnya derajat/tingkat keasaman suatu larutan (pH = potenz Hydrogen potenz Hydrogen))))
bergantung pada konsentrasi ion H
bergantung pada konsentrasi ion H++ dalam larutan.Semakin besar konsentrasidalam larutan.Semakin besar konsentrasi
ion H
Materi: Asam, Basa, dan Garam
Materi: Asam, Basa, dan Garam
13
13
Umumnya konsentrasi ion H
Umumnya konsentrasi ion H++ pada larutan sangat kecil, maka untukpada larutan sangat kecil, maka untuk
menyederhanakan penulisan digunakan konsep pH untuk
menyederhanakan penulisan digunakan konsep pH untuk
menyatakan konsentrasi ion H
menyatakan konsentrasi ion H++. . Nilai Nilai pH pH sama sama dengan dengan negatif negatif logaritmalogaritma
konsentrasi ion H
konsentrasi ion H++ dan secara matematika dinyatakan dengan persamaandan secara matematika dinyatakan dengan persamaan
pH = - log (H
pH = - log (H++))
Analog dengan pH, konsentrasi ion OH
Analog dengan pH, konsentrasi ion OH–– juga juga dapat dapat dinyatakan dinyatakan dengandengan
cara yang sama, yaitu pOH (
cara yang sama, yaitu pOH (Potenz HydroxidePotenz Hydroxide) dinyatakan dengan persamaan) dinyatakan dengan persamaan
berikut.
berikut.
pOH = - log (OH-)
pOH = - log (OH-)
Derajat keasaman suatu zat (pH) ditunjukkan dengan skala0
Derajat keasaman suatu zat (pH) ditunjukkan dengan skala0——14.14.
a. Larutan dengan pH < 7 bersifat asam.
a. Larutan dengan pH < 7 bersifat asam.
b. Larutan dengan pH = 7 bersifat netral.
b. Larutan dengan pH = 7 bersifat netral.
c. Larutan dengan pH > 7 bersifat basa.
c. Larutan dengan pH > 7 bersifat basa.
Jumlah harga pH dan pOH = 14. Misalnya, suatu larutan memiliki pOH = 5,
Jumlah harga pH dan pOH = 14. Misalnya, suatu larutan memiliki pOH = 5,
maka harga pH = 14
maka harga pH = 14 –– 5 = 9. Harga pH untuk beberapa jenis zat yang dapat kita 5 = 9. Harga pH untuk beberapa jenis zat yang dapat kita
temukan di lingkungan sehari-hari dinyatakan dalam tabel berikut.
temukan di lingkungan sehari-hari dinyatakan dalam tabel berikut.
Tabel 1.7 Harga pH untuk beberapa jenis zat
Tabel 1.7 Harga pH untuk beberapa jenis zat
No.
No. Harga pH Harga pH Contoh MaterialContoh Material 1.
1. 1 1 Larutan Larutan HCHCℓ 0,1 Mℓ 0,1 M
2.
2. <5,6 <5,6 Hujan Hujan asamasam 3.
3. 6 6 SusuSusu
4.
4. 7 7 Air Air mineralmineral 5.
5. 7,2 7,2 DarahDarah 6.
6. 14 14 Larutan Larutan NaOH NaOH 1 1 MM
3. Menentukan pH Suatu Larutan
3. Menentukan pH Suatu Larutan
Derajat keasaman (pH) suatu larutan dapat ditentukan menggunakan indikator
Derajat keasaman (pH) suatu larutan dapat ditentukan menggunakan indikator
universal, indikator
universal, indikator stick , larutan indiaktor, dan pH meter.stick , larutan indiaktor, dan pH meter.
a. Indikator Universal
a. Indikator Universal
Indikator universal merupakan campuran dari bermacam-macam indikator
Indikator universal merupakan campuran dari bermacam-macam indikator
yang dapat menunjukkan pH suatu larutandari perubahan warnanya. Indikator
yang dapat menunjukkan pH suatu larutandari perubahan warnanya. Indikator
universal ada dua macamyaitu indikator yang berupa
universal ada dua macamyaitu indikator yang berupa kertas dan larutan.kertas dan larutan.
gambar 1.7 indikator universal gambar 1.7 indikator universal
Materi: Asam, Basa, dan Garam
Materi: Asam, Basa, dan Garam
14
14
b. Indikator Kertas (Indikator
b. Indikator Kertas (Indikator
Stick
Stick
)
)
Indikator kertas berupa kertas serap dan tiap kotak kemasan indikator
Indikator kertas berupa kertas serap dan tiap kotak kemasan indikator
jenis
jenis ini ini dilengkapi dilengkapi dengan dengan peta peta warna. warna. Penggunaannya Penggunaannya sangat sangat sederhana,sederhana,
sehelai indikator dicelupkan ke dalam larutan yang akan diukur pH-nya.
sehelai indikator dicelupkan ke dalam larutan yang akan diukur pH-nya.
Kemudian dibandingkan dengan peta warna yang tersedia.
Kemudian dibandingkan dengan peta warna yang tersedia.
c. Larutan Indikator
c. Larutan Indikator
Salah satu contoh indikator universal jenis larutan
Salah satu contoh indikator universal jenis larutan
adalah
adalah larutan larutan metil metil jingga jingga (Metil (Metil Orange Orange = = MO). MO). Pada Pada pHpH
kurang dari 6 larutan ini berwarna jingga, sedangkan pada pH
kurang dari 6 larutan ini berwarna jingga, sedangkan pada pH
lebih dari 7 warnanya menjadi kuning (gambar di samping
lebih dari 7 warnanya menjadi kuning (gambar di samping
berikut). Contoh indikator cair lainnya adalah indikator
berikut). Contoh indikator cair lainnya adalah indikator
fenolftalin (Phenolphtalein
fenolftalin (Phenolphtalein = pp). = pp). pH di pH di bawah 8, bawah 8, fenolftalinfenolftalin
tidak berwarna, dan akan berwarna merah anggur apabila pH
tidak berwarna, dan akan berwarna merah anggur apabila pH
larutan di atas 10.
larutan di atas 10.
d. pH Meter
d. pH Meter
Pengujian sifat larutan asam basa dapat juga
Pengujian sifat larutan asam basa dapat juga
menggunakan pH meter. Penggunaan alat ini
menggunakan pH meter. Penggunaan alat ini
dengan cara dicelupkan pada larutan yang
dengan cara dicelupkan pada larutan yang
akan diuji, pada pH meter akan muncul angka
akan diuji, pada pH meter akan muncul angka
skala yang menunjukkan pH larutan.
skala yang menunjukkan pH larutan.
Rangkuman
Rangkuman
Larutan dapat
Larutan dapat bersifat bersifat asam, asam, basa, atau basa, atau garam. Larutan garam. Larutan asam rasanyaasam rasanya
masam, memiliki pH <7, serta bereaksi dengan logam dan bahan lainnya. Reaksi
masam, memiliki pH <7, serta bereaksi dengan logam dan bahan lainnya. Reaksi
asam dengan logam bersifat korosif. Adapun larutan basa rasanya pahit, terasa licin,
asam dengan logam bersifat korosif. Adapun larutan basa rasanya pahit, terasa licin,
dan harga pH lebih > 7. Garam merupakan hasil reaksi dari asam dan basa. Ada tiga
dan harga pH lebih > 7. Garam merupakan hasil reaksi dari asam dan basa. Ada tiga
jenis garam,
jenis garam, yaitu yaitu garam garam normal normal (pH (pH = = 7), 7), garam garam asam asam (pH (pH < < 7), 7), dan dan garam garam basabasa
(pH > 7).
(pH > 7).
Harga
Harga pH pH atau atau derajat derajat keasaman dapat keasaman dapat diukur diukur dengan menggunakandengan menggunakan
indikator, misalnya kertas lakmus, indikator fenolftalin, indikator universal, dan
indikator, misalnya kertas lakmus, indikator fenolftalin, indikator universal, dan
indikator alami, seperti warna bunga sepatu dan
indikator alami, seperti warna bunga sepatu dan kunyit.kunyit.
Sifat daya hantar listrik suatu larutan dapat diuji dengan menggunakan alat uji
Sifat daya hantar listrik suatu larutan dapat diuji dengan menggunakan alat uji
elektrolit. elektrolit. gambar 1.8 contoh gambar 1.8 contoh larutan indikator larutan indikator gambar 1.9 pH Mete gambar 1.9 pH Meterr