Pemicu 1 : Kinetika
Pertumbuhan Sel
Kelompok 4 Angelina (1406533522) Mauhibah Yumna (1406577650) M Galih Utomo (1406533554) Wawan Irawan (1406544636) Woro Bismo (1406533472)1. Bagaimana mekanisme biokimia secara
umum dalam pertumbuhan sel? Bagaimana
pula fase-fase yang dialami oleh sel dalam
masa pertumbuhannya?
Apa itu Biokimia?
Biokimia
adalah
ilmu
yang
mempelajari reaksi yang terjadi di dalam
atau berhubungan dengan makhluk hidup.
Reaksi
biokimia
umumnya
mempelajari
tentang reaksi makromolekul kehidupan
(karbohidrat, lemak, protein, asam nukleat),
dan molekul atau ion lain yang berhubungan
dengan
kehidupan
makhluk
hidup
(contohnya air).
Bagaimana
peranan
biokimia
dalam pertumbuhan sel?
Reaksi-reaksi biokimia sangat berperan dalam
siklus hidup sel,
karena tanpa reaksi-reaksi
tersebut sebuah sel tidak dapat bertahan
hidup.
Mempelajari reaksi-reaksi biokimia
dapat membuat kita mengerti lebih jauh
tentang siklus hidup dan pertumbuhan sel,
serta memanfaatkan pengetahuan itu untuk
diaplikasikan di bidang-bidang lain, seperti
medis dan pertanian.
Sasaran Biokimia
Mempelajari pertumbuhan sel baik kecepatan/produk dan waktu yang dapat direkayasa
Mempelajari jalur-jalur metabolisme dalam pertumbuhan sel & mekanisme pengendaliannya
Struktur kimia dari komponen makhluk hidup dan hubungan antara struktur kimia dengan fungsi biologis
Mempelajari metabolisme, yaitu keseluruhan reaksi kimia dalam makhluk hidup
Proses kimia dan substansi yang menyimpan dan mengirimkan informasi biologis
Kurva Pertumbuhan Sel
Fase Lag
• Terlihat mendatar pada kurva karena tingkat pertumbuhan sel sangat sedikit.
• Sel mulai beradaptasi dan mengumpulkan energi dengan memulai reaksi enzimatis untuk menguraikan substrat dan nutrien.
• Lamanya bergantung pada medium tumbuh dan jumlah awal sel yang mempengaruhi waktu adaptasi.
Fase Akselerasi
Fase dimana sel sudah selesai
melakukan masa adaptasi namun
Fase Eksponensial
• Tingkat aktivitas sel
mencapai kecepatan
maksimum yang dapat terlihat dari bentuk kurva yang eksponensial.
• Dipengaruhi oleh
beragam faktor biologis dan nonbiologis, seperti
sifat sel, asosiasi
organisme di medium
tumbuh, kandungan
Fase Pengurangan (
reduction
)
Tingkat pertumbuhan sel
mengalami penurunan,
karena nutrien yang
dibutuhkan sudah
hampir habis atau sel-sel
yang terdapat pada
medium mati karena
terpapar hasil
metabolisme yang
bersifat racun atau
persaingan dengan
Fase Stasioner
• Kurva mendatar menunjukan tingkat pertumbuhan sel sama dengan tingkat kematian sel. Pada fase ini sel mengalami resistensi yang lebih tinggi terhadap faktor eksternal seperti suhu dan zat kimia.
• Nutrisi di medium sangat berkurang • Terbentuk senyawa penghambat
Fase Kematian
• Tingkat kematian sel
sudah lebih banyak
dibandingkan tingkat pertumbuhan sel.
• Nutrien sudah habis sehingga sel tidak lagi
dapat melakukan
pertumbuhan, namun
hasil metabolisme yang bersifat toksik semakin banyak dan persaingan
antar organisme
semakin ketat sehingga sel yang mati lebih banyak dari sel yang hidup.
2. Bagaimana Anda mengukur dan
menganalisis pertumbuhan sel?
Jumlah Total Sel
Pertambahan atau pengurangan
banyaknya sel N dari sampel yang diambil
berbanding lurus dengan jumlah total
sebenarnya
di mana
• µ = laju pertumbuhan spesifik per
waktu
• X(t) = jumlah total sel per waktu
Aktivitas Populasi Mikrobial
dalam
Biakan Sistem Tertutup
di mana
• Xo: jumlah sel pada waktu nol,
• X: jumlah sel pada waktu t,
• t: waktu pertumbuhan diamati.
Doubling Time
Untuk memperkirakan kerapatan populasi
pada waktu yang akan datang dengan μ
sebagai konstanta pertumbuhan yang
berlaku. Parameter penting untuk konstanta
pertumbuhan populasi secara eksponensial
adalah waktu generasi (waktu
penggandaan). Penggandaan populasi terjadi
saat X / Xo =2, sehingga:
Laju Pertumbahan Sel
Untuk mengukur pertumbuhan sel, kita
dapat menentukannya dengan
menggunakan persamaan laju pertumbahan
sel (r
x)
dimana :
• μ = konstanta kecepatan pertumbuhan
• C
X= konsentrasi sel kering per unit volum
Cara Mengukur dan Menganalisis
Pertumbuhan Sel
Aktivitas dari pertumbuhan sel dapat diukur
secara kuantitatif, baik jumlah maupun
perubahan laju dari massa sel. Terdapat dua
kategori metode yang dapat digunakan:
Pengukuran Banyaknya
Sel
Pengukuran Mikroskopis
Langsung
Secara umum, metode yang
dilakukan adalah menghitung
sel pada slide kaca. Dengan
slide Petroff-Hauser, dapat
digunakan untuk menghitung
banyaknya sel pada setiap
kamar/kotak hemocytometer.
Massa Jenis Sel = Rata − rata sel per kotak Volume kotak
Diperlukan staining karena
jumlah sel mati dan hidup
tidak terlihat.
Plat Penghitung Sel Hidup
• Teknik yang dilakukan pada metode ini adalah dengan membuat
mikroba bertumbuh pada medium (kloning). Kemudian mikroba yang ada dihitung pada plat penghitung sel hidup dengan teknik
pengukuran koloni yang terbentuk (CFU).
• Dapat juga diaplikasikan pada mikroba pada lingkungan bebas. Namun, perlu diketahui bahwa mikroba yang terkandung pasti banyak sehingga pertumbuhan pada medium tertentu akan berbeda.
Plating and CFU Counting (Sumber: upload.wikimedia.org)
Penghitung Coulter
Penghitung yang ditemukan oleh Coulter ini menggunakan arus listrik melaui sebuah lubang. Setiap mikroba yang melewati lubang, tahanan akan bertambah dan arus menurun. Jumlah arus ini dapat terekam pada suatu alat dan dapat menunjukkan pengurangan arus sebandung dengan volume sel. Instrumen ini dapat memberikan banyaknya sel dan distribusi ukuran sel tetapi tidak memberikan info tentang bentuk sel. Partikel yang dapat dihitung adalah partikel yang berukuran 0,5-200 µm.
Aliran Cytometer (Flow
Cytometri)
Metode ini dilakukan dengan memanfaatkan sifat optis dari sel. Sampel yang telah dikultur di encerkan di aliran yang akan memisahkan sel secara membujur dari sel lain. Aliran melaui laser beam, absorption, flouresence, atau
light diffusion untuk menyampaikan perhitungan sel. Selektifitas juga dapat ditingkatkan dengan melabel
dengan flouresencent dye.
Pengurutan sel selesai dengan memasukkan muatan pada tetes
yang mengandung sel yang
diinginkan. Muatan membuat tetes tersebut terbelokkan ke detektor.
Flow Cytometer
Dry Cell Weight (Berat Sel
Kering)
Teknik ini dilakukan dengan mengeringkan sampel dengan proses sentrifugasi atau filtrasi, dicuci dengan air atau buffer, dan dikeringkan pada 80 derajat celcius. DCW sering digunakan pada fermentor. Sampel broth diambil dari fermentor kemudian ukur volumenya. Sel dipisahkan dengan sentrifugasi atau filtrasi, namum biasanya masih terdapat pengotor lain yang bukan merupakan sel sehingga perlu diperlakukan beberapa metode seperti penambahan buffer untuk menhilangkan asam. Kemudian sel dikeringkan dan ditimbang.
Packed Cell Volume
(PCV)
PCV sering digunakan pada industry plant untuk mengikuti kinerik fermentasi. PCV tergantung tidak hanya pada massa sel, tetapi juga pada kecepatan sentrifugal dan waktu, banyaknya padatan non-selular, mofologi kultur, dan
osmolaritas dari medium. Kondisi sentrifugasi biasanya di set untuk mengurangi efek dari
variabel lain. Banyaknya padatan nonselular akan berkurang seiring dengan pertambahan waktu. Padatan akan mengendap lebih dulu daripada sel sehingga dapat menghitung berat padatan yang ada.
Turbiditas (kekeruhan)
Turbiditas adalah teknik yang paling sering
digunakan pada pengukuran pertumbuhan mikroba.
Spektrofotometer
Visual method
Nephelometric method
Image Analysis
• Khusus
untuk
kasus
pertumbuhan
filamentous dan pembentukan pellet, sulit
untuk mengukur pertumbuhan dari sel
atau massa total sel.
• Analisis ini dapat menjadi alat berguna
untuk mengklasifikasi biomassa.
• Diambil gambar dari broth fermentasi dan
diproses dengan software komputer.
3. Bagaimana substrat dan pembentukan
produk dalam sel dapat menginhibisi
pertumbuhan sel? Dapatkah anda
menjelaskan faktor-faktor lainnya yang
dapat menginhibisi laju pertumbuhan sel?
Faktor-faktor yang Menginhibisi
Reaksi Pertumbuhan Sel
• Senyawa Kimia
• Pembentukan
Produk
• pH
• Suhu
• Cahaya
• Air
• Kelembaban
• Potensial Oksidasi
– Reduksi
• Keberadaan Gas
• Keberadaan
Antibiotik
• Salinitas
• Kondisi osmotik
• Logam Berat
• Inhibisi oleh substrat ini sering dianggap sebagai sifat biokimia dari substrat yang aneh dan menganggu
proses berjalannya reaksi kimia.
• Mekanisme inhibisi oleh substrat ditunjukkan pada Gambar 2. Terlihat substrat menyerang kompleks
enzim substrat sehingga membentuk kompleks enzim-substrat-substrat.
Grafik pengaruh kadar substrat terhadap kecepatan pertumbuhan spesifik Sumber: Julianti, Elisa. 2013)
• Tahap Reaksi: 𝐸 + 𝑆 𝑘1 𝐸 ∙ 𝑆 𝐸 ∙ 𝑆𝑘−1 𝐸 + 𝑆 𝐸 ∙ 𝑆 𝑘2 𝐸 + 𝑃 𝑆 + 𝐸 ∙ 𝑆 𝑘3 𝑆 ∙ 𝐸 ∙ 𝑆 (𝑖𝑛𝑎𝑘𝑡𝑖𝑓) 𝑆 ∙ 𝐸 ∙ 𝑆𝑘−3 𝑆 + 𝐸 ∙ 𝑆
Mekanisme inhibisi oleh substrat (Sumber:http://www1.lsbu.ac.uk/)
• Inhibisi oleh produk kadang disebut sebagai negative feedback
atau inhibition feedback.
• Inhibisi oleh produk adalah suatu tipe inhibisi enzim dimana produk dari suatu reaksi enzimatis menempel pada enzim dan menghambat aktivitasnya.
• Hal ini penting pada regulasi metabolisme sebagai suatu bentuk negative feedback yang mengontrol siklus metabolisme.
Gambar x.Mekanisme inhibisi oleh produk (Sumber:
http://www.csun.edu/)
Inhibisi oleh Pembentukan
Produk
• Pada dasarnya, inhibisi oleh produk adalah suatu hal yang merugikan dan dalam bioteknologi selalu berusaha dihilangkan karena dapat meningkatkan yield produksi, contohnya dalam produksi antibiotik. • Pada inhibisi ini, produk secara struktur mirip dengan
substrat sehingga akan berkompetisi dengan substrat untuk menempel pada sisi aktif enzim.
Contoh inhibisi oleh produk (Sumber: http://www.citruscollege.edu/)
Inhibisi oleh Pembentukan
Produk (2)
• Faktor-faktor lainnya yang dapat menginhibisi reaksi enzimatis adalah inhibitor kompetitif, non-kompetitif, dan inkompetitif, serta isomerisasi kompleks EI menjadi EI* yang inaktif.
• Inhibitor kompetitif mempunyai struktur yang mirip dengan substrat sehingga akan berkompetisi dengan substrat untuk menempel pada sisi yang sama pada enzim yaitu sisi aktifnya. • Inhibitor non-kompetitif tidak mirip secara struktural dengan
substrat sehingga akan menempel pada sisi yang berbeda dengan sisi aktif enzim, namun mengubah bentuk enzim sehingga substrat tak dapat menempel dengan enzim.
• Pada inhibisi inkompetitif, inhibitor dapat hanya dapat menempel pada enzim apabila enzim telah berikatan dengan suatu substrat atau lebih.
Inhibisi oleh
Faktor
Lainnya
Mekanisme inhibisi kompetitif (Sumber: http://www.csun.edu/)
Mekanisme inhibisi Inkompetitif (Sumber: http://www.csun.edu/)
4. Dengan adanya pertumbuhan sel ini, dapatkah anda menjelaskan mekanisme-mekanisme reaksi
yang mungkin dijalani oleh sel dalam masa pertumbuhannya? Bagaimana menentukan laju
reaksinya dari masing-masing mekanisme tersebut?
• Pertumbuhan pada sel melibatkan metabolisme energi, di mana Metabolisme adalah suatu proses komplek yang terjadi didalam sel dimana terjadi perubahan makanan menjadi energi dan panas melalui suatu proses kimia, berupa proses pembentukan dan penguraian zat.
• Metabolisme bertujuan untuk menghasilkan energi yang berguna bagi kelangsungan hidup, baik untuk pembelahan sel maupun transpor molekul ke luar dan ke dalam sel.
• Metabolisme sering disebut dengan reaksi enzimatis, karena metabolisme terjadi selalu menggunakan katalisator enzim.
Mekanisme Reaksi
Pertumbuhan Sel
• Anabolisme merupakan rangkaian reaksi kimia yang substrat awalnya adalah molekul kecil dan produk akhirnya adalah molekul besar, bertujuan untuk penyusunan atau sintesis molekul.
• Contoh : Pada reaksi fotosintesis berikut.
Fotosintesis
Gelap Terang
Proses Penyerapan Energi Cahaya
Beratus- ratus pigmen fotosintesis (fotosistem) meyerap foton
Energi eksitasi dibawa oleh pigmen ke pigmen lainnya hingga ke klorofil a
Klorofil a teraktivasi memberikan elektron ke molekul penerima elektron dalam sistem transpor elektron
Proses Penyerapan Energi Cahaya
Fotosintesis Gelap
(Calvin-Benson)
• Berlangsung dalam gelap, dan hanya dapat berlangsung jika ada ATP dan NADPH (yang dihasilkan proses terang) • Memerlukan ATP, hidrogen, dan elekton dari NADPH, karbon dan oksigen dari karbon dioksida, enzim yang
mengkatalisis setiap reaksi, dan RuBP.
Karbon dioksida diikat oleh RuBP menjadi senyawa 6 karbon, yang lalu memecah menjadi 2 fosfogliserat (PGA)
Masing masing PGA menerima gugus fosfat dari ATP dan menerima hidrogen serta
elektron dari NADPH, menghasilkan PGAL
Untuk setiap 6 molekul CO2 yang diikat menghasilkan 12 PGAL
Dari 12 PGAL, 10 molekul kembali ke tahap awal menjadi RuBP, dan seterusnya RuBP akan mengikat CO2 yang baru
2 PGAL lainnya akan berkondensasi menjadi glukosa 6 fosfat
𝐶
6𝐻
12𝑂
6+ 6𝑂
26𝐶𝑂
2+ 6𝐻
2𝑂
Merupakan rangkaian reaksi yang bertujuan
untuk pembongkaran atau penguraian suatu
molekul.
Bersifat eksergonik.
Berfungsi menyediakan bahan baku untuk
sintesis molekul lain .
Menyediakan energi kimia yang dibutuhkan
untuk melakukan aktivitas kehidupan.
Pati Glukosa Maltosa dan polimer glukosa Glukosa dan galaktosa Glukosa dan fruktosa Sukrosa Laktosa Ptialin Amilase Sukrase Laktase Maltase dan 𝛼 − 𝑑𝑒𝑘𝑠𝑡𝑟𝑖𝑛𝑎𝑠𝑒
Pemecahan polisakarida dan
disakarida menjadi monosakarida
• Pertumbuhan sel merupakan salah satu dari rangkaian aktivitas sel yang fungsinya untuk mempertahankan kehidupannya. Setiap pertumbuhan sel mengikuti aturan-aturan berikut,
𝐶𝑠𝑜𝑢𝑟𝑐𝑒 + 𝑁𝑠𝑜𝑢𝑟𝑐𝑒 + 𝑝ℎ𝑜𝑠𝑝ℎ𝑎𝑡𝑒 + 𝑂2 𝐶𝑒𝑙𝑙 𝑚𝑎𝑠𝑠 +
𝐶𝑂2 + 𝐻2𝑂 + 𝑝𝑟𝑜𝑑𝑢𝑐𝑡 + ℎ𝑒𝑎𝑡
• Bila pertumbuhan sel terjadi saat kondisi aerob, maka
𝑐𝑒𝑙𝑙𝑠 + 𝑐𝑎𝑟𝑏𝑜𝑛 𝑠𝑜𝑢𝑟𝑐𝑒 + 𝑛𝑖𝑡𝑟𝑜𝑔𝑒𝑛 𝑠𝑜𝑢𝑟𝑐𝑒 + 𝑜𝑥𝑦𝑔𝑒𝑛 𝑠𝑜𝑢𝑟𝑐𝑒 + 𝑝ℎ𝑜𝑠𝑝ℎ𝑎𝑡𝑒 𝑠𝑜𝑢𝑟𝑐𝑒 + ⋯ 𝑐𝑢𝑙𝑡𝑢𝑟𝑒 𝑚𝑒𝑑𝑖𝑎 𝑐𝑜𝑛𝑑𝑖𝑡𝑖𝑜𝑛 (𝑝𝐻,𝑇,𝑒𝑡𝑐.) 𝐶𝑂2 + 𝐻2𝑂 + 𝑝𝑟𝑜𝑑𝑢𝑐𝑡 + 𝑚𝑜𝑟𝑒𝑐𝑒𝑙𝑙𝑠
Persamaan Monod
• Persamaan laju pertumbuhan sel mengikuti
alur mekanisme sel sebagai berikut:
𝑐𝑒𝑙𝑙𝑠 + 𝑠𝑢𝑏𝑠𝑡𝑟𝑎𝑡𝑒 𝑚𝑜𝑟𝑒 𝑐𝑒𝑙𝑙𝑠 + 𝑝𝑟𝑜𝑑𝑢𝑐𝑡
• Persamaan Monod
untuk pertumbuhan
eksponensial (log phase) adalah sebagai
berikut
𝑟
𝑔= 𝜇 𝐶
𝑐dimana
𝑟
𝑔adalah
cell growth rate
(g/dm
3.s)
𝐶
𝑐adalah
cell concentration
(g/dm
3)
Laju Pertumbuhan Spesifik
• Laju
pertumbuhan
spesifik
𝜇
dapat
ditunjukkan dengan persamaan
𝜇 = 𝜇
𝑚𝑎𝑥𝐶
𝑠𝑘
𝑠+ 𝐶
𝑠• 𝜇
𝑚𝑎𝑥adalah laju reaksi pertumbuhan
spesifik maksimum (s
-1)
• 𝑘
𝑠adalah konstanta Monod (g/dm
3)
• 𝐶
𝑠adalah konsentrasi substrat (g/dm
3)
• Nilai
𝜇
𝑚𝑎𝑥dan
𝑘
𝑠yang biasa digunakan,
masing-masing, adalah 1,3 h
-1dan 2,2 x 10-5
mol/dm
3.
• Apabila persamaan Monod dan laju pertumbuhan spesifik digabungkan maka didapatkan persamaan
𝑟𝑔 = 𝜇𝑚𝑎𝑥 𝐶𝑠 𝐶𝑐 𝑘𝑠 + 𝐶𝑠
• Apabila konstanta 𝑘𝑠 kecil maka 𝑟𝑔= 𝜇𝑚𝑎𝑥 𝐶𝑐.
• Inhibitor produk dapat mempengaruhi
pertumbuhan sel sebagai contoh fermentasi
glukosa yang memproduksi etanol dan diinhibisi oleh etanol itu sendiri.
• Maka persamaan empirisnya adalah
𝑟𝑔 = 𝑘𝑜𝑏𝑠 𝜇𝑚𝑎𝑥𝐶𝑠 𝐶𝑐 𝑘𝑠 + 𝐶𝑠
Monod + Laju Pertumbuhan
Spesifik
Persamaan-Persamaan Laju
Pertumbuhan Sel
• Persamaan lain untuk menentukan laju
pertumbuhan sel adalah persamaan Tessier, yakni
𝑟𝑔 = 𝜇𝑚𝑎𝑥 1 − exp − 𝐶𝑠
𝑘 𝐶𝑐
• dan Persamaan Moser
𝑟𝑔 = 𝜇𝑚𝑎𝑥 𝐶𝑐
1 + 𝑘𝐶𝑠−𝜆
• dimana λ dan k adalah konstanta empiris.
• Persamaan Moser dan Tessier sering digunakan karena keduanya menemukan data eksperimen yang tepat dan lebih baik pada awal atau akhir fermentasi.
Fase Kematian Sel
• Pada fase kematian sel persamaan lajunya menjadi
𝑟𝑑 = 𝑘𝑑 + 𝑘𝑡𝐶𝑡 𝐶𝑐
• dimana 𝐶𝑡 adalah konsentrasi racun yang
mengenai sel
• 𝑘𝑑 adalah kematian alami
• 𝑘𝑡 adalah kematian yang disebabkan oleh racun • Nilai representatif 𝑘𝑑 berada di antara 0,1 h-1
hingga di bawah dari 0,0005 h-1, sedangkan 𝑘
𝑡
5. Bagaimana Anda menghitung laju
reaksi dari suatu data konsentrasi
menggunakan diferensiasi grafis?
Hukum Laju dari Grafik
Konsentrasi Terhadap Waktu
• Reaksi pada orde 0
• Terbentuk garis yang linier • Laju reaki (r) = d[A]/dt = k
[A] versus t
• Reaksi pada orde 1
• Terbentuk garis yang linier
• Laju reaki (r) = d[A]/dt = k [A]
• Reaksi pada orde 2
• Laju reaki (r) = d[A]/dt = k[A]2
1 / [A] versus t
(sumber: http://www.chem.purdue.edu/gchelp/howt osolveit/Kinetics/CalculatingRates.html#Top)
Metode untuk menentukan tingkat reaksi.
Perubahan konsentrasi pereaksi dalam selang waktu tertentu
Penggunaan persamaan laju secara langsung.
Menentukan Laju Reaksi dengan
Metode Diferensiasi Grafis
dengan mengukur laju perubahan konsentrasi reaktan terhadap waktu
a A + b B → c C + dD
perubahan konsentrasi reaktan terhadap waktu selama reaksi berlangsung
Diferensiasi grafis dari data konsentrasi dengan menggambar tangent
Menentukan Laju Reaksi dengan
Metode Diferensiasi Grafis
Langkah - Langkah
Menebak bentuk persamaan reaksi serta orde reaksinya
Menyusun neraca
massa Membuat grafik
Garis Tidak Lurus
Garis Lurus
Metode Least Square
Pada metoda diferensial, variable
dalam bentuk derivatif yang besarnya
dapat dicari dengan metoda numeris :
t C C t C C t Limit dt dC A
t
t
At
Ai
Ai
A
1
0100 ml larutan A dengan konsentrasi A 10 gmol/L dalam reaktor bereaksi membentuk B, selama terjadi reaksi diamati konsentrasi A, diperoleh data sebagai berikut :
Contoh Soal
Waktu (menit) CA(gmol/L)
5 6,8 10 4,9 15 4,0 20 3,2 25 2,9 30 2,5
Bagaimana bentuk persamaan kecepatan reaksinya, tentukan laju reaksi dan konstanta kecepatan reaksinya!
1. Menentukan orde reaksi
Untuk menentukan, dilakukan percobaan
terhadap orde reaksi, percobaan pertama
terhadap reaksi orde 1 dengan persamaan kecepatan reaksi :
2. Menyusun neraca massa
Kecepatan bahan masuk − Kecepatan bahan Keluar − Kecepatan bahan bereaksi = Kecepatan akumulasidt
V
dC
V
kC
A
A
0
0
Volume dianggap konstan, maka :
dt dC kCA A 0 0 Persamaan Derivatif linier
Untuk membuat grafik tersebut diperlukan
pengolahan data konsentrasi A dan waktu menjadi sehingga dihasilkan data sebagai berikut :
3. Membuat grafik
Waktu
(menit) CA (gmol/L) ĉA(gmol/L)
-5 6,8 5,85 0,38 10 4,9 4,45 0,18 15 4,0 3,60 0,16 20 3,2 3,05 0,06 25 2,9 2,70 0,008 30 2,5 dt dCA
3. Membuat grafik
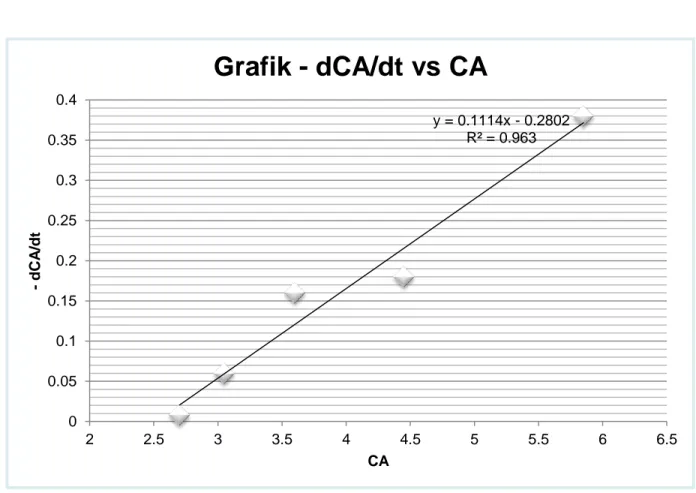
y = 0.1114x - 0.2802 R² = 0.963 0 0.05 0.1 0.15 0.2 0.25 0.3 0.35 0.4 2 2.5 3 3.5 4 4.5 5 5.5 6 6.5 -d CA /dt CA Grafik - dCA/dt vs CAKesimpulan
• Dari grafik tersebut , hubungan
mendekati garis lurus maka bisa
disimpulkan bahwa reaksi tersebut
merupakan reaksi orde satu dengan
persaman kecepatan reaksi r
A=kC
A.Nilai konstanta kecepatan reaksi (k)
adalah slope dari garis tersebut
k =
0,118 (
1/menit).
6. Bagaimana anda menjelaskan
hubungan kinetik untuk reaksi-reaksi
berorde nol, satu, dan
Kinetika Orde Nol
• Reaksi dalam kinetika orde nol,
mempunyai laju reaksi yang tidak
dipengaruhi oleh konsentrasi
reaktan. Berikut adalah
persamaannya.
r
A= k
0• Kita dapat menuliskan :
Kinetika Orde Satu
• Laju reaksi dalam reaksi kinetika
orde satu dipengaruhi oleh
konsentrasi reaktan, berikut adalah
hubungan antara laju reaksi dan
konsentrasi reaktan :
Kita asumsikan suatu reaksi dalam
suatu sistem tertutup, dan berada
dalam volume konstan, dan kita akan
mengukur
konsentrasi
reaktan
A
sebagai fungsi waktu. Dibawah kondisi
tersebut,
𝑟
A
=
−d
𝐶A
d
𝑡• Untuk menentukan apakah reaksi
tersebut merupakan kinetika orde
satu,
pertama-tama
kita
mengintegrasi persamaan diatas dan
𝑟
A
=
−d
𝐶A
d
𝑡lalu
melakukan
pengecekan
terhadap
data
konsentrasi
terhadap
persamaan
yang dihasilkan.
Memisahkan variabel dan mengintegrasi
persamaan diatas dengan kondisi awal
𝐶
A
=
𝐶
A
0dengan t = 0 :
𝐶
A
= 𝐶
A
0𝑒
−𝑘1 𝑡ln 𝐶
A
= ln 𝐶
𝐴0− 𝑘
1𝑡
Jadi, untuk reaksi orde satu, plot grafik dari
ln 𝐶
A terhadap waktu memberikan garis
lurus dengan gradien
−𝑘
1.
• Kinetika Michaelis-Menten
Kinetika dari sebagian besar reaksi enzimatik
menggunakan persamaan Michaelis Menten:
𝑟
A
=
𝑣max
𝐶A
𝐾
m
+ 𝐶A
• Mekanisme
Michaelis
Menten
biasanya
digunakan untuk reaksi katalis enzim dengan
persamaan sebagai berikut :
Pada saat
kecepatannya
menjadi
maksimum sehingga:
Enzyme Source Substrate Km (mM) Alcohol dehydrogenase Saccharomyces cerevisiae Ethanol 13,0 α-Amylase Bacillus stearothermophilus Starch 1,0
Porcine pancreas Starch 0,4
β-Amylase Sweet potato Amylose 0,07
Aspartase Bacillus cadaveris L-Aspartate 30,0
β-Galactosidase Escherichia coli Lactose 3,85
Glucose oxidase Aspergillus niger D-Glucose 33,0
Penicillium notatum D-Glucose 9,6
Histidase Pseudomonas fluorescens L-Histidine 8,9
Invertase Saccharomyces
cerevisiae
Sucrose 9,1
Neurospora crassa Sucrose 6,1
Lactate
dehydrogenase
Bacillus subtilis Lactate 30,0
Penicillinase Bacillus licheniformis Benzylpenicillin 0,049
Urease Jack bean Urea 10,5
Konstanta Michaelis untuk enzim tertentu. Sumber : B. Atkinson andF.
Mavituna, 1991, Biochemical Engineering and Biotechnology Handbook, 2nd edn, Macmillan, Basingstoke
• Michaelis-Menten,
yang
akan
dibahasi
disini
adalah
reaksi
sederhana yang dari sifat kinetik dari
banyak enzim adalah :
Michaelis-Menten (laju reaksi kimia
penguraian substrat saat dipengaruhi
oleh katalis enzim)
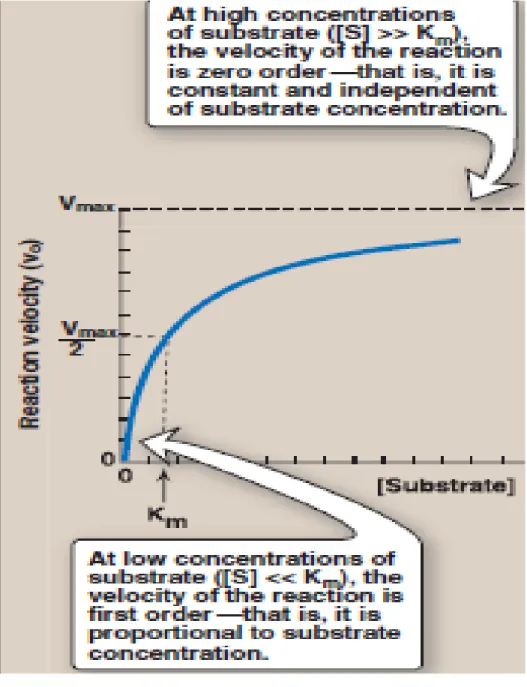
• Persamaan Michaelis-Menten adalah persamaan paling baik yang dapat mendeskripsikan kinetika dari berbagai enzim yang dipakai di industri, walaupun ada pengecualian terhadap enzim seperti glucose isomerase dan amyloglucosidase. • Saat konsentrasi substrat [S] jauh lebih kecil
daripada konstanta Michaelis-Menten Km, laju
reaksi berbanding lurus dengan konsentrasi
substrat. Ini merupakan laju reaksi orde satu
sehubungan dengan substrat.
• Saat konsentrasi substrat [S] jauh lebih besar daripada konstanta Michaelis-Menten Km, laju
reaksinya konstan dan sama dengan laju
maksimum (Vmax). Laju reaksi tidak bergantung pada konsentrasi substrat. Ini merupakan laju reaksi orde nol terhadap substrat.
Grafik laju reaksi orde 0 dan 1 (Richard A. Harvey : Biochemistry)
7. Bagaimana anda menentukan
parameter kinetika enzimatik,
V
maxdan Km dari suatu data
konsentrasi? Berikan contoh!
Reaksi Enzimatik
• Reaksi enzimatik merupakan suatu reaksi
yang melibatkan enzim sebagai katalis.
• Enzim berfungsi sebagai katalis yang akan
membuat reaksi berlangsung lebih cepat
untuk menghasilkan produk.
• Peneliti yang bernama Leoner Michaelis
dan Maud Menten mengajukan suatu
model untuk suatu reaksi enzimatik.
Berikut ini adalah reaksi yang
digambarkan oleh Michaelis-Menten:
P
E
ES
S
E
k 1 k2 k1'Peneliti yang bernama Leoner Michaelis dan Maud Menten mengajukan suatu model untuk suatu raksi
enzimatik. Berikut ini adalah reaksi yang
digambarkan oleh Michaelis-Menten:
P
E
ES
S
E
k1
k2
k1'] [ ] [ 2 ES k v dt P d ] [ ] ][ [ ] ][ [ ] [ 2 ' 1 1 E S k E S k ES k dt ES d
Laju Pembentukan Produk
]
[
]
[
]
[
]
[
]
[
]
[
E
tot
E
ES
E
E
tot
ES
Enzim berperan sebagai katalis, sehingga konsentrasi enzim itu tetap atau dapat dikatakan tidak terkonsumsi maka persamaan konsentrasi enzim dapat dituliskan menjadi sebagai
berikut:
Dari reaksi diatas, kita dapat mendapatkan persamaan laju pembentukan produk dan kompleks substrat-enzim sebagai berikut:
Laju Pembentukan Kompleks Substrat-Enzim
P
E
ES
S
E
k1
k2
k1'Reaksi yang menggunakan enzim sebagai katalis, akan menghasilkan grafik seperti berikut ini jika kita lakukan plot antara laju pembentukan produk terhadap konsentrasi substrat:
Keterangan : Km adalah konstanta Michaelis Menten (Konsentrasi substrat dimana kecepatan sudah mencapai ½ kecepatan maksimal.
Plot Michaelis - Menten
• V
maxdan K
mdapat ditentukan dari grafik, V
maxadalah sebagai laju s
~ dan K
mnilai dari s saat
V=V
max/2. Pengakurasian metode ini memiliki
kelemahan karena sulit untuk menentukan t
mx.
Plot Lineweaver - Burk
• Metode ini digunakan untuk langkah linearisasi untuk menghasilkan plot garis lurus yang bisa menentukan Vmax dan Km dengan persamaan:
1 𝑉 = 𝐾𝑚 𝑉𝑚𝑎𝑥𝑆 + 1 𝑉𝑚𝑎𝑥
• Sehingga plot dari 1/v vs 1/s harus menghasilkan garis lurus dengan slop Km/Vmax dan intercept 1/Vmax. Plot ini dikenal sebagai Lineweaver-Burk plot. Bagaimanapun juga, proses linearisasi yang
digunakan pada data eksperimen error pada v,
sehingga kesalahan ini diperkuat pada
Plot Eadie - Hofstee
• Jika persamaan 1 𝑉 = 𝐾𝑚 𝑉𝑚𝑎𝑥𝑆 + 1 𝑉𝑚𝑎𝑥 dikalikan dengan 𝑉(𝑉𝑚𝑎𝑥𝐾𝑚 ), dan kemudian disusun, bentuk linearisasi
lainnya dari persamaan Michaelis-Menten adalah
𝑉 𝑆 = 𝑉𝑚𝑎𝑥 𝐾𝑚 − 𝑉 𝐾𝑚
• Pada persamaan di atas, plot v/s versus Vmax/Km akan menghasilkan garis lurus dengan slop -1/Km dan intercept Vmax/Km yang dikenal dengan Hofstee plot. Seperti plot Lineweaver-burk, Eadie-Hofstee linearisasi mendistorsi kesalahan dalam data, sehingga metode ini telah mengurangi akurasi.
Plot Langmuir
• Dengan mengalikan persamaan 1
𝑉 =
𝐾𝑚
𝑉𝑚𝑎𝑥𝑆 + 1
𝑉𝑚𝑎𝑥 dengan S, maka bentuk linearisasi
persamaan Michaelis-Menten menjadi Langmuir adalah: 𝑆 𝑉 = 𝐾𝑚 𝑉𝑚𝑎𝑥 + 𝑆 𝑉𝑚𝑎𝑥
• Sehingga sebuah plot Langmuir pada S/V versus S harus menghasilkan garis lurus dengan slop 1/Vmax dan intercept Km/Vmax. Linearisasi dari metode ini menghasilkan kesalahan yang kecil, sehingga metode Langmuir direkomendasikan metode untuk menentukan Km dan Vmax.
Direct Linear Plot
Garis lurus dihasilkan pada (-s,v) akan mendapatkan titik yang unik (Km dan Vmax), yaitu dimana semua hasil garis lurus dari –S dan V akan menghasilkan titik potong yang banyak di suatu titik. Ketika data yang diplot mengandung kesalahan, maka akan diperoleh titik persimpangan. Setiap persimpangan akan memberikan suatu nilai perkiraan Vmax dan Km, kemudian median Vmax dan Km yang dijadikan sebagai parameter kinetik reaksi.
Contoh soal
Laktosa yang juga dikenal sebagai β-galactosidase, yang mengkatalis hidrolisis laktosa untuk memproduksi glukosa dan galaktosa dari susu. Eksperimen dilakukan
untuk menentukan parameter kinetik untuk enzim.
Konsentrasi Laktosa (mol/L)
Initial reaction velocity (mol-1 min-1 x 103) 0,0250 1,94 0,0227 1,91 0,0184 1,85 0,0135 1,80 0,0125 1,78 0,00730 1,46 0,00460 1,17 0,00204 0,779
• Untuk menentukan parameter kinetika enzim dengan metode Langmuir, Langmuir Plot dengan
mengalikan persamaan 1 𝑉 = 𝐾𝑚 𝑉𝑚𝑎𝑥𝑆 + 1 𝑉𝑚𝑎𝑥 dengan
s, maka bentuk linearisasi persamaan Michaelis-Menten menjadi Langmuir adalah :
𝑆 𝑉 = 𝐾𝑚 𝑉𝑚𝑎𝑥 + 𝑆 𝑉𝑚𝑎𝑥
• Sehingga sebuah plot Langmuir pada s/v versus s harus menghasilkan garis lurus dengan slop 1/vmax dan intercept Km/Vmax. Linearisasi dari metode ini menghasilkan kesalahan yang kecil, sehingga metode Langmuir direkomendasikan sebagai metode untuk menentukan Km dan Vmax.
s (mol/L) s/v (min) 0,0250 12,89 0,0227 11,88 0,0184 9,95 0,0135 7,50 0,0125 7,02 0,00730 5,00 0,00460 3,93 0,00204 2,62 y = 444,8x + 1,702 R² = 0.9984 0 2 4 6 8 10 0.00204 0.0046 0.0073 0.0125 0.0135 S/ V ( min ) S (mol/L)
Hubungan S/V vs S dalam Reaksi Hidrolisis Laktosa
Data Plot Langmuir
Gambar Grafik Plot Data Perhitungan Langmuir
Persamaan garis pada grafik adalah
y = 444,8x + 1,702
•
1𝑉𝑚𝑎𝑥
= 445 mol
-1
min
• V
max= 2,25
×
10
-3mol min
-1•
𝐾𝑚𝑉𝑚𝑎𝑥
= 1,70
• K
m= 1,70
×
2,25
×
10
-3= 3,83
×
10
-3mol
-1• Jadi K
mbernilai 3,83
×
10
-3mol
-1dan V
max
=
8. Bagaimana pengaruh suhu
terhadap laju reaksi enzimatik?
• Enzim umumnya merupakan protein globular. Aktivitas enzim ditentukan oleh
struktur tiga dimensinya (struktur
kuaterner). Walaupun struktur enzim
menentukan fungsinya, prediksi aktivitas enzim baru yang hanya dilihat dari strukturnya adalah hal yang sangat sulit.
• Kebanyakan enzim berukuran lebih besar daripada substratnya. Enzim terdiri dari sisi aktif dan inaktif.
• Enzim merupakan rantai asam amino
yang melipat. Tiap-tiap urutan asam amino menghasilkan struktur pelipatan dan sifat-sifat kimiawi yang khas.
Enzim
adalah biomolekul berupa protein
yang berfungsi sebagai katalis (senyawa
yang mempercepat proses reaksi tanpa
habis
bereaksi)
dalam
suatu
reaksi
biokimia. Hal ini akan menyebabkan
zat awal yang disebut substrat akan
dipercepat
perubahannya
menjadi
molekul lain yang disebut produk.
E + S
ES
E + P
• Pada reaksi antara substrat dan enzim, saat terjadi pemanasan, aktivitas enzim meningkat, sehingga terjadi gerakan termodinamik atau tumbukan antara substrat dan enzim.
• Pada suhu rendah, aktivitas enzim rendah, bahkan bisa berhenti sama sekali.
• Pada suhu diatas suhu optimum, aktivitas enzim menurun karena terjadi denaturasi pada enzim.
• Karena enzim tersusun dari protein maka enzim sangat peka terhadap temperatur. Temperatur terlalu tinggi dapat menyebabkan denaturasi protein.
KIRI
Molekul enzim & substrat bergerak lambat. Dengan naiknya suhu, energi kinetik mereka meningkat dan gerakan yang terjadi lebih cepat . Semakin tinggi suhu, semakin cepat gerakan dan lebih sering terjadi tabrakan dan menyebabkan reaksi berlangsung lebih cepat.
TENGAH
Suhu terbaik untuk reaksi, disebut suhu optimum.
KANAN
Setelah mencapai suhu optimum, laju reaksi mulai melambat. Hal ini karena enzim molekul mulai didenaturasi dan tidak lagi cocok menjadi situs aktif, sampai akhirnya tidak ada reaksi terjadi sama sekali.
Hampir semua enzim memiliki aktivitas optimum pada suhu sekitar
30oC & denaturasi dimulai pada
temperatur 45oC (Winarno,1986).
Hubungan antara suhu dan laju reaksi secara
empiris dinyatakan dengan ketetapan
Arrhenius
k : Laju Reaksi
A : Tetapan Arrhenius
R : Konstanta gas (1,987 kal / g-mole K)
T : Temperatur K
E
A: Energi Aktivasi ( J mol
-1)
Perubahan nilai k terhadap perubahan suhu (T) yang dinyatakan dalam hubungan
Arrhenius
Contoh
• Dari data tabel di bawah ini terlihat bahwa
beberapa enzim memiliki suhu optimal
yang
berbeda-beda
dan
bervariasi
tergantung pada jenis enzim itu sendiri.
• Dari tabel Hasil Pengamatan Pegaruh Suhu
Terhadap Aktivitas Enzim Amilase yang
diambil dari hasil praktikum Biokimia Gizi
(IPB 2013) di bawah ini, dapat terlihat
bahwa enzim amylase memiliki suhu
optimum dan bekerja efektif pada suhu
25
oC.
Tabel Hasil Pengamatan Pegaruh Suhu
Terhadap Aktivitas Enzim Amilase (IPB, 2013)
Suhu (oC) ∆A / menit (V) 0 0,106 25 0,146 Suhu Ruang 0,043 37 0,047 60 0,038 100 0,031
9. Bagaimana menghitung yields pada
kultur sel dan peran pentingnya
sebagai salah satu parameter kinetika
reaksi?
Konsep Dasar
Yield
(theoritical
yield)
Faktor Yield
Nutrisi yang dibutuhkan Karakteristik produksi
Biaya
Definisi
• Yield merupakan suatu koefisien yang
berguna untuk menghubungkan substrat
terkonsumsi, sel-sel baru yang dihasilkan,
dan produk yang dihasilkan.
• Ketika
kita
mengikutsertakan
proses
pertumbuhan
sel
pada
perhitungan
maka
akan menggunakan banyak enzim
dan konversi kimia. Meskipun kompleks,
prinsip-prinsip yield dapat diterapkan untuk
metabolisme yang berkaitan dengan aliran
substrat untuk pembentukan biomassa.
Yield terkespresikan dengan menggunakan
koefisien yield atau faktor yield
Y
FG= faktor yield
ΔF = massa yang diproduksi
ΔG = massa yang dikonsumsi
Pada kultur sel, nilai ΔF dan ΔG dihitung sebagai perbedaan antara nilai awal dan nilai akhir. Nilai ini merepresentasikan sebagai nilai rata-rata seluruh yield dari keseluruhan langkah.
Y
FG
Y
xs
Sebagai contoh, YXS pada suatu waktu tertentu:
Yield akan bervariasi pada setiap periode, oleh karena itu selain harus menghitung nilai keseluruhan yield kita juga harus menghitung nilai yield pada titik waktu tertentu.
Massa atau mol produk yang terbentuk per satuan massa atau mol substrat dikonsumsi.
YPS
Massa atau mol biomassa yang dihasilkan per satuan massa atau mol substrat dikonsumsi.
YXS
X = biomassa S = substrat
P = produk
C = karbon dioksida (carbon dioxyde)
O = oksigen
Massa atau mol karbon dioksida yang terbentuk per satuan massa atau mol substrat
dikonsumsi.
YCS YPX
Massa atau mol produk yang terbentuk per satuan massa atau mol biomasa terbentuk.
Massa atau mol biomasa yang terbentuk per satuan massa atau mol oksigen yang dikonsumsi.
YXO
RQ
Respiratory Quotient. Mol karbon dioksida yang terbentuk per mol dikonsumsi oksigen. Hasil ini disebut hasil bagi pernafasan.
Massa atau mol biomassa terbentuk per mol ATP
terbentuk.
Massa atau mol biomassa yang terbentuk per kilo kalori panas yang berkembang selama fermentasi.
YCAL YATP
Biomass Yield
Biomass yield dipengaruhi oleh banyak faktor, seperti: - komposisi medium
- sumber karbon dan nitrogen
- pH
- temperatur
MW cell = biomass formula-weight ditambah residu catatan: tidak terdapat extracellular product
10. Bagaimana anda mengevaluasi
proses kultivasi sel, mulai dari
pertumbuhan sel, serapan substrat
hingga laju produksinya?
Kultivasi Sel
• Kultivasi adalah menumbuhkan sel/
bakteri dalam biakan murni
• Hal yang perlu diperhatikan untuk
mengevaluasi proses kultivasi sel:
Laju Pertumbuhan Serapan Substrat
Laju Pertumbuhan Sel
Hal yang perlu diketahui:
konsentrasi sel
Metode pengukuran konsentrasi sel:
Metode pengukuran langsung jumlah sel
Metode pengukuran berat kering sel
Metode turbidity (tingkat kekeruhan kultur)
Metode pengukuran produk yang terbentuk
Terlepas dari metode di atas, terdapat
suatu teknik pengukuran konsentrasi sel,
yaitu
diferensiasi grafik konsentrasi
.
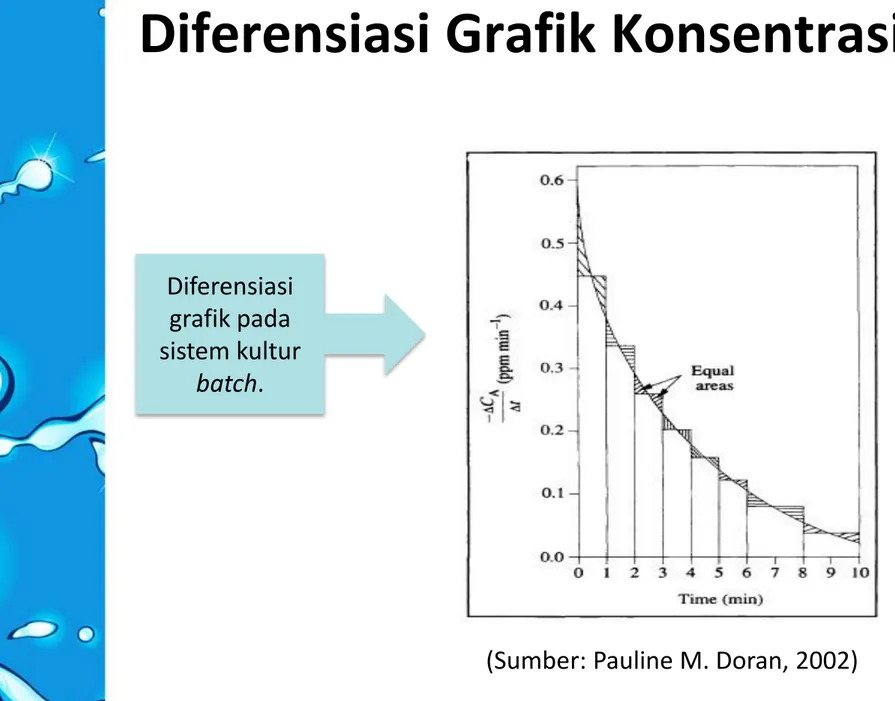
Diferensiasi Grafik Konsentrasi
• Berguna untuk -> menyatakan laju pertumbuhanvolumetrik (rx) dalam kultur batch.
Ketika rx diketahui, maka laju pertumbuhan spesifik (μ) dapat dihitung dengan membagi rx terhadap konsentrasi sel.
μ = rx/x
• Laju volumetrik serapan substrat dan pembentukan produk, rS dan rP, juga dapat dievaluasi dengan metode diferensiasi grafik konsentrasi substrat dan produk.
Ketika rS dan rP diketahui, laju pembentukan produk spesifik qP dan laju serapan substrat spesifik qS dapat diperoleh dengan membagi laju volumetriknya masing-masing terhadap konsentrasi sel.
Diferensiasi Grafik Konsentrasi
(Sumber: Pauline M. Doran, 2002) Diferensiasi
grafik pada sistem kultur
Kinetika Serapan Substrat Sel
• Tidak hanya untuk pertumbuhan serta
pembentukan (sintesis) produk, penambahan substrat juga ditujukan untuk mengenerasi energi untuk menjaga aktivitas selnya.
• Laju spesifik serapan substrat untuk menjaga
aktivitas sel dikenal sebagai maintenance
coefficient (mS).
• Dimensi untuk mS adalah T-1 dengan satuan (kg
biomassa)-1s-1. Nilai koefisien ini berbeda pada
Maintenance coefficient
beberapa
organisme dengan glukosa sebagai energi
Kinetika Serapan Substrat Sel
• Persamaan laju serapan substrat sebagai
fungsi dari konsentrasi biomassa:
Keterangan:
rs = laju volumetrik konsumsi substrat (kgm-3s-1) qS = laju spesifik serapan substrat
x = konsentrasi biomassa.
Kinetika Serapan Substrat Sel
• Pada kondisi dimana tidak terjadi pembentukan
produk, diasumsikan jika seluruh substrat
digunakan untuk pertumbuhan dan fungsi
pemeliharaan (maintenance), persamaan laju
aktivitas selnya adalah:
Keterangan:
rX = laju volumetrik pembentukan biomassa YXS = yield biomassa dari substrat
mS = maintenance coefficient x = konsentrasi biomassa
Kinetika Serapan Substrat Sel
• Untuk kondisi dimana terjadi pembentukan substrat yang disertai dengan metabolisme energi, laju konsumsi substrat merupakan fungsi dari 3 faktor, yaitu laju pertumbuhan, laju pembentukan produk, dan laju serapan substrat
untuk pemeliharaan (maintenance).
Persamaannya, yaitu:
Keterangan:
rS =laju volumetrik konsumsi substrat rP =laju volumetrik pembentukan produk YPS = yield produk dari substrat.
Daftar Pustaka
• Anonim. Inhibition of Enzyme Activity [pdf]. Terdapat pada <http://www.csun.edu/~hcchm001/5enzyme.pdf> diakses pada 17 April 2016.
• Anonim.2009. Teknik Fermentasi. <akademik.che.itb.ac.id/ /fer-teknik-fermentasi.pdf>. [ONLINE]. Diakses pada
tanggal 18 April 2016.
• Doran, Pauline M., 1995. Bioprocess Engineering Principles. Elsevier Science & Technology Books
• Fogler, H. Scott. 2006. Elements of Chemical Reaction Engineering 4th edition. USA: Pearson Education, Inc.
• Julianti, Elisa., 2013. Kinetika Pertumbuhan Mikroba [pdf] Terdapat pada
<http://elisajulianti.files.wordpress.com/2013/03/kinetika-pertumbuhan-mikroba.pdf> diakses pada 17 April 2016