BAB II
TINJAUAN PUSTAKA 2.1 Bahan Tambahan Pangan
Bahan tambahan pangan dalam Peraturan Menteri Kehatan RI No. 1168/Menkes/PER/X/1999 adalah bahan yang biasanya tidak digunakan sebagai makanan dan biasanya bukan merupakan komponen khas makanan, mempunyai atau tidak mempunyai nilai gizi, yang dengan sengaja ditambahkan ke dalam makanan untuk maksud teknologi pada pembuatan, pengolahan, penyiapan, perlakuan, pengepakan, pengemasan dan penyimpanan (Cahyadi, 2008).
Tujuan penggunaan bahan tambahan pangan adalah dapat meningkatkan atau mempertahankan nilai gizi dan kualitas daya simpan. Bahan tambahan pangan yang digunakan hanya dapat dibenarkan apabila, tidak digunakan untuk menyembunyikan atau menutupi penggunaan bahan yang salah atau yang tidak memenuhi persyaratan dan tidak digunakan untuk menyembunyikan cara kerja yang bertentangan dengan cara produksi yang baik untuk pangan serta tidak digunakan untuk menyembunyikan kerusakan bahan pangan (BPOM, 2003).
Bahan Tambahan Pangan (BTP) yang diizinkan penggunaannya antara lain antioksidan, antikempal, pengatur keasamam, pemanis buatan, pemutih, pengental, pengawet, pengeras, pewarna, penyedap rasa dan sekuestran (Cahyadi, 2008). Bahan Tambahan Pangan (BTP) yang sering digunakan adalah pemanis buatan, pewarna dan pengawet (BPOM, 2003).
2.2 Bahan Pewarna
Zat pewarna dibagi menjadi dua kelompok yaitu certified color dan uncertified color. Certified color merupakan zat pewarna sintetik yang diijinkan
penggunaannya dalam makanan (Tabel 1). Untuk pewarna sintetik dikatakan aman apabila kandungan arsennya tidak boleh lebih dari 0,00014% dan timbalnya tidak lebih dari 0,001%, sedangkan logam berat lainnya tidak ada. Uncertified color adalah zat pewarna yang berasal dari bahan alami (Tabel 2) (Winarno, 2004). Beberapa zat pewarna sintetik yang dilarang penggunaannya dalam makanan adalah Rhodamin B, Sudan-I, Metanil Yellow, dan Ponceau 3R (Tabel 3).
Penambahan bahan pewarna pangan dilakukan untuk beberapa tujuan, yaitu untuk memberi kesan menarik bagi konsumen, menyeragamkan warna makanan, menutupi perubahan warna selama proses pengolahan dan mengatasi perubahan warna selama penyimpanan (BPOM, 2003).
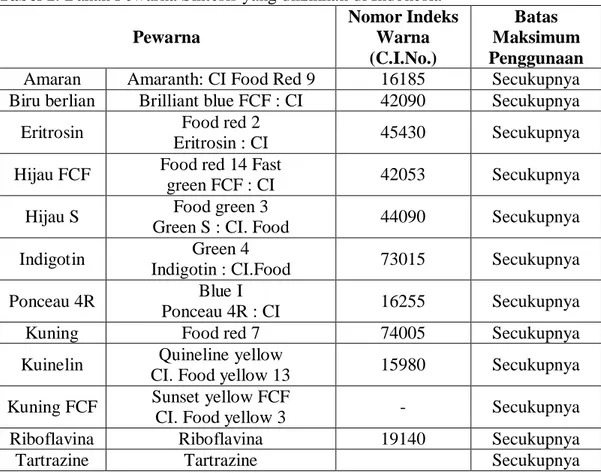
Tabel 1. Bahan Pewarna Sintesis yang diizinkan di Indonesia Pewarna Nomor Indeks Warna (C.I.No.) Batas Maksimum Penggunaan Amaran Amaranth: CI Food Red 9 16185 Secukupnya Biru berlian Brilliant blue FCF : CI 42090 Secukupnya
Eritrosin Food red 2
Eritrosin : CI 45430 Secukupnya Hijau FCF Food red 14 Fast
green FCF : CI 42053 Secukupnya Hijau S Food green 3
Green S : CI. Food 44090 Secukupnya Indigotin Green 4
Indigotin : CI.Food 73015 Secukupnya Ponceau 4R Blue I
Ponceau 4R : CI 16255 Secukupnya
Kuning Food red 7 74005 Secukupnya
Kuinelin Quineline yellow
CI. Food yellow 13 15980 Secukupnya Kuning FCF Sunset yellow FCF
CI. Food yellow 3 - Secukupnya
Riboflavina Riboflavina 19140 Secukupnya
Tartrazine Tartrazine Secukupnya
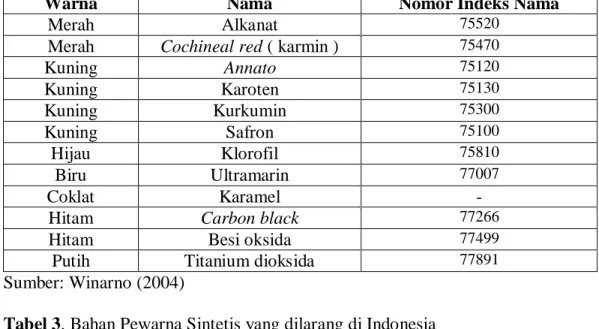
Tabel 2. Zat Pewarna Alami bagi Makanan dan Minuman yang Diijinkan di Indonesia
Warna Nama Nomor Indeks Nama
Merah Alkanat 75520
Merah Cochineal red ( karmin ) 75470
Kuning Annato 75120 Kuning Karoten 75130 Kuning Kurkumin 75300 Kuning Safron 75100 Hijau Klorofil 75810 Biru Ultramarin 77007 Coklat Karamel -
Hitam Carbon black 77266
Hitam Besi oksida 77499
Putih Titanium dioksida 77891
Sumber: Winarno (2004)
Tabel 3. Bahan Pewarna Sintetis yang dilarang di Indonesia
Bahan Pewarna Nomor Indeks Warna
(C.I.No.)
Citrus red No.2 12156
Ponceau 3 R (Red G) 161155
Ponceau SX (Food Red No. 1) 14700
Rhodamine B (Food Red No. 5) 45170
Guinea Green B (Acid Green No. 3) 42085
Magenta (Basic Violet No. 14) 42510
Chrysoidine (Basic Orange No. 2) 11270 Butter Yellow (Solveent yellow No. 2) 11020
Sudan I (Food Yellow No. 2) 12055
Methanil Yellow (Food Yellow No. 14) 13065 Auramine (Ext. D & C Yellow No.1) 41000 Oil Oranges SS (Basic Yellow No. 2) 12100 Oil Oranges XO (Solvent Oranges No. 7) 12140 Sumber: Cahyadi (2008).
2.3 Rhodamin B
Rhodamin B merupakan zat warna sintetik yang umum digunakan sebagai pewarna tekstil. Nama lazim dari rhodamin B adalah tetraethylrhodamine; D&C Red No. 19; rhodamine B chloride dan rumus kimia C28H31N2O3Cl, rumus bangun rhodamin B (pada Gambar 1), BM 479.
O
COOH
(H3CH2C)2N N+(CH2CH3)
Cl
-Gambar 1. Rumus Bangun Rhodamin B
Pemerian rhodamin B yaitu hablur hijau atau serbuk ungu kemerahan dan berfluoresensi. Rhodamin B sangat mudah larut dalam air dan dalam alkohol; sukar larut dalam asam encer dan dalam larutan alkali. Rhodamin B digunakan sebagai pewarna untuk sutra, katun, wol, nilon, serat asetat, kertas, tinta dan pernis, sabun, pewarna kayu, bulu, kulit dan pewarna untuk keramik China (Budavari, 1996).
Penggunaan rhodamin B pada makanan dan minuman dalam waktu lama (kronis) akan mengakibatkan kanker dan gangguan fungsi hati. Namun demikian, bila terpapar rhodamin B dalam jumlah besar maka dalam waktu singkat akan terjadi gejala akut keracunan rhodamin B. Bila rhodamin B tersebut masuk melalui makanan akan mengakibatkan iritasi pada saluran pencernaan dan mengakibatkan gejala keracunan dengan urine yang berwarna merah maupun merah muda. Selain melalui makanan dan minuman, rhodamin B juga dapat mengakibatkan gangguan kesehatan, jika terhirup akan terjadi iritasi pada saluran pernafasan. Mata yang terkena rhodamin B juga akan mengalami iritasi yang ditandai dengan mata kemerahan dan timbunan cairan atau udem pada mata.Jika terpapar pada bibir dapat menyebabkan bibir akan pecah-pecah, kering, gatal, bahkan kulit bibir terkelupas (Yulianti, 2007).
2.4 Analisis Kualitatif dan Kuantitatif Rhodamin B
Analisis kualitatif rhodamin B dapat dilakukan dengan beberapa cara seperti cara reaksi kimia, cara kromatografi kertas, kromatografi lapis tipis (KLT) dan spektrofotometer sinar tampak, sedangkan untuk analisis kuantitatif rhodamin B dilakukan secara spektrofotometer sinar tampak.
2.4.1 Cara Reaksi Kimia
Cara reaksi kimia dilakukan dengan cara menambahkan pereaksi-pereaksi berikut : HCl pekat, H2SO4 pekat, NaOH 10%, dan NH4OH 10%. Lalu diamati perubahan warna yang terjadi pada masing-masing sampel yang sudah dilakukan pemisahan dari bahan-bahan pengganggu (Cahyadi, 2008).
2.4.2 Cara Kromatografi Kertas
Sejumlah cuplikan ditambahkan dengan asam asetat encer kemudian dimasukkan benang wool bebas lemak dipanaskan di atas penangas air sambil diaduk-aduk. Benang wool dicucu dengan air hingga bersih. Pewarna dilarutkan dari benang wool dengan penambahan amoniak 10% diatas penangas air hingga sempurna. Totolkan pada kertas kromatografi, juga totolkan baku pembanding. Elusi dengan eluen I (etilmetalketon : aseton : air = 70 : 30 : 30) den eluen II (2 g NaCl dalam 100 ml etanol 50%) (Cahyadi, 2008).
2.4.3 Metode Kromatografi Lapis Tipis (KLT)
Kromatogafi Lapis Tipis (KLT) adalah metode kromatografi cair yang paling sederhana. Kromatografi Lapis Tipis (KLT) yang dapat dipakai dengan dua tujuan. Pertama, digunakan untuk uji identifikasi senyawa baku. Untuk meyakinkan identifikasi dapat dilakukan dengna menggunakan lebih dari 1 fase gerak dan jenis semprot. Teknik spiking dengan menggunakan senyawa baku
yang telah diketahui sangat dianjurkan untuk lebih memantapkan pengambilan keputusan identifikasi senyawa. Kedua digunakan untuk analisis kuantitatif dengan KLT. Pertama bercak diukur langsung pada lempeng dengan menggunakan ukuran luas atau densitometri. Cara kedua adalah dengan mengerok bercak lalu menetapkan kadar senyawa yang terdapat dalam bercak tersebut dengan metode analisis lain, misalkan dengan metode spektrofotometri (Rohman, 2007).
Analisis kualitatif rhodamin B dengan menggunakan metode Kromatografi Lapis Tipis (BPOM, 2000) dengan prinsip membandingkan harga Rf, jika dilihat secara visual berwarna merah jambu dan jika dilihat dibawah sinar UV 254nm berfluoresensi kuning.
Faktor–faktor yang mempengaruhi gerakan noda dalam kromatografi lapisan tipis yang juga mempengaruhi harga Rf:
a. Struktur kimia dari senyawa yang sedang dipisahkan b. Sifat dari penyerap dan derajat aktifitasnya
c. Tebal dan kerataan dari lapisan penyerap d. Pelarut dan derajat kemurnian fase gerak
e. Derajat kejenuhan dari uap dalam bejana pengembangan yang digunakan f. Teknik percobaan
g. Jumlah cuplikan yang digunakan h. Suhu
2.4.4 Metode Spektrofotometri Sinar Tampak
Analisis kualitatif dan kuantitatif Rhodamin B dapat dilakukan dengan metode spektrofotometer sinar tampak (BPOM, 2006). Untuk analisis kualitatif Rhodamin B dengan menggunakan spektrofotometer sinar tampak yaitu dengan membandingkan kurva absorbansi yang diukur secara spektrofotometer sinar tampak pada panjang gelombang 450-750nm (kenkel, 1994) dan untuk analisis kuantitatif dengan spektrofotometer sinar tampak dengan mengukur absorbansinya kemudian kadar rhodamin B dalam sampel dapat dihitung dengan menggunakan kurva kalibrasi dengan persamaan regresi y = ax + b.
Spektrofotometri Sinar Tampak adalah pengukuran absorbansi energi cahaya oleh suatu sistem kimia pada suatu panjang gelombang tertentu (Day, 2002). Spektrum UV-Vis mempunyai bentuk yang lebar dan hanya sedikit informasi tentang struktur yang bias didapatkan dari spektrum ini. Tetapi spektrum ini sangat berguna untuk pengukuran secara kuantitatif. Konsentrasi dari analit di dalam larutan bisa ditentukan dengan mengukur absorban pada panjang gelombang tertentu dengan menggunakan hukum Lambert-Beer (Darchriyanus, 2004; Rohman, 2007). Sinar ultraviolet mempunyai panjang gelombang antara 200-400 nm, dan sinar tampak mempunyai panjang gelombang 400-750 nm (Darchriyanus, 2004; Ditjen POM, 1995).
Hukum Lambert-Beer (Beer’s Law) adalah hubungan linieritas antara absorban dengan konsentrasi larutan analit (Darchriyanus, 2004). Menurut Rohman (2007) dan Day (2002), Hukum Lambert-Beer menyatakan bahwa intensitas yang diteruskan oleh larutan zat penyerap berbanding lurus dengan tebal dan konsentrasi larutan dan berbanding terbalik dengan transmitan.
Panjang gelombang yang digunakan untuk analisis kuantitatif adalan panjang gelombang yang mempunyai absorbansi maksimal, dilakukan dengan membuat kurva hubungan antara absorbansi dengan panjang gelombang dari suatu larutan baku pada konsentrasi tertentu.
Ada beberapa alasan mengapa harus menggunakan panjang gelombang maksimal, yaitu :
1. Pada panjang gelombang maksimal, kepekaannya juga maksimal karena pada panjang gelombang maksimal tersebut, perubahan absorbansi untuk setiap satuan konsentrasi adalah yang paling besar.
2. Disekitar panjang gelombang maksimal, bentuk kurva absorbansi datar dan pada kondisi tersebut hukum Lambert-Beer akan terpenuhi.
3. Jika dilakukan pengukuran ulang maka kesalahan yang disebabkan oleh pemasangan ulang panjang gelombang akan kecil sekali, ketika digunakan panjang gelombang maksimal.
Ada beberapa tahapan yang harus dilakukan dalam analisis dengan spektrofotometri ultraviolet dan cahaya tampak yaitu:
1. Penentuan Panjang Gelombang Serapan Maksimum
Panjang gelombang yang digunakan untuk analisis kuantitatif adalah panjang gelombang dimana terjadi absorbansi maksimum. Untuk memperoleh panjang gelombang maksimum dapat diperoleh dengan membuat kurva hubungan antara absorbansi dengan panjang gelombang dari suatu larutan baku dengan konsentrasi tertentu.
2. Waktu kerja (operating time)
Tujuannya ialah untuk mengetahui waktu pengukuran yang stabil. Waktu kerja ditentukan dengan mengukur hubungan antara waktu pengukuran dengan absorbansi larutan.
3. Pembuatan Kurva Kalibrasi
Dilakukan dengan membuat seri larutan baku dalam berbagai konsentrasi kemudian absorbansi tiap konsentrasi diukur lalu dibuat kurva yang merupakan hubungan antara absorbansi dengan konsentrasi. Kurva kalibrasi yang lurus menandakan bahwa hukum Lambert-Beer terpenuhi.
4. Pembacaan absorbansi sampel
Absorbansi yang terbaca pada spektrofotometer hendaknya terletak antara 0,2 sampai 0,8 atau 15% sampai 70% jika dibaca sebagai transmitan. Hal ini disebabkan karena kisaran nilai absorbansi tersebut kesalahan fotometrik yang terjadi adalah paling minimal.
5. Perhitungan Kadar
Perhitungan kadar dapat dilakukan dengan metode regresi yaitu dengan menggunakan persamaan garis regresi yang didasarkan pada harga serapan dan larutan standar yang dibuat dalam beberapa konsentrasi, paling sedikit menggunakan 5 rentang konsentrasi yang meningkat yang dapat memberikan serapan linier, kemudian di plot menghasilkan suatu kurva kalibrasi, konsentrasi suatu sampel dapat dihitung berdasarkan kurva tersebut (Rohman, 2007).
Rumus Perhitungan Kadar Rhodamin B. K = BS Fp x V x X
X = kadar Rhodamin sesudah pengenceran V = Volume sampel (ml)
Fp = Faktor Pengenceran BS= Berat sampel
2.6 Perolehan Kembali
Persen perolehan kembali digunakan untuk menyatakan kecermatan. Kecermatan merupakan ukuran yang menunjukkan derajat kedekatan hasil analisis dengan kadar analit sebenarnya. Kecermatan dapat ditentukan dengan dua cara yaitu metode simulasi (spiked-placebo recovery) dan metode penambahan baku (standard addition method). Dalam metode simulasi, sejumlah analit bahan murni pembanding kimia ditambahkan ke dalam campuran bahan pembawa sediaan farmasi (plasebo) lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan. Metode adisi dapat dilakukan dengan menambahkan sejumlah analit dengan konsentrasi tertentu pada sampel yang diperiksa lalu dianalisis lagi dengan metode tersebut (WHO, 1992).
Menurut WHO (1992), perolehan kembali dapat dihitung dengan rumus
sebagai berikut : Uji perolehan kembali (%) = C*A
CA
CF − x 100%
Keterangan : CF = konsentrasi sampel yang diperoleh setelah penambahan larutan baku
CA= konsentrasi sampwl sebelum panambahan baku
2.7 Batas Deteksi dan Batas Kuantitatif
Batas Deteksi adalah konsentrasi analit terendah dalam sampel yang masih dapat dideteksi. Batas Deteksi dapat diperoleh dari kalibrasi standar yang diukur sebanyak 6 sampai 10 kali (Gandjar, 2007;Satiadarma, 2004).
Batas deteksi dapat dihitung dengan rumus.
Batas Deteksi =
slope SD x
3
Batas Kuantitatif adalah kuantitatif terkecil analit dalam sampel yang masih dapat diukur dalam kondisi percobaan yang sama dan masih memenuhi criteria cermat dan seksama (WHO,1992).
Batas kuantitatif dapat dihitung dengan rumus.
Batas Kuantitatif =
slope SD x