6 BAB II
TINJAUAN PUSTAKA
2.1 Tinjauan Umum Tanaman Jeruk Keprok (Citrus reticulata)
Jeruk keprok SoE (Citrus reticulata Blanco) merupakan salah satu jeruk unggul Indonesia yang telah ditetapkan sebagai varietas unggul nasional (SK Menteri Pertanian No. 863/Kpts/TP.240/11/98) dan sebagai jeruk substitusi impor, khususnya untuk jenis mandarin. Penelitian (Adar et al, 2003) menunjukkan, jeruk keprok SoE memiliki mutu yang dapat bersaing dengan jeruk impor yang dipasarkan di Indonesia.
Varietas yang masuk dalam kelompok ini adalah semua jenis jeruk keprok dan Siam yang di kenal di Inonesia. Deskripsi yang diberikan untuk kelompok ini adalah:
“Ukuran buah kecil hingga besar sedang, bentuk buah bulat, bulat pipih, bagian atas kadang berkerah, bagian bawah cenderung datar, Kulit tipis hingga tebal, kadang cukup rekat, permukaan halus berpori, kadang berminyak, warna kulit kuning ke oranye saat matang, juring antara 10-14, axis ada yang rapat.”
Beberapa varietas lokal Indonesia yang masuk dalam kelompok ini adalah Keprok dan Siam. Balai Penelitian Tanaman Jeruk dan Buah Suptropika saat ini memiliki 83 varietas Mandarin yang berasal dari introduksi (42 jenis) dan domistik (41 jenis). Beberapa jenis domestik yang telah dikembangkan diantaranya Keprok Soe, Keprok Beras Sitepu, Keprok Batu 55, Siem Maga dan Siem Madu Batu 55, Soe, Berasitepu, dan Garut. Terdapat beberapa varietas Common Mandarin yang sangat terkenal di seluruh dunia adalah Clementine Algeria, Dancy Tangerine, Freemont, Murcott, Ponkan, Oseola, Robinson (Martasari, C, 2017).
2.1.1 Klasifikasi
Kingdom : Plantae
Division : Magnoliophyta Class : Magnoliopsida
Order : Sapindales Family : Rutaceae Subfamily : Aurantoideae
Genus : Citrus
Species : Citrus reticulata L. (CCRC, 2014) .
Gambar 2. 1 Buah jeruk keprok (Citrus reticulata) 2.1.2 Morfologi
Duri pada C. reticulata Blanco panjang durinya antara 1-4 cm, Bentuk daun obovate terlihat pada jenis C. reticulata Blanco (keprok Batu), ovalis obovate terlihat pada C. reticulata Blanco (keprok Pulung), dasar daun tumpul pada C.
reticulata Blanco, Ujung daun pada C. reticulata Blanco (keprok Batu dan keprok Pulung) yaitu runcing, membulat pada C. reticulata Blanco (keprok Cinakonde).
Panjang helaian daun C. reticulata Blanco 7,8-9,8 cm. Rasio panjang dan lebar daun rasio 1,5-2:1 pada C. reticulata Blanco (keprok Cinakonde dan keprok Batu) rasio 2-2,5:1 pada keprok Pulung. Tangkai daun bentuk sayap pada C. reticulata Blanco terdapat variasi, yaitu linear pada keprok Batu dan obovate pada keprok Pulung. Rentangan panjang sayap pada C. reticulata Blanco 0,3-1,6 cm. C.
reticulata Blanco rasio perbandingan panjang dan lebar sayap yaitu 1-3:1 pada keprok Batu dan 3,5:1 pada keprok Pulung. Kerapatan kelenjar dalam 1 cm2 pada C. reticulata Blanco rentangannya 112-232, kecuali khusus pada keprok Batu memiliki rentangan yang kecil yaitu 24-40. Jumlah bunga pada perbungaannya 1-8 pada C. reticulata Blanco. Jumlah perhiasan bunga (kelopak dan mahkota) adalah 4. ujung kelopak meruncing pada C. reticulata Blanco. Jumlah kelenjar minyak di mahkota berkisar antara 35-90 μm dan 20-53 μm. Panjang anthera (benang sari)
pada C. reticulata Blanco memilki rentangan antara 0,5-0,8 cm. Jumlah benang sari secara umum merupakan kelipatan dari jumlah perhiasan bunga. Jumlah benang sari pada C. reticulata Blanco berjumlah 20-30. Tinggi putik (stilus) memiliki rentangan 0,5-1,7 cm. Jumlah ruang karpel (bakal buah) pada C. reticulata Blanco 10-15. Bentuk serbuk sari diamati dari pandangan kutub, yaitu bulat. Ukuran serbuk sari dari pandangan kutub antara 12-24 μm (Hardiyanto et al, 2006)
2.1.3 Khasiat
Khasiat dari Citrus reticulata antara lain untuk pertahanan tubuh, antikanker, memerangi infeksi virus, dan menurunkan kadar kolesterol (Wirakusumah, 2002). Beberapa khasiat yang dimiliki Jeruk Citrus reticulata yakni pada bagian kulit buahnya antitoksik, deuretik, pencahar, pusing, bunga untuk stimulant jantung, sakit perut, mual, batang digunakan untuk stimulant jantung.
Tumbuhan ini juga memiliki khasiat sebagai antikarsnogenik, hiperglikemia, antiinflamasi, antialergi, analgesik, antimikroba, antidepresan, antibakteri dan antiplatelet (Sidana, 2013).
2.1.4 Kandungan
Menurut (Lim, 2012) kandungan yang terdapat dalam tumbuhan jeruk keprok yaitu vitamin c, asam askorbat, flavonoid, senyawa fenol, limonid dan pectin yang penting untuk nutrisi dan kesehatan. Buah jeruk keprok termaksud merupakan sumber kaya flavonoid seperti flavonon, flavon dan flavonol. Buah jeruk sangat kaya akan mineral, vitamin C dan senyawa polifenol, yang berkontribusi terhadap aktivitas antioksidan (Tripoli et al, 2007).
Ekstraksi minyak atsiri dengan menggunakan pelarut menghasilkan concrete. Concrete adalah produk yang dihasilkan dari proses ekstraksi pada bahan tanaman yang mengandung minyak atsiri menggunakan pelarut, yang mengandung zat pewangi alamiah, sejumlah kecil lilin, albumin dan pigmen (Guenther, 1987)
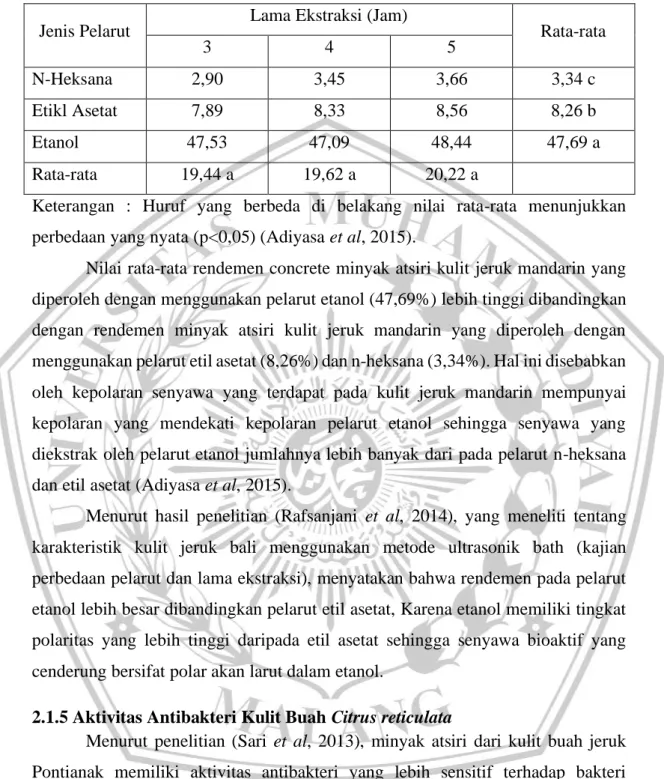
Tabel II. 1 Nilai rata-rata rendemen (%) Concrete minyak atsiri kulit jeruk mandarin
Jenis Pelarut Lama Ekstraksi (Jam)
Rata-rata
3 4 5
N-Heksana 2,90 3,45 3,66 3,34 c
Etikl Asetat 7,89 8,33 8,56 8,26 b
Etanol 47,53 47,09 48,44 47,69 a
Rata-rata 19,44 a 19,62 a 20,22 a
Keterangan : Huruf yang berbeda di belakang nilai rata-rata menunjukkan perbedaan yang nyata (p<0,05) (Adiyasa et al, 2015).
Nilai rata-rata rendemen concrete minyak atsiri kulit jeruk mandarin yang diperoleh dengan menggunakan pelarut etanol (47,69%) lebih tinggi dibandingkan dengan rendemen minyak atsiri kulit jeruk mandarin yang diperoleh dengan menggunakan pelarut etil asetat (8,26%) dan n-heksana (3,34%). Hal ini disebabkan oleh kepolaran senyawa yang terdapat pada kulit jeruk mandarin mempunyai kepolaran yang mendekati kepolaran pelarut etanol sehingga senyawa yang diekstrak oleh pelarut etanol jumlahnya lebih banyak dari pada pelarut n-heksana dan etil asetat (Adiyasa et al, 2015).
Menurut hasil penelitian (Rafsanjani et al, 2014), yang meneliti tentang karakteristik kulit jeruk bali menggunakan metode ultrasonik bath (kajian perbedaan pelarut dan lama ekstraksi), menyatakan bahwa rendemen pada pelarut etanol lebih besar dibandingkan pelarut etil asetat, Karena etanol memiliki tingkat polaritas yang lebih tinggi daripada etil asetat sehingga senyawa bioaktif yang cenderung bersifat polar akan larut dalam etanol.
2.1.5 Aktivitas Antibakteri Kulit Buah Citrus reticulata
Menurut penelitian (Sari et al, 2013), minyak atsiri dari kulit buah jeruk Pontianak memiliki aktivitas antibakteri yang lebih sensitif terhadap bakteri Escherichia coli dibandingkan Staphylococcus aureus. Hasil diameter rata-rata zona hambat dari tiap konsentrasi pada bakteri uji Staphylococcus aureus secara berurutan yakni 0,5;1,5; dan 2,5 mg/mL sebesar 15; 16; dan 19 mm sedangkan pada bakteri Escherichia coli yakni sebesar 16, 33; 18; dan 21 mm
Pada penelitian sebelumnya ekstrak kulit Citrus reticulata yang diperoleh dengan metode destilasi hidrolik dengan digunakan metode difusi cakram. Dari proses penelitian tersebut didapatkan hasil bahwa dengan kulit buah Citrus reticulata memberikan zona hambat sebesar 16 mm dengan dosis 9 µL/ml (Sultana et al., 2012).
2.2 Tinjauan Pustaka Bakteri Escherichia coli
Escherichia coli adalah spesies bakteri yang sangat beragam yang menunjukkan fleksibilitas metabolisme yang cukup besar dengan kemampuan untuk menjajah banyak inang hewan. Escherichia coli adalah bagian dari bakteri komensal nonpathogenik yang membentuk bagian dari flora usus normal manusia dan berbagai hewan (Kaper, Nataro, & Mobley, 2004). Namun, beberapa varian E.
coli telah dijelaskan yang menyebabkan infeksi pada sistem pencernaan (disebut sebagai E. coli patogen usus). Strain E. coli patogen usus umumnya dibagi menjadi yang menyebabkan diare dengan: (1) mengekspresikan toksin panas-panas atau toksin stabil-panas (enterotoksigenik E. coli (ETEC)) atau toksin Shiga (penghasil racun Shiga, E. coli (STEC), termasuk enterohemorrhagic E. coli (EHEC)); (2) menyerang mukosa usus (enteroinvasive E. coli (EIEC)); (3) menyebabkan lesi menempel dan menghilangkan pada mukosa usus (enteropathogenic E. coli (EPEC)); dan (4) mekanisme lain yang kurang terdefinisi dengan baik (mis., enteroaggregative E. coli (EaggEC)) (Nataro & Kaper, 1998). Sementara ETEC, EIEC, EPEC, dan EaggEC tetap menjadi penyebab penting diare di antara anak- anak di negara berkembang, strain E. coli patogen usus yang paling umum di negara maju adalah STEC / EHEC. EHEC yang paling umum, E. coli O157: H7, biasanya diperoleh masyarakat melalui makanan atau air yang terkontaminasi. Sebuah garis keturunan klon yang baru dikenal milik serotipe O104: H4 yang membawa sifat virulensi EHEC dan EaggEC bertanggung jawab atas wabah besar diare berdarah, sindrom hemolitik-uremik, dan kematian di Jerman pada tahun 2011 yang ditelusuri pada tauge yang terkontaminasi (Buchholz et al., 2011).
2.2.1 Klasifikasi Escherichia coli
Adapun klasifikasi bakteri Escherichia coli sebagai berikut (Melliawati, 2009):
Divisi : Bacteriophyta Kelas : Bacteria Bangsa : Eubacteriales Suku : Bacteriaceae Genus : Escherichia Spesies: Escherichia coli
Gambar 2. 2 Bakteri Escherichia coli 2.2.2 Morfologi
Escherichia coli berbentuk batang, tebal 0,5μm; panjang antara 1,0 - 3,0 μm; bervariasi dari bentuk koloid sampai berbentuk seperti filamen yang panjang;
tidak berbentuk spora; motil dan filamen perithin beberapa galur tidak memiliki flagella; bersifat Gram negatif (Merchant dan Parker, 1961). Escherichia coli adalah bakteri gram negatif yang berbentuk batang panjang, biasanya berukuran 0,5 x 1-3 μ, bersifat aerob dan anaerob fakultatif, memfermentasikan laktosa dan glukosa dengan menghasilkan asam dan gas, menunjukkan hasil positif pada uji indol, lisin dekarboksilase (Melliawati, 2009).
2.2.3 Tinjauan Pewarnaan Gram
Pewarnaan Gram ditemukan oleh Christian Gram dan merupakan salah satu pewarnaan yang sering digunakan (Dewi, 2013). Pewarnaan Gram digunakan untuk membedakan bakteri Gram positif dan Gram negatif. Bakteri Gram positif berwarna ungu disebabkan kompleks zat warna kristal violet-yudium tetap dipertahankan meskipun diberikan larutan pemucat. Sedangkan, bakteri Gram negatif berwarna merah disebabkan kompleks tersebut larut pada saat pemberian larutan pemucat
sehingga mengambil warna merah safranin. perbedaan warna pada bakteri Gram positif dan Gram negatif yaitu karena perbedaan struktur dinding sel antara kedua jenis bakteri tersebut. Bakteri Gram positif memiliki struktur dinding sel yang terdiri dari peptidoglikan tebal. Sedangkan, bakteri Gram negatif memiliki struktur dinding sel yang terdiri dari peptidoglikan tipis dan mempunyai kandungan lipid yang tinggi (Fitri & Yasmin, 2011).
2.2.4 Habitat
Escherichia coli merupakan bakteri yang secara normal terdapat di dalam usus dan berperan dalam proses pembusukan sisa-sisa makanan. Keberadaan bakteri ini merupakan parameter ada tidaknya materi fekal di dalam suatu habitat khususnya air. Escherichia coli adalah salah satu jenis bakteri yang ada dalam tinja manusia dan dapat mengakibatkan gangguan pencernaan seperti diare (Dewi, 2010). Escherichia coli adalah bakteri anaerob fakultatif dominan dari flora kolon manusia. Organisme biasanya mengkolonisasi saluran pencernaan bayi dalam beberapa jam kehidupan dan setelah itu E. coli dan inang mendapatkan manfaat bersama. E. coli biasanya tetap tidak terbatas pada lumen usus. Namun, pada inang yang lemah atau imunosupresi, atau ketika hambatan gastrointestinal dilanggar, bahkan “nonpathogenik” normal strain E. coli dapat menyebabkan infeksi. Terlebih lagi, anggota spesies kita yang paling kuat pun bisa saja rentan infeksi oleh salah satu dari beberapa klon E. coli yang sangat beradaptasi yang bersama-sama telah mengembangkan kemampuan untuk menyebabkan spektrum yang luas dari penyakit manusia. Infeksi karena E. coli yang patogen mungkin terbatas pada permukaan mukosa atau dapat menyebar ke seluruh tubuh (Nataro et al, 1998).
2.2.5 Terapi
E. coli adalah penyebab utama infeksi saluran kemih (urinary tract infection/UTI) dan juga dapat menyebabkan meningitis akut, pneumonia, infeksi intra-abdominal, infeksi enterik, dan lain-lain (GJ Holt, et al 1994, GF Brooks et al, 2001). Resistensi E. coli terhadap berbagai antibiotika telah banyak dilaporkan.
Seperti halnya Enterobacteriaceae, E. coli telah banyak yang resisten terhadap golongan β-laktam, fosfomisin, dan golongan kuinolon. Tetapi, saat ini fosfomisin dan kuinolon justru paling sering digunakan untuk mengobati kasus UTI (Lindgren et al, 2003, Huang CH et al, 2001, Nilsson AI et al, 2003).
2.2.6 Daya Kerja Antibakteri Kloramfenikol
Kloramfenikol merupakan antibiotika spektrum luas dengan aktifitas mengobati bermacam–macam infeksi yang disebabkan oleh bakteri patogen. Pada dasarnya kloramfenikol bersifat sebagai bakteriostatik dan pada konsentrasi tinggi kadang-kadang bersifat sebagai bakterisid terhadap bakteri-bakteri tertentu (Oktavia, 2016). Mekanisme kerja dari kloramfenikol yaitu dengan cara bereaksi pada subunit 50S ribosom dan menghalangi aktivitas enzim peptidil transferase.
Fungsi enzim ini untuk membentuk ikatan peptide antara asam amino baru yang masih melekat pada tRNA dengan asam amino terakhir yang sedang berkembang.
Akibatnya, sintesis protein bakteri akan berheti seketika (Pratiwi, 2008).
2.3 Tinjauan Tentang Ekstrak
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat aktif dari simplisia nabati atau simplisia hewani menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan dan massa atau serbuk yang tersisa diperlakukan sedemikian hingga memenuhi baku yang telah ditetapkan (Farmakope Indonesia Edisi V, 2014).
2.4 Tinjauan Tentang Metode Ekstraksi 2.4.1 Definisi Ekstraksi
Ekstraksi adalah penarikan zat aktif yang diinginkan dari bahan mentah obat menggunakan pelarut yang dipilih sehingga zat yang diinginkan akan larut.
Pemilihan sistem pelarut yang akan digunakan dalam ekstraksi harus berdasarkan kemampuannya dalam melarutkan jumlah yang maksimal dari zat aktif dan seminimal mungkin bagi unsur yang tidak diinginkan (Ansel, 1989). Melarutkan senyawa polar dalam pelarut polar dan senyawa non-polar dalam pelarut non-polar adalah prinsip dasar ekstraksi. Serbuk simplisia diekstraksi berturut-turut dengan pelarut yang polaritasnya berbeda (Harbone,1996). Faktor utama untuk pertimbangan pemilihan cairan penyari terdiri dari berbagai aspek, yaitu selektivitas, kemudahan bekerja dan proses dengan cairan tersebut ekonomis, ramah lingkungan, dan keamanan (Depkes RI, 2000).
2.4.2 Suhu Ekstraksi
Pada umumnya kelarutan zat aktif yang diekstrak akan bertambah besar dengan bertambah tingginya suhu. Akan tetapi, peningkatan suhu ekstraksi juga perlu diperhatikan, karena suhu yang terlalu tinggi dapat menyebabkan kerusakan pada bahan yang sedang diproses (Margaretta et al., 2011). Komponen bioaktif seperti flavonoid, tanin, dan fenol rusak pada suhu diatas 500C karena dapat mengalami perubahan struktur serta menghasilkan ekstrak yang rendah (Handayani dan Sriherfyna, 2016).
2.4.3 Tujuan Ekstraksi
Tujuan dari ekstraksi bahan alam adalah untuk menarik komponen kimia yang terdapat pada bahan alam. Ekstraksi didasarkan pada prinsip perpindahan massa komponen zat ke dalam pelarut, dimana perpindahan mulai terjadi pada lapisan antar muka kemudian berdifusi masuk ke dalam pelarut (Ditjen POM, 1986).
2.4.4 Jenis Metode Ekstraksi 2.4.4.1 Maserasi
Maserasi adalah proses pengekstrakan simplisia dengan metode pencapaian konsentrasi pada keseimbangan. Maserasi kinetik berarti dilakukan pengadukan yang kontinu (terus-menerus). Remaserasi berarti dilakukan pengulangan penambahan pelarut setelah dilakukan penyaringan maserat pertama dan seterusnya (Depkes RI, 2000). Ekstraksi dilakukan dengan menggunakan metode maserasi dengan 3 kali pengulangan tiap pelarut. Sampel kering direndam dengan perbandingan berat sampel dan volume pelarut 1 : 10 selama 24 jam (El Hady et al, 2007).
2.4.4.2 Perkolasi
Menurut (Depkes RI, 2000) Perkolasi adalah ekstraksi dimana biasanya pelarut yang digunakan harus selalu baru dan dilakukan pada suhu ruangan. Proses ekstraksi dilakukan dengan beberapa tahapan yaitu pertama tahap pengembangan bahan, kemudian tahap maserasi antara, setelah itu dilakukan tahapan perkolasi sebenarnya (penetesan/penampungan ekstark), tahapan tersebut dilakukan terus menerus sampai diperoleh ekstrak (perkolat) yang jumlahnya mencapai 1-5 kali bahan.
2.4.4.3 Soxhlet
Soxhlet adalah metode ekstraksi yang biasanya menggunakan pelarut yang selalu baru dan kebanyakan dilakukan dengan alat khusus sehingga dapat terjadi ekstraksi kontinu dengan jumlah pelarut yang relatif konstan (Depkes RI, 2000).
Teknik ini dilakukan menempatkan serbuk sampel dalam sarung selulosa (dapat digunakan kertas saring) dalam klonsong yang ditempatkan di atas labu dan di bawah kondensor. Pelarut yang sesuai dimasukkan ke dalam labu dan suhu penangas diatur di bawah suhu reflux. Keuntungan dari metode ini adalah proses ektraksi yang kontinyu, sampel terekstraksi oleh pelarut murni hasil kondensasi sehingga tidak membutuhkan banyak pelarut dan tidak memakan banyak waktu.
Kerugiannya adalah senyawa yang bersifat termolabil dapat terdegradasi karena ekstrak yang diperoleh terusmenerus berada pada titik didih (Mukhriani, 2014).
2.4.4.4 Refluks & Ekstraksi Uap
Refluks adalah ekstraksi dengan pelarut pada temperature titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik. Umumnya dilakukan pengulanngan proses residu pertama sampai 3-5 kali sehingga dapat termasuk proses ekstraksi sempurna (Depkes RI, 2000).
Destilasi uap memiliki proses yang sama dan biasanya digunakan untuk mengekstraksi minyak esensial (campuran berbagai senyawa menguap). Selama pemanasan uap terkondensasi dan destilat (terpisah sebagai dua bagian yang tidak saling bercampur) ditampung dalam wadah yang terhubung dengan kondensor.
Kerugian dari metode ini adalah senyawa yang bersifat termolabil dapat terdegradasi (Mukhriani, 2014).
2.4.4.5 Dekoksi
Pada cara dekoksi ini bagian tanaman berupa batang, kulit kayu, cabang, ranting, rimpang, atau akar direbus dalam air mendidih dengan volume tertentu dan selama waktu tertentu. Selanjutnya didinginkan dan ditekan atau disaring untuk memisahkan cairan ekstrak dari ampasnya. Proses ini sesuai untuk mengekstrak bahan bioaktif yang dapat larut dalam air dan tahan terhadap panas. Rasio antara massa bagian tanaman dengan volume air biasanya 1:4 atau 1:16. Air harus menguap secara terus-menerus selama berlangsungnya proses perebusan, sehingga
volume cairan ekstrak yang diperoleh biasanya hanya seperempat dari volume semula. Kemudian ekstrak yang telah pekat selanjutnya disaring dan segera digunakan atau diproses lebih lanjut (Kumoro, 2015).
2.5 Fraksinasi
Menurut (Venn, 2008), definisi dari fraksinasi yaitu pemisahan antara zat cair dengan zat cair berdasarkan tingkat kepolarannya. Pemisahan ekstrak dilakkukan dengan cara peningkatan polaritas seperti petroleum eter, n-heksana, kloroform, etil asetat, dan etanol. Pemilihan pelarut pada ekstraksi tergantung pada sifat analitnya dimana pelarut dan analit harus memiliki sifat yang sama, contohnya analit yang sifat lipofilitasnya tinggi akan terekstraksi pada pelarut yang relatif nonpolar seperti n-heksana sedangkan analit yang semipolar terlarut pada pelarut yang semipolar.
Fraksinasi merupakan proses pemisahan fraksi yang terkandung dalam suatu larutan atau suspensi yang mempunyai karateristik berbeda (Yuliasih et al, 2007). Menurut (Haznawati, 2012) salah satu peralatan laboratorium yang biasa digunakan untuk memisahkan komponen-komponen dalam campuran antara dua fase pelarut yang memiliki massa jenis berbeda yang tidak tercampur yaitu corong pisah.
2.6 Tinjauan Tentang Pelarut
Dalam ekstraksi pemilihan pelarut yang sesuai merupakan faktor terpenting karena jenis dan mutu dari pelarut yang digunakan sangat menentukan keberhasilan proses ekstraksi tersebut. Proses ekstraksi menggunakan pelarut didasarkan pada sifat kepolarannya. Senyawa polar akan larut pada pelarut polar (air, etanol, metanol, dan butanol), senyawa non-polar akan larut pada pelarut non-polar (n- heksan, eter, kloroform) (Kasminah, 2016).
2.6.1 Etil Asetat
Etil asetat mempunyai rumus (C4H8O6) yang dapat digunakan sebagai pelarut, meskipun juga digunakan sebagai flavoring agent. Bentuk etil asetat yaitu cairan, tidak berwarna, mudah menguap, dan berbau sedap, serta mudah terbakar.
Etil asetat dapat bereaksi keras dengan oksidasi kuat, asam kuat, dan nitrat yang dapat menimbulkan ledakan atau kebakaran. Etil asetat dapat dihasilkan dari
destilasi campuran etanol dan asam asetat dengan adanya asam sulfat pekat. Hal ini juga disusun dari etilen menggunakan katalis aluminium alkoksida (HPE, 2015).
Menurut (Putri et al, 2013), etil asetat adalah pelarut dengan toksisitas rendah yang bersifat semi polar sehingga diharapkan dapat menarik senyawa yang bersifat polar maupun nonpolar. Dari reaksi asam asetat dan etanol inilah akan menghasilkan etil asetat dengan persamaan reaksinya :
CH3COOH + C2H5OH ⇌ CH3COOC2H5 + H2O Asam asetat Etanol Etil asetat Air Beberapa kegunaan etil asetat :
1. Sebagai bahan pelarut cat dan bahan baku pembuatan plastik 2. Untuk kebutuhan industri farmasi
3. Sebagai bahan baku bagi industri tinta cetak
4. Sebagai bahan baku bagi pabrik parfum, flavor, kosmetik, dan minyak atsiri (McKetta and Cuningham, 1994).
2.7 Uji Kepekaan Terhadap Antimikroba Secara In Vitro
Tujuan pengukuran aktivitas antibakteri adalah untuk menentukan potensi suatu zat yang diduga atau telah memiki aktivitas sebagai antibakteri dalam larutan terhadap suatu bakteri (Jawetz et al., 2001). Pada dasarnya ada tiga cara yang bisa dilakukan untuk uji kepekaan terhadap antimikroba yaitu dengan metode dilusi, metode difusi cakram dan metode bioautografi (Soleha, 2015).
2.7.1 Metode Difusi Cakram
Metode difusi merupakan metode kuantitatif yang digunakan untuk mendeteksi zat penghambat dalam susu di Amerika Serikat dan sering digunakan dalam pengujian antimikroba. Pada perosedur metode difusi cakram kertas saring (diameter sekitar 6 mm) diletakkan pada permukaan agar (media padat) yang telah diinokulasi dengan mikroorganisme uji. Cawan petri di inkubasi setelah itu, zona hambatnnya diukur (Choma & Grzelak, 2010). Menurut Soleha (2015) Minimum Inhibitory Concentration (MIC) merupakan konsentrasi terendah bakteri yang dapat menghambat pertumbuhan bakteri dengan hasil yang dilihat dari pertumbuhan koloni pada agar atau kekeruhan pada pembiakan cair. Pada metode difusi cakram yang diamati adalah diameter daerah hambatan pertumbuhan
mikroba. Hal ini dikarena difusi obat merupakan titik awal pemberian ke daerah difusi, dimana pemberian tersebut sebanding dengan kadar obat yang diberikan.
Metode difusi cakram dilakukan dengan cara menanam mikroba pada media agar padat tertentu kemudian diletakkan kertas samir atau disk yang mengandung obat atau dapat juga dibuat sumuran kemudian di isi obat dan dilihat hasilnya (Jawetz et al, 2012).
2.7.2 Metode Dilusi
Pada metode ini yang diamati adalah ada atau tidaknya pertumbuhan bakteri atau kuman atau jika mungkin, tingkat kesuburan dari pertumbuhan kuman, dengan cara menghitung jumlah koloni, maka dapat ditentukan Kadar Hambat Minimum (KHM) dan Kadar Bunuh Minimum (KBM), (Jawetz et al., 2012).
Menurut (Pratiwi, 2008) metode ini dilakukandengan mencampurkan zat antimikroba dan media agar, yang kemudian sinokulasikan dengan mikroba uji.
Hasil pengamatan yang akan diperoleh berupa tumbuh atau tidaknya mikroba didalam media. Aktivitas zat antimikroba ditentukan dengan melihat koonsentrasi hambat minimum (KHM) yang merupakan konsentrasi terkecil dari zat antimikkroba uji.
Metode dilusi dibedakan menjadi dua yaitu dilusi cair dan dilusi padat.
1) Metode dilusi cair
Metode ini mengukur KHM (Kadar Hambat Minimum) dan KBM (Kadar Bakterisidal Minimum). Cara yang dilakukan adalah dengan membuat seri pengenceran agen antimikroba pada medium cair yang ditambahkan dengan mikroba uji (Pratiwi, 2008).
2) Metode dilusi padat
Metode ini serupa dengan metode dilusi cair namun menggunakan media padat (solid). Keuntungan metode ini adalah satu konsentrasi agen antimikroba yang diuji dapat digunakan untuk menguji beberapa mikroba uji (Pratiwi, 2008).
2.7.3 Metode Bioautografi
Metode bioautografi adalah metode spesifik untuk mendeteksi bercak pada kromatogram hasil Kromatografi Lapis Tipis (KLT) dan kromatografi kertas yang mempunyai aktivitas antibakteri, antifungi, antibiotik dan antiviral (Djie, 2003).
Prosedur metode bioautografi mirip dengan yng digunakan dalam metode difusi
agar. Perbedaannya adalah senyawa uji berdifusi dari kertas kromatografi ke media agar yang diinokulasi (Choma, 2010). Metode ini merupakan alternatif untuk deteksi zat aktif, mencari antibakteri atau anti kapang baru, kontrol kualitas antimikroba, dan mendeteksi golongan senyawa (Kusumaningtyas, 2008). Ada 3 macam metode bioautografi, yaitu:
2.7.3.1 Bioautografi Langsung
Uji bioautografi langsung dilakukan dengan menyemprot lempeng KLT dengan suspensi mikroorganisme atau dengan diletakkan lempeng KLT pada permukaan media agar yang telah ditanami mikroorganisme. Bioautografi langsung lebih sensitif dan memiliki kemampuan untuk mendeteksi antibakteri pada konsentrasi rendah sekalipun (Pratiwi, 2008).
2.7.3.2 Bioautografi Overlay
Uji bioautografi overlay dilakukan dengan menuangkan media agar yang telah dicampur dengan mikroorganisme di atas permukaan lempeng KLT, media ditunggu hingga padat, kemudian diinkubasi. Area hambatan dilihat melalui penyemprotan dengan tetrazolium klorida. Senyawa aktif antimikroba akan terlihat sebagai area jernih dengan latar belakang ungu (Pratiwi, 2008).
2.7.3.3 Bioautografi Kontak
Uji bioautografi kontak dilakukan dengan cara meletakkan lempeng kromatogram hasil elusi senyawa yang akan diuji di atas media padat yang sudah diinokulasi dengan mikroba uji. Daerah jernih yang tidak ditumbuhi mikroba menandakan adanya senyawa antimikroba (Kusumaningtyas, 2008).
Menurut (Dewanjee et al, 2015), bioautografi kontak, antimikroba berdifusi dari plat TLC maju atau kertas ke plat agar yang diinokulasi. Lalu kromatogram ditempatkan menghadap ke bawah pada lapisan agar yang diinokulasi. Hal tersebut dilakukan sampai waktu tertentu supaya lapisan tersebut dapat berdifusi. Setelah itu kromtogram terhapus dan lapisan agar diinkubasi. Waktu inkubasi untuk pertumbuhan biasanya sekitar 16-24 jam tetapi waktu tersebut dapat dipersingkat menjadi 5-6 jam dengan cara dilakukanya penyemprotan dengan menggunakan 2,6- Dichlorophenol-indophenol atau 2,3,5-tetrazoliumchloride. Metode ini biasanya digunakan pada penelitian antibiotik menggunakan mikroorganisme.
2.8 Tinjauan Media Mueller Hinton Agar (MHA)
Media MHA adalah media terbaik untun pemerikasaan uji sensitivitas bakteri menggunnakan metode Kirby-Bauer pada bakteri nonfastidious baik aerob dan aerob fakultatif. Media ini ditemukan oleh Mueller dan Hinton tahun 1941, pada awalnya media Mueller Hinton digunakan untuk mengisolasi bakteri Neisseria sp. Komposisi media MuellerHinton Agar adalah beef extract 2 g, Acid Hydrolysate of Casein 17,5 g, Starch 1,5 g Agar 17 g, dan Aquadest 1 liter.
Media MHA digunakan untuk tes sensitivitas bakteri karena:
1. Semua bakteri dapat tumbuh karena media ini bukan media selektif dan media differensial
2. Mengandung starch (tepung padi) yang berfungsi untuk menyerap racun yang dikeluarkann bakteri, sehingga tidak mengganggu antibiotik.
3. Rendah Sulfonamide, trimethroprin dan tetracycline inhibitors.
4. Mendunkung pertumbuhan bakteri non-fastidious yang pathogen
5. Banyak data penelitian yang telah dikumpulkan tentang uji sensitivitas menggunnakan media ini (Atmojo, 2016).
2.9 Tinjauan Media Eosin Methylene Blue Agar (EMBA)
Media Eosin Methylene Blue Agar (EMBA) adalah medium selektif dan diferensial digunakan untuk mengisolasi coliform fecal. Eosin Y dan metilen blue adalah pewarna indikator pH yang bergabung untuk membentuk endapan ungu gelap pada pH rendah (asam), mereka juga berfungsi untuk menghambat pertumbuhan organisme yang paling gram positif. Sukrosa dan laktosa berfungsi sebagai sumber karbohidrat dapat difermentasi yang mendorong pertumbuhan coliform. Fermentor yang kuat dari laktosa atau sukrosa akan menghasilkan jumlah asam yang cukup untuk membentuk kompleks warna ungu tua. Pertumbuhan organisme ini akan muncul berwarna ungu tua sampai hitam. Escherichia coli, suatu fermentor yang kuat, sering menghasilkan warna koloni hijau metalik.
Fermentor lambat atau lemah akan menghasilkan koloni merah muda mukoid atau berlendir. Biasanya koloni berwarna atau tidak berwarna menunjukkan bahwa organisme fermentor laktosa atau sukrosa tersebut bukan merupakan coliform fecal (Cheeptham, 2012).
2.10 Tinjauan DMSO
DMSO atau Sulfoxide Dimetil merupakan pelarut polar aprotik dengan rumus (CH3)2SO. Ciri-ciri pelarut ini yaitu tidak berwarna dan dapat melarutkan baik senyawa polar maupun non-polar serta dapat larut dalam berbagai pelarut organik maupun air (BPOM, 2011). Menurut (Costa et al 2017), DMSO digunakan sebagai pelarut untuk senyawa farmakologis, terapeutik, eksipien untuk formulasi terapeutik, dan sebagai kontrol untuk menguji produk alami.
Menurut (Wadhwani 2008), dimetil sulfoksida (DMSO) dan etanol sering digunakan sebagai pelarut untuk senyawa antibakteri alami maupun sintetis, untuk menentukan MIC (Minimum Inhibitory Concentration). DMSO dinilai lebih baik selanjutnya ada metanol dan etanol, dalam hal kompatibilitasnya dengan determinasi MIC (Minimum Inhibitory Concentration). Namun DMSO kurang beracun pada 1-3% dibanding metanol, dengan cara lain pada kisaran konsentrasi 4-6%. Rata-rata, pada tingkat 5%, DMSO dan etanol memberikan toksisitas hampir sama. Meskipun DMSO dan etanol umumnya dianggap aman di bawah 3% v / v3.
Konsentrasi pelarut yang lebih rendah, ternyata tidak mempengaruhi pertumbuhan bakteri secara signifikan, masih dapat memberi potensi efek senyawa antibakteri yang diuji.
Sebagai pelarut netral yang juga berperan sebagai surfaktan, DMSO banyak digunakan sebagai pelarut ekstrak pada berbagai penelitian terkait uji antimikrobia ekstrak tanaman. (Onyegbule et al. 2011) telah menggunakan DMSO sebagai pelarut ekstrak etil asetat Napoleoneae imperalis dan sebagai kontrol negatif dalam prosedur uji luas zona hambatnya terhadap Escherichia coli, Bacillus subtilis, dan Pseudomonas aeruginosa.
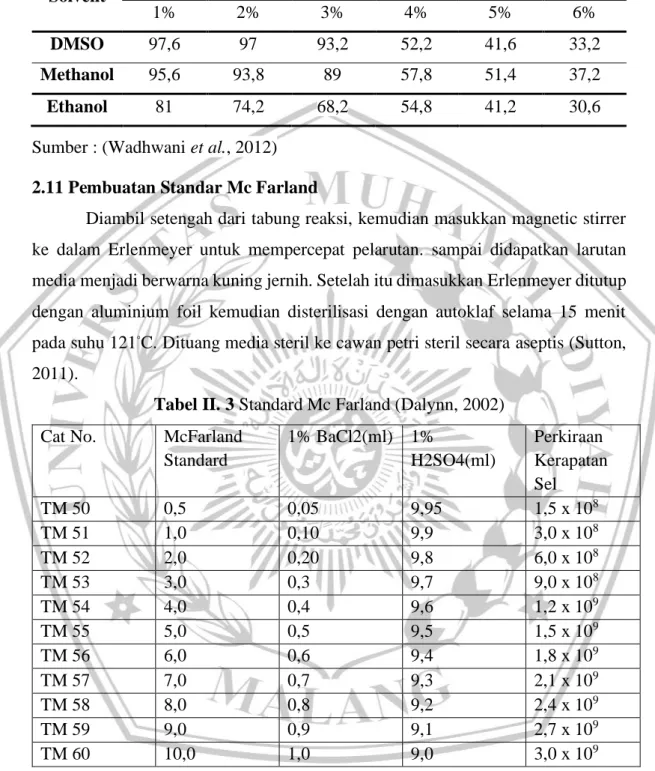
Tabel II. 2 Perbandingan Pelarut dalam Menghambat Pertumbuhan Bakteri
Solvent Average % growth for all organism
1% 2% 3% 4% 5% 6%
DMSO 97,6 97 93,2 52,2 41,6 33,2
Methanol 95,6 93,8 89 57,8 51,4 37,2
Ethanol 81 74,2 68,2 54,8 41,2 30,6
Sumber : (Wadhwani et al., 2012) 2.11 Pembuatan Standar Mc Farland
Diambil setengah dari tabung reaksi, kemudian masukkan magnetic stirrer ke dalam Erlenmeyer untuk mempercepat pelarutan. sampai didapatkan larutan media menjadi berwarna kuning jernih. Setelah itu dimasukkan Erlenmeyer ditutup dengan aluminium foil kemudian disterilisasi dengan autoklaf selama 15 menit pada suhu 121◦C. Dituang media steril ke cawan petri steril secara aseptis (Sutton, 2011).
Tabel II. 3 Standard Mc Farland (Dalynn, 2002) Cat No. McFarland
Standard
1% BaCl2(ml) 1%
H2SO4(ml)
Perkiraan Kerapatan Sel
TM 50 0,5 0,05 9,95 1,5 x 108
TM 51 1,0 0,10 9,9 3,0 x 108
TM 52 2,0 0,20 9,8 6,0 x 108
TM 53 3,0 0,3 9,7 9,0 x 108
TM 54 4,0 0,4 9,6 1,2 x 109
TM 55 5,0 0,5 9,5 1,5 x 109
TM 56 6,0 0,6 9,4 1,8 x 109
TM 57 7,0 0,7 9,3 2,1 x 109
TM 58 8,0 0,8 9,2 2,4 x 109
TM 59 9,0 0,9 9,1 2,7 x 109
TM 60 10,0 1,0 9,0 3,0 x 109