i
UJI TOKSISITAS INFUSA DAUN SIRSAK (Annona muricata L.) TERHADAP KADAR KREATININ DAN GAMBARAN HISTOLOGIS GINJAL PADA
TIKUS SECARA SUBKRONIS
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Christiana Lambang Kristanti
NIM : 098114041
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
iv
Halaman Persembahan
TUHAN MEMILIKI RANCANGAN TERINDAH DALAM SETIAP LANGKAH HIDUPKU DAN AKU PERCAYA ITU
“Kalau kamu punya keyakinan, keinginan, cita-cita, mimpi, dan harapan, kamu taruh
„disini‟ (sambil meletakkan telunjuk di depan kening). Kamu taruh „disini‟... jangan menempel di kening...
Biarkan dia...
menggantung... mengambang... 5 cm...
di depan kening kamu...
Jadi, dia tidak akan pernah lepas dari mata kamu. Kamu bawa dia setiap hari, kamu lihat setiap hari, dan percaya bahwa kamu bisa. Dan... sehabis itu yang kamu perlu... cuma... Cuma kaki yang akan berjalan lebih jauh dari biasanya, mata yang
akan menatap lebih lama dari biasanya, leher yang akan lebih sering melihat ke atas, lapisan tekad yang seribu kali lebih keras dari baja, dan hati yang akan
bekerja lebih keras dari biasanya, serta mulut yang akan selalu berdoa...”
(Donny Dhirgantoro – 5 cm)
“ E U G G I ...
...BONDO SING ORA ISO ENTEK - E I I G I W ”
(Bapak)
Aku persembahkan karya ku ini untuk:
Tuhan Yesus Kristus dan Bunda Maria,
Papa dan mama ku tercinta beserta kakak
Almamaterku tercinta Universitas Sanata Dharma
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
v
vi
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma:
Nama : Christiana Lambang Kristanti Nomor mahasiswa : 098114041
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
UJI TOKSISITAS INFUSA DAUN SIRSAK (Annona muricata L.) TERHADAP KADAR KREATININ DAN GAMBARAN HISTOLOGIS GINJAL PADA TIKUS SECARA SUBKRONIS
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama saya tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini saya buat dengan sebenarnya.
Dibuat di Yogyakarta
Pada tanggal: 5 Februari 2013 Yang menyatakan
(Christiana Lambang Kristanti)
vii PRAKATA
Puji syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas segala
perlindungan dan berkat yang telah diberikan sehingga skripsi berjudul “Uji
Toksisitas Infusa Daun Sirsak (Annona muricata L.) Terhadap Kadar Kreatinin
dan Gambaran Histologis Ginjal pada Tikus secara Subkronis” yang disusun
untuk memenuhi persyaratan memperoleh gelar Sarjana Strata Satu Program Studi
Farmasi (S.Farm.) dapat dikerjakan dengan baik dan lancar.
Penulis menyadari bahwa penulisan skripsi ini tidak terlepas dari berbagai
pihak. Kesempatan ini penulis pergunakan untuk mengungkapkan rasa terima kasih
kepada:
1. Dekan Fakultas Farmasi Universitas Sanata Dharma yang telah mengijinkan
penulis menjalankan pembelajaran selama masa studi.
2. Ibu Phebe Hendra, M.Si., Ph.D., Apt. selaku dosen pembimbing skripsi yang
telah membimbing, mendampingi dan memberikan saran selama pembuatan
skripsi ini.
3. Ibu Rini Dwiastuti, S.Farm., Apt., M.Sc., selaku Dosen Pembimbing Akademik
penulis selama masa studi di Universitas Sanata Dharma.
4. Bapak Ipang Djunarko, M.Sc., Apt., selaku dosen penguji yang telah
memberikan kritik dan saran selama penyusunan skripsi.
5. Bapak Yohanes Dwiatmaka, M.Si., selaku dosen penguji yang telah memberikan
viii
6. Pak Heru, Pak Parjiman, Mas Kayat, Dokter Ari, Pak Ratijo, dan Pak Wagiran
selaku Staff Laboratorium Fakultas Farmasi Universitas Sanata Dharma yang
telah membantu penulis dalam pengerjaan penelitian di laboratorium.
7. Segenap dosen dan karyawan atas ilmu yang diberikan.
8. Keluargaku tercinta, Bapak Heribertus Sedyo Budi Utomo, Mama Elisabeth
Sulastri, Mbak Lucia Citra Puspita dan Mas Christian Benardo Kandou yang
selalu memberikan doa, kasih sayang, dan semangat kepada penulis.
9. Keluarga besar Hardjo Dikromo dan Yoso Sentono yang telah mendukung dan
memberikan doa kepada penulis.
10. Wandul, Berthul, Herul, Raras, Yansen, dan Danny sebagai sahabat yang selalu
memberikan semangat, kebersamaan, dan doa kepada penulis selama ini.
11. Raras, Suster Imelda, Meita, Dita, Niken, dan Galuh sebagai rekan kerja yang
telah menyediakan waktu untuk memberikan saran dan kritik baik dalam hal
penyusunan skripsi maupun hal-hal lainnya serta bekerja bersama di
laboratorium.
12. Dhimas Bayu Kinasih yang selalu mendukung penulis dalam suka dan duka
dalam pembuatan skripsi ini.
13. Teman-teman FKK dan FST 2009 yang selalu mengisi hari-hari dan memberikan
semangat penulis dalam pembuatan skripsi ini.
14. Teman-teman penghuni kost „Wisma Goreti‟ yang selalu memberikan dukungan
kepada penulis dalam pembuatan skripsi ini.
ix
15. Seluruh teman, baik di Fakultas Farmasi maupun teman-teman lain atas
dukungannya.
16. Semua pihak yang tidak dapat penulis sebutkan satu per satu sehingga penulis
dapat menyelesaikan tugas akhir ini dengan baik.
Penulis menyadari bahwa tugas akhir ini belum sempurna dan masih banyak
kekurangan sehingga penulis berharap kritik dan saran dari semua pihak. Akhir kata,
penulis berharap semoga tugas akhir ini dapat bermanfaat bagi semua pihak terutama
di bidang ilmu Farmasi.
x
DAFTAR ISI
halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN PENULIS ... v
LEMBAR PERNYATAN PERSETUJUAN PUBLIKASI KARYA ... vi
xi
2. Faktor yang mempengaruhi kadar kreatinin darah ... 27
3. Metode pemeriksaan kreatinin ... 28
G. Kerusakan Ginjal ... 29
1. Penyakit yang mengenai glomerulus... 31
2. Penyakit yang mengenai tubulus dan interstisium ... 31
3. Penyakit yang mengenai pembuluh darah ... 35
H. Uji Toksisitas Subkronis ... 35
I. Uji Reversibilitas ... 39
J. Keterangan Empiris... 39
BAB III METODE PENELITIAN ... 40
A. Jenis dan Rancangan Penelitian ... 40
B. Variabel dan Definisi Operasional ... 40
1. Variabel utama ... 40
2. Variabel pengacau ... 40
3. Definisi operasional... 40
C. Bahan dan Alat Penelitian ... 42
1. Bahan penelitian ... 42
2. Alat penelitian ... 43
xii
1. Determinasi tanaman sirsak ... 43
2. Pengumpuan bahan ... 44
3. Pembuatan simplisia daun sirsak ... 44
4. Penetapan kadar air dalam daun sirsak... 44
5. Pembuatan infusa daun sirsak ... 45
6. Penetapan dosis infusa daun sirsak ... 45
7. Uji toksisitas ... 46
a. Penyiapan hewan uji... 46
b. Pengelompokan hewan uji ... 46
c. Prosedur pelaksanaan ... 47
8. Pembuatan preparat histologis ... 48
9. Pengamatan efek toksik ... 48
a. Pemeriksaan kreatinin ... 48
b. Pemeriksaan histologis ginjal ... 48
c. Uji reversibilitas ... 48
d. Pengamatan berat badan, asupan makan dan minum tikus . 49 E. Analisis dan Evaluasi Hasil ... 49
BAB IV HASIL DAN PEMBAHASAN ... 51
A. Determinasi Tanaman Sirsak ... 51
B. Pembuatan Simplisia ... 53
C. Penetapan Kadar Air ... 53
D. Penetapan Dosis Infusa ... 53
E. Uji Toksisitas Subkronis ... 54
1. Pemeriksaan kadar kreatinin dalam darah ... 55
2. Pemeriksaan histologis ginjal ... 63
xiii
BAB V KESIMPULAN DAN SARAN... 81
A. Kesimpulan ... 81
B. Saran ... . 81
DAFTAR PUSTAKA ... 82
LAMPIRAN ... 87
xiv
DAFTAR TABEL
halaman
Tabel I. Kadar kreatinin darah tikus jantan pada awal sebelum
pemberian dan setelah pemberian infusa daun sirsak
selama 30 hari secara oral ... 57
Tabel II. Kadar kreatinin darah tikus betina pada awal sebelum
pemberian dan setelah pemberian infusa daun sirsak
selama 30 hari secara oral ... 59
Tabel III. Uji Scheffe kreatinin dalam darah pada tikus jantan pada
hari ke-31 ... 60
Tabel IV. Uji Scheffe kreatinin dalam darah pada tikus betina pada
hari ke-31 ... 62
Tabel V. Hasil pemeriksaan histologis ginjal pada tikus jantan ... 64
Tabel VI. Hasil pemeriksaan histologis ginjal pada tikus jantan ... 67
Tabel VII. Purata berat badan ± SEM tikus jantan akibat pemberian
infusa daun sirsak ... 76
Tabel VIII. Purata berat badan ± SEM tikus betina akibat pemberian
infusa daun sirsak ... 76
xv
DAFTAR GAMBAR
halaman
Gambar 1. Struktur ginjal ... 15
Gambar 2. Struktur nefron ... 16
Gambar 3. Struktur glomerulus dan kapiler glomerular ... 17
Gambar 4. Korpuskular ginjal secara mikroskopik ... 18
Gambar 5. Mikrograf elektron pembesaran lemah glomerulus ginjal .. 19
Gambar 6. Tubulus kontortus proksimal dan tubulus kontortus distal secara mikroskopik ... 20
Gambar 7. Duktus koligens secara mikroskopik ... 20
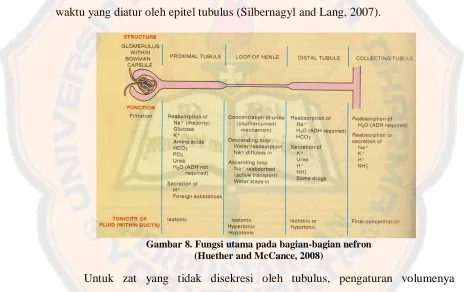
Gambar 8. Fungsi utama pada bagian-bagian nefron ... 22
Gambar 9. Mekanisme pembentukan urin melalui proses filtrasi, reabsorpsi, dan sekresi ... 26
Gambar 10. Gambaran mikroskopik ginjal normal... 30
Gambar 11. Mekanisme cedera tubulointerstisium kronik pada glomerulonefritis ... 33
Gambar 12. Gambaran mikroskopik interstitial nephritis kronik ... 34
Gambar 13. Diagram batang rata-rata kadar kreatinin dalam darah tikus jantan ... 61
Gambar 14. Diagram batang rata-rata kadar kreatinin dalam darah tikus betina ... 63
Gambar 15. Fotomikroskopik ginjal tikus jantan kontrol akuades yang normal atau tidak adanya kerusakan ... 65
xvi
Gambar 17. Fotomikroskopik ginjal tikus betina kelompok perlakuan
infusa daun sirsak 108 mg/kgBB yang normal atau tidak
adanya kerusakan ... 68
Gambar 18. Fotomikroskopik ginjal tikus betina kelompok kontrol
akuades yang mengalami perubahan gambaran histologis
secara struktural yaitu infiltrasi limfosit di daerah
interstisium ... 68
Gambar 19. Fotomikroskopik ginjal tikus jantan hasil uji
reversibilitas kelompok perlakuan infusa daun sirsak 301
mg/kgBB yang normal atau tidak adanya kerusakan ... 73
Gambar 20. Fotomikroskopik ginjal tikus betina hasil uji
reversibilitas kelompok kontrol akuades dan perlakuan
infusa daun sirsak 108 mg/kgBB yang mengalami
perubahan gambaran histologis secara struktural yaitu
infiltrasi limfosit di daerah interstisium ... 73
Gambar 21. Grafik perubahan berat badan tikus jantan selama
pemberian infusa daun sirsak pada hari ke-0 sampai ke-28 77
Gambar 22. Grafik perubahan berat badan tikus betina selama
pemberian infusa daun sirsak pada hari ke-0 sampai ke-28 77
Gambar 23. Grafik asupan makan tikus jantan selama pemberian
infusa daun sirsak pada hari ke-0 sampai ke-28 ... 78
Gambar 24. Grafik asupan makan tikus betina selama pemberian
infusa daun sirsak pada hari ke-0 sampai ke-28 ... 79
Gambar 25. Grafik asupan minum tikus jantan selama pemberian
infusa daun sirsak pada hari ke-0 sampai ke-28 ... 80
xvii
Gambar 26. Grafik asupan minum tikus betina selama pemberian
xviii
DAFTAR LAMPIRAN
halaman
Lampiran 1. Foto tanaman sirsak dan daun sirsak ... 88
Lampiran 2. Hasil determinasi tanaman sirsak ... 88
Lampiran 3. Foto infusa daun sirsak ... 88
Lampiran 4. Surat pengesahan determinasi ... 89
Lampiran 5. Surat Ethics Committee Approval ... 90
Lampiran 6. Perhitungan berat halus serbuk dan rendemen ... 91
Lampiran 7. Perhitungan kadar air daun sirsak... 91
Lampiran 8. Perhitungan dosis infusa daun sirsak ... 91
Lampiran 9. Perhitungan konversi dosis infusa daun sirsak dari tikus ke manusia ... 92
Lampiran 10. Analisis statistik kadar kreatinin tikus jantan sebelum pemberian infusa daun sirsak ... 93
Lampiran 11. Data statistik kadar kreatinin tikus betina sebelum pemberian infusa daun sirsak ... 95
Lampiran 12. Data statistik kadar kreatinin tikus jantan setelah pemberian infusa daun sirsak ... 98
Lampiran 13. Data statistik kadar kreatinin tikus betina setelah pemberian infusa daun sirsak ... 100
Lampiran 14. Data statistik Paired T test kreatinin pre dan post pada tikus jantan ... 103
Lampiran 15. Data statistik Paired T test kreatinin pre dan post pada tikus betina ... 104
Lampiran 16. Analisis statistik berat badan tikus jantan ... 105
Lampiran 17. Analisis statistik berat badan tikus betina ... 107
Lampiran 18. Data rata-rata asupan makan tikus jantan selama 30 hari ... 111
xix
Lampiran 19. Data rata-rata asupan makan tikus betina selama
30 hari ... 112
Lampiran 20. Data rata-rata asupan minum tikus jantan selama
30 hari ... 113
Lampiran 21. Data rata-rata asupan minum tikus betina selama
30 hari ... 114
Lampiran 22. Surat pengesahan hasil histologis ... 115
Lampiran 23. Gambar fotomikroskopik ginjal tikus jantan setelah
pemberian infusa daun sirsak selama 30 hari
(perbesaran 100 dan 400) ... 117
Lampiran 24. Gambar fotomikroskopik ginjal tikus betina setelah
pemberian infusa daun sirsak selama 30 hari
(perbesaran 100 dan 400) ... 119
Lampiran 25. Gambar fotomikroskopik ginjal tikus jantan selama
uji reversibilitas (perbesaran 100 dan 400) ... 120
Lampiran 26. Gambar fotomikroskopik ginjal tikus betina selama
xx INTISARI
Bukti empiris penggunaan daun sirsak sudah banyak dilaporkan, namun bukti ilmiah tentang ketoksikan penggunaannya belum banyak dilaporkan khususnya risiko penggunaan jangka panjang. Penelitian ini bertujuan untuk mengetahui wujud efek toksik infusa daun sirsak terhadap kadar kreatinin dan histologis ginjal secara subkronis.
Penelitian menggunakan metode eksperimental murni dengan rancangan penelitian acak lengkap pola searah. Subjek uji berupa tikus putih galur Sprague Da wley, umur 2-3 bulan, berat badan 150-250 gram. Lima puluh ekor tikus dibagi 5 kelompok (1 kontrol, 4 perlakuan), setiap kelompok terdiri 5 jantan dan 5 betina. Dosis infusa daun sirsak yaitu 108; 180; 301; 503 mg/kgBB dan kontrol aquadest 8333 mg/kgBB, selama 30 hari. Dilakukan pemeriksaan kreatinin (hari ke-0 dan 31), histologis ginjal (hari ke-31), uji reversibilitas selama 14 hari, serta pengamatan berat badan, asupan makan dan minum setiap harinya. Analisis menggunakan Anova pola satu arah dan dilanjutkan uji Scheffe.
Hasil menunjukkan bahwa keempat dosis infusa daun sirsak menghasilkan nilai berbeda tidak bermakna antara kadar kreatinin sebelum dan sesudah perlakuan, gambaran ginjal yang relatif normal, dan tidak terjadi kerusakan ginjal selama uji reversibilitas. Disimpulkan bahwa pemberian infusa daun sirsak tidak meningkatan kadar kreatinin darah dan efek toksik pada ginjal, tidak ada hubungan kekerabatan antara dosis dengan spektrum efek toksik.
Kata kunci: infusa, daun sirsak, kreatinin, ginjal, toksisitas, subkronis.
xxi ABSTRACT
Empirical evidence using soursop leaves are widely reported, but the scientific facts as the result for its toxicity has not been widely reported particularly the risk of long-term use. This study is aimed to determine the toxic effects infusa form of soursop leaf to creatinine levels and renal histology with subchronically.
This study purely using randomized experimental design, complete with its unidirectional pattern. The test subjects for these studies are strained Sprague Dawley rats, aged 2-3 months, and 150-250 grams for its weight. Fifty rats were divided into 5 groups (1 control group and 4 treatment groups), each group consisted of 5 male and 5 female. For the dose infusa of soursop leaves are 108; 180; 301; 503 mg/kg and distilled water control 8333 mg/kg, for 30 days. The rats examination for its creatinine (day 0 and 31), renal histology (day 31), reversibility testing around 14 days, and the observations its of body weight, food intake and water for each day. Analysis using of the one-way Anova and Scheffe test.
The results showed that all four doses infusa soursop leaf yield values do not differ significantly among creatinine levels before and after treatment, the kidney picture is relatively normal, and not occur kidney damage during reversibility testing. It was concluded that the administration infusa soursop leaves no increase of blood creatinine levels and toxic effects on the kidneys, there is no relationship among these dose spectrum of toxic effects.
1
BAB I
PENGANTAR
A. Latar Belakang
Berdasarkan Peraturan Menteri Kesehatan Republik Indonesia Nomor
003/Menkes/Per/I/2010 Pasal 1, obat tradisional adalah bahan atau ramuan bahan
yang berupa bahan tumbuhan, bahan hewan, bahan mineral, sediaan sarian (galenik),
atau campuran dari bahan tersebut yang secara turun temurun telah digunakan untuk
pengobatan, dan dapat diterapkan sesuai dengan norma yang berlaku di masyarakat
(Menteri Kesehatan RI, 2010).
Atas dasar pengetahuan tradisional masyarakat secara turun-temurun dan
didukung oleh berbagai penelitian tentang khasiat tanaman sirsak, kini pengobat
tradisional di Indonesia bahkan sebagian dokter telah meresepkan tanaman sirsak
untuk mengatasi beberapa penyakit (Mardiana dan Ratnasari, 2011). Bagian dari
tanaman sirsak yang paling sering digunakan sebagai obat tradisional adalah daunnya.
Daun sirsak telah digunakan oleh sebagian masyarakat sebagai obat
tradisional untuk mengobati berbagai penyakit seperti abses, asma, batuk, diabetes,
diuretik, demam, influensa, hipertensi, gangguan pencernaan, infeksi, cacingan,
gangguan hati, malaria, reumatik, kurap, kejang, dan terutama penyakit kanker
(Mardiana dan Ratnasari, 2011).
Penelitian ilmiah daun sirsak yang telah dilaporkan yaitu estrak air daun
sirsak mempunyai potensi ketoksikan akut pada mencit dengan letal dosis tengah
semu lebih dari 5000 mg/kgBB secara oral. Penelitian ini juga menunjukkan
pemberian ekstrak air daun sirsak dosis 100, 1000, dan 2500 mg/kgBB selama 14 hari
pada tikus menyebabkan hipoglikemik pada dosis 1000 mg/kgBB dan hipolipidemik
pada dosis 100 mg/kgBB, sedangkan pada dosis 2500 mg/kgBB dapat menyebabkan
gagal ginjal dan efek toksik pada fungsi rahim (Arthur, Woode, Terlabi, and Larbie,
2011). Penelitian ekstrak air daun sirsak ini belum dilakukan uji reversibilitas.
Penelitian ilmiah lainnya antara lain ekstrak air daun sirsak dosis 50
mg/kgBB dan 400 mg/kgBB memiliki potensi menurunkan bilirubin sehingga efektif
untuk penyakit hiperbilirubinemia atau penyakit kuning (Arthur, Woode, Terlabi, and
Larbie, 2012); ekstrak air daun sirsak juga memberikan efek hipoglikemik dan efek
antioksidan dalam melindung sel β pankreas pada tikus jantan dan betina terinduksi
streptozotocin dengan dosis 75 mg/kgBB (Adewole and Martins, 2006).
Ginjal merupakan organ ekskresi yang sangat penting dan vital. Ginjal
melakukan fungsi vital sebagai pengatur komposisi dan volume kimia darah dengan
mengekskresikan solut dan air secara selektif yang dikontrol oleh filtrasi glomerulus,
reabsorpsi, dan sekresi tubulus (Price and Wilson, 1985). Sebagai bagian dari sistem
urin, ginjal berfungsi menyaring kotoran dari darah dan membuangnya bersama
dengan air dalam bentuk urin.
Sebagian besar produk sisa buangan yang dikeluarkan melalui urin
diantaranya kreatinin. Kreatinin merupakan produk akhir dari metabolisme kreatin
otot dan kreatin fosfat (protein), disintese dalam hati, ditemukan dalam otot rangka
3
diekskresikan dalam urine (Lu, 1995). Kreatinin adalah suatu metabolit kreatin dan
diekskresi seluruhnya dalam urin melalui filtrasi glomerulus. Meningkatnya kadar
kreatinin dalam darah merupakan indikasi rusaknya fungsi ginjal (Lu, 1995).
Daun sirsak memiliki khasiat sebagai antikanker yang pada umumnya
digunakan masyarakat dalam jangka panjang yaitu secara rutin selama 1 bulan hingga
hitungan tahun. Bukti empiris tentang penggunaan daun sirsak sudah banyak
dilaporkan, namun bukti ilmiah tentang ketoksikan penggunaannya belum banyak
dilaporkan khususnya risiko penggunaan pada jangka panjang. Sejauh ini pula belum
ditemukan adanya penelitian mengenai toksilogi dari daun sirsak yang secara khusus
bersifat khas memberikan efek terhadap ginjal, melainkan memberikan efek dalam
spektrum yang luas.
Maka dari itu, perlu dilakukan penelitian mengenai pengaruh daun sirsak
terhadap kadar kreatinin dan gambaran histologis ginjal pada tikus sebagai hewan uji
secara subkronis selama 30 hari dan dilakukan uji reversibilitas pada hari ke-15
setelah 30 hari pemberian infusa daun sirsak. Penelitian uji subkronis yang akan
dilakukan ini merupakan penelitian payung, namun dalam hal ini akan difokuskan
pada kadar kreatinin dan gambaran histologis ginjal tikus.
1. Permasalahan
Berdasarkan latar belakang yang telah dikemukakan sebelumnya, timbul
beberapa masalah yang akan diteliti sebagai berikut:
a. seberapa besar spektrum efek toksik sediaan uji terhadap kadar kreatinin
dalam darah dan organ ginjal yang dilihat dari histologis ginjal?
b. apakah terdapat hubungan kekerabatan antara dosis infusa daun sirsak
dengan efek toksisitas subkronis pada kadar kreatinin dan organ ginjal?
c. apakah terjadi keterbalikan (reversibilitas) spektrum efek toksik?
2. Keaslian penelitian
Penelitian yang telah dipublikasikan adalah sebagai berikut:
1. Toksisitas Akut dan Subkronis Estrak Air Annona muricata Linn. terhadap
Hewan (Arthur, et al., 2011).
Ekstrak air daun sirsak mempunyai potensi ketoksikan akut pada mencit
dengan LD50 diperkirakan lebih dari 5000 mg/kgBB (oral). Uji toksisitas
subkronis selama 14 hari pada tikus menyebabkan hipoglikemik pada dosis
1000 mg/kgBB dan hipolipidemik pada dosis 100 mg/kgBB, sedangkan pada
dosis 2500 mg/kgBB dapat menyebabkan gagal ginjal dan efek toksik pada
fungsi rahim.
2. Perubahan Morfologi dan Efek Hipoglikemik dari Ekstrak Daun Annona
muricata Linn. (Annonaceae) pada sel β pankreas dari Induksi
Streptozotocin-Tikus Diabetes (Adewole and Martins, 2006).
Ekstrak air A. Muricata memberikan efek hipoglikemik dan efek antioksidan
dalam melindung sel β pankreas, sehingga disimpulkan bahwa daun sirsak
5
3. Perlindungan Efek Ekstrak Air Daun Annona muricata Linn. (Annonaceae)
pada Profil Lipid Serum dan Stres oksidatif dalam Hepatosit dari Pengobatan
Streptozotocin Tikus Diabetes (Adewole and Ojowole, 2009).
Pengobatan streptozotocin (STZ) berhubungan dengan stres oksidatif pada
jaringan hati dan penelitian ini menunjukkan bahwa ekstrak air daun Annona
muricata memiliki aktivitas antioksidan yang mampu menghambat dan/atau
mencegah kerusakan oksidatif hati yang dihasilkan dari pengobatan STZ.
4. Antikanker Payudara dari Pengaruh Ekstrak Daun Annona muricata pada Sel
T47D (Rachmani, Suhesti, Widiastuti, and Aditiyono, 2012).
Hasil penelitian menunjukkan bahwa ekstrak etanol dari daun sirsak
memiliki aktivitas sitotoksik dengan nilai IC50 yaitu 17,149 mg/mL. Hasil
dari empat fraksi yang diperoleh dengan cara fraksinasi di mana fraksi F3
adalah fraksi yang memiliki aktivitas sitotoksik terbaik dengan nilai IC50
30,112 mg/mL. Hasil uji apoptosis menunjukkan bahwa fraksi F3 mampu
menginduksi apoptosis sel.
5. Sirsak (Annona muricata L.): Hematologi Darah dan Biokimia Serum pada
Tikus Sprague Da wley (Syahida, Maskat, Suri, Mamot, and Hadijah, 2012).
Uji in vivo yang dilakukan selama 28 hari pada dosis bertingkat
menunjukkan hasil bahwa ekstrak daging buah Annona muricata L. tidak
menimbulkan efek negatif terhadap hematologi darah meskipun tercatat
adanya peningkatan signifikan secara statistik (p < 0,05) pada tingkat
platelet. Hasil dari uji biokimia serum menunjukkan bahwa ekstrak ini tidak
menimbulkan gagal hati dan ginjal. Total a ntioxidant status (TAS)
meningkat secara signifikan sebagai dosis meningkat. Namun peningkatan
itu masih dalam batas normal.
Perbedaan dengan penelitian ini adalah penelitian ini menguji ekstrak daging
buah sirsak, sedangkan penelitian yang akan dilakukan ini menggunakan
bahan uji berupa infusa daun sirsak.
Berdasarkan hasil penelusuran pustaka yang telah dilakukan, penelitian uji
toksisitas infusa daun sirsak (Annona muricata L.) terhadap kadar kreatinin dan
gambaran histologis ginjal pada tikus secara subkronis selama 30 hari belum
pernah dilakukan.
3. Manfaat penelitian
a. Manfaat teoritis. Penelitian ini diharapkan dapat bermanfaat bagi
pengembangan ilmu kefarmasian, ilmu kedokteran, dan pengetahuan tentang
obat-obat tradisional, khususnya daun tanaman sirsak.
b. Manfaat praktis. Penelitian ini juga diharapkan dapat memberikan informasi
kepada masyarakat tentang wujud efek toksik subkronis pada kadar kreatinin
7
B.Tujuan Penelitian
1. Tujuan umum
Penelitian ini bertujuan untuk mengetahui wujud efek toksik subkronis
terhadap kadar kreatinin dan gambaran histologis ginjal akibat pemakaian infusa
daun sirsak.
2. Tujuan khusus
Tujuan khusus penelitian ini ialah untuk:
a. mengungkapkan spektrum efek toksik sediaan uji terhadap kadar kreatinin
dalam darah dan organ ginjal yang dinilai dari histologis ginjal.
b. mengungkapkan kekerabatan antara dosis dengan spektrum efek toksik.
mengevaluasi keterbalikan (reversibilitas) spektrum efek toksik yang terjadi.
8
BAB II
PENELAAHAN PUSTAKA
A. Obat Tradisional
Bangsa Indonesia telah lama mengenal dan menggunakan tanaman
berkhasiat obat sebagai salah satu upaya dalam menanggulangi masalah kesehatan.
Pengetahuan tentang tanaman berkhasiat obat berdasar pada pengalaman dan
ketrampilan yang secara turun temurun telah diwariskan dari satu generasi ke
generasi berikutnya (Oktora, 2006).
Berdasarkan Peraturan Menteri Kesehatan Republik Indonesia Nomor
003/Menkes/Per/I/2010 Pasal 1, obat tradisional adalah bahan atau ramuan bahan
yang berupa bahan tumbuhan, bahan hewan, bahan mineral, sediaan sarian (galenik),
atau campuran dari bahan tersebut yang secara turun temurun telah digunakan untuk
pengobatan, dan dapat diterapkan sesuai dengan norma yang berlaku di masyarakat
(Menteri Kesehatan RI, 2010).
WHO merekomendasi penggunaan obat tradisional dalam pemeliharaan
kesehatanmasyarakat, pencegahan danpengobatan penyakit, terutamauntuk penyakit
kronis, penyakit degeneratif dan kanker. WHO juga mendukung upaya-upaya dalam
peningkatan keamanan, khasiat, dan kualitasdari obat tradisional (WHO, 2008).
Penggunaan obat tradisional secara umum dinilai lebih aman dari pada
penggunaan obat modern. Hal ini disebabkan karena obat tradisional memiliki efek
9
tradisional relatif kecil jika digunakan secara tepat antara lain kebenaran bahan,
ketepatan dosis, ketepatan waktu penggunaan, ketepatan cara penggunaan, ketepatan
telaah informasi, tanpa penyalahgunaan, dan ketepatan pemilihan obat untuk indikasi
tertentu (Oktora, 2006).
B. Tanaman Sirsak
1. Sistematika
Sistematika dari tanaman sirsak menurut Tjitrosoepomo (1989) adalah sebagai
berikut:
Kingdom : Plantae
Divisi : Magnoliophyta
Sub divisi : Spermatophyta
Kelas : Dicotyledonae
Anak kelas : Dialypetalae
Ordo : Polycarpicae
Famili : Annonaceae
Genus : Annona
Spesies : Annona muricata L.
2. Habitat
Sirsak dapat tumbuh pada semua jenis tanah dengan derajat keasaman (pH)
antara 5-7. Jadi, tanah yang sesuai adalah tanah yang agak asam sampai agak
alkalis. Di Indonesia tanaman sirsak menyebar dan tumbuh baik mulai dari daratan
rendah beriklim kering sampai daerah basah dengan ketinggian 1000 m dari
permukaan laut. Suhu udara yang sesuai untuk tanaman sirsak adalah 22-320C.
Curah hujan yang dibutuhkan tanaman sirsak antara 1500-3000 mm/tahun
(Sunarjono, 2005).
3. Morfologi daun sirsak
Dilihat secara makroskopik, daun sirsak termasuk daun tunggal dan berwarna
kehijauan sampai hijau kecoklatan. Helaian daun seperti kulit, berbentuk bundar
panjang, lanset atau bundar telur terbalik. Helaian daun mempunyai panjang 6 cm
sampai 18 cm dan lebar 2 cm sampai 6 cm. Ujung daun meruncing pendek,
pangkal daun runcing, dan tepi rata. Panjang tangkai daun yaitu lebih kurang 0,7
cm. Permukaan licin agak mengkilat, tulang daun menyirip dan ibu tulang daun
menonjol pada permukaan bawah. Daun berbau agak keras dan rasa agak kelat
(Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1995 d).
4. Kandungan kimia
Daun sirsak mengandung saponin, tanin terkondensasi, glikosida dan
flavonoid, serta mengandung adanya zat kelompok acetogenins (Arthur, et al.,
2011). Acetogenins dari Annona merupakan kelas penting dari produk alami yang
memiliki berbagai macam sifat biologis seperti sitotoksik, antitumoral, antiparasit,
insektisida, dan aktivitas imunosupresif (Gleye, Laurens, Hocquemiller, Figadere,
and Cave, 1996).
Acetogenin bekerja menghambat mitochondrial complex I pada rantai
11
mitokondria normal maka pertumbuhan sel kanker dapat terkendali. Mekanisme
kerjanya acetogenin masuk ke dalam sel kanker dan menempel pada inner
membrane of mitochondria, lalu merusak produksi ATP di dalam mitokondria.
Akibat kekurangan ATP sebagai sumber energi, akhirnya sel kanker menjadi
lemah dan mati (Villo, 2008). Salah satu senyawa acetogenin dari daun sirsak
adalah annonacin, di mana senyawa tersebut mampu menyebabkan neurotoksisitas
(Potts, Luzzio, Smith, Hetman, Champy, and Litfan, 2011).
Menurut penelitian analisis fitokimia oleh Prachi (2010), ekstrak air daun
sirsak mengandung metabolit sekunder seperti karbohidrat, steroid, tanin, dan
glikosida kardiak. Daun sirsak juga mengandung alkaloid dan minyak atisiri
(Winarni, 2002).
5. Khasiat dan kegunaan
Daun sirsak secara tradisional dapat dimanfaatkan untuk mengobati abses,
arthritis, asthenia, asma, bronkitis, kolik, batuk, diabetes, diuretik, disentri,
demam, gangguan empedu, influensa, jantung, hipertensi, gangguan pencernaan,
infeksi, cacingan, gangguan hati, malaria, reumatik, kurap, kejang, tumor, dan
borok. Pada tahun 1976, The National Cancer Institute meneliti khasiat sirsak
sebagai antitumor dan antikanker. Hasil penelitian tersebut menunjukkan bahwa
daun sirsak mampu menyerang dan menghancurkan sel-sel kanker (Mardiana dan
Ratnasari, 2011).
Penelitian yang dilakukan Zeng, Wu, Oberlies, McLaughlin, dan
Sastrodihadjo (1996), menyatakan bahwa cis-a nnonacin, salah satu senyawa
acetogenins dalam daun sirsak bersifat selektif mematikan sel-sel kanker usus
besar dan memiliki kekuatan 10.000 kali lebih besar dibandingkan dengan
adriamycin (obat kemoterapi). Hasil penelitian Wu, Gu, Zeng, Zhao, Zhang, dan
McLaughlin (1995) menunjukkan senyawa annonaceous acetogenins selektif
sebagai agen sitotoksik terhadap sel tumor paru-paru pada manusia.
Menurut hasil penelitian di Brazil pada tahun 2010 menyebutkan bahwa
ekstrak etanol daun sirsak memiliki aktivitas anti-inflamasi pada hewan percobaan
(Zuhud, 2011). Selain itu, menurut Hasrat, Bruyne, De Backer, Vauquelin, dan
Vlietinck (1997), terdapat efek antidepresi pada daun sirsak disebabkan oleh 3
senyawa alkaloid yang berupa annonaine, nornuciferine dan asimilobine yang
diujikan kepada tikus. Alkaloid tersebut mampu menghambat pengambilan
serotonin di otak. Ekstrak air daun sirsak juga memiliki potensi menurunkan
bilirubin sehingga efektif untuk penyakit hiperbilirubinemia atau penyakit kuning
(Arthur, et al, 2012).
C. Simplisia
Simplisia adalah bahan alamiah yang dipergunakan sebagai obat yang belum
mengalami pengolahan apapun juga kecuali dinyatakan lain, berupa bahan yang telah
dikeringkan. Simplisia nabati adalah simplisia yang berupa tanaman atau eksudat
tanaman. Eksudat tanaman adalah isi sel yang secara spontan keluar dari tanaman
atau isi sel dengan cara tertentu dipisahkan dari selnya, atau zat-zat nabati lainnya
13
murni. Simplisia hewani ialah simplisia yang berupa bahan utuh bagian hewan atau
zat-zat yang berguna, yang dihasilkan oleh hewan atau zat-zat berguna yang
dihasilkan oleh hewan dan belum berupa zat kimia murni. Simplisia pelikan (mineral)
ialah simplisia yang berupa bahan pelikan (mineral) yang belum diolah atau telah
diolah dengan cara sederhana dan belum berupa zat kimia murni (Direktorat Jendral
Pengawasan Obat dan Makanan RI, 1995 c).
Simplisia nabati atau simplisia hewani harus dihindarkan dari serangga atau
cemaran atau mikroba dengan pemberian bahan atau penggunaan cara yang sesuai,
sehingga tidak meninggalkan sisa yang membahayakan kesehatan (Direktorat Jendral
Pengawasan Obat dan Makanan RI, 1995 c).
D. Infusa
Salah satu metode penyarian adalah infusa. Bahan yang digunakan dalam
infusa berasal dari bahan yang lunak (simplisia daun dan bunga) (Suranto, 2004).
Pembuatan sediaan dalam bentuk infusa merupakan cara yang sederhana dan mudah
dilakukan serta untuk menyari kandungan zat aktif yang larut dalam air. Infusa adalah
sediaan yang dibuat dengan mengekstraksi simplisia nabati dengan air pada suhu
900C selama 15 menit (Direktorat Jendral Pengawasan Obat dan Makanan RI, 1986
a).
Pembuatan infusa dilakukan dengan cara simplisia yang telah dihaluskan
sesuai derajat kehalusan yang telah ditetapkan dimasukkan dalam air secukupnya.
Kemudian dipanaskan di atas penangas air selama 15 menit terhitung mulai suhu
mencapai 900C sambil berkali-kali diaduk, diserkai selagi panas melalui kain flanel,
menambahkan air panas secukupnya melalui ampas sehingga diperoleh volume infusa
yang dikehendaki. Jika infusa simplisia yang mengandung minyak atsiri harus
diserkai setelah dingin (Direktorat Jendral Pengawasan Obat dan Makanan RI, 1986
a). Penyarian dengan cara ini menghasilkan sari yang tidak stabil dan mudah tercemar
oleh kapang. Oleh sebab itu sari yang diperoleh dengan cara ini tidak boleh disimpan
lebih dari 24 jam (Direktorat Jendral Pengawasan Obat dan Makanan RI, 1986 a).
E. Ginjal
Ginjal adalah sepasang organ bersimpai yang terletak di area
retroperitoneum (McPhee and Ganong, 2010). Secara lebih rinci, struktur anatomi
dan fungsi fisiologi dari ginjal dijelaskan sebagai berikut:
1. Struktur anatomi ginjal
Ginjal berbentuk menyerupai kacang. Ginjal kanan dikelilingi oleh hati,
kolon, dan duodenum sehingga letaknya lebih rendah dari yang kiri. Sedangkan
ginjal kiri dikelilingi oleh lien, lambung, pankreas, jejenum, dan kolon. Ginjal
dibungkus oleh jaringan fibrus tipis dan mengkilat yang disebut kapsula ginjal dan
di luar terdapat jaringan lemak perirenal (Setiadi, 2007).
Ginjal manusia dewasa memiliki berat sekitar 150 g. Secara histologis ginjal
terdiri dari unsur utama yaitu glomerulus, tubulus dan interstitium, dan pembuluh
15
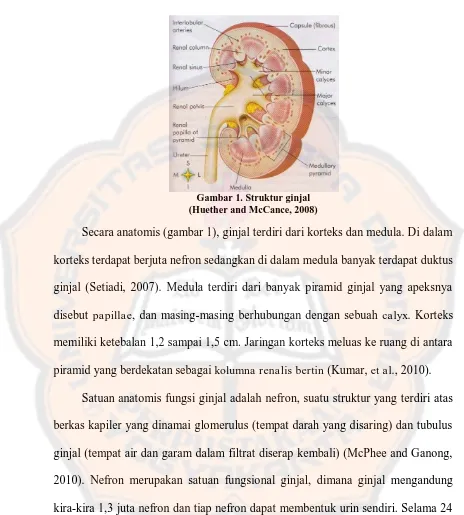
Gambar 1. Struktur ginjal (Huether and McCance, 2008)
Secara anatomis (gambar 1), ginjal terdiri dari korteks dan medula. Di dalam
korteks terdapat berjuta nefron sedangkan di dalam medula banyak terdapat duktus
ginjal (Setiadi, 2007). Medula terdiri dari banyak piramid ginjal yang apeksnya
disebut papillae, dan masing-masing berhubungan dengan sebuah calyx. Korteks
memiliki ketebalan 1,2 sampai 1,5 cm. Jaringan korteks meluas ke ruang di antara
piramid yang berdekatan sebagai kolumna renalis bertin (Kumar, et al., 2010).
Satuan anatomis fungsi ginjal adalah nefron, suatu struktur yang terdiri atas
berkas kapiler yang dinamai glomerulus (tempat darah yang disaring) dan tubulus
ginjal (tempat air dan garam dalam filtrat diserap kembali) (McPhee and Ganong,
2010). Nefron merupakan satuan fungsional ginjal, dimana ginjal mengandung
kira-kira 1,3 juta nefron dan tiap nefron dapat membentuk urin sendiri. Selama 24
jam dapat menyaring 170 liter darah (Setiadi, 2007).
Gambar 2. Struktur nefron
(McPhee, Lingappa, Ganong, dan Lange, 1995)
Setiap nefron terdiri dari Bowman’s capsule, yang mengitari rumbai kapiler
glomerulus, proximal tubule, loop of Henle, dan distal tubule, yang kemudian
mengosongkan diri ke collecting duct (gambar 2) (Price and Wilson, 1985).
Bagian dari nefron tersebut, akan dijelaskan masing-masing yaitu sebagai berikut:
a. Korpuskular ginjal. Korpuskular ginjal terdiri dari kapsula Bowman dan rumbai
kapiler glomerulus (Price and Wilson, 1985). Glomerulus adalah masa kapiler
yang berbentuk bola yang terdapat sepanjang arteriol. Fungsinya untuk filtrasi
air dan zat terlarut dalam darah (Lesson, 1996). Sedangkan kapsula bowman
merupakan suatu pelebaran nefron yang dibatasi oleh epitel yang menyelubungi
glomerulus untuk mengumpulkan zat terlarut yang difiltrasi oleh glomerulus
17
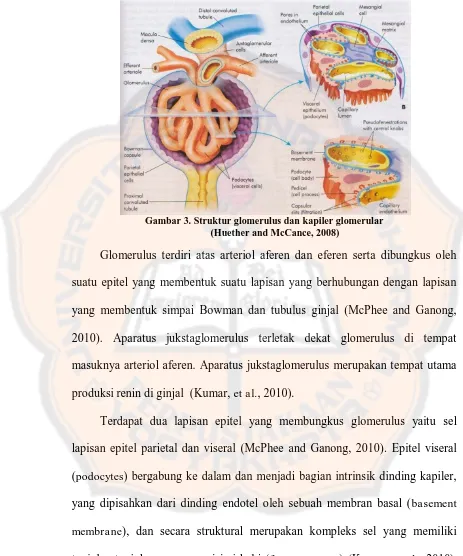
Gambar 3. Struktur glomerulus dan kapiler glomerular (Huether and McCance, 2008)
Glomerulus terdiri atas arteriol aferen dan eferen serta dibungkus oleh
suatu epitel yang membentuk suatu lapisan yang berhubungan dengan lapisan
yang membentuk simpai Bowman dan tubulus ginjal (McPhee and Ganong,
2010). Aparatus jukstaglomerulus terletak dekat glomerulus di tempat
masuknya arteriol aferen. Aparatus jukstaglomerulus merupakan tempat utama
produksi renin di ginjal (Kumar, et al., 2010).
Terdapat dua lapisan epitel yang membungkus glomerulus yaitu sel
lapisan epitel parietal dan viseral (McPhee and Ganong, 2010). Epitel viseral
(podocytes) bergabung ke dalam dan menjadi bagian intrinsik dinding kapiler,
yang dipisahkan dari dinding endotel oleh sebuah membran basal (basement
membrane), dan secara struktural merupakan kompleks sel yang memiliki
tonjolan-tonjolan menyerupai jari kaki (foot processes) (Kumar, et al., 2010).
Membran basal ini terletak di antara sel epitel dan kapiler. Sedangkan epitel
parietal terletak pada kapsul Bowman, bentuknya gepeng, dan membentuk
bagian terluar dari kapsula (Price and Wilson, 1985).
Sel-sel endotel membentuk bagian terdalam dari rumbai kapiler. Sel-sel
endotel, membran basal, dan sel epitel viseral merupakan tiga lapisan yang
membentuk membran filtrasi glomerulus. Fungsi dari membran filtrasi
glomerulus adalah ultrafiltrasi darah (Price and Wilson, 1985).
Sel-sel mesangial adalah sel-sel endotel yang membentuk suatu jalinan
kontinu antara lengkung-lengkung kapiler glomerulus dan berfungsi sebagai
jalinan penyokong (Price and Wilson, 1985). Ruang antara kapiler-kapiler di
glomerulus disebut mesangium (McPhee and Ganong, 2010).
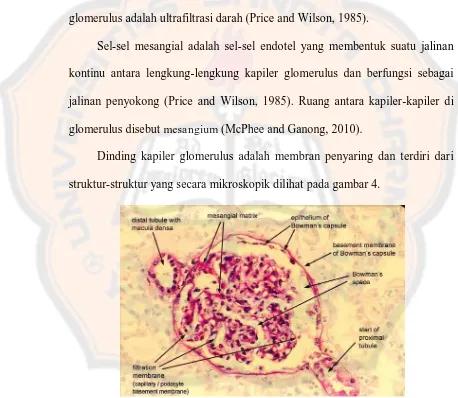
Dinding kapiler glomerulus adalah membran penyaring dan terdiri dari
struktur-struktur yang secara mikroskopik dilihat pada gambar 4.
19
Gambar 5. Mikrograf elektron pembesaran lemah glomerulus ginjal. CL, lumen kapiler; MES, mesangium; END, endotel; EP, sel epitel viseral dengan foot processes (tonjolan kaki)
(Kumar, et al., 2010)
b. Tubulus kontortus proksimal. Cairan yang difiltrasi akan mengalir ke tubulus
kontortus proksimal. Letak tubulus ini di dalam korteks ginjal, panjangnya 14
mm dengan diameter 50-60 nm (gambar 6). Bentuknya berkelok-kelok dan
berakhir sebagai saluran yang lurus yang berjalan kearah medula, yaitu ansa
henle (Lesson, 1996).
c. Ansa henle. Ansa henle merupakan nefron pendek yang memiliki segmen yang
tipis yang membentuk lengkung tajam berbentuk huruf U. Bagian pa rs
desendens dari ansa henle terbentang dari korteks ke bagian medula, sedangkan
pars asendens berjalan kembali dari medula ke arah korteks ginjal (Lesson,
1996).
d. Tubulus distal. Setelah melewati ansa henle, maka akan berlanjut ke bagian
nefron tubulus distal. Pada gambar 6, tubulus kontortus distal lebih pendek dari
tubulus proksimal. Bagian tubulus distal ini berkelok-kelok di bagian korteks
dan berakhir di duktus koligens (Lesson, 1996; Sherwood, 2006).
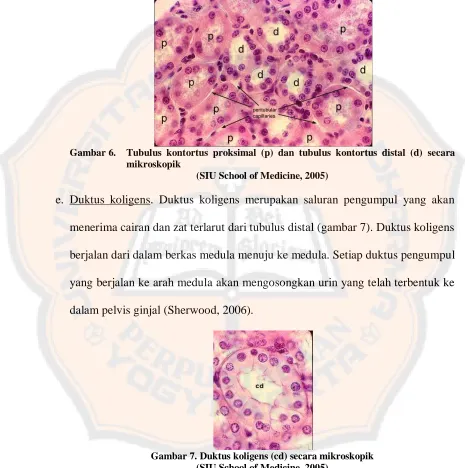
Gambar 6. Tubulus kontortus proksimal (p) dan tubulus kontortus distal (d) secara mikroskopik
(SIU School of Medicine, 2005)
e. Duktus koligens. Duktus koligens merupakan saluran pengumpul yang akan
menerima cairan dan zat terlarut dari tubulus distal (gambar 7). Duktus koligens
berjalan dari dalam berkas medula menuju ke medula. Setiap duktus pengumpul
yang berjalan ke arah medula akan mengosongkan urin yang telah terbentuk ke
dalam pelvis ginjal (Sherwood, 2006).
Gambar 7. Duktus koligens (cd) secara mikroskopik (SIU School of Medicine, 2005)
Di korteks normal, rongga interstisium tersusun rapat, ditempati oleh kapiler
21
Ginjal kaya akan pembuluh darah, dan meskipun kedua ginjal hanya
membentuk 0,5% dari berat tubuh total, tetapi keduanya menerima sekitar 25%
curah jantung. Korteks adalah bagian ginjal yang paling kaya pembuluh darah,
menerima 90% dari total aliran darah ginjal. Arteri renalis bercabang menjadi
bagian anterior dan posterior di hilum (Kumar, et al., 2010). Pembuluh darah
utama pada ginjal adalah sebagai berikut:
a. Renal arteries. Terletak sebagai cabang kelima dari aorta abdominal, membagi
menjadi cabang-cabang anterior dan posterior pada hilus ginjal, dan kemudian
membagi lagi menjadi arteri lobus.
b. Interlobar arteries. Pembuluh ini mengalirkan darah ke ginjal dari arteri aferen
glomerular.
c. Arcuate arteries. Cabang arteri interlobar yang terletak di cortical medullary
junctions.
d. Glomerular capillaries. Berfungsi membawa darah menuju peritubular
capillaries.
e. Peritubular capillaries. Berfungsi untuk mengelilingi atau membelit tubulus
proksimal, tubulus distal, dan lengkung Henle.
f. Vasa recta. Jaringan kapiler yang membentuk loop dan mengikuti lengkung
Henle, dan berfungsi menyuplai darah menuju medula.
g. Renal veins. Mengikuti jalan arteri dan memiliki nama yang sama dengan arteri,
dan akhirnya membuang darah ke inferior vena cava (Huether and McCance,
2008).
2. Fisiologi ginjal
Ginjal melakukan fungsi vital sebagai tempat ekskresi zat yang tidak
terpakai serta pengatur komposisi dan volume kimia darah dengan
mensekskresikan solut dan air secara selektif yang dikontrol oleh filtrasi
glomerulus, reabsorpsi, dan sekresi tubulus (Price and Wilson, 1985). Kemampuan
ginjal untuk mengatur komposisi cairan ekstraseluler merupakan fungsi per satuan
waktu yang diatur oleh epitel tubulus (Silbernagyl and Lang, 2007).
Gambar 8. Fungsi utama pada bagian-bagian nefron (Huether and McCance, 2008)
Untuk zat yang tidak disekresi oleh tubulus, pengaturan volumenya
berhubungan dengan laju filtrasi glomerulus (LFG). Seluruh zat yang larut dalam
filtrasi glomerulus dapat direabsorpsi atau disekresi oleh tubulus (Silbernagyl and
23
Pada gambar 8 menjelaskan fungsi-fungsi utama pada setiap bagian nefron
secara sistematis, untuk penjelasan secara rinci mengenai fungsi fisiologi ginjal
adalah sebagai berikut:
a. Filtrasi glomerulus. Cairan yang difiltrasikan melalui glomerulus ke dalam
kapsula Bowman disebut filtrat glomerulus. Sel-sel endotel, membran basal,
dan lapisan epitel viseral merupakan tiga lapisan yang membentuk membran
filtrasi glomerulus. Pada filtrat harus melewati membran tersebut sehingga baru
dapat dialirkan ke kapsula Bowman (Setiadi, 2007).
Komposisi cairan filtrat glomerulus mempunyai komposisi yang hampir
sama dengan cairan yang terserap masuk dari ujung arteri kedalam cairan
interstisium. Tidak mengandung eritrosit dan hanya mengandung 0,03% protein
di dalam plasma. Elektrolit dan komposisi solut lain dari filtrat glomerulus juga
ditemukan pada cairan interstisium (Setiadi, 2007).
Jumlah filtrat glomerulus yang dibentuk setiap menit dalam semua nefron
kedua ginjal disebut laju filtrasi glomerulus (GFR = Glomerula r Filtration
Rate). GFR ditentukan oleh tiga faktor yaitu keseimbangan tekanan-tekanan
yang bekerja pada dinding kapiler (tekanan hidrostatik kapiler glomeruli dan
tekanan onkotik kapsul Bowman mendorong terjadinya filtrasi sedangkan
tekanan onkotik kapiler glomeruli dan tekanan hidrostatik kapsul Bowman
menghambatnya), kecepatan aliran darah ke ginjal (renal blood flow = RBF)
atau kecepatan aliran plasma melalui glomeruli (glomerular plasma flow =
GPF) dan permeabilitas serta luas permukaan kapiler yang berfungsi
(Laboratorium Amerind Bio-Clinic, 2010).
Penentuan nilai GFR dapat dihitung dengan menggunakan rumus. Rumus
Cockcroft dan Gault merupakan rumus umum yang biasa digunakan dengan
mempertimbangkan umur, berat badan, dan nilai kreatinin plasma (Pcr)
(Huether and McCance, 2008).
GFR (mL/min) = 140− � ( �)
� � 72 x 0,85 (wanita)
Selain itu, The National Kidney Foundation merekomendasikan
perhitungan GFR dengan rumus Modification of Diet in Renal Disease
(MDRD) yaitu:
GFR (mL/min) = 186 x Pcr-1,154 x umur-0,203 x (0,742 pada wanita; 1,210
pada pria) (Huether and McCance, 2008).
Pada keadaan normal, banyaknya GFR sekitar 120 mL/menit. Urin dalam
bentuk awal tersebut merupakan ultrafiltrat plasma kecuali sejumlah kecil
protein yang dapat diabaikan dan yang kemudian akan direabsorpsi di tubuli
(Laboratorium Amerind Bio-Clinic, 2010).
b. Transport tubular. Di tubuli proksimal terjadi reabsorpsi 2/3 dari ultrafiltrat
glomeruli secara isoosmotik. Akibat susunan anatomik nefron yang amat
khusus maka di glomeruli tekanan hidrostatik lebih besar daripada tekanan
25
yaitu tekanan hidrostatik lebih kecil daripada tekanan onkotik (Laboratorium
Amerind Bio-Clinic, 2010).
Selain air dan Na+, direabsorpsi juga sebagian besar HCO3- (bikarbonat),
asam amino dan glukosa. Sebaliknya kadar Cl- di dalam tubulus meningkat.
Pada bagian menurun ansa Henle terjadi pengeluaran air secara pasif sehingga
urin menjadi hipertonik. Pada bagian naik ansa Henle tidak permeabel untuk air
sedangkan NaCl keluar. Urin yang sampai ke tubulus distal bersifat
hipoosmotik, terjadi reabsorpsi Na+ secara aktif. Aldosteron berperan menahan
natrium serta air dan sebaliknya melepaskan kalium. Hormon antidiuretik
(ADH) berperan mereabsorpsi air pada bagian akhir tubulus distal dan saluran
pengumpul (collecting duct) sehingga urin yang hipotonik dapat menjadi
hipertonik (lihat Gambar 9) (Laboratorium Amerind Bio-Clinic, 2010).
Selain ADH, ada juga hormon aldosteron yang berperan dalam membantu
merangsang reabsorpsi natrium dalam tubulus distal dan duktus koligen. ADH
bersama dengan aldosteron bergungsi untuk mengendalikan tekanan darah.
Pada ginjal, dikenal sistem renin-angiotensin. Pengeluaran renin dari ginjal
akan mengakibatkan perubahan angiotensinogen (suatu glikoprotein yang
dibuat dalam hati) menjadi angiotensin I. Angiotensin I kemudian dirubah
menjadi angiotensin II oleh converting enzyme yang ditemukan di dalam
kapiler paru-paru. Angiotensin II meningkatkan tekanan darah dengan
menyebabkan vasokonstriksi arteriol perifer dan merangsang sekresi
aldosteron. Peningkatan kadar aldosteron akan merangsang reabsorpsi natrium
dalam tubulus distal dan duktus koligen. Peningkatan reabsorpsi natrium akan
mengakibatkan peningkatan reabsorpsi air dan dengan demikian volume plasma
meningkat. Peningkatan volume plasma ini ikut berperan dalam peningkatan
tekanan darah yang seterusnya akan mengurangi iskemia ginjal (Price and
Wilson, 1985).
Gambar 9. Mekanisme pembentukan urin melalui proses filtrasi, reabsorpsi, dan sekresi
(Laboratorium Amerind Bio-Clinic, 2010)
Urin yang dikeluarkan mengandung air dengan ureum, kreatinin, fosfat
dan sulfat hasil proses katabolisme. Juga terdapat asam urat, K+, dan H+ hasil
penukaran dengan Na+ atas pengaruh aldosteron di tubulus distal. Protein dalam
keadaan normal diekskresi dalam jumlah sedikit. Glukosa yang difiltrasi akan
direabsorpsi di tubulus proksimal, tetapi dengan makin tinggi kadarnya dalam
filtrat glomeruli maka makin banyak pula glukosa yang dikeluarkan bersama
urin. Terdapat pula eritrosit, leukosit, dan kristal metabolit serta sel-sel epitel
27
F. Pemeriksaan Kreatinin
Kreatinin merupakan produk akhir dari metabolisme kreatin otot dan kreatin
fosfat (protein), yang disintesis dalam hati, ditemukan dalam otot rangka dan darah,
dan diekskresikan dalam urine. Meningkatnya kadar kreatinin dalam darah
merupakan indikasi rusaknya fungsi ginjal (Lu, 1995).
1. Metabolisme kreatinin
Kreatinin berasal dari pemecahan kreatinifosfat otot. Kreatinin adalah
produk akhir dari metabolisme kreatin. Kreatin sebagian besar ditemukan di otot
rangka, tempat zat ini terlibat dalam penyimpanan energi sebagai kreatin fosfat.
Dalam sintesis ATP dari ADP, kreatin fosfat diubah menjadi kreatin dengan
katalasi enzim kreatin kinase. Reaksi ini berlanjut seiring dengan pemakaian
energi sehingga dihasilkan kreatin fosfat. Dalam prosesnya, sejumlah kecil
kreatin diubah secara ireversibel menjadi kreatinin, yang dikeluarkan dari
sirkulasi oleh ginjal. Jumlah kreatinin yang dihasilkan setara dengan massa otot
rangka yang dimiikinya (Sacher and Richard, 2004).
2. Fakor yang mempengaruhi kadar kreatinin darah
Kreatinin umumnya dianggap tidak dipengaruhi oleh asupan protein namun
sebenarnya ada pengaruh diet terutama protein tetapi tidak sebesar pengaruhnya
terhadap kadar ureum. Kreatinin terutama dipengaruhi oleh massa otot. Karena
itu kadar kreatinin darah lebih tinggi pada laki-laki daripada perempuan,
meningkatnya pada atlit dengan massa otot banyak, dan juga pada kelainan
pemecahan otot (rhabdomiolisis). Sebaliknya kadar kreatinin menurun pada usia
(orang usia lanjut) yang massa ototnya berkurang (Laboratorium Amerind
Bio-Clinic, 2010).
3. Metode pemeriksaan kreatinin
Macam pemeriksaan kreatinin darah adalah:
a. Jaffe Reaction. Dasar dari metode ini adalah kreatinin dalam suasana alkalis
dengan asam pikrat membentuk senyawa kuning jingga. Alat yang
digunakan photometer.
b. Kinetik. Dasar metodenya relatif sama hanya dalam pengukuran dibutuhkan
sekali pembacaan. Alat yang digunakan autoanalyzer.
c. Enzimatik. Dasar metode ini adalah dengan adanya substrat dalam sampel
bereaksi dengan enzim membentuk senyawa enzim substrat dengan
menggunakan alat photometer.
Meskipun sejumlah kecil disekresi, tes kliren kreatinin merupakan suatu tes
untuk memperkirakan GFR dalam klinik. Untuk melakukan tes kliren kreatinin,
cukup mengumpulkan contoh urin atau darah selama 24 jam (Price and Wilson,
1985).
Dalam keadaan normal, produksi kreatinin secara kasar sama dengan
ekskresi kreatinin, sehingga kadar kreatinin serum konstan. Pada seorang penderita
dengan filtrasi glomerulus yang menurun, kreatinin serum akan terakumulasi sesuai
dengan derajat hilangnya filtrasi glomerulus pada ginjal. Konsentrasi kreatinin serum
29
pemantauan fungsi ginjal yang cepat dan sesuai. Secara farmakokinetik, klirens
kreatinin dapat ditakrifkan sebagai laju ekskresi kreatinin melalui urin atau kreatinin
serum. Klirens kreatinin secara klinik dinyatakan dalam mL/menit dan konsentrasi
kreatinin serum dalam mg% (Shargel and Yu, 1988). Persamaan berikut digunakan
untuk menghitung klirens kreatinin dalam mL/menit:
CLcr = (Ucr × V) / (Scr × t)
Di mana Ucr = urine creatinine concentration, V = urine volume, Scr = serum
creatinine concentration, dan t = duration of the urine collection (Dipiro, Yee,
Matzke, Wells, and Posey, 2008).
Menurut Huether dan McCance (2008), nilai normal dari pla sma creatinine
concentration adalah 0,7-1,2 mg/dL. Konsentrasi kreatinin plasma ini akan memiliki
nilai yang stabil ketika nilai GFR juga stabil, karena laju produksi kreatinin sama
besar dengan hasil metabolisme otot. Nilai normal kreatinin dalam darah pada tes
fungsi ginjal yang normal pada manusia adalah sebesar 0,6-1,5 mg/dL (laki-laki) dan
0,6-1,1 mg/dL (perempuan). Sedangkan nilai rata-rata kadar kreatinin normal pada
tikus strain Sprague-Da wley adalah 0,860 mg/dL (jantan) dan 0,713 mg/dL (betina)
(Derelanko and Hollinger, 2002).
G. Kerusakan Ginjal
Fungsi utama dari ginjal adalah organ eliminasi penting bagi tubuh.
Meskipun terdapat banyak faktor yang mempengaruhi kerentanan ginjal terhadap
efek toksik, tetapi tingginya aliran curah jantung dan peningkatan konsentrasi produk
ekskresi karena adanya reabsorpsi air dari cairan tubuler merupakan faktor terpenting.
Akibatnya, beberapa obat atau zat kimia yang beredar dalam sirkulasi sistemik akan
dibawa ke ginjal dalam kadar yang cukup tinggi. Sebagai akibatnya akan terjadi
proses perubahan struktur dari ginjal itu sendiri, terutama di tubulus ginjal karena
disinilah terjadi proses reabsorpsi dan eksresi dari zat- zat toksik tersebut
(Manggarwati, 2010).
Gambaran kondisi ginjal normal dapat dilihat secara mikroskopik (gambar
10).
Gambar 10. Gambaran mikroskopik ginjal normal (diwarnai dengan haematoxylin dan eosin). (A) Korteks ginjal, 1: renal corpuscle; 2: proximal convoluted tubules; 3: distal convoluted tubules; 4: Bowman's capsulae space. (B) Medula ginjal, 1: thick ascending limb of the loop of Henle; 2: interstitial connective tissue
(Gunin, 2000)
Penyakit ginjal sangat kompleks sama seperti strukturnya, tetapi untuk
memahaminya bisa dipermudah dengan membagi penyakit ginjal berdasarkan empat
komponen morfologik dasar ginjal yaitu glomerulus, pembuluh darah, tubulus, dan
31
sedangkan penyakit pada tubulus dan interstisium sering disebabkan oleh bahan
toksik atau infeksi (Kumar, et al., 2010).
1. Penyakit yang mengenai glomerulus
Penyakit glomerulus dapat digolongkan lebih lanjut berdasarkan gambaran
klinis. Sebagian penyakit bermanifestasi sebagai proteinuria berat tetapi tanpa
tanda reaksi peradangan selular (penyakit nefrotik), sementara yang lain
memperlihatkan proteinuria dengan derajat bervariasi yang disertai oleh adanya
sel darah merah dan putih di urin (penyakit nefritik) (McPhee and Ganong,
2010).
Penyakit nefrotik biasanya memperlihatkan pengendapan kompleks imun
tepat di atau di bawah sel epitel, sering dengan perubahan morfologis foot
process. Sedangkan penyakit nefritik memperlihatkan pengendapan kompleks
imun di lokasi subendotel atau di membran basal glomerulus atau mesangium
(McPhee and Ganong, 2010).
2. Penyakit yang mengenai tubulus dan interstisium
Sebagian besar cidera tubulus juga melibatkan interstisium. Interstisium
adalah ruang antar tubulus. Adanya kerusakan dalam tubulus ginjal akibat zat
nefrotoksik dilihat dengan adanya penyempitan tubulus kontortus proksimal,
nekrosis sel epitel tubulus kontortus proksimal, atau adanya hyaline cast di
tubulus distal (Manggarwati, 2010).
Salah satu penyakit yang mengenai tubulus dan interstisium adalah nefritis
tubulointerstisium (reaksi peradangan di tubulus dan interstisium). Nefritis
tubulointerstisium dapat bersifat akut atau kronis. Nefritis tubulointerstisium akut
memperlihatkan secara histologiss ditandai dengan edema interstisial, sering kali
disertai infiltrasi leukositik di interstisum dan tubulus, dan nekrosis tubulus fokal.
Nekrosis adalah pembengkakan sel yang kemudian mengalami lisis. Sel yang
nekrotik terlihat membesar dan lebih asidofik (merah) daripada sel normal.
Nekrosis melibatkan kematian sekelompok sel dan terlihat adanya respon
peradangan. Pada nefritis tubulointerstisium kronik, terjadi infiltrasi terutama
oleh leukosit menonukleus, fibrosis interstisium, dan atrofi tubulus luas.
Gambaran morfologik yang membedakan bentuk akut dan kronik pada nefritis
tubulointerstisium adalah edema dan (jika ada) eosinofil dan neutrofil pada
bentuk akut, dan fibrosis serta atrofi tubulus pada bentuk kronik (Kumar, et al.,
2010).
Mekanisme utama dalam nefritis tubulointerstitial akut adalah reaksi
hipersensitivitas terhadap obat seperti penisilin, anti-inflammatory drugs
(NSAIDs), dan obat sulfa. Mekanisme lain adalah cedera selular akut yang
disebabkan oleh infeksi, virus atau bakteri, sering dikaitkan dengan obstruksi
atau refluks. Ginjal sangat tahan terhadap kerusakan struktural karena infeksi
bakteri, dan dengan tidak adanya obstruksi, kerusakan dari infeksi bakteri dalam
parenkim ginjal sangat mungkin terjadi (Alper, 2011).
Cedera yang bermanifestasi sebagai kerusakan tubulus dan inflamasi
interstisium, salah satunya disebabkan oleh fibrosis tubulointerstisium. Banyak
33
segmen-segmen tubulus di sebelah hilir glomerulus sklerotik, dan berkurang dan
hilangnya pasokan darah kapieler peritubulus. Berdasarkan penelitian pada
hewan secara in vitro, proteinuria diduga menyebabkan cedera langsung dan
mengaktifkan sel tubulus. Sebaliknya, sel tubulus aktif akan mengekspresikan
molekul-molekul adhesi dan dan mengeluarkan sitokin proinflamasi, kemokin
dan faktor pertumbuhan yang berperan dalam fibrosis interstisium (Kumar, et al.,
2010).
Gambar 11. Mekanisme cedera tubulointerstisium kronik pada glomerulonefritis. ET-1, endotelin-1, PAI-1, plasminogen activator inhibitor-1; TIMP-1, tissue inhibitor of metaloproteinases.
(Kumar, et al., 2010).
Dilihat pada gambar 11, berbagai komponen filtrat kaya protein dan sitokin
yang berasal dari leukosit, menyebabkan aktivasi sel tubular dan sekresi sitokin,
faktor pertumbuhan, dan mediator lainnya. Seluruhnya bersama produk-produk
makrofag, menyebabkan inflamasi interstisium dan fibrosis (Kumara, et al.,
2010).
Nefritis interstitial sama halnya dengan nefritis tubulointerstisium yaitu
peradangan pada daerah interstisium yang disebabkan oleh reaksi alergi obat,
penyakit autoimun, infeksi atau infiltrasi penyakit lainnya. Dalam nefritis
interstitial akut, kerusakan tubular menyebabkan disfungsi tubular ginjal, dengan
atau tanpa gagal ginjal. Terlepas dari tingkat keparahan kerusakan epitel tubular,
disfungsi ginjal ini umumnya reversibel (Kumara, et al., 2010) (Kumara, et al.,
2010).. Menurut Wulandari (2010), nefritis intersitial ini secara morfologi
ditandai dengan sitoplasma yang keruh, pembengkakan sel-sel tubulus proksimal
sehingga lumennya menyempit bahkan menghilang. Nefritis interstitial
merupakan jejas tubular yang manifestasi awalnya berupa edema tubulus
proksimal dimana sel-sel epitel tubulus proksimal dan intertisium membengkak
dengan sitoplasma yang granuler karena terjadi pergeseran air ekstraseluler ke
intrasel. Pergeseran cairan ini terjadi karena toksin menyebabkan perubahan
muatan listrik permukaan sel epitel tubulus, transport ion aktif dan asam organik,
dan kemampuan mengkonsentrasikan dari ginjal yang akhirnya mengakibatkan
tubulus rusak (Wijaya dan Miranti, 2005).
Gambar 12. Gambaran mikroskopik nefritis interstitial kronik (diwarnai dengan
35
Pada gambar 12 menjelaskan nefritis interstitial kronik di mana tubulus
muncul menyusut dan atrofi (ditunjukkan oleh panah), dan dipisahkan oleh
fibrosis interstisial yang luas (ditunjukkan oleh panah) (Perazella and Markowitz,
2010).
Interstisium korteks yang melebar dikatakan abnormal. Pelebaran ini dapat
disebabkan oleh edema atau infiltrasi oleh sel radang akut, seperti pada penyakit
interstisium akut, atau mungkin juga oleh akumulasi sel radang kronik dan
jaringan fibrosa, serta pada penyakit interstisium kronik. Jumlah proteoglikan di
jaringan interstisium medula meningkat seiring usia dan adanya iskemia (Kumar,
et al., 2010).
3. Penyakit yang mengenai pembuluh darah
Hampir semua penyakit ginjal melibatkan pembuluh darahnya secara
sekunder. Salah satu contoh penyakitnya adalah nefrosklerosis jinak yaitu istilah
yang digunakan untuk patologi ginjal akibat sklerosis arteriol dan arteri kecil
ginjal. Efek yang terjadi adalah iskemia fokal parenkim yang disuplai oleh
pembuluh yang dindingnya menebal dan lumennya menyempit (Kumar, et al.,
2010).
H. Uji Toksisitas Subkronis
Uji ketoksikan subkronis ialah uji ketoksikan sesuatu senyawa yang
diberikan dengan dosis berulang pada hewan uji tertentu, selama kurang dari tiga
bulan. Uji ini ditujukan untuk mengungkapkan spektrum efek toksik senyawa uji,
serta untuk memperlihatkan apakah spektrum efek toksik itu berkaitan dengan
takaran dosis (Donatus, 2001).
Pengamatan dan pemerikasaan yang dilakukan dari uji ketoksikan subkronis
meliputi:
1. Perubahan berat badan yang diperiksa paling tidak tujuh hari sekali.
2. Masukan makanan untuk masing-masing hewan atau kelompok hewan yang
diukur paling tidak tujuh hari sekali.
3. Gejala kronis umum yang diamati setiap hari.
4. Pemeriksaan hematologi paling tidak diperiksa dua kali pada awal dan akhir uji
coba.
5. Pemeriksaan kimia darah paling tidak dua kali pada awal dan akhir uji coba.
6. Analisis urin paling tidak sekali.
7. Pemeriksaan histopatologi organ pada akhir uji coba (Loomis, 1978).
Hasil uji ketoksikan subkronis akan memberikan informasi yang bermanfaat
tentang efek utama senyawa uji dan organ sasaran yang dipengaruhinya. Selain itu
juga dapat diperoleh info tentang perkembangan efek toksik yang lambat berkaitan
dengan takaran yang tidak teramati pada uji ketoksikan akut. Kekerabatan antar kadar
senyawa pada darah dan jaringan terhadap perkembangan luka toksik dan
keterbalikan efek toksik (Donatus, 2001).
Tujuan utama dari uji ini adalah untuk mengungkapkan dosis tertinggi yang
diberikan tanpa memberikan efek merugikan serta untuk mengetahui pengaruh
37
hispatologi organ (organ-organ yang terkena efek toksik), gejala-gejala toksik, wujud
efek toksik (kekacauan biokimia, fungsional, dan struktural) serta sifat efek toksik
(Eatau and Klaassen, 2001).
Jenis wujud toksik digolongkan berdasarkan perubahan biokimia,
fungsional, dan struktural. Jenis wujud efek toksik berdasarkan perubahan biokimia
berkaitan dengan respons dan perubahan atau kekacauan biokimia terhadap luka sel,
akibat antaraksi antara racun dan tempat aksi yang terbalikan. Antaraksi yang
terbalikan yang dimaksud adalah reaksi yang terjadi antara molekul racun dan tempat
aksi yang khas, seperti reseptor-reseptor neurotransmitter, tempat aktif enzim, dan
lain sebagainya. Jenis wujud efek toksik berdasarkan perubahan fungsional berkaitan
dengan antaraksi racun yang terbalikan dengan reseptor atau tempat aktif enzim,
sehingga mempengaruhi fungsi homeostatis tertentu. Sedangkan pada jenis efek
toksik berdasarkan perubahan struktural diantaranya perlemakan (degenarasi
melemak), nekrosis, karsinogenesis, mutagenesis, dan teratogenesis (Donatus, 2001).
Ketoksikan racun dipengaruhi oleh banyak faktor yaitu meliputi faktor yang
berasal dari racun pangan (faktor intrinsik racun) dan yang berasal dari makhluk
hidupnya (faktor intrinsik makhluk hidup). Faktor intrinsik racun ialah faktor kimia
fisika, kondisi pemejanan, pengolahan, pengawetan, pengentalan, dan pengepakan
racun. Yang termasuk dalam kondisi pemejanan yaitu antara lain:
a. Jenis pemejanan. Ada dua jenis pemejanan yaitu akut dan kronis. Ketoksikan akut
berlaku bagi peristiwa keracunan yang terjadi segera setelah pemejanan racun,