ISOLASI DAN KARAKTERISASI SENYAWA FLAVONOID
DARI BIJI MANGGA ARUMMANIS (Mangifera indica L) DAN
UJI AKTIVITASNYA SEBAGAI ANTIOKSIDAN
Skripsidisusun untuk memenuhi salah satu syarat untuk memperoleh gelar Sarjana Sains
Program Studi Fisika
oleh
Marathur Rodhiyah 4211416025
JURUSAN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS NEGERI SEMARANG
iii
PERNYATAAN
Dengan ini, sayanama : Marathur Rodhiyah NIM : 4211416025
program studi : Fisika
menyatakan bahwa skripsi berjudul Isolasi dan Karakterisasi Senyawa Flavonoid dari Biji Mangga Arummanis (Mangifera indica L) dan Uji Aktivitasnya sebagai Antioksidan ini benar-benar karya saya sendiri bukan jiplakan dari karya orang lain atau pengutipan dengan cara-cara yang tidak sesuai dengan etika keilmuan yang berlaku baik sebagian atau seluruhnya. Pendapat atau temuan orang atau pihak lain yang terdapat dalam skrisi in telah dikutip atau dirujuk berdasarkan kode etik ilmiah. Atas pernyataan ini, saya secara pribadi siap menanggung resiko/sanksi hokum yang dijatuhkan apabila ditemukan adanya pelanggaran terhadap etika keilmuan dalam karya ini.
Semarang, 19 Maret 2020
Marathur Rodhiyah NIM 4211416025
v
MOTTO DAN PERSEMBAHAN
MOTTO“ Man jadda wa jadda, dimana ada kemauan disitu ada jalan”
PERSEMBAHAN Untuk orang tua Bapak Masturi Almamater tercinta
vi
PRAKATA
Segala puji bagi Allah yang telah memberikan kemudahan sehingga penulis dapat menyelesaikan skripsi yang berjudul Isolasi dan Karakterisasi Senyawa Flavonoid dari Biji Mangga Arummanis (Mangifera indica L) dan Uji Aktivitasnya sebagai Antioksidan. Penulis menyadari sepenuhnya bahwa penelitian ini tidak akan selesai tanpa bantuan dari berbagai pihak, untuk itu penulis mengucapkan terimakasih kepada
1. Orang tua saya Bapak Arif Mahmudi dan Ibu Mundari serta keluarga di rumah yang selalu mendukung dan mendoakan
2. Bapak Masturi selaku dosen pembimbing yang telah membimbing dengan baik
3. Bapak Susilo dan Bapak Dante Alighiri selaku penguji yang telah memberi masukan selama sidang skripsi
4. Teknisi Laboratorium Fisika Unnes yang telah membantu selama proses penelitian skripsi
5. Alif dan rikha yang selalu bersedia mendengar keluh kesah
6. Teman-teman laboratorium fisika komposit terapan: Mbak Ina, Mae, Mbak riska, Mbak saras, dan Faisal, serta teman-teman kimia: Mbak zanna, Mbak Luzy, Mas Amrul dan Lutfi yang selalu membantu
7. Adhe yang telah membantu selama persiapan ujian skripsi 8. Dany wijaya partner dalam segala hal
9. Teman-teman Fisika 2016 yang selalu rangkul merangkul berjuang bersama 10. Serta berbagai pihak yang tidak dapat saya sebutkan satu persatu.
Penulis berharap semoga skripsi ini bisa bermanfaat bagi pembaca dan dapat dijadikan referensi untuk melakukan penelitian selanjutnya.
Semarang, 19 Maret 2020
Marathur Rodhiyah NIM 4211416025
vii
ABSTRAK
Rodhiyah, Marathur. 2020. Isolasi dan Karakterisasi Senyawa Flavonoid dari Biji Mangga Arummanis (Mangifera indica L) dan Uji Aktivitasnya sebagai Antioksidan. Skripsi, Jueusan Fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam,
Universitas Negeri Semarang. Pembimbing Dr. Masturi, M.Si. Kata kunci: Biji mangga arummanis, fenol, flavonoid, antioksidan.
Mangga (Mangifera indica L) tumbuh diberbagai Negara beriklim tropis. Salah satu jenis manga yang melimpah di Indonesia adalah mangga arummanis.Telah diteliti bahwa dalam biji mangga arummanis mengandung senyawa flavonoid. Flavonoid adalah antioksidan kuat yang memiliki kemampuan untuk menangkal radikal bebas. Tujuan dilakukannya penelitian ini adalah untuk mengisolasi senyawa flavonoid dan uji aktivitasnya sebagai antioksidan. Biji mangga arummanis diekstrak menggunakan metode refluks. Sebelum diisolasi, ekstrak biji mangga tersebut diuji terlebih dahulu menggunakan Kromatografi Lapis Tipis (KLT) untuk mengatahui pelarut apa yag dapat memisahkan senyawa flavonoid dari ekstrak biji mangga arummanis secara optimum. Ekstrak biji mangga tersebut kemudian diisolasi menggunakan metode Kromatografi Kolom Gravitasi (KKG). Hasil dari KLT menunjukkan bahwa flavonoid dapat terpisahkan secara optimum ketika di pisahkan menggunakan fasa diam plat silika gel60 dan fase gerak berupa pelarut toluene: etil asetat: asam format: methanol dengan perbandingan 6: 3: 1: 0,6. Pelarut-pelerut dengan perbandingan tersebut kemudian digunakan untuk mengelusi ekstrak bii mangga menggunakan metode KKG. Pemisahan menggunakan metode KKG menghasilkan 3 fraksi dengan nilai RF masing-masing adalah 0,48, 0,44 dan 0,42. Ketiga sampel tersebut kemudian dikarakterisasi menggunakan FTIR, LCMS dan UV-Vis. Hasil FTIR menunjukkan bahwa pada ketiga sampel tersebut mengandung senyawa fenol dan flavonoid yang dibuktikan dengan ditemukannya gugus fungsi O-H dan gugus C=O. Gugus O-H berturutu-turut pada sampel A, B, dan C ditunjukkan pada bilangan gelombang 3442,37, 3430,44, dan 3433,06 𝑐𝑚−1. Sedangkan gugus C=O pada sampel A, B, dan C berturut-turut ditunjukkan pada bilangan gelombang 1620,27, 1598,39, dan 1625,17 𝑐𝑚−1. Hasil pengujian FTIR tersebut diperkuat oleh hasil pengujian kandungan fenol total dan kandungan flavonoid total menggunakan spektrofotometer UV-Vis. Dari pengujian kandungan fenol total didapatkan hasil bahwa dalam sampel A, B, dan C berturut-turut mengandung senyawa fenol sebesar 18,58, 20,35, dan 3,65 mg/g. Sedangkan dari pengujian kandungan flavonoid total didapatkan hasil bahwa dalam sampel A, B, dan C berturut-turut mengandung senyawa flavonoid sebesar 291,25, 308,77 dan 34,82 mg/g. Selanjutnya dilakukan pengujian menggunakan LCMS untuk megetahui jenis senyawa flavonoid yang terkandung dalam ekstrak biji mangga arummanis. Hasil pengujian LCMS menunjukkan bahwa pada sampel A, B dan C mengandung beberapa senyawa turunan flavonoid dengan kadar yang berbeda-beda. Aktivitas antioksidan senyawa flavonoid yang ditunjukkan oleh nilai 𝐼𝐶50 dari sampel A, B, dan C berturut-turut adalah sebesar 38,85, 52,47, dan 165,03 µg/mL. Semaikn kecil nilai 𝐼𝐶50 maka aktivitas antioksidannya akan semakin kuat.
viii
ABSTRACT
Rodhiyah, Marathur. 2020. Isolation and Characterization Flavonoid Compounds from the Arummanis Mango Seed (Mangifera Indica L) and Activity as an Antioxidant. Thesis, Department of Physics, Faculty of Mathematics and Natural Science, Universitas Negeri Semarang. Supervisor Dr. Masturi, M.Si.
Key words: Arummanis mango seed, phenol, flavonoid, antioxidant.
Mango grows in various countries in the world, especially in tropical climates. Arummanis is one kind of mango that grows in Indonesia. The previous research proved that in arummanis mango’s seed contains flavonoid compound. Flavonoid was powerful antioxidant have ability to ward off free radical. The research aims to isolate and characterize the flavonoids compounds from the arum manis mango seed and the testing of their activities as antioxidants. Mango seed extracted using reflux method. Before isolation process, mango seed extract was tested using Thin Layer Chromatograph (TLC) to find the solvent can separated flavonoid compound of mango seed extract optimally. Mango seed extract was isolated using Gravity Coloumn Chromatograph (GCC) method. The result of TLC show that flavonoid can separated optimally when using silent phase silica gel60 and mobile phase solvent toluene: ethyl acetate: formic acid: methanol with ratio 6: 3: 1: 0,6. That solvents used to isolated the flavonoid using GCC method. The separating using GCC method produce 3 fractions with the value of RF were 0,48, 0,44 and 0,42. The samples was characterized using FTIR, LCMS and UV-Vis. The result of FTIR show that the samples contains phenol and flavonoid compound that was proved by founding functional group of O-H and C=O. O-H group of sample A, B and C showed by wave number 1620,27, 1598,39, dan 1625,17 𝑐𝑚−1. The result of FTIR was supported with the tested of Total Phenol Content and Total Flavonoid Content using UV-Vis. The TPC testing show that sample A, B and C contains 18,58, 20,35, and 3,65 mg/g of phenol compound. Whereas the TFC testing show that sample A, B and C contains 291,25, 308,77 and 34,82 mg/g of flavonoid compound. The LCMS result show that in sample A, B and C contains various derifative flavonoid compound with the different content. The antioxidant activity was showed by 𝐼𝐶50 value of sample A, B and C were 38,85, 52,47, and 165,03 µg/ml. The most little the number of 𝐼𝐶50 show the strongest the antioxidant activity.
ix
DAFTAR ISI
PERSETUJUAN PEMBIMBING... Error! Bookmark not defined.
PERNYATAAN ... iii
PENGESAHAN ... Error! Bookmark not defined. MOTTO DAN PERSEMBAHAN ... v
PRAKATA ... vi
ABSTRAK ... vii
ABSTRACT ... viii
DAFTAR ISI ... ix
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
BAB I ... 1 PENDAHULUAN ... 1 1.1 Latar Belakang... 1 1.2 Rumusan masalah ... 2 1.3 Tujuan penelitian ... 2 1.4 Manfaat penelitian ... 2 1.5 Batasan masalah ... 2 1.6 Sistematika Penulisan ... 2 BAB II ... 4 TINJAUAN PUSTAKA ... 4
2.1 Mangga Arum Manis (Mangifera indica L) ... 4
2.2 Flavonoid ... 5
2.3 Ekstraksi ... 6
2.4 Kromatografi Lapis Tipis ... 7
2.5 Kolom Kromatografi ... 8
2.6 Antioksidan ... 8
BAB III ... 10
METODE PENELITIAN ... 10
x
3.2 Alat dan Bahan ... 10
3.2.1 Alat ... 10
3.2.2 Bahan... 10
3.3 Prosedur Penelitian ... 10
3.3.1 Preparasi sampel ... 10
3.3.2 Proses Ekstraksi dan Evaporasi ... 11
3.3.3 Kromatografi Lapis Tipis ... 11
3.3.4 Kromatografi Kolom Gravitasi ... 12
3.3.5 Penentuan Kandungan Fenol total ... 12
3.3.6 Penentuan Kandungan Flavonoid total ... 12
3.3.7 Pengujian Antioksidan ... 13
3.3.8 Karakterisasi ... 13
BAB IV ... 15
HASIL DAN PEMBAHASAN ... 15
4.1 Kromatografi Lapis Tipis ... 15
4.2 Kromatografi Kolom Gravitasi ... 17
4.3 Hasil Uji FTIR ... 18
4.4 Hasil Uji UV-Vis ... 20
4.4.1 Kandungan Fenol Total ... 20
4.4.2 Kandungan Flavonoid Total ... 21
4.5 Hasil Uji LC-MS ... 23 4.6 Aktivitas Antioksidan ... 37 BAB V ... 41 PENUTUP ... 41 5.1 Kesimpulan... 41 5.2 Saran ... 41 DAFTAR PUSTAKA ... 42 LAMPIRAN ... 46
xi
DAFTAR TABEL
Tabel 4.1 Interpretasi spectra IR ……….19
Tabel 4.2 Kadar fenol masing-masing sampel……….21
Tabel 4.3 Kadar flavonoid masing-masing sampel…….……….22
Tabel 4.4 Interpretasi senyawa dan kadar sampel A…………..………..27
Tabel 4.5 Interpretasi senyawa dan kadar sampel B ………….………..32
Tabel 4.6 Interpretasi senyawa dan kadar sampel C ………….………..36
Tabel 4.7 Nilai IC50 masing-masig sampel……...………..39
xii
DAFTAR GAMBAR
Gambar 2.1 Mangga arummanis (Mangifera indica L)……….4
Gambar 2.2 Biji mangga arummanis (Mangifera indica L)……….…….5
Gambar 2.3 Struktur kimia flavonoid……….6
Gambar 2.4 Plat Kromatografi Lapis Tipis (KLT)………7
Gambar 4.1 KLT menggunakan 4 pelarut………..15
Gambar 4.2 Hasil KLT sampel dengan pembanding……….16
Gambar 4.3 Sampel hasil kromatografi kolom gravitasi……...……….17
Gambar 4.4 Spektra IR………..……….18
Gambar 4.5 Kurva kalibrasi standar asam galat……….20
Gambar 4.6 Kurva kalibrasi standar kuersetin………..……….22
Gambar 4.7 Komatogram sampel A………..……….23
Gambar 4.8 Struktur dan nama senyawa puncak pertama sampel A……….24
Gambar 4.9 Struktur dan nama senyawa puncak kedua sampel A…...………….24
Gambar 4.10 Struktur dan nama senyawa puncak ketiga sampel A………..25
Gambar 4.11 Struktur dan nama senyawa puncak keempat sampel A…………..26
Gambar 4.12 Struktur dan nama senyawa puncak kelima sampel A……….26
Gambar 4.13 Struktur dan nama senyawa puncak keenam sampel A…………...27
Gambar 4.14 Komatogram sampel B…………....……….28
Gambar 4.15 Struktur dan nama senyawa puncak pertama sampel B…………...29
xiii
Gambar 4.17 Struktur dan nama senyawa puncak ketiga sampel B………..30
Gambar 4.18 Struktur dan nama senyawa puncak keempat sampel B…………..31
Gambar 4.19 Struktur dan nama senyawa puncak kelima sampel B……….31
Gambar 4.20 Struktur dan nama senyawa puncak keenam sampel B………32
Gambar 4.21 Komatogram sampel C…..………33
Gambar 4.22 Struktur dan nama senyawa puncak pertama sampel C………34
Gambar 4.23 Struktur dan nama senyawa puncak kedua sampel C………34
Gambar 4.24 Struktur dan nama senyawa puncak ketiga sampel C………...35
Gambar 4.25 Struktur dan nama senyawa puncak keempat sampel C…………...36
Gambar 4.26 Kurva satndar baku DPPH untuk sampel A……...……….…37
Gambar 4.27 Kurva satndar baku DPPH untuk sampel B ……….…38
1
BAB I
PENDAHULUAN
1.1 Latar Belakang
Mangga (Mangifera indicaL) merupakan buah yang memiliki kandungan air yang cukup banyak dan termasuk dalam golonganAnacardiaciaea. Mangga tumbuh diberbagai Negara di dunia, terutama di daerah beriklim tropis (Masud Parvez, 2016). Produksi mangga di Asia sudah meningkat sekitar 15% dari 2009 hingga 2011, sekitar 30,2 juta ton dalam komoditas pasar internasional (Santhirasegaram et al, 2015), di Indonesia sendiri produksi mangga dari tahun 2015-2019 sekitar 145 ribu ton (Kementrian Pertanian, 2019). Buah mangga memiliki manfaat yang besar ketika dikonsumsi oleh tubuh, mangga sangat kaya akan vitamin A dan C. Selain itu dalam buah mangga juga terkandung sejumlah vitamin dan mineral lain seperti riboflavin, niasin, kalsium, fosfor dan zat besi(Kabiru et al, 2013). Akan tetapi disamping manfaat yang besar tersebut ada permasalahan yang perlu diatasi yaitu limbah yang dihasilkan dari mangga itu sendiri. Limbah yang dihasilkan dari mangga antara lain yaitu daun,batang, kulit, dan biji.Menurut penelitian yang telah dilakukan sebelumnya dilaporkan bahwa dalam kulit mangga mengandung senyawa-senyawa seperti polifenol,karotenoid,enzim dan serat makanan (Ajila et al, 2007), selain itu juga diaplikasikan pada bidang biomedical seperti pengobatan penyakit kelebihan logam besi (Pardo-Andreu et al, 2008), dan aktivitas antikanker (Mertens-Talcott et al, 2003). Sedangkanbiji buah mangga diproduksi sebagai limbah dan saat ini limbah biji terebut masih sedikit aplikasinya dalam bidang komersial maupun biomedical. Oleh karena itu, biji buah mangga hanya menjadi masalah lingkungan saja.
Flavonoid adalah antioksidan kuat yang memiliki kemampuan untuk menangkal radikal bebas,transisi ion logam dan menghambat enzim yang bertanggung jawab atas inisiasi reaksi berantai ini (Rzepecka-stojko et al, 2018). Flavonoid adalah suatu kelompok senyawa fenol terbesar ditemukan di alam yang menunjukkan aktivitas biokimia misalnya antioksidan, antivirus, antibakteri, dan anti kanker (Fowler & Koffas,2009). Berdasarkan uraian diatas maka penilitian ini
2
dilakukan untuk mengisolasi dan mengkarakterisasi senyawa flavonoid dari biji mangga arummanis serta pengujian aktivitasnya sebagai antioksidan.
1.2 Rumusan masalah
Berdasarkan uraian pada latar belakang dari penelitian ini,rumusan masalah yang diajukan dalam penelitian ini adalah
1. Bagaimana proses isolasi senyawa flavonoid dari biji mangga arum manis? 2. Bagaimana aktivitas antioksidan dari senyawa flavonoid?
1.3 Tujuan penelitian
Berdasarkan rumusan masalah tersebut, penelitian dilakukan dengan tujuan
1. Memisahkan senyawa flavonoid biji mangga arummanis. 2. Mengetahui aktivitas antioksidan senyawa flavonoid.
1.4 Manfaat penelitian
Manfaat dilakukan penelitian ini yaitu:
1. Memberikan informasi tentang metode isolasi biji mangga arum manis sebagai salah satu bentuk pemanfaatan material biowate.
2. Memberikan informasi tentang aktivitas senyawa flavonoid dari biji buah mangga arum manis sebagai antioksidan dalam rangka peningkatan nilai tambah material biowaste yang melimpah di Indonesia.
1.5 Batasan masalah
Batasan masalah dalam peneitian ini yaitu biji yang digunakan pada penelitian ini dari satu jenis buah mangga yaitu mangga arumanis.
1.6 Sistematika Penulisan
Penulisan skripsi dibagi menjadi tiga bagian utama, yaitu bagian pendahuluan skripsi, bagian isi skripsi, dan bagian akhir skripsi.
1. Bagian pendahuluan skripsi, terdiri dari halaman judul, abstrak, halaman pengesahan, motto dan persembahan, kata pengantar, daftar isi, daftar gambar, daftar tabel, dan daftar lampiran.
3
2. Bagian isi skripsi, terdiri atas lima bab yang meliputi :
BAB 1. Pendahuluan, berisi latar belakang, rumusan permasalahan, batasan permasalahan, tujuan penelitian, manfaat penelitian, dan sistematika skripsi. BAB 2. Kajian pustaka, berisi teori-teori pendukung penelitian.
BAB 3. Metodologi penelitian, berisi tempat pelaksanaan penelitian, alat dan bahan yang digunakan, langkah kerja, pengujian, dan karakterisasi yang dilakukan dalam penelitian.
BAB 4. Hasil penelitian dan pembahasan, dalam bab ini dibahas tentang hasil-hasil penelitian yang telah dilakukan.
BAB 5. Penutup, yang berisi tentang simpulan hasil penelitian yang telah dilakukan serta saran-saran yang berkaitan dengan hasil penelitian.
3. Bagian akhir skripsi memuat referensi yang digunakan sebagai acuan dari penulisan skripsi dan lampiran-lampiran penelitian.
4
BAB II
TINJAUAN PUSTAKA
2.1Mangga Arum Manis (Mangifera indica L)
Mangga merupakan salah satu jenis buah tropis yang menduduki urutan ke 5 dalam total produksi dunia (Kabiru et al, 2013). Mangga termasuk salah satu jenis buah musiman yang menjadi komoditas andalan sektor pertanian dan dikonsumsi secara local di Indonesia. Terdapat berbagai varietas mangga yang tumbuh di Indonesia, antara lain Mangifera indica seperti arum manis, dodol, golek, madu, manalagi, cengkir, wangi, dan Mangifera foetida yaitu kemang dan kweni. Salahsatuvarietasbuahmanggayang memiliki potensiekspor tinggiadalahmanggaarum maniskarenavarietasmangga initidakdihasilkanoleh negara penghasil dan pengekspor mangga dunia, seperti India, Meksiko, dan negaraAmerikaLatinlainnya. Berikut merupakan klasifikasi dari tanaman manga arum manis Kerajaan : Plantae Filum : Magnoliophyta Kelas : Magnoliopsida Ordo : Sapindales Famili : Anacardiaceae Genus : Mangifera Spesies : M. indica
Nama binomial : Mangifera indica L.
Mangga dengan spesies Mangifera indica varietas arummanis ditunjukkan pada Gambar 2.1.
5
Mangga mengandung senyawa fenolik seperti flavonol,xanthones dan gallotannis (Engels et al, 2010). Beberapa penelitian juga membandingkan kandungan biji buah mangga varietas India dan Indochina,didapatkan hasil bahwa masing-masing mengandung 6.00 dan 4.95% protein, 5.09 dan 10.36% air, 11.00 dan 15% lemak, 74.41 dan 64.23% karbohidrat, 4.33 dan 2.47% serat, 8.00 dan 12.00% asam lemak, dan 1.20 dan 1.30% abu (Okpala & Gibson, 2013). Biji mangga arummanis ditunjukkan pada Gambar 2.2.
Gambar 2.2 Biji mangga arum manis (Mangifera indica L)
2.2Flavonoid
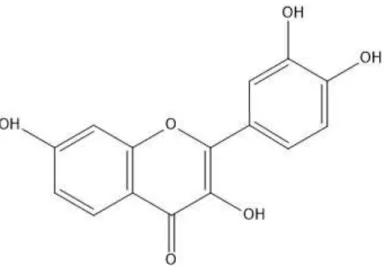
Flavonoid adalah kelas polifenol tumbuhan yang dapat dikonsumsi untukdiet manusia melalui sayuran, buah-buahan, sereal, rempah-rempah, dan produk nabati lainnya. Ilmu epidemiologis menunjukkan bahwa semakin tinggi asupan makanan dan minuman yang banyak mengandung flavonoid berkaitan dengan hasil kognitif yang lebih baik pada individu usia di atas 65 tahun, termasuk penurunan kognitif (Letenneur et al, 2007), mengurangi risiko demensia (Commenges et al, 2000) dan kemampuan kognitif yang lebih baik (Christian et al, 2009). Flavonoid adalah polifenol yang mengandung lima belas atom karbon. Kerangka karbon terdiri dari dua cincin benzene yang dihubungkan oleh tiga rantai karbon pendek (C6-C3-C6). Salah satu karbon dalam rantai ini terhubung ke atom karbon di salah stau cincin benzene, baik melalui jembatan oksigen atau langsung, yang menghasilkan cincin tengah heterosiklik ketiga. Kelas flavonoid yaitu antara lain flavonol, flavon, flavonol, isoflavonoid, dan
6
antosianidin. Kelimanya berbeda dalam dalam tingkat oksidasi dan saturasi cincin (Rzepecka-stojko et al, 2018). Struktur flavonoid ditunjukkan pada Gambar 2.3.
Gambar 2.3 Struktur kimia flavonoid
2.3Ekstraksi
Ekstraksi adalah suatu proses pemisahan kandungan kimia dari jaringan tumbuhan ataupun hewan dengan menggunakan penyari tertentu (Simanjuntak,2008). Pengambilan bahan aktif dari suatu tanaman, dapat dilakukan dengan ekstraksi. Proses ekstraksi ini menyebabkan bahan aktif akan terlarut oleh zat penyari yang sesuai sifat kepolarannya. Metode ekstraksi dipilih berdasarkan beberapa faktor seperti sifat dari bahan mentah obat, daya penyesuaian dengan tiap macam metode ekstraksi dan kepentingan dalam memperoleh ekstrak yang sempurna atau mendekati sempurna (Sjahid, 2008).
a. Meserasi
Maserasi merupakan cara ekstraksi yang paling sederhana. Bahan simplisia yang dihaluskan sesuai dengan syarat farmakope (umumnya terpotongpotong atau berupa serbuk kasar) disatukan dengan bahan pengekstraksi. Selanjutnya rendaman tersebut disimpan terlindung dari cahaya langsung (mencegah reaksi yang dikatalisis cahaya atau perubahan warna) dan dikocok kembali. Mesrasi biasanya dilakukan 1x24 jam. Metode ekstraksi maserasi digunakan untuk mengekstrak suatu komponen kimia yang tahan panas maupun tidak.
7
Kekurangan dari metode ini, yaitu diperlukan waktu yang lama dan banyak menggunakan larutan pengekstrak(Gafur et al, 2012).
b. Refluks
Metode Refluks merupakan metode ektraksi cara panas (membutuhkan pemanasan pada prosesnya), secara umum pengertian refluks sendiri adalah ekstraksi dengan pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut yang ralatif konstan dengan adanya pendingin balik. Ekstraksi dengan cara ini pada dasarnya adalah ekstraksi berkesinambungan.
2.4 Kromatografi Lapis Tipis
Kromatografi lapis tipis merupakan jenis kromatografi cair-cair dimana fase diamnya berupa lapis tipis air yang terserap oleh lembaran kaca atau plastik yang dilapisi dengan lapisan tipis adsorben. Adsorben KLT dapat berupa alumina, silika gel, selulosa atau materi lainnya. Pemisahan kromatografi lapis tipis lebih akurat dibanding kromatografi kertas. Hal ini disebabkan karena kromatografi lapis tipis bersifat boleh ulang (reprodusible). Metode ini sangat cepat karena dapat dilakukan kurang dari satu hari dan dapat mendeteksi senyawa yang mempunyai konsentrasi rendah karena noda yang dihasilkan sangat rapat (Latifah, 2015).
Harga Rf merupakan parameter karakteristik kromatografi kertas dan kromatografi lapis tipis. Harga Rf (Rate of Low) didefinisikan sebagai perbandingan antara jarak senyawa dari titik awal dan jarak tepi muka pelarut dari titik awal. Plat KLT ditunjukkan pada Gambar 2.4.
8
Gambar2.4 Plat Kromatografi Lapis Tipis (KLT)
Rf = a
b
harga Rf berkisar antara 0,1 – 0,99 dan dipengaruhi oleh beberapa factor antara lain:
1. Ukuran partikel lapisan penyerap 2. Derajat keaktifan lapisan penyerap 3. Kemurnian pelarut
4. Kejenuhan ruang elusi 5. Ketebalan lapisan pelarut
2.5Kolom Kromatografi
Kromatografi kolom merupakan suatu bentuk kromatografi serapan (adsorption chromatography). Kromatografi kolom disebut juga kromatografi elusi (elution chromatography) karena senyawa-senyawa yang terpisah dielusikan dari dalam kolom. Prinsip kromatografi kolom sama dengan prinsip KLT yaitu senyawa senyawa dalam campuran dipisahkan oleh partisi yaitu antara padatan penyerap yang berfungsi sebagai fasa diam dan pelarut sebagai fasa bergerak yang mengalir melewati fase diam.
2.6Antioksidan
Antioksidan adalah vitamin, mineral, atau sejenis nutrisi yang berperan dalam menjaga dan memperbaiki sel-sel tubuh yang rusak akibat radikal bebas.Radikal bebas merupakan salah satu bentuk senyawa reaktif, yang memiliki elektron yang tidak berpasangan di kulit terluarnya. Radikal bebas dapat berasal dari polusi, debu maupun diproduksi secara kontinyu sebagai konsekuensi dari metabolism normal yang dapat berdampak buruk bagi tubuh. Antioksidan dapat melawan pengaruh bahaya dari radikal bebas atau Reactive OxygenSpecies(ROS) yang terbentuk sebagai hasil dari metabolism oksidatif yaitu hasil dari reaksireaksi kimia dan proses metabolic yang terjadi dalam tubuh. Antioksidan dapat
9
diklasifikasikan menjadi dua jenis yaitu antioksidan sintetik dan antioksidan alami. Antioksidan sintetik diperoleh dari hasil sintesa reaksi kimia, sedangkan antioksidan alami diperoleh dari hasil ekstraksi bahan-bahan alami diantaranya yaitu tokoferol, lesitin, fosfatida, sesamol, gosipol, karoten, asam tanat, gallic acid (senyawa phenolic), ferulic acid (senyawa phenolic), quercetin (flavonoid) dan sebagainya (Ni Nyoman & Desmira, 2015)
41
BAB V PENUTUP
5.1Kesimpulan
1. Senyawa flavonoid telah berhasil dipisahkan menjadi tiga sampel dengan masing-masing kadar flavonoidnya sebesar 291,25, 308,77 dan 34, 82 mg/g. 2. Aktivitas antioksidan yang dinyatakan dalam nilai 𝐼𝐶50 masing-masing ketiga
sampel tersebut adalah sebesar 38,85, 52,47 dan 165,03 µg/mL 5.2Saran
1. Perlu dilakukan penelitian pengaplikasian senyawa flavonoid
42
DAFTAR PUSTAKA
Ajila, C. M., Naidu, K. A., Bhat, S. G., & Rao, U. J. S. P. (2007). Bioactive compounds and antioxidant potential of mango peel extract. Food Chemistry, 105(3), 982–988. https://doi.org/10.1016/j.foodchem.2007.04.052
Ashok kumar, R., & Ramaswamy, M. (2014). Phytochemical screening by FTIR spectroscopic analysis of leaf extracts of selected Indian Medicinal plants. Int.J.Curr.Microbiol.App.Sci, 3(1), 395–406.
Christian, a, Grethe, S., & Harald, a. (2009). Intake of Flavonoid-Rich Wine , Tea , and Chocolate by Elderly Men and ... J Nutr, 139(1), 120–127. https://doi.org/10.3945/jn.108.095182.oxidant
Commenges, D., Scotet, V., Renaud, S., Jacqmin-Gadda, H., Barberger-Gateau, P., & Dartigues, J. F. (2000). Intake of flavonoids and risk of dementia. European
Journal of Epidemiology, 16(4), 357–363.
https://doi.org/10.1023/A:1007614613771
Engels, C., Gänzle, M. G., & Schieber, A. (2010). Fractionation of gallotann ins from mango (Mangifera indica L.) kernels by high-speed counter-current chromatography and determination of their antibacterial activity. Journal of Agricultural and Food Chemistry, 58(2), 775–780. https://doi.org/10.1021/jf903252t
Fowler, Z. L., & Koffas, M. A. G. (2009). Biosynthesis and biotechnological production of flavanones: Current state and perspectives. Applied Microbiology and Biotechnology, 83(5), 799–808. https://doi.org/10.1007/s00253-009-2039-z
Gafur, M. A., Isa, I., & Bialangi, N. (2012). ISOLASI DAN IDENTIFIKASI SENYAWA FLAVONOID DARI DAUN JAMBLANG (Syzygium cumini). Jurusan Kimia Fakultas Mipa Universitas Negeri Gorontalo, 11.
43
Kabiru, A. A., Joshua, A. A., & Raji, A. O. (2013). Drying kinetics of mango (Mangifera Indica). International Journal of Research and Reviews in Applied Sciences, 15(April), 41–50.
Letenneur, L., Proust-Lima, C., Le Gouge, A., Dartigues, J. F., & Barberger-Gateau, P. (2007). Flavonoid intake and cognitive decline over a 10-year period. American Journal of Epidemiology, 165(12), 1364–1371. https://doi.org/10.1093/aje/kwm036
Masturi, Alighiri, D., Nuzulina, K., Rodhiyah, M., & Drastisianti, A. (2019). Optimization of condition extraction in quantification of total flavonoid content in the seeds of the Arummanis (Mangifera indica L.) mango from Indonesia. Journal of Physics: Conference Series, 1321(2). https://doi.org/10.1088/1742-6596/1321/2/022041
Masud Parvez, G., & Masud Parvez, C. G. (2016). Pharmacological Activities of Mango (Mangifera Indica): A Review. Journal of Pharmacognosy and Phytochemistry JPP, 1(53), 1–7.
Mertens-Talcott, S. U., Talcott, S. T., & Percival, S. S. (2003). Low Concentrations of Quercetin and Ellagic Acid Synergistically Influence Proliferation, Cytotoxicity and Apoptosis in MOLT-4 Human Leukemia Cells–. The Journal of Nutrition, 133(8), 2669–2674. https://doi.org/10.1093/jn/133.8.2669
Molyneux, P. (2004). The Use of the Stable Free Radical Diphenylpicryl-hydrazyl (DPPH) for Estimating Antioxidant Activity. Songklanakarin Journal of Science
and Technology, 26(December 2003), 211–219.
https://doi.org/10.1287/isre.6.2.144
Noh, C. H. C., Azmin, N. F. M., Amid, A., & Asnawi, A. L. (2017). Algorithm for rapid identification of flavonoids classes. International Food Research Journal, 24(December), 410–415.
44
Okpala, L. C., & Gibson-Umeh, G. I. (2013). Physicochemical Properties of Mango Seed Flour. Nigerian Food Journal, 31(1), 23–27. https://doi.org/10.1016/s0189-7241(15)30052-7
Pardo-Andreu, G. L., Barrios, M. F., Curti, C., Hernández, I., Merino, N., Lemus, Y., … Delgado, R. (2008). Protective effects of Mangifera indica L extract (Vimang), and its major component mangiferin, on iron-induced oxidative damage to rat serum and liver. Pharmacological Research, 57(1), 79–86. https://doi.org/10.1016/j.phrs.2007.12.004
Park, Y. S., Jung, S. T., Kang, S. G., Heo, B. G., Arancibia-Avila, P., Toledo, F., … Gorinstein, S. (2008). Antioxidants and proteins in ethylene-treated kiwifruits.
Food Chemistry, 107(2), 640–648.
https://doi.org/10.1016/j.foodchem.2007.08.070
Ribeiro, S. M. R., Barbosa, L. C. A., Queiroz, J. H., Knödler, M., & Schieber, A. (2008). Phenolic compounds and antioxidant capacity of Brazilian mango (Mangifera indica L.) varieties. Food Chemistry, 110(3), 620–626. https://doi.org/10.1016/j.foodchem.2008.02.067
Rzepecka-stojko, A., Kubina, R., Iriti, M., Wojtyczka, R. D., Buszman, E., & Stojko, J. (n.d.). comparative study. (21).
Santhirasegaram, V., Razali, Z., & Somasundram, C. (2015). Effects of sonication and ultraviolet-C treatment as a hurdle concept on quality attributes of Chokanan mango (Mangifera indica L.) juice. Food Science and Technology International, 21(3), 232–241. https://doi.org/10.1177/1082013214528188
Senthilkumar, S. R., Sivakumar, T., Arulmozhi, K. T., & Mythili, N. (2017). FT-IR IR analysis and correlation studies on the antioxidant activity , total phenolics and total flavonoids of Indian commercial teas ( Camellia sinensis L .) - A novel approach. International Research Journal of International Science Community Association International Research Journal of Biological Sciences Int. Res. J.
45
Biological Sci, 6(3), 1–7.
Sharma, V., & Janmeda, P. (2017). Extraction, isolation and identification of flavonoid from Euphorbia neriifolia leaves. Arabian Journal of Chemistry, 10(4), 509–514. https://doi.org/10.1016/j.arabjc.2014.08.019
Singh, R., & Mendhulkar, V. D. (2015). FTIR studies and spectrophotometric analysis of natural antioxidants, polyphenols and flavonoids in Abutilon indicum (Linn) Sweet leaf extract. Journal of Chemical and Pharmaceutical Research,
7(6), 205–211. Retrieved from
https://pdfs.semanticscholar.org/b5ca/0c44315041dfc93c6298ed67fbfe3ed8d4a4 .pdf
Sjahid, Landyyun R. 2008. Isolasi dan Identifikasi Flavonoid dar Daun Dewandru (Eugenia uniflora L.). Surakarta : Fakultas Farmasi Universitas Muhammadiyah Surakarta.
Strategis, R., & Pertanian, K. (2019). 2015 - 2019.
Trifunschi, S., Munteanu, M. F., Agotici, V., Pintea, S., & Gligor, R. (2015). Determination of Flavonoid and Polyphenol Compounds in Viscum Album and Allium Sativum Extracts. International Current Pharmaceutical Journal, 4(5), 382–385. https://doi.org/10.3329/icpj.v4i5.22861
Yuliani, Ni Nyoman & Dienima, Desmira Primanty. 2015 .Uji Aktivitas Antioksidan Infusa Daun Kelor (Moringa oleifera, Lamk) dengan Metode DPPH 1,1-diphenyl-2-picrylhydrazyl (DPPH). Jurna Info Kesehatan ,Vol 14, Nomor 2 Desember 2015.