PENINGKATAN KETAHANAN KOROSI TEMPERATUR TINGGI BAJA
KARBON RENDAH (AISI 1020) DENGAN PELAPISAN CELUP PANAS
ALUMINIUM UNTUK APLIKASI
PADA PIPA GAS PANAS BUMI
Mohammad Badaruddin 1), Suharno 2)
1)Jurusan Teknik Mesin, Fakultas Teknik Universitas Lampung 2)Jurusan Teknik Geofisika, Fakultas Teknik Universitas Lampung
ABSTRAK
Baja AISI 1020 telah dilapisi dengan mencelupkan ke dalam bak Al-cair pada temperatur 700 C selama 16 detik. Lapisan yang terbentuk setelah proses pembuatan baja lapis Al-celup panas adalah: Al dengan sedikit elemen Fe, FeAl3, dan Fe2Al5. Baja Al-coated dioksidasi pada temperatur 700 °C selama periode paling lama 64 jam dalam lingkungan udara, NaCl, dan Na2SO4. Keberadaan deposit NaCl maupun Na2SO4 pada permukaan spesimen dapat mempercepat proses korosi baja Al-coated. Pembentukan gas metal-klorida yang mudah menguap, menjadi pemicu laju korosi yang dipercepat. Sedangkan Al-sulfida yang terlarut dalam lapisan Al2O3 dipercaya sebagai pemicu peningkatan laju oksidasi baja Al-coated dalam Na2SO4. Pembentukan lapisan aluminida pada permukaan baja dapat menjadi suplai Al untuk membentuk lapisan protektif Al2O3yang dapat memperlambat difusi spesies gas oksidan (O2, Cl2, SO2dan SO3)
Kata Kunci: Baja AISI 1020, Al-celup panas, metal-klorida, metal sufida, Al2O3
I. PENDAHULUAN
Baja AISI 1020, yang relatif murah dan banyak diproduksi untuk komponen sistem perpipaan bertekanan rendah. Proses perancangan sistem perpipaan untuk saluran uap panas dari sumur-sumur produksi harus mendapat perhatian khusus dari sisi ketahanan oksidasi/korosi dan kekuatan bahan yang digunakan selama aplikasi pada temperatur tinggi dalam lingkungan yang mengandung gas-gas korosif. Hal ini perlu dilakukan agar diperoleh rancangan yang optimal baik dari sisi operasional maupun dari sisi keamanannya [1].
Sudah dikenal dengan baik bahwa keberadaan gas korosif klorin dan sulfur dalam atmosfer udara meningkatkan laju korosi baja dan paduanya. Beberapa penelitian sebelumnya menunjukan bahwa gas klorin dan sulfur di dalam atmosfer berkontribusi sangat besar terhadap korosi temperatur tinggi [2,3]. Salah satu metode untuk meningkatkan ketahanan baja dan paduanya terhadap serangan korosi klorin dan sulfur pada temperatur tinggi adalah dengan metode pelapisan Al-celup panas. Metode ini lebih murah dan lebih efektif dibandingkan dengan metode lainya [3]. Oleh karena itu, pelapisan dengan Al-celup panas lebih tepat dilakukan pada baja AISI 1020, untuk menurunkan ongkos produksi dan perawatan dalam memanfaatkan uap panas sebagai sumber pembangkit
energi listrik. Lapisan aluminium yang terbentuk pada permukaan baja dapat menjadi lapisan pelindung selama aplikasi pada temperatur tinggi dengan membentuk lapisan protektif tipis Al2O3[4].
Penelitian ini fokus pada oksidasi baja AISI 1020 yang dilapisi Al-celup panas pada temperatur 700 C selama 64 jam dalam udara, NaCl dan Na2SO4. Temperatur ini
merupakan batas temperatur tinggi yang mungkin dialami oleh komponen baja dari sistem perpipaan. Laju reaksi, morfologi produk korosi dan perubahan komposisi yang terjadi pada baja Al-celup panas dianalisis untuk memberikan wawasan tentang mekanisme korosi.
II. METODOLOGI
Bahan yang digunakan adalah baja AISI 1020. Spesimen dibuat dengan ukuran 20 mm × 10 mm × 2 mm. Spesimen dilobangi dengan mata bor diameter 1 mm untuk menggantungnya pada saat proses pelapisan. Semua permukaan spesimen diamplas dengan kertas amplas mulai 200 sampai 1200. Kemudian dicuci dengan aceton dan ethanol, lalu dikeringkan dengan pengering udara. Sebelum proses pelapisan Al-celup panas. Semua spesimen dibersihkan dengan menggunakan larutan kimia 5%NaOH, 15%H3PO4 kemudian dicelupkan dalam Al-fluks. Proses
pelapisan baja dilakukan dengan mencelupkan ke dalam bak Al-cair pada temperatur 700 °C selama 16 detik.
Deposit NaCl atau Na2SO4 diperoleh dengan
menyemprotkan larutan 20% NaCl maupun Na2SO4 ke
permukaan spesimen yang diletakan di atas hot plate pada temperatur 200 C selama 10 detik. Setelah deposit terbentuk dan ditimbang, kemudian spesimen dimasukan ke krusibel 15 mL untuk diekpos dalam furnace pada temperatur 700 C selama periode waktu 164 jam. Plot kurva penambahan berat (weight gain) versus oxidation time (h) diperoleh untuk memprediksi ketahanan oksidasi bare steel dan Al-coated pada temperatur 700 °C. Hanya morfologi, mikrostruktur dan komposisi kimia dari spesimen Al-coated yang diobservasi menggunakan optical microscope (OM), scanning electron microscopy (SEM) dan electron dispersive spectroscopy (EDS). Fasa-fasa yang terbentuk dianalisis dengan X-ray diffraction (XRD).
III. HASIL DAN PEMBAHASAN
1. Kinetika oksidasi
Data penambahan berat (weight gain) bare steel dan Al-coated diplot pada Gambar 1. Plot linier dari kurva weight gain versus oxidation time menunjukan perilaku oksidasi bare steel, mengikuti tren parabolik. Peningkatan laju oksidasi mengikuti pertambahan waktu oksidasi. Gambar 1 menunjukan dengan jelas peningkatan ketahanan oksidasi Al-coated dibandingkan dengan bare steel yang dioksidasi dalam lingkungan udara baisa, NaCl dan Na2SO4.
Bila bare steel dioksidasi dalam NaCl dan Na2SO4,
masing-masing weight gain meningkat sebesar 1.5 dan 1.7 kali dibandingkan dengan bare steel yang dioksidasi dalam udara biasa selama 49 jam.
Nilai weight gain yang lebih besar ditemukan pada spesimen Al-coated yang dioksidasi dalam NaCl daripada Al-coated yang dioksidasi dalam Na2SO4 selama 64 jam.
Nilai weight gain yang paling rendah ditemukan pada spesimen Al-coated yang dioksidasi dalam udara biasa, seperti yang diharapkan.
Pada Gambar 1 juga dapat dilihat bahwa pelapisan Al-celup panas sangat signifikan dalam melindungi substrat baja dari serangan korosi klorin maupun sulfur yang ada dalam lingkungan atmosfer. Selama 64 jam oksidasi, ketahanan baja Al-coated yang diekpos dalam NaCl dapat ditingkatkan sampai faktor 1.3. Sedangkan baja Al-coated yang diekpos dalam Na2SO4, ketahanan korosinya dapat
ditingkatkan sampai faktor 1.7. Lapisan intermetalik FeAl yang terbentuk pada permukaan baja memainkan peranan penting dalam menyuplai pembentukan lapisan protektif alumina (Al2O3) yang dapat berfungsi memperlambat difusi
ke dalam spesies oksidan gas (O, Cl dan S) dan difusi keluar dari penguapan aluminium klorida [5].
.
Gambar 1. Plot linier kurva weight gain vs. oxidation time
Untuk mengetahui secara jelas perilaku oksidasi bare steel dan Al-coated, plot kurva weight gain versus square root time (t1/2) dilakukan untuk menentukan laju kinetika
oksidasi. Pierragi [6] menyarankan plot kinetik data (W/Ao)
= kp.tn untuk menentukan laju kinetika korosi (kp) secara
akurat. Berdasarkan hasil regresi linier, seperti ditampilkan pada Gambar 2 diperoleh nilai laju kinetika oksidasi (kp)
untuk bare steel, yaitu: 8.456 × 1010g2cm4s1dan baja yang
dilapisi Al (Al-coated) adalah 1.073 × 1012g2cm4s1.
Gambar 2. Plot parabolik kurva weight gain vs. t1/2
Nilai kp Al-coated menunjukan dua order lebih rendah
daripada bare steel untuk oksidasi dalam udara biasa. Ini mengindikasikan bahwa ketahanan oksidasi baja AISI 1020 dapat ditingkatkan secara signifikan melalui Al-celup panas dalam lingkungan udara. Hasil lengkap perhitungan nilai kp
untuk bare steel dan Al-coated ditabulasikan pada Tabel 1.
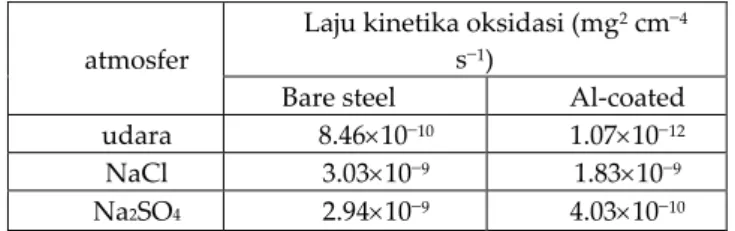
Tabel 1. Laju kinetika oksidasi bare steel dan Al-coated yang dioksidasi pada 700 C dalam lingkungan yang berbeda.
atmosfer
Laju kinetika oksidasi (mg2cm4
s1)
Bare steel Al-coated udara 8.461010 1.071012
NaCl 3.03109 1.83109
Ada perbedaan substansi weight gain pada spesimen Al-coated yang dioksidasi dalam NaCl maupun Na2SO4. Laju
korosi untuk baja Al-coated dalam NaCl ditemukan pada 4 jam pertama lebih cepat (kp= 6.36 109mg2cm4s1), dan
selama 9 jam, laju oksidasi mengalami stagnasi, kemudian setelah 9 jam sampai 64 jam laju korosinya adalah 1.83109
mg2 cm4 s1. Sedangkan laju korosi untuk spesimen
Al-coated yang dioksidasi dalam Na2SO4selama 4 jam pertama
adalah lebih lambat, yaitu kp= 2.25 1010mg2cm4s1, dan
selanjutnya oksidasi berjalan dengan cepat sampai 64 jam ekposur dengan laju oksidasi sebesar 4.03 1010 mg2 cm4
s1.
2. Mikrostruktur dan karakterisasi spesimen hasil oksidasi
SEM pada penampang permukaan spesimen Al-coated menunjukan bahwa lapisan utama terdiri dari: Al dengan sedikit Fe dan lapisan intermetalik Fe2Al5dan FeAl3(Gambar
3). XRD analisis mengkonfirmasi fasa yang terbentuk di atas substrat baja setelah proses Al-celup panas (Gambar 4). Dapat diamati pada Gambar 3 bahwa lapisan aluminida menunjukan homogen dan ikatan yang baik dengan substrat baja. Tidak ada pori dan retak yang diamati, yang menunjukan lintasan difusi Al-cair dengan Fe-padat selama proses Al-celup panas. Selain itu hasil EDS analisis mengkonfirmasi komposisi kimia lapisan FeAl3 and Fe2Al5
masing-masing adalah sekitar 80.02Al−19.8Fe dan 69.29Al−30.691Fe (at.%).
Gambar 3. BEI penampang permukaan spesimen Al-coated
Morfologi fasa Fe2Al5 menunjukan struktur kolumnar
(tongue-like morphology) yang dikaitkan dengan cacat kekosongan dari struktur Fe2Al5sekitar 30% dan oleh karena
itu, Al dapat berdifusi lebih cepat ke dalam substrat baja daripada difusi keluar Fe. Selain itu, kekosongan ini memberikan lintasan difusi yang mudah dalam arah c aksis, yang memicu pertumbuhan cepat Fe2Al5. Tebal lapisan Al
dan lapisan Fe2Al5 + FeAl3 setelah proses Al-celup panas,
masing-masing adalah sekitar 10 µm dan 75 µm.
Penampang permukaan spesimen Al-coated yang dioksidasi pada temperatur 700 C selama 125 jam dalam
lingkungan NaCl dan Na2SO4 ditunjukan pada Gambar 5.
Selama oksidasi berlangsung, transformasi fasa yang terjadi pada lapisan Al pada permukaan baja menunjukan bahwa lapisan aluminida yang terbentuk mempunyai karakteristik dan fasa intermetalik yang sama dengan baja Al-coated yang dioksidasi dalam atmosfer biasa [7]. Pada satu jam eksposur lapisan Al dan FeAl3 menghilang digantikan oleh lapisan
Fe2Al5 dan FeAl2 (Gambar 5a). Selain itu lapisan tipis FeAl
terbentuk di atas substrat baja. Pembentukan lapisan aluminida (Fe-Al) yang terbentuk karena difusi keluar atom Fe dari substrat baja dan difusi ke dalam atom-atom Al dalam periode waktu tertentu.
Gambar 4. Kurva hasil XRD analisis pada spesimen Al-coated
Ketebalan lapisan intermetalik menjadi sekitar 79 µm dengan lapisan tipis Al2O3 pada permukannya dan deposit
NaCl atau Na2SO4 yang tersisa, yang diikuti menebalnya
lapisan Fe2Al5+ FeAl2 di atas lapisan FeAl. Seiring dengan
waktu oksidasi ditingkatkan sampai 16 jam, ketebalan lapisan aluminida hampir sama untuk semua periode waktu pengujian (Gambar 5b). Namun, dominasi ketebalan lapisan Fe2Al5 + FeAl2yang terbentuk telah bertransformasi secara
bertahap untuk membentuk FeAl karena atom-atom Al berdifusi keluar. Peranan Al dalam lapisan aluminida terutama ada dua: (1) difusi keluar untuk membentuk Al2O3,
dan (2) Al berdifusi ke dalam menuju substrat baja.
Dengan demikian, FeAl terbentuk antara substrat baja dan pada antarmuka fasa Fe2Al5+ FeAl2.
Bila waktu oksidasi ditingkatkan sampai 25 jam, serangan sulfur tidak begitu parah dibanding dengan serangan klorin pada permukaan lapisan intermetalik, seperti ditunjukan pada Gambar 5c. Namun kavitasi dan pori-pori yang terbentuk dapat diamati pada permukaan terluar lapisan Fe2Al5 + FeAl2, membuktikan bahwa Al
berdifusi keluar tidak hanya membentuk Al2O3 tapi juga
membentuk Al-sulfida. Sedangkan penampang permukaan yang khas dari spesimen Al-coated yang dioksidasi dalam NaCl selama 25 jam (Gambar 5d) menunjukan bahwa lapisan Fe2Al5 + FeAl2mengalami degradasi yang terparah.
Lapisan ini kehilangan fungsi dalam menyuplai Al untuk membentuk Al2O3, dikarenakan Al mengalami reaksi
oksiklorida.
Gambar 5. OM penampang permukaan spesimen Al-coated yang dioksidasi pada 700 C (a) selama 1 jam, (b) selama 16 jam,
dan (cd) selama 25 jam.
Namun, lapisan FeAl di atas substrat baja mengambil tempat sebagai lapisan pelindung terhadap difusi oksigen maupun klorin ke dalam substrat baja, sehingga laju oksidasi dapat diturunkan. Sebagaimana telah disebutkan oleh Kobayashi [8], Fe2Al5dan FeAl2tidak stabil pada temperatur
tinggi karena mempunyai cacat kekosongan yang tinggi, sehingga Al cenderung mudah berdifusi keluar.
Observasi SEM dan EDS analisis pada spesimen yang dioksidasi selama 49 jam (Gambar 6a) menunjukan bahwa konsentrasi oksigen (0.05 wt%) dan klor (0.06 wt%) pada lokasi titik 4 lebih rendah daripada lokasi titik 1 sampai titik 3. Konsentrasi klor (0.56 wt%) tertinggi terdetek pada lokasi titik 4. Begitu juga untuk spesimen Al-coated yang dioksidasi dalan Na2SO4 selama 49 jam (Gambar 6b), Al2S3
(Al-sulfida) ditemukan terlarut dalam lapisan Al2O3,
sedangkan Fe2O3 tumbuh di atas lapisan protektif Al2O3. Dari
EDS analisis yang dilakukan pada titik 1 pada Gambar 6b, konsentrasi sulfur adalah 9.21 wt%. Sulfur tidak ditemukan pada lokasi titik 3 dan 4.
Meskipun temperatur pengujian pada penelitian ini di bawah temperatur cair NaCl (801 C) dan Na2SO4(884 C)
[9]. Namun, Gambar 1 membuktikan keberadaan deposit NaCl maupun Na2SO4 pada permukaan spesimen dapat
mempercepat proses korosi. Salah satu karakteristik oksidasi selama 4 jam pada spesimen Al-coated yang diekpos dalan NaCl, laju korosi meningkat cepat, meskipun Al2O3
terbentuk. Oleh karena itu, harus ada reaksi lain yang berkontribusi untuk menaikan weight gain.
Gambar 6. BEI penampang permukaan spesimen Al-coated yang dioksidasi pada 700 C selama 49 jam dalam (a) NaCl, dan (b)
Na2SO4(tanda panah 1-4 menunjukan lokasi EDS analisis)
Seperti ditunjukan pada Gambar 7a, dapat diamati whisker Al2O3tumbuh di atas lapisan Al2O3. Karena tekanan
partial oksigen diturunkan pada antarmuka gas/lapisan oksida-Al. Maka klorin dapat berdifusi atau masuk melalui retak atau celah yang terbentuk pada lapisan aluminida. Pada saat yang sama tekanan parsial klorin lebih tinggi, maka Al bereaksi membentuk Al-klorida yang mudah menguap, 2Al + 3Cl2(g) = 2AlCl3(g)(G700= 471.6 kJ). Fakta
bahwa titik didih AlCl3lebih rendah (182 C) [9], memaksa
AlCl3 yang berada pada atmosfer tekanan parsial oksigen
rendah, keluar menuju ke atmosfer tekanan parsial oksigen tinggi melalui pori atau retak pada lapisan Fe2Al5 + FeAl2,
yang menyebabkan whisker Al2O3 tumbuh melalui reaksi
4AlCl3(g) + 3O2(g)= 2Al2O3(s) + 6Cl2(g)(G700 = 592.4kJ). Selama
kondisi ini berlangsung, Al terus berdifusi keluar dari lapisan Fe2Al5 + FeAl2 ke antarmuka oksida-logam dan
bereaksi dengan klorin untuk membentuk senyawa yang mudah menguap, menyebabkan penipisan lapisan ini. Oleh karena itu, laju korosi turun drastis menuju kondisi stagnasi. Semakin besar zona di mana konsentrasi Al menurun, aktivitas Al pada antarmuka Al-oksida akan menurun. Pada saat yang sama kecenderungan Fe bereaksi dengan klorin akan meningkat. Oleh karena itu, reaksi cepat berikutnya adalah 2Fe + 3Cl2(g) = 2FeCl3(g) (G700 = 157.5 kJ), yang
FeCl3(g)diubah menjadi oksida besi melalui reaksi: 4FeCl3(g) +
3O2(g)= 2Fe2O3+ 6Cl2(g) (G700=109.3 kJ). Bila tekanan parsial
oksigen lebih tinggi dari tekanan parsial oksida aktif dan klorin, maka semua FeCl3(g) dikonversikan menjadi Fe2O3.
Selain itu, sebagian klor yang dihasilkan dari oksidasi FeCl3
dapat berdifusi keluar melalui lapisan Fe2Al5 + FeAl2 dan
memicu siklus reaksi oksidasi/kloridasi yang berkelanjutan. Siklus reaksi ini menyebabkan Fe2O3 tetap tumbuh dalam
bentuk nodul, seperti ditunjukan pada Gambar 7b, yang memicu peningkatan weight gain.
Tingginya konsentrasi sulfur (9.21 wt.%) dalam Al-oksida menunjukan bahwa sulfur bisa masuk ke dalam oksida. Kemungkinan gas sulfur dihasilkan dari reaksi Al(s)+
Na2SO4(s) + 3/2O2(g) = Al2O3(s) + Na2O(s) + SO3(g). Pada
temperatur 700 C, keberadaan eutektik Na2SO4/Na2O yang
berasal dari reaksi Na2SO4dengan Al, dipercaya mengambil
tempat dalam pembentuk Al-sulfida [10].
Gambar 7. SEM topografi permukaan spesimen Al-coated yang dioksidasi pada 700 C selama (ab) 4 dan 64 jam
di NaCl, dan (cd) 4 dan 64 jam di Na2SO4
Tekanan parsial oksigen (pO2) dan gas sulfur (pSO3),
masing-masing adalah 9.5 103atm dan 9.9 104atm [11].
Ini memungkinkan untuk sulfur masuk dan berdisosiasi, kemudian reaksi 2Al(s) + 3/2S(s) = Al2S3 akan terbentuk di
dalam Al-rich oksida, seperti ditunjukan Gambar 5b.
SEM topografi pada permukaan spesimen Al-coated yang dioksidasi selama 4 jam pada Gambar 7c, menunjukan bahwa spalasi terjadi karena interaksi termal pertumbuhan antara Fe-oksida dan Al-oksida, yang memicu laju korosi pada tahap ini lebih rendah (Gambar 1). Namun seiring dengan lamanya waktu oksidasi 64 jam, Fe-rich oksida semakin tebal tumbuh di atas lapisan Al2O3dan oleh karena
itu weight gain ditingkatkan. Fe2O3tumbuh mengikuti batas
butir menunjukan bahwa difusi keluar Fe lebih mendominasi daripada difusi Fe melalui cacat kekosongan Al2O3(Gambar 7d).
IV. KESIMPULAN
Ketahanan oksidasi baja AISI 1020 pada temperatur 700C dalam lingkungan udara, NaCl dan Na2SO4 dapat
ditingkatkan melalui pelapisan Al-celup panas. Serangan korosi yang paling parah dialami oleh baja Al-coated dalam lingkungan NaCl melalui pembentukan gas metal-klorida yang mudah menguap, sehingga difusi Al dan Fe dalam lapisan Fe2Al5+ FeAl2ditingkatkan, yang memicu degradasi.
Sehingga lapisan ini kehilangan fungsi dalam menyuplai Al untuk membentuk Al2O3. Sedangkan Al-sulfida terbentuk
pada lapisan Al2O3 dalam bentuk terlarut. Difusi Fe dari
lapisan aluminida melalui batas butir menyebabkan Fe2O3
tumbuh diatas lapisan Al2O3.
DAFTAR PUSTAKA
[1] Ghosh, S.J., (2007), Failure Analysis of a Jacking Oil Pump, Failure Analysis and Prevention, Vol.7. pp 23 – 27.
[2] Tsaur, CC., Rock, JC., Wang, CJ., Su, YH., (2005), The Hot Corrosion of 310 Stainless Steel with Pre-coated NaCl/Na2SO4 Mixtures at 750 °C, Materials Chemistry and Physics, Vol.89. pp 445 – 453.
[3] Wang CJ., Lee JW,, Twu TH., (2003), Corrosion Behaviors of Low Carbon steel, SUS310 and Fe-Mn-Al Alloy with Hot-dipped Aluminum Coatings in NaCl-Induced Hot Corrosion, Surface Coating Technology, Vol.163164. pp 37 43.
[4] Wang, CJ, Badaruddin M., (2010), The Dependence of High Temperature Resistance of Aluminized Steel Exposed to Water-Vapour Oxidation, Surface and Coating Technology, Vol.205. pp 1200 1205.
[5] Han, G., Cho, WD., (2002), High Temperature Corrosion of Fe3Al in 1%Cl2/Ar, Oxidation of Metals, Vol. 58,
No.3/4. pp 391 413.
[6] Pieraggi B., (1987), Calculations of Parabolic Reaction Rate Constants, Oxidation of Metals, Vol.27. pp 177 185.
[7] Badaruddin, M., Suharno, Hanif, AW., (2012), Isothermal oxidation behavior of aluminized AISI 1020 steel at the temperature of 700 C, Proceeding of National Seminar of Mechanical Engineering XI, October 1617, Yogyakarta, Vol. 1, No.1. pp 1439 1444. [8] Kobayashi, S., Yakou, T., (2002), Control of Intermetallic
Compound Layers at Interface Between Steel and Aluminum by Diffusion-Treatment, Materials Science and Engineering A, Vol.338. pp. 44 53.
[9] Speight, JG., (2002), Lange’s Handbook of Chemistry, 16thEd. Mc Grawa-Hill, pp 18 56.
[10] Buscaglia. V., Nanni, P., Bottino, C., (1990), The Mechanism of Sodium Sulphate-Induced Low Temperature Hot Corrosion of Pure Iron, Corrosion Science, Vol. 30, No.4/5. pp 327 – 349.
[11] Niu Y., Gesmundo F., Viani F., Wu W., (1994), The Corrosion of Ni3Al in a Combustion Gas With and
Without Na2SO4-NaCl Deposits at 600-800 C, Oxidation