UJI AKTIVITAS ANTIBAKTERI FRAKSI DARI EKSTRAK METANOL DAUN Piper Crocatum Ruiz & Pav. TERHADAP Staphylococcus aureus
RESISTEN AMPICILLIN
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Diajukan oleh:
Anastasianus Hendriana
NIM : 158114032
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
UJI AKTIVITAS ANTIBAKTERI FRAKSI DARI EKSTRAK METANOL DAUN Piper Crocatum Ruiz & Pav. TERHADAP Staphylococcus aureus
RESISTEN AMPICILLIN
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Diajukan oleh:
Anastasianus Hendriana
NIM : 158114032
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iii
9
iv
HALAMAN PERSEMBAHAN
“Therefore do not worry about tomorrow
For tomorrow will worry about itself
Each day has enoµg
h trouble of it’s own”
Matthew 6 : 34
Karya ini kupersembahkan untuk :
Allah Bapa di Surga, Tuhan Yesus Kristus, Serta Bunda Maria Pengantara Doaku
Bapak, Ibu, Mas Banar, Mas Ardi, serta seluruh keluarga besar tercinta
Anindyasari dan seluruh teman-teman yang selalu menyemangatiku
vii PRAKATA
Puji dan syukur kepada Tuhan Yang Maha Esa atas segala rahmat
penyertaan, bimbingan dan kasih karunia-Nya sehingga penulis dapat
menyelesaikan skripsi yang berjudul “UJI AKTIVITAS ANTIBAKTERI FRAKSI DARI EKSTRAK METANOL DAUN Piper Crocatum Ruiz & Pav. TERHADAP
Staphylococcus aureus RESISTEN AMPICILLIN” dengan baik. Skripsi ini disusun sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi (S.
Farm) di Fakultas Farmasi Universitas Sanata Dharma.
Dalam penyusunan skripsi ini, penulis mendapatkan banyak bantuan,
dukungan, dan bimbingan dari berbagai banyak pihak, baik secara langsung
maupun tidak langsung. Oleh karena itu, pada kesempatan ini, penulis ingin
mengucapkan terima kasih yang sebesar-besarnya kepada :
1. Ibu Dr. Yustina Sri Hartini, M.Si., Apt., selaku Dekan Fakultas Farmasi
Universitas Sanata Dharma Yogyakarta serta selaku Dosen Pembimbing
skripsi yang telah sabar memberikan banyak sekali ilmu, saran, masukan,
bantuan dan bimbingan selama penelitian dan penyusunan skripsi ini
2. Ibu Dr. Chrstine Patramurti, Apt., selaku Ketua Program Studi Fakultas
Farmasi Universitas Sanata Dharma Yogyakarta.
3. Ibu Damiana Sapta Candrasari, S.Si., M.Sc., selaku Kepala Laboratorium
Fakultas Farmasi Universitas Sanata Dharma yang telah memberikan izin
untuk penggunaan segala fasilitas laboratorium selama penelitian, serta
selaku penguji skripsi yang telah memberikan saran, masukan dan bantuan
selama penyusunan skripsi ini.
4. Ibu Dr. Erna Tri Wulandari, M.Si., Apt. selaku dosen penguji skripsi yang
telah memberikan saran, masukan dan bantuan selama penyusunan skripsi
ini.
5. Mas Antonius Dwi Priyana dan Mas Sarwanto selaku Sekretariat S1
Fakultas Farmasi Universitas Sanata Dharma yang memberikan informasi
viii
6. Pak Yohanes Wagiran dan Mbak Intan yang telah membantu pengerjaan
penelitian skripsi ini di laboratorium.
7. Seluruh dosen dan karyawan Fakultas Farmasi Universitas Sanata Dharma
Yogyakarta yang telah mengajar dan membantu saya selama perkuliahan
8. Orang Tua saya Bapak Waradi Margiyanta dan Ibu Yohana Mujiem yang
telah mendidik serta menyayangi saya hingga sampai saat ini, Mas Ardi,
Mas Banar dan seluruh keluarga besar yang telah menyemangati dan
memberi dukungan selama proses pengerjaan skripsi ini.
9. Josephine Anindyasari Kristanto yang telah memberikan semangat dalam
bentuk cinta dan kasih sayang selama proses pengerjaan skripsi ini
10. Johannes Sianturi Baskoro teman seperjuangan dari SMA hingga kuliah ini
yang selalu memberikan dukungan selama kuliah dan pengerjaan skripsi ini.
11. Teman-teman meja 2, Tommy, Epen, Cinta, Misty, Galang, Tiara dan Erlin
yang selalu semangat dalam bekerjasama dalam keadaan senang dan sedih
setiap praktikum
12. Teman-teman skripsi saya, Nadia, Epen, Manda, Galang, Pipit, Bryant yang
selalu membantu dan menyemangati saya dalam proses pengerjaan skripsi
ini.
13. Teman-teman kelas FSMA 2015 serta seluruh angkatan 2015 yang telah
memberikan keceriaan didalam kelas maupun diluar kelas selama saya
berkuliah di Fakultas Farmasi Universitas Sanata Dharma ini.
14. Pengurus inti PSM Cantus Firmus 2017/2018, Erlin, Charles, Kevin, Nindy,
Yovita, Klara, Rista yang telah menyemangati saya selama ini.
15. Segenap keluarga besar PSM Cantus Firmus yang telah memberikan warna
dalam dinamika kehidupan dan perkuliahan lewat alunan lagu yang sering
kita nyanyikan bersama
16. Pengurus Dewan Perwakilan Mahasiswa Fakultas Farmasi Universitas
x ABSTRAK
Latar belakang : Meningkatnya resistensi bakteri Staphylococcus aureus terhadap antibiotik memerlukan pengobatan lain salah satunya dengan daun sirih merah, ekstrak metanol daun sirih merah diketahui memiliki senyawa antibakteri seperti fenol, flavonoid dan terpenoid, maka dalam penelitian ini dibuat fraksi VLC dari ekstrak metanol daun sirih merah untuk mengetahui aktivitas antibakteri, serta dideteksi dengan metode bioautografi kontak untuk melihat senyawa antibakteri yang berperan dalam menghambat bakteri Staphylococcus aureus resisten ampicillin.
Metode : Uji zona hambat, KHM dan KBM serta metode bioautografi kontak digunakan untuk menguji aktivitas senyawa antibakteri yang berperan dalam menghambat bakteri Staphylococcus aureus. Uji statistik menggunakan Kruskal-Wallis dan perbedaan tiap kelompok uji dengan post hocMann-Whitney.
Hasil : Uji aktivitas antibakteri fraksi VLC dari ekstrak metanol daun sirih merah menunjukkan bahwa fraksi 3 dan 4 memiliki aktivitas antibakteri dengan zona hambat berturut-turut 8,33 mm dan 4,17 mm dan nilai KBM pada konsentrasi 250 mg/ml. Analisis statistik dengan post hoc Mann-Whitney menunjukkan adanya perbedaan bermakna dari tiap perlakuan dengan nilai signifikansi <0,05.
Kesimpulan : Fraksi VLC dari ekstrak metanol daun sirih merah memiliki aktivitas antibakteri terhadap Staphylococcus aureus resisten ampicillin dengan diameter zona hambat sebesar 8,33 ± 0,2887 mm dan nilai KHM 15,6 mg/ml serta KBM 250 mg/ml, metode bioautografi kontak dalam penelitian ini belum mendeteksi senyawa antibakteri yang berperan secara spesifik dan melalui uji kualitatif dideteksi terdapat salah satu senyawa antibakteri yaitu flavonoid.
xi ABSTRACT
Background The increasing resistance of Staphylococcus aureus to antibiotics requires another treatment, one of which is red betel leaf, methanolic extract of red betel leaf is known to have antibacterial compounds such as phenols, flavonoids and terpenoids, in this study VLC fraction of methanol extract of red betel leaves was used to determine antibacterial activity , and detected by contact bioautography methods to see antibacterial compounds that play a role in inhibiting ampicillin-resistant Staphylococcus aureus.
Method : The inhibitory zone test, KHM, KBM and bioautography methods are used to test the aktivitas of antibacterial compounds that play a role in inhibiting
Staphylococcus aureus bacteria. Statistical tests using Kruskal-Wallis and differences in each test group with post-hoc Mann-Whitney.
Results : The antibacterial aktivitas of methanol fraction of red betel leaf showed that fractions 3 and 4 had antibacterial aktivitas with inhibition zones, respectively 8.33 mm and 4.17 mm and KBM values at a concentration of 250 mg / ml. The post hoc Mann-Whitney statistical analysis showed a significant difference from each treatment with a significance value <0.05.
Conclusion : VLC fraction from methanol extract of red betel leaf has antibacterial activity against ampicillin-resistant Staphylococcus aureus with inhibition zone diameter of 8.33 ± 0.2887 mm and MIC value of 15.6 mg / ml and KBM 250 mg / ml, contact bioautography method in research this has not detected antibacterial compounds that play a specific role and through qualitative tests detected there is one antibacterial compound, namely flavonoids.
xii DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
LEMBAR PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI... vi
PRAKATA ... vii
ABSTRAK ... x
ABSTRACT ... xi
DAFTAR ISI ... xii
DAFTAR TABEL ... xiii
DAFTAR GAMBAR ... xiv
DAFTAR LAMPIRAN ... xv
PENDAHULUAN ... 1
METODE PENELITIAN ... 3
HASIL DAN PEMBAHASAN ... 8
KESIMPULAN DAN SARAN ... 20
DAFTAR PUSTAKA ... 21
LAMPIRAN ... 24
xiii
DAFTAR TABEL
Tabel 1. Penggabungan fraksi berdasarkan uji KLT ... 10
xiv
DAFTAR GAMBAR
Gambar 1. Profil KLT hasil fraksi VLC ekstrak metanol daun sirih merah ... 9
Gambar 2. Kontrol media dan kontrol pertumbuhan bakteri ... 10
Gambar 3. Uji resistensi bakteri Staphylococcus aureus ... 11
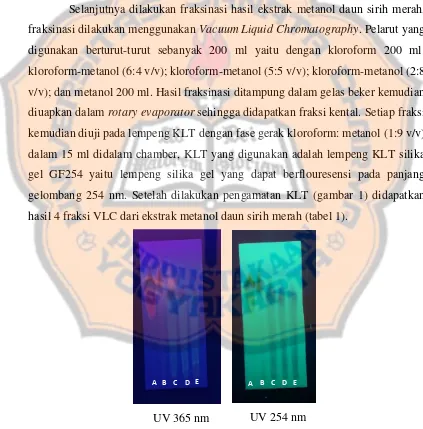
Gambar 4. Uji zona hambat fraksi dari ekstrak metanol daun sirih merah ... 12
Gambar 5. Uji KHM fraksi VLC dari ekstrak metanol daun sirih merah ... 14
Gambar 6. Uji KBM fraksi VLC dari ekstrak metanol daun sirih merah ... 15
Gambar 7.Optimasi fase gerak etil asetat : toluen (9:1 v/v) ... 15
Gambar 8. Uji bioautogtafi kontak... 16
Gambar 9. Uji Tabung senyawa flavonoid ... 17
xv
DAFTAR LAMPIRAN
Lampiran 1. Surat determinasi tanaman Piper crocatum Ruiz & Pav. ... 24
Lampiran 2. Surat identifikasi bakteri Staphylococcus aureus ... 25
Lampiran 3. Sertifikat pengujian statistik dengan SPSS ... 26
1 PENDAHULUAN
Staphylococcus aureus merupakan bakteri patogen yang menyebabkan infeksi klinis. Infeksi yang disebabkan oleh bakteri Staphylococcus aureus yaitu bakteremia, endokarditis infektif, osteoartikular, infeksi pada kulit dan jaringan
lunak serta pleuropulmonari (Tong et al, 2015). Infeksi akibat bakteri ini sering terjadi melalui folikel rambut, tusukan jarum atau melalui saluran pernafasan.
Bakteri ini dapat menghasilkan enzim koagulase yang mengkoagulasi fibrin
disekitar lesi dan didalam saluran getah bening, mengakibatkan pembentukan
jaringan fibrosis. Salah satu obat untuk mengatasi infeksi akibat bakteri ini adalah
antibiotik, namun penggunaan antibiotik yang kurang tepat (irrasional), terlalu singkat, dosis yang terlalu rendah, diagnosa awal yang salah dapat menjadi
beberapa faktor yang menyebabkan resistensi terhadap bakteri ini. Faktor yang
berhubungan dengan pasien yaitu pengetahuan pasien yang rendah akan
pengobatan cenderung menganggap penggunaan antibiotik wajib digunakan dalam
penanganan penyakit yang tidak sesuai indikasinya seperti flu, batuk, pilek dan
demam yang bukan karena infeksi bakteri. Kemampuan ekonomi pasien dalam
membeli obat juga mempengaruhi ketuntasan regimen terapi yang dijalani pasien
(Triana, 2014).
Intensitas penggunaan antibiotik yang relatif tinggi dapat menimbulkan
permasalahan bagi kesehatan terutama terjadinya resistensi bakteri terhadap
antibiotik. Resistensi ini berdampak pada morbiditas dan mortalitas, juga memberi
dampak negatif terhadap ekonomi dan sosial yang sangat tinggi. Pada awalnya
resistensi terjadi di tingkat rumah sakit, tetapi lambat laun juga berkembang di
lingkungan masyarakat, khususnya Streptococcus pneumoniae (SP),
Staphylococcus aureus, dan Escherichia coli. Penggunaan antibiotik seperti penisilin dan metisilin di pertengahan abad ke-20 efektif untuk melawan bakteri
Staphylococcus aureus. Namun, bakteri Staphylococcus aureus cepat mengalami resistensi terhadap antibiotik tersebut karena penggunaan antibiotik yang kurang
2
tetap menjadi ancaman bagi kesehatan manusia di dunia. Menurut data dari central for Disease Kontrol and Prevention (2014), Diestimasi terdapat 72.444 kasus infeksi MRSA yang terjadi di Amerika Serikat pada tahun 2014. Menurut
Kementrian Kesehatan Republik Indonesia (2015), angka kematian akibat
resistensi antimikroba sampai tahun 2014 sebesar 700.000 per tahun.
Kejadian resistensi bakteri terhadap antibiotik yang terus meningkat dapat
diatasi dengan penggunaan tanaman obat sebagai alternatif antibiotik. Salah satu
tanaman obat yang sering digunakan yaitu sirih merah. Tanaman sirih diketahui
memiliki efek antiseptik. Sirih merah diolah secara tradisional menjadi sediaan
infusia dan digunakan sebagai antiseptik, anti diabetes, anti kanker, dan untuk
mengobati berbagai penyakit infeksi (Lister et al. 2014). Senyawa fitokimia pada tanaman yang memiliki aktivitas antibakteri yaitu fenol, polifenol, quinon,
flavonoid, tannin, terpenoid, alkaloid. Ekstraksi dengan pelarut metanol dapat
digunakan untuk melarutkan senyawa terpenoid, tannin, flavonoid dan alkaloid
(Pharsant et al, 2011).
Penelitian sebelumnya menunjukkan hasil ekstrak metanol daun sirih
merah dengan konsentrasi 150 mg/mL, 300 mg/mL, 450 mg/mL dan 600 mg/mL
memiliki zona hambat sebesar 9,0 mm; 11,2 mm; 13,6 mm dan 15,7 mm terhadap
bakteri Staphylococcus aureus resisten metisilin (MRSA), serta melalui skrining fitokimia didapatkan senyawa flavonoid, triterpenoid, saponin dan tannin (Rinanda,
2012). Pada penelitian (Reveny et al. 2012) fraksi hasil VLC dari ekstrak metanol daun sirih merah dapat menghambat bakteri Staphylococcus aureus dengan KHM 10% serta pada penelitian (Rachmawaty et al, 2018) KBM dan KHM ekstrak metanol daun sirih merah pada konsentrasi 12,5% dan melalui uji KLT didapatkan
senyawa tannin dan flavonoida. Pada penelitian (Kusumaningtyas et al, 2008) metode bioautografi kontak digunakan untuk mendeteksi senyawa antibakteri dari
bahan alam yang berperan dalam menghambat bakteri. Oleh karena itu, peneliti
ingin mengetahui KHM dan KBM fraksi hasil VLC dari ekstrak metanol daun sirih
merah dalam menghambat pertumbuhan bakteri Staphylococcus aureus resisten antibiotik serta mengetahui senyawa antibakteri teraktif yang terdapat pada daun
3 METODE PENELITIAN
Alat dan Bahan
Alat yang digunakan dalam penelitian ini : Erlenmeyer, tabung reaksi, labu
ukur, pipet tetes, pH meter, cawan petri, batang pengaduk, gelas ukur, sendok,
pelubang sumuran, shaker, autoclave, oven, rotary evaporator, incubator,
microbiology safety cabinet, neraca analitik, bunsen, jarum ose, flakon, chamber, mikrokapiler, kertas saring, lempeng KLT.
Bahan yang digunakan dalam penelitian ini : Bakteri Staphylococcus aureus, media Nutrient Agar, Nutrient Broth, DMSO 10%, marker kuersetin, etil asetat, metanol, kloroform, toluen, Bufferd Pepton water, aquades steril dan daun sirih merah.
Determinasi Tanaman
Determinasi tanaman sirih merah dilakukan di Laboratorium Sistematika
Tumbuhan, Fakultas Biologi, Universitas Gadjah Mada Yogyakarta
Pengumpulan Bahan Uji
Daun sirih merah diperoleh dari daerah Sleman, Yogyakarta. Daun sirih
merah yang dipilih adalah daun sirih dengan permukaan halus, tidak berlubang dan
bewarna hijau kemerahan dan keperakan.
Pembuatan Simplisia
Daun sirih merah dipisahkan dari pengotor dan dibersihkan dengan air
mengalir. Setelah dicuci, daun dijemur selama 1 hari di sinar matahari tidak secara
langsung namun ditutup kain hitam, kemudian daun dipotong melintang. Setelah
dipotong, daun dikeringkan dengan oven dengan suhu 60°C. Daun yang telah
kering diserbuk dengan blender dan diayak dengan pengayak nomor 50 (Direktorat
Jendral Bina Kefarmasian dan Alat Kesehatan RI, 2011; Departemen Kesehatan RI,
4
Pembuatan Ekstrak Metanol Daun Sirih Merah
Pada penelitian ini ekstraksi berdasarkan penelitian sebelumnya dilakukan
dengan pelarut kloroform terlebih dahulu, ampas dari hasil ekstraksi dengan pelarut
kloroform kemudian diekstraksi dengan pelarut metanol. Tahapan maserasi yaitu
dengan merendam 10 gram serbuk daun sirih merah, kemudian dilarutkan dalam
100 ml metanol. Maserasi dilakukan selama 1x24 jam dengan bantuan shaker. Hasil maserat yang diperoleh disaring dengan corong Buchner yang dilapisi kertas saring
dengan bantuan pompa vakum. Serbuk hasil penyaringan dimaserasi dengan pelarut
metanol kembali sebanyak 100 ml selama 1x24 jam. Hasil maserat pertama dan
kedua kemudian diuapkan dengan rotary evaporator pada suhu 60°C untuk menguapkan pelarut pada ekstrak. Ekstrak diletakan pada cawan petri dan diuapkan
kembali pada waterbath pada suhu 60°C untuk menghilangkan pelarut yang mungkin masih ada dalam ekstrak. Ekstrak yang didapat merupakan ekstrak kental
dengan bobot tetap yang telah dipersyaratkan. Selanjutnya, rendemen dihitung
dengan rumus:
% Rendemen = x 100%
Pembuatan Fraksi VLC dari Ekstrak Metanol Daun Sirih Merah (FMDSM) Fraksinasi dilakukan dengan metode Vacum Liquid Chromatography
dengan fase gerak yang digunakan secara berturut-turut dalam volume 200 ml
adalah kloroform 200 ml; kloroform-metanol (6:4 v/v); kloroform-metanol (5:5
v/v); kloroform-metanol (2:8 v/v); dan metanol 200 ml (Hartini et al, 2013). Hasil dari fraksinasi akan diuapkan dengan rotary evaporator untuk menghilangkan pelarut yang masih tertinggal dalam fraksi, lalu setiap fraksi akan dielusi dalam 15
ml volume fase gerak kloroform-metanol (1:9 v/v) lalu diamati profil senyawanya
pada KLT, profil senyawa yang diamati adalah jarak faktor retensi (Rf),
pengamatan visual berupa warna senyawa pada setiap spot yang nampak pada
lempeng KLT setelah disinari dengan sinar UV 254 nm dan UV 365 nm (Kumar et al, 2012). Hasil profil senyawa yang sama akan digabungkan menjadi satu fraksi.
Bobot ekstrak (g)
5 Pembuatan Larutan Stok Ciprofloxacin
Tablet ciprofloxacin 500 mg digerus dan dilarutkan dalam 100 ml aquadest
steril sehingga didapat konsentrasi 5 mg/ml, lalu diambil 1 ml kemudian
dimasukkan pada labu takar 100 ml dan ditambahkan aquadest steril hingga batas
tanda atau tepat pada volume 100 ml, sehingga didapatkan konsentrasi larutan
antibiotik ciprofloxacin sebesar 50 µg/ml.
Uji Resistensi Bakteri Staphylococcus aureus terhadap Ampicillin
Biakan bakteri diinokulasikan pada medium NA dengan cara spread plate. Cakram ampicillin 10 µg diletakkan pada permukaan medium kemudian diinkubasi
pada suhu 37ºC selama 24 jam. Zona hambat yang dihasilkan disekitar cakram
diukur. Dinyatakan resisten bila diameter zona hambat ≤28 mm, intermediet dan sensitif bila zona hambat ≥29 mm (CLSI, 2017).
Penyiapan Bakteri Uji dan Suspensi Bakteri
Penyiapan bakteri uji mengikuti pedoman Clinical and Laboratory Standards Institute (2017). Kultur bakteri Staphylococcus aureus diambil 2-3 ose ke NB steril dan digores ke NA miring kemudian diinkubasi (37°C, 24 jam) untuk
mendapatkan stok bakteri. Sebelum digunakan, stok bakteri diambil secukupnya
dan diencerkan dengan Buffered Pepton Water (BPW) kemudian disetarakan kekeruhannya dengan larutan standar Mc Farland 0.5 dengan nephelometer
Pembuatan Kontrol Pertumbuhan dan Kontrol Kontaminasi Media
Kontrol pertumbuhan bakteri dibuat dengan cara menambahkan 1 mL
suspensi bakteri pada media NA steril yang masih cair, lalu divortex agar media
NA dengan suspensi bakteri dapat tercampur, kemudian secara pour dituang didalam cawan petri lalu biarkan memadat, dan diinkubasi selama 24 jam lalu
dilakukan pengamatan. Kontrol kontaminasi media dibuat dengan cara
6
Uji Daya Antibakteri Fraksi VLC dari Ekstrak Metanol Daun Sirih Merah Penyiapan cawan petri, dituang 5 ml NA steril ke dalam cawan petri lalu
dibiarkan memadat sebagai base layer agar. Lalu diambil 1 ml suspensi bakteri
Staphylococcus aureus, lalu diinokulasikan ke dalam 15 ml media NA secara pour plate, kemudian dituang secara merata sebagai seed layer agar diatas base layer agar, lalu dibiarkan memadat. Dibuat 6 sumuran dengan pelubang sumuran no.4, setiap sumuran berisi 50 µL kontrol positif (berupa antibiotik ampicillin), 50 µL
kontrol negatif (berupa DMSO 10%), dan sisanya berisi 50 µL tiap fraksi lalu
diinkubasi selama 24 jam. Lalu dilihat fraksi yang memiliki aktivitas antibakteri
paling baik, dilihat dari diameter zona hambat yang dihasilkan. Pengukuran zona
hambat dilakukan setelah inkubasi dan dalam satuan mm. Zona hambat yang
terukur adalah zona di sekitar sumuran yang keruh namun masih lebih jernih
dibandingkan dengan pertumbuhan bakteri Staphylococcus aureus sekitarnya.
Uji Kadar Hambat Minimum (KHM) dan Kadar Bunuh Minimum (KBM) Penentuan nilai KHM menggunakan dilusi cair. Fraksi VLC dari ekstrak
metanol daun sirih merah dilarutkan dalam DMSO 10% dan dibuat dalam
konsentrasi 250; 125; 62,5; 31,3; 15,6; 7,8; 3,9; 1,9 mg/ml. Kemudian
masing-masing konsentrasi fraksi yang telah dilarutkan diambil 1 mL dan dimasukkan ke
dalam tabung reaksi yang telah berisi 10 mL media NB, kemudian diinokulasikan
1 mL suspensi bakteri Staphylococcus aureus dan di vortex, lalu di inkubasi pada suhu 37°C selama 24 jam dan dilakukan pengamatan. Pada media NB pada
konsentrasi fraksi terkecil yang tidak terdapat pertumbuhan bakteri ditandai dengan
tingkat kekeruhanya ditentukan sebagai KHM.
Identifikasi Kualitatif Senyawa Flavonoid
Uji kualitatif senyawa flavonoid dilakukan dengan uji tabung dan uji KLT.
Sampel fraksi VLC dari ekstrak metanol daun sirih merah yang paling aktif
dilarutkan dengan metanol dan ditambahkan logam Mg dan 5-6 tetes asam klorida,
7
warna oranye jika terdapat flavanon. Uji secara KLT dengan fase diam silica gel
dan fase gerak etil asetat : toluen (9:1 v/v) akan terbentuk warna kuning pada sinar
tampak, pemadaman pada sinar UV 254 nm, dan warna hitam, kuning, biru atau
hijau pada sinar UV 365 nm (Hartini et al, 2013).
Preparasi Lempeng Kromatografi Lapis Tipis untuk Uji Bioautografi Kontak Senyawa antibakteri pada fraksi teraktif dari ekstrak metanol daun sirih
merah diambil meggunakan pipa kapiler lalu diteteskan sebanyak 10 tetes pada
lempeng KLT dengan fase diam silika gel dan dielusi dalam 15 ml volume fase
gerak dengan perbandingan pelarut etil asetat : toluen (9:1 v/v).
Uji Bioautografi Kontak
Lempeng KLT yang sudah dipreparasi di tempelkan menghadap lapisan
media NA yang sudah berisi suspensi bakteri Staphylococcus aureus yang telah di
spread pada permukaan media, kemudian ditunggu selama 45 menit agar senyawa dalam lempeng KLT dapat terdifusi dalam media NA, kemudian lepas lempeng
KLT tersebut dan diinkubasi selama 24 jam untuk melihat daya hambat yang
terjadi. Adanya daya hambat bakteri ditunjukan dengan zona jernih dari setiap spot
yang terdapat pada permukaan media agar.
Tata Cara Analisis Hasil
Analisis data diukur secara statistik yang diawali dengan menguji distribusi
normalitas dengan uji Shapiro-Wilk. Uji homogenitas dilakukan dengan uji Levene. Apabila didapati data terdistribusi normal dengan nilai p > 0,05 dan variansi data
homogen, maka dilanjutkan dengan uji One Way ANOVA. Apabila ditemukan perbedaan, maka dilanjutkan Post-Hoc Tukey pada taraf kepercayaan 95%. Jika data tidak terdistribusi secara normal yaitu p < 0,05 maka dilanjutkan dengan uji
8 HASIL DAN PEMBAHASAN
Determinasi sampel tanaman daun sirih merah dilakukan di Laboratorium
Sistematika Tumbuhan, Fakultas Biologi Universitas Gadjah Mada Yogyakarta.
Determinasi dilakukan dengan mencocokan ciri-ciri morfologi pada tanaman sirih
merah dengan acuan kepustakaan, disertai dengan surat keterangan (Lampiran 1).
Hasil determinasi menunjukkan bahwa tanaman yang digunakan adalah Piper crocatum Ruiz & Pav. dan dikenal dengan nama lokal yaitu sirih merah.
Daun sirih merah yang telah dikumpulkan kemudian dilakukan sortasi
basah untuk memisahkan sampel yang hendak diambil dengan bahan-bahan lain
yang kemungkinan terdapat pada sampel, misalnya batang, pengotor dan bagian
tanaman lain yang tidak diperlukan dan dicuci dengan air mengalir. Selanjutnya
dilakukan proses pengeringan bertujuan untuk mempermudah proses penyerbukan
daun sirih merah dan mengurangi kadar air pada simplisia sehingga diharapkan
tidak ditumbuhi oleh bakteri ataupun jamur. Pengeringan dilakukan dalam oven,
dan dilakukan hingga daun sirih merah telah kering sempurna, ditandai dengan
daun mudah diremas sehingga mudah dibuat dalam bentuk serbuk, hasil
penimbangan setelah daun sirih merah kering yaitu 244 gram. Selanjutnya
dilakukan penyerbukan dan pengayakan simplisia daun sirih merah kering dan
didapatkan serbuk daun sirih merah sebanyak 236 gram. Selanjutnya ditetapkan
kadar air dengan destilasi toluena, diestilasi toluena digunakan untuk menentukan
kadar air terutama bagi bahan alam yang mengandung senyawa aromatik, destilasi
dilakukan pada suhu 40-60ºC (Steltenphol et al, 2005). Sirih merah diketahui memiliki beberapa senyawa aromatik salah satunya yaitu terpenoid (Pharsant et al, 2011) dan pada penelitian ini suhu yang digunakan untuk destilasi toluena yaitu 50
ºC dan hasil kadar air yang didapatkan sebesar 4,8879%. Kadar air pada serbuk
simplisia yang baik <10% (Direktorat Jendral Bina Kefarmasian dan Alat
Kesehatan RI, 2011) sehingga kadar air pada simplisia daun sirih merah yang
digunakan sudah memenuhi kriteria serbuk simplisia yang baik.
Pada penelitian ini pembuatan ekstrak dilakukan secara maserasi,
digunakan ekstrasi dengan cara maserasi karena bertujuan agar senyawa yang tidak
9
tersebut yang diharapkan terdapat dalam pengujian efek antibakteri (Liu et al. 2014). Ekstrak yang didapat kemudian disaring menggunakan corong Buchner dan
serbuk hasil penyaringan dilakukan remaserasi kembali menggunakan pelarut
metanol. Hasil maserasi kemudian diuapkan dengan rotary evaporator pada suhu 60°C selanjutnya didapatkan ekstrak kental dan diukur bobot tetap yaitu dengan
cara 2 kali penimbangan secara berturut-turut tidak lebih dari 0,5 mg (Depkes RI,
1986). Ekstrak kental yang didapatkan yaitu sebesar 21,1446 gram dan rendemen
yang didapatkan sebesar 9,087%.
Selanjutnya dilakukan fraksinasi hasil ekstrak metanol daun sirih merah,
fraksinasi dilakukan menggunakan Vacuum Liquid Chromatography. Pelarut yang digunakan berturut-turut sebanyak 200 ml yaitu dengan kloroform 200 ml;
kloroform-metanol (6:4 v/v); kloroform-metanol (5:5 v/v); kloroform-metanol (2:8
v/v); dan metanol 200 ml. Hasil fraksinasi ditampung dalam gelas beker kemudian
diuapkan dalam rotary evaporator sehingga didapatkan fraksi kental. Setiap fraksi kemudian diuji pada lempeng KLT dengan fase gerak kloroform: metanol (1:9 v/v)
dalam 15 ml didalam chamber, KLT yang digunakan adalah lempeng KLT silika
gel GF254 yaitu lempeng silika gel yang dapat berflouresensi pada panjang
gelombang 254 nm. Setelah dilakukan pengamatan KLT (gambar 1) didapatkan
hasil 4 fraksi VLC dari ekstrak metanol daun sirih merah (tabel 1).
UV 365 nm UV 254 nm
Gambar 1. Profil KLT hasil fraksi VLC ekstrak metanol daun sirih merah
10
Keterangan gambar : A. Fraksi 1 (metanol 200 ml); B. Fraksi 2 (Kloroform-metanol 2:8 v/v); C. Fraksi 3 (Kloroform-metanol 5:5 v/v); D. Fraksi 4 (Kloroform-metanol 6:4 v/v); E. Fraksi 5 (Kloroform 200 ml).
Tabel 1. Penggabungan fraksi berdasarkan hasil uji KLT fraksi hasil VLC ekstrak metanol daun Piper crocatum Ruiz & Pav.
Selanjutnya dilakukan sterilisasi alat dan bahan yang akan digunakan untuk
uji antibakteri. Pertama dilakukan uji kontrol kontaminasi media yaitu dengan
menuangkan 20 ml media NA steril kedalam cawan petri lalu diinkubasi selama 24
jam pada suhu 37°C, selanjutnya pembuatan kontrol pertumbuhan bakteri uji,
bakteri Staphylococcus aureus yang digunakan telah dideterminasi di laboratorium (lampiran 2) yaitu dengan menuangkan 20 ml media NA yang telah diitambahkan
1 ml bakteri Staphylococcus aureus dan telah divortex ke dalam cawan petri dan diinkubasi selama 24 jam pada suhu 37°C, lalu dilakukan pengamatan.
(a) (b)
11
Dari hasil pengamatan didapatkan bahwa pada kontrol kontaminasi media
terlihat jernih, maka media NA yang digunakan tidak terdapat kontaminan,
sedangkan pada kontrol pertumbuhan bakteri, didapatkan bakteri Staphylococcus aureus dapat tumbuh dan tersebar merata, sehingga media NA yang digunakan dapat digunakan untuk menumbuhkan bakteri Staphylococcus aureus.
Selanjutnya dilakukan uji resistensi bakteri Staphylococcus aureus
terhadap antibiotik ampicillin, dengan cara menuangkan 0,2 ml bakteri
staphylococcus aureus ke permukaan media NA yang telah memadat dengan bantuan spreader, dilakukan hingga suspensi bakteri tersebar merata, lalu di tengah diletakkan cakram ampicillin 10 µg dan diinkubasi selama 24 jam dengan suhu
37°C.
Gambar 3. Uji resistensi bakteri Staphylococcus aureus terhadap ampicillin Menurut CLSI (2017) zona hambat ampicillin terhadap bakteri
Staphylococcus aureus diukur dan dinyatakan resisten apabila diameter zona
hambat ≤ 28 mm, intermediet dan sensitif bila ≥ 29 mm, dari hasil pengamatan diperoleh diameter zona hambat sebesar 1 mm hal tersebut membuktikan bahwa
bakteri Staphylococcus aureus yang digunakan resisten terhadap antibiotik ampicillin.
Selanjutnya persiapan uji antibakteri dari masing-masing fraksi VLC dari
ekstrak metanol daun sirih merah. Pertama, dilakukan pemilihan pelarut fraksi yang
akan digunakan yaitu DMSO 10%, pelarut tersebut digunakan karena tidak
12
dilakukan pengenceran setiap fraksi dengan DMSO 10% yaitu sebesar 250 mg/mL
setiap fraksi. Kemudian dilakukan pengenceran antibiotik sebagai kontrol positif
yaitu antibiotik ciprofloxacin sebesar 50 µ g/ml dan pembuatan suspensi bakteri uji
Staphylococcus aureus dengan konsentrasi setara 0,5 larutan Mc Farland. Kemudian, pembuatan base layer yaitu dengan menuangkan 5 mL media NA steril kedalam cawan petri dan ditunggu hingga memadat, dilanjutkan 15 mL media NA
yang telah ditambahkan 1 mL suspensi bakteri Staphylococcus aureus yang telah di vortex dituangkan pada permukaan base layer dan dibiarkan memadat sehingga terbentuk seed layer.
Gambar 4. Uji zona hambat fraksi VLC dari ekstrak metanol daun sirih merah
Keterangan gambar: 1. Kontrol positif (ciprofloxacin 50 µg/ml), 2. Kontrol negatif (DMSO 10%), 3. Fraksi 1 (250 mg/ml); 4. Fraksi 2 (250 mg/ml); 3. Fraksi 3 (250 mg/ml); 4. Fraksi 4 (250 mg/ml).
Hasil uji aktivitas antibakteri menunjukkan bahwa fraksi VLC dari ekstrak
metanol daun sirih merah yaitu fraksi 3, fraksi 4 dan kontrol positif (antibiotik
ciprofloxacin 50 µg/ml) membentuk zona hambat disekitar lubang sumuran, secara
berturut-turut diameter zona hambat yang terbentuk yaitu 8,33; 4,17 dan 18,5 mm,
sedangkan pada fraksi 1 dan fraksi 2 tidak terdapat zona hambat yang terbentuk,
dikarenakan pada fraksi 1 dan fraksi 2 memungkinkan adanya kontaminasi
sehingga tidak terbentuk zona hambat, serta adanya endapan pada fraksi tersebut
mengakibatkan adanya bercak pada sekeliling lubang sumuran dan cairan fraksi
13
yang terbentuk diskeliling lubang sumuran, sehingga pada fraksi 1 dan 2 tidak
terbentuk zona hambat bakteri yang ditandai dengan adanya zona jernih. Pada
kontrol negatif yaitu DMSO 10% tidak terbentuk zona hambat, hal ini
membuktikan bahwa pelarut yang digunakan dalam pembuatan konsentrasi tiap
fraksi tidak memiliki efek antibakteri sedangkan pada penelitian sebelumnya
(Rinanda, 2012) menunjukkan hasil ekstrak metanol daun sirih merah dengan
konsentrasi 150 mg/mL, 300 mg/mL, 450 mg/mL dan 600 mg/mL memiliki zona
hambat sebesar 9,0 mm; 11,2 mm; 13,6 mm dan 15,7 mm terhadap bakteri
Staphylococcus aureus resisten antibiotik. Dari hasil tersebut dapat dikatakan bahwa fraksi 3 dengan konsentrasi 250 mg/ml merupakan fraksi teraktif yang
memiliki aktivitas antibakteri terhadap bakteri Staphylococcus aureus resisten ampicillin namun aktivitas antibakteri yang dihasilkan tidak sebesar aktivitas
antibakteri dari ekstrak metanol daun sirih merah pada penelitian sebelumnya
(Rinanda, 2012). Menurut (Nopiyanti et al, 2016) dikatakan diameter zona hambat
sangat kuat jika ≥ 20 mm, kuat jika 10-20 mm, sedang 5-10 mm dan dikatakan
lemah jika ≤ 5mm, maka zona hambat fraksi 3 sebesar 8,3 mm menunjukkan zona
hambat yang sedang terhadap bakteri Staphylococcous aureus resisten ampicillin. Konsentrasi hambat minimum (KHM) merupakan konsentrasi terkecil
dari senyawa antibakteri yang dapat menghambat penuh pertumbuhan bakteri. Pada
penentuan KHM ini digunakan fraksi 3 karena memiliki aktivitas antibakteri paling
besar dibandingkan fraksi yang lain. KHM ditentukan dengan menggunakan dilusi
cair dengan media yang digunakan adalah nutrient broth (NB) dan hasilnya dibandingkan dengan kontrol pertumbuhan bakteri dan kontrol media. Fraksi VLC
dari ekstrak metanol daun sirih merah dibuat dalam berbagai varian konsentrasi,
yaitu 250; 125; 62,5; 31,3; 15,6; 7,8; 3,9; 1,9 mg/ml, setiap varian konsentrasi fraksi
VLC dari ekstrak metanol daun sirih merah dimasukkan kedalam tabung yang berisi
NB dan 1 ml bakteri Staphylococcus aureus lalu divortex dan diinkubasi selama 24 jam. Dari hasil pengamatan terlihat bahwa konsentrasi 15,6; 7,8; 3,9; dan 1,9 masih
terlihat keruh sama seperti kontrol pertumbuhan, sedangkan konsentrasi 250; 125;
62,5; dan 31,3 terdapat perbedaan warna dikarenakan adanya warna yang
14
Berdasarkan hasil tersebut dapat dikatakan bahwa konsentrasi 15,6 mg/ml fraksi
VLC dari ekstrak metanol daun sirih merah merupakan KHM sedangkan pada
penelitian (Rachmawaty et al, 2018) KHM ekstrak metanol daun sirih merah pada konsentrasi 12,5%, hasil tersebut menunjukkan bahwa fraksi VLC dari ekstrak
metanol daun sirih merah memiliki KHM yang lebih besar dibandingkan ekstrak
metanol daun sirih merah, sehingga dibutuhkan konsentrasi fraksi VLC dari ekstrak
metanol daun sirih merah untuk menghambat bakteri Staphyloccous aureus resisten ampicillin.
Gambar 5. Hasil uji konsentrasi hambat minimum (KHM) fraksi VLC dari ekstrak metanol daun sirih merah
Keterangan gambar : 1. Kontrol media, 2. FMDSM 250 mg/ml; 3. FMDSM 125 mg/ml; 4. FMDSM 62,5 mg/ml; 5. FMDSM 31,3 mg/ml; 6. FMDSM 15,6 mg/ml; 7.
FMDSM 7,8 mg/ml; 8. FMDSM 3,9 mg/ml ; 9. FMDSM 1,9 mg/ml dan 10. Kontrol pertumbuhan.
Selanjutnya dilakukan pengujian konsentrasi bunuh minimum (KBM).
KBM merupakan konsentrasi terkecil dari senyawa antibakteri yang dapat
membunuh penuh bakteri. KBM dilakukan dengan cara sub kultur dari media NB
dari konsentrasi FMDSM 250; 125; 62,5 dan 31,3 mg/ml kedalam media NA steril
yang telah dibagi menjadi 4 kuadran dengan cara streak plate dan diinkubasi selama 24 jam. Hasil yang didapatkan bahwa FMDSM 125; 62,5 dan 31,3 mg/ml masih
terdapat pertumbuhan bakteri Staphylococcus aureus sedangkan pada FMDSM 250 mg/ml terlihat jernih dan tidak terdapat pertumbuhan bakteri Staphylococcus aureus. Sehingga nilai KBM fraksi VLC dari ekstrak metanol daun sirih merah adalah pada konsentrasi 250 mg/ml, sedangkan pada penelitian (Rachmawaty et al,
15
2018) KBM ekstrak metanol daun sirih merah pada konsentrasi 12,5% sehingga
pada penilitan ini dibutuhkan lebih banyak konsentrasi fraksi VLC dari ekstrak
metanol untuk membunuh bakteri Staphyloccous aureus resisten ampicillin.
Gambar 6. Hasil uji konsentrasi bunuh minimum (KBM) fraksi VLC dari ekstrak metanol daun sirih
merah. Keterangan gambar: 1. FMDSM 250 mg/ml;
2. FMDSM 125 mg/ml; 3. FMDSM 62,5 mg/ml; 4.
Selanjutnya dilakukan optimasi fase gerak pada lempeng KLT untuk
melihat pemisahan profil senyawa pada fraksi VLC dari ekstrak metanol daun sirih
merah, fase gerak yang digunakan yaitu etil asetat : toluen (9:1 v/v) dalam volume
15 ml, optimasi dilakukan dengan meneteskan 2 tetes fraksi VLC dari ekstrak
metanol daun sirih merah yang teraktif yaitu fraksi 3 dengan konsentrasi 250 mg/ml
dan didapatkan hasil pemisahan senyawa yang cukup baik pada gambar 7.
Selanjutnya dilakukan bioautografi, uji ini menggunakan metode
bioautografi kontak, metode ini dugunakan untuk mendeteksi adanya senyawa
antibakteri ditandai dengan adanya daerah jernih yang tidak ditumbuhi oleh bakteri
(Kusumaningtyas et al., 2018). Lempeng KLT ditotolkan FMSDM 250 mg/ml sebanyak 10 tetes dan dielusi dengan fase gerak etil asetat : toluen (9:1 v/v),
lempeng KLT yang sudah kering lalu ditempelkan pada media NA yang
16
media diinkubasi selama 24 jam. Hasil bioautografi menunjukkan adanya aktivitas
antibakteri dengan ditunjukannya zona jernih pada permukaan media NA pada
gambar 8B, namun senyawa yang berperan dalam menghambat bakteri pada uji
bioautografi ini tidak jelas karena senyawa tidak terpisah secara sempurna atau
tailing pada gambar 8A, hal tersebut dikarenakan beberapa fakor lain seperti fase gerak yang tidak bisa memisahkan senyawa secara baik, konsentrasi zat antibakteri
yang terlalu kecil, sifat lipofilitas senyawa antibakteri dengan media agar yang
digunakan, jika sifatnya tidak sama maka kemampuan senyawa antibakteri untuk
berdifusi pada media sangat rendah, sehingga menyebabkan terbentuknya zona
jernih pada permukaan media agar kurang baik (Dewanjee et al,2014). Pada uji bioautografi kontak tidak adanya aktivitas antibakteri bisa terjadi karena interaksi
beberapa senyawa pada fraksi (Ambarwati, 2017) serta konsentrasi fraksi hasil
kromatografi yang didapat terlalu kecil dapat berpengaruh terhadap aktivitas
antibakteri yang terjadi karena kandungan komponen senyawa yang terdapat pada
fraksi menentukan aktifitas bioaktif dari bahan tersebut (Ali et al, 2016).
Gambar 8. Uji aktivitas antibakteri fraksi VLC dari ekstrak metanol daun sirih merah dengan metode kontak bioautografi.
Keterangan gambar : A. Hasil profil senyawa elusi pada plat KLT, B. Hasil profil bioautografi kontak pada media NA setelah inkubasi 24 jam
Selanjutnya dilakukan uji kualitatif kandungan senyawa flavonoid pada
fraksi VLC dari ekstrak metanol daun sirih merah. Menurut (Kesarkar et al, 2009) dalam 0,05% larutan senyawa dalam pelarut metanol mengandung sekitar 5-10 µg
17
flavonoid, maka dalam penilitan ini dilakukan 2 uji kualitatif yaitu dengan uji
tabung dan uji KLT, Uji tabung dilakukan melarutkan fraksi VLC dari ekstrak
metanol daun sirih merah kemudian ditambahkan logam Mg dan 5-6 tetes asam
klorida, larutan akan menjadi merah untuk flavonol dan oranye untuk flavanon
(Hartini et al, 2013).
(a) (b)
Gambar 9. Uji kualitatif kandungan senyawa flavonoid dengan uji tabung
Dari hasil pengamatan terdapat perubahan warna menjadi warna merah
setelah dilakukan uji tabung pada fraksi VLC dari ekstrak metanol daun sirih merah,
perubahan warna merah mengindikasikan adanya senyawa flavonol yaitu salah satu
jenis flavonoid dan dapat dikatakan bahwa fraksi VLC dari ekstrak metanol daun
sirih merah mengandung senyawa flavonoid. Senyawa flavonol contohnya adalah
kuersetin, maka pada uji kualitatif selanjutnya dilakukan uji KLT dengan marker
kuersetin.
Selanjutnya dilakukan uji kualitatif kandungan senyawa flavonoid pada
fraksi VLC dari ekstrak metanol daun sirih merah, sebagai marker digunakan senyawa kuersetin. Senyawa kuersetin dan fraksi VLC dari ekstrak metanol daun
sirih merah dengan konsentrasi 250 mg/ml di totolkan pada lempeng KLT dan
dielusi dengan fase gerak etil asetat : toluen (9:1 v/v), adanya flavonoid ditunjukkan
dengan terbentuknya warna kuning pada sinar tampak, pemadaman pada sinar UV
254 nm, dan warna hitam, kuning, biru atau hijau pada sinar UV 365 nm (Hartini,
18
a.UV 365 nm b.UV 254 nm c FeCl3
Gambar 10. Uji kualitatif kandungan senyawa flavonoid dengan metode KLT
Keterangan gambar : A. Marker Kuersetin B. FMDSM
Pada uji KLT didapatkan hasil bahwa fraksi VLC dari ekstrak metanol
daun sirih merah memiliki kandungan flavonoid yaitu kuersetin, dengan nilai rf
marker kuersetin sebesar 0,71 dan nilai Rf kandungan flavonoid pada FMDSM
sebesar 0,7. Deteksi senyawa flavonoid digunakan penyemprotan FeCl3, sehingga senyawa flavonoid terdeteksi menjadi warna biru kehitaman. Menurut (Kesarkar et al, 2009) pada sinar UV 254 nm flavonoid dapat berflouresensi hal tersebut ditunjukan pada lempeng KLT gambar 10b bahwa pada deteksi sinar UV 254 nm
senyawa flavonoid pada no 3 bewarna kuning kehitaman, sedangan pada sinar UV
365 nm senyawa flavonoid akan tampak dengan warna kuning, hal tersebut sesuai
pada lempeng KLT gambar 10a dengan deteksi sinar UV 365 nm, terdapat warna
kuning pada no.3, senyawa flavonol seperti kuersetin, myricetin dan senyawa
glikosida lain akan menghasilkan warna oranye-kuning saat penyemprotan reagen,
menurut (Alcantara et al, 2017) reagen FeCl3 dapat digunakan untuk mendeteksi senyawa flavonoid dan fenol dan menurut (Ghosh, 1987) reagen yang paling efektif
19
Tabel 2. Keterangan nilai Rf dan warna pada deteksi flavonoid dengan KLT
Berdasarkan analisis statistik (lampiran 4) untuk mengetahui
kebermaknaan perbedaan antara masing-masing fraksi VLC dari ekstrak metanol
daun sirih merah dengan kontrol positif dan kontrol negatif didapatkan uji Shapiro-Wilk dengan nilai signifikansi <0,05 menunjukkan data tidak terdistribusi secara normal. Uji Levene dengan nilai signifikansi <0,05 menunjukkan distribusi data tidak homogen, sehingga dilanjutkan uji Kruskal-Wallis yang menunjukkan adanya perbedaan signifikan pada data dengan nilai signifikansi <0,05 selanjutnya
dilanjutkan uji Post-Hoc Mann-Whitney. Diameter zona hambat fraksi 3 dan fraksi 4 berbeda bermakna secara statistik terhadap kontrol positif dan kontrol negatif,
pada perbandingan dengan kontrol negatif didapatkan perbedaan nilai zona hambat
yang bermakna karena pada kontrol negatif tidak ada nilai zona hambat yang
terbentuk. Sedangkan pada kontrol positif nilai zona hambat yang dihasilkan jauh
lebih besar dibandingkan nilai zona hambat yang dihasilkan oleh fraksi 3 dan 4
sehingga terlihat perbedaan yang bermakna, maka didapatkan bahwa daya aktivitas
antibakteri fraksi 3 > fraksi 4 dalam konsentrasi fraksi 250 mg/ml.
UV 365 nm nm
20 KESIMPULAN DAN SARAN
Fraksi VLC dari ekstrak metanol daun sirih merah teraktif yang memiliki
aktivitas antibakteri terhadap Staphylococcus aureus yaitu pada fraksi 3 dengan konsentrasi 250 mg/ml dan dengan hasil diameter zona hambat sebesar 8,33 ±
0,2887 mm, sedangkan nilai KHM 15,6 mg/ml dan KBM fraksi VLC dari ekstrak
metanol daun sirih merah berada pada konsentrasi 250 mg/ml. Deteksi senyawa
antibakteri dengan metode bioautografi kontak belum terdeteksi secara baik karena
senyawa antibakteri mengalami tailing pada permukaan media agar, dan uji kualitatif senyawa antibakteri didapatkan positif senyawa flavonoid pada fraksi
VLC dari ekstrak metanol daun sirih merah.
Saran, perlu dilakukan uji bioautografi kontak dengan fase gerak lain yang
dapat memisahkan senyawa secara baik, dengan mempertimbangkan sifat
lipofilitas senyawa dan media agar yang digunakan, serta konsentrasi senyawa yang
dapat berdifusi pada media agar sehingga didapatkan senyawa antibakteri spesifik
yang menghambat pertumbuhan bakteri Staphylococcus aureus resisten ampicillin, atau dapat menggunakan uji bioautografi yang lain seperti direct TLC bioautographic detection dan immersion or agar overlay bioautography untuk mendeteksi senyawa antibakteri. Perlu dilakukan identifikasi senyawa antibakteri
lain selain flavonoid, dan dilakukannya isolasi senyawa antibakteri dari daun sirih
21
DAFTAR PUSTAKA
Alcantara, K.P., Abirs M.J.C., Calpotura, M.P., Macarasami S., Manalo, Matias,
F.C, and Tamodong C., 2017.Phytochemical Analysis and Determination
of Angio Suppresive and Antioxidant Properties of Leaf Extract of Dillenia sibuyanensis (Dilleniaceae): A Pioneer Study. Journal of Cancer Biology & Research 5(3).pp 1-6.
Ali, A., Kursia, S., and Nadia. 2016. Deteksi Antibakteri Pada Ekstrak Daun Murbei
(Morus Albal.) Dari Beberapa Lokasi Pengambilan Sampel Tanaman Di Sulawesi Selatan. Jurnal Bionature 17(2). pp 69-75.
Ambarwati, N.S.S., Malik, A., Listari, A., Nirwana, Elya, B and Hanafri, M., 2017.
Antibacterial Activity Of Fractions Of Ethyl Acetate Extract Of Garcinia Lattissima Miq. Fruits. Asian Journal of Pharmaceutical and Clinical Research 10(5). pp.81-84.
Centers for Disease Kontrol and Prevention. 2014. Active Bacterial Core Surveillance Report, Emerging Infections Program Network, Methicillin-Resistant Staphylococcus aureus. https://www.cdc.gov/abcs/reports-findings/survreports/mrsa14.pdf. Diakses tanggal 14 Juni 2018.
Clinical and Laboratory Standards Institute. 2017. M100 Performance Standards for Antimicrobial Susceptibility Testing. 27th Edition. pp 55-58.
Dantes R, et al., 2013. National burden of invasive methicillin-resistant
Staphylococcus aureus infections, United States, 2011. JAMA Intern Med. 8(21). p.173.
Departemen Kesehatan RI, 1985. Cara Pembuatan Simplisia. Jakarta: Departemen Kesehatan RI, 1-18.
Departemen Kesehatan RI, 2000. Parameter Standar Umum Esktrak Tumbuhan Obat. Cetakan 1, Jakarta: Departemen Kesehatan RI, hal. 9-12.
22
Direktorat Jendral Bina Kefarmasian Kefarmasian dan Alat Kesehatan RI, 2011. Farmakope Herbal. Suplemen II. Edisi I, Jakarta: Kementerian Kesehatan RI, hal. 110-111.
Gosh, P., Sil P., and Thakur, S., 1987. Spray Reagent for the Detection of
Coumarins and Flavonoids on Thin Layer Plates. Journal of
Chromatography 403. Pp. 285-287.
Hartini, Y. S., Wahyuono, S., Widyarini, S., dan Yuswanto, A., 2013. Uji Aktivitas
Fagositosis Makrofag Fraksi-fraksi dari Ekstrak Metanol Daun Sirih Merah
(Piper crocatum Ruiz & Pav.) Secara In Vitro. Jurnal Ilmu Kefarmasian Indonesia, 11 (2), pp. 108-115.
Kesarkar, S., Bhandage, A., Deshmukh, S., Shevkar., K and Abhyankar, M.,
Flavonoids : An Overview. Journal of Pharmacy Research 2(6). Poona
Districts Education Association’s Seth Govid Raghunath Sable College of
Pharmacy, Saswad, Pune. pp. 1148-1154.
Kumar, S., Jyotirmayee, K., and Sarang, M., 2012. Thin Layer Chromatography: A
Tool of Biotechnology for Isolation of Bioactive Compounds from Medicinal
Plants. International Journal of Pharmaceutical Sciences Review and Research 18 (1). pp. 126-132.
Kusumaningtyas, E., Astuti, E., & Darmono., 2008. Sensitivitas Metode
Bioautografi Kontak dan Agar Overlay dalam Penentuan Senyawa Antikapang. Jurnal Ilmu Kefarmasian Indonesia. 6 (2), 75-79.
Lister I.N.E., et al. 2014. Antimicrobial activities of metanol extract of Sirih Merah
(Piper crocatum L.) leaf. Journal of Chemical and Pharmaceutical Research. 6(12). pp. 650-654.
Liu, L., Wang. Y.G., Leng, F.F., Li., Y.C., 2014. Optimization of Total Flavonoids
Extraction from Coreopsis tinctoriaNytt. by Respone Surface Methodology.
23
Nopiyanti, H.T., Agustirani, F., Isnaini, M. 2016. Screening of Nypa Fructions as
Antibacterial of Bacillus subtilis, E. coli and S. aureus. Journal Maspori. 8:2, pp. 83-90.
Prashant Tiwari, B., Kumar, M.K. & Gurpreet Kaur, H.K., 2011. Phytochemical
screening and extraction - A review. Internationale Pharmaceutica Sciencia, 1(1), pp.98–106.
Rachmawaty, F. J., 2018. Optimasi Ekstrak Metanol Daun Sirih Merah (Piper
Crocatum) sebagai Antibakteri terhadap Bakteri Staphylococcus aureus.
Jurnal Kedokteran dan Kesehatan Mutiara Medika. Vol 18 (1). pp 13-19. Reveny, J., 2011. Antimicrobial Aktivitas of the Extract and Fraction of Red Betel
Leaf (Piper betle Linn.). Jurnal Ilmu Dasar 12 (1). p.8.
Rinanda, T., et al. 2012. Antibacterial aktivitas of red betel (Piper crocatum) leaf methanolic extracts against methicillin resistant Staphylococcus aureus. 8th
Uniterd Bioscience. pp 270-273.
Steltenpohl, P., Chlebovec, M., and Graczová, E., 2005. Simulation of Toluene
Extractive Distillation from a Mixture with Heptane. Chem. Pap. 59 (6a). pp 421—427.
Triana, D., 2014. Frekuensi β-Lactamase Hasil Staphylococcus aureus Secara Iodometri Di Laboratorium Mikrobiologi Fakultas Kedokteran Universitas
Andalas. Jurnal Gradien 10 (2). pp. 992-995.
Tong, S.Y.C., et al., 2015. Staphylococcus aureus Infections: Epidemiology,
24
Lampiran 1. Surat determinasi tanaman sirih merah
25
26
27 Lampiran 4. Hasil perhitungan statistik
Tests of Normality
Perlakuan
Kolmogorov-Smirnova Shapiro-Wilk
Statistik df Sig. Statistik df Sig.
Zona Hambat Kontrol Positif .175 3 . 1.000 3 1.000
Kontrol Negatif . 3 . . 3 .
Fraksi 1 . 3 . . 3 .
Fraksi 2 . 3 . . 3 .
Fraksi 3 .385 3 . .750 3 .000
Fraksi 4 .385 3 . .750 3 .000
Test of Homogeneity of Variances
Levene Statistik df1 df2 Sig.
Zona Hambat Based on Mean 3.855 5 12 .026
Based on Median 1.333 5 12 .315
Based on Median and with
adjusted df
1.333 5 6.000 .364
29
Exact Sig. [2*(1-tailed Sig.)] .100b
a. Grouping Variable: Replikasi
30
Mann-Whitney Test
Test Statistiksa
Zona Hambat
Mann-Whitney U .000
Wilcoxon W 6.000
Z -1.993
Asymp. Sig. (2-tailed) .046
Exact Sig. [2*(1-tailed Sig.)] .100b
a. Grouping Variable: Replikasi
b. Not corrected for ties.
Mann-Whitney Test
Ranks
Replikasi N Mean Rank Sum of Ranks
Zona Hambat Kontrol Positif 3 5.00 15.00
Fraksi 4 3 2.00 6.00
Total 6
Ranks
Replikasi N Mean Rank Sum of Ranks
Zona Hambat Kontrol Positif 3 5.00 15.00
Fraksi 3 3 2.00 6.00
31
Test Statistiksa
Zona Hambat
Mann-Whitney U .000
Wilcoxon W 6.000
Z -1.993
Asymp. Sig. (2-tailed) .046
Exact Sig. [2*(1-tailed Sig.)] .100b
a. Grouping Variable: Replikasi
32
BIOGRAFI PENULIS
Penulis skripsi bernama Anastasianus Hendriana, lahir di
Sleman, 22 April 1995. Penulis akrab dipanggil Rian
merupakan anak ketiga dari tiga bersaudara dari pasangan
Warady Margiyanta dan Yohana Mujiem. Penulis
menempuh pendidikannya di SD Kanisius Demangan
Baru, SMP Negeri 4 Depok, SMA Kolese De Britto dan
SMA Sang Timur Yogyakarta, pada tahun 2015
melanjutkan pendidikan di Program Studi Farmasi
Universitas Sanata Dharma Yogyakarta. Selama perkuliahan penulis aktif dalam
mengikuti kegiatan kepanitian dan organisasi seperti Pharmacy Performance Road to School, Dewan Perwakilan Mahasiswa Fakultas Farmasi Universitas Sanata Dharma 2016/2017 dan Unit Kegiatan Mahasiswa Paduan Suara Cantus Firmus
serta kepanitian fakultas maupun universitas lainnya. Selain itu, penulis juga pernah
menjadi juara lomba paduan suara Asia Pacific Choir Games di Colombo, Sri Lanka, Festival folklore Nusantara, Jakarta dan Pesparawi Mahasiswa Nasional
XIV, Medan. Selain itu, penulis juga menerima dan melaksanakan Program
Kreativitas Mahasiswa dalam bidang Pengabdian Masyarakat yang