SINTESIS DAN KARAKTERISASI BIOKOMPATIBILITAS Si:Ca10(PO4)6(OH)2 DENGAN METODE HIDROTERMAL UNTUK
APLIKASI BONE FILLER
SKRIPSI
GILANG DARIL UMAMI
PROGRAM STUDI S-1 TEKNOBIOMEDIK DEPARTEMEN FISIKA
FAKULTAS SAINS DAN TEKNOLOGI UNIVERSITAS AIRLANGGA
SINTESIS DAN KARAKTERISASI BIOKOMPATIBILITAS Si:Ca10(PO4)6(OH)2 DENGAN METODE HIDROTERMAL UNTUK
APLIKASI BONE FILLER
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Teknik Bidang Teknobiomedik Pada Departemen Fisika
Fakultas Sains dan Teknologi Universitas Airlangga
Oleh :
GILANG DARIL UMAMI NIM : 080810009
Tanggal Lulus : 14 September 2012
Disetujui oleh:
Pembimbing I,
Ir. Aminatun, M.Si NIP. 19681028 199303 2 003
Pembimbing II,
LEMBAR PENGESAHAN NASKAH SKRIPSI
PEDOMAN PENGGUNAAN SKRIPSI
Skripsi ini tidak dipubilkasikan, namun tersedia di perpustakaan dalam lingkungan Universitas Airlangga, diperkenankan untuk dipakai sebagai referensi kepustakaan, tetapi pengutipan harus seizin penyusun dan harus menyebutkan sumbernya sesuai kebiasaan ilmiah.
KATA PENGANTAR
Puji syukur ke hadirat Allah SWT yang senantiasa memberikan hidayah, inayah, dan rahmat-Nya sehingga penyusun dapat menyelesaikan naskah skripsi yang berjudul “Sintesis Dan Karakterisasi Biokompatibilitas Si:Ca10(PO4)6(OH)2 Dengan Metode Hidrotermal Untuk Aplikasi Bone Filler”. Tidak lupa semoga segala rahmat selalu terlimpahkan pada junjungan
kita, Nabi Muhammad SAW yang telah membimbing umat ini dari zaman jahiliyah menuju zaman pencerahan.
Naskah skripsi ini disusun untuk memenuhi salah satu syarat kelulusan. Pada kesempatan ini, penyusun menyampaikan terima kasih yang sebesar-besarnya kepada:
1. Ayah, ibu, my little bro and little sis yang selalu mendukung dan mendoakan. 2.Ketua Departemen Fisika, Bapak Drs. Siswanto, M.Si, yang telah memberikan
informasi tentang penyusunan naskah skripsi ini.
3.Ketua Program Studi S1 Teknobiomedik, Ibu Dr. Retna Apsari, M.Si, yang telah memberikan informasi tentang penyusunan naskah skripsi ini.
4.Ibu Ir. Aminatun, M.Si selaku pembimbing I yang selalu memberikan masukan dan meluangkan waktu bagi penyusun untuk berkonsultasi.
5.Ibu Dr.Dwi Winarni, M.Si selaku pembimbing II yang selalu memberikan masukan dan meluangkan waktu bagi penyusun untuk berkonsultasi.
7. Seluruh bapak dan ibu dosen FST UNAIR yang telah member dan membekali kami dengan ilmu dan moral.
8. Mas Budi (Lab. ITS), Mbak Iis dan Ibu Har (Material ITS), Mbak Diah (UBAYA), Mbak Rosi dan Mbak Putri (PUSVETMA) yang telah melancarkan peminjaman alat sintesis sampel dan pengujian sampel.
9. Seluruh angkatan 2008 Teknobiomedik, Biomatlovers (Fara, Agnes, Adit, Miranda, Windy, Ary, Yuyun, Arindha, Wida, Wita, Nurul) yang menemani dan bersama berjuang dalam dan luar lab, teman-teman instrumentasi medis yang telah bersama selama ini, Riska dan Ima (let’s sing along), temen-temen LapanC, teman-teman Universitas Negeri Malang (Popy, Titis, Choir).
10. Staf dan karyawan FSAINTEK UNAIR, serta semua pihak yang telah membantu penyusun selama proses penyusunan naskah skripsi ini.
Penyusun menyadari bahwa naskah skripsi ini masih banyak kekurangan. Oleh karena itu, kritik dan saran yang membangun sangat diharapkan untuk perbaikan naskah skripsi ini.
Surabaya, 14 September 2012
Penyusun
Umami, Gilang Daril, 2012, Sintesis Dan Karakterisasi Biokompatibilitas Si:Ca10(PO4)6(OH)2 Dengan Metode Hidrotermal Untuk Aplikasi Bone Filler.
Skripsi di bawah bimbingan Ir. Aminatun, M.Si, Departemen Fisika dan Dr. Dwi Winarni, M.Si, Departemen Biologi, Fakultas Sains dan Teknologi, Universitas Airlangga, Surabaya
ABSTRAK
Telah dilakukan sintesis hidroksiapatit dan silikon-hidroksapatit kandidat
bone filler dengan metode hidrotermal. Prosedur penelitian dilakukan dengan mencampurkan kalsium nitrat tetrahidrat yang dilarutkan dalam aquades dan di tambah NH3. Kemudian, ammonium trifosfat juga dilarutkan dalam aquades dan
ditambah NH3. Kedua larutan ini dicampur untuk kemudian di stirrer selama 30
menit. Untuk sampel Si-HA, ditambahkan TEOS terlebih dahulu sebelum di
stirrer. Penambahan TEOS dengan variasi berat sebesar 0; 0,2; 0,4; 0,6; 0,8. Tahap selanjutnya adalah proses hidrotermal 200oC, dicuci, dikeringkan 100oC
dan sintering 800oC. Berdasarkan uji mikroskopik (XRD) ditunjukkan
terbentuknya hidroksiapatit dan trikalsium fosfat pada semua sampel, tidak terbentuk puncak baru setelah penambahan silikon. Hasil FTIR hidroksiapatit terdeteksi adanya gugus fosfat (PO43-), gugus karbonat (CO32-) dan gugus
hidroksil (OH-). Hasil FTIR silikon-hidroksiapatit pada sampel IV, sampel yang
memiliki variasi Si sebesar 0,6 %berat, terdeteksi gugus fungsi pada 812,849 cm-1
diindikasi sebagai vibrasi Si-O. Hasil uji MTT menunjukkan sel hidup pada semua sampel. Sampel silikon-hidroksiapatit pada variasi 0,2% berat Si memiliki sel hidup paling banyak sebesar 95,85473% menunjukkan sampel II lebih bioaktif dari sampel yang lain.
Umami, Gilang Daril, 2012, Synthesis and Biocompatibility Characteristic of Si:Ca10(PO4)6(OH)2 with Hydrothermal Method for Bone Filler Aplication.
Final project was under guidance of Ir. Aminatun, M.Si, Department of Physics and Dr. Dwi Winarni, M.Si, Department of Biology, Faculty of Science and Technology, Airlangga University, Surabaya
ABSTRACT
In this study, hydroxyapatite and silicon-hidroksapatit for bone filler candidate has been done by hydrothermal method. Procedure of the research done by mixing calcium nitrate tetrahydrate was dissolved in distilled water and added NH3. Then, ammonium triphosphate was also dissolved in distilled water and
added NH3. The two solutions are mixed for later stirrer for 30 minutes. For Si-HA samples, added TEOS before in stirrer. The addition of TEOS to the weight variation of 0; 0.2; 0.4; 0.6; 0.8. The next stage is the process of hydrothermal 200oC, washed, dried 100oC and 800oC sintering. Based on microscopic assay
(XRD) indicated the formation of hydroxyapatite and tricalcium phosphate in all samples, no new peaks formed after the addition of silicon. FTIR results of hydroxyapatite detected phosphate (PO43-), group carbonate (CO32-) and hydroxyl
groups (OH-). FTIR results of silicon-hydroxyapatite on sample IV, which has a
variety of samples of 0.6 wt% Si, detected functional groups at 812.849 cm-1 is
indicated as Si-O vibrations. The results of MTT assay showed live cells in all samples. Samples of silicon-hydroxyapatite on a variation of 0.2% by weight Si has the maximum amount of live cells showed samples II 95.85473% more bioactive than other samples.
DAFTAR ISI
2.1.4 Pertumbuhan dan perbaikan tulang ... 11
2.2 Bone graft ... 14
2.3 Biomaterial ... 15
2.2.1 Hidroksiapatit . ... 16
2.4 Silikon ……... ... 17
2.7 Silikon-hidroksiapatit ... 21
2.8 X-Ray Diffraction (XRD) ... 23
2.8 Fourier transform infrared spectroscopy (FTIR) ... 25
2.9 MTT assay ….. ... 26
BAB III METODE PENELITIAN... 29
3.1 Waktu dan tempat penelitian ... 29
3.2 Bahan dan peralatan penelitian ... 29
3.2.1 Bahan penelitian ... 29
3.2.2 Alat penelitian ... 30
3.3 Prosedur penelitian ... 30
3.3.1 Persiapan sampel ... 31
3.3.2 Pembuatan sampel ... 31
3.3.3 Sintesis hidroksiapatit dan silikon-hidroksiapatit ... 32
3.3.4 Karakterisasi sampel ... 32\
BAB IV HASIL DAN PEMBAHASAN ... 36
4.1 Hasil ………. ... 36
4.1.1 Hasil uji XRD ... 36
4.1.2 Hasil uji FTIR ... 41
4.1.3 Hasil uji MTT assay ... 45
4.2 Pembahasan ... 46
BAB V KESIMPULAN DAN SARAN ... 50
5.1 Kesimpulan ... 50
5.2 Saran ... 50
DAFTAR TABEL
Nomor Judul Tabel Halaman
2.1 Kandungan unsur anorganik pada tulang ... 8
2.2 Sifat fisis dan mekanik polikristal hidroksiapatit ... 16
3.1 Variasi komposisi Si-HA ... 32
4.1 Persen intensitas HA dan TCP dalam tiap sampel ... 40
4.2 Parameter kisi dari HA dan Si-HA ... 41
4.3 Puncak spektra sampel I sampai V... 45
DAFTAR GAMBAR
Nomor Judul Gambar Halaman
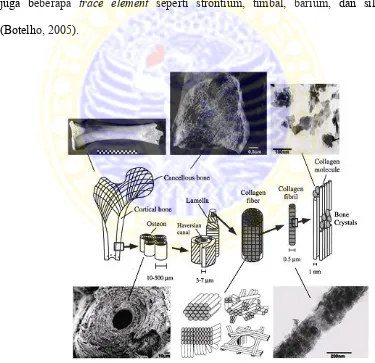
2.1 Gabungan skematik dan mikrografi dari struktur hirearki dari tulang ... 7
2.2 Transmisi electron mikrograf dari tulang ... 9
2.3 Sketsa osteoblas ... 10
2.4 Mikrograf elektron dari osteosit, menunjukkan retikulum endoplasma (rER) yang besar dan Golgi ... 10
2.5 Gambar sketsa dari osteoklas meresordsi tulang, a – adesi dan sitodeferensiasi; b – sekresi dan resorpsi ... 11
2.6 Proses dari osifikasi endokondral... 12
2.7 a. Bentuk kontak antar partikel serbuk, b. Pembentukan awal batas butir, c. Pembesaran batas butir tahap pertengahan dan pengecilan pori, d. Bentuk batas butir pada akhir sintering ... 20
2.8 Skema dari difraksi sinar X ... 23
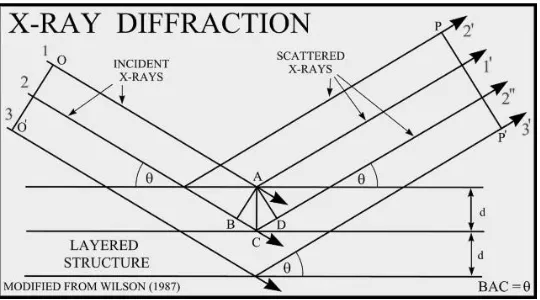
2.9 Sinar X didifraksikan oleh lapisan atom dari material kristal ... 24
2.10 Skema dari FTIR ... 26
2.11 MTTassay plate ... 28
3.1 Diagram alir penelitian ... 30
3.2 Bahan dasar pembuatan HA dan Si-HA. a – kalsium nitrat tetrahidrat, b – ammonium fosfat, c – TEOS ... 31
3.3 Alat Xpert-Pro PANalytical ... 33
3.4 Alat FTIR Bruker Tensor 27 ... 33
3.5 Pellet dari campuran sampel dan KBr ... 34
4.1 Grafik search match XRD sampel HA sebelum sintering ... 37
4.2 Grafik search match XRD sampel I (HA) ... 37
4.3 Grafik search match XRD sampel II (0,2%Si – HA) ... 38
4.4 Grafik search match XRD sampel III (0,4%Si - HA) ... 38
4.5 Grafik search match XRD sampel IV (0,6% Si – HA) ... 39
4.8 Grafik FTIR sampel I (HA) ... 42
4.9 Grafik FTIR sampel II (0,2%Si – HA)... 42
4.10 Grafik FTIR sampel III (0,4%Si – HA) ... 43
4.11 Grafik FTIR sampel IV (0,6%Si – HA) ... 43
4.12 Grafik FTIR sampel V (0,8%Si – HA) ... 44
4.13 Grafik variasi pesentase Si terhadap viabilitas sel ... 46
DAFTAR LAMPIRAN
Nomor Judul Lampiran
Lampiran 1 ICDD Trikalsium Fosfat Lampiran 2 ICDD Hidroksiapatit
Lampiran 3 Data hasil XRD sampel HA sebelum sintering Lampiran 4 Data hasil XRD sampel I (HA)
Lampiran 5 Data hasil XRD sampel II (0,2% Si - HA) Lampiran 6 Data hasil XRD sampel III (0,4% Si - HA) Lampiran 7 Data hasil XRD sampel IV (0,6% Si - HA) Lampiran 8 Data hasil XRD sampel V (0,8% Si - HA) Lampiran 9 Data hasil FTIR sampel I (HA)
Lampiran 10 Data hasil FTIR sampel II (0,2% Si - HA) Lampiran 11 Data hasil FTIR sampel III (0,4% Si - HA) Lampiran 12 Data hasil FTIR sampel IV (0,6% Si - HA) Lampiran 13 Data hasil FTIR sampel V (0,8% Si - HA) Lampiran 14 Hasil dan perhitungan uji MTT
“Menjaga amanah dan berkata jujur
dapat mendatangkan rezeki,
sedangkan khianat dan berkata
bohong dapat mendatangkan
kefakiran dan kemunafikan”
a.s.-BAB I PENDAHULUAN
1.1. Latar Belakang
Tingkat kecelakaan transportasi dan frekuensi bencana alam di Indonesia, dalam kurun waktu sepuluh tahun terakhir terbilang cukup tinggi. Kecelakaan transportasi dan kecelakaan tersebut dapat menjadi salah satu penyebab terjadinya patah tulang. Jumlah kasus operasi patah tulang di RS Sanglah di Denpasar, pada bulan Januari, mencapai 24 orang. Jumlah tersebut hanya pasien yang masuk di IRD. Tiap satu kamar operasi di Instalasi Bedah Sentral (IBS), rata-rata pasien patah tulang tiap hari mencapai 2-3 pasien (Bali post, 2011).
Melihat cukup banyaknya kasus operasi patah tulang, diperlukan penanganan yang tepat pada kasus patah tulang atau kerusakan tulang. Hal ini merupakan pekerjaan yang serius sehingga membutuhkan material yang tepat untuk implan tulang, mengingat tulang memiliki fungsi yang penting sebagai penyokong tubuh. Material yang digunakan haruslah biokompatibel, tidak beracun dan berintegrasi dengan cepat. Dengan kata lain, material ini haruslah menyerupai sifat dari tulang asli.
regenerasi tulang di tempat implantasi. Bone graft yang bagus harus memiliki beberapa karakteristik, antara lain: memiliki kemampuan untuk membentuk tulang, permukaannya harus dapat menstimulasi sel tulang untuk berdifferensiasi, mempunyai permukaan yang bioaktif sehingga jaringan tulang dapat beregenerasi. Dengan kata lain, material tersebut harus osteogenic, osteoinductive dan
osteoconductive. Bonegraft dapat dibedakan menurut asalnya, autograft jika jaringan tersebut diperoleh dari pasien itu sendiri, allograft jika jaringan tersebut diperoleh dari donor lain tetapi masih satu spesies, xenograft jika jaringan tersebut diperoleh dari donor lain dan berbeda spesies atau bone graft sintetis (alloplastic) (Botelho, 2005). Salah satu contoh dari bone graft sintetis (alloplastic) adalah bone filler, yaitu material implan osteokonduktif yang digunakan untuk mengisi rongga dan celah, contoh rongga di tulang kaki, tulang belakang atau panggul, yang menganggu stabilitas struktur tulang. Biasanya, rongga ini didapat dari cacat saat pembedahan atau cedera traumatis ke tulang.
Biokeramik menjadi salah satu jenis dari bone graft sintetis yang diminati. Hal ini dikarenakan biokeramik dapat digunakan untuk mengisi ruang, sebagai coating
atau sebagai komposit. Biokeramik dapat dibagi berdasarkan reaksi biologis yang dimiliki, yaitu inert, bioaktif dan resorbable. Hidroksiapatit termasuk biokeramik yang bersifat bioaktif (Botelho, 2005).
\ Hidroksiapatit (HA) memiliki rumus kimia Ca10(PO4)6(OH)2, adalah
dari dua dekade, banyak usaha yang telah dilakukan untuk membuat hidroksiapatit untuk aplikasi jaringan tulang karena biokompatibilitas dan bioaktivitasnya yang bagus (Kothapalli dalam Bang, 2009).
Silikon (Si) berperan dalam perkembangan tulang dan kerangka. Peran dari silikon dalam sistem kerangka pertama kali ditulis oleh Carlisle yang menemukan bahwa osteosit tulang tibia dari tikus dan mencit mengandung silikon sebanyak 0.5% berat (Coe, 2008). Silikon dalam tulang manusia terdapat sekitar ≤ 1% berat dan termasuk elemen trace level. Meskipun jumlah silikon ini kecil, tapi silikon berperan dalam pertumbuhan atau kalsifikasi tulang (Pietak et al. dalam Aminian et al., 2011), sehingga Si ditambahkan pada HA dan membentuk Si-HA untuk meningkatkan bioaktivitasnya.
Silikon-hidroksiapatit atau Si-HA dapat disintesis dengan berbagai cara, setiap cara memiliki keunggulan dan kelemahan. Ruys (Coe, 2008) melakukan sintesis Si-HA dengan metode sol-gel. Namun metode ini menimbulkan fase sekunder seiring dengan pemberian silikon. Boyer et al., 1997 menggunakan metode
Metode selain yang disebutkan di atas adalah metode hidrotermal. Metode hidrotermal biasanya dapat menghasilkan derajat kristalinitas yang tinggi dan rasio Ca/P yang dekat dengan nilai stokiometri. Ukuran kristal yang dihasilkan melalui metode ini memiliki rentang dari nanometer sampai mikrometer. (C. M. Botelho et al.
dalam Aminian et al., 2011). Kenyataannya, hanya metode hidrotermal dan presipitasi yang menyebabkan pembentukan bahan monofase (M. Palard, 2008).
Berdasarkan kajian terhadap berbagai metode sintesis Si-HA seperti yang disebutkan di atas maka pada penelitian kali ini, akan dilakukan sintesis Si-HA dengan metode hidrotermal menggunakan hidroksiapatit sintetis dan variasi % berat Si sebesar ≤ 1% berat, sehingga diharapkan diperoleh jumlah Si yang tepat dan dapat meningkatkan bioaktivitas untuk dikembangkan sebagai biomaterial implan tulang.
1.2. Rumusan Masalah
Berdasarkan latar belakang di atas, maka dapat dirumuskan beberapa permasalahan sebagai berikut.
1.3. Batasan Masalah
Dalam penelitian ini, penulis membatasi masalah agar tidak menyimpang dari tujuan.
1. Variasi TEOS sebagai sumber Si sebesar 0; 0,2; 0,4; 0,6; 0,8 %berat.
2. Karakterisasi mikrokopik menggunakan X-Ray Diffraction (XRD) dan Fourier Transform Infrared Spectroscopy (FTIR)
3. Karakterisasi sitotoksik menggunakan MTT assay sel fibroblast.
1.4. Tujuan Penelitian
1. Mensintesis silikon-hidroksiapatit dengan metode hidrotermal.
2. Mengetahui mikroskopik silikon-hidroksiapatit hasil sintesis hidrotermal. 3. Mengetahui sitotoksik silikon-hidroksiapatit hasil sintesis hidrotermal.
1.5. Manfaat penelitian
BAB II
TINJAUAN PUSTAKA
2.1. Tulang
Tulang merupakan jaringan kuat pembentuk kerangka tubuh manusia. Tulang sebagai pembentuk kerangka manusia memiliki empat fungsi utama yaitu fungsi mekanik, protektif, metabolik dan hemopoietik. Fungsi mekanik yaitu sebagai penyokong tubuh dan tempat melekatnya jaringan otot untuk pergerakan. Fungsi protektif yaitu sebagai pelindung berbagai alat vital dalam tubuh dan sumsum tulang. Fungsi metabolik yaitu sebagai cadangan dan tempat metabolisme berbagai mineral yang penting seperti kalsium dan fosfat. Fungsi hemopoietik yaitu sebagai tempat berlangsungnya proses pembentukan dan perkembangan sel darah (Leeson et al, dalam Dewi, 2009). Tulang merupakan komponen yang sangat penting dalam tubuh manusia, oleh karena itu penanganan yang tepat pada kerusakan tulang merupakan masalah kesehatan yang serius dalam setiap pekerjaan klinik.
2.1.1. Komposisi tulang
Tulang disusun oleh matriks organik, anorganik dan air. Komponen organik menyusun sekitar 20% dari tulang, sedangkan komponen anorganik menyusun sekitar 65% tulang dan sisa 10% air. Komponen organik disusun oleh 80-90% berupa kolagen dan sisanya disusun oleh proteoglycan dan beberapa protein non-kolagen, seperti osteocalcin, osteopontin, bone sialoprotein,
menguatkan bagian organik dengan garam kalsium. Matriks tulang kolagen disusun oleh kolagen tipe I dan V, tetapi kolagen tipe I yang paling berlimpah. Matriks tulang protein memiliki karakteristik yang berbeda-beda, sebagai contoh
osteopontin dan bone sialoprotein mempunyai urutan RGD yang dapat dikenali oleh αvβ3 sehingga membantu pelekatan sel (cell attachment) dan pengikatan HA.
Matriks tulang mineral selalu mempunyai gugus karbonat (CO32-). Tetapi tidak
hanya gugus karbonat, ada juga natrium, magnesium, kalium, florida, klorida dan juga beberapa trace element seperti strontium, timbal, barium, dan silikon (Botelho, 2005).
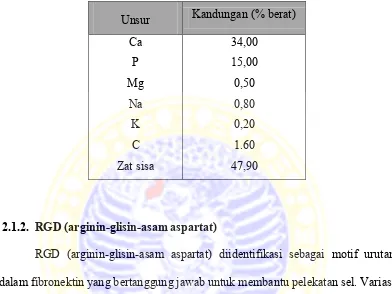
Tabel 2.1. Kandungan Unsur Anorganik pada Tulang (Aoki dalam Prasetyanti, 2008)
Unsur Kandungan (% berat)
Ca 34,00
P 15,00
Mg 0,50
Na 0,80
K 0,20
C 1.60
Zat sisa 47,90
2.1.2. RGD (arginin-glisin-asam aspartat)
RGD (arginin-glisin-asam aspartat) diidentifikasi sebagai motif urutan dalam fibronektin yang bertanggung jawab untuk membantu pelekatan sel. Variasi dari berbagai protein, meliputi protein matriks ekstraseluler, mengandung urutan tripeptida ini yang diperpanjang dan perulangan fleksibel. Fungsi RGD sebagai adhesi sel dan agregasi domain yang dikenal oleh subset dari keluarga reseptor permukaan sel yang dikenal dengan integrin, yang menghubungkan interaksi protein-protein ekstraseluler dengan intraseluler sitoskeleton dari sel.
Peptida ini memasuki sel dan secara langsung menginduksi autoprocessing dan aktifitas enzimatik bentuk zymogen capacase-3, salah satu dari jenis capacase
yang diperlukan untuk kematian sel dengan apoptosis. Peptida RGD mungkin menginduksi apoptosis dengan interaksi langsung dengan tempat pelekatan RGD yang ada dalam procaspase-3, memicu perubahan konformasi yang menimbulkan
autoprocessing dan aktivasi dari procaspase-3 (Anonim, 2003). 2.1.3. Tipe sel tulang
Terdapat tiga tipe sel di dalam tulang yang berhubungan dengan formasi tulang, perawatan dan resorpsi yaitu osteoblas, osteosit dan osteoklas.
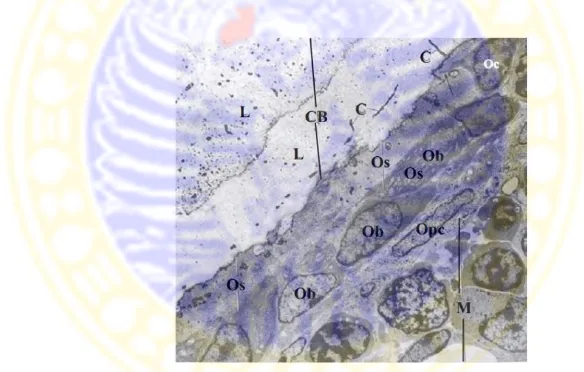
Gambar 2.2. Transmisi elektron mikrograf dari tulang. M – marrow cavity
(rongga sumsum); Opc – osteoprogenitor cells ; Ob –
osteoblasts; Os – osteoid; Oc – osteocyte; CB – calcified bone matrix; C – canaliculi; and L – batas antara dua lamella yang berdekatan (Ross dalam Botelho, 2005)
Gambar 2.3. Gambar skematik osteoblas (Botelho, 2005)
Selama remodelling tulang, beberapa osteoblas terkubur dalam osteoid dan berdeferensiasi menjadi osteosit.
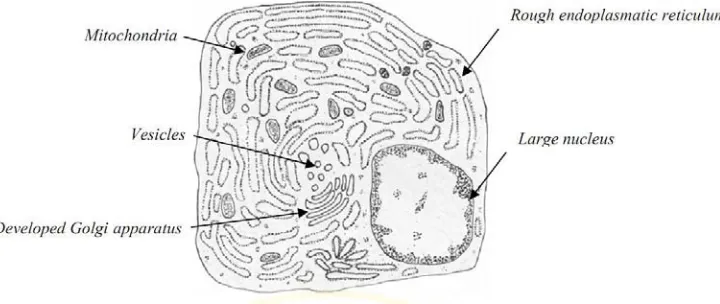
Gambar 2.4. Mikrograf electron dari osteosit, menunjukkan retikulum endoplasma (rER) yang besar dan Golgi (Botelho, 2005)
volume dan organelanya. Seiring waktu, osteosit terletak semakin dalam di tulang mengamulasi glikogen dalam sitoplasma. Diduga, sel ini memiliki peran sebagai mekanosensor dan aktivasi dari pergantian tulang.
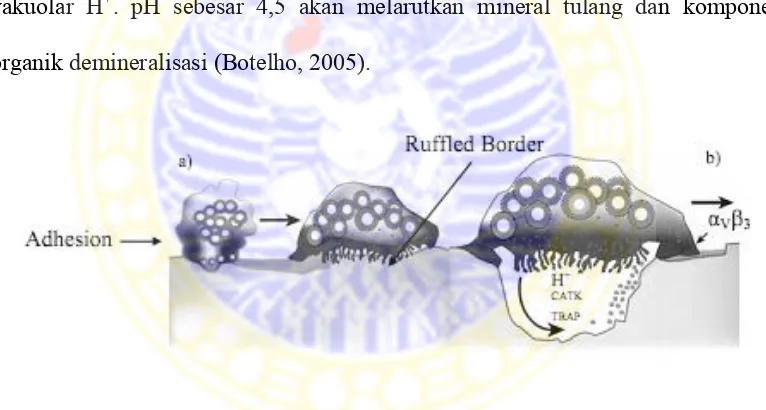
Osteoklas adalah sel besar yang menghancurkan tulang. Sel ini berperan penting dalam proses fisiologi normal dari pergantian tulang dan osifikasi endokondral. Sel ini memiliki banyak nukleus (4-20 nuklei) dan terdeferensiasi sempurna. Osteoklas akan menempel pada tulang yang akan dimakan atau di resorpsi. Proses ini meliputi pengasaman dari lingkungan mikro termediasi oleh vakuolar H+. pH sebesar 4,5 akan melarutkan mineral tulang dan komponen
organik demineralisasi (Botelho, 2005).
Gambar 2.5. Gambar sketsa dari osteoklas meresordsi tulang, a – adesi dan sitodeferensiasi; b – sekresi dan resorpsi (Botelho,2005)
2.1.4. Pertumbuhan dan perbaikan tulang
1. Osifikasi intra membran
Tulang pipih dari tengkorak dan wajah, mandibula klavikula dibentuk melalui osifikasi intra membran. Osifikasi intra membrane ini pertama terjadi pada tahap awal dari perkembangan embrionik. Pada tahap ini, sel mesenkim bergerak dan berkumpul di daerah tertentu, dimana tulang akan terbentuk. Sel mesenkim kemudian berproliferasi dan deferensiasi menjadi sel osteoprogenitor. Beberapa sel yang lain berdeferensiasi menjadi osteoblas. Sel – sel baru ini bertumpuk menjadi tulang rawan (Botelho, 2005).
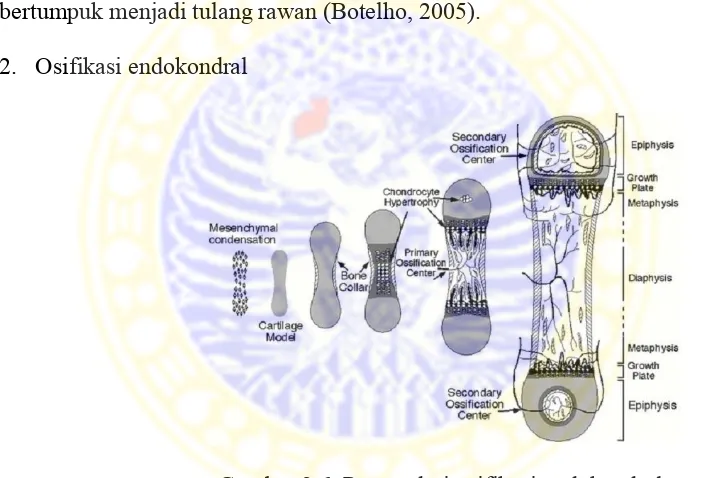
2. Osifikasi endokondral
Gambar 2.6. Proses dari osifikasi endokondral
kondrosit baru yang berdeferensiasi dari lapisan kondrogenik. Osteoblas dibawah perikondrium dalam tulang janin mendepositkan tulang bagian luar dari poros tulang rawan. Saat proses ini terjadi, perikondrium dikenal dengan periosteum, yang mendepositkan lebih banyak lapisan tulang. Lapisan osteogenik dalam periosteum dikarenakan sel di lapisan ini berdeferensiasi menjadi osteoblas (Botelho, 2005).
Penyembuhan tulang dapat dibagi menjadi tiga fase. Fase inflamasi adalah fase pertama dari penyembuhan. Sesegera setelah terjadi fraktur atau patahan, terbentuknya clot darah, diikuti masuknya inflamasi, sel pembersih pada daerah luka. Hal ini diikuti oleh aliran sitokin yang membawa sel perbaikan kedalam celah fraktur. Sel-sel ini dengan segera memulai berdifferensiasi menjadi sel yang terspesialisasi membangun jaringan tulang baru (osteoblas) dan kartilago atau tulang rawan baru (kondroblas). Beberapa bulan kemudian, sel-sel ini mulai proses perbaikan, meletakkan matriks tulang dan kartilago baru. Di tahap awal ini, sel osteoklas larut dan memakai kembali serpihan tulang.
Kedua, tahap perbaikan dimulai sekitar dua minggu setelah patahan terjadi. Dalam tahapan ini, protein yang diproduksi oleh osteoblas dan kondroblas mulai bergabung yang dikenal sebagai soft callus. Substansi lembut ini secara bertahap mengeras menjadi hard callus sejalan dengan tulang dirajut selama enam sampai dua belas minggu.
Anyaman tulang berubah menjadi tulang lamella yang lebih kuat karena aksi dari sel osteoblas pembentuk tulang dan sel osteoklas resorpsi tulang (Brown, 2009).
2.2. Bone graft
Bone graft digunakan dalam beberapa prosedur operasi ortopedik untuk mengembalikan keutuhan tulang yang telah diganggu oleh penyakit, trauma atau penuaan dan juga untuk membantu penyembuhan tulang. Bone graft memiliki fungsi mekanik dan biologi yang harus membantu atau mengisi celah dan mempercepat regenerasi tulang pada tempat implantasi. Beberapa karakteristik yang harus dimiliki bone graft adalah kemampuan untuk membentuk tulang atau membawa sel-sel tulang, harus dapat menstimulasi sel osteoprogenitor untuk berdeferensiasi membentuk tulang dan menyediakan permukaan yang bioaktif sehingga jaringan tulang dapat beregenerasi. Ada beberapa macam bone graft, yaitu autograft jika jaringan diperoleh dari tubuh pasien itu sendiri, allograft jika jaringan diperoleh dari donor manusia lain, xenograft jika jaringan diperoleh dari hewan dan bone graft sintetik (Botelho, 2005).
Bone filler merupakan salah satu contoh dari bone graft sintetik. Bone filler ini diharuskan memiliki sifat tidak toksik dan osteokonduktif sehingga dapat digunakan untuk mengisi rongga dan celah, contoh rongga di tulang kaki, tulang belakang atau panggul, yang menganggu stabilitas struktur tulang. Biasanya, rongga ini didapat dari cacat saat pembedahan atau cedera traumatis ke tulang.
teregenerasi. Oleh karena itu, pasien menerima bone filler hanya sekali dan dapat mengurangi beban fisik dan psikis yang dialami jika menerima jenis implan yang lain yang harus diganti beberapa kali.
2.3. Biomaterial
Biomaterial adalah material tak hidup yang digunakan dalam suatu alat medis untuk diterapkan ke dalam tubuh manusia. Biomaterial berinteraksi dengan sistem biologis manusia dalam proses penyembuhan, perbaikan, dan penggantian begian-bagian tubuh manusia. Jenis-jenis biomaterial berdasarkan bahan materialnya, antara lain logam (surgical alloy), polimer (biomedical polimer), keramik (biomedical ceramic), dan komposit (biomedical composite) (Smallman dalam Dyah, 2008).
Suatu material yang diimplantasikan ke dalam tubuh manusia akan menimbulkan satu respon dari jaringan tuan rumah tempat dimana biomaterial tersebut diimplantasikan. Respon tersebut dikategorikan menjadi salah satu dari empat respon yaitu pertama jika material tersebut bersifat toksik maka jaringan sekelilingnya mati (nekrosis), yang kedua yaitu jika material bersifat inert secara biologi maka timbul semacam jaringan ikat di sekeliling jaringan material implant terutama untuk material berbahan logam dan polimer. Ketiga yaitu jika material bersifat bioaktif maka terbentuk ikatan antarmuka (interfacial bond) antara implant dan jaringan, dan yang keempat yaitu jika material bersifat resorbable
biokompatibilitas artinya mempunyai kemampuan bekerja sesuai dengan respon jaringan dan tidak menimbulkan pengaruh buruk.
2.3.1. Hidroksiapatit
Hidroksiapatit (HA) merupakan kristal apatit yang paling stabil. HA termasuk kelompok apatit yang paling banyak digunakan di bidang medis karena memilki sifat biokompatibel dan osteokonduktif. Rumus kimia HA adalah Ca10(PO4)6(OH)2 yang memiliki molar Ca : P adalah 1,67. Struktur HA adalah
heksagonal. Dimensi parameter kisi HA pada tulang adalah nilai a = b = 9,419 Å dan c = 6,880 Å dan sudut α = β = 90o dan γ =120o. (Shi, dalam Dewi, 2009)
Tabel 2.2. Sifat Fisis Dan Mekanik Polikristal HA (Joon et al. dalam Wijayanti, 2010)
Properties Values
Elastic modulus 40-117 GPa
Compressive strength 294 MPa
Bending strength 147 MPa
Hardness (vickers) 3,43 GPa
Melting point 1227 °C
Density 3,16 g/cm3
2.4. Silikon
Silikon atau Si adalah elemen non-metal dengan berat atom 28. Merupakan elemen melimpah kedua di lapisan kerak bumi, dengan persentase 28%. Tetapi sulit ditemukan dalam bentuk elemennya karena reaksi dengan oksigen, membentuk silika dan silikat, yang mana 92%, adalah mineral yang paling umum.
Silikon dalam sistem tulang ditemukan pertama kali oleh Carlisle (Carlisle dalam Coe, 2008) bahwa di dalam tulang anak ayam mengandung 0.5% silikon. Penelitian-penelitian lain pada hewan (ayam dan tikus) telah menunjukkan bahwa peningkatan silikon memiliki efek yang bagus pada sintesis kolagen (Calomme dalam Coe, 2008) dan bila kekurangan menyebabkan penurunan formasi jaringan ikat (Seaborn dalam Coe, 2008). Silikon juga terlihat berpengaruh pada formasi matriks ekstraselular dari tulang dan mineralisasi, ditunjukkan dalam tulang tikus (Carlisie dalam Coe, 2008). Silikon dalam tulang manusia terdapat sekitar ≤ 1% berat atau termasuk elemen trace level. Meskipun jumlah dari silikon ini kecil, tapi silikon berperan dalam pertumbuhan atau kalsifikasi tulang dan sistem jaringan ikat (Pietak et al dalam Aminian et a.l, 2011).
menunjukkan keuntungan yang mungkin didapat dari penyatuan silikon kedalam struktur biomaterial yang ditujukan untuk aplikasi regenerasi jaringan tulang.
2.5. Hidrotermal
Metode sintesis hidrotermal dapat didefinisikan sebagai sebuah proses yang menggunakan reaksi fase tunggal atau heterogen dalam media encer pada suhu tinggi (T>25oC) dan tekanan (P>100kPa) untuk mengkristalkan material
keramik secara langsung dari larutan. Sintesis ini biasanya dilakukan pada tekanan autogeneous (10 bar), yang sesuai dengan tekanan uap dari larutan pada suhu tertentu dan komposisi larutan hidrotermal. Batas atas dari sintesis hidrotermal >1000oC dan tekanan 500 MPa (R. Roy dalam Suchanek et al., 2006).
Namun kondisi yang disukai untuk proses komersial dimana suhu kurang dari 350oC dan tekanan kira-kira kurang dari 50 MPa.
Salah satu keuntungan dari metode sintesis hidrotermal adalah hampir semua bentuk dapat disintesis dengan metode hidrotermal, yaitu serbuk, serat, kristal tunggal, keramik monolitik, dan coating pada logam dan polimer. Keuntungan lain dari metode sintesis hidrotermal ini adalah kemurnian dari bubuk yang disintesis dengan hidrotermal secara signifikan melampaui kemurnian dari material semula. Hal ini dikarenakan impuritas akan dihilangkan dari sistem bersamaan dengan mengkristalnya larutan.
Berbagai bubuk keramik telah bisa disintesis dengan metode hidrotermal. Paling umum adalah material oksida, baik oksida sederhana, seperti ZrO2, TiO2,
kompleks, seperti BaTiO3, SrTiO3, PZT, PbTiO3, KNbO3, KTaO3, LiNbO3, ferit,
apatit, tungstates, vanadates, molybdates, zeolites, dsb., beberapa diantaranya adalah senyawa metastabil, yang tidak dapat diperoleh dengan menggunakan metode sintesis klasik pada suhu tinggi. Teknik hidrotermal ini juga cocok untuk non-oksida, seperti elemen murni (contoh Si, Ge, Te, Ni, berlian, carbon nanotube), selenida (CdSe, HgSe, CoSe2, NiSe2, CsCuSe4), telurida (CdTe,
Bi2Te3, CuxTey, AgxTey), sulfida (CuS, ZnS, CdS, PbS, PbSnS3), fluorida,
nitrida, aresenida, dsb (Suchanek et al., 2006).
Aminian et al. (2011) telah berhasil mensistesis HA dan Si-HA melalui metode hidrotermal menggunakan suhu 200oC. Hal ini ditunjukkan oleh hasil
pencocokan data penelitian dengan data JCPDS. Selain itu, pada suhu 200oC tidak
ditemukan adanya fase yang lain.
Ivankovic et al. (2010) juga telah melakukan penelitian sintesis HA dengan melakukan variasi suhu hidrotermal dari 140oC sampai 220oC. Hasil
penelitian menunjukkan pada suhu 200oC, kalsium karbonat dan ammonium
fosfat yang merupakan bahan pembentuk menjadi HA secara keseluruhan.
2.6. Sintering
diantara butir (proses difusi) dan sumber energi untuk mengaktifkan gerakan tersebut.
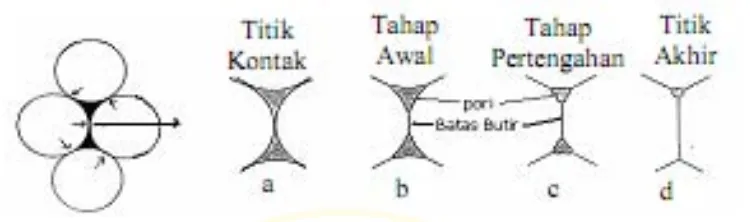
Gambar 2.7. a. Bentuk kontak antar partikel serbuk, b. Pembentukan awal batas butir, c. Pembesaran batas butir tahap pertengahan dan pengecilan pori, d. Bentuk
batas butir pada akhir sintering
banyak jumlah titik kontak tersebut maka makin rendah suhu sintering yang dibutuhkan pelet dalam penyinterannya. Jumlah titik kontak antar partikel tentu juga lebih banyak dan perambatan panas dalam pelet juga lebih cepat, akibatnya laju densifikasi atau laju penyinteran lebih tinggi sehingga suhu penyinterannya lebih rendah (Purwamargapratala dkk, 2007)
Dalam sintesis HA, suhu sintering menentukan fase yang terbentuk. Reaksi pertama yang terjadi dalam material Ca-P adalah kondensasi dari ion HPO42- pada suhu 150-300oC. Ion karbonat juga mulai terdekomposisi menjadi air
dan CO2 pada suhu 100-300oC. Pada suhu yang lebih tinggi (500-1000oC), ion
karbonat terdekomposisi dengan sendirinya menjadi CO2 dan ion O2-. Pada
kisaran suhu 800oC, umumnya terjadi restrukturisasi ulang dari kristal apatit
berdasarkan rasio Ca/P. Pada rasio Ca/P 1,667 terbentuk hidroksiapatit skoikiometri (Sprio, 2008).
2.7. Silikon-hidroksiapatit
Salah satu cara untuk meningkatkan bioaktivitas dari HA adalah dengan menambahkan silikon. Secara lebih spesifik, gugus fosfat dapat disubtitusi dengan gugus silikat.
Beberapa cara telah dilakukan oleh peneliti untuk membuat komposit silikon-HA. Ruys membuat dengan metode sol-gel tetapi fase sekunder dari kalsium silikofosfat [Ca5(PO4)3SiO2] dan α- atau β- TCP terbentuk bergantung
1.71 yang mana lebih tinggi dari 1.67 milik HA, yang mengindikasikan substitusi tidak terjadi. Gibson et al., (1999) membuat 0.4 % berat silikon disubstitusi HA menggunakan metode presipitasi. Penghalusan Rietvelt dari data difraksi menghasilkan penurunan kecil sepanjang sumbu a dan kenaikan di sumbu c dan hal ini diperkirakan karena substitusi dari grup silikat yang lebih besar dari grup fosfat. (Coe, 2008)
Paljar et al.,(2008) melakukan sintesis silikon-HA dengan menggunakan metode hidrotermal. Hasil menunjukkan bahwa TEOS paling cocok untuk reaksi in situ Si-HA. Hasil XRD menunjukkan puncak HA menurun dengan kenaikan jumlah silikon, dan TCP yang terbentuk juga meningkat. Hasil FTIR menunjukkan penurunan intensitas puncak karena subtitusi silikat pada fosfat yang menyebabkan hilangnya beberapa OH-.
Aminian et al. (2011) mensistesis Si-HA melalui metode hidrotermal menggunakan dua fosfat yang berbeda, (NH4)3PO4 dan (NH4)2HPO. Gugus Si
2.8. X-Ray Diffraction (XRD)
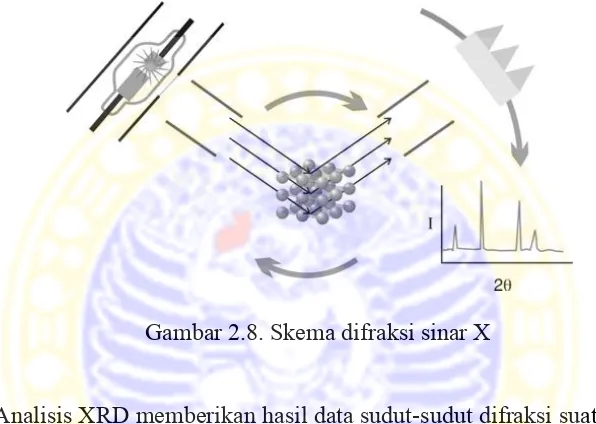
Difraktometer sinar X (XRD) merupakan salah satu peralatan yang digunakan untuk menentukan komposisi senyawa yang terkandung dalam HA. Sinar X ditembakkan ke sampel dan hasil difraksi ini ditangkap oleh detektor untuk ditampilkan dalam bentuk grafik, seperti pada Gambar 2.7.
Gambar 2.8. Skema difraksi sinar X
Analisis XRD memberikan hasil data sudut-sudut difraksi suatu bahan dan besar intensitas difraksi pada sudut difraksi tersebut. Hasil dari analisis XRD menunjukkan fasa-fasa HA.
Gambar 2.9. Sinar X didifraksikan oleh lapisan atom dari material kristal
Suatu berkas sinar-x yang panjang gelombangnya yang jatuh pada suatu
kristal dengan sudut terhadap permukaan himpunan bidang Bragg yang jarak antar bidangnya d. Berkas sinar-x yang didifraksikan oleh atom O dan N yang memenuhi persyaratan ialah sudut difraksi bersama-sama dengan sudut jatuh dari berkas semula terletak sebidang. Selain itu harus memenuhi persamaan Bragg, yaitu
2 d sin = n (2.2)
Dimana d adalah jarak antar bidang, adalah sudut difraksi, n adalah orde difraksi
(n=1,2,3,…) dan adalah panjang gelombang sinar-x.
Dari hasil uji XRD dihasilkan pola difraksi berupa spektrum kontinu yang
meliputi sudut-sudut difraksi pada atom-atom bahan (2 ), besar intensitas (I), nilai
Dengan, Ix adalah jumlah intensitas senyawa X, sedangkan Itotal adalah jumlah intensitas keseluruhan.
2.9. Fourier Transform Infrared Spectroscopy (FTIR)
Fourier transform infrared spectroscopy (FTIR) merupakan metode analisis spektroskopi dengan menggunakan sinar infra merah. FTIR dikembangkan karena adanya kebutuhan untuk bisa mengukur frekuensi inframerah suatu sampel secara bersamaan. Pada spektroskopi ini, sinar infra merah melaju dengan menembus sampel. Spektrum yang dihasilkan menunjukkan transmisi dan absorpsi molekuler, yang hasilnya berupa spektrum. Spektrum infra merah yang dihasilkan oleh dua sampel yang unik dan berbeda akan berbeda juga (Anonim dalam Pratiwi, 2011).
Gambar 2.10. Skema dari FTIR
Analisis sampel pada spektroskopi FTIR diawali dengan dipancarkannya sinar infra merah dari sumber benda hitam. Sinar tersebut melaju dan melewati celah yang mengontrol jumlah energi yang disediakan untuk sampel. Sinar ini masuk ke dalam interferometer di mana ada kode khusus. Hasil interferogramnya kemudian keluar dari interferometer (Anonim dalam Pratiwi, 2011).
Sinar tersebut kemudian memasuki ruang sampel, di mana sinar tersebut ditransmitasikan keluar atau dipantulkan kembali oleh permukaan sampel, tergantung dari tipe analisis yang diselesaikan. Setelah itu, sinar tersebut masuk ke detektor untuk analisis akhir. Hasil analisis akhir diolah menjadi sinyal digital dan dikirimkan ke komputer di mana ada transformasi Fourier di dalamnya.
2.10. MTTassay
MTT adalah molekul larut berwarna kuning, yang dapat digunakan untuk menilai aktifitas enzimatik seluler yang didasarkan pada kemampuan sel hidup untuk mereduksi garam MTT. Prinsip dari pewarnaan MTT adalah dengan pengubahan dari cincin tetrazolium oleh karena aktivitas dari mitokondria pada sel hidup. Pada sel yang mati, tidak terjadi perubahan dari cincin tetrazolium. Mekanisme yang terjadi adalah formazan garam tetrazolium berwarna kuning tersebut akan direduksi di dalam sel yang mempunyai aktivitas metabolik. Mitokondria sel hidup yang berperan penting dalam hal ini adalah mitokondria yang menghasilkan dehidrogenase. Bila dehidrogenase tidak aktif karena efek sitotoksik, maka formazan tidak akan terbentuk. Jumlah formazan yang terbentuk berbanding lurus dengan aktivitas enzimatik sel hidup (Rachadini, 2007)
MTT assay didasarkan pada kemampuan sel hidup untuk mereduksi garam
MTT yang berwarna kuning dan larut menjadi formazan yang berwarna biru-ungu dan tidak larut. Reduksi garam tetrazolium terjadi intraseluler sehubungan dengan enzim succinic dehidrogenae dari mitokondria. Namun Berridge membuktika bahwa reduksi utamanya melibatkan enzim reticulum endoplasma yang bergantung pada NADH, sedangkan enzim mitokondria hanya berperan dalam porsi yang kecil.
pula jumlah sel yang hidup (Rachadini, 2007). Presentase jumlah sel hidup untuk uji MTT dapat dihitung dengan persamaan (2.4)
(2.4)
Dengan % sel hidup = prosentase jumlah sel setelah perlakuan, OD treatment = nilai densitas sampel optik setelah perlakuan, OD control media = nilai densitas media kontrol optik, OD controlcell = nilai densitas sel control optik.
Jumlah sel dapat diukur sebagai hasil produk MTT dengan spektrofotometer pada panjang gelombang 540 – 570 nm, sehingga prosentase densitas optik yang semakin tinggi menunjukkan sel metabolik yang aktif sehingga dapat mereduksi MTT semakin baik pula (Rachadini, 2007).
BAB III
METODE PENELITIAN
3.1. Waktu dan tempat penelitian
Waktu penelitian dilakukan selama ±6 bulan pada tahun 2012. Penelitian ini dilakukan di Laboratorium Fisika Material Fakultas Sains dan Teknologi Universitas Airlangga untuk pembuatan HA dan campuran Si-HA, Laboratorium Studi Energi dan Rekayasa ITS Surabaya untuk sintesis Si-HA dengan metode hidrotermal, Jurusan Teknik Material dan Metalurgi ITS Surabaya untuk uji XRD, Laboratorium Polimer dan Membran Teknik Kimia UBAYA untuk uji FTIR, Laboratorium Peningkatan Mutu dan Pengembangan Produksi Pusat Veterinaria Farma (PUSVETMA) Surabaya untuk MTT assay.
3.2. Bahan dan alat penelitian 3.2.1. Bahan penelitian
Bahan yang digunakan untuk pembuatan sampel dalam penelitian ini yaitu kalsium nitrat tetrahidrat [Ca(NO3)2.4H2O], ammonium trifosfat [(NH4)3PO4],
aquades, larutan NH3, dan Tetra ethyl ortho silicate [Si(OCH2CH3)4]. Untuk MTT
3.2.2. Alat penelitian
Alat yang digunakan untuk pembuatan sampel penelitian ini yaitu spatula, tabung ukur, gelas beaker, corong, pipet, timbangan digital, autoclave, oven, kertas saring. Alat yang digunakan dalam penelitian ini untuk karakterisasi sampel antara lain difraktometer sinar-X (XRD) Xpert-Pro PANalytical, fourier transform infrared spectroscopy (FTIR) Bruker Tensor 27, microplate reader
ELISA.
3.3. Prosedur penelitian
Tahap pelaksanaan dalam penelitian ini yaitu proses pembuatan larutan HA dan variasi larutan Si-HA, proses sintesis HA dan Si-HA, serta proses karakterisasi (XRD, FTIR dan MTT assay).
3.3.1. Persiapan sampel
Bahan dasar dari pembuatan sampel HA dan Si-HA berupa padatan untuk kalsium nitrat tetrahidrat dan ammonium fosfat, berupa cairan untuk TEOS.
(a) (b) (c)
Gambar 3.2. Bahan dasar pembuatan HA dan Si-HA. a – kalsium nitrat tetrahidrat, b – ammonium fosfat, c – TEOS
3.3.2. Pembuatan sampel
Pembuatan sampel dimulai dengan menyiapkan kalsium nitrat tetrahidrat yang dilarutkan dalam aquades dan di tambah NH3 sampai pH lebih dari 10.
Kemudian, ammonium trifosfat juga dilarutkan dalam akuades dan ditambah NH3
sampai pH lebih dari 11. Kedua larutan ini dicampur untuk kemudian di stirrer
Tabel 3.1. Variasi komposisi Si-HA
Nama
Sampel % berat TEOS mol Ca(NO3)g 2 mol (NH4)3POg 4 mol TEOS g
I 0 0,025 5,9 0,0150 2,235 0 0
II 0,2 0,025 5,9 0,0148 2,2052 0,000175 0,0364 III 0,4 0,025 5,9 0,0146 2,1754 0,00035 0,0728 IV 0,6 0,025 5,9 0,0144 2,1456 0,000525 0,1092 V 0,8 0,025 5,9 0,0142 2,1158 0,000725 0,1508
3.3.3. Sintesis hidroksiapatit dan silikon-hidroksiapatit
Larutan awal dari HA dan Si-HA disintesis dengan metode hidrotermal menggunakan autoclave dan oven. Larutan tersebut dimasukkan dalam autoclave dan ditutup rapat. Kemudian autoclave dimasukkan dalam oven dalam suhu 200oC selama 8 jam. Pemilihan suhu 200oC sebagai suhu hidrotermal
dikarenakan pada suhu ini, HA sudah dapat tersintesis tanpa menimbulkan adanya fase yang lain (Aminian et al., 2011 dan Ivankovic et al., 2010). Presipitat hasil kemudian dicuci tiga kali, dan kemudian dikeringkan dalam suhu 100oC
selama 12 jam. Tiap sampel kemudian di sintering dalam suhu 800oC selama satu jam (Aminian et al., 2011). Suhu sintering 800oC ini diharapkan dapat
membentuk HA yang lebih kristalin (Sprio, 2008). 3.3.4. Karakterisasi sampel
3.3.4.1. Uji XRD
setelah itu sampel diletakkan pada alat uji. Hasil uji XRD tersaji dalam bentuk grafik spektrum dan tabel. Pola difraksi berupa spektrum hasil uji XRD memberikan informasi mengenai sudut-sudut terjadinya difraksi pada atom bahan (2 ) pada sumbu horizontal dan besar intensitas yang dihasilkan pada sumbu vertikal. Identifikasi fase diperoleh dengan membandingkan pola difraksi HA dan Si-HA dengan data ICDD. Parameter kisi dari sampel dihitung dengan program PCW (Powder Cell for Windows).
Gambar 3.3. Alat Xpert-Pro PANalytical
3.3.4.2.Uji FTIR
Sampel yang diuji dicampur dengan KBr. Perbandingan KBr:sampel sebesar 1:20. Sampel dan KBr kemudian dicampur dan dibentuk pellet. Pellet
tipis tersebut kemudian dimasukkan ke dalam tabung perangkat FTIR dan disinari, puncak-puncak spektrum karakteristik akan muncul dan bilangan gelombang akan keluar secara otomatis dalam bentuk print out.
Gambar 3.5. Pellet dari campuran sampel dan KBr
3.3.4.3.MTT assay
3.3.4.3.1. Persiapan Kultur Sel
Persiapan dilakukan didalam laminar air flow, kultur sel BHK-21 dalam bentuk monolayer dengan media Eagle’s dan FBS 10% ditanam dalam botol kultur roux, kemudian diinkubasi pada suhu 37°C selama 48 jam. Kultur sel dicuci dengan PBS sebanyak 5 kali yang bertujuan untuk membuang sisa serum yang tersisa. Kemudian ditambahkan tripsine versene untuk melepaskan sel dari dinding botol dan memisahkan ikatan antar sel agar tidak menggerombol. Kemudian tahap terakhir yaitu memasukkan sel dengan kepadatan 2 x 105 dalam
3.3.4.3.2. Uji MTT pada Kultur Sel
Penambahan 25 μL pereaksi MTT 5 mg/mL yang telah dilarutkan dalam PBS dalam media untuk setiap sumuran. Selanjutnya dilakukan inkubasi dalam inkubator selama 4 jam pada suhu 37 °C. Kemudian ditambahkan pelarut DMSO sebanyak 50 μL yang dimasukkan ke setiap sumuran. Kemudian di sentrifuse 30 rpm selama 5 menit. Selanjutnya nilai optik formazan dihitung dengan Elisa reader pada panjang gelombang 630 nm. Makin pekat warnanya, makin tinggi nilai absorbansinya semakin banyak jumlah selnya (Rachadini, 2007).
3.4. Analisis data
Dari data difraksi sinar-X (XRD), dilakukan pencocokan dengan data standar (search match). Hasil search match berupa grafik dengan identifikasi fase dari senyawa-senyawa pada puncak-puncak difraksinya. Penghalusan Rietveld menggunakan data yang diperoleh dengan data standar untuk memperoleh konstanta kisi. Hasil grafik yang menurun dan kontanta kisi yang berbeda dari HA, menunjukkan Si telah bergabung dengan HA. Dari data FTIR dilakukan pencocokan dengan data yang ada untuk menemukan gugus SiO4 sebagai tanda
BAB IV
HASIL DAN PEMBAHASAN
Pada penelitian ini dilakukan sintesis dan analisis sampel HA dan Si-HA. Sampel HA dan Si-HA disintesis menggunakan autoklaf. Langkah berikutnya adalah karakterisasi sampel dengan melakukan beberapa uji. Pengujian sifat mikro menggunakan XRD, dilanjutkan dengan search match untuk mengetahui fasa-fasa yang ada dan penentuan parameter kisi menggunakan program PCW. Pengujian kimia fisis menggunakan FTIR untuk mengetahui struktur molekul dan gugus-gugus karakteristik dalam sampel HA dan Si-HA. Pengujian sitotoksisitas dilakukan menggunakan uji MTT assay.
4.1 Hasil
4.1.1. Hasil Uji XRD
Gambar 4.1. Grafik search match XRD sampel HA sebelum sintering
Gambar 4.2. Grafik search match XRD sampel I (HA) Position [°2Theta] (Copper (Cu))
20 30 40 50
Counts
0 200 400
Hidroksiapatit
Position [°2Theta] (Copper (Cu))
20 30 40 50
Counts
0 500 1000 HA
Hydroxylapatite, syn Calcium Phosphate
Gambar 4.3. Grafik search match XRD sampel II (0,2%Si – HA)
Gambar 4.4. Grafik search match XRD sampel III (0,4%Si - HA)
Position [°2Theta] (Copper (Cu))
20 30 40 50
Counts
0 200 400 600 800
HA+ Si 0,2% Calcium Phosphate Hydroxylapatite, syn
Position [°2Theta] (Copper (Cu))
20 30 40 50
Counts
0 500 1000
Gambar 4.5. Grafik search match XRD sampel IV (0,6% Si – HA)
Gambar 4.6. Grafik search match XRD sampel V (0,8%Si – HA)
Hasil search match dari hidroksiapatit sebelum sintering dan sampel I sampai V ditunjukkan selengkapnya pada lampiran 1. Pada gambar 4.1 sampai 4.6 terlihat grafik search match XRD dengan puncak-puncak difraksi pola struktur
Position [°2Theta] (Copper (Cu))
20 30 40 50
Counts
0 500
1000 HA+ Si 0,6%
Hydroxylapatite, syn Calcium Phosphate
Position [°2Theta] (Copper (Cu))
20 30 40 50
Counts
0 200 400 600
800 HA+ Si 0,8%
kristal. Dari hasil search match yang telah diperoleh, dapat diketahui bahwa sampel I sampai V memunculkan hidroksiapatit (HA) [Ca10(PO4)6(OH)2] dengan
tanda ( ) di puncaknya dan trikalsium fosfat (TKF) [Ca3(PO4)2] dengan tanda ( )
di puncaknya. Persen intensitas HA dan TKF setelah search match dalam tiap sampel ditunjukkan dalam Tabel 4.1.
Tabel 4.1. Persen intensitas HA dan TKF dalam tiap sampel
Sampel Persen intensitas (%)
HA TKF
I 29 71
II 26 74
III 11 89
IV 32 68
V 33 67
Hasil dari perbandingan grafik XRD dari sampel I sampai V ditunjukkan pada gambar 4.7.
0 500 1000 Counts
Position [°2Theta] (Copper (Cu))
20 30 40 50
Dari gambar 4.7 menunjukkan bahwa penambahan TEOS sebagai sumber Si tidak menunjukkan efek yang signifikan atau membentuk puncakbaru dari pola difraksi hidroksiapatit atau HA.
Tabel 4.2. Parameter kisi dari HA dan Si-HA
Parameter ICSD Sampel I Sampel II Sampel III Sampel IV Sampel V
Rp - 37,82 33,42 42,93 35,24 29,83
Rwp - 49,59 44,08 56,37 45,83 39,79
Rexp - 2,38 2,17 2,90 2,28 1,91
Konstanta kisi
a = b 9,419 9,419 9,406 9,349 9,406 9,405
C 6,880 6,897 6,872 6,809 6,870 6,872
Salah satu hasil refinement dari program PCW adalah parameter-parameter kisi kristal, seperti yang terlihat di Tabel 4.2. Dapat dilihat bahwa terjadi sedikit penurunan pada parameter kisi a dan c. Sampel I memiliki nilai parameter kisi yang hampir mendekati nilai parameter kisi HA dari literatur (a = 9,419 Å dan c = 6,880 Å). Sampel II sampai V menunjukkan penurunan pada nilai parameter kisi a dan c dibandingkan dengan sampel I.
4.1.2. Hasil Uji FTIR
Uji FTIR digunakan untuk mengetahui struktur molekul yang terbentuk dalam sampel. Hasil FTIR sampel I sampai V digambarkan dalam grafik spektrum dengan sumbu x sebagai wavenumber (cm-1) dan sumbu y sebagai besarnya nilai
Gambar 4.8. Grafik FTIR sampel I (HA) CO3
2-PO4
3-OH
-OH
-PO4
2-Gambar 4.10. Grafik FTIR sampel III (0,4%Si – HA)
Gambar 4.11. Grafik FTIR sampel IV (0,6%Si – HA) OH
-PO4
3-OH
-PO4
3-CO3
4-Gambar 4.12. Grafik FTIR sampel V (0,8%Si – HA)
Dari uji FTIR diketahui bahwa untuk sampel I yang merupakan HA dan sampel II sampai IV yang merupakan Si-HA (variasi 0,2% - 0,8%) masing-masing menunjukkan gugus serapan karakteristik. Data tersebut digunakan sebagai acuan untuk mendeteksi bergabungnya Si kedalam HA.
Spektrum FTIR karaketeristik HA ditunjukkan oleh frekuensi serapan OH-
pada 3600-3200 cm-1, PO43- pada 1100-960 cm-1 dan 660-450 cm-1, CO32- pada
1550-1410 cm-1 yang berkaitan dengan HA (Aminian et al, 2011). Spektrum FTIR
karakteristik dari sampel I sampai V ditunjukkan dalam Tabel 4.3. OH
-PO4
2-Tabel 4.3. Puncak spektra sampel I sampai V Hasil dari uji toksisitas dibaca menggunakan ELISA Reader. Hasil pembacaan
ELISA Reader dari sampel HA dan Si-HA menunjukkan bahwa sampel tidak bersifat toksik pada sel fibroblas, hal ini ditunjukkan oleh presentase sel yang hidup masih diatas 60% (≥60%) yaitu densitas optik dari perlakuan masih mendekati densitas optik dari kontrol sel. Presentase sel hidup dihitung dengan persamaan (2.4), ditunjukkan dalam Tabel 4.4
Tabel 4.4. Persentase sel fibroblas dengan MTT assay
SAMPEL Optical Density (OD) % sel hidup
I 0.21425 87.8944
II 0.241375 95.85473
III 0.203875 84.8496
IV 0.20075 83.9325
Sampel I menunjukkan hasil uji sebesar 87,8944% yang menunjukkan sampel ini tidak toksik. Sampel II menunjukkan hasil uji sebesar 95,85473%. Sampel III menunjukkan hasil uji sebesar 84.8496%. Sampel IV menunjukkan hasil uji sebesar 83.9325%. Sampel V menunjukkan hasil uji sebesar 86.97726%.
Gambar 4.13. Grafik variasi pesentase Si terhadap viabilitas sel
4.2 Pembahasan
Sintesis hidroksiapatit (HA) dan silikon-hidroksiapatit (Si-HA) menggunakan metode hidrotermal pada suhu 200oC selama 8 jam tanpa sintering menghasilkan hidroksiapatit 100% seperti terlihat pada Gambar 4.1. Namun, dalam grafik ini masih terlihat kurangnya kristalinitas pada sampel. Setelah dilakukan sintering 800oC selama 1 jam, terdeteksi trikalsium fosfat (TKF) pada
sampel I sampai sampel V. TKF yang muncul disini diduga merupakan deformasi dari HA karena HA hasil sintesis masih termasuk stabil sampai pada suhu 750oC dan akan terdekomposi menjadi TKF jika melampaui suhu tersebut (Jain, 2010).
TKF yang muncul disini diduga merupakan β-TKF, hal ini dapat dilihat dari ukuran unit sel a dan c dalam ICDD 01-072-7587 sebesar 10.4352 Å dan 37.4029 Å. Sedikit penurunan intensitas di puncak HA pada grafik XRD sampel II sampel V dapat dikarenakan subtitusi dari beberapa gugus PO43- dengan SiO44-
sehingga HA menjadi kehilangan beberapa sifat kristalinitasnya (Nakata et al, 2009).
Gambar 4.14. Skema struktur heksagonal HA
Bidang sepanjang kisi a dalam HA banyak diisi oleh ion kalsium (Ca) yang bermuatan positif, sedangkan sepanjang kisi c diisi oleh grup fosfat (P) yang bermuatan negatif. Data penelitian menunjukkan bahwa terjadi penurunan pada nilai parameter kisi a dan c. Hal ini diduga disebabkan oleh terdeformasinya HA menjadi TKF, mengingat jumlah ion Ca dan P pada HA dan TKF. HA memiliki ion 10 Ca dan 6 P sedangkan TKF memiliki ion 3 Ca dan 3 P.
Hasil FTIR menunjukkan gugus OH- dan PO
43- yang merupakan gugus
ini kemungkinan disebabkan gugus karbonat hilang waktu kalsinasi. Pada sampel IV menunjukkan puncak pada 812,849 cm-1 yang terindikasi sebagai vibrasi Si-O. Tidak terdeteksinya puncak Si pada sampel yang lain, diduga dapat disebabkan campuran larutan yang kurang homogeny sehingga Si tidak terikat secara sempurna dalam struktur HA. Hal lain yang dapat mempengaruhi tidak terdeteksinya SiO44- dalam uji FTIR adalah temperatur sintering. Dalam sintering
suhu tinggi, keramik oksida logam terkadang dapat terdekomposisi karena proses dehidrasi atau oksidasi melalui interaksi dengan gas lingkungan (Kokubo, 2008).
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari hasil penelitian dan pembahasan yang telah dilakukan, dapat disimpulkan bahwa :
1. Hidroksiapatit dan silikon-hidroksiapatit dapat disintesis dengan metode hidrotermal, namun memunculkan fase sekunder yaitu trikalsium fosfat (TKF).
2. Hasil XRD menunjukkan penambahan silikon tidak menunjukkan puncak difraksi baru dan terjadi penurunan pada parameter kisi a dan c. Hasil FTIR menunjukkan gugus karakteristik OH-, PO43-, CO32- yang termasuk dalam
hidroksiapatit. Puncak dari gugus Si-O muncul pada sampel IV pada 812,849 cm-1.
3. Hasil MTT assay menunjukkan semua sampel tidak toksik pada sel fibroblas. %sel hidup paling besar ditunjukkan pada sampel II (0,2%Si – HA).
5.2 Saran
Untuk mendapatkan hasil yang lebih baik, perlu dilakukan:
1. Penggunaan variasi suhu dan lama waktu sintering sehingga kemunculan trikalsium fosfat dapat dihindari.
3. Variasi silikon lebih kecil dari 0,2% silikon-hidroksiapatit untuk mengetahui pengaruhnya pada viabilitas sel yang dihasilkan.
DAFTAR PUSTAKA
Aminian, Alieh, Mehran Solati-Hashjin, Ali Samadikuchaksaraei, Farhad Bakhshi, Fazel Gorjipour, Arghavan Farzdi, Fattolah Moztarzadeh, Martin Schmiicker. 2011. Synthesis of silicon-substituted hydroxyapatite by a hydrothermal method with two different phosphorous sources. Ceramic International 37 page 1219-1229.
Anonim. 2011. Pasien Bedah Ortopedi di RS Sanglah Antre Sampai 24 Orang,
Kebanyakan Multitrauma. http://www.balipost.co.id/mediadetail.php?
Anonim. 2001. The O’ Cells. http://depts.washington.edu/bonebio/bonAbout/bone cells.html [diakses pada tanggal 30 Desember 2011].
Bang, Le Thi. 2009. Synthesis And Characterization Of Hydroxyapatite (Ha) And Silicon Substituted Hydroxyapatite (Si-Ha) Produced By A Precipitation
Method. Thesis of AUN/SEED-Net, Penang
Botelho, Cláudia Manuela da Cunha Ferreira. 2005. Silicon-Substituted Hydroxyapatite for Biomedical Applications. Thesis of Faculdade de Engenharia Universidade do Porto. Thesis of Faculdade de Engenharia Universade do Porto.
Brown, Susan E.. 2009. How To Speed Fracture Healing, Center for Better Bone. New York. Center for Better Bones.
Coe, Samuel Christopher, BSc (Hons). 2008. The Deposition, Characterisation and Biocompatibility of Hydroxyapatite and Silicon Doped Hydroxyapatite Thin Film Coatings for Orthopaedic Applications. Thesis of The University of Nottingham.
Dewi, Setia Utami. 2009. Pembuatan Komposit Kalsium Fosfat – Kitosan dengan Metode Sonikasi. Tesis Sekolah Pascasarjana Institut Pertanian Bogor. Jain, Sakshi. 2010. Processing of Hydroxyapatite by Biomimetic Process. Thesis
Kokubo, Tadashi. 2008. Bioceramics and their clinical applications. England. Woodhead Publishing Limited, Abington Hall, Abington.
Nakata, Kentaro, Takashi Kubo, Chiya Numako, Takamasa Onoki, Atsushi Nakahira. 2009. Synthesis and Characterization of Silicon-Doped Hydroxyapatite. Material Transactions vol 50 no 5 page 1046-1049. Palard, Mickael, Eric Champion, Sylvie Foucaud. 2008. Synthesis of silicated
hydroxyapatite Ca10(PO4)6-x(SiO4)x(OH)2-x. Journal of Solid State Chemistry vol 181 page 1950-1960.
Pramodhawardhani, Anjartika, 2010, Mekanisme Pembentukan Tulang, Fakultas Kesehatan Masyarakat Universitas Jember.
Prasetyanti, Fitriani. 2008. Pemanfaatan Cangkang Telur Ayam untuk Sintesis Hidroksiapatit dengan Reaksi Kering. Skripsi FMIPA Institut Pertanian Bogor.
Pratiwi, Niken. 2011. Sintesis dan Karakterisasi Hidroksiapatit Scaffold. Skripsi FMIPA Institut Pertanian Bogor.
Prihartini, Ardini. 2011. Sintesis dan Karakterisasi Semen Gigi Berbasis Nano Zinc Oxide. Skripsi FMIPA Universitas Airlangga.
Purwamargapratala, Yustinus, Didin S.Winatapura, Engkir Sukirman. 2007.
Pengaruh Suhu Dan Waktu Sinter Terhadap Penumbuhan Fasa Superkonduktor Gdba2cu3o7-X. Tangerang. Pusat Teknologi Bahan Industri Nuklir (PTBIN)-BATAN.
Rachadini, Novianita. 2007. Uji Sitotoksisitas Ekstrak Serbuk Kayu Siwak (Salvadora Persica) Pada Kultus Sel Fibroblas Dengan Uji MTT. Skripsi FKG Universitas Airlangga.
Sadi, Amir Yadi, Mohammad Ali Shokrgozar, Seyed Shahin Homaeigohar, Alireza Khavandi. 2007. Biological evaluation of partially stabilized zirconia added HA/HDPE composites with osteoblast and fibroblast cell lines. J Mater Sci: Mater Med vol 19 page 2359-2365.
Sprio, Dott. Simone. 2008. Synthesis And Characterization Of Implants For Bone Substitutions Made Of Biomedical Apatites Containing Silicon. Thesis of Alma Mater Studiorum – Università di Bologna.
Suchanek, Wojciech L. dan Richard E. Riman. 2006. Hydrothermal Synthesis of
Advanced Ceramic Powders. Advances in Science and Technology vol. 45
Lampiran 1. ICDD Trikalsium Fosfat
Formula from original source: Ca3 (P O4)2
I CSD Collection Code: 97500
Calculated Pattern Original Remarks: Stable from 193 to 1408 K (2nd ref.,
Unit Cell Data Source: Powder Diffraction.
References
Primary reference: Calculated from ICSD using POWD-12+ +
Structure: Hoshikawa, A., Kamiyama, T., Sakai, A., Yashima, M.,
Lampiran 2. ICDD Hidroksiapatit
Name and formula
Reference code: 01-072-1243
Mineral name: Hydroxylapatite, syn
Compound name: Calcium Phosphate Hydroxide
Formula from original source: Ca10 (P O4)6 (O H)2
I CSD Collection Code: 16742
Calculated Pattern Original Remarks: New refinement based on previously measured
intensities
Minor Warning: No e.s.d reported/ abstracted on the cell dimension.
7% < R factor< 12% (for single crystal)
Wyckoff Sequence: i h4 f a(P63/ M)
Unit Cell Data Source: Single Crystal.
References
Primary reference: Calculated from ICSD using POWD-12+ + , (1997)
Structure: Posner, A.S., Diorio, A.F., Acta Crystallogr., 11, 308,
Lampiran 3. Data hasil XRD sampel HA sebelum sintering
Anchor Scan Parameters
Dataset Name: Hidroksiapatit
File name: E:\ Data\ DATA PENGUJI AN\ Agustus\ Gilang\ Hidroksiapatit.xrdml
Comment: Configuration= Reflection-Transmission Spinner, Owner= User-1,
Creation date= 12/ 2/ 2011 8:19:55 AM
Goniometer= PW3050/ 60 (Theta/ Theta); Minimum step size 2Theta:0.001; Minimum step size Omega:0.001
Sample stage= Reflection-Transmission Spinner PW3064/ 60; Minimum step size Phi:0.1
Diffractometer system= XPERT-PRO
Measurement program= C:\ PANalytical\ Data Collector\ Programs\ scan 10-60_spin.xrdmp, I dentifier= {
2A5A38DC-5C72-434B-9732-ACCA00EEB45E} Scan 10-60
Measurement Date / Time: 8/ 9/ 2012 8:13:54 AM
Operator: I nstitut Teknologi
Raw Data Origin: XRD measurement (* .XRDML)
Scan Axis: Gonio
Measurement Temperature [ °C] : 25.00
Anode Material: Cu
K-Alpha1 [ Å]: 1.54060
K-Alpha2 [ Å]: 1.54443
K-Beta [ Å] : 1.39225
K-A2 / K-A1 Ratio: 0.50000
Generator Settings: 30 mA, 40 kV
Diffractometer Type: 0000000011119014
Diffractometer Number: 0
Goniometer Radius [ mm] : 240.00
Dist. Focus-Diverg. Slit [ mm] : 100.00 I ncident Beam Monochromator: No
Spinning: No
Graphics
Peak List
43.9607 24.27 0.4684 2.05974
- Modification time = "8/ 14/ 2012 10:37:26 AM" - Modification editor = "Teknik Material"
Default properties:
- Measurement step axis = "None"
- I nternal wavelengths used from anode material: Copper (Cu) - Original K-Alpha1 wavelength = "1.54060"
- Used K-Alpha1 wavelength = "1.54060" - Original K-Alpha2 wavelength = "1.54443" - Used K-Alpha2 wavelength = "1.54443" - Original K-Beta wavelength = "1.39225" - Used K-Beta wavelength = "1.39225" - I rradiated length = "10.00000" - Spinner used = "No"
- Receiving slit size = "0.10000" - Step axis value = "0.00000" - Offset = "0.00000" - Sample length = "10.00000"
- Step Size = "0.01"
- Modification time = "8/ 14/ 2012 10:37:26 AM" - Modification editor = "PANalytical"
- Method = "Minimum 2nd derivative" - Modification time = "7/ 16/ 2012 11:31:58 AM" - Modification editor = "Teknik Material"
Search & Match:
- Allow pattern shift = "Yes" - Auto residue = "Yes"
- Data source = "Profile and peak list" - Demote unmatched strong = "Yes" - Multi phase = "Yes" - Minimum scale factor = "0.1" - I ntensity threshold = "0" - Use line clustering = "Yes" - Line cluster range = "1.5" - Search sensitivity = "1.8" - Use adaptive smoothing = "Yes" - Smoothing range = "1.5" - Threshold factor = "3"
Lampiran 4. Data hasil XRD sampel I (HA)
This is the simple example template containing only headers for each report item and the bookmarks. The invisible bookmarks are indicated by text between brackets.
Modify it according to your own needs and standards.
Measurement Conditions: (Bookmark 1)
Dataset Name HA
File name E:\ Data\ DATA PENGUJI AN\ Juli\ Gilang UNAIR\ HA\ HA.xrdml
Comment Configuration= Reflection-Transmission Spinner, Owner= User-1,
Creation date= 12/ 2/ 2011 8:19:55 AM
Goniometer= PW3050/ 60 (Theta/ Theta); Minimum step size
2Theta:0.001; Minimum step size Omega:0.001
Sample stage= Reflection-Transmission Spinner PW3064/ 60;
Minimum step size Phi:0.1
Diffractometer system= XPERT-PRO
Measurement program= C:\ PANalytical\ Data Collector\ Programs\ scan
10-60_spin.xrdmp, I dentifier= { 2A5A38DC-5C72-434B-9732-ACCA00EEB45E}
Scan 10-60
Measurement Date / Time 7/ 11/ 2012 9:03:39 AM
Operator I nstitut Teknologi
Raw Data Origin XRD measurement (* .XRDML)
Scan Axis Gonio
Measurement Temperature [ °C] 25.00
Anode Material Cu
K-Alpha1 [ Å] 1.54060
K-Alpha2 [ Å] 1.54443
K-Beta [ Å] 1.39225
K-A2 / K-A1 Ratio 0.50000
Generator Settings 30 mA, 40 kV