ABSTRAK
EFEK ANTIMIKROBA EKSTRAK ETANOL DAUN SALAM (Syzygium polyanthum) TERHADAP Escherichia coli DAN Bacillus subtilis
SECARA IN VITRO
Vanny Setiawan, 2014; dr. Penny Setyawati Martioso, SpPK., M.Kes
Foodborne illness merupakan masalah kesehatan masyarakat Indonesia. Keracunan makanan akibat kontaminasi dengan bakteri disebabkan karena kebersihan diri dan sanitasi lingkungan yang kurang baik. Ekstrak daun salam (Syzygium polyanthum) mengandung minyak atsiri, tanin, flavonoid, alkaloid, and saponin yang diduga memiliki efek antimikroba.
Tujuan penelitian ini adalah untuk mengetahui efek antimikroba ekstrak etanol daun salam terhadap pertumbuhan koloni Escherichia coli dan Bacillus subtilis sebagai bakteri penyebab keracunan makanan.
Penelitian eksperimental laboratorik ini menilai efek antimikroba daun salam pada koloni E. coli dan Bacillus subtilis menggunakan metode difusi cakram dengan mengukur zona inhibisi yang terbentuk. Data diolah dengan uji ANAVA satu arah diikuti tes Post Hoc LSD Fisher, dengan p<0.05.
Zona inhibisi tidak terbentuk pada media yang diinokulasi koloni E. coli. Rerata diameter zona inhibisi yang dibentuk oleh Bacillus subtilis pada media dengan konsentrasi ekstrak 100% adalah 14.16 mm tapi hasil ini lebih kecil dibandingkan dengan Gentamisin sebagai kontrol positif.
Ekstrak etanol daun salam memiliki efek antimikroba terhadap Bacillus subtilis tetapi, tidak memiliki efek antimikroba terhadap E. coli.
ABSTRACT
ANTIMICROBIAL EFFECT OF ETANOL EXTRACT OF SALAM LEAVES (Syzygium polyanthum)
AGAINST Escherichia coli AND Bacillus subtilis IN VITRO
Vanny Setiawan, 2014; dr. Penny Setyawati Martioso, SpPK., M.Kes
Foodborne illness remains as public health problem in Indonesia. It is caused because of bacterial contamination partly due to personal hygiene and bad environmental sanitation. Extract of salam leaves (Syzygium polyanthum) contain agents such as essential oil, tannin, flavonoid, alkaloid, and saponin that supposed to have antimicrobial effect.
The aim of this study is to determine the antimicrobial effects of ethanol extract of salam leaves on the Escherichia coli and Bacillus subtilis colonies’ growth as causes of food poisoning.
The aim of this laboratory experimental study was to assess antimicrobial effect of salam leaves to E. coli and Bacillus subtilis colonies with disk diffusion method by measuring inhibition zones. Data were analyzed with one-way ANOVA test and post hoc Fisher’s LSD, with p <0.05.
Result showed no inhibition zone formed on media inoculated with E.coli colonies. The average of inhibition zone diameter formed by Bacillus subtilis colonies on media with 100% extract concentration was 14.16 mm but this result is smaller than Gentamicin as positive control.
Ethanol extract of Salam leaves have antimicrobial effect to Bacillus subtilis, but not against Escherichia coli.
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PERSETUJUAN ... ii
SURAT PERNYATAAN ... iii
ABSTRAK ... iv
ABSTRACT ... v
KATA PENGANTAR ... vi
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN 1.1 Latar Belakang... 1
1.2 Identifikasi Masalah... 2
1.3 Tujuan Penelitian ... 3
1.4 Manfaat Penelitian ... 3
1.4.1 Manfaat Akademis... 3
1.4.2 Manfaat Praktis... 3
1.5 Kerangka Pemikiran dan Hipotesis... 4
1.5.1 Kerangka Pemikiran... 4
1.5.2 Hipotesis Penelitian ... 5
BAB II TINJAUAN PUSTAKA 2.1 Keracunan Makanan ... 6
2.1.1 Definisi Keracunan Makanan ... 6
2.1.2 Klasifikasi ... 6
2.1.3 Faktor yang Berperan Meningkatkan Insidensi Keracunan Makanan .... 7
2.1.4 Faktor yang Berperan dalam Perkembangan Bakteri... 7
2.1.5 Media Penyebaran Kontaminan ... 8
2.1.6 Vektor Penyebar Kontaminan... 12
2.1.7 Faktor-faktor Risiko atau Derajat Keparahan Keracunan ... 12
2.1.8 Gejala Keracunan Makanan... 14
2.2 Escherichia coli ... 14
2.2.1 Taksonomi ... 15
2.2.3 Struktur Antigen... 16
2.2.4 Sifat Pertumbuhan ... 17
2.2.5 Daya Tahan Bakteri... 17
2.2.6 Patogenitas ... 18
2.2.7 Gambaran Klinik ... 18
2.3 Bacillus subtilis... 20
2.3.1 Taksonomi... 20
2.3.2 Karakteristik ... 20
2.3.3 Patogenitas ... 21
2.3.4 Gejala Klinik ... 21
2.4 Daun Salam ... 22
2.4.1 Taksonomi ... 22
2.4.2 Deskripsi Tanaman... 22
2.4.3 Kandungan Daun Salam ... 24
2.4.4 Kegunaan Daun Salam ... 25
2.4.5 Efek Samping Daun Salam ... 25
2.4.6 Ekstrak Etanol Daun Salam ... 26
2.5 Aktivitas Antibakteri In Vitro... 26
2.5.1 Metode Difusi Cakram... 27
2.5.2 Metode Dilusi ... 28
2.6 Gentamisin ... 29
2.7 Mekanisme Kerja Antibiotik ... 30
2.7.1 Mekanisme Resistensi Bakteri terhadap Antibiotik ... 31
2.7.2 Mekanisme Resistance Plasmids... 34
2.8 Penelitian-penelitian Efek Antimikroba Herbal ... 36
BAB III BAHAN DAN METODE PENELITIAN 3.1 Alat dan Bahan ... 37
3.1.1 Alat ... 37
3.1.2 Bahan ... 37
3.2 Metode Penelitian ... 38
3.2.1 Desain Penelitian... 38
3.2.2 Variabel Penelitian ... 38
3.2.3 Definisi Operasional Variabel ... 38
3.2.4 Alur Penelitian... 39
3.2.5 Besar Jumlah Replikasi ... 40
3.3 Prosedur Kerja ... 40
3.3.1 Pembuatan Ekstrak Etanol Daun Salam ... 40
3.3.2 Sterilisasi Alat ... 40
3.3.3 Persiapan Media Agar ... 41
3.3.4 Pembiakan Bakteri ... 41
3.3.5 Pembuatan Suspensi Bakteri... 42
dan Bacilus subtilis ... 43
3.4 Metode Analisis ... 44
3.5 Kriteria Uji ... 44
3.6 Tempat dan Waktu Penelitian... 44
BAB IV HASIL DAN PEMBAHASAN 4.1 Hasil dan Pembahasan Penelitian ... 45
4.1.1 Pengamatan Uji Aktivitas Anti Bakterial Ekstrak Etanol Daun Salam (Syzygium polyanthum) ... 45
4.2 Uji Hipotesis ... 48
4.2.1 Hipotesis Penelitian 1 ... 48
4.2.2 Hipotesis Penelitian 2 ... 49
BAB V KESIMPULAN DAN SARAN 5.1 Kesimpulan ... 51
5.2 Saran ... 51
DAFTAR PUSTAKA ... 52
LAMPIRAN ... 56
DAFTAR TABEL
Tabel Halaman
2.1 Zona Kepekaan Antibiotik………..28 4.1 Rerata Zona Inhibisi yang Ditimbulkan oleh Ekstrak Etanol Daun Salam
dan Gentamisin terhadap Bacillus subtilis dan Escherichia coli... 45 4.2 ANAVA Satu Arah terhadap Zona Inhibisi pada Setiap Konsentrasi
Ekstrak Etanol Daun Salam untuk Bacillus subtilis ... 46 4.3 Uji Post hoc LSD terhadap Zona Inhibisi yang Ditimbulkan Ekstrak Etanol
DAFTAR GAMBAR
Gambar Halaman
2.1 Escherichia coli ... 15
2.2 Bacillus subtilis... 20
2.3 Daun Salam ... 22
2.4 Bunga salam ...23
2.5 Buah salam ...23
2.6 Metode difusi cakram ...27
2.7 Diagram fungsi protein Tet ...33
2.8 Diagram horizontal gene transfer...34
DAFTAR LAMPIRAN
Lampiran Halaman
1 Prosedur Kerja ...56
2 Hasil Penelitian ...57
3 Data Hasil Penelitian...60
BAB I
PENDAHULUAN
1.1 Latar Belakang
Foodborne illness (infection/intoxication) yaitu penyakit akibat keracunan atau
infeksi karena mengonsumsi makanan terkontaminasi mikroorganisme.
Foodborne illness masih menjadi masalah kesehatan masyarakat di Indonesia
karena kurangnya higiene perorangan dan sanitasi lingkungan sehubungan
dengan pengolahan bahan makanan dan proses memasak (Supraptini, 2002).
Foodborne illness seringkali diberitakan akibat mengkonsumsi hidangan pesta,
makanan jajanan, makanan catering, bahkan makanan segar. Data nasional yang
dirangkum Badan POM selama 4 tahun (2004-2007) juga menjelaskan, bahwa
industri jasa boga (catering) dan produk makanan rumah tangga memberikan
kontribusi paling besar (31%) dibandingkan dengan makanan olahan (20%),
jajanan (13%) dan lain-lain (5%) (BPKN, 2007).
Data dari Badan POM tentang kejadian luar biasa (KLB) foodborne illness
dari tahun 2001-2006 menunjukkan peningkatan baik dari jumlah kejadian
maupun jumlah korban yang sakit dan meninggal. Walaupun demikian, korban
meninggal diperkirakan mungkin hanya 1% saja (BPKN, 2007).
Tan pada tahun 2013 melaporkan bahwa penyebab foodborne di Indonesia
adalah mikroorganisme (Tan, 2013). Tingkat kontaminasi makanan oleh
Escherichia coli masih cukup tinggi yaitu 65,5% (Djaja, 2008). Escherichia coli
Teknologi bidang kedokteran khususnya di bidang antibiotika banyak
memberikan kemudahan bagi kehidupan manusia. Selain dampak positif juga
timbul dampak negatif yang tidak dapat dicegah, misalnya semakin meningkatnya
kemampuan mikroba penyebab infeksi untuk mempertahankan diri melalui
mekanisme-mekanisme adaptasi sehingga makin sulit untuk diberantas. Selain itu,
penggunaan preparat atau sediaan antimikroba secara tidak rasional berdampak
pada munculnya strain baru yang resisten terhadap antimikroba (Wahjono, 1994).
Adanya fakta-fakta tersebut maka diperlukan alternatif lain untuk mengeliminasi
mikroba tersebut, yaitu dengan menggunakan bahan alami antimikroba.
Daun salam (Syzygium polyanthum) berasal dari tanaman asli Indonesia. Daun
salam selain digunakan sebagai bumbu, juga dapat dijadikan bahan obat
tradisional. Daun salam secara empiris telah digunakan untuk obat hipertensi,
diabetes, asam urat, diare, dan maag (Utami & Puspaningtyas, 2013). Malik dan
Ahmad mendapatkan bahwa daun salam memiliki efek antimikroba (Malik &
Ahmad, 2013). Kandungan daun salam yang bersifat antimikroba adalah minyak
atsiri/essential oil, tanin, flavonoid, alkaloid, dan saponin (Sudarsono, 2002;
Dalimartha, 2003). Latar belakang penelitian ini menarik minat penulis untuk
melakukan penelitian untuk mengamati sifat antimikroba daun salam terhadap E.
coli dan Bacillus subtilis dengan menilai pembentukkan zona inhibisi yang
terbentuk dengan tes sensitivitas masing-masing bakteri tersebut pada agar MHA.
1.2 Identifikasi Masalah
Masalah-masalah yang dapat diidentifikasi berdasarkan latar belakang
penelitian yaitu:
Apakah daun salam memiliki efek antimikroba terhadap Escherichia coli.
1.3 Tujuan Penelitian
Untuk mengetahui apakah daun salam memiliki efek antimikroba terhadap
Escherichia coli.
Untuk mengetahui apakah daun salam memiliki efek antimikroba terhadap
Bacillus subtilis.
1.3
Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan manfaat baik di bidang akademis
dalam pengembangan ilmu pengobatan herbal dan juga manfaat praktis bagi praktisis
dunia kedokteran dan masyarakat umumnya.
1.4.1 Manfaat Akademis
Penelitian ini diharapkan menambah wacana penggunaan herbal sebagai
antimikroba dengan mengetahui efektivitas ekstrak etanol daun salam terhadap
penghambatan pertumbuhan bakteri.
1.4.2 Manfaat Praktis
1.5
Kerangka Pemikiran dan Hipotesis
1.5.1
Kerangka Pemikiran
Daun salam mengandung minyak atsiri, tanin, flavonoid, alkaloid, dan saponin
(Sudarsono, 2002; Dalimartha, 2003).
Minyak atsiri mengandung sekuisterpenoid dan eugenol. Minyak atsiri dapat mendenaturasi protein dinding sel bakteri karena mengandung senyawa lipofilik sekuisterpenoid yang dapat merusak membran sel bakteri. Eugenol berperan mendetoksifikasi dengan cara netralisasi racun
(Sugarlini, 2001).
Efek antimikroba tanin yaitu dengan cara inaktivasi adhesin dan enzim DNA topoisomerase. Inaktivasi adhesin mengakibatkan bakteri tidak dapat menempel atau melekat pada permukaan mukosa sistem gastrointestinal. Inaktivasi enzim DNA topoisomerase mengakibatkan bakteri tidak dapat bereplikasi
(Robinson, 1995; Nuria, 2009).
Selain kedua mekanisme antimikroba tersebut, tanin juga dapat menghambat transpor protein guna pembentukan dinding sel akibatnya dinding sel bakteri tidak sempurna dan mudah lisis karena terdapat pada suasana hipotonik sehingga sel bakteri akan mati(Cowan, 1999; Sari,
2011).
Tanin bersifat astringency maka dapat menyebabkan sel-sel jaringan biologis mengkerut termasuk mukosa saluran cerna, maka dapat meningkatkan proteksi mukosa terhadap invasi mikroorganisme dan lebih tahan terhadap zat iritan(Harborne, 1996).
Flavonoid juga memiliki efek antimikroba. Mekanisme antimikroba flavonoid
yaitu melalui pembentukan senyawa kompleks dengan protein ekstraseluler sifatnya
larut dan merusak membran sel bakteri dan diikuti dengan keluarnya senyawa
intraseluler (Cowan, 1999; Nuria, 2009).
Saponin juga dapat bekerja sebagai antimikroba. Mekanisme kerja saponin adalah
menurunkan tegangan permukaan dinding sel bakteri mengakibatkan naiknya
permeabilitas atau kebocoran sel dan mengakibatkan senyawa intraseluler akan keluar
(Robinson, 1995).
1.5.2
Hipotesis Penelitian
Daun salam memiliki efek antimikroba terhadap Escherichia coli
BAB V
SIMPULAN DAN SARAN
5.1 Simpulan
Simpulan yang didapat dari penelitian “Efek Antimikroba Ekstrak Etanol Daun Salam (Syzigium polyanthum) terhadap Escherichia coli dan Bacillus subtilis secara In Vitro” adalah:
Daun salam memiliki efek antimikroba terhadap Bacillus subtilis. Daun salam tidak memiliki efek antimikroba terhada Escherichia coli
5.2 Saran
Saran-saran penulis untuk peneliti selanjutnya agar didapatkan hasil penelitian yang lebih baik yaitu:
Perlu dilakukan penelitian efek bakterisid ekstrak etanol lebih lanjut tentang efek ekstrak etanol daun salam (Syzygium polyanthum) terhadap bakteri spesies lain atau jamur.
DAFTAR RIWAYAT HIDUP
Nama : Vanny Setiawan
Tempat, tanggal lahir : Tasikmalaya, 21 Desember 1992
Alamat : JL. Lingkar Dadaha no. 10, Tasikmalaya Email : vanny.setiawan@yahoo.com
Riwayat Pendidikan :
1999, lulus TK BPK Penabur, Tasikmalaya. 2005, lulus SD BPK Penabur, Tasikmalaya. 2008, lulus SMP BPK Penabur, Tasikmalaya. 2011, lulus SMA Negeri 1, Tasikmalaya.
EFEK ANTIMIKROBA EKSTRAK ETANOL DAUN SALAM (Syzygium polyanthum) TERHADAP Escherichia coli DAN Bacillus subtilis
SECARA IN VITRO
ANTIMICROBIAL EFFECT OF ETANOL EXTRACT OF SALAM LEAVES (Syzygium polyanthum) AGAINST Escherichia coli AND Bacillus subtilis
IN VITRO
Vanny Setiawan1, Penny Setyawati Martioso2
1
Fakultas Kedokteran, Universitas Kristen Maranatha
2
Bagian Patologi Klinik, Fakultas Kedokteran, Universitas Kristen Maranatha, Jalan Prof. Drg. Suria Sumantri MPH No. 65 Bandung 40164 Indonesia
ABSTRAK
Foodborne illnessmasih merupakan masalah kesehatan masyarakat di Indonesia. Foodborne illnessterjadi akibat kontaminasi bakteri karena higiene perorangan dan sanitasi lingkungan yang masih kurang baik. Minyak atsiri, tanin, flavonoid, alkaloid, dan saponin yang terkandung dalam ekstrak daun salam (Syzygium polyanthum) diduga memiliki efek antimikroba. Tujuan penelitian ini adalah untuk mengetahui efek antimikroba ekstrak etanol daun salam terhadap pertumbuhan koloni Escherichia colidan Bacillus subtilis sebagai bakteri penyebab foodborne illness.
Penelitian eksperimental laboratorium ini untuk menilai efek antimikroba daun salam terhadap koloni E. coli dan Bacillus subtilismelalui pembentukan zona inhibisi pada metode difusi cakram. Data dianalisis dengan tes one way ANOVA, lalu denganPost Hoc Test Fisher LSD, p<0,05. Hasil uji ekstrak daun salam 25%, 50%, 75%, dan 100% dengan metode difusi cakram terhadap koloni E. coli tidak ada yang menunjukkan pembentukan zona inhibisi. Hasil uji ekstrak daun salam 25%, 50%, 75%, dan 100% dengan metode difusi cakram terhadap koloni Bacillus subtilis
semua menunjukkan adanya pembentukan zona inhibisi dan diameter zona inhibisi paling lebar adalah pada konsentrasi 100% dengan rerata 14,16 mm, tetapi masih lebih kecil dibandingkan zona inhibisi kontrol positif Gentamisin yaitu 17,09 mm.
Ekstrak etanol daun salam memiliki efek antimikroba terhadap Bacillus subtilis tetapi, tidak memiliki efek antimikroba terhadap E. coli.
Kata Kunci: ekstrak etanol daun salam, efek antimikroba, metode difusi cakram
ABSTRACT
Foodborne illness remains as public health problem in Indonesia. It is caused because of bacterial contamination partly due to personal hygiene and bad environmental sanitation. Extract of salam leaves (Syzygium polyanthum) contain agents such as essential oil, tannin, flavonoid, alkaloid, and saponin that supposed to have antimicrobial effect. The aim of this study is to determine the antimicrobial effects of ethanol extract of salam leaves on the Escherichia coli and Bacillus subtilis colonies’ growth as causes of food poisoning.
disk diffusion method. Data were analyzed with one-way ANOVAtest and Post Hoc Test FisherLSD, p <0,05.
Result of ethanol extract of salam leaves 25%, 50%, 75%, and 100% with disk diffusion method on E. coli colonies showed no inhibition zone. Result of ethanol extract of salam leaves 25%, 50%, 75%, and 100% with disk diffusion method on Bacillus subtilis colonies all consentrations showed the formation of zone inhibition on media with 100% extract concentration was 14,16 mm but this result is smaller than Gentamicin as positive control with 17,09 mm.
Ethanol extract of Salam leaves have antimicrobial effect to Bacillus subtilis, but not against Escherichia coli.
Keywords: ethanol extract of salam leaves, antimicrobial effectiveness, disk diffusion method.
PENDAHULUAN
Foodborne illness yaitu penyakit akibat keracunan atau infeksi karena mengonsumsi makanan terkontaminasi mikroorganisme.
Foodborne illness masih menjadi masalah kesehatan masyarakat di Indonesia karena kurangnya higiene perorangan dan sanitasi lingkungan sehubungan dengan pengolahan bahan makanan dan proses memasak1. Tan pada tahun 2013 melaporkan bahwa penyebab foodborne di Indonesia adalah mikroorganisme2akibat tingkat kontaminasi makanan oleh Escherichia coli masih cukup tinggi yaitu 65,5%3. Escherichia coli dapat ditemukan pada daging sapi mentah atau
undercooked, susu yang tidak dipasteurisasi, buah dan sayur mentah4. Bacillus subtillis
juga dilaporkan sebagai salah satu etiologi
foodborne illness pada daging atau sayuran isi pastry/kue, daging atau produk unggas yang telah dimasak, roti atau roti manis,
sandwich, dan seafood5.
Daun salam (Syzygium polyanthum) berasal dari tanaman asli Indonesia. Daun salam selain digunakan sebagai bumbu, juga dapat dijadikan bahan obat tradisional. Daun salam secara empiris telah digunakan untuk obat hipertensi, diabetes, asam urat, diare, dan maag6. Malik dan Ahmad tahun 2013 melaporkan bahwa daun salam mengandung zat yang berkasiat sebagai antimikroba7 yaitu minyak atsiri (essential oil), tanin, flavonoid, alkaloid, dan saponin8,9.
BAHAN DAN METODE
Penelitian eksperimental laboratorium ini dilakukan untuk menilai efek antimikroba daun salam terhadap pertumbuhan koloni bakteri E. coli dan Bacillus subtilis dengan metode difusi cakram. Suspensi bakteri
E. coli dan Bacillus subtilismasing-masing sesuai standard Mc Farland diinokulasikan pada media agar Müeller Hinton yang berbeda, dimana diletakkan cakram yang mengandung ekstrak etanol daun salam dengan konsentrasi 25%, 50%, 75%, dan 100% lalu diinkubasi pada suhu 37ºC selama 24 jam. Efek antimikroba ekstrak daun salam dievaluasi dengan cara mengamati ada atau tidaknya pembentukan zona inhibisi, serta ukuran diameter zona inhibisi yang terbentuk dengan menggunakan jangka sorong dalam satuan millimeter (mm). Cakram Gentamisin digunakan sebagai kontrol positif yang diletakkan pada media agar Müeller Hinton yang telah diinokulasi masing-masing dalam cawan petri yang berbeda dengan suspensi bakteri E. coli dan
Bacillus subtilis. Diameter zona inhibisi sensitif Gentamisin untuk E. coli 11 mm dan
Bacillus subtilis17,09 mm.
ANALISIS DATA
Data dianalisis dengan tes one way ANOVA
HASIL DAN PEMBAHASAN
Ekstrak etanol daun salam den gan konsentrasi 25%, 50%, 75%, dan 100%,
semua menunjukkan adanya pembentukan zona inhibisi terhadap pertumbuhan koloni
Bacillus subtilis dengan rerata diameter zona inhibisi berturutan 10,194 mm, 12,45 mm, 12,972 mm, dan 14,16 mm. Diameter zona inhibisi ekstrak etanol daun salam terbesar diperoleh pada konsentrasi 100% yaitu 14,16 mm masih lebih kecil dibandingkan rerata diameter zona inhibisi kontrol positif Gentamisin yaitu 17.09 mm.
Zona inhibisi tidak terbentuk pada media dengan konsentrasi ekstrak etanol daun salam 25%, 50%, 75%, maupun 100% yang diinokulasi E. coli, sedangkan pada kontrol positif yang diberi cakram Gentamisin didapatkan rerata diameter zona inhibisi sebesar 11 mm.
Analisis one way ANOVA efek antimikroba ekstrak daun salam terhadap
Bacillus subtilis menunjukkan hasil yang sangat signifikan (p=0,000) seperti pada Tabel 4.1.
Tabel 4.1 ANOVA Ekstrak Daun Salam dan Gentamisin
Hasil uji ANOVA diperoleh p=0,000, hal ini menunjukkan adanya perbedaan rerata diameter zona inhibisi antara pemberian ekstrak konsentrasi 25%, 50%, 75%, dan 100% tetapi efektivitasnya masih dibawah
kontrol positif Gentamisin. Untuk
mengetahui kelompok mana yang berbeda dilakukan uji Post hoc Test Fisher LSD.
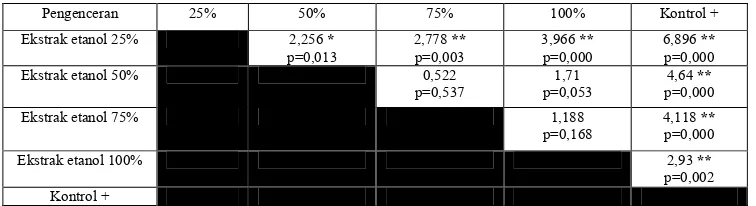
Tabel 4.2 Uji Post Hoc Test Fisher LSD terhadap Zona Inhibisi yang Ditimbulkan Ekstrak Etanol Daun Salam Bacillus subtilis
Pengenceran 25% 50% 75% 100% Kontrol +
Ekstrak etanol 25% 2,256 *
p=0,013
2,778 **
p=0,003
3,966 **
p=0,000
6,896 **
p=0,000
Ekstrak etanol 50% 0,522
p=0,537
1,71 p=0,053
4,64 **
p=0,000
Ekstrak etanol 75% 1,188
p=0,168
4,118 **
p=0,000
Ekstrak etanol 100% 2,93 **
p=0,002 Kontrol +
Hasil Post Hoc Test Fisher LSD pada tabel 4.2 menunjukkan pada perbandingan semua konsentrasi didapatkan perbedaan yang sangat bermakna pada rerata diameter zona inhibisi yang terbentuk. Tetapi pada perbandingan konsentrasi 25% dengan 50% didapatkan perbedaan bermakna (p=0,013) berdasarkan rerata diameter zona inhibisi yang terbentuk. Potensi antimikroba ekstrak etanol 50% tidak menunjukkan perbedaaan bermakna dengan ekstrak etanol konsentrasi
75% (p=0,537) dan 100% (p=0,053)
berdasarkan rerata diameter zona inhibisi
didapatkan pula bila konsentrasi 75% dibandingkan dengan 100% (p=0,168). Zona inhibisi pada Escherichia colitidak terbentuk dapat diakibatkan faktor-faktor berikut. Hugo & Russell (1983) melaporkan bahwa bakteri gram negatif bersifat lebih resisten terhadap antibiotik10. Soetan (2003) mengemukakan bahwa kapsul bakteri gram negatif memiliki efek protektif maka zat aktif sulit penetrasi melalui membran sel mikroba11. Tschesche & Wulff (1973) melaporkan bahwa efek antibakteri saponin pada umumnya lemah12. Sulistia (1995)
Metode Sum of Squares Df Mean Square Sig. Between Groups
127.771 4 31.943 .000
Within Groups
34.665 20 1.733
mikroba yang rendah, adanya pembentukan biofilm, kegagalan antimikroba penetrasi masuk ke dalam sel mikroba dan rendahnya
afinitas obat pada ribosom dapat
menyebabkan tidak terbentuknya zona inhibisi13. Syukrinawati (2014) melaporkan bahwa zona inhibisi tidak terbentuk karena zat aktif tidak dapat mencapai tempat kerjanya di dalam sel mikroba. Pada bakteri gram negatif, molekul zat aktif/antibiotik yang kecil dan polar dapat menembus dinding luar dan masuk ke dalam sel melalui lubang-lubang kecil yaitu porin. Bila porin meghilang atau mengalami mutasi maka masuknya zat aktif ini akan terhambat. Mekanisme lain ialah bakteri mengurang mekanisme transpor aktif yang berperan dalam masuknya zat aktif ke dalam sel mikroba. Mikroba juga memiliki mekanisme pertahanan melalui aktivasi pompa efluks untuk mengeluarkan zat antimikroba dari dalam sel mikroba. Faktor lain adalah inaktivasi obat karena mikroba mampu membuat enzim yang merusak zat aktif tersebut, mikroba mengubah binding sitezat aktif sehingga afinitasnya menurun14. Todar (2008) mengemukakan bahwa salah satu mekanisme resistensi Escherichia coli
terhadap antibiotika melalui plasmid yaitu dengan memindahkan gen resistensi melalui
horizontal gene transfer (HGT), umumnya secara transduksi dan konjugasi15.
Sudarsono dkk (2002) mengemukan bahwa terdapat zat-zat aktif dalam ekstrak etanol daun salam yang dapat menghambat pertumbuhan mikroba antara lain minyak atsiri (essential oil), tanin, flavonoid, alkaloid, dan saponin. Minyak atsiri dapat mendenaturasi protein dinding sel mikroba. Eugenol dapat menetralisir racun. Penelitian Alexander O. Gill dan Richard A. Holley (2004) mendapatkan bahwa eugenol dapat menghambat peningkatan ATP intraseluler. Eugenol juga memiliki sifat bakterisidal dengan menghancurkan dinding sel mikroba melalui penghambatan gradien proton atau enzim F1F0 ATP-ase. Hal tersebut didukung penelitian Rico-Munoz yang mendapatkan bahwa komponen fenolik butilhidrokuinin tersier dan propyl gallate dalam eugenol dapat mengurangi aktivitas ATP-ase pada membran sel bakteri16. Robinson (1995) mengemukakan bahwa mekanisme kerja saponin sebagai antibakteri yaitu dengan cara menurunkan tegangan permukaan
dinding sel akibatnya permeabilitas dinding sel meningkat dan terjadi kebocoran sel diikuti keluarnya senyawa intraseluler17.
African Journal of Biotechnology (2006) melaporkan bahwa “saponin mempunyai efek inhibisi pada bakteri Gram positif tetapi tidak pada bakteri Gram negatif dan fungi”. Penelitian tersebut mendukung dengan hasil penelitian ini, yaitu ekstrak etanol daun salam yang mengandung saponin mampu membentuk zona inhibisi sebagai indikator adanya penghambatan pertumbuhan bakteri Gram positif Bacillus subtilis, tetapi tidak terhadap bakteri Gram negatif E. coli18.
DAFTAR PUSTAKA
1. Supraptini S. 2002. Kejadian
Foodborne illness dan Penyebabnya di Indonesia 1995-2000. Litbang Depkes. 2. Tan I. 2013. Evaluasi Praktek
Penyajian Beef Teriyaki Siap Saji pada Restoran Swalayan di Semarang: Aspek Sanitasi dan Mikrobiologi. Unika Soegijapranata.
3. Djaja IM. 2008. Kontaminasi E. coli Pada Makanan dari Tiga Jenis Tempat Pengolahan Makanan (TPM) di Jakarta Selatan 2003. Makara Kesehatan.
4. Foodsafety.gov. 2014. Foodsafety.gov. Retrieved October 9, 2014, from Foodsafety.gov:
http://www.foodsafety.gov/
5. Cambridge. 2014. Bacillus Food Poisoning. Cambridge City Council.
6. Utami P., & Puspaningtyas DE. 2013.
The Miracle of Herbs. Jakarta: Agro Media Pustaka.
7. Malik A., & Ahmad AR. 2013.
Antidiarrheal Activity of Etanolic Extract of Bay Leaves (Syzygium Polyanthum [Wight.] Walp.). International Research Journal of Pharmacy, 107.
8. Sudarsono. 2002. Tumbuhan Obat II : Hasil Penelitian, Sifat-sifat, dan Penggunaan. Yogyakarta: Pusat Studi Obat Tradisional UGM.
9. Dalimartha S. 2003. Atlas Tumbuhan Obat Indonesia, Jilid III.Jakarta: Puspa Swara.
10. Hugo W., & Russell A. 1983.
Blackwell Scientific Publications, 33-35, 51.
11. Soetan K. 2003. Evaluation of some pharmaceutical and haematological activities of saponins in guinea corn (Sorghum bicolor L Moench) M.Sc Dissertation.
12. Tschesche R., & Wulff G. 1973.
Chemistry and Biology of Saponins. Fortschr. Chem.Org. Naturist.
13. Sulistia G. 1995. Farmakologi dan Terapi.Jakarta: Balai Penerbit FKUI.
14. Syukrinawati R. 2014. Resistensi. Repository USU.
15. Todar K. 2008. Todar's online textbook of bacteriology. Retrieved October
2014, from
http://textbookofbacteriology.net
16. Gill AO., & Holley RA. 2004.
Mechanisms of Bactericidal Action of Cinnamaldehyde against Listeria monocytogenes and of Eugenol against L. monocytogenes and Lactobacillus sakei. NCBI.
17. Robinson T. 1995. Kandungan Organik Tumbuhan Tinggi. Bandung: Institut Teknologi Bandung.
DAFTAR PUSTAKA
Anonim. (2007). http://daunsalam.blogspot.com. Retrieved 2014, from http://daunsalam.blogspot.com/2013/07/awas-efek-samping-daun-salam-mengintai.html
Arisman. 2009. Keracunan Makanan Buku Ajar Ilmu Gizi. Jakarta: EGC.
Bauman R. 2009. Microbiology. England: Pearson Education, inc.
Bhattacharjee I, Chatterjee SK, Chatterjee S, & Chandra G. 2006. Antibacterial potentiality of Argemone mexicana solvent extracts against some pathogenic bacteria.
Botta A, & Conn G. 2008. PBWorks. Retrieved November 3, 2014, from PBWorks: http://chem35132007.pbworks.com/
BPKN. 2007, March 30. Retrieved October 9, 2014, from Ditjen SPK. Kemendag: http://ditjenspk.kemendag.go.id/files/pdf/2013/06/04/hasil-kajian-badan- perlindungan-konsumen-nasional-bpkn-di-bidang-pangan-terkait-perlindungan-konsumen-id0-1370355071.pdf
BPOM. 2008. Keracunan Pangan Akibat Bakteri Patogen.
Brooks G. 2005. Jawetz, Melnick, & Adelberg’s Medical Microbiology: Twenty-third Edition ed. USA: McGraw Hill.
Cambridge. 2014. Bacillus Food Poisoning. Cambridge City Council .
Constantin C. 2008. Cereulide producing Bacillus cereus and amylosin producing Bacillus subtilis and Bacillus mojavensis: characterization of strains and toxigenicities.
Cowan MM. 1999. Plant Products as Antimicrobial Agents. Clinical Microbiology Reviews.
Dalimartha S. 2003. Atlas Tumbuhan Obat Indonesia, Jilid III. Jakarta: Puspa Swara.
Deshpande, S S. 2002. Handbook of Food Toxicology. CRC Press.
Engelkirk, P. G., & Duben-Engelkirk, J. (2008). Laboratory Diagnosis of Infectious Diseases. Philadelphia: Lippincott Williams and Wilkins.
Federer WT. 1967. Experimental design, theory and application. New Delhi: Oxford and IBH Publ. Co.
Foodsafety.gov. 2014. Foodsafety.gov. Retrieved October 9, 2014, from Foodsafety.gov: http://www.foodsafety.gov/
Gill AO., & Holley RA. 2004. Mechanisms of Bactericidal Action of Cinnamaldehyde against Listeria monocytogenes and of Eugenol against L. monocytogenes and Lactobacillus sakei. NCBI.
Graumann P. 2007. Bacillus: Cellular and Molecular Biology. Caister Academic Press.
Harborne J. 1996. Metode Fitokimia : Penuntun Cara Modern Menganalisa Tumbuhan. (Diterjemahkan oleh : K. Padmawinata dan i. Soediro). Bandung: Penerbit ITB.
Harborne J. 1987. Metode Fitokimia. Penerjemah Dr. Kosasih P. dan Dr. Iwang S. Cetakan kedua. Bandung: ITB.
Harmita. 2005. Analisis Hayati. Jakarta: Departemen Farmasi FMIPA Universitas Indonesia.
Harris P, Nagy S, & Vardaxis N. 2009. Mosby's Dictionary of Medicine, Nursing and Health Professions - Australian & New Zealand Edition. Elsevier Health Sciences.
Hugo W., & Russell A. 1983. Pharmaceutical Microbiology. Hugo WB, Russell A.D (eds) 3rd edition Blackwell Scientific Publications, 33-35, 51.
Jawetz M. 2012. Medical Microbiology. 26ed. McGraw-Hill Medical Publishing Division.
Levinson ME. 2005. Acute Respiratory Tract Infection. In: DL Kasper(Ed.): Harrison's Principles of Internal Medicine, Vol. 2. 15th edition. New York: McGraw-Hill Companies. Inc. p.1475
Malik A., & Ahmad AR. 2013. Antidiarrheal Activity of Etanolic Extract of Bay Leaves (Syzygium Polyanthum [Wight.] Walp.). International Research Journal of Pharmacy, 107.
Murtidjo, BA. 2007. Pemotongan dan Penanganan Daging Ayam. Yogyakarta: Kanisius.
Nuria MC. 2009. Uji Antibakteri Ekstrak Etanol Daun Jarak Pagar ( Jatropha cuircas L) terhadap Bakteri Staphylococcus aureus ATCC 25923, Escherichia coli ATCC 25922, dan Salmonella typhi ATCC 1408. 4.
Pelczar M., & Chan. 1984. Dasar-Dasar Mikrobiologi. Alih Bahasa: Ratna Siri Hadioetomo, dkk. Jakarta: Penerbit Universitas Indonesia Press.
Robinson T. 1995. Kandungan Organik Tumbuhan Tinggi. Bandung: Institut Teknologi Bandung.
Rowe-Magnus DA., Davies J., Mazel D. 2002. Impact and Transposons on The Evolution of Resistance and Virulence. In: J Hacker & J. B Kaper: Pathogenicity Island and The Evolution of Pathogenic Microbes. Vol. 2. United States of America: Springer-Verlag. P167-88
Sari FP. 2011. Ekstraksi Zat Aktif. Antimikroba dari Tanaman Yodium (Jatropha multifida Linn) sebagai Bahan Baku Alternatif Antibiotik Alami. 6.
Satish G. 1990. Mikrobiologi Dasar. Terjemahan E. Suryawidjaja : The Short Textbook of Medical Microbiologi. Jakarta: Bina Rupa Aksara.
Siagian A. 2002. Mikroba Patogen pada Makanan dan Sumber Pencemarannya. USU Digital Library.
Soetan K. 2003. Evaluation of some pharmaceutical and haematological activities of saponins in guinea corn (Sorghum bicolor L Moench) M.Sc Dissertation.
Soetan KO. 2006. Evaluation of the Antimicrobial Activity of Saponins Extract of Sorghum Bicolor L. Moench. African Journal of Biotechnology.
Sudarsono. 2002. Tumbuhan Obat II : Hasil Penelitian, Sifat-sifat, dan Penggunaan. Yogyakarta: Pusat Studi Obat Tradisional UGM.
Sugarlini. 2001. Telaah Fitokimia dan Bahan Aktif Anti Radang dari Daun Salam (Syzygium polyanthum). Tesis S2 Departemen Farmasi ITB.
Sulistia G. 1995. Farmakologi dan Terapi. Jakarta: Balai Penerbit FKUI.
Supardi I., & Sukamto. 1998. Mikrobiologi dalam Pengolahan dan Keamanan Pangan. Jakarta: PT Gramedia Pustaka Utama.
Supraptini S. 2002. Kejadian Keracunan Makanan dan Penyebabnya di Indonesia 1995-2000. Litbang Depkes.
Syukrinawati R. 2014. Resistensi. Repository USU.
Tan I. 2013. Evaluasi Praktek Penyajian Beef Teriyaki Siap Saji pada Restoran Swalayan di Semarang: Aspek Sanitasi dan Mikrobiologi. Unika Soegijapranata.
Todar K. 2008. Todar's online textbook of bacteriology. Retrieved October 2014, from http://textbookofbacteriology.net
Tschesche R., & Wulff G. 1973. Chemistry and Biology of Saponins. Fortschr. Chem.Org. Naturist.
Utami P., & Puspaningtyas DE. 2013. The Miracle of Herbs. Jakarta: AgroMedia Pustaka.
Van Steenis C. 1988. Flora-flora. Jakarta: P.T. Paramitra.
Voight R. 1984. Buku Pelajaran Teknologi Farmasi. Penerjemah S.N. Soewandi. Edisi kelima. Yogyakarta: Penerbit Gadjah Mada University Press.
Wahjono H. 1994. Penggunaan Antibiotika secara Rasional pada Penyakit Infeksi.