INTISARI
Nyeri merupakan perasaan sensoris dan emosional yang tidak nyaman
sehingga menyebabkan seseorang datang untuk mencari pertolongan medis. Oleh
karena itu diperlukan analgesik untuk mengatasi nyeri. Penelitian ini bertujuan
untuk mengetahui pengaruh pemberian sediaan fraksi etanol-heksan ekstrak
metanol-air daun Macaranga tanarius L. terhadap efek analgesik pada mencit
betina galur Swiss yang terinduksi asam asetat 1%.
Penelitian ini merupakan penelitian eksperimental murni dengan
rancangan acak lengkap pola searah. Dua puluh lima ekor mencit umur 2-3 bulan
dan berat badan 20-30 gram dikelompokkan ke dalam 5 kelompok yaitu
kelompok kontrol negatif (Aquadest dosis 191,8 mg/kg BB), kelompok kontrol
positif (Asetosal dosis 91mg/kg BB), dan kelompok fraksi etanol-heksan ekstrak
metanol-air daun Macaranga tanarius L. dalam tiga peringkat dosis yaitu 47,95;
95,9; dan 191,8 mg/kg BB. Kontrol dan bahan uji diberikan secara per oral,
kemudian diberi asam asetat 1% secara intraperitoneal sebagai penginduksi nyeri
dengan selang waktu pemberian selama 10 menit. Pengamatan geliat dilakukan
setiap 5 menit selama 1 jam. Jumlah geliat digunakan untuk menghitung nilai %
proteksi, dan nilai perubahan % proteksi. Hasil dianalisis dengan uji Shapiro Wilk,
dilanjutkan uji One Way ANOVA dan uji Scheffe dengan taraf kepercayaan 95%.
Hasil penelitian menunjukkan bahwa fraksi etanol-heksan ekstrak
metanol-air daun Macaranga tanarius L. memiliki efek analgesik dengan %
proteksi pada dosis 47,95; 95,9; dan 191,8 mg/kg BB secara berturut-turut adalah
57,83; 65,12; dan 79,24 dan perubahan % proteksi secara berturutturut adalah
-6,42; 5,35; dan 28,21. Tidak terdapat kekerabatan antara efek analgesik dan dosis
fraksi yang diberikan.
ABSTRACT
Pain is an unpleasant sensory and emotional experience, causing a person
to find medical help. Therefore it needs an analgesic to relieve pain. In this
present study, the writer has investigated the analgesic effect of ethanol-hexane
fraction from methanol-water extract of Macaranga tanarius L. leaves using
models of acetic acid-induced writhing response in female Swiss mice.
This study is pure experimental with completely randomized design.
Twenty-five mice aged 2-3 months and weighed 20-30 grams are grouped into 5
groups: negative control group (Aquadest dose of 191.8 mg / kg), a positive
control group (aspirin dose of 91mg / kg), and the group of ethanol-hexane
fraction of methanol-water extract of Macaranga tanarius L. leaves in three doses
ie 47.95; 95.9; and 191.8 mg / kg. Aspirin and fraction are given orally, then
given a 1% acetic acid intraperitoneally as an inducer of pain with an interval of
administration for 10 minutes. Observation of writhing response is done every 5
minutes in 1 hour. The amount of writhing response is used to calculate the value
of percent protection, that used to calculate change of percent protection to
determine the analgesic effect writhing test compounds against asetosal. The
results obtained were analyzed by Shapiro Wilk test, followed by One Way
ANOVA test and Scheffe test with 95% confidence level.
The results showed that ethanol-hexane fraction of methanol-water extract
of Macaranga tanarius L. leaves has an analgesic effect. Percent protection at
doses of 47.95; 95.9; and 191.8 mg / kg respectively was 57.83; 65.12; and
79.24% and change of % protection was -6.42; 5.35; and 28.21. There is no
kinship between the analgesic effect and dose fractions are given.
UJI ANALGESIK FRAKSI ETANOL EKSTRAK METANOL
DENGAN METODE GELIAT
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
UJI ANALGESIK FRAKSI ETANOL-HEKSAN EKSTRAK METANOL-AIR DAUN Macaranga tanarius DENGAN METODE GELIAT PADA MENCIT GALUR SWISS
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh :
Silvia Dwi Puspa Susanti NIM : 128114086
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
YOGYAKARTA 2015
HEKSAN
Macaranga tanarius L.
UJI ANALGESIK FRAKSI ETANOL EKSTRAK METANOL
DENGAN METODE GELIAT
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
i
UJI ANALGESIK FRAKSI ETANOL-HEKSAN EKSTRAK METANOL-AIR DAUN Macaranga tanarius DENGAN METODE GELIAT PADA MENCIT GALUR SWISS
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh :
Silvia Dwi Puspa Susanti NIM : 128114086
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
YOGYAKARTA 2015
HEKSAN
Macaranga tanarius L.
ii
Persetujuan Pembimbing
UJI ANALGESIK FRAKSI ETANOL-HEKSAN EKSTRAK METANOL-AIR DAUN Macaranga tanarius L. DENGAN METODE GELIAT PADA MENCIT GALUR SWISS
Skripsi yang diajukan oleh: Silvia Dwi Puspa Susanti
NIM : 128114086
telah disetujui oleh:
Pembimbing Utama
Phebe Hendra, M.Si., Ph.D., Apt. tanggal:
Pembimbing Pendamping
iii
Pengesahan Skripsi Berjudul
UJI ANALGESIK FRAKSI ETANOL-HEKSAN EKSTRAK METANOL-AIR DAUN Macaranga tanarius L. DENGAN METODE GELIAT PADA MENCIT GALUR SWISS
Oleh:
Silvia Dwi Puspa Susanti NIM : 128114086
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sanata Dharma pada tanggal: ………..…….
Mengetahui Fakultas Farmasi Universitas Sanata Dharma
Dekan
Aris Widayati, M.Si., Apt., Ph.D
Panitia Penguji : Tanda tangan
1. Phebe Hendra, M.Si., Ph.D., Apt. ………...
2. Christianus Heru Setiawan, M.Sc., Apt. ………
3. Dita Maria Virginia, M.Sc., Apt. ………
iv
HALAMAN PERSEMBAHAN
Opportunity follows struggle. It follows effort. It follows hard work. It doesn’t come before.
-Shelby Steele-
Kupersembahkan skripsi ini untuk:
Tuhan Yesus sebagai sumber kekuatan dan anugerah dalam hidupku, Santo Yudas Tadeus yang menjadi perantara doa dan mukjizat,
Kedua orang tuaku Bapak F.X. Suripto dan Ibu V.Y. Sulisti yang telah memberikan doa, dukungan, perjuangan, serta kasih sayang,
v
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarisme dalam naskah ini, maka saya bersedia menanggung segala sanksi sesuai peraturan perundang-undangan yang berlaku.
Yogyakarta,………..
Penulis
vi
vii
PRAKATA
Puji dan syukur penulis haturkan ke hadirat Tuhan yang Maha Esa, atas
berkat, kasih, dan penyertaan-Nya hingga penelitian dan penyusunan skripsi
berjudul “Uji Analgesik Fraksi Etanol-Heksan Ekstrak Metanol-Air Daun
Macaranga tanarius L. dengan Metode Geliat pada Mencit Galur Swiss” dapat
penulis selesaikan. Proses penyusunan skripsi ini tidak lepas dari peran,
dukungan, dan bantuan berbagai pihak. Oleh karena itu, pada kesempatan ini
penulis ingin menyampaikan terimakasih kepada:
1. Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta
2. Bapak Enade Perdana Istyatono, Ph.D., Apt., selaku Dosen Pembimbing
Akademik yang telah memberikan dukungan dan bimbingan selama menjalani
proses perkuliahan di Fakultas Farmasi hingga saat ini.
3. Ibu Phebe Hendra, M.Si., Ph.D., Apt., selaku Dosen Pembimbing Utama atas
bimbingan, semangat, bantuan, dan pengarahan selama proses penelitian
hingga penyusunan skripsi ini.
4. Christianus Heru Setiawan, M.Sc., Apt., selaku Dosen Pembimbing
Pendamping atas bimbingan, pengarahan, saran, serta masukan selama proses
penelitian hingga penyusunan skripsi ini.
5. Ibu Dita Maria Virginia, M.Sc., Apt. selaku Dosen Penguji yang telah
memberikan saran dan kritik hingga skripsi ini tersusun.
6. Ibu Damiana Sapta Candrasari, M.Sc. selaku Dosen Penguji yang telah
viii
7. Bapak, Ibu, Mbak Ivon, Mas Theo, Surya, Christie, dan Mbah Marjono yang
selalu memberikan doa, dukungan, semangat, bantuan, dan kasih sayang.
8. Pak Heru, Pak Wagiran, Pak Suparjiman, dan Pak Kayatno yang telah
membantu dalam proses penelitian di laboratorium.
9. Sahabat yang setia membantu, mendukung, dan memberi semangat dalam
perjuangan menyelesaikan skripsi ini, Nurul Kusumawardani, Antonia Vidya
Kartika, dan Kristiyani Irawati. Terimakasih atas kesempatan berjuang
bersama kalian.
10.Teman-teman FSM B dan FKK B 2012.
11.Seorang sahabat sekaligus kekasih, Benediktus Prasetyo Adhi Kurniawan.
Terimakasih atas dukungan, pengertian, kesabaran, doa, saran, dan kasih
sayang yang diberikan.
Penulis menyadari bahwa skripsi ini tentunya masih jauh dari sempurna,
untuk itu penulis sangat terbuka pada masukan dan kritik dari pembaca. Akhir
kata, semoga karya ini dapat berguna bagi pembaca dan bagi perkembangan ilmu
pengetahuan.
Yogyakarta, November 2015
ix
DAFTAR ISI
HALAMAN JUDUL ……….. i
HALAMAN PERSETUJUAN PEMBIMBING ……… ii
HALAMAN PENGESAHAN ……… iii
HALAMAN PERSEMBAHAN ……… iv
PERNYATAAN KEASLIAN KARYA ……… v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS ………... vi
PRAKATA ………. vii
DAFTAR ISI ……….. ix
DAFTAR TABEL ……….. xii
DAFTAR GAMBAR ………. xiii
DAFTAR LAMPIRAN ……….. xv
INTISARI ……….. xvii
ABSTRACT ... xviii
BAB I. PENGANTAR ………... 1
A. Latar Belakang ………. 1
1. Rumusan Masalah ……….. 4
2. Keaslian Penelitian ………. 4
3. Manfaat Penelitian ………. 6
B. Tujuan Penelitian ………. 6
BAB II. PENELAAHAN PUSTAKA………... 7
x
B. Analgesik ……..……….. 12
C. Asetosal ……….. 15
D. Macaranga tanarius L ..……….. 16
E. Senyawa Fenolik ……….. 21
F. Metode penyarian ..……….. 21
G. Proses penyarian senyawa aktif ...……… 23
H. Pelarut ……..……… 26
I. Metode uji Analgesik ……….……….. 28
J. Asam asetat ..……… 31
K. Landasan Teori ………. 32
L. Hipotesis ……….. 33
BAB III. METODE PENELITIAN ………... 34
A. Jenis dan Rancangan penelitian ………... 34
B. Variabel dan Definisi Operasional ………... 34
C. Bahan Penelitian ……….. 38
D. Alat Penelitian ……….. 39
E. Tata Cara Penelitian ………. 39
F. Analisis Hasil ………...… 50
G. Ruang Lingkup Penelitian ……… 52
BAB IV. HASIL DAN PEMBAHASAN ……….. 53
A. Determinasi Tanaman Macaranga tanarius L. ……… 53
B. Pengumpulan dan Penyerbukan Daun macaranga tanarius L. ……….. 53
xi
D. Pembuatan Fraksi Etanol-Heksan Ekstrak Metanol-Air Daun
Macaranga tanarius L. ……… 56
E. Hasil Pengujian Senyawa Metabolit Sekunder ……… 62
F. Uji Pendahuluan ……….. 67
G. Uji Efek Analgesik Fraksi Daun Macaranga tanarius L. ……… 69
BAB V. KESIMPULAN DAN SARAN ……… 83
A. Kesimpulan ……….. 83
B. Saran ………. 83
DAFTAR PUSTAKA ……… 84
LAMPIRAN ……….. 89
xii
DAFTAR TABEL
Tabel I. Penelitian terkait daun Macaranga tanarius L. ………. 4
Tabel II. Hasil pengujian fraksi etanol-heksan ekstrak metanol-air daun
Macaranga tanarius L. ……….. 62
Tabel III. Rata-rata jumlah kumulatif geliat mencit pada penentuan
selang waktu pemberian asam asetat 50 mg/kg BB …………... 68
Tabel IV. Hasil uji T tidak berpasangan untuk data jumlah geliat pada
penentuan selang waktu …...……….. 68
Tabel V. Hasil rata-rata jumlah kumulatif geliat, rata-rata persen
proteksi, dan rata-rata perubahan persen proteksi pada
kelompok kontrol negatif, kontrol positif, dan 3 peringkat
dosis fraksi daun Macaranga tanarius L. ……….. 71
Tabel VI. Hasil uji Scheffe untuk jumlah kumulatif geliat pada kelompok
kontrol negatif, kontrol positif, dan 3 peringkat dosis fraksi
Macaranga tanarius L. ……….. 74
Tabel VII. Hasil uji Scheffe untuk persen proteksi pada kelompok kontrol
negatif, kontrol positif, dan 3 peringkat dosis fraksi
xiii
DAFTAR GAMBAR
Gambar 1. Struktur kimia Asetosal ……… 15
Gambar 2. Macaranga tanarius L. ……… 16
Gambar 3. Struktur senyawa dari daun Macaranga tanarius L. yang
memiliki aktivitas terhadap penangkapan radikal bebas
DPPH ……… 20
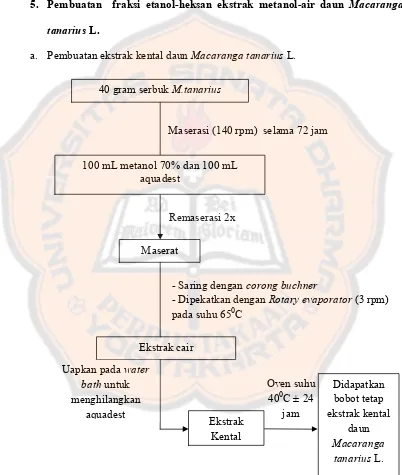
Gambar 4. Flowchart langkah pembuatan ekstrak metanol-air daun
Macaranga tanarius L. ……… 41
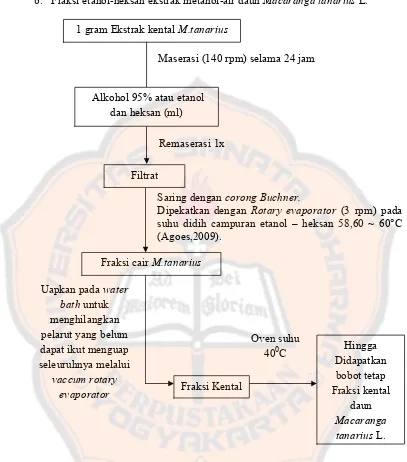
Gambar 5. Flowchart langkah pembuatan fraksi etanol-heksan dari
ekstrak kental metanol-air daun Macaranga tanarius L. …. 42
Gambar 6. Skema perlakuan hewan uji ……….. 49
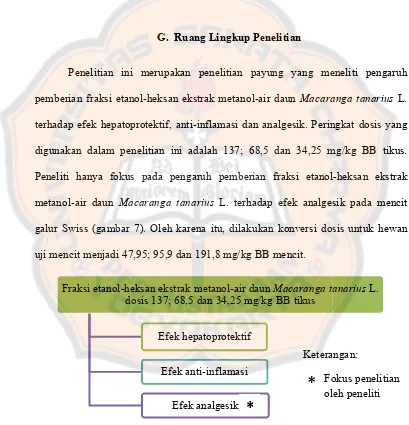
Gambar 7. Fokus penelitian ………... 53
Gambar 8. (a) Histogram rata-rata jumlah kumulatif geliat (b)
Histogram rata-rata persen proteksi, dan (c) Histogram
rata-rata perubahan persen proteksi pada uji efek analgesik
kelompok uji yaitu kontrol negatif, kontrol positif, dan 3
peringkat dosis fraksi daun Macaranga tanarius L. ……… 72
Gambar 9. Daun Macaranga tanarius L. ………... 94
Gambar 10. Serbuk daun Macaranga tanarius L. ………... 94
Gambar 11. Hasil ekstrak metanol-air daun Macaranga tanarius L. …. 94
Gambar 12. Hasil fraksi etanol-heksan dari ekstrak metanol-air daun
xiv
Gambar 13. Sediaan fraksi etanol-heksan dari ekstrak metanol-air daun
Macaranga tanarius L. ……… 94
Gambar 14. Injeksi intraperitoneal ………... 95
Gambar 15. Geliat mencit yang memenuhi kriteria ………. 95
Gambar 16. Geliat mencit yang tidak memenuhi kriteria ……… 95
Gambar 17. Hasil uji Alkaloid dengan reagen Mayer ………. 95
Gambar 18. Hasil uji Alkaloid dengan reagen Dragendorff ………….. 96
Gambar 19. Hasil uji Flavonoid ……….. 96
Gambar 20. Hasil uji Terpenoid ……….. 96
Gambar 21. Hasil uji Fenolik ……….. 96
Gambar 22. Hasil uji Tanin ………. 96
Gambar 23. Hasil uji Saponin ………. 96
xv
DAFTAR LAMPIRAN
Lampiran 1. Surat determinasi tanaman Macaranga tanarius L. ……... 90
Lampiran 2. Surat keterangan penetapan kadar air serbuk daun
Macaranga tanarius L. dari LPPT UGM ………... 91
Lampiran 3. Surat Ethical Clearance dari Fakultas Kedokteran UGM ... 92
Lampiran 4. Surat legalitas analisa data oleh Pusat Kajian CE&BU
Fakultas Kedokteran UGM ……… 93
Lampiran 5. Daun dan serbuk daun Macaranga tanarius L.; hasil ekstrak
air dan hasil fraksi etanol-heksan ekstrak
metanol-air daun Macaranga tanarius L., serta sediaan fraksi daun
Macaranga tanarius L……… 94
Lampiran 6. Injeksi intraperitoneal ……… 95
Lampiran 7. Kriteria geliat mencit ………. 95
Lampiran 8. Hasil pengujian fitokimia fraksi etanol-heksan ekstrak
metanol-air daun Macaranga tanarius L. ……….. 96
Lampiran 9. Hasil analisis statistik jumlah geliat pada penentuan selang
waktu pemberian asam asetat 50mg/kg BB ………... 97
Lampiran 10. Hasil analisis statistik jumlah geliat pada uji efek analgesik
fraksi etanol-heksan ekstrak metanol-air daun Macaranga
xvi
Lampiran 11. Hasil analisis statistik % proteksi pada uji efek analgesik
fraksi etanol-heksan ekstrak metanol-air daun Macaranga
tanarius L. ………. 109
Lampiran 12. Perhitungan persen rendamen fraksi etanol-heksan ekstrak
metanol-air daun Macaranga tanarius L. ……….. 117
Lampiran 13. Perhitungan konversi dosis 191,8 mg/kg BB mencit ke
xvii
INTISARI
Nyeri merupakan perasaan sensoris dan emosional yang tidak nyaman sehingga menyebabkan seseorang datang untuk mencari pertolongan medis. Oleh karena itu diperlukan analgesik untuk mengatasi nyeri. Penelitian ini bertujuan untuk mengetahui pengaruh pemberian sediaan fraksi etanol-heksan ekstrak metanol-air daun Macaranga tanarius L. terhadap efek analgesik pada mencit betina galur Swiss yang terinduksi asam asetat 1%.
Penelitian ini merupakan penelitian eksperimental murni dengan rancangan acak lengkap pola searah. Dua puluh lima ekor mencit umur 2-3 bulan dan berat badan 20-30 gram dikelompokkan ke dalam 5 kelompok yaitu kelompok kontrol negatif (Aquadest dosis 191,8 mg/kg BB), kelompok kontrol positif (Asetosal dosis 91mg/kg BB), dan kelompok fraksi etanol-heksan ekstrak metanol-air daun Macaranga tanarius L. dalam tiga peringkat dosis yaitu 47,95; 95,9; dan 191,8 mg/kg BB. Kontrol dan bahan uji diberikan secara per oral, kemudian diberi asam asetat 1% secara intraperitoneal sebagai penginduksi nyeri dengan selang waktu pemberian selama 10 menit. Pengamatan geliat dilakukan setiap 5 menit selama 1 jam. Jumlah geliat digunakan untuk menghitung nilai % proteksi, dan nilai perubahan % proteksi. Hasil dianalisis dengan uji Shapiro Wilk, dilanjutkan uji One Way ANOVA dan uji Scheffe dengan taraf kepercayaan 95%.
Hasil penelitian menunjukkan bahwa fraksi etanol-heksan ekstrak metanol-air daun Macaranga tanarius L. memiliki efek analgesik dengan % proteksi pada dosis 47,95; 95,9; dan 191,8 mg/kg BB secara berturut-turut adalah 57,83; 65,12; dan 79,24 dan perubahan % proteksi secara berturutturut adalah -6,42; 5,35; dan 28,21. Tidak terdapat kekerabatan antara efek analgesik dan dosis fraksi yang diberikan.
Kata kunci: analgesik, fraksi etanol-heksan, ekstrak metanol-air, daun
xviii
ABSTRACT
Pain is an unpleasant sensory and emotional experience, causing a person to find medical help. Therefore it needs an analgesic to relieve pain. In this present study, the writer has investigated the analgesic effect of ethanol-hexane fraction from methanol-water extract of Macaranga tanarius L. leaves using models of acetic acid-induced writhing response in female Swiss mice.
This study is pure experimental with completely randomized design. Twenty-five mice aged 2-3 months and weighed 20-30 grams are grouped into 5 groups: negative control group (Aquadest dose of 191.8 mg / kg), a positive control group (aspirin dose of 91mg / kg), and the group of ethanol-hexane fraction of methanol-water extract of Macaranga tanarius L. leaves in three doses ie 47.95; 95.9; and 191.8 mg / kg. Aspirin and fraction are given orally, then given a 1% acetic acid intraperitoneally as an inducer of pain with an interval of administration for 10 minutes. Observation of writhing response is done every 5 minutes in 1 hour. The amount of writhing response is used to calculate the value of percent protection, that used to calculate change of percent protection to determine the analgesic effect writhing test compounds against asetosal. The results obtained were analyzed by Shapiro Wilk test, followed by One Way ANOVA test and Scheffe test with 95% confidence level.
The results showed that ethanol-hexane fraction of methanol-water extract of Macaranga tanarius L. leaves has an analgesic effect. Percent protection at doses of 47.95; 95.9; and 191.8 mg / kg respectively was 57.83; 65.12; and 79.24% and change of % protection was -6.42; 5.35; and 28.21. There is no kinship between the analgesic effect and dose fractions are given.
1
BAB I PENGANTAR
A. Latar Belakang
Nyeri adalah perasaan sensoris dan emosional yang tidak nyaman,
berkaitan dengan (ancaman) kerusakan jaringan yang dapat disebabkan oleh
rangsangan mekanis, kimiawi atau fisis (kalor dan listrik). Rangsangan tersebut
memicu pelepasan zat-zat tertentu yang disebut mediator nyeri, antara lain
histamin, bradikinin, leukotrien, dan prostaglandin (Tjay dan Rahardja, 2007).
Nyeri menjadi masalah kesehatan yang menjadi alasan seseorang datang
untuk mencari pertolongan medis. Menurut Goldberg dan Summer (2011), secara
global diperkirakan 20% orang dewasa mengalami nyeri dan sebanyak 10% orang
dewasa terdiagnosa mengalami nyeri kronik setiap tahunnya.
Dalam pengatasan nyeri diperlukan analgesik yaitu zat-zat yang dapat
mengurangi atau menghalau rasa nyeri. Analgesik dapat diperoleh dari tanaman
obat yang dipercaya oleh masyarakat secara turun-temurun, maupun yang telah
terbukti dapat mengatasi nyeri. Menurut penelitian Musa, Aliyu, Yaro, Magaji,
Hassan dan Abdullahi (2009), pengobatan herbal masih digunakan sebagai
pengobatan utama di negara berkembang, yaitu sekitar 75-80% dari total jumlah
penduduk. Beberapa tahun terakhir, pengobatan herbal di negara maju mulai
meningkat.
Salah satu tanaman obat yang terbukti memiliki aktivitas terhadap proteksi
nyeri adalah Macaranga tanarius L. melalui penelitian yang dilakukan oleh
memiliki efek analgesik pada mencit betina galur Swiss. Selain itu, penelitian oleh
Andini (2010) juga membuktikan bahwa ekstrak metanol-air daun Macaranga
tanarius L. memiliki efek analgesik pada mencit betina galur Swiss. Penelitian
terkait kandungan senyawa yang bertanggung jawab untuk proteksi nyeri telah
dilakukan oleh Matsunami et al. (2006) dan Matsunami et al. (2009) yang
melaporkan adanya senyawa glikosida yang diisolasi dari daun Macaranga
tanarius L. yaitu mallophenol B, macarangioside A, B, C, dan E, serta
pinoresinol 4-O-[6”-O-galloyl]-β-D-glucopyranoside yang tersari melalui fraksi
butanol dan menunjukkan aktivitas penangkapan radikal DPPH.
Penelitian oleh Puteri dan Kawabata, (2010) juga berhasil mengisolasi dan
mengidentifikasi empat senyawa ellagitannin dari ekstrak metanol-air daun
Macaranga tanarius L. yang berperan sebagai antidiabetes melalui pemisahan
secara kromatografi sehingga diperoleh senyawa mallotinic acid, corilagin,
chebulagic acid, dan macatannins B dengan nilai koefisien partisi secara
berturut-turut adalah 1,65; 1,10; 2,30; dan 2,57. Koefisien partisi pada rentang ≤ 2 hingga
≤ 4 bersifat semipolar. Ellagitannin termasuk golongan polifenol kompleks yang
memiliki efek terhadap penangkapan radikal DPPH. Konsentrasi total ellagitannin
memiliki korelasi positif terhadap aktivitas antioksidan (Jordao, Correia,
DelCampo, dan SanJose, 2012).
Tjay dan Rahardja (2007) menyatakan bahwa ada kaitan antara
penangkapan radikal bebas dengan penghambatan mediator-mediator nyeri dan
peradangan. Adanya aktivitas antioksidan atau penangkapan radikal DPPH oleh
kemampuan senyawa tersebut dalam menangkap radikal bebas dalam tubuh yang
dilepaskan pada proses pembentukan mediator-mediator nyeri dan peradangan.
Radikal bebas akan dilepaskan ketika asam arakidonat diubah menjadi
endoperoksida dan asam hidroksiperoksida melalui jalur siklooksigenase dan
lipooksigenase. Radikal bebas merupakan molekul yang tidak stabil sehingga
akan mengambil elektron dari molekul atau sel lain di dalam tubuh untuk
mestabilkan diri. Proses pengambilan elektron ini akan menyebabkan terjadinya
kerusakan jaringan dan pelepasan mediator-mediator nyeri. Apabila radikal bebas
tersebut dapat dihambat, maka terjadinya nyeri dapat terhambat.
Penelitian ini dilakukan untuk mengetahui apakah senyawa ellagitannin
dalam daun Macaranga tanarius L. yang bersifat sebagai antioksidan dan telah
terbukti memiliki efek antidiabetes juga memiliki aktivitas sebagai analgesik.
Selain itu, penelitian efek analgesik daun Macaranga tanarius L. dari bentuk
sediaan fraksi belum pernah dilakukan. Berdasarkan uraian latar belakang ini,
penulis tertarik untuk melakukan penapisan efek analgesik fraksi etanol-heksan
ekstrak metanol-air daun Macaranga tanarius L. dengan metode geliat pada
mencit galur Swiss. Tujuan penyarian dengan metode fraksinasi adalah untuk
menyari secara spesifik dua senyawa ellagitanin dalam daun Macaranga tanarius
L. yaitu chebulagic acid dan macatannins B yang bersifat semipolar. Pemilihan
pelarut didasarkan pada prinsip like dissolve like, sehingga pelarut yang digunakan
adalah campuran pelarut etanol-heksan dengan nilai log p campuran 2,97 yang
memiliki rentang polaritas semipolar sehingga dapat menyari senyawa chebulagic
1. Rumusan masalah
a. Apakah pemberian fraksi etanol-heksan ekstrak metanol-air daun
Macaranga tanarius L.memiliki efek analgesik pada mencit galur Swiss?
b. Berapa persen proteksi geliat fraksi etanol-heksan ekstrak metanol-air daun
Macaranga tanarius L. pada mencit galur Swiss?
c. Berapa perubahan persen proteksi geliat fraksi etanol-heksan ekstrak
metanol-air daun Macaranga tanarius L. pada mencit galur Swiss?
d. Apakah terdapat kekerabatan antara efek analgesik dan dosis fraksi
etanol-heksan ekstrak metanol-air daun Macaranga tanarius L.?
2. Keaslian penelitian
Penelitian yang telah dilakukan terkait daun Macaranga tanarius L. dapat
dilihat pada tabel I.
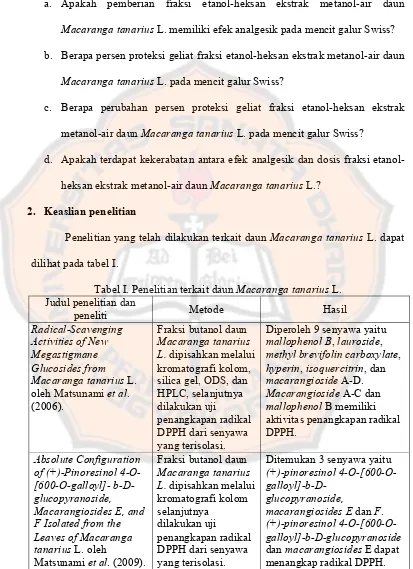
Tabel I. Penelitian terkait daun Macaranga tanarius L. Judul penelitian dan
peneliti Metode Hasil
Radical-Scavenging Activities of New Megastigmane Glucosides from Macaranga tanarius L. oleh Matsunami et al. (2006).
Fraksi butanol daun
Macaranga tanarius L. dipisahkan melalui kromatografi kolom, silica gel, ODS, dan HPLC, selanjutnya dilakukan uji
penangkapan radikal DPPH dari senyawa yang terisolasi.
Diperoleh 9 senyawa yaitu
mallophenol B, lauroside,
methyl brevifolin carboxylate,
hyperin, isoquercitrin, dan
macarangioside A-D.
Macarangioside A-C dan
mallophenol B memiliki aktivitas penangkapan radikal DPPH.
Absolute Configuration of (+)-Pinoresinol 4-O-[600-O-galloyl]- b-D-glucopyranoside, Macarangiosides E, and F Isolated from the Leaves of Macaranga tanarius L. oleh
Matsunami et al. (2009).
Fraksi butanol daun
Macaranga tanarius L. dipisahkan melalui kromatografi kolom selanjutnya
dilakukan uji
penangkapan radikal DPPH dari senyawa yang terisolasi.
Ditemukan 3 senyawa yaitu
(+)-pinoresinol 4-O-[600-O-
galloyl]-b-D-glucopyranoside,
macarangiosides E dan F.
(+)-pinoresinol 4-O-[600-O-galloyl]-b-D-glucopyranoside
Tabel I. Lanjutan
Novel α-glucosidase Inhibitors from
Macaranga tanarius L.
Leaves oleh Puteri dan Kawabata (2010).
Ekstrak etanol daun
Macaranga tanarius
L. dianalisis dengan kromatografi (HPLC) untuk mengisolasi senyawa aktif yang memiliki aktivitas
penghambatan α-glucosidase yang penting dalam pengobatan hiperglikemia.
Ditemukan 5 senyawa
ellagitannin yang berhasil diisolasi dan diidentifikasi. Senyawa tersebut adalah
mallotinic acid, corilagin,
chebulagic acid, dan dua senyawa baruyaitu
macatannin A dan B.
Efek Analgesik Ekstrak Metanol-Air Daun
Macaranga tanarius L. pada Mencit Betina Galur Swiss (Andini, 2010).
Pengujian efek analgesik menggunakan rangsang kimia yaitu asam asetat sebagai penginduksi nyeri.
Ekstrak metanol-air daun
Macaranga tanarius L. memiliki efek analgesik dengan persen proteksi pada dosis 711, 2.133, dan 6.400 mg/kg BB berturut-turut adalah 41,94; 76,94, dan 84,92%. Besar perubahan proteksi pada dosis 711, 2.133, dan 6.400 mg/kg BB berturut-turut adalah -48,1; 2,7; dan 35,9. Besar ED50
ekstrak metanol-air daun M.tanarius adalah 1.470 mg/kg BB.
Efek Analgesik Infusa Daun Macaranga tanarius L. pada Mencit Betina Galur Swiss oleh Wulandari (2010).
Pengujian efek analgesik menggunakan rangsang kimia yaitu asam asetat sebagai penginduksi nyeri.
Infusa daun Macaranga tanarius L. memiliki efek analgesik dengan persen proteksi pada dosis 666,68; 3333,4 dan 16667 mg/kg BB berturut turut adalah 57,6; 64,5; dan 73,7%. Besar perubahan persen proteksi pada dosis 666,68; 3333,4 dan 16667 mg/kgBB berturut turut adalah -9,7%, 1,2% dan 15,6%. ED50 infusa daun Macaranga tanarius L.adalah 154,88 mg/kg BB.
Sejauh pengetahuan penulis, penelitian efek analgesik fraksi etanol-heksan
3. Manfaat penelitian
a. Manfaat teoritis. Penelitian ini diharapkan dapat memberikan informasi
mengenai khasiat daun Macaranga tanarius L. yang dapat digunakan
sebagai analgesik.
b. Manfaat praktis. Penelitian ini diharapkan dapat memberikan informasi
kepada masyarakat tentang ada tidaknya efek analgesik fraksi
etanol-heksan ekstrak metanol-air daun Macaranga tanarius L.
B. Tujuan Penelitian 1. Tujuan umum
Mengetahui pengaruh pemberian sediaan fraksi etanol-heksan ekstrak
metanol-air daun Macaranga tanarius L. terhadap efek analgesik pada mencit
galur Swiss yang terinduksi asam asetat 1%.
2. Tujuan khusus
a. Mengetahui besar persen proteksi geliat fraksi etanol-heksan ekstrak
metanol-air daun Macaranga tanarius L.pada mencit galur Swiss.
b. Mengetahui besar perubahan proteksi geliat fraksi etanol-heksan ekstrak
metanol-air daun Macaranga tanarius L.pada mencit galur Swiss.
c. Mengetahui ada tidaknya kekerabatan antara efek analgesik dan dosis
7
BAB II
PENELAAHAN PUSTAKA
A. Nyeri 1. Pengertian nyeri
Nyeri adalah perasaan sensoris dan emosional yang tidak nyaman,
berkaitan dengan (ancaman) kerusakan jaringan. Nyeri merupakan suatu perasaan
subjektif pribadi dan ambang toleransi nyeri berbeda-beda bagi setiap orang. Rasa
nyeri dalam kebanyakan hal hanya merupakan suatu gejala yang berfungsi sebagai
isyarat bahaya tentang adanya gangguan di jaringan, seperti peradangan, infeksi
jasad renik atau kejang otot. Nyeri yang disebabkan oleh rangsangan mekanis,
kimiawi atau fisis (kalor, listrik) dapat menimbulkan kerusakan pada jaringan.
Rangsangan tersebut memicu pelepasan zat-zat tertentu yang disebut mediator
nyeri, antara lain histamin, bradikinin, leukotrien dan prostaglandin (Tjay dan
Rahardja, 2007).
2. Ambang dan toleransi nyeri
Ambang nyeri adalah tingkat stimulus yang pertama kali dipersepsikan
sebagai nyeri (Corwin, 2009). Toleransi nyeri adalah kemampuan individu untuk
menahan stimulus nyeri tanpa memperlihatkan tanda fisik nyeri. Toleransi nyeri
bergantung pada pengalaman sebelumnya, harapan budaya, serta keadaan emosi
dan fisik individu. Faktor yang menurunkan toleransi nyeri adalah pajanan
berulang nyeri, kelelahan, kekurangan tidur, rasa cemas, dan ketakutan (Hartwig
3. Klasifikasi nyeri
Nyeri dapat diklasifikasikan ke dalam beberapa golongan berdasarkan
pada tempat, berat ringannya, waktu lamanya serangan dan mekanisme terjadinya:
a. Nyeri berdasarkanA tempatnya:
1) Pheriperal pain, yaitu nyeri yang terasa pada permukaan tubuh misalnya
pada kulit, mukosa.
2) Deep pain, yaitu nyeri yang terasa pada permukaan tubuh yang lebih
dalam atau pada organ-organ tubuh viseral.
3) Refered pain, yatu nyeri dalam yang disebabkan karena penyakit
organ/struktur dalam tubuh yang ditransmisikan ke bagian tubuh di daerah
yang berbeda, bukan daerah asal nyeri.
4) Central pain, yaitu nyeri yang terjadi karena perangsangan pada sistem
saraf pusat, spinal cord, batang otak, dan thalamus.
(Asmadi, 2008).
b. Nyeri berdasarkan berat ringannya:
1) Nyeri ringan, yaitu nyeri dengan intensitas rendah.
2) Nyeri sedang, yaitu nyeri yang menimbulkan reaksi.
3) Nyeri berat, yaitu nyeri dengan intensitas yang tinggi.
(Asmadi, 2008).
c. Nyeri berdasarkan waktu lamanya serangan:
1) Nyeri Akut
Nyeri akut berlangsung secara tiba-tiba dan umumnya
mengindikasikan adanya suatu kerusakan atau cedera yang baru saja
terjadi. Sensasi dari nyeri akut biasanya menurun sejalan dengan adanya
proses penyembuhan. Nyeri akut memiliki tujuan untuk memperingatkan
adanya suatu cedera atau masalah. Nyeri akut umumnya berlangsung
kurang dari enam bulan (Muttaqin, 2008).
2) Nyeri Kronis
Nyeri kronis merupakan suatu keadaan yang berlangsung secara
konstan atau intermiten dan menetap sepanajang suatu periode waktu.
Keadaan ketidaknyamanaan yang dialami individu dapat berlangsung
selama enam bulan atau lebih. Nyeri kronis memiliki pola yang beragam.
Nyeri ada yang timbul dengan periode yang diselingi interval bebas dari
nyeri lalu nyeri akan timbul kembali, ada pula pola nyeri kronis yang
konstan, artinya rasa nyeri tersebut terus-menerus terasa dan semakin lama
intensitasnya meningkat walaupun telah diberikan pengobatan (Muttaqin,
2008).
d. Nyeri berdasarkan mekanismenya:
1) Nyeri nosiseptif
Terjadinya nyeri oleh karena stimuli yang sangat kuat sehingga
merusak jaringan. Jaringan yang dirusak mengalami inflamasi dan
mengeluarkan berbagai mediator inflamasi, seperti bradikinin, leukotrien,
prostaglandin, purin dan sitokin yang dapat mengaktivasi atau
mensensitisasi nosiseptor secara langsung maupun tidak langsung.
stimulus untuk meregang, dan substansi kimia yang dilepaskan oleh
jaringan yang kehilangan oksigen, jaringan yang terganggu atau proses
inflamasi. Nyeri yang ditimbulkan dapat dibagi lagi menjadi nyeri somatik
yaitu nyeri yang disebabkan oleh aktivasi nosiseptor pada permukaan
jaringan misalnya kulit, mukosa pada mulut dan hidung; serta nyeri
viseral, yaitu nyeri yang disebabkan karena aktivasi nosiseptor pada organ
dalam tubuh seperti organ pada rongga perut atau rongga dada (WHO,
2012).
2) Nyeri neuropatik
Merupakan nyeri yang didahului dan disebabkan adanya kerusakan
dan disfungsi pada sistem saraf di perifer maupun di sistem saraf pusat
yang diakibatkan oleh trauma, kompresi, keracunan toksin, atau gangguan
metabolik. Akibat adanya lesi, maka terjadi perubahan khususnya pada
Serabut Saraf Aferen (SSA) atau fungsi neuron sensorik yang dalam
keadaan normal dipertahankan secara aktif oleh keseimbangan antara
neuron dengan lingkungannya, sehingga menimbulkan gangguan
keseimbangan. Gangguan keseimbangan tersebut dapat melalui perubahan
molekuler sehingga aktivasi SSA (mekanisme perifer) menjadi abnormal
yang selanjutnya menyebabkan gangguan fungsi sentral (WHO, 2012).
4. Mekanisme terjadinya nyeri:
Munculnya nyeri sangat berkaitan erat dengan reseptor dan adanya
rangsangan. Reseptor nyeri yang dimaksud adalah nosiseptor, merupakan ujung-
mukosa. Reseptor nyeri dapat memberikan respon akibat adanya stimulasi atau
rangsangan yang melebihi nilai ambang tertentu (nilai ambang nyeri). Stimulasi
tersebut dapat berupa kimiawi, termal, listrik, atau mekanis. Stimulasi
menyebabkan lepasnya histamine, bradikinin, prostaglandin, K+, leukotrien,
serotonin dan substansi P (Hidayat dan Hidayat, 2008).
Rangkaian proses perjalanan yang menyertai antara kerusakan jaringan
sampai nyeri yang dapat dirasakan adalah suatu proses elektrofisiologi. Menurut
Timby (2009), ada 4 proses yang mengikuti proses nosiseptitif yaiu:
a. Transduksi. Transduksi adalah perubahan rangsangan nyeri (noxious stimuli)
menjadi aktivitas listrik pada ujung-ujung saraf sensoris. Mediator nyeri
seperti prostaglandin, serotonin, bradikinin, leukotrien, substansi P, histamine,
dan potassium akan mengaktifkan atau mensensitisasi reseptor-reseptor nyeri.
Reseptor nyeri merupakan anyaman ujung-ujung bebas serat-serat afferent
A-delta dan C. Reseptor-reseptor ini banyak dijumpai di jaringan kulit,
periosteum, di dalam pulpa gigi dan jaringan tubuh yang lain. Serat saraf
afferent A-delta dan C adalah serat-serat saraf sensorik yang mempunyai
fungsi meneruskan sensorik nyeri dari perifer ke sentral ke sistem saraf pusat.
Interaksi antara mediator nyeri dengan reseptor nyeri menyebabkan
terbentuknya impuls nyeri. Transduksi adalah proses dari stimulasi dikonversi
menjadi bentuk yang dapat diakses oleh otak. Proses transduksi dimulai ketika
nosiseptor teraktivasi. Aktivasi nosiseptor merupakan bentuk respon terhadap
b. Transmisi. Transmisi adalah serangkaian kejadian-kejadian neural yang
membawa impuls listrik melalui sistem saraf ke area otak. Proses transmisi
melibatkan saraf aferen yang terbentuk dari serat saraf berdiameter kecil ke
diameter sedang, serta yang berdiameter besar. Saraf aferen akan berakson
pada dorsal horn di spinalis. Selanjutnya transmisi ini dilanjutkan melalui
sistem contralateral spinothalamic melalui ventral lateral dari thalamus
menuju cortex serebral.
c. Modulasi. Proses modulasi mengacu kepada aktivitas neural dalam upaya
mengontrol jalur transmisi nosiseptor tersebut. Proses modulasi melibatkan
sistem neural yang komplek. Ketika terdapat impuls nyeri akan dikontrol oleh
sistem saraf pusat dan impuls nyeri ini ditransmisikan ke bagian lain dari
sistem saraf seperti bagian cortex. Selanjutnya impuls nyeri ini akan
ditransmisikan melalui saraf-saraf descenden ke tulang belakang untuk
memodulasi efektor.
d. Persepsi. Persepsi adalah proses yang subyektif. Proses persepsi ini tidak
hanya berkaitan dengan proses fisiologis atau proses anatomis saja, akan tetapi
juga meliputi pengenalan dan mengingat. Oleh karena itu, faktor psikologis,
emosional, dan perilaku juga muncul sebagai respon dalam mempersepsikan
pengalaman nyeri tersebut.
B. Analgesik
Analgesik adalah senyawa yang dalam dosis terapeutik meringankan atau
kerja, mekanisme kerja dan efek samping, analgesik dibedakan dalam dua
kelompok:
1. Analgesik Nonopioid
Senyawa ini mengobati nyeri ringan sampai sedang dengan mempengaruhi
sintesis prostaglandin. Pada perifer, prostaglandin diproduksi oleh sel-sel
inflamasi yang mensensitisasi reseptor prostaglandin pada saraf perifer sehingga
membentuk stimulus nyeri. Pada nyeri sentral sitokin dilepaskan sebagai respon
inflamasi sehingga menginduksi produksi prostaglandin pada sumsum tulang
belakang. Prostaglandin ini mensensitisasi saraf nosiseptif sekunder sehingga
meningkatkan persepsi nyeri. Antiinflamasi nonsteroid (NSAIDs) menghambat
prostaglandin untuk sensitisasi saraf perifer dan sentral ketika terjadi proses
inflamasi (Goland, 2011).
Agen antiinflamasi nonsteroid menghambat aktivitas enzim
siklooksigenasi (COX-1 dan COX-2) yang dibutuhkan untuk produksi
prostaglandin. Penghambatan sistem siklooksigenase menyebabkan asam
arakhidonat dan asam-asam C20 tak jenuh lain tidak diubah menjadi
endoperoksida siklik. Endoperoksida siklik merupakan prazat dari prostaglandin
serta prazat dari tromboksan A2 dan prostasiklin (Goland, 2011).
NSAIDs mempengaruhi mekanisme nyeri melalui 3 cara. Pertama,
NSAIDs mengurangi aktifasi ambang pintu perifer pada saraf nosiseptor afferent
primer. dengan mengurangi pembentukan prostaglandin, NSAIDs dapat
menurunkan inflamasi hyperalgesia dan allodynia. Kedua, NSAIDs menurunkan
blood-brain barrier dan mencegah prostaglandin yang bekerja untuk memproduksi
neuromodulator di sumsum tulang belakang (Goland, 2011).
2. Analgesik Opioid
Menurut Staf Pengajar Departemen Farmakologi Fakultas Kedokteran
Universitas Sriwijaya (2008), analgesik opioid adalah golongan obat penghilang
nyeri alamiah, semisintetis, dan sintetis yang sebagian sifat-sifatnya sama atau
hampir sama dengan opium atau morfin. Penggunaan utama opioid ini adalah
untuk mengatasi rasa nyeri yang tidak hilang dengan analgesik biasa. Analgesik
opioid bekerja dengan berikatan dengan reseptor stereospesifik di sistem saraf
pusat, dengan mengubah persepsi dan respons emosi terhadap nyeri.
Analgesik opioid menyerupai peptide opioid endogen (terutama dinorfin)
yang dilepaskan pada batang otak maupun medulla spinalis bersama input inhibisi
lainnya yaitu serabut enkefalinergik, noradrenergik, dan serotonergik desendens
sehingga dapat menurunkan aktivitas neuron relay kornu posterior yang berperan
menyampaikan informasi nyeri ke korteks sensoris melalui neuron dalam
thalamus sehingga dapat menyebabkan analgesia (Neal, 2006).
Efek peptide opioid diperantarai oleh reseptor opioid spesifik yang
terdistribusi luas dalam sistem saraf pusat dan sudah diklasifikasikan menjadi tiga
tipe utama. Reseptor µ mempunyai konsentrasi yang paling tinggi dalam daerah
otak yang terlibat dalam nosisepsi dan merupakan reseptor yang berinteraksi
dengan sebagian besar analgesik opioid untuk menghasilkan analgesia. Reseptor
δ dan κ masing-masing menunjukkan selektivitas untuk enkefalin dan dimorfin.
µ (misalnya morfin) yang menyebabkan euphoria, agonis κ (misalnya pentazosin,
nalbufin) berhubungan dengan disforia (Neal, 2006).
Morfin dan alkaloid opium alamiah diperoleh dari opium (candu) yang
merupakan getah kering tanaman
golongan zat kimia penting, yaitu golongan
golongan Benzyl-isokinolin
diturunkan morfin, kodein, dan berbagai analgesik semisintesis morfin, seperti
heroin, hodrokodon, oksikodon, dan antagonis opioid (Staf Pengajar Departemen
[image:36.595.103.503.296.526.2]Farmakologi Fakultas Kedokteran Universitas Sriwijaya, 2008).
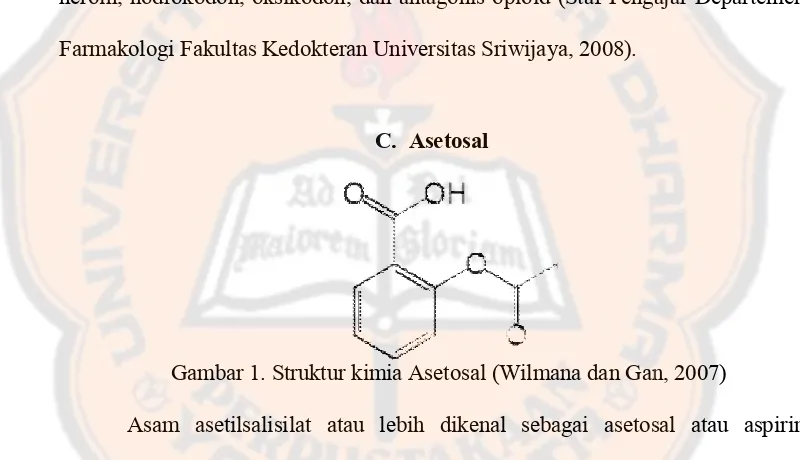
Gambar 1
Asam asetilsalisilat atau lebih dikenal sebagai asetosal atau aspirin
(gambar 1) merupakan ester salisilat dari asam, berbentuk kristal
batang atau jarum dan berbau. A
dalam alkohol. Asetosal termasuk dalam golongan analgesik non
indikasi sebagai pereda nyeri, sakit kepala, nyeri ringan yang berhubungan dengan
adanya inflamasi, nyeri ringan sampai sedang setelah operasi, dan sakit gigi
(Dinkes, 2010).
µ (misalnya morfin) yang menyebabkan euphoria, agonis κ (misalnya pentazosin,
ubungan dengan disforia (Neal, 2006).
Morfin dan alkaloid opium alamiah diperoleh dari opium (candu) yang
merupakan getah kering tanaman Papaver somniferum. Dalam opium terdapat 2
golongan zat kimia penting, yaitu golongan fenantren (morfin dan kodein), da
isokinolin (papaverin dan noskapin). Dari golongan fenantren,
diturunkan morfin, kodein, dan berbagai analgesik semisintesis morfin, seperti
heroin, hodrokodon, oksikodon, dan antagonis opioid (Staf Pengajar Departemen
s Kedokteran Universitas Sriwijaya, 2008).
C. Asetosal
1. Struktur kimia Asetosal (Wilmana dan Gan, 2007
Asam asetilsalisilat atau lebih dikenal sebagai asetosal atau aspirin
merupakan ester salisilat dari asam, berbentuk kristal
batang atau jarum dan berbau. Asetosal sedikit larut dalam air dan
dalam alkohol. Asetosal termasuk dalam golongan analgesik
non-indikasi sebagai pereda nyeri, sakit kepala, nyeri ringan yang berhubungan dengan
nyeri ringan sampai sedang setelah operasi, dan sakit gigi µ (misalnya morfin) yang menyebabkan euphoria, agonis κ (misalnya pentazosin,
Morfin dan alkaloid opium alamiah diperoleh dari opium (candu) yang
. Dalam opium terdapat 2
(morfin dan kodein), dan
(papaverin dan noskapin). Dari golongan fenantren,
diturunkan morfin, kodein, dan berbagai analgesik semisintesis morfin, seperti
heroin, hodrokodon, oksikodon, dan antagonis opioid (Staf Pengajar Departemen
Wilmana dan Gan, 2007)
Asam asetilsalisilat atau lebih dikenal sebagai asetosal atau aspirin
merupakan ester salisilat dari asam, berbentuk kristal putih, seperti
setosal sedikit larut dalam air dan sangat larut
-narkotik dengan
indikasi sebagai pereda nyeri, sakit kepala, nyeri ringan yang berhubungan dengan
Asetosal adalah obat anti-nyeri tertua yang sampai saat ini paling banyak
digunakan di seluruh dunia. Zat ini juga berkhasiat anti-demam kuat (antipiretik)
dan pada dosis rendah (80 mg) berdaya menghambat agregasi trombosit. Pada
dosis lebih besar dari normal (diatas 5 gram sehari) obat ini juga berkhasiat
antiradang akibat gagalnya sintesis prostaglandin-E (Tjay dan Rahardja, 2007).
Asetosal adalah prototip dari obat-obat antiinflamasi nonsteroid dan
bekerja dengan jalan menghambat enzim siklo-oksigenase tetapi tidak enzim
lipooksigenase. Asetosal cepat dideasetilasi oleh esterase dalam tubuh,
menghasilkan salisilat, yang mempunyai efek anti-inflamasi, antipiretik, dan
analgesik (Mycek, Richard, dan Pamela, 2001).
Mekanisme asetosal dalam menekan rasa nyeri adalah dengan menurunkan
sintesis PGE2. Prostaglandin E2 (PGE2) akan mensensitisasi ujung saraf terhadap
efek bradikinin, histamine, dan mediator kimiawi lainnya yang dilepaskan secara
lokal oleh proses inflamasi. Salisilat digunakan terutama untuk menanggulangi
rasa sakit intensitas ringan sampai sedang yang timbul dari struktur integumen
daripada yang berasal dari visera ( Mycek, Richard, dan Pamela 2001).
[image:37.595.101.506.261.691.2]D. Macaranga tanarius L.
1. Taksonomi
Kerajaan : Plantae
Divisi : Maginoliophyta
Kelas : Maginoliospida
Ordo : Malpighiales
Famili : Euphorbiaceae
Sub Famili : Acalyphoides
Bangsa : Acalypheae
Sub Bangsa : Macaranginae
Genus : Macaranga
Spesies : Macaranga tanarius (L.) Benth. Mull. Arg
(Magadula, 2014).
2. Nama lain
Tanaman Macaranga tanarius L. dikenal dengan beberapa nama daerah
antara lain Tutu Ancur (Jawa), Mapu (Batak), Mara (Sunda) (Ong, 2008).
3. Morfologi
Macaranga tanarius L. (gambar 2) merupakan pohon kecil sampai
sedang, dengan dahan agak besar. Daun berseling, agak membundar, dengan
stipula besar yang luruh. Perbungaan malai di ketiak, bunga ditutupi oleh daun
gagang. Buah kapsul berkokus 2, ada kelenjar kekuningan di luarnya. Biji
4. Ekologi penyebaran dan budidaya
Tumbuhan Macaranga tanarius L. umum dijumpai di daratan Asia
Tenggara (Thailand Selatan, Semenanjung Malaya), dan pada banyak pulau antara
lain Sumatera, Borneo, Kepulauan Sunda Kecil, Sulawesi, Nugini, seluruh
kepulauan Filipina. Tumbuhan ini dapat ditemukan di sepanjang Asia Timur dan
Selatan, khususnya Cina Selatan, Koreaa dan Jepang (Ong, 2008).
5. Kandungan kimia
Daun Macaranga tanarius L. mengandung tanarifuranonol,
tanariflavanone C, dan tanariflavanone D bersama dengan 7 kandungan yang
telah diketahui yaitu nymphaeol A, nymphaeol B, nymphaeol C, tanariflavanone
B, blumenol A (vomifoliol), blumenol B (7,8 dihydrovomifoliol) dan annuionone
E (Phommart Suthivaiyakit, Chimnoi, Ruchirawat, dan Suthivaiyakit, 2005).
Dilaporkan terdapat 4 kandungan dari fraksi butanol daun Macaranga tanarius L.,
yaitu macarangiosides A-D, mallophenol B, lauroside E, methyl brevifolin
carboxylate, hyperin dan isoquercitrin (Matsunami et al., 2006). Pada daun
Macaranga tanarius L. juga ditemukan tujuh senyawa flavonoid baru yaitu
macaflavanones A-G dari penelitian oleh Kawakami, Harinantenaina, Matsunami,
Otsuka, Shinzato, dan Takeda (2008) serta (+)-pinoresinol
4-O-[6”-O-galloyl]-β-D-glucopyranoside, macarangiosides E dan F, bersama dengan 15 komponen lain
yang telah dilaporkan terdapat pada daun Macaranga tanarius L. (Matsunami et
al., 2009). Penelitian oleh Puteri dan Kawabata (2009) membuktikan bahwa daun
Macaranga tanarius L. memiliki kandungan ellagitannin berupa mallotinic acid,
koefisien partisi secara berturut-turut adalah 1,65; 1,10; 2,30; dan 2,57. Koefisien
partisi yang berada pada rentang ≤ 2 hingga ≤ 4 memiliki sifat semi polar.
6. Aktivitas Penangkapan Radikal Bebas DPPH
Radikal bebas merupakan salah satu bentuk senyawa reaktif, yang
memiliki elektron yang tidak berpasangan di kulit terluarnya sehingga bersifat
tidak stabil, dan dapat menimbulkan peradangan. Untuk menetralisasi radikal
bebas, tubuh membutuhkan antioksidan untuk melindungi tubuh dari serangan
radikal bebas dan meredam dampak negatifnya. Metode penentuan aktivitas
penangkapan radikal bebas adalah dengan menggunakan larutan
1,1-difenil-2-pikrilhidrazil (DPPH). Kemampuan penangkapan radikal berhubungan dengan
kemampuan komponen senyawa dalam menyumbangkan elektron atau hidrogen
yang akan bereaksi dan akan memudarkan DPPH (Toripah, Abidjulu, dan
Wehantouw, 2014).
Senyawa dalam daun Macaranga tanarius L. yang telah terbukti bersifat
poten terhadap penangkapan radikal bebas DPPH anatara lain adalah 4 senyawa
glikosida, yaitu mallophenol B, macarangioside A, macarangioside B, dan
macarangioside C (Matsunami et al., 2006); (+)-pinoresinol
4-O-[6”-O-galloyl]-β-D-glucopyranoside dan macarangioside E (Matsunami et al., 2009); dan
senyawa ellagitannin berupa mallonic acid, corilagin, chebulagic acid, dan
macatannin B (Puteri dan Kawabata, 2009). Struktur senyawa dalam daun
Macaranga tanarius L. yang bersifat poten terhadap penangkapan radikal bebas
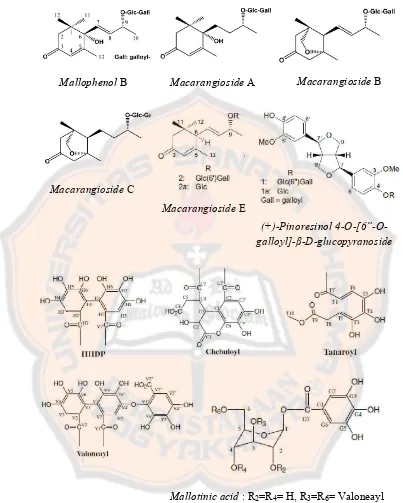
Gambar 3. Struktur senyawa dari daun Macaranga tanarius L. yang memiliki aktivitas terhadap penangkapan radikal bebas DPPH (Matsunami et al., 2006; Matsunami et al., 2009 dan Puteri dan Kawabata, 2009)
Mallophenol B Macarangioside A Macarangioside B
Macarangioside C
Macarangioside E
(+)-Pinoresinol 4-O-[6”-O-galloyl]-β-D-glucopyranoside
Mallotinic acid : R2=R4= H, R3=R6= Valoneayl Corilagin : R2=R4= H, R3=R6= HHDP
[image:41.595.98.501.105.608.2]E. Senyawa Fenolik
Fenolik adalah senyawa yang memiliki satu atau lebih cincin aromatik
dengan satu atau lebih gugus hidroksil. Senyawa fenolik merupakan senyawa
metabolit sekunder yang paling banyak ditemukan pada tanaman, dengan lebih
dari 8000 struktur fenolik yang telah diketahui, mulai dari struktur yang sederhana
seperti asam fenolat, hingga senyawa yang sangat terpolimersasi seperti tannin
(Dai dan Mumper, 2010).
Fenolik pada tanaman terdiri dari asam fenolat, flavonoid, dan tannin, serta
sedikit ligan. Flavonoid adalah jenis polifenol yang paling sering dikonsumsi.
Flavonoid dibagi ke dalam 6 sub grup yaitu flavones, flafonols, flavanols,
flavanones, isoflavones, dan antosianin berdasarkan bagian oksidasi dari cincin C
pusat. Variasi struktur pada setiap sub grup dapat disebabkan karena tingkat dan
pola hidroksilasi, metoksilasi, prenilasi, atau glikosilasi (Dai dan Mumper, 2010).
Tannin merupakan kelompok utama lainnya dari polifenol yang terdiri dari
dua kelompok yaitu tannin terhidrolisis dan tannin terkondensasi. Tannin
terhidrolisis merupakan senyawa yang mengandung inti pusat dari glukosa atau
polyol lain yang teresterifikasi dengan gallic acid, yang biasa disebut dengan
gallotanins atau teresterifikasi dengan hexahydroxydiphenic acid yang biasa
disebut dengan ellagitanin (Dai dan Mumper, 2010).
F. Metode Penyarian
Menurut Departemen Kesehatan RI (1986), penyarian merupakan
oleh cairan penyari, sehingga terjadi larutan zat aktif dalam cairan penyari
tersebut. Secara umum metode penyarian dapat dibedakan menjadi:
1. Infundasi
Infundasi merupakan proses penyarian yang umumnya digunakan untuk
menyari kandungan zat aktif yang larut dalam air dari bahan-bahan nabati.
Penyarian dengan cara ini menghasilkan sari yang tidak stabil dan mudah
tercemar oleh kuman dan kapang. Oleh karena itu, sari yang diperoleh dengan
cara ini tidak boleh disimpan lebih dari 24 jam. Infusa adalah sediaan cair yang
dibuat dengan mengekstraksi simplisia nabati dengan air pada suhu 90°C selama
15 menit.
2. Maserasi
Maserasi merupakan cara penyarian yang sederhana. Maserasi dilakukan
dengan cara merendam serbuk simplisia dalam cairan penyari. Cairan penyari
akan menembus dinding sel dan masuk ke dalam rongga sel yang mengandung zat
aktif. Zat aktif akan larut karena adanya perbedaan konsentrasi antara larutan zat
aktif di dalam dan di luar sel, maka larutan yang terpekat didesak keluar. Peristiwa
tersebut berulang sehingga terjadi keseimbangan konsentrasi antara larutan di luar
dan di dalam sel.
3. Perkolasi
Perkolasi merupakan cara penyarian yang dilakukan dengan mengalirkan
cairan penyari melalui serbuk simplisia yang telah dibasahi. Prinsip perkolasi
adalah simplisia ditempatkan dalam suatu bejana silinder yang di bagian
melalui serbuk tersebut dan akan melarutkan zat aktif dari sel-sel yang dilalui
sampai mencapai keadaan jenuh.
4. Ekstrak
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat
aktif dari simplisia nabati atau hewani menggunakan pelarut yang sesuai,
kemudian semua atau hampir semua pelarut diuapkan dan massa serbuk yang
tersisa diperlakukan sedemikian rupa hingga baku yang telah ditetapkan.
G. Proses penyarian senyawa aktif 1. Pembuatan ekstrak
a. Pembuatan serbuk simplisia dan klasifikasinya. Proses awal pembuatan
ekstrak adalah tahap pembuatan serbuk simplisia kering (penyerbukan).
Proses ini dapat mempengaruhi mutu ekstrak karena makin halus
simplisia, proses ekstraksi makin efektif-efisien, namun makin halus
serbuk, maka makin rumit secara teknologi peralatan untuk tahap filtrasi.
Dalam hal simplisia sebagai bahan baku (awal) dan produk siap
dikonsumsi langsung, dapat dipertimbangkan 3 konsep untuk menyusun
parameter standar umum :
1) Bahwa simplisia sebagai bahan kefarmasian seharusnya memenuhi 3
parameter mutu umum suatu bahan (material), yaitu kebenaran jenis
(identifikasi), kemurnian (bebas dari kontaminasi kimia dan biologis),
serta aturan penstabilan (wadah, penyimpanan, dan transportasi).
2) Bahwa simplisia sebagai bahan dan produk konsumsi manusia sebagai
kefarmasian lainnya, yaitu Quality-Safety-Efficacy
(Mutu-Aman-Manfaat).
3) Bahwa simplisia sebagai bahan dengan kandungan kimia yang
bertanggung jawab terhadap respon biologis harus mempunyai
spesifikasi kimia, yaitu informasi komposisi (jenis dan kadar) senyawa
kandungan.
(Departemen Kesehatan RI, 2000).
b. Cairan pelarut. Cairan pelarut dalam proses pembuatan ekstrak merupakan
pelarut yang baik (optimal) untuk senyawa kandungan yang berkhasiat
atau yang aktif, dengan demikian senyawa tersebut dapat terpisahkan dari
bahan dan dari senyawa kandungan lainnya, serta ekstrak hanya
mengandung sebagian besar senyawa kandungan yang diinginkan. Dalam
hal ekstrak total, maka cairan pelarut dipilih yaitu yang melarutkan hampir
semua metabolit sekunder yang terkandung. Faktor utama untuk
pertimbangan pada pemilihan cairan penyari adalah sebagai berikut:
1) Selektivitas
2) Kemudahan bekerja dan proses dengan cairan ersebut
3) Ekonomis
4) Ramah lingkungan
5) Keamanan
(Departemen Kesehatan RI, 2000).
c. Maserasi. Maserasi dihasilkan dengan merendam bahan tanaman dalam
ruangan. Pada proses ekstraksi ini, bahan tanaman direndam dengan
pelarut dalam wadah tertutup. Larutan diaduk untuk meningkatkan
penyarian senyawa aktif dari bahan tanaman. Setelah penyarian
berlangsung sempurna, bahan tanaman dipisahkan dari pelarutnya melalui
penyaringan. Bahan tanaman selanjutnya ditambah dengan pelarut yang
baru untuk merendam bahan tanaman tersebut. Langkah ini dapat diulang
selama beberapa kali untuk memastikan bahwa penyarian zat aktif dari
bahan tanaman berlangsung sempurna. Maserasi dapat membutuhkan
waktu dalam hitungan jam hingga hari untuk satu kali proses ekstraksi,
dan membutuhkan waktu hingga beberapa minggu untuk melakukan
remaserasi. Walaupun maserasi membutuhkan waktu yang relatif lama,
tetapi dapat digunakan untuk menyari senyawa yang bersifat tidak stabil
terhadap panas, karena prosesnya dilakukan pada suhu ruangan (Tiwari,
Brunton, dan Brennan, 2013).
d. Pemekatan/ Penguapan. Pemekatan berarti peningkatan jumlah senyawa
terlarut melalui penguapan pelarut, tetapi tidak sampai menjadi kering,
ekstrak hanya menjadi kental/pekat (Departemen Kesehatan RI, 2000).
e. Pengeringan ekstrak. Pengeringan berarti menghilangkan perarut dari
bahan sehingga menghasilkan serbuk, masa kering rapuh, tergantung
proses dan peralatan yang digunakan. Ada berbagai proses pengeringan
ekstrak, yaitu dengan cara pengeringan evaporasi, vaporasi, sublimasi,
f. Rendemen. Rendemen adalah perbandingan antara ekstrak yang diperoleh
dengan simplisia awal (Departemen Kesehatan RI, 2000).
2. Ekstraksi bertingkat
Menurut Damayanti dan Suparjana (cit Prasetyo, 2013), metode ekstraksi
bertingkat menggunakan sederet pelarut dengan kepolaran yang berbeda.
Penyarian menggunakan metode ekstraksi bertingkat yang dilakukan dengan
maserasi menggunakan beberapa cairan penyari disebut sebagai fraksinasi karena
cairan penyari yang digunakan berbeda kepolarannya sehingga senyawa dalam
fraksi yang didapat telah mengalami pemisahan bersadarkan kepolarannya.
Keuntungan metode ekstraksi bertingkat ini adalah semua senyawa yang berbeda
polaritasnya dapat diekstraksi berdasarkan kepolaran terhadap pelarut tertentu.
H. Pelarut 1. Metanol
Pelarut yang cocok digunakan untuk campuran dengan air (panas atau
dingin) adalah metanol, etanol, aseton, dan etil asetat. Metanol dan etanol telah
banyak digunakan untuk mengekstrak antioksidan (Sultana et al., 2009).
Metanol atau methyl alkohol memiliki rumus molekul CH4O, merupakan
cairan yang tidak berwarna dan mudah menguap dengan bau yang menyengat
seperti etil alkohol, selain itu metanol dapat bercampur sempurna dengan air.
Metanol memiliki titik didih 650C dan nilai polaritasnya sebesar 5,1 sehingga
bersifat polar (National Center for Biotechnology Information, 2015).
Metanol banyak digunakan sebagai larutan penyari pada metode ekstraksi
komponen baik yang bersifat polar, semi polar, maupun non-polar sehingga
metanol disebut sebagai pelarut universal (Al-Ash’ary, Supriyanti, dan Zackiyah,
2010). Metanol jika terhirup atau tertelan dapat menyebabkan gangguan
penglihatan, seperti kabur. (United States Environmental Protection Agency,
2013).
2. Etanol
Etanol atau ethyl alkohol dengan rumus molekul C2H6O dan titik didih
78,20C, merupakan cairan jernih tidak berwarna dapat dengan cepat diserap oleh
saluran pencernaan dan didistribusikan ke seluruh tubuh. Etanol memiliki
aktivitas bakterisida dan sering digunakan sebagai desinfektan topikal, selain itu
juga banyak digunakan sebagai pelarut dan pengawet dalam sediaan farmasi, dan
bahan utama minuman beralkohol (National Center for Biotechnology
Information, 2015).
Etanol di dalam tubuh akan mengalami oksidasi oleh suatu enzim hati
yaitu alkohol dehydrogenase. Hasil dari oksidasi etanol adalah asetaldehid dan
asam asetat. Namun, hasil oksidasi tersebut kurang toksik dibandingkan dengan
metanol yang menghasilkan toksik seperti formaldehid dan asam formiat (Stoker,
2010).
3. Heksan
Heksan atau N-Hexane memiliki rumus molekul C6H14 dengan titik didih
68,70C merupakan cairan jernih tidak berwarna dengan bau seperti minyak.
Heksan tidak dapat larut air dan banyak digunakan sebagai pelarut, thinner, reaksi
kimia dan sebagai agen pembersih (National Center for Biotechnology
Penggunaan heksan dalam proses fraksinasi adalah untuk memisahkan
senyawa-senyawa nonpolar seperti klorofil, triterpen, lemak dan senyawa
nonpolar lain. Hal ini dikarenakan heksan merupakan senyawa hidrokarbon yang
memiliki polaritas 0 sehingga dapat digunakan untuk menarik senyawa-senyawa
non polar yang tidak diinginkan dalam hasil proses ekstrak maupun fraksi (Agoes,
2009).
I. Metode Uji Analgesik
Pengujian efek analgesik dalam penemuan dan pengembangan agen
analgesik baru yang dilakukan pada hewan uji di laboratorium antara lain:
1. Golongan Analgesik Narkotik
a. Metode jentikan ekor. Pada uji ini ekor mencit atau tikus dicukur dan
dilapisi dengan cat penyerap panas berwarna hitam. Hewan uji
ditempatkan pada balok dengan lampu inframerah yang panas sehingga
ekor dapat menerima panas secara maksimum. Jarak antara waktu sebelum
hewan uji menjentikkan ekornya untuk keluar dari balok inframerah
dicatat. Prosedur pengujian diulangi dengan menggunakan hewan uji yang
sudah diberi dosis agen analgesik yang diteliti, dan perpanjangan waktu
selama ekor hewan uji masih berada pada balok yang panas dicatat
(Cannon, 2007).
b. Metode potensi petidin. Metode ini kurang baik untuk skrining awal,
karena dibutuhkan hewan uji dalam jumlah yang relatif besar untuk
melakukan uji ini, namun metode ini dapat digunakan untuk pengujian
setengah dari kelompok dibagi menjadi 3 bagian dan diberi petidin dengan
dosis berturut-turut 2, 4, dan 8 mg/kg. Setengah kelompok yang lain diberi
petidin dengan senyawa uji dengan dosis 25% dari LD50. Persen analgesik
dihitung dengan bantuan metode rangsang panas. Pengujian ini
memanfaatkan seperangkat alat laboratorium yang berupa lempeng panas
dengan suhu yang telah ditentukan. Hewan uji diletakkan pada lempeng
panas dan jarak waktu sebelum hewan uji menunjukkan tanda
ketidaknyamanan dicatat. Prosedur uji ini diulang dengan menggunakan
hewan uji yang telah diberi dosis agen analgesik, kemudian diamati jarak
waktu selama hewan uji masih dapat tinggal pada lempeng panas sebelum
menunjukkan tanda ketidaknyamanan. Kurva antara dosis dan respon
dibuat dan dilakukan analisis secara statistik (Cannon, 2007).
2. Golongan Analgesik Non-narkotik
a. Metode rangsang kimia. Metode ini sering digunakan sebagai protokol
pada penapisan aktivitas analgesik perifer suatu bahan obat. Prinsip dalam
metode ini adalah senyawa uji dinilai kemampuannya dalam menekan atau
menghilangkan rasa nyeri yang diinduksi secara kimia. Rasa nyeri ini pada
hewan uji diperlihatkan dalam bentuk respon gerakan geliatan. Frekuensi
gerakan ini dalam waktu tertentu menyatakan derajat nyeri yang
dirasakannya. Pada metode ini hewan uji diberikan senyawa kimia yang
dapat menginduksi nyeri berupa fenilkuinon, benzokuinon atau asam
asetat, secara intraperitoneal (i.p). Selanjutnya dilakukan pengamatan pada
meregangkan, gerakan pinggang yang memuntir, menarik kaki belakang,
dan penarikan abdomen sehingga bagian perut menyentuh lantai. Setiap
geliat yang terjadi dicatat sebagai respon positif. Pemberian analgesik akan
mengurangi jumlah geliat dalam jangka waktu tertentu. Penghambatan
geliat yang merupakan persen proteksi senyawa analgesik diukur dengan
persamaan Handerson- Forsaith yaitu:
% = 100% − ( × 100%)
Keterangan :
O = Jumlah kumulatif geliat hewan uji kelompok perlakuan K = jumlah kumulatif geliat hewan uji kelompok kontrol
(Turner, 1965).
b. Metode rektodolorimeter. Metode ini menggunakan tegangan listrik yang
dihubungkan dari voltmeter ke kandang tikus. Pada metode ini tikus
diletakkan dalam sebuah kandang yang dibuat khusus dengan lantai berupa
tembaga yang dihubungkan dengan sebuah penginduksi yang berupa
gulungan. Ujung gulungan tersebut dihubungkan dengan silinder elektroda
tembaga, sedangkan ujung yang lainnya lagi dihubungkan pada ekor
hewan uji. Sebuah voltmeter yang peka terhadap adanya perubahan
tegangan sebesar 0,1 volt selanjutnya dihubungkan dengan konduktor
yang berada di gulungan bagian atas. Tegangan yang dibutuhkan untuk
menimbulkan teriakan pada tikus adalah 1-2 volt. Respon teriakan hewan
J.Asam asetat
Asam asetat atau asam cuka (CH3COOH) adalah golongan asam
karboksilat yang sering digunakan sebagai pemberi rasa asam pada makanan,
penurun pH pada industri makanan dan sebagai zat pengawet. Asam asetat murni
dikenal sebagai asam asetat glasial yang merupakan senyawa berbentuk cairan,
tak berwarna, berbau menyengat, memiliki rasa asam yang tajam dan larut dalam
air, alkohol, gliserol, dan eter, dan memiliki titik leleh 16,6o C (Sutresna, 2007).
Pada pengujian efek analgesik asam asetat glasial digunakan sebagai
senyawa kimia yang menginduksi nyeri. Asam asetat glasial dapat merusak
membran sel dan fosfolipid yang akan merangsang munculnya mediator nyeri
(Katzung, 2002).
Pada pengujian efek analgesik, asam asetat bekerja sebagai iritan yang
merusak jaringan secara lokal. Setelah pemberian secara intraperitoneal, asam
asetat mengubah pH di dalam rongga perut akibat pelepasan ion H+<