Peubah Kualitas Air dan Kelulushidupan Udang Windu (Penaeus monodon) Pada
Penggunaan Probiotik yang di isolasi dari Sedimen Laut, Sedimen Tambak dan
Daun Mangrove
Muliani, Nurbaya, dan Ince Ayu Khairana Kadriah
Balai Riset Perikanan Budidaya Air Payau (BRPBAP)Jl. Makmur Dg. Sitakka 129, Maros, Sul-Sel 90511 Telp. (04110 371544; Fax (0411) 371545
E-mail: [email protected]
Abstract
Muliani, Nurbaya, and I.A.K. Kadriah. 2009. Evaluation of water quality and survival rate of tiger shrimp (Penaeus monodon) by using probiotic bacteria isolated from sea sediment, mangrove leaf and pond sediment. Aquacultura Indonesiana, 10 (1): 25–34. The aim of this experiment was to know the water quality and survival
rate of tiger shrimp (Penaeus monodon) by using probiotic bacteria isolated from sea sediment, mangrove leaf and pond sediment. This experiment was conducted in the Research Institute for Coastal Aquaculture (RICA) using 27 aquaria of 40x30x27 cm3 in size, layered with 10 cm thick of pond soil, and filled with 15 L of 28 ppt salinity of sea water. Each aquarium was then stocked with 30 pcs of tiger shrimp post larvae (PL25). A completely randomized design (CRD) with 9 treatments was applied in this experiment. The treatments were (A) BL542; (B) BT951; (C) MY1112; (D) BL542+BT951; (E) BL542+MY1112; (F) BT951+MY1112; (G) BL542+BT951+MY1112; (H) commercial probiotic; (I) control (without probiotic) in triplicates. The post larvae were reared until two months. Some water quality parameters were monitored beweekly include TOM (Total Organic Matter), Ammonium, Nitrite, Nitrate, phosphate, H2S, total bacteria, total Vibrio sp., total SRB, and total SOB. Survival rates of tiger shrimp were observed at the end of the experiment. The result showed that concentration of TOM, NO2-N, NO3-N, NH4-N PO4 -P, and H2S during experiment were fluctuated. The highest survival rate of tiger shrimp was obtained from treatment with probiotic bacteria from pond sediment, BT951 (treatment B) i.e. 68.9%, followed with BL542+BT951+MY1112 (treatment G) i.e. 64.5%, and the lowest one was in treatment with commercial probiotic (treatment H) i.e. 37.7%. Statistical analysis showed that the survival rate of tiger shrimp in B and G were significantly different (P<0.05) than H, but there was not significantly different (P>0.05) with the others treatments.
Keywords: Penaeus monodon, Probiotic, Survival rate, Water quality.
Abstrak
Penelitian bertujuan untuk mengetahui peubah kualitas air dan kelulushidupan udang windu (Penaeus
monodon) pada penggunaan probiotik yang diisolasi dari laut, daun mangrove dan sedimen tambak. Penelitian ini
dilaksanakan di Balai Riset Perikanan Budidaya Air Payau (BRPBAP) menggunakan 27 buah akuarium berukuran 40x30x27 cm3 yang diisi tanah tambak setebal 10 cm dan air laut sebanyak 15 L salinitas 28 ppt. Hewan uji yang digunakan berupa benur windu PL25 sebanyak 30 ekor/bak. Penelitian diset dalam Rancangan Acak Lengkap (RAL) dengan 9 perlakuan : (A) BL542; (B) BT951; (C) MY1112; (D) BL542+BT951; (E) BL542+MY1112; (F) BT951+MY1112; (G) BL542+BT951+MY1112; (H) probiotik komersil; (I) kontrol (tanpa probiotik). Masing-masing perlakuan diulang 3 kali dengan lama pemeliharaan 2 bulan. Pengamatan parameter kualitas air dilakukan setiap 2 minggu yang meliputi; BOT, amoniak, nitrit, nitrat, fospat, total bakteri, total Vibrio sp., total Sulfate Reducing Bacteria (SRB), dan Total
Sulfur Oxidazing Bacteria (SOB). Sedangkan pengamatan kelulushidupan udang windu dilakukan pada akhir
penelitian. Hasil penelitian menunjukkan bahwa konsentrasi BOT, amoniak, nitrit, nitrat, fospat, dan H2S mengalami fluktuasi. Kelulushidupan udang windu tertinggi pada perlakuan yang menggunakan bakteri probiotik yang diisolasi dari sedimen tambak, BT951 (perlakuan B) yaitu 68,9%, disusul perlakuan yang menggunakan BL542+BT951+MY1112 (perlakuan G) yaitu 64,5%, dan terendah pada perlakuan yang menggunakan probiotik komersil (perlakuan H) yaitu 37,7%. Hasil analisis statistik menunjukkan bahwa kelulushidupan udang windu pada perlakuan B dan G berbeda nyata (P<0,05) dengan perlakuan H, namun tidak berbeda nyata (P>0,05) dengan perlakuan lainnya.
Pendahuluan
Pencegahan penyakit pada budidaya udang khususnya budidaya udang windu, diarahkan kepada pencegahan penyakit secara biologis, baik melalui penggunaan tandon dan biofilter maupun melalui penggunaan probiotik. Pengelolaan limbah budidaya udang menggunakan tandon dan biofilter, serta sistem resirkulasi air telah dirintis oleh Balai Riset Perikanan Budidaya Air Payau (BRPBAP), Badan Riset Kelautan dan Perikanan, Departemen Kelautan dan Perikanan sejak tahun 1990-an dan sampai sekarang masih terus dikembangkan untuk lebih menyempurnakan metode-metode yang telah ada (Atmomarsono et al. 1995 ; Muliani et al. 1998; Gunarto et al., 2004; Gunarto et al., 2006b). Penggunaan probiotik mulai dikembangkan sejak awal tahun 2000-an. Namun demikian, hasilnya belum sesuai yang diharapkan dan kasus-kasus penyakit di tambak masih terus terjadi. Dengan demikian usaha-usaha untuk menanggulangi penyakit pada budidaya udang harus terus dilakukan, salah satu diantaranya adalah penggunaan probiotik.
Kajian tentang sumber-sumber bakteri probiotik serta pemanfaatannya untuk penanggulangan penyakit pada udang telah banyak dilakukan. Beberapa peneliti dan praktisi budidaya mengisolasi bakteri probiotik dari lingkungan seperti dari laut (Tjahyadi et al., 1994; Haryanti et al., 2000; Muliani et al., 2003; Radjasa et al., 2005; Schulze et al., 2006), air perbenihan (Rosa et al., 1997; Schulze et al., 2006), mangrove (Muliani et
al., 2004), tambak (Vaseeharan and Ramasamy,
2003; Vaseeharan et al., 2004; Lio-Po et al., 2005; Muliani et al., 2006; Vijayan et al., 2006), seabream (Sparus aurata, L.) (Chabrillon et al., 2006), usus ikan ikan lele (Sugita et al., 2007), ikan nila (Aly
et al., 2008a), dan usus ikan (Balcazar et al., 2008).
Penggunaan probiotik pada budidaya udang selain untuk menggantikan peran antibiotik dan obat-obatan untuk mengendalikan patogen juga untuk memperbaiki kualitas air akibat penumpukan bahan organik yang berasal dari sisa pakan dan feses udang. Menurut Verschuere et al. (2000), suatu jenis probiotik yang dapat digunakan untuk penanggulangan penyakit pada usaha budidaya adalah yang dapat berfungsi sebagai biokontrol dan antimikroba.
Beberapa jenis bakteri yang banyak digunakan sebagai probiotik di antaranya
Aeromonas spp. (Lategan et al., 2004), A. hydrophila (Irianto and Austin, 2002), A. sobria
(Brunt et al., 2007), Arthobacter sp. (Li et al., 2006), Bacillus sp (Brunt et al., 2007), B. subtilis (Kumar et al., 2006; Ghosh et al., 2007; Keysami
et al., 2007), B. firmus (Muliani et al., 2006; Aly et al., 2008a), B. pumillus (Aly et al., 2008a,
2008b), Citrobacter freundii (Aly et al., 2008a),
Enterococcus faecium (Wang et al., 2008), Lactobacillus spp. (Balcazar et al., 2008; Suzer et al., 2008), L. lactis (Sugita et al., 2007), Listonella anguillarum (Chabrillon et al., 2006), Pediococcus acidilactici (Catex et al., 2008), Pseudomonas spp. (Vijayan, et al., 2006; Aly et al., 2008a; Clermont et al., 2008), Pseudoalteromonas sp, (Haryanti et al., 2001;
Muliani et al, 2004), Shewanella sp. (Clermont
et al., 2008; Markidis et al., 2008).
Penggunaan bakteri probiotik sudah sangat meluas dihampir semua kegiatan budidaya, termasuk pada budidaya udang, baik udang windu maupun udang vannamei. Tetapi tidak semua pembudidaya udang mendapatkan hasil panen udang yang baik. Hal ini disebabkan karena tidak semua probiotik yang beredar di pasaran cocok untuk diaplikasikan pada lingkungan budidaya udang. Berdasarkan hal tersebut maka telah dilakukan eksploirasi bakteri-bakteri dari lingkungan yang potensial sebagai bakteri probiotik untuk budidaya udang dengan harapan bakteri tersebut akan lebih efektif karena diisolasi dari lingkungan tambak.
Penelitian bertujuan untuk mengetahui kualitas air dan kelulushidupan udang windu (P. monodon) pada penggunaan probiotik yang diisiolasi dari sedimen laut, daun mangrove dan sedimen tambak serta kombinasinya.
Materi dan Metode
Penelitian ini dilaksanakan di Balai Riset Perikanan Budidaya Air Payau (BRPBAP) dalam skala laborotorium menggunakan 27 buah akuarium berukuran 40x30x27 cm3 yang diisi tanah tambak setebal 10 cm dan air laut sebanyak 15 L salinitas 28 ppt. Hewan uji yang digunakan berupa benur windu PL 25 sebanyak 2 ekor/L yang sebelumnya telah dilakukan pengecekan bebas WSSV dengan test PCR. Sedangkan bakteri probiotik yang digunakan diisolasi dari sedimen laut (BL542), sedimen tambak (BT951), dan daun mangrove (MY1112). Untuk mengetahui efektifitas dari
probiotik yang diisolasi dari sedimen laut, sedimen tambak, dan daun mangrove serta kombinasinya maka dibandingkan dengan bakteri probiotik komersil dan kontrol (tanpa probiotik). Penelitian diset dalam Rancangan Acak Lengkap (RAL) dengan perlakuan; (A) BL542; (B) BT951; (C) MY1112; (D) BL542+BT951; (E) BL542+MY1112; (F) BT951+MY1112; (G) BL542+BT951+MY1112; (H) probiotik komersil; (I) kontrol. Masing-masing perlakuan diulang 3 kali. Penelitian dilakukan selama 2 bulan. Pengamatan parameter kualitas air dilakukan setiap 2 minggu yang meliputi (a) parameter kimia yaitu; BOT, amoniak, nitrit, nitrat, fospat dan H2S; (b) parameter biologi yaitu; total bakteri dalam air dan sedimen menggunakan media Triptic Soy Agar (TSA), total Vibrio dalam air dan sedimen menggunakan media Triple Citrate
Bile Sucrose Agar (TCBSA) dan total Sulfat Reducing Bacteria (SRB) menggunakan Battersby’s Media dan Sulfur Oxidazing Bacteria
(SOB) menggunakan SOB Enrichment Media. Sedangkan pengamatan kelulushidupan udang windu dilakukan pada akhir penelitian. Data kelulushidupan udang yang diperoleh dianalisis ragamnya dan dilanjutkan dengan uji Beda Nyata Terkecil (Steel dan Torrie 1981).
Hasil dan Pembahasan
Kualitas Air a. BOT
Konsentrasi BOT selama penelitian disajikan pada Gambar 1. Pada gambar tersebut terlihat bahwa konsentrasi BOT dari awal hingga akhir penelitian mengalami fluktuasi. Hal ini terjadi baik pada perlakuan yang menggunakan probiotik maupun yang tidak menggunakan probiotik (kontrol). Konsentrasi BOT pada awal penelitian (sebelum pemberian bakteri probiotik) tertinggi pada perlakuan D (BL542+BT951) dan terendah pada perlakuan (kontrol). Memasuki minggu kedua, konsentrasi BOT pada beberapa perlakuan mengalami penurunan dan terendah pada perlakuan D (BL542+BT951), sedangkan pada perlakuan G (BL542+BT951+MY1112), H (probiotik komersil) dan I (kontrol) konsentrasi BOT relatif stabil. Pada minggu ke empat, konsentrasi BOT terendah pada perlakuan A (BL542), sementara perlakuan lainnya relatif stabil. Memasuki minggu ke enam, konsentrasi BOT pada semua perlakuan cenderung
meningkat dari minggu keempat, kecuali pada perlakuan C (MY1112) yang menurun. Setelah memasuki minggu ke delapan (minggu terakhir) konsentrasi BOT menurun dan terendah pada perlakuan yang menggunakan A (BL542), sedangkan MY1112 meningkat. Meskipun konsentrasi BOT berfluktuasi namun ada kecenderungan bahwa BOT pada perlakuan yang menggunakan BL542 lebih rendah dibanding pada perlakuan lainnya. Konsentrasi BOT pada penelitian ini sedikit lebih tinggi jika dibanding dengan yang dilaporkan oleh Gunarto et al. (2006a) yaitu pada tambak yang menggunakan probiotik komersial dimana konsentrasi BOT berkisar 7,05–14,8 mg/L, sedangkan yang tidak menggunakan probiotik berkisar 8,4–17,0 mg/L.
b. Amoniak
Seperti halnya dengan konsentrasi BOT, konsentarsi amoniak pada penelitian ini juga berfluktuasi (Gambar 1). Pada awal penelitian konsentrasi amoniak terendah pada perlakuan G (BL542+BT951+MY1112) dan tertinggi pada perlakuan H (probiotik komersil). Pada minggu ke dua konsentarasi amoniak pada semua perlakuan mengalami penurunan. Memasuki minggu ke empat konsentrasi amoniak kembali meningkat dan tertinggi diperlihatkan oleh perlakuan G (BL542+BT951+MY1112) dan terendah oleh perlakuan F (BT951+MY1112). Pada minggu ke enam, konsentrasi amoniak kembali menurun dan terendah pada perlakuan G dan tertinggi pada perlakuan E. Pada akhir penelitian yaitu minggu ke delapan, konsentrasi amoniak kembali mengalami peningkatan pada semua perlakuan, tertinggi pada perlakuan A yaitu 0,0839 mg/L dan terendah diperlihatkan oleh perlakuan F yaitu 0,0536 mg/L. Hal ini menunjukkan bahwa penggunaan kombinasi probiotik BT951+MY1112 relatif lebih bagus menekan konsentarsi amoniak dalam air pemeliharaan udang windu. Konsentrasi amoniak pada penelitian ini jauh lebih rendah dibanding penelitian sebelumnya yang menggunakan rasio bakteri probiotik yang berbeda yaitu antara 0,1770 mg/L pada perlakuan S sampai dengan 0,3393 mg/L pada kontrol (Muliani et al., 2008a) c. Nitrit
Konsentrasi nitrit selama penelitian disajikan pada Gambar 1C. Pada gambar tersebut terlihat
bahwa pada minggu ke dua konsentrasi nitrit pada semua perlakuan mengalami peningkatan yang cukup darastis. Selanjutnya menurun kembali pada minggu ke empat kecuali pada perlakuan kontrol dan terus menurun sampai pada minggu 6. Memasuki minggu ke 8 konsentrasi nitrit sedikit mengalami peningkatan dan pada akhir penelitian tertinggi pada kontrol yaitu 0,1041 mg/L dan terendah pada perlakuan C (MY1112) yaitu 0,0406 mg/L. Muliani et al. (2007), melaporkan bahwa konsentrasi nitrit pada penelitian yang menggunakan probiotik dengan komposisi jenis dan kepadatan
yang berbeda yaitu berkisar antara 0,2933–1,6141 mg/L, sedangkan pada penggunaan probiotik tunggal yaitu berkisar antara 0,2390 mg/L pada perlakuan yang menggunakan probiotik BL542 sampai dengan 0,2670 mg/L pada perlakuan yang menggunakan probiotik BR931 (Muliani et al., 2008b).
d. Nitrat
Lain halnya dengan konsentrasi nitrit, konsentrasi nitrat pada dua minggu pertama relatif stabil (Gambar 1D). Konsentrasi nitrat tertinggi Gambar 1. Konsentarsi BOT (A), NH4-N (B), NO2-N (C), NO3-N (D), dan PO4-P (E) (mg/L) dalam
terjadi pada minggu ke empat yaitu pada perlakuan A (BL542) dan D (BL542+BT951) yaitu masing-masing dan kembali menurun pada minggu ke enam. Pada semua perlakuan konsentrasi nitrat terus menurun sampai akhir penelitian. Konsentrasi nitrat pada akhir penelitian diperlihatkan oleh perlakuan A (BL542) yaitu 0,2277 mg/L dan terendah oleh perlakuan H (probiotik komersil) yaitu 0,0014 mg/L. Konsentrasi nitrat pada penelitian ini jauh lebih rendah dibanding konsentrasi nitrat pada penelitian sebelumnya yang menggunakan probiotik secara tunggal yaitu berkisar antara 1,3006 mg/L pada perlakuan yang menggunakan isolat MY1112 sampai dengan 2,2037 mg/L pada perlakuan yang menggunakan isolat MR55 (Muliani et al., 2008b). e. Fospat
Konsentrasi fospat selama penelitian disajikan pada Gambar 1E. Pada gambar tersebut terlihat bahwa konsentrasi fospat pada semua perlakuan dari awal penelitian hingga memasuki minggu ke enam mengalami peningkatan, namun peningkatan tersebut sangat kecil dan bertahap dari minggu ke minggu. Setelah memasuki minggu ke delapan, konsentrasi fospat mengalami peningkatan yang sangat drastis, hal ini terjadi pada semua perlakuan. Konsentrasi fospat pada akhir penelitian tertinggi pada perlakuan F (BT951+MY1112) dan terendah pada kontrol (tanpa probiotik). Hal yang serupa dilaporkan oleh Muliani et al., (2008b) dimana pada penggunaan probiotik secara tunggal, konsentrasi fospat terendah pada kontrol dan tertinggi pada Konsentrasi fospat pada saat itu tertinggi pada perlakuan yang menggunakan isolat PK446.
Laporan lain mengatakan bahwa konsentrasi fospat pada penelitian yang menggunakan rasio bakteri probiotik yaitu berkisar antara 0,29843 mg/L pada perlakuan O (bakteri laut 104cfu/ml+bakteri mangrove 104 cfu/mL +bakteri tambak 104 cfu/ml) sampai dengan 0,3823 mg/L pada perlakuan M
(bakteri laut 102cfu/mL+bakteri mangrove
102 cfu/mL+bakteri tambak 104 cfu/mL)
(Muliani et al., 2008a). f. H2S
Konsentrasi H2S selama penelitian disajikan pada Tabel 1. pada tabel tersebut terlihat bahwa H2S pada awal penelitian tidak dapat terdeteksi. Memasuki minggu ke dua konsentrasi H2S sedikit meningkat sehingga sudah dapat dideteksi namun konsentrasinya sangat kecil dan hal ini terjadi pada semua perlakuan. Setelah memasuki minggu ke
empat konsentrasi H2S kembali mengalami
penurunan sehingga tidak dapat diteksi, namun setelah memasuki minggu ke enam, konsentrasi H2S kembali mengalami kenaikan sehingga dapat dideteksi. Peningkatan terus terjadi hingga pada minggu ke delapan. Pada saat itu konsentrasi H2S tertinggi terdapat pada perlakuan G (BL542+BT951+MY1112) dan terendah pada perlakuan D (BL542+BT951) (Tabel 1). Pada hasil penelitian sebelumnya konsentrasi H2S terendah pada perlakuan yang menggunakan probiotik BT951 yaitu sekitar 0,0089 mg/L dan tertinggi pada kontrol (tanpa probiotik) yaitu 0,0120 mg/L (Muliani et al. 2008b). Hal ini menunjukkan bahwa penggunaan probiotik dapat menekan konsentrasi H2S dalam air pemeliharaan udang windu.
Tabel 1. Konsentrasi H2S (mg/L) dalam media air pemeliharaan udang windu selama penelitian.
Perlakuan Concentration of H2S (mg/L) Minggu 0 2 4 6 8 A= BL542 ttd <0,0001 ttd <0,0001 0,0252 B= BT951 ttd <0,0001 ttd <0,0001 0,0232 C= MY1112 ttd <0,0001 ttd <0,0001 0,0320 D= BL542+BT951 ttd <0,0001 ttd <0,0001 0,0132 E= BL542+MY1112 ttd <0,0001 ttd <0,0001 0,0267 F= BT951+MY1112 ttd <0,0001 ttd <0,0001 0,0285 G= BL542+BT951+MY1112 ttd <0,0001 ttd <0,0001 0,0376 H= Probiotik Komersil ttd <0,0001 ttd <0,0001 0,0306 = Kontrol/control ttd <0,0001 ttd <0,0001 0,0334 H= Probiotik Komersil ttd <0,0001 ttd <0,0001 0,0306 J= Kontrol/control ttd <0,0001 ttd <0,0001 0,0334
Populasi Bakteri
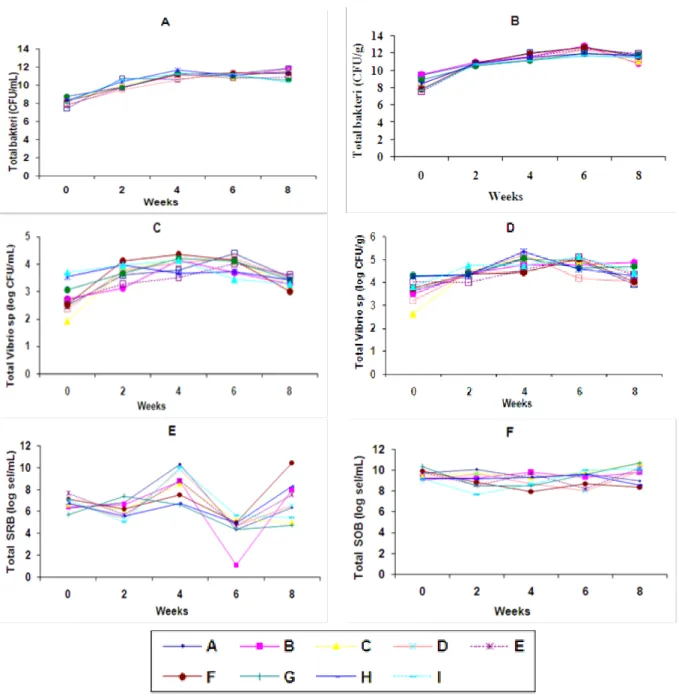
a. Total bakteri dalam air dan sedimen Total bakteri dalam air pemeliharaan udang windu selama penelitian disajikan pada Gambar 2. Pada gambar tersebut terlihat bahwa total bakteri
dalam air dari awal hingga memasuki minggu ke empat cenderung mengalami kenaikan dan relatif stabil hingga akhir penelitian. Pada akhir penelitian total bakteri tertinggi pada perlakuan A (BL542) dan E (BL542+MY1112) yaitu 7,24x1011 CFU/mL dan terendah pada kontrol yaitu 2,24x1010 CFU/mL. Hal ini menunjukkan bahwa probiotik yang diberikan
Gambar 2. (A)Total bakteri dalam air pemeliharan (CFU/mL); (B) Total bakteri dalam sediment (CFU/g); (C) Total Vibrio sp. dalam air (CFU/mL); (D) Total Vibrio sp dalam sedimen (CFU/g); (E) Total SRB dalam sediment (CFU/g) dan (F) Total SOB dalam sediment (CFU/g) selama penelitian
Notes:
A = BL542, B = BT951, C = MY1112, D = BL542+BT951, E = BL542+MY1112 F = BT951+MY1112, G = BL542+BT951+MY1112, H = commercial Probiotic, I = control
mampu tumbuh dan berkembang dalam air pemeliharaan udang windu. Menurut Poernomo (2004) probiotik yang diaplikasikan ke dalam tambak harus mampu hidup di dalam tambak, mampu tumbuh, mampu berkembang biak, dan mampu berfungsi/ bekerja aktif sesuai peranan masing-masing sebagaimana yang diharapkan.
Adapun total bakteri dalam sedimen selama penelitian disajikan pada Gambar 2B. Seperti halnya dengan total bakteri dalam air, total bakteri dalam sedimen juga mengalami peningkatan. Total bakteri dalam sedimen terus meningkat hingga minggu ke enam dan cenderung menurun setelah memasuki minggu ke delapan (akhir penelitian). Pada saat itu total bakteri dalam sedimen tertinggi pada perlakuan E (BL542+MY1112) yaitu sekitar 1,02x1012 CFU/g dan terendah pada perlakuan B (MY1112) yaitu sekitar 5,89x1010 CFU/g.
b. Total Vibrio sp dalam Air dan Sedimen Total Vibrio sp dalam air pemeliharaan udang windu selama penelitian disajikan pada Gambar 2C. Pada gambar tersebut terlihat bahwa total
Vibrio sp. dalam air pemeliharaan udang windu pada
awal penelitian berkisar antara 8,13x101–5,01x103 CFU/mL. Total Vibrio sp. mengalami kenaikan pada minggu ke dua dan relatif stabil hingga minggu ke 6. Memasuki minggu ke delapan (akhir penelitian) total Vibrio sp. dalam air pemeliharaan udang windu kembali mengalami penurunan, namun tentunya tidak lagi serendah pada awal penelitian. Total Vibrio sp. pada akhir penelitian tertinggi pada perlakuan E yaitu 4,07x103 CFU/mL (BL542+MY1112) Hal ini sebagai konsekuensi tingginya total bakteri pada perlakuan tersebut. Sedangkan total Vibrio sp. terendah pada perlakuan F (BT951+MY1112) yaitu 1,0x103 CFU/mL.
Total Vibrio sp. dalam sedimen selama penelitian disajikan pada Gambar 2. Sebagaimana dengan total Vibrio sp. dalam air, total Vibrio sp. dalam sedimen juga mengalami peningkatan jika dibanding pada awal penelitian. Dari gambar 5, terlihat bahwa total Vibrio sp. terus meningkat hingga minggu ke empat, meskipun peningkatan tersebut sangat kecil. Memasuki minggu ke enam, total Vibrio sp. dalam sedimen sedikit mengalami penurunan dan terus menurun hingga minggu ke delapan (akhir penelitian). Pada saat itu total
Vibrio sp. tertinggi pada perlakuan B yaitu
7,76x104 CFU/g dan terendah pada perlakaun A (BL542) yaitu 8,91x103 CFU/g. Berdasarkan hasil skrening sebelumnya isolat BL542 yang merupakan bakteri laut paling bagus menghambat V. harveyi secara in-vitro dalam cawan petri (Muliani et al., 2003).
c. Total SRB dan SOB dalam sedimen
Total bakteri SRB dalam sedimen disajikan pada gambar 2E. Pada gambar tersebut terlihat bahwa total SRB pada semua perlakuan berfluktuasi dari awal hingga akhir penelitian. Pada minggu ke dua konsentrasi SRB relatif mengalami penurunan, Sedangkan dari minggu ke dua ke minggu ke empat konsentrasi SRB mengalami peningkatan. Sebaliknya dari minggu ke empat ke minggu ke enam konsentrasi SRB mengalami penurunan yang cukup drastis terutama pada perlakuan B dari
5,50x108 CFU/g sediman turun menjadi
1,35x101 CFU/g sedimen. Pada minggu ke delapan (akhir penelitian) Konsentrasi SRB kembali meningkat, dan terlihat bahwa konsentrasi SRB tertinggi pada perlakuan F yaitu 2,95x1010 CFU/g sedimen dan terendah pada perlakuan G yaitu 1,78x104 CFU/g sedimen.
Total Bakteri SOB disajikan pada Gambar 2F. Pada gambar tersebut terlihat bahwa total SOB pada beberapa perlakuan relatif stabil dari awal hingga akhir penelitian, meskipun ada beberapa perlakuan yang mengalami penurunan, namun penurunan tersebut sangat kecil. Total SOB pada akhir penelitian tertinggi pada perlakuan C (MY1112) dan G (BL542+BT951+MY1112) yaitu 5,01x1010 CFU/g dan terendah pada perlakuan F (BT951+MY1112) yaitu 2,24x108 CFU/g.
Kelulushidupan Udang Windu
Kelulushidupan udang windu pada akhir penelitian disajikan pada Tabel 2. Pada tabel tersebut terlihat bahwa kelulushidupan udang windu tertinggi pada perlakuan yang menggunakan bakteri probiotik yang diisolasi dari sedimen tambak, BT951 (perlakuan B) yaitu 68,9%, disusul oleh perlakuan kombinasi antara BL542+BT951+MY1112 (perlakuan G) yaitu 64,5%, dan terendah pada perlakuan yang menggunakan probiotik komersil (perlakuan H) yaitu 37,7%. Kelulushidupan udang windu pada penelitian ini sedikit lebih rendah jika dibanding hasil penelitian sebelumnya yang menggunakan probiotik dengan rasio yang berbeda
yaitu 81,3–93,3% (Muliani et al., 2008a). Hasil analisis statistik menunjukkan bahwa kelulushidupan udang windu pada perlakuan B dan G berbeda nyata (P<0,05) dengan perlakuan H, namun tidak berbeda nyata dengan (P>0,05) dengan perlakuan lainnya.
Kesimpulan
Konsentrasi BOT pada perlakuan yang menggunakan BL542 cenderung lebih rendah dibanding pada perlakuan lainnya. Sedangkan parameter kualitas air lainnya masih berfluktuasi, namun beberapa diantaranya mengalami penurunan pada akhir penelitian.
Kelulushidupan udang windu tertinggi pada pada perlakuan B (BT951), disusul oleh perlakuan (BL542+BT951+MY1112) dan keduanya berbeda nyata (P<0,05) dengan kelulushidupan udang windu pada perlakuan H (probiotik komersil), namun tidak berbeda nyata dengan perlakuan lainnya.
Ucapan Terima Kasih
Kepada rekan-rekan peneliti dan teknisi baik yang terlibat langsung maupun tidak, diucapkan terima kasih yang setinggi-tingginya atas terlaksananya penelitian ini. Penelitian ini dibiayai oleh APBN T/A 2007. dengan judul kegiatan “Riset Managemen Kesehatan Ikan dan Lingkungan”, subkegiatan “Pencegahan penyakit udang windu melalui penggunaan bakteri probiotik”
Daftar Pustaka
Aly, M.S., A.M.E. Rahman, G. John and M.F. Mohamed.
2008a. Characterization of some bacteria isolated from Oreochromis niloticus and their potential use as probiotic, Aquaculture, 277: 1–6.
Tabel 2. Kelulushidupan udang windu (%) setelah 2 bulan pemeliharaan.
Aly, M.S., M.F. Mohamed and G. John. 2008b. Effect of
probiotic on the survival, Growth and challenge infection in Tilapia nilotica (Oreochromis
niloticus). Aquaculture Research, 39: 647–656. Atmomarsono, M. Muliani dan S. Ismawati. 1995.
Prospek penggunaan tandon pada Budidaya udang windu. Makalah disajikan pada “Aplikasi Paket Teknologi di Instalasi Penelitian dan Pengkajian Teknologi Pertanian (IPPTP) Wonocolo, Surabaya 2-4 Juli 1995. 10 hlm.
Balcazar, J. L., D. Vendrell, I.D. Blas, I.R. Zarzuela, J.L. Muzquiz and O. Girones. 2008.
Characterization of probiotic properties of lactic acid bacteria isolated from intestinal microbiota of fish. Aquaculture, 278: 188–191.
Brunt, J., A.N. Fyzul and B. Austin. 2007. The
development of probiotics for control of multiple bacteria diseases of rainbow trout, Oncorhynchus
mykiss (Walbaum). Journal of Fish Diseases, 30:
573–579.
Catex, M., L. Chim, D. Pham, P. Lemaire, N. Wabete, J.L. Nicolas, P. Scmidely and C. Mariojouls. 2008.
Probiotic P. acidilactici application in shrimp
Litopenaeus stylorostris culture subject to
vibriosis in new Caledonia. Aquaculture, 275: 182–193.
Chabrillon, M., S. Arijo, P.D. Rosales, M.C. Balebona and M.A. Morinigo. 2006. Interferente of Listonelle anguillarum with potential probiotic
microorganisms isolated from farmed gilthead seabream (Sparus aurata, L.). Aquaculture
Research, 37: 78–86.
Clermont, E.G., T. Wahli, J. Frey and S.E. Burr. 2008.
Identification of bacteria from the normal flora of perch, Perca fluviatilis L., and evaluation of their inhibitory potential towards Aeromonas species.
Journal of Fish Diseases, 31: 353–359.
Ghosh, S., A. Sinha and C. Sahu. 2007. Effect of probiotic
on reproductive performance in female live bearing ornamental fish. Aquaculture Research, 38: 518–526.
Gunarto, Muslimin dan Muliani. 2004. Kualitas air
(NO3-N, PO4-P, NH4-N, BOT) dan total Vibrio sp dalam budidaya udang windu system resirkulasi. hlm: 156–164. Dalam Irianto, A.; Sukardi, P., Budhi, T.P., Sukanto, Rokhmani, Santoso, S. Prosiding Pengendalian Penyakit Pada Ikan dan Udang Berbasis Imunisasi dan Biosecurity. Seminar Nasional penyakit Ikan dan Udang IV. Poerwokerto, 18–19 Mei 2004. Indonesia.
Gunarto, A.M. Tangko, B.R. Tampangallo dan Muliani.
2006a. Budidaya udang windu (Penaeus
monodon) di tambak dengan penambahan
probiotik. Jurnal Riset Akuakultur,
1:303–313. Perlakuan Kelulushidupan (%) A= BL542 45,6ab B= BT951 68,9a C= MY1112 43,4ab D= BL542+BT951 48,9ab E= BL542+MY1112 51,1ab F= BT951+MY1112 46,7ab G= BL542+BT951+MY1112 64,5a H= Probiotik Komersil 37,7b J= Kontrol/control 43,4ab
Gunarto, Muslimin, Muliani dan Sahabuddin. 2006b.
Analisis kejadian serangan White Spot Syndrome Virus (WSSV) dengan beberapa parameter kualitas air pada budidaya udang windu menggunakan sistem tandon dan biofilter. Jurnal
Riset Akuakultur, 1: 255–270.
Haryanti, K. Sugama, S. Tsamura and T. Nishijima.
2000. Vibriostatic bacterium isolated from seawater: Potentiality as probiotic agent in the rearing of Penaeus monodon larvae. Indonesia
Fisheries Resource. Journal, 6: 26–32.
Haryanti, K. Sugama, S. Tsumura and T. Nishijima. 2001.
Enhance production of black tiger shrimp
Penaeus monodon post larvae by Probiotic
bacterium Alteromonas sp. Indonesia Fisheries
Research Journal, 6: 26–32.
Irianto, A. and B. Austin. 2002. Use of probiotics to
control furunculosis in rainbow trout,
Oncorhynchus mykiss (Walbaum). Journal of Fish Diseases, 25: 333–342.
Keysami, M.A., C.R. Saad, K. Sijam, H.M. Daud and A. R. Alimon. 2007. Effect of Bacillus subtilis on
growth development and survival of larvae
Macrobrachium rosenbergii (de Man). Aquaculture Nutrition, 13: 131–136.
Kumar, R., S.C. Mukherjee, K.P. Prasad and A.K. Pai.
2006. Evaluation of Bacillus subtilis as a probiotic to Indian major carp Labeo rohita (Ham.).
Aquaculture Research, 37: 1215–1221.
Lategan, M.J., F.R. Torpy, and L.F. Gibson, 2004. Control
of saprolegniosis in the eel Anguilla australis Richardson, by Aeromonas media strain A199.
Aquaculture, 240: 19–27.
Li, J., B. Tan, K. Mai, Q. Ai, W. Zhang, W. Xu, Z. Liufu and H. Ma. 2006. Comparative study between
probiotic bacterium Arthrobacter XE-7 and chloranphenicol on protection of Penaeus
chinensis post-larvae from pathogenic vibrios. Aquaculture, 253: 140–147.
Lio-Po, G.E., M.D. Leoano, M.M.D. Penaranda, A.U. Villa-Franco, C.D. Sombito and N.G. Guanson. 2005.
Anti-luminous Vibrio factors associated with the ‘green water’ grow-out culture of the tiger shrimp
Penaeus monodon. Aquaculture, 250: 1–7. Makridis, P., S. Martins, J. Reis and M.T. Dinid. 2008.
Use of probiotic bacteria in the rearing of Senegalese sole (Solea senegalensis) larvae.
Aquaculture Research, 39: 627–634.
Muliani, M. Atmomarsono dan M.I. Madeali. 1998.
Pengaruh penggunaan kekerangan sebagai biofilter terhadap kelimpahan dan komposisi jenis bakteri pada budidaya udang windu (Penaeus
monodon) dengan sistem resirkulasi air. Jurnal Penelitian Perikanan Indonesia, 3: 54–61. Muliani, A. Suwanto dan Y. Hala. 2003. Isolasi dan
karakterisasi bakteri asal laut Sulawesi untuk
biokontrol penyakit vibriosis pada larva udang windu (Penaeus monodon Fab.). Hayati, 10: 6–11.
Muliani, Nurbaya, A. Tompo dan M. Atmomarsono. 2004.
Eksplorasi bakteri filosfer dari tanaman mangrove sebagai bakteri probiotik pada budidaya udang windu Penaeus monodon, Jurnal Penelitian
Perikanan Indonesia, 2: 47–57.
Muliani, Nurbaya dan M. Atmomarsono. 2006.
Penapisan bakteri yang diisolasi dari tambak udang sebagai kandidat probiotik pada budidaya udang windu, Penaeus monodon. Jurnal Riset
Aquaculture, 1: 73–85.
Muliani, Nurbaya dan B.R. Tampangallo. 2008a.
Pengaruh rasio bakteri probiotik terhadap perubahan kualitas air dan sintasan udang windu,
Penaeus monodon dalam akuarium. Jurnal Riset Akuakultur, 3: 33–42.
Muliani, Nurbaya dan M. Atmomarsono. 2008b. Uji
performansi bakteri probiotik pada pemeliharaan pascalarva udang windu (Penaeus monodon) dalam bak terkontrol. Makalah telah diseminarkan pada “Gelar teknologi Budidaya” Pusat Riset Perikanan Budidaya. Badan Riset Kelautan dan Perikanan. Departemen Kelautan dan Perikanan di Manado pada tanggal 2–3 Mei 2008.
Poernomo, A. 2004. Technology of probiotics to solve
the problems in shrimp pond culture and the culture environment. Paper presented in the National Symposium on Development and Scientific and Technology Innovation in Aquaculture, Semarang, January 27–29, 2004. 24 pp.
Radjasa, O.K., T. Martens, H.P. Grassart, A. Sabdono, M. Simon and T. Bachtiar. 2005. Antibacterial
property of a coral-associated bacterium
Pseudoalteromonas luteoviolcea against shrimp
pathogenic Vibrio harveyi (in-vitro study).
Hayati, 12: 71–81
Rosa, D., Zafran, I. Tufik dan M.A. Girsang. 1997.
Pengendalian Vibrio harveyi secara biologis pada larva udang windu (Penaeus monodon): I. isolassi bakteri penghambat. Jurnal Penelitian
Perikanan Indonesia, 3: 1–10.
Schulze, A.D., A.O. Alabi, A.R. Tattersal-Sheldrake and K.M. Miller. 2006. Bacterial diversity in a marine
hatchery: Balance between pathogenic and potentially probiotic bacterial strains.
Aquaculture, 256: 50–73.
Sugita, H., K. Ohta, A. Kuruma and T. Sagesaka. 2007.
An antibacterial effect of Lactococcus lactis isolated from the intestinal tract of the amur catfish, Silurus asotus Linnaeus. Aquaculture
Research, 38: 1002–1004.
Suzer, C., D. Coban, H.O. Kamaci, S. Saka and K. Firat.
in gilthead sea bream (Sparus aurata, L.) larvae: Effects on growth performance and digestive enzyme activities. Aquaculture, 280: 140–145
Tjahjadi, M.R., S.L. Angka and A. Suwanto. 1994.
Isolation and evaluation of marine bacteria for biocontrol of luminous bacterial diseases in tiger shrimp larvae (Penaeus monodon Fab.). Aspac.
Journal Molecullar Biology Biotechnology, 2:
347–352.
Vaseeharan, B., J. Lin and P. Ramasamy. 2004. Effect of
probiotics, antibiotic sensitivity, pathogenicity, and plasmid profiles of Listonella anguillarum-like bacteria isolated from Penaeus monodon culture system. Aquaculture, 241: 77–91.
Vaseeharan, B. and P. Ramasamy. 2003. Control of
pathogenic Vibrio spp. by Bacillus subtilis BT23, a possible probiotic treatment for black tiger
shrimp Penaeus monodon. Letter Applied
Microbiology, 37: 443–447. 36: 83–87.
Verschuere, L., G. Rombaut, P. Sogeloos and W. Verstraete. 2000. Probiotic bacteria as biological
control agents in aquaculture. Microbiology
Molecullar Biology Review, 64 (4): 655–671. Vijayan, K.K., I.S.B. Singh, N.S. Jayaprakash, S.V.
Alavandi, S.S. Pai, R. Preeta, J.J.S. Rajan and T.C. Santiago. 2006. A brackish water isolate of Pseudomonas PS-102, a potential antagonistic
bacterium against pathogenic vibrios in penaeid and non-penaeid rearing systems. Aquaculture, 251:192–200.
Wang, Y.B., Z.Q. Tian, J.T. Yao and W.F. Li. 2008. Effect
of probiotics, Enteroccus faecium, on tilapia (Oreochromis niloticus) growth performance and immune response, Aquaculture, 277: 203–207.