1
BAB I PENDAHULUAN
A. Latar Belakang
Indonesia memiliki banyak tanaman dan juga rempah-rempah yang sangat bermanfaat untuk kesehatan tubuh, salah satunya adalah temulawak. Tanaman temulawak (Curcuma xanthorrhiza Roxb.) merupakan salah satu dari sembilan tanaman unggulan yang ditetapkan oleh Badan Pengawasan Obat dan Makanan Republik Indonesia. Pengembangan tanaman temulawak di Indonesia sangat potensial karena produksi rimpang temulawak mengalami peningkatan sejak tahun 2001 - 2002 (BPS, 2003).
Kandungan kimia rimpang temulawak yang dapat dimanfaatkan dalam bidang industri makanan, minuman maupun farmasi adalah pati, kurkuminoid dan minyak atsiri (Sidik dkk., 1995). Kurkuminoid merupakan komponen berwarna kuning, sehingga dapat digunakan sebagai zat warna dalam industri pangan dan kosmetik. Fraksi kurkuminoid yang terdapat pada temulawak terdiri dari dua komponen, yaitu kurkumin dan demetoksikurkumin (Sidik dkk., 1995). Menurut Khanna (1999), kurkumin memiliki khasiat sebagai antioksidan, antiinflamasi, antimikroba, antiparasit, antimutagen, dan antikanker.
Selama ini, permintaan temulawak dari luar negeri cukup tinggi. Namun, temulawak Indonesia ternyata belum bisa diterima pasar luar negeri karena berada di
bawah standar mutu internasional. Oleh karena itu, diperlukan kontrol kualitas terhadap temulawak yang tumbuh di Indonesia. Kontrol kualitas temulawak biasanya dilakukan dengan analisis kuantitatif kurkumin dengan teknik kromatografi cair kinerja tinggi (KCKT) (Jiang dkk., 2006; Jadhav dkk., 2007; Bos dkk., 2007; Lee dkk., 2011). Meskipun demikian, metode KCKT memiliki keterbatasan yaitu perlu waktu yang lama, memerlukan ahli untuk melakukan analisis, dan memerlukan tahap penyiapan sampel yang relatif kompleks (Tanaka dkk., 2008). Keterbatasan lainnya adalah jika sampelnya sangat kompleks, maka resolusi yang baik sulit diperoleh (Munson, 1991). Oleh karena itu, diperlukan metode yang praktis dan efisien.
Dewasa ini, penggunaan spektrofometer Fourier transformed infrared (FTIR) yang dikombinasikan dengan kalibrasi multivariat untuk analisis suatu komponen dalam tumbuhan telah banyak dikembangkan. Spektrofometer FTIR yang dikombinasikan dengan kalibrasi multivariat dapat mengukur sampel secara cepat tanpa merusak dan mampu menganalisis beberapa komponen secara serentak (Rohaeti dkk., 2011). Penggunaan spektrofotometer FTIR dalam analisis tumbuhan masih terbatas karena matriks dan spektrum yang dihasilkan cukup kompleks. Kombinasi dengan kemometrik dapat memperluas potensi spektroskopi FTIR sebagai metode alternatif untuk menganalisis komponen dalam tumbuhan. Metode analisis ini dikembangkan dengan memanfaatkan informasi pola sidik jari yang bersifat khas (Wold dkk., 2001). Kemometrik memanfaatkan ciri serapan IR yang khas dari setiap molekul untuk mengklasifikasi sampel atau untuk membuat model kalibrasi
multivariat (dengan melibatkan data referensi) yang dapat digunakan dalam prediksi hasil pengukuran suatu sampel (Naes dkk., 2002).
Kombinasi spektrum FTIR dengan kalibrasi multivariat telah banyak digunakan diantaranya model klasifikasi asal daerah meniran (Dharmaraj dkk., 2006), penentuan kadar senyawa atau golongan senyawa aktif tumbuhan obat (Rohaeti dkk., 2006), metode deteksi pemalsuan atau diskriminasi bahan baku pangan atau obat herbal (Liu dkk., 2008; Chen dkk., 2009) dan prediksi kapasitas antioksidan total pada minuman anggur (Versari dkk., 2010). Selain itu, kombinasi spektroskopi Near Infrared (NIR) dengan kalibrasi multivariat pernah dilakukan sebelumnya oleh Tanaka dkk. (2008) untuk mengkuantifikasi kurkumin dalam ekstrak metanol kunyit. Pemakaian yang luas tersebut karena teknik ini memberikan hasil yang cukup teliti dan akurat walaupun dengan matriks sampel yang kompleks (Rohaeti dkk., 2011). Namun, analisis kurkumin dalam ekstrak etanolik temulawak menggunakan metode spektrofotometer FTIR yang dikombinasikan dengan kalibrasi multivariat belum pernah dilaporkan. Oleh karena itu, penelitian ini dilakukan untuk mengembangkan metode spektroskopi FTIR yang dikombinasikan dengan kemometrika kalibrasi multivariat untuk analisis kurkumin dalam ekstrak etanolik temulawak.
B. Rumusan Masalah
Berdasarkan uraian latar belakang di atas dapat diambil suatu perumusan masalah yaitu:
1. Apakah metode spektrofotometri FTIR yang dikombinasikan dengan kalibrasi multivariat dapat diterapkan dalam analisis kuantitatif kurkumin dalam ekstrak etanolik temulawak?
2. Bagaimana hubungan antara hasil analisis kuantitatif kurkumin dalam ekstrak etanolik temulawak yang dianalisis dengan KCKT dan spektrofotometri FTIR yang dikombinasikan dengan kalibrasi multivariat (Partial Least Square, PLS)?
C. Pentingnya Penelitian Dilaksanakan
Kontrol kualitas kandungan kurkumin dalam tanaman temulawak penting dilakukan agar dapat memenuhi standar mutu yang dipersyaratkan oleh pasar dalam dan luar negeri.Selain itu, keamanan, dosis, dan efikasi penggunaan ekstrak temulawak dapat dipastikan. Kontrol kualitas ekstrak temulawak yang umum dilakukan adalah melalui penentuan kandungan senyawa aktif kurkumin dalam tanaman. Tentunya hal ini perlu didukung dengan metode analisis kurkumin dalam ekstrak temulawak yang efisien, valid, dan praktis. Spektrofotometri FTIR yang dikombinasikan dengan metode kalibrasi multivariat Partial Least Square (PLS) merupakan teknik yang tidak merusak, valid, cepat, dan membutuhkan sedikit persiapan sampel. Selain itu, spektrofotometri FTIR menawarkan teknik sidik jari yang mana 2 ekstrak etanolik tanaman yang berbeda tidak akan memiliki profil spektra inframerah yang sama sehingga identifikasinya menjadi lebih reliable. Hasil dari penelitian ini dapat dimanfaatkan oleh peneliti lain sebagai dasar acuan untuk
analisis kurkumin dalam ekstrak etanolik temulawak.
D. Tujuan
Penelitian ini secara umum bertujuan untuk menganalisis kurkumin dalam ekstrak etanolik temulawak yang efisien, valid, dan praktis menggunakan spektrofotometer FTIR dikombinasikan dengan Partial Least Square (PLS). Tujuan penelitian ini secara rinci adalah:
1. Melakukan analisis kurkumin dalam ekstrak etanolik temulawak dengan spektrofotometri FTIR yang dikombinasikan dengan kalibrasi multivariat. 2. Mencari hubungan konsentrasi kurkumin dalam ekstrak etanolik temulawak
yang dianalisis dengan KCKT dan dengan metode spektrofotometri FTIR yang dikombinasikan dengan kalibrasi multivariat (Partial Least Square, PLS).
E. Tinjauan Pustaka 1. Temulawak (Curcuma xanthorrhiza Roxb.)
Rimpang induk temulawak (Gambar 1) dapat memiliki 3-4 buah rimpang. Warna kulit rimpang adalah cokelat kemerahan atau kuning tua, sedangkan warna daging rimpang adalah oranye tua atau kuning. Rimpang temulawak terbentuk di dalam tanah pada kedalaman sekitar 16 cm. Tiap rumpun umumnya memiliki 6 buah rimpang tua dan 5 buah rimpang muda (Anonim, 2007; Departemen Kesehatan RI, 2008). Klasifikasi Ilmiah tanaman temulawak adalah sebagai berikut:
Divisi : Spermatophyta Sub Divisi : Angiospermae Kelas : Monocotyledonae Ordo : Zingiberales Keluarga : Zingiberaceae Genus : Curcuma
Spesies : Curcuma xanthorrhiza Roxb. (Rukmana, 1995).
(a) (b)
Gambar 1. Penampakan temulawak yang digunakan untuk penelitian. (a) contoh temulawak yang
digunakan yang berasal dari pasar Bantul, (b) contoh irisan temulawak.
Kandungan rimpang temulawak segar adalah pati (48-59,64%), kurkuminoid (1,6-2,2%) dan minyak atsiri (1,48-1,63%) (Sidik dkk., 1995). Minyak atsiri atau minyak menguap merupakan komponen dalam temulawak yang memberikan bau karakteristik, sedangkan kurkuminoid terdiri dari beberapa zat warna kuning.
Manfaat temulawak terutama diperoleh dari kurkuminoid yang merupakan senyawa aktif dalam rimpang tanaman temulawak. Temulawak dilaporkan memiliki berbagai aktivitas yakni antitumor, antiinflamasi, antioksidan, hepatoprotektif, dan atibakteri. Aktivitas tersebut disebabkan komponen aktif temulawak berupa kurkuminoid dan xanthorrizol (Hwang, 2006).
2. Kurkumin
Kurkumin [1,7-bis(4'-hidroksi-3'-metoksifenil)-1,6-heptadien-3,5-dion] merupakan salah satukomponen kurkuminoid yang terdapat pada rimpang tanaman
Curcuma sp. (Tonnesen, 1989; Masuda dkk., 1992; Masuda dkk., 1993). Dua komponen kurkuminoid lainnya adalah demetoksikurkumin dan
bis-demetoksikurkumin. Kurkuminoid merupakan polifenol yang bertanggung jawab pada warna kuning Curcuma xanthorrhiza Roxb. . Rumus molekul dan berat molekul kurkumin berturut-turut adalah C21H2006 dan 368,67. Kurkumin bersifat semipolar yang relatif tidak larut dalam air, tetapi larut dalam pelarut organik seperti aseton, dimetilsulfoksida dan etanol. Studi kinetika peruraian kurkumin pada pH 1-11 oleh Tonnesen dan Karlsen (1985) menunjukkan bahwa kurkumin dalam larutan air mengalami degradasi melalui reaksi hidrolisis. Pada pH < 1, kurkumin terprotonasi sehingga berwarna merah. Pada pH 1-7, kurkumin dalam bentuk netral yang berwarna kuning dan memiliki kelarutan dalam air yang sangat rendah; dan pada pH > 7,5, kurkumin berwarna oranye hingga merah, dan sangat tidak stabil. Kecepatan
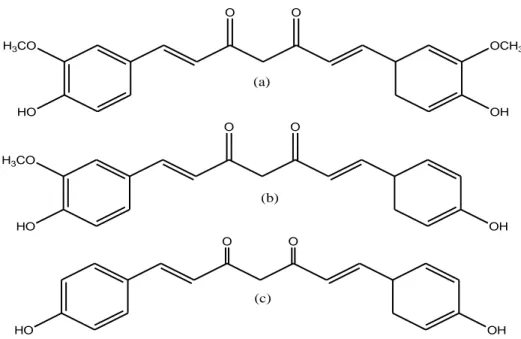
degradasi pada pH 7 lebih lambat dibanding pada pH > 7. Bentuk kristal kurkumin berupa batang atau prisma, dengan titik leleh 183-185ºC. Struktur senyawa komponen kurkuminoid sebagaimana dalam Gambar 2.
H3CO HO OH OCH3 O O H3CO HO OH O O HO OH O O (a) (b) (c)
Gambar 2.Struktur kimia (a) kurkumin, (b) demetoksikurkumin, dan (c) bis
-demetoksikurkumin (Gambar diadopsi dari Hwang, 2006).
Kurkumin merupakan senyawa yang berperan sebagai antioksidan untuk mengurangi dampak negatif radikal bebas (Sugiharto, 2007). Kurkumin dapat berperan sebagai antioksidan karena mengandung gugus -OH fenolik. Priyadarsini dkk. (2003) menyatakan bahwa gugus -OH dari senyawa fenolik sangat potensial beraktivitas sebagai antioksidan. Efek farmakologis lainnya adalah sebagai antitumor, antiinflamasi, dan hepatoprotektif (Hwang, 2006).
Beberapa peneliti telah melaporkan analisis kuantitatif kurkuminoid dengan berbagai metode analisis. Salah satu metode penentuan kurkuminoid atau produk berbasis kurkumin adalah dengan spektrofotometri UV-Vis (Jayaprakasha dkk., 2005; Pothitirat dan Gritsanapan, 2006). Meskipun demikian, kehadiran senyawa lain dalam ekstrak temulawak yang dapat menyerap pada panjang gelombang yang sama dengan panjang gelombang kurkuminoid akan mempengaruhi akurasi hasil (Jayaprakhasa dkk., 2005). Prosedur analisis sederhana menggunakan Flow Injection Analysis (FIA) juga dilakukan untuk pengukuran kurkumin (Thongcai dkk., 2009; Inoue dkk., 2001).
Metode berbasis kromatografi adalah teknik analisis yang umum untuk analisis kuantitatif dan kualitatif kurkuminoid seperti kromatografi lapis tipis (Anderson dkk., 2000; Forgacs dan Cserhati, 2002; Zhang dkk., 2008), KCKT (Sun dkk., 2005; Ruslay dkk.,2007; Jiang dkk., 2006; Jadhav dkk., 2007; Bos dkk., 2007; Lee dkk., 2011), dan kromatografi gas (Almeida dkk., 2005; Zhang dkk., 2008; Anderson dkk., 2000). Rendahnya volatilitas dan sifatnya yang labil pada pemanasan, menjadikan kurkuminoid kurang populer ditetapkan menggunakan kromatografi gas. Elektoforesis kapiler adalah alat pemisahan yang kuat, yang berkembang pesat dan banyak diterapkan untuk analisis produk farmasi, dan komponen bioaktif tumbuhan. Beberapa faktor, yaitu persiapan sampel, kapasitas pemisahan, dan tingkat deteksi harus diperhitungkan ketika elektroforesis digunakan untuk analisis kurkuminoid (Li dkk., 2006). Analisis kurkuminoid dalam makanan dan produk farmasi sangat
penting, karena itu diperlukan metode yang cepat, handal, murah dan tidak merusak sampel seperti spektrofotometri inframerah.
3. Ekstraksi
Ekstraksi atau penyarian adalah peristiwa pemindahan zat aktif yang semula di dalam sel akan ditarik oleh cairan penyari, sehingga zat aktif berada di dalam cairan penyari. Penyarian ini menghasilkan suatu ekstrak. Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat aktif dari simplisia nabati atau simplisia hewani menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan (Departemen Kesehatan RI, 1995). Metode penyarian yang digunakan tergantung wujud dan kandungan zat dalam bahan yang akan disari.
Proses ekstraksi dipengaruhi oleh derajat kehalusan serbuk dan perbedaan konsentrasi, mulai dari pusat butir serbuk simplisia sampai ke permukaannya. Semakin besar perbedaan konsentrasi, semakin besar daya dorong tersebut sehingga mempercepat penyarian. Cairan penyari harus dapat mencapai seluruh serbuk dan secara terus-menerus mendesak ke luar larutan yang memiliki konsentrasi yang lebih tinggi (Departemen Kesehatan RI, 1986).
Metode ekstraksi tergantung pada polaritas senyawa yang diekstraksi. Suatu senyawa menunjukkan kelarutan yang berbeda-beda dalam pelarut yang berbeda. Hal-hal yang perlu diperhatikan dalam pemilihan pelarut adalah murah dan mudah diperoleh, stabil secara fisika dan kimia, bereaksi netral, dan tidak mudah terbakar,
selektif yaitu hanya menarik zat berkhasiat yang dikehendaki, tidak mempengaruhi zat berkhasiat dan diperbolehkan oleh peraturan yang berlaku (Departemen Kesehatan RI, 1986). Ada beberapa metode ekstraksi yang sering digunakan yaitu maserasi, perkolasi, dan soxhletasi.
Maserasi adalah proses ekstraksi simplisia dengan menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur ruangan. Teknik ini dilakukan untuk mengekstrak jaringan tanaman yang belum diketahui kandungan senyawanya yang mungkin bersifat tidak tahan panas (Harbone, 1987). Remaserasi berarti dilakukan pengulangan penambahan pelarut setelah dilakukan penyaringan maserat pertama, dan seterusnya.
Maserasi merupakan cara penyarian yang sederhana. Maserasi dilakukan dengan cara merendam serbuk simplisia dalam cairan penyari. Cairan penyari akan menembus dinding sel dan masuk ke dalam rongga sel yang mengandung zat aktif, dan zat aktif akan larut. Karena adanya perbedaan konsentrasi antara larutan zat aktif di dalam dan di luar sel, maka larutan yang konsentrasinya tinggi akan terdesak keluar. Peristiwa tersebut berulang hingga terjadi keseimbangan konsentrasi di dalam dan di luar sel (Departemen Kesehatan RI, 1986).
Pada penyarian dengan cara maserasi dilakukan pengadukan yang bertujuan untuk meratakan konsentrasi larutan di luar butir serbuk simplisia. Selain itu, dengan pengadukan akan terjaga perbedaan konsentrasi yang sekecil-kecilnya antara larutan di dalam sel dengan larutan di luar sel. Hasil penyarian dengan cara maserasi perlu
dibiarkan dalam selang waktu tertentu. Waktu tersebut diperlukan untuk mengendapkan zat-zat yang tidak diperlukan tetapi ikut terlarut dalam cairan penyari (Departemen Kesehatan RI,2000).
Keuntungan cara penyarian dengan maserasi adalah cara pengerjaan dan peralatan yang digunakan sederhana dan mudah diusahakan. Sementara kerugiannya adalah pengerjaan lama dan penyariannya kurang sempurna (Departemen Kesehatan RI, 2000).
Proses ekstraksi dengan metode maserasi dikombinasikan dengan alat
vaccum rotary evaporator yang bertujuan untuk mendapat hasil pemisahan yang maksimal. Vaccum rotary evaporator merupakan alat yang dirancang untuk memindahkan pelarut yang mudah menguap dalam jumlah yang besar dari larutan pada penurunan tekanan, meninggalkan komponen yang tidak mudah menguap. Perbedaan utama pekerjaan ini dengan kerja distilasi adalah dilakukannya pemutaran labu distilasi selama pemindahan pelarut. Pemutaran memiliki fungsi penting yakni dapat menghindari resiko bumping dan meningkatkan kecepatan pemindahan pelarut (Firdaus, 2011).
4. Spektrofotometer Fourier Transform Infrared (FTIR)
Radiasi inframerah (Infrared, IR) tidak memiliki cukup energi untuk menyebabkan transisi elektronik. Bila radiasi IR dilewatkan melalui suatu cuplikan, maka molekul akan menyerap energi sehingga terjadi vibrasi (Hendayana dkk.,
1994). Panjang gelombang serapan oleh suatu ikatan bergantung pada jenis getaran ikatan antar atom. Oleh karena itu, tipe ikatan yang berlainan akan menyerap radiasi IR pada panjang gelombang yang berbeda (Fessenden dan Fessenden, 1986).
Spektrum inframerah kurkumin terdiri dari gugus fungsional alkena, karbonil, alkana, benzena dan hidroksi. Kesamaan serapan alkena terhadap serapan aromatik menyebabkan sukar untuk mendeteksi gugus alkena dalam molekul aromatik. Puncak sedang hingga kuat di daerah 1650-1450 cm-1 sering diinterpretasikan sebagai cincin aromatik. Kenampakan yang paling umum dari serapan C-H ulur (alkana) adalah munculnya dua pita kuat di sebelah kanan 3000 cm-1 dan C-H tekuk di sekitar 1390 cm-1. Gugus karbonil (C=O) memberi puncak kuat di daerah 1820-1600 cm-1 (Sastrohamidjojo, 2007).
Molekul-molekul hanya akan menyerap sinar inframerah pada frekuensi tertentu jika di dalam molekul ada transisi tenaga sebesar ΔΕ=hυ. Transisi yang terjadi di dalam molekul berkaitan dengan perubahan-perubahan vibrasi di dalam molekul. Sebagai contoh, pita kuat di daerah 1700 cm-1 mempunyai frekuensi yang sama dengan ikatan C=O yang mengalami vibrasi ulur. Ikatan-ikatan yang berbeda (C-C, C=C, C≡C, C-O, C=O, O-H, N-H dsb.) mempunyai frekuensi vibrasi yang berbeda dan kita dapat mendeteksi adanya ikatan-ikatan tersebut dalam molekul organik dengan mengidentifikasi frekuensi-frekuensi karakteristiknya sebagai pita serapan dalam spektrum inframerah (Sastrohamidjojo, 2007).
Kedudukan pita serapan dapat dinyatakan dalam satuan frekuensi υ (det-1 atau Hz), atau panjang gelombang λ (mikrometer μm) atau bilangan gelombang (cm-1). Sebagian besar kimiawan menggunakan bilangan gelombang (cm-1), dan sedikit menggunakan panjang gelombang (μm) (Sastrohamidjojo, 2007). Penggunaan spektroskopi inframerah pada bidang kimia organik menggunakan daerah dari 650 – 4000 cm-1. Daerah inframerah dibagi menjadi tiga sub daerah, yaitu inframerah dekat (14000-4000 cm-1), inframerah sedang (4000-400 cm-1), dan inframerah jauh (400 - 40 cm-1) (Griffiths dan Chalmers, 1999). Umumnya analisis senyawa dilakukan pada daerah IR sedang (Tanaka dkk., 2008). Masing-masing daerah tersebut lebih jauh dan lebih dekat dengan spektrum tampak. Inframerah jauh, mengandung sedikit serapan yang bermanfaat bagi kimiawan organik.
Terdapat dua macam vibrasi, yaitu vibrasi ulur dan tekuk. Vibrasi ulur merupakan suatu gerakan berirama di sepanjang sumbu ikatan sehingga jarak antar atom akan bertambah atau berkurang. Vibrasi tekuk dapat terjadi karena perubahan sudut-sudut ikatan antara ikatan-ikatan pada sebuah molekul (Silverstein dan Bassler, 1998). Vibrasi dua atom yang dihubungkan secara ikatan kimia dapat disamakan dengan vibrasi dua bola yang dihubungkan dengan pegas. Dengan menggunakan analogi ini, kita dapat menerangkan sejumlah gambar dari spektra inframerah. Sebagai contoh untuk merentangkan pegas kita membutuhkan tenaga yang lebih besar daripada untuk menekuknya, dan serapan rentangan/ulur dari suatu ikatan
muncul pada frekuensi yang lebih tinggi dalam spektrum inframerah daripada serapan tekuk dari ikatan yang sama (Sastrohamidjojo, 2007).
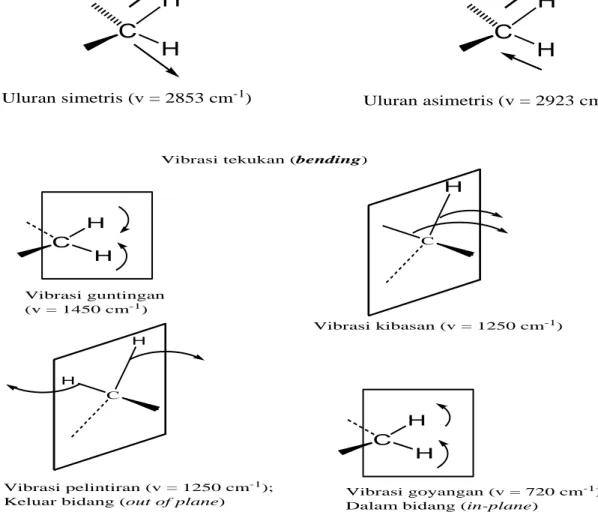
Secara umum, vibrasi uluran asimetrik terjadi pada bilangan gelombang yang lebih tinggi dibanding vibrasi uluran simetrik; demikian juga, vibrasi uluran juga terjadi pada bilangan gelombang yang lebih tinggi dibanding vibrasi tekukan. Vibrasi tekuk sendiri terdiri dari 4 macam yakni guntingan, ayunan, kibasan dan pelintiran. Istilah tersebut digunakan dalam pustaka untuk merujuk bilangan gelombang yang merupakan asal pita inframerah (Pavia dkk., 2009). Gambar 3 menunjukkan bahwa gugus metilen tunggal memberikan sejumlah ragam vibrasi, dan setiap atom yang dihubungkan dengan dua atom lain akan mengalami vibrasi, ketika terjadi perbedaan momen dipol.
Vibrasi uluran (stretching)
Uluran simetris (v = 2853 cm-1) Uluran asimetris (v = 2923 cm-1)
C H
H C
H
H
Vibrasi tekukan (bending)
Vibrasi guntingan (v = 1450 cm-1)
Vibrasi kibasan (v = 1250 cm-1)
Vibrasi goyangan (v = 720 cm-1);
Dalam bidang (in-plane) Vibrasi pelintiran (v = 1250 cm-1);
Keluar bidang (out of plane)
C H H C H H C H C H H
Gambar 3. Berbagai jenis vibrasi untuk gugus metilen (Gambar diadopsi dari Pavia dkk., 2009).
Bagian pokok spektrofotometer inframerah adalah sumber cahaya inframerah, monokromator dan detektor. Cahaya dari sumber dilewatkan melalui sampel, dipecah menjadi frekuensi-frekuensi individunya dalam monokromator, dan intensitas relatif dari frekuensi individu diukur oleh detektor (Sastrohamidjojo, 2007).
Spektra inframerah mempunyai karakteristik yang unik untuk setiap molekul, maka dalam spektrum IR diperoleh pita-pita serapan yang karakteristik juga. Bentuk pita ini dikenal sebagai “finger print” dari suatu molekul. Daerah yang mengandung sejumlah besar vibrasi tertentu yang tak pernah ditelaah yang berkisar di frekuensi 1400 - 900 cm-1 sering disebut daerah finger print (Sastrohamidjojo, 2007).
Spektroskopi FTIR dapat digunakan untuk analisis kualitatif maupun kuantitatif.
a) Analisis Kualitatif
Analisis kualitatif dengan spektroskopi FTIR secara umum digunakan untuk identifikasi gugus-gugus fungsional yang terdapat dalam suatu senyawa yang dianalisis (Silverstein dan Bassler, 1998).
b) Analisis Kuantitatif
Analisis kuantitatif dengan spektroskopi FTIR secara umum digunakan untuk menentukan konsentrasi analit dalam sampel. Dalam penentuan analisis kuantitatif dengan Inframerah digunakan hukum Lambert Beer’s. Hukum Lambert Beer’s dinyatakan sebagai berikut:
A= ε b c
Yang mana A merupakan absorbansi, ε untuk absorptivitas, b untuk tebal tempat sampel dan c untuk konsentrasi sampel. Jika c dinyatakan dalam mol/liter atau Molar (M) maka ε dinyatakan sebagai absortivitas molar. Bila absorbansi A dihubungkan terhadap konsentrasi c untuk sampel yang tebalnya b dalam cm, maka
akan dihasilkan suatu garis lurus (linier) dengan lereng AB dalam daerah yang mana hukum Lambert Beer’s berlaku (Pescok dkk., 1976; Skoog & West, 1971). Oleh karena itu, hanya spektra berbentuk absorbansi yang dapat digunakan untuk analisis kuantitatif. Kurvanya bisa dilihat pada Gambar 4.
Gambar 4. Kurva hubungan absorbansi terhadap konsentrasi (Gambar diadopsi dari Pecsok dkk.,
1976).
Aplikasi spektofotometer FTIR untuk analisis inframerah kuantitatif secara konvensional telah dilakukan sejak tahun 1966 oleh Hans venning. Peneliti ini melakukan kuantifikasi meta- dan para-xilena secara kuantitatif dengan spektroskopi inframerah menggunakan orto-xilena sebagai standar internal dan sikloheksana sebagai pelarut. Stuart (2004) juga menganalisis aspirin yang dilarutkan dalan kloroform. Spektroskopi inframerah dalam analisis kuantitatif mempunyai keterbatasan yang tidak dapat diabaikan yaitu tidak adanya hubungan antara hukum
Lambert Beer’s dengan kompleksitas spektrum sehingga tumpang-tindihnya puncak-puncak tidak dapat diukur (Pescok dkk., 1976).
Saat ini, analisis kuantitatif dengan metode spektroskopi FTIR yang dikombinasikan dengan kemometrika metode kalibrasi multivariat sudah banyak dikembangkan karena penggunaannya yang lebih efisien dan cepat. Aplikasi untuk menganalisis kuantitatif kurkumin dalam ekstrak metanolik kunyit telah dilakukan oleh Tanaka dkk. (2008) dengan menggunakan spektroskopi Near-infrared (NIR) yang dikombinasikan dengan kalibrasi multivariat (Partial Least Square, PLS). Selain itu, spektroskopi FTIR dihubungkan dengan kalibrasi multivariat telah digunakan untuk mendeteksi adanya minyak sawit dalam VCO (Rohman dan Che Man, 2011), untuk mendeteksi adanya lemak babi dalam berbagai minyak nabati (Rohman dkk., 2011b) dan untuk mendeteksi minyak dedak padi dalam minyak zaitun ( Rohman dan Che Man, 2012).
Dua variasi instrumental dari spektrameter inframerah adalah metode dispersif dan metode Fourier Transform. Berbeda dari spektrometer dispersif, spektrofotometer FTIR tidak mengukur panjang gelombang satu demi satu, melainkan dapat mengukur intensitas pada berbagai panjang gelombang secara serempak (Skoog dan West, 1971). Pada spektrofotomete FTIR digunakan suatu interferometer sebagai pengganti monokromator. Interferometer ini akan memberikan sinyal ke detektor sesuai dengan intensitas frekuensi vibrasi molekul yang berupa interferogram (Bassler, 1996). Interferogram merupakan plot dari intensitas versus
waktu. Plot ini diganti dengan plot intensitas versus bilangan gelombang. Suau operasi matematika yang disebut Fourier Transform dapat digunakan untuk memisahkan suatu frekuensi absorbsi dari interferogram sehingga membentuk pita yang dapat diartikan seperti pita hasil spektrofotometer IR (Stuart, 2004).
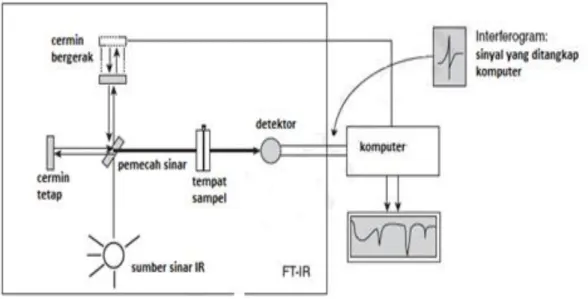
Sistem optik spektrofotometer FTIR seperti dalam Gambar 4, yang dilengkapi dengan cermin yang bergerak tegak lurus dan cermin yang diam. Radiasi inframerah akan menimbulkan perbedaan jarak yang ditempuh menuju cermin yang bergerak dan jarak menuju cermin yang diam. Perbedaan jarak tempuh radiasi disebut sebagai retardasi (δ). Hubungan antara intensitas radiasi IR yang diterima detektor terhadap retardasi disebut sebagai interferogram, sedangkan sistem optik dari spektrofotometer IR yang didasarkan atas bekerjanya interferometer disebut sebagai sistem optik Fourier Transform InfraRed (Pavia dkk., 2001).
Gambar 5. Komponen spektrofotometer FTIR secara skematik (Gambar diadopsi dari Pavia dkk.,
Salah satu teknik penanganan sampel yang umum dilakukan pada spektroskopi FTIR adalah dengan teknik Attenuated Total Reflection (ATR). Teknik ATR hanya membutuhkan sedikit preparasi sampel atau bahkan tidak ada preparasi sama sekali. ATR menggunakan aksesoris dalam kompartemen sampel spektrofotometer FTIR. Cermin pada aksesoris membawa sinar IR pada suatu fokus di permukaan kristal. Jika kristal mempunyai indeks bias yang sesuai dan sinar mempunyai sudut datang yang sesuai, maka akan terjadi pemantulan internal total. Energi IR akan memantul pada permukaan kristal (Stuart, 2004).
5. Kromatografi Cair Kinerja Tinggi (KCKT)
Kromatografi merupakan salah satu metode pemisahan komponen-komponen campuran dalam keadaan kesetimbangan diantara dua fase, yaitu fase diam yang dapat menahan sampel dan fase gerak yang dapat membawa sampel. Kromatografi berdasarkan fase geraknya dapat dibedakan menjadi dua, yaitu kromatografi gas dan kromatografi cair (Day dan Underwood, 2002). Fase diam berguna untuk menjerap komponen zat, sedangkan fase bergerak berguna untuk mengangkut komponen zat lain yang tidak terikat. Oleh karena adanya sistem pengangkutan dan sistem pengikatan ini, maka suatu komponen zat dapat dipisahkan dari komponen lainnya. Metode berbasis kromatografi adalah teknik analisis dalam analisis kimia yang telah sesuai untuk penentuan secara kualitatif dan kuantitatif sejumlah besar sampel (Gritter dkk., 1991).
Menurut Harborne (1987), terdapat empat macam teknik kromatografi, yaitu kromatografi kertas (KKt), kromatografi lapis tipis (KLT), kromatografi gas cair, dan kromatografi cair kinerja tinggi (KCKT). Metode pemisahan dan pemurnian kandungan tumbuhan terutama dilakukan dengan menggunakan salah satu dari empat teknik atau gabungan teknik tersebut.
KLT dan KKt serupa dalam hal fase diamnya yang berupa lapisan tipis dan fase geraknya mengalir karena kerja kapiler. Perbedaan keduanya dalam sifat dan fungsi fase diam (Gritter dkk., 1991). KKt dapat digunakan terutama bagi kandungan tumbuhan yang mudah larut dalam air (karbohidrat, asam amino, dan senyawa fenolat). KLT dapat digunakan untuk tujuan preparatif dan kuantitatif (Rasmussen dkk., 2000). KCKT adalah metode pilihan untuk analisis kurkuminoid dikaitkan dengan presisi dan akurasi yang tinggi dan mempunyai batas deteksi yang rendah.
KCKT merupakan salah satu contoh kromatografi cair yang menggunakan zat cair sebagai fase gerak. Selain untuk pemisahan, metode ini juga dapat digunakan untuk analisis kualitatif dan kuantitatif. Instrumen dasar KCKT terdiri dari pompa, sistem pemasukan sampel, kolom, detektor, dan rekorder atau pencatat (Hendayana dkk., 1994).
KCKT merupakan sistem pemisahan dengan kecepatan dan efisiensi yang tinggi. Hal ini karena didukung oleh kemajuan dalam teknologi kolom, sistem pompa tekanan tinggi, dan detektor yang sangat sensitif dan beragam. KCKT mampu
menganalisis berbagai sampel secara kualitatif maupun kuantitatif, baik dalam komponen tunggal maupun campuran (Direktorat Jenderal POM, 1995).
KCKT dapat disamakan dengan Kromatografi Gas Cair dalam hal kepekaan dan kemampuan menghasilkan data kualitatif dan kuantitatif dengan sekali kerja saja. Perbedaannya adalah fase diam dalam KCKT terikat pada polimer berpori yang terdapat pada kolom baja tahan karat yang bergaris tengah kecil dan fase gerak cair mengalir akibat tekanan yang besar (Harbone, 1987). Fase gerak atau eluen biasanya terdiri atas campuran pelarut yang dapat bercampur yang secara keseluruhan berperan dalam daya elusi dan resolusi. Daya elusi dan resolusi ini ditentukan oleh polaritas keseluruhan pelarut, polaritas fase diam, dan sifat komponen-komponen sampel (Johnson dan Stevenson, 1991).
Komponen yang terelusi mengalir ke detektor dan dicatat sebagai puncak-puncak yang secara keseluruhan disebut sebagai kromatogram. Kromatogram dapat digunakan untuk tujuan kualitatif dan kuantitatif. Disamping itu, kromatogram dapat digunakan untuk mengevaluasi efisiensi pemisahan dan kinerja kolom.Pelarut yang akan digunakan harus dihilangkan gelembung udaranya (degassing), karena udara yang terlarut akan keluar melewati detektor yang dapat menghasilkan banyak noise
sehingga data tidak dapat digunakan (Putra, 2007).
KCKT adalah metode yang paling banyak digunakan untuk analisis kurkuminoid karena fleksibilitas dan kemudahan dalam penggunaanya. Aplikasi KCKT untuk penetapan kurkuminoid oleh He dkk. (1998) menunjukkan bahwa
kurkuminoid danseskuiterpenoid dalam kunyit dapat dianalisis dengan KCKT spektrometri massa. Jiang dkk. (2006) menyatakan bahwa metode KCKT dengan
Photodiode Array Detector (PAD) dapat digunakan untuk identifikasi secara langsung kurkuminoid dalam serbuk kunyit. Bos dkk. (2007) melaporkan penggunaan metode KCKT-PAD untuk analisis kurkuminoid dalam berbagai spesies asli Curcuma dan digunakan untuk pengobatan di Indonesia, dengan menggunakan campuran fase gerak metanol, asam trifluoroasetat, dan asetonitril.
KCKT digabungkan dengan detektor UV-Vis adalah metode analisis kurkuminoid dalam sampel kunyit yang paling umum digunakan. Tonnesen dan Karlsen (1983), pertama melaporkan metode ini untuk analisis kurkumin dan komponen lain dalam kunyit, serta Smith dan Withowska (1984) membandingkan detektor UV dan detektor elektrokimia yang digabung dengan KCKT untuk analisis kurkumin dalam serbuk kunyit. Rouseff (1988) meningkatkan pemisahan kurkuminoid pada kolom oktadesilsilana (C18) dengan menggunakan teknik gradien (air dan tetrahidrofuran) selama 22 menit. Jayaprakasha dkk. (2002) melaporkan pengembangan metode KCKT-UV untuk analisis kurkuminoid dengan teknik elusi gradien pada campuran fase gerak metanol, asam asetat, dan asetonitril selama 20 menit. Meskipun demikian, teknik KCKT ini memerlukan biaya yang mahal karena menggunakan banyak bahan kimia dan alat yang canggih.
6. Kemometrika
Istilah kemometrika pertama kali diperkenalkan oleh ilmuwan berkebangsaan Swedia yaitu Swante Wold dan ilmuwan berkebangsaan Amerika Serikat yaitu Bruce R. Kowalski. Definisi kemometrika adalah cabang ilmu kimia yang memanfaatkan metode-metode matematika dan statistika. Kemometrika digunakan untuk merancang atau memilih prosedur pengujian dan pengukuran yang optimal. Selain itu, kemometrika digunakan untuk menarik informasi kimia sebanyak-banyaknya dengan menganalisis suatu data (Otto, 2007).
Menurut Miller dan Miller (2010), kemometrika merupakan cabang ilmu pengetahuan yang mengaplikasikan ilmu statistika dan matematika untuk mengolah data kimia. Keuntungan kemometrika yang dikombinasikan spektroskopi FTIR adalah penggunaannya yang cepat dan efisien karena menggunakan komputer modern dan teknik statistik yang valid (Lee, 2006). Selain itu, dimungkinkan adanya pengukuran data multivariat, yang mana beberapa variabel (absorbansi dalam banyak bilangan gelombang) diukur untuk suatu sampel yang dituju (Miller dan Miller, 2010).
Kemometrika banyak berhubungan dengan pengukuran data multivariat (Adams, 2004). Banyak contoh penggunaan pengukuran data multivariat dalam kimia analisis. Pertama untuk analisis korelasi, seperti penentuan adanya keterkaitan antara spektrum FTIR ekstrak dan aktivitasnya. Kedua untuk mengelompokkan data, contohnya mengelompokkan tanaman dari berbagai daerah yang memilki aktivitas
sama dengan cara membandingkan data serapan inframerah pada daerah sidik jari (Darusman dkk., 2007). Keuntungan pengukuran data multivariat adalah dapat mengurangi noise akibat mempertimbangkan banyak variabel secara bersamaan. Selain itu, dengan pengukuran data multivariat dapat dideteksi adanya sampel palsu. Hal ini dapat dilakukan karena bentuk profil yang diukur mencerminkan profil yang sebenarnya. Jika sampel merupakan komponen yang berbeda, maka akan tampak bila sampelpalsu (Bro, 2003).
Ada 3 jenis kemometrika yaitu 1) Kemometrika yang terkait dengan teknik pemrosesan spektra; 2) Kemometrika untuk pengelompokkan; dan 3) Kemometrika dengan metode kalibrasi multivariat (Moros dkk., 2010). Metode kalibrasi multivariat yang sering digunakan dalam mengolah data kimia yaitu regresi komponen utama (Principle Component Regression/PCR) dan regresi kuadrat terkecil sebagian (Partial Least Square/PLS) yang digunakan untuk menghubungkan antara spektrum FTIR dengan sifat sampel yang dapat dikuantifikasi, misalnya konsentrasi analit. Konsentrasi analit berada pada variabel respon, dan absorbansi pada bilangan gelombang yang berbeda berada pada variabel prediksi (Miller dan Miller, 2010).
a) Principle Component Regression (PCR)
Principle Component Regression atau yang biasa disebut PCR merupakan salah satu metode yang digunakan untuk mengatasi masalah multivariat kolinieritas yang sering muncul dalam analisis multivariat (Myers, 1990). PCR berfungsi sebagai teknik pengurangan jumlah data multivariat ketika muncul korelasi antar
data/variabel. Teknik kalibrasi multivariat ini diawali dengan PCA kemudian dilanjutkan dengan regresi antara komponen utama yang baru dengan respon (Nawa, 2012). Ketika variabel prediksi tidak saling berhubungan, maka teknik ini tidak berguna. Variabel yang dikurangi dalam hal ini adalah variabel prediksi dengan menggunakan komponen utama (principle component, PC) yang berasal dari metode pengelompokkan Principal component analysis (PCA) dibandingkan dengan variabel aslinya. Keuntungan dari jenis regresi ini adalah berkurangnya jumlah variabel prediktor yang digunakan untuk kalibrasi daripada jumlah variabel asalnya (Miller dan Miller, 2010). Namun, PCR hanya mempertimbangkan korelasi variabel prediksi dengan komponen utama (PC) tanpa memperhatikan kekuatan hubungan dengan variabel respon.
b) Partial Least Square (PLS)
Partial least square, atau yang biasa disebut PLS pertama kali dikembangkan oleh H. Wold di bidang ekonometri pada akhir tahun 1960 (Gemperline, 2006). PLS digunakan untuk memperkirakan serangkaian variabel tidak bebas (respon) dari variabel bebas (prediktor yang jumlahnya sangat banyak, memiliki struktur sistematik linier atau nonlinier, dengan atau tanpa data yang hilang, dan memiliki kolinieritas yang tinggi (Herve, 2003). Pada metode kemometrika PLS, variabel yang dipilih merupakan variabel yang memiliki korelasi yang baik dengan respon, sehingga variabel tersebut akan memberikan prediksi yang lebih efektif (Adams, 1995).
Regresi PLS dihitung dengan alogaritma kuadrat terkecil yang menghubungkan antara dua matriks, data spektra pada matriks X dan nilai referen pada matriks Y. PLS sering digunakan dalam spektroskopi FTIR untuk mengekstrak informasi dari spektra yang kompleks yang mengandung puncak-puncak yang tumpang tindih, serta adanya noise dari instrumen yang digunakan untuk mengumpulkan data (Syahariza dkk., 2005).
PLS menggunakan kombinasi linier dari variabel prediksi terhadap variabel sebenarnya. Variabel yang menunjukkan korelasi tinggi dengan variabel respon diberikan bobot tambahan karena lebih efektif untuk prediksi. Dengan cara ini, kombinasi linier dari variabel prediksi dipilih dari yang memiliki korelasi tinggi dengan variabel respon dan juga menjelaskan variasi dalam variabel prediksi (Miller dan Miller, 2010). Model regresi ini memberikan kelebihan berupa pembentukan komponen model PLS yang dapat menggambarkan korelasi antara spektra FTIR dan konsentrasi analit, meskipun jika diamati visual tidak terlihat adanya perbedaan nyata pada spektra (Yang dkk., 2006). Setiap komponen pada regresi PLS diperoleh dengan memaksimalkan korelasi variasi antara variabel y dengan setiap fungsi linier yang memungkinkan dari variabel x (Romia dan Bernardez, 2009).
Dalam penelitian ini diperlukan metode untuk menguji validitas model analisis dengan menggunakan data uji di luar data yang digunakan dalam pembentukan analisis. Metode ini disebut “Validasi Silang” yang digunakan untuk menentukan seberapa kuat model prediksi yang dibuat untuk dapat
diimplementasikan (Nawa, 2012). Ada 3 macam teknik validasi silang yaitu Leave One Out, K-Fold Cross Validation dan 2-Fold Cross Validation. Teknik yang dipakai dalam penelitian ini adalah Leave One Out, yaitu dengan cara nilaisampel pertama dikeluarkan dari serangkaian data dan nilai sampel sisanya digunakan untuk membuat persamaan terprediksi, lalu sampel yang pertama diujikan pada persamaan terprediksi yang baru dan diperoleh nilai terprediksi untuk sampel pertama. Nilai terprediksi diperoleh untuk seluruh nilai sampel yang ada, kemudian didapat selisih dari nilai sampel sebenarnya dengan nilai terprediksi untuk tiap sampel. Total kuadrat selisih nilai-nilai ini disebut dengan Predicted Residual Error Sum of Squares (PRESS) (Miller dan Miller, 2010).
F. Landasan Teori
Salah satu komoditas bahan alam andalan Indonesia, yakni temulawak (Curcuma xanthorrhiza Roxb.), merupakan bahan yang sangat strategis untuk dikembangkan mengingat banyaknya manfaat yang ditunjukkan oleh bahan aktif kurkuminoid yang terkandung di dalamnya. Kurkumin merupakan senyawa komponen kurkuminoid dengan persentase paling besar.
Metode kuantifikasi kurkumin dalam ekstrak etanolik temulawak yang cepat dan efisien mutlak diperlukan. Salah satu metode kuantifikasi cepat dan efisien yang ditawarkan adalah metode spektroskopi Fourier Transform Infrared (FTIR) yang dikombinasikan dengan kalibrasi multivariat. Metode spektroskopi FTIR telah
terbukti menjadi alat yang ampuh untuk analisis kualitatif dan kuantitatif konstituen dalammakanan, tanaman dan produk farmasi (Roggo dkk., 2007; Burns dkk., 2001). Metode kalibrasi multivariat dengan teknik Partial Least Square (PLS) dalam penelitian ini dapat digunakan untuk menghasilkan korelasi yang baik antara data spektrum FTIR dan informasi yang telah diketahui dari sampel, yang dalam hal ini berupa konsentrasi kurkumin. Konsentrasi kurkumin dari setiap sampel diukur dengan menggunakan metode acuan yang diakui, yaitu metode Kromatografi Cair Kinerja Tinggi (KCKT).
Tanaka dkk. (2008) membuktikan bahwa kemometrika PLS dapat digunakan untuk menganalisis kuantitatif kurkumin dalam ekstrak metanolik kunyit dengan menggunakan spektroskopi Near-infrared (NIR). Dengan metode yang sama, diharapkan kemometrika PLS juga dapat digunakan untuk analisis kuantitatif kuantitatif kurkumin dalam ekstrak etanolik temulawak.
Pola spektrum FTIR (terutama pada daerah sidik jari) merupakan pola yang kompleks, penafsirannya memerlukan bantuan metode kemometrik. Optimasi spektroskopi FTIR dengan digabungkan dengan metode kemometrika tertentu seperti kalibrasi multivariat (Partial Least Square, PLS) dapat digunakan untuk analisis kuantitatif kurkumin dalam ekstrak etanolik temulawak.
G. Hipotesis
hipotesis sebagai berikut:
1. Kandungan kurkumin dalamekstrak etanolik temulawak dapat dianalisis menggunakan metode spektrofotometri FTIR yang dikombinasikan dengan kalibrasi multivariat.
2. Kandungan kurkumin dalam ekstrak etanolik temulawak yang dianalisis dengan metode KCKT dan spektrofotometri inframerah akan menghasilkan korelasi yang baik dengan bantuan model kalibrasi multivariat (Partial Least Square, PLS).