BAB II
TINJAUAN PUSTAKA
2.1 Poli Asam Laktat
Salah satu jenis biodegradable polyester adalah Poli asam laktat (polylactic acid). Poli asam laktat (PLA) ditemukan pada tahun 1932 oleh Carothers (DuPont) yang memproduksi PLA dengan berat molekul rendah dengan memanaskan asam laktat pada kondisi vakum. Pada tahap selanjutnya, DuPont dan Ethicon memfokuskan pembuatan aplikasi medical grade satures, implan dan kemasan obat. Baru-baru ini, beberapa perusahaan seperti Shimadzu dan Mitsui Tuatsu di Jepang telah memproduksi sejumlah PLA untuk aplikasi plastik. Poli asam laktat atau Poli laktida (PLA) dengan rumus kimia (CH3CHOHCOOH)n adalah sejenis polimer atau plastik yang bersifat biodegradable, thermoplastic dan merupakan poliester alifatik yang terbuat dari bahan-bahan terbarukan seperti pati jagung atau tanaman tebu. Walaupun PLA sudah dikenal sejak abad yang lalu, namun baru diproduksi secara komersial dalam beberapa tahun terakhir dengan keunggulan kemampuan untuk terdegradasi secara biologi (en.wikipedia.org).
Gambar 2.1 rumus struktur poli asam laktat
Poli asam laktat merupakan keluarga aliphatic polyesters yang biasanya dibuat dari alfa asam hidroksi yang ditambahkan asam poliglicolat atau polimandelat. Poli asam laktat memiliki sifat tahan panas, kuat, & merupakan polimer yang elastic (Auras, 2002). Poli asam laktat yang terdapat di pasaran dapat dibuat melalui fermentasi karbohidrat ataupun secara kimia melalui polimerasi kondensasi dan kondensasi azeotropik (Auras, 2006). Polimer Poli asam laktat dapat terurai di tanah baik dalam kondisi aerob ataupun anaerob dalam kurun waktu enam bulan sampai lima tahun (Auras, 2002).
Poli asam laktat, menggabungkan sifat terbaik dari bahan alami dan bahan buatan. Karena bahan ini dibuat dari gula tumbuhan, maka bahan ini menggunakan sumber yang dapat diperbaharui dan dapat diuraikan kembali sepenuhnya. Selain itu,
bahan ini juga mempunyai sifat-sifat yang sama dengan plastik biasa yang terbuat dari hidrokarbon, yaitu kuat, lentur dan murah harganya. Setelah para pecinta lingkungan mulai menunjukkan kepedulian akan merosotnya persediaan bahan bakar dan menghilangnya lahan pembuangan, para pengusaha pabrik sudah mencoba untuk mengembangkan beberapa bahan alternatif untuk pengganti plastik biasa yang terbuat dari hidrokarbon.
Hasil-hasil riset terbaru menunjukkan poli asam laktat mempunyai keunikan dan kelebihan baik dalam permebelitas, transmisi oksigen, suhu transisi, dan kecepatan mengompos dibandingkan dengan jenis plastik lain. Poli asam laktat memiliki permeabilitas uap air yang relatif rendah sehingga memungkinkan layak dijadikan kemasan. Poli asam laktat juga memiliki laju transmisi oksigen (udara) relatif lebih tinggi sehingga bisa digunakan untuk pangan yang diinginkan dalam bentuk cair. Suhu perubahan Poli asam laktat adalah antara 50-60° C sehingga dapat digunakan untuk kemasan makanan dingin
2.2 Aplikasi PLA Sebagai Pengganti Plastik Konvensional
Poli asam laktat mempunyai potensi yang sangat besar dikembangkan sebagai pengganti plastik konvensional. Poli asam laktat bersifat termoplastik, memiliki kekuatan tarik dan modulus polimer yang tinggi, bobot molekul dapat mencapai 100.000 hingga 500.000, dan titik leleh antara 175-200ºC (Oota, 1997). Pada umumnya PLA dipergunakan untuk menggantikan bahan yang transparan dengan densitas dan harga tinggi. Bahan plastik yang digantikan dari jenis PET (1.4 g/cc, 1.4 usd/kg), PVC lentur (1.3 g/cc, 1 usd/kg) dan selofan film. Dibanding PP (0.9 g/cc, 0.7 usd/kg) dan HIPS (1.05 g/cc, 1 usd/kg), PLA dapat dikatakan kurang menguntungkan, namun mempunyai kelebihan lain yaitu ramah lingkungan. PP dan HIPS berasal dari minyak bumi dan jika dibakar akan menimbulkan efek pemanasan gobal, (Syah Johan, 2008).
Kelebihan poli asam laktat pada jenis BOPLA (bioriented PLA atau bentuk stretch dua arah) dimana twist dan deadfold mirip seperti selofan dan PVC, karena itu BOPLA dipergunakan juga untuk film yang tipis untuk pembungkus permen. BOPLA mempunyai barier yang bagus untuk menahan aroma, bau, molekul solven dan lemak sebanding dengan PET atau nilon 6. Sebagai bahan polar poli asam laktat
mempunyai tegangan 38 dynes/cm2 sehingga mudah untuk di-print dengan berbagai tinta tanpa proses „flame dan corona„ seperti halnya BOPP atau film yang lain. Poli asam laktat merupakan penyekat yang bagus dengan suhu gelas atau Tg 55-65 deg, inisiasi sealing bisa dimulai pada suhu 80 deg sama dengan sealant dari 18% EVA. Gabungan antara kemudahan untuk di-seal dan tingginya barier untuk aroma dan bau maka PLA dapat digunakan sebagai lapisan paling dalam untuk pengemas makanan, (Syah Johan, 2008).
Kekurangan PLA adalah densitas lebih tinggi (1.25 g/cc) disbanding PP dan PS dan mempunyai polaritas lebih tinggi sehingga sulit direkatkan dengan PE dan PP yang non polar dalam system film multi lapis. PP mempunyai densitas 0.9 g/cc, denga harga 0.7 usd per kg dan HIPS mempunyai densitas 1.05 g/cc dan harga 1 usd per kg. PLA juga mempunyai ketahanan panas, moisture dan gas barier kurang bagus dibanding dengan PET. Hal lain yang paling penting adalah harganya yang masih tinggi yaitu 2.6 usd per kg. usaha untuk menurunkan harga teruus dilakukan oleh Cargill Dow hingga 2 usd per kg supaya kompetitif. Sifat barier terhadap uap air, oksigen dan CO2 lebih rendah disbanding PET, PP atau PVC. Perbaikan sifat barier dapat dilakukan dengan system laminasi dengan jenis film lain seperti PE, PVOH, Alufoil, Nanopartikel dan lainnya, (Syah Johan, 2008).
Menurut Botelho (2004), kelebihan poli asam laktat dibandingkan dengan plastik yang terbuat dari minyak bumi adalah:
1. Biodegradable, artinya poli asam laktat dapat diuraikan secara alami di lingkungan oleh mikroorganisme.
2. Biocompatible, dimana pada kondisi normal, jenis plastik ini dapat diterima oleh sel atau jaringan biologi.
3. Dihasilkan dari bahan yang dapat diperbaharui (termasuk sisa industri) dan bukan dari minyak bumi.
4. 100% recyclable, melalui hidrolisis asam laktat dapat diperoleh dan digunakan kembali untuk aplikasi yang berbeda atau bisa digabungkan untuk menghasilkan produk lain.
5. Tidak menggunakan pelarut organik/bersifat racun dalam memproduksi poli asam laktat.
6. Dapat dibakar sempurna dan menghasilkan gas CO2 dan air.
Saat ini, poli asam laktat sudah digunakan untuk beragam aplikasi, diantaranya dibidang medis, kemasan dan tekstil. Dibidang medis, PLA sudah lama digunakan sebagai benang jahit pada saat operasi serta bahan pembungkus kapsul. Selain itu pada dasawarsa terakhir Poli asam laktat juga dikembangkan dalam upaya perbaikan jaringan tubuh manusia dan juga telah dikembangkan untuk pembuatan kantong plastik (retail bags), kontainer, bahkan edible film untuk sayuran dan buah. Dalam bentuk film dan bentuk foam digunakan untuk pengemas daging, produk susu, atau roti. Dapat juga digunakan dalam bentuk botol dan cangkir sekali pakai untuk kemasan air, susu, jus dan minuman lainnya. Piring, mangkok, nampan, tas, film pertanian merupakan penggunaan lain dari jenis plastik ini.Selain itu dibidang tekstil PLA juga telah diaplikasikan untuk pembuatan kaos dan tas. Di Jepang, PLA bahkan sudah dikembangkan sebagai bahan dasar pembuatan compact disc (CD) oleh Sanyo.
2.3 Proses Pembuatan Poli Asam Laktat (PLA)
Menurut Averous (2008), sintesa poli asam laktat adalah sebuah proses yang terdiri dari beberapa langkah, dimulai dari produksi asam laktat sampai pada tahap polimerisasi. Poli asam laktat dapat diproduksi melalui tiga metode, yaitu:
(1) Polikondensasi langsung (direct condensation-polymerization) asam laktat yang menghasilkan poli asam laktat dengan berat molekul rendah dan rapuh sehingga sebagian besarnya tidak dapat digunakan kecuali jika ditambahkan chain coupling agent untuk meningkatkan panjang rantai polimer;
(2) Kondensasi dehidrasi azeotropik (Azeotropic dehydration condensation) asam laktat dengan menggunakan pelarut azeotropik, yang dapat menghasilkan poli asam laktat dengan berat molekul mencapai 15.400 dan rendemen sebesar 89% dan,
(3) polimerisasi pembukaan cincin (ring opening polymerization, ROP), yang dilakukan melalui tiga tahapan yaitu polikondensasi asam laktat, depolimerisasi sehingga membentuk dimer siklik (lactide) dan dilanjutkan dengan polimerisasi pembukaan cincin, sehingga diperoleh poli asam laktat dengan berat molekul tinggi. Polimerisasi pembukaan cincin menghasilkan poli asam laktat dengan berat molekul 2×104 hingga 6.8×105. Metoda ROP
ini telah dipatenkan oleh Cargill (Amerika Serikat) pada tahun 1992.
Gambar 2.2. Metode sintesa Poli asam laktat untuk mendapatkan berat molekul tinggi, (Averous, 2008).
2.3.1 fermentasi Asam Laktat
Langkah pertama dalam sintesa Poli asam laktat adalah produksi asam laktat. Asam laktat (IUPAC: 2-hydroxypropanoic acid) yang biasa disebut sebagai asam susu adalah salah bahan kimia yang berperan penting dalam industri biokimia. Asam laktat pertama kali berhasil diisolasi oleh ahli kimia Swedia, Carl Wilhelm Scheele pada tahun 1780. Asam laktat mempunyai rumus kimia C3H6O3, termasuk keluarga asam hidroksi propionat dengan rumus molekul CH3CHOHCOOH. Asam laktat dalam larutan akan kehilangan satu proton dari gugus asam dan menghasilkan ion laktat CH3CH(OH)COO-. Asam laktat larut dalam air dan etanol serta bersifat higroskopik (en.wikipedia.org).
Asam laktat dapat dihasilkan melalui proses fermentasi atau secara sintesis kimiawi. Reaksi dasar proses kimiawi adalah mengubah laktonitril (asetaldehid
sianohidrin) menjadi asam laktat. Beberapa metode kimia yang memungkinkan sintesis asam laktat adalah degradasi gula dengan alkali seperti kapur atau NaOH, interaksi asetaldehid dan karbonmonoksida pada suhu dan tekanan yang dinaikkan, dan hidrolisa dari asam α-kloropropionat (Tito,2009).
Fermentasi merupakan metoda yang paling banyak digunakan oleh industri untuk menghasilkan asam laktat. Menurut Hofvendahl dan Hahn–Hägerdal (2000), dari 80.000 ton dari asam laktat yang dihasilkan di seluruh dunia setiap tahun sekitar 90% dibuat dengan cara fermentasi bakteri asam laktat dan sisanya dihasilkan melalui sintesis kimia yaitu hidrolisis laktonitril. Averous (2008) juga menjelaskan hal senada dengan perkiraan produksi asam laktat dunia 200.000 ton pertahun. Salah satu keunggulan metode fermentasi adalah asam laktat yang dihasilkan bisa diatur hanya terdiri dari satu enantiomer berdasarkan bakteri yang digunakan (Hofvendahl dan Hahn–Hägerdal, 2000).
Proses fermentasi dapat digolongkan berdasarkan jenis bakteri yang digunakan; (1) metoda heterofermentatif, menghasilkan kurang dari 1.8 mol asam laktat per
mol heksosa dengan hasil fermentasi lainnya dengan jumlah yang signifikan diantaranya asam asetat, etanol, gliserol, manitol dan karbondioksida;
(2) metoda homofermantatif yang hanya menghasilkan asam laktat, atau menghasilkan produk samping dengan jumlah yang sangat kecil. Metoda homofermentatif ini banyak digunakan di industri, dengan konversi yield glukosa menjadi asam laktat lebih dari 90% (Hofvendahl dan Hahn– Hägerdal, 2000).
2. 3.2 Polimerisasi Asam Laktat
Langkah selanjutnya dari sintesa poli asam laktat adalah polimerisasi asam laktat. Polimerisasi asam laktat sendiri terdiri dari tiga metode, yaitu:
Polimerisasi poli asam laktat dengan metode Polikondensasi Langsung
Polimerisasi kondensasi adalah metoda paling murah untuk menghasilkan Poli asam laktat, namun sangat sulit untuk mendapatkan Poli asam laktat dengan berat molekul yang tinggi (Averous, 2008). Polikondensasi langsung (konvensional) ini dimungkinkan, karena adanya gugus hidroksil dan karboksil pada asam laktat. Namun, reaksi polikondensasi konvensional asam laktat ini tidak cukup dapat meningkatkan bobot molekulnya dan pada metode ini dibutuhkan waktu yang sangat lama karena sulitnya untuk mengeluarkan air dari produk yang memadat, sehingga produk air yang dihasilkan justru akan menghidrolisis polimer yang terbentuk. Reaksi polikondensasi konvensional hanya mampu menghasilkan poli asam laktat denggan bobot kurang dari 1,6×104 (Tito, 2009) yang cirinya seperti kaca yang getas (britle). Pada perkembangannya, polikondensasi langsung ini selalu melibatkan pengurangan kadar air hasil kondensasi dengan menggunakan pelarut pada tekanan vakum dan temperatur tinggi.
Berat molekul dapat ditingkatkan dengan penggunaan coupling atau esterification-promoting agents yang berfungsi memperpanjang ikatan kimia, namun biaya produksi meningkat karena proses yang cukup rumit dan panjang (multistep process). Chain-extending agents berfungsi untuk mereaksikan gugus hidroksil (OH) atau karboksil yang berada di ujung molekul poli asam laktat sehingga membentuk polimer telechelic. Penggunaan agen ini memberikan beberapa keuntungan karena reaksi hanya melibatkan sedikit agen dan bisa diselesaikan tanpa perlu dipisahkan dengan proses yang lain. Kemampuan untuk mengembangkan desain kopolimer dengan gugus fungsi yang beraneka macam juga bisa diperluas. Kelemahannya adalah polimer mungkin masih mengandung chain-extending agents yang tidak bereaksi, oligomer dan sisa-sisa pengotor logam yang berasal dari katalis. Beberapa chain-extending agents juga dapat mengurangi sifat biodegradabilitas polimer. Beberapa agen yang digunakan diantaranya anhydride, epoxide and isocyanate. Produk-produk seperti ini digunakan untuk pengembangan poli asam
laktat yang cocok untuk bahan dasar pencampuran (PLA-based blends). Kelemahan penggunaan isosianat sebagai chain extenders adalah sifatnya yang beracun (eco-toxicity).
Keuntunggan penggunaan esterification-promoting adjuvents adalah produk akhir dengan kemurnian yang tinggi dan bebas dari sisa-sisa katalis dan/atau oligomer. Kekurangannya adalah biaya yang tinggi sehubungan dengan banyaknya tahap yang dilibatkan dan pemurnian tambahan dari residu dan produk samping, karena produk samping yang dihasilkan harus dinetralkan atau bahkan dihilangkan (Averous, 2008).
Polimerisasi Poli asam laktat dengan metode Polikondensasi Azeotropik
Reaksi polikondensasi azeotropik merupakan modifikasi dari reaksi polikondensasi konvensional yang dapat menghasilkan bobot molekul yang lebih tinggi dan tidak menggunakan chain-extenders atau adjuvents dan beberapa kelemahannya (Averous, 2008). Mitsui Chemical (Jepang) telah mengkomersialkan proses ini dimana asam laktat dan katalis didehidrasi secara azeotropik dalam sebuah refluxing, pemanasan dengan temperatur tinggi, pelarut aprotic pada tekanan rendah untuk menghasilkan poli asam laktat dengan berat molekul mencapai ≥ 300.000.
Reaksi polikondensasi azeotropik menggunakan pelarut seperti difenil eter, xilena, bifenil dan klorobenzena untuk memudahkan pemisahan air dari produk pada atmosfer normal atau tekanan rendah. Reaksi ini juga dapat menggunakan berbagai jenis katalis seperti asam protonat, logam, oksida logam, logam halida dan garam asam organik dari logam. Logam memiliki orbital p dan d yang bebas dan dapat menginisiasi terbentuknya kompleks koordinasi. Salah satu logam yang yang dapat digunakan sebagai katalis reaksi polikondensasi azeotropik adalah logam timah. Logam timah memiliki toksisitas yang rendah, merupakan katalis yang direkomendasikan FDA dan dapat dipisahkan dari polimer setelah polimerisasi. Fungsinya adalah untuk mempercepat reaksi pembentukan poli asam laktat. Polikondensasi azeotropik dalam larutan dapat mencegah terjadinya reaksi pesaing, yaitu pembentukan laktida dan reaksi degradasi poli asam laktat yang terbentuk (tito dkk, 2009).
Polimerisasi Poli asam laktat dengan metode Ring Opening Polymerization (ROP)
Ring opening polymerization (ROP, reaksi polimerisasi pembukaan cincin) merupakan metoda yang lebih baik untuk menghasilkan poli asam laktat dengan bobot molekul yang tinggi, dan sekarang telah diadaptasi untuk proses komersial seiring dengan kemajuan teknologi fermentasi dekstrosa jagung. Metoda ini pertama kali diperkenalkan oleh Carothers pada tahun 1932, namun belum bisa menghasilkan poli asam laktat dengan bobot molekul yang tinggi sampai teknik pemurnian asam laktat membaik, seperti yang dikembangkan oleh DuPont pada tahun 1954. Mekanisme-mekanisme ROP bisa berupa reaksi ionik (anionik atau kationik) atau coordination–insertion, bergantung kepada sistem katalisnya (Averous, 2008).
Secara umum, proses ROP pada produksi poli asam laktat dimulai dari polimerisasi kondensasi asam laktat untuk menghasilkan poli asam laktat dengan bobot molekul rendah (prepolimer), dilanjutkan dengan depolimerisasi untuk menghasilkan dimer laktida yang berbentuk molekul siklik. Laktida kemudian dengan bantuan katalis dipolimerisasi ROP untuk menghasilkan PLA dengan bobot molekul yang tinggi.
Dalam Pra-rancangan pembuatan Pabrik Poli asam laktat (PLA) ini dipilih proses fermentasi dengan menggunakan bakteri dengan sumber karbon dekstrosa dan nutrient pembatas Diamonuim posfat (N). Sedangkan proses polimerisasi Poli asam laktat dengan metode Ring opening polymerization (ROP, reaksi polimerisasi pembukaan cincin) karena Ring opening polymerization (ROP, reaksi polimerisasi pembukaan cincin) merupakan metoda yang lebih baik untuk menghasilkan poli asam laktat dengan bobot molekul yang tinggi.
.
2.4 Deskripsi Proses Pembuatan Poli Asam Laktat dari dekstrosa
Proses pembuatan poliasam laktat dengan bahan baku dektrosa, terdiri dari beberapa tahap yaitu; tahap fermentasi, tahap pemurnian asam laktat, tahap prapolimerisasi dan tahap polimerisasi.
Tahap awal adalah tahap menghasilkan asam laktat yaitu melalui proses fermentasi dekstrosa dan pemurnian asam laktat. Dektsrosa difermentasi di dalam fermentor dengan bantuan bakteri lactobacillus derbucki, sebuah molekul glukosa akan diubah menjadi 2 buah molekul asam laktat. Dimana dalamm proses fermentasi ditambahkan media-media yang berfungsi menbantu proses kerja bakteri yang ada didalam fermentor. Penambahan diammonium fosfat dan malt sprouts berfungsi sebagai nutrient untuk bakteri sedangkan penambahan kalsium karbonat secara berkala berfungsi untuk menetralakan pH fermentor agar pH nya tidak terlalu rendah dimana proses fermentasi berlangsung pada pH 4-6 dengan suhu 40 °C. Proses fermentasi berlangsung selama 24-48 jam.
Reaksi fermentasi yang terjadi di dalam fermenter: C6H10O6 2C3H6O3 + biomass
Untuk mencegah produk asam laktat yang dihasilkan memiliki pH yang terlalu tinggi maka perlu dilakukan penambahan kalsium hidroksida (Ca(OH)2) pada tangki
koagulasi sehingga terbentuk Ca-laktat dimana proses ini dipanaskan dengan uap dalam tangki koagulasi dan selanjutnya disaring sehingga bebas dari bahan yang tidak diinginkan.
Reaksi pembentukan kalsium laktat:
2C3H6O3 + Ca(OH) 2 C3H5O3-Ca+O3-H5C3 + 2H2O
Kemudian larutan Ca-laktat dipekatkan di dalam evaporator untuk menghasilkan kalsium laktat 32%.
Untuk mendapatkan asam laktat, kalsium laktat selanjutnya diasamkan dengan menambahkan larutan asam sulfat di dalam acidifier pada temperatur 70°C sehingga menghasilkan asam laktat dan gypsum ( kalsium sulfat dihidrat ).
Reaksi dalam acidifier ( pembentukan asam laktat dan gypsum ): bakteri
C3H5O3-Ca+O3-H5C3 + H2SO4 CaSO4 + 2C3H6O3
Gypsum dan asam laktat disaring sehingga asam laktat terpisah dari gypsum kemudian asam laktat dipekatkan lagi di dalam evaporator 99% pada evaporator II.
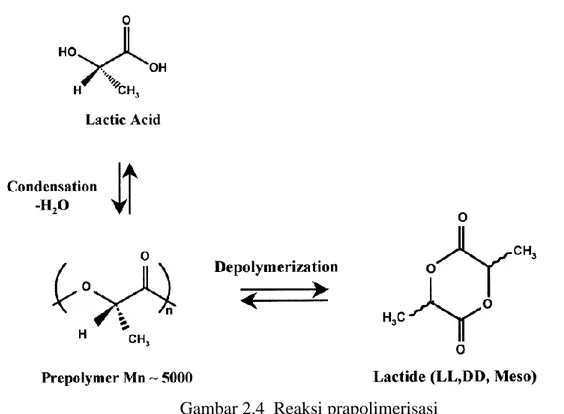
Setelah tahap proses fermentasi dan proses pemurnian untuk menghasilkan asam laktat, maka proses selanjutnya adalah tahap prapolimerisasi dan tahap polemirsasi. Tahap prepolimerisasi merupakan reaksi polikondensasi dimana terjadi proses pemutusan molekul air dari 2 buah molekul asam laktat sehingga molekul air air akan terpisah dan kemudian dilanjutkan dengan proses depolimerisasi untuk menghasilkan senyawa dimer siklik (laktida). Pada tahapan ini berat molekul yang dihasilkan antara 100-5000.
Gambar 2.4 Reaksi prapolimerisasi
Asam laktat yang dihasilkan kemudian dialirkan ke dalam reaktor prapolimer, reaktor ini dilengkapi dengan pengaduk dan suhu dalam reaktor dijaga pada suhu 160°C-200°C selama 1 jam. Dimana reaktor ini berfungsi untuk melepaskan molekul air dengan proses polikondensasi. Ke dalam reaktor juga ditambahkan katalis SnO sebanyak 0,005-0,5% dan kemudian diaduk di dalam reaktor, suhu reaktor dijaga antara 170°C - 200°C. Uap yang dihasilkan akan didestilasi sedangkan larutan yang tidak terkonversi akan ditampung dan dipisahkan katalisnya sehingga dapat digunakan kembali. Didalam kolom destilasi uap air dan uap asam laktat akan keluar
bagian atas kolom destilasi kemudian akan dikompres dan akan ditampung. Sedangkan produk bagian bawah kolom destilasi adalah produk yang diinginkan.
Kemudian dialirkan menuju reaktor polimerisasi, kemudian ditambahkan katalis (zinc β Diimate ). Jenis reaktor yang digunakan adalah fix bed reactor, suhu reaktor dijaga pada temperature 170°C. Kemudian hasilnya akan dipisahkan dengan menggunakan sentrifuse dan poli asam laktat yang dihasilkan akan dimasukkan ke dalam cristallyzer yang dilengkapi dengan pelletilizer sehingga produk yang dihasilkan berbentuk pellet.
2.5 Sifat –sifat Reaktan, Bahan Pembantu dan Produk 2.5.1 Dekstrosa (C6H12O6 )
Berbentuk bubuk Kristal berwarna putih Tidak berbau
Berat molekul : 180,76 gr/mol
Kelarutan : 1 g/1.1 ml air pada 25°C (77F) Densitas : 1.54 pada 25°C/4°C
pH : 5,9 untuk 0,5 M
Titik leleh : 146° C
Ketika dipanaskan akan terurai menghasilkan karbon dioksida dan karbon monoksida
Stabil dalam kondisi yang tidak umum baik dalam pemakaian ataupun dalam penyimpanan. (http://jtbaker.com)
2.5.2 Air (H2O)
A.Sifat Fisika :
Berat Molekul : 18.0153 g/mol
Densitas : 0.998 g/cm³
Titik Didih : 100 °C
Titik Lebur : 0 °C
Kalor Jenis : 4184 J/(kg·K) Pelarut universal
Bersifat kohesi dan adhesi
B.Sifat Kimia :
Mengalami elektrolisis Reaksi :
Reaksi NaOh dengan CO2 menghasilkan air dan Natrium karbonat
Reaksi : 2NaOH + CO2 Na2CO3 + H2O
Netralisasi asam menghasilkan air dan garam Reaksi : NaOH + HCl NaCl + H2O
Reaksi etanol dengan asam asetat menghasilkan air dan etil asetat Reaksi : CH3CH2OH + CH3COOH → CH3COOCH2CH3 + H2O
Oksidasi butana menghasilkan asam asetat dan air Reaksi : 2 C4H10 + 5 O2 → 4 CH3COOH + 2 H2O
Reaksi natrium karbonat dan asam asetat didapat natrium karbonat dan air Reaksi : NaHCO3 + CH3COOH → CH3COONa + CO2+ H2O
Reaksi air dengan asam sulfat menghasilkan ion hidonium Reaksi : H2SO4 + H2O → H3O+ + HSO4
(http://en.wikipedia.org)
2.5.3 Kalsium Hidroksida (Ca(OH)2)
Sifat fisika : Wujud cairan
Rumus Molekul : Ca(OH)2
Berat Molekul : 74,093 g mol-1 Densitas : 2240 kg m-3 Titik didih : 244,30° C Titik leleh : 21° C Suhu Kritis : 873,59°C Tekanan Kritis : 10769,94 kPa Volume Kritis : 0,2824 m
3
kgmole
Sifat kimia :
Ketika dipanaskan sampai suhu 510
о
C akan terdekomposisi menjadi kalsium oksida dan air.
Ca(OH)2CaO + H2O
Kalsium Hidroksida Kalsium Oksida air
2.5.4 Diammonium Fosfat ((NH4)2HPO4)
Wujud : padatan
Berat Molekul : 132,056 g mol-1 Densitas : 1620 kg m-3 Titik didih : 305,36 °C Suhu Kritis : 745,08°C Tekanan Kritis : 6570,27 kPa Volume Kritis : 0,3748 m3kgmole-3 Kemurnian : 93% (2% air )
Ion ammonium akan terkonversi menjadi ammonia pada pH tinggi.
2.5.5 Bakteri: Wujud padatan
Spesies : Lactobacillus delbrueckii Berat Molekul : 25,5 g mol-1
Densitas : 3340 kg m-3
Titik didih : 333,56°C Suhu Kritis : 1386,38°C Tekanan Kritis : 13201,2 kPa
Volume Kritis : 0,3491 m3 kgmole-1
Kemurnian : 100%
Lactobacillus delbrueckii ialah bakteri yang dapat mengubah karbohidrat
menjadi asam laktat dan bekerja optimal pada suhu 46
о C. C 6H12O6 fermentasi 2CH 3CHOHCOOH
Karbohidrat Asam Laktat
2.5.6 Malt sprout
Data ini diperoleh dari database HYSYS 3.2 Wujud padatan
Berat Molekul : 416,189 g mol-1 Densitas : 4761 kg m-3
Titik didih : 2183,87
о
C Suhu Kritis : 4288,43°C Tekanan Kritis : 1324,68 kPa Volume Kritis : 9,7321 m 3 kgmole -1 Kemurnian : 100% 2.5.7 Asam Sulfat (H2SO4) Sifat Fisika :
Wujud berupa cairan
Berat Molekul : 98,079 g mol-3 Densitas : 1850,81 kg m-3 Titik didih : 253,86°C Suhu Kritis : 762,89°C Tekanan Kritis : 8698,43 kPa Volume Kritis : 0,3031 m
3
kgmole-1 Kemurnian : 98% (2% air)
Sifat Kimia :
Dengan basa membentuk garam dan air. Reaksi : H2SO4+ 2 NaOH ⎯→ Na2SO4+ H2O
Dengan alkohol membentuk eter dan air.
Reaksi : 2C2H5OH + H2SO4 -→ C2H5OC2H5 + H2O + H2SO4
Reaksi :NaCl + H2SO4 ⎯→ NaSO4 + 2HCl
Bereaksi dengan MgCO3 membentuk MgSO4
Reaksi : MgCO3 + H2SO4 ⎯→ MgSO4 + H2O + CO2
Korosif terhadap semua logam.
2.5.8 Tin octanoate (C16H32O4Sn)
Berbentuk cairan
Tidak berbau menyengat
Berat molekul : 405,1 gr/mol Spesific gravity : 1,2
Tidak larut dalam air dingin
Tidak bersifat korosif dalam wadah gelas
2.5.9 Beta Diiminate Zinc Complex C23H24N2O2ZnF3
Berat molekul : 482,8204 gr/mol Massa jenis 25oC : 1 gr/cm3
Berfungsi sebagai katalis selektif dalam reaksi polimerisasi Wujud pada suhu kamar : cair
Kuantitas penggunaan sebagai katalis 0,1 – 4 % dari total monomer (Windholz, 1983)
2.5.10 Kalsium Laktat (C6H10O6Ca)
Berbentuk serbuk kristal Berwarna putih
Kelarutan dalam air : 9gr/100ml air pada 25°C
Titik leleh : 240°C
Berat Molekul : 308,3 gr/mol Tidak berbau
Dapat diabsorpsi pada berbagai pH, (http:// www.sciencelab.com)
Berbentuk cairan yang berwarna kekuning-kuningan Berat molekul : 90,08 gr/mol
Titik leleh : 17°C
Titik didih : 122 °C pada 12 mmHg Spesific gravity : 1,2
Titik flash : 112 °C
Larut dalam air
Stabil dalam kondisi umum, (http:// www.sciencelab.com)
2.5.12 Gypsum ( CaSO4)
Berbentuk padatan dengan warna putih keabu-abuan ataupun kemrah-merahan
Bentuk Kristal : prismatik Sistem Kristal : monoklinik Skala kekerasan : 1,5-2 Spesific gravity : 2,31-2,33 Indeks refraksi : 1,522
Tidak bereaksi dengan asam, (http:// www.sciencelab.com)
2.5.13 Laktida (C6H8O4)
Berat molekul : 144 gr/mol Titik leleh : 93–97°C
Specific Heat Capacity :Solid at 25°C 1.3 J g–1 K–1 Liquid at 130°C 2.2 J g–1 K–1
Kemurnian : ≥ 98.0%
Kandungan senyawa asam : ≤ 2.0% (http://www.natureworksllc.com)
2.5.14 Poli asam laktat
Berbentuk padatan berwarna putih Tidak berbau
Titik flash : 121°C
Kekristalan : 37%
Temperatur glass transition : 60-65 °C Tensile modulus : 2.7-16 GPa Spesifik gravity : 1,23-1,30 gr/cm3 Tidak mudah larut