70 BAB 3
METODOLOGI PENELITIAN
3.1. Rancangan Penelitian
Penelitian ini merupakan studi analitik dengan desain one group pretest-posttest
untuk mengetahui perbedaan nilai faal pendarahan dan tumor marker pada pasien
kanker paru bukan sel kecil yang menjalani kemoterapi dan menilai ada atau tidaknya
hubungan antara faal pendarahan dan tumor marker pada pasien kanker paru bukan
sel kecil dengan kemoterapi dan seberapa kuat tingkat korelasi keduanya.
3.2. Tempat dan Waktu Penelitian
Penelitian dilakukan di Departemen Pulmonologi dan Kedokteran Respirasi,
RSUP. H. Adam Malik Medan. Penelitian dilakukan selama kurun waktu 17 bulan
dimulai sejak 1 januari 2015 sampai 31 Mei 2016.
3.3. Populasi, Sampel dan Besar Sampel
3.3.1. Populasi Penelitian
Populasi penelitian ini adalah semua pasien yang telah terdiagnosa
dengan kanker paru kanker paru bukan sel kecil di RSUP H. Adam
Malik Medan berdasarkan hasil sitologi dan histopatologi jaringan. Tipe
tumor dibagi kedalam grup berdasarkan sistem TNM edisi ke-7 tahun
2007.
3.3.2. Sampel Penelitian
Sampel adalah pasien yang telah terdiagnosa dengan kanker paru bukan
sel kecil di RSUP H. Adam Malik Medan yang memenuhi kriteria
inklusi dan eksklusi pada kurun waktu 1 januari 2015 sampai 31 Mei
2016 dan dilakukan kemoterapi, tiap-tiap pasien akan di follow-up
selama selama kemoterapi. Semua pasien yang diikutkan dalam
penelitian wajib membaca dan mengerti serta menandatangai inform consent.
3.3.3. Besar Sampel
Besar sampel
[
α
β
[
]
]
Keterangan :
n : Jumlah sampel yang akan diperiksa
72
Z α : 1,96
β : Kesalahan tipe II (0,1)
Z β : 1,282
r : Perkiraan koefisien korelasi (0,5)
[
[
]
]
Maka diperoleh besar sampel : 37 orang,
Dari perhitungan sampel diatas jumlah besar sampel adalah 36, dengah
memperhitungkan kasus yang drop outsebesar 10%, maka ditetapkan jumlah sampel adalah :
Ndo= N = 37 = 41
(1-do) (1-0,1)
Berdasarkan perhitungan besar sampel diatas, besar sampel yang dibutuhkan
sebesar 41 pasien
3.4. Kriteria Inklusi dan Eksklusi 3.4.1. Kriteria Inklusi:
Pasien memiliki hasil patologi anatomi berupa sitologi maupun
Histopatologi yang diperoleh dari bronkoskopi, aspirasi jarum halus
transtorakal maupun open biopsy.
Pasien dengan performa status dibawah 2 kategori WHO dan faal hati
dan faal ginjal yang baik.
Pasien direncanakan kemoterapi dengan platinum based medicine
3.4.2. Kriteria eksklusi :
Pasien dengan kelainan hematologi, dan sedang mengunakan obat
antikoagulan oral maupun injeksi.
Riwayat Operasi.
Riwayat Radioterapi.
Riwayat Diabetes dan Hipertensi.
74 3.5. Defenisi Operasional
No Variabel Defenisi Klasifikasi Lampir
an
2 Usia Umur pasien kanker paru saat datang pertama sekali berobat ke IGD
Jenis histologi sel berdasarkan hasil sitologi maupun histopatologi
4 Stage Kanker Tingkat keparahan kanker paru. 1. stage I-II 2. stage III 3. stage IV
I, no 16
5 Riwayat Merokok
Faktor kebiasaan host (pasien) dalam hal merokok. Dinilai saat pasien
Tingkat kebiasaan merokok 1. ringan 2. sedang 3. berat
I, no 9
7 Jenis rokok Jenis rokok dalam kebiasaan host 1. kretek 2. putih 3. campuran
I, no 9
8 Jenis Kemoteapi
Pilihan terapi kombinasi platinum based yang dipakai dalam menangani pasien kanker paru
5. lainnya 11 Riwayat
penyakit paru sebelumnya
Keluhan pernapasan dan penyakit paru yang pernah diderita pasien sebelum terdiagnosa dengan kanker paru dengan kontras yang telah dilakukan ke pasien dalam hal penegakkan
13 Bronkoskopi Tindakan invasif dalam menilai saluran napas mengunakan alat bronkoskopi serat optik yang diindikasikan dalam menilai diagnostik pasien dengan kanker paru
Marker darah dalam menilai tingkat koagulasi darah
Marker darah dalam,menilai kemajuan dan prognostik pasien kanker paru dengan terapi
1. CEA diperoleh setelah menjalani pemeriksaan penunjang berupa imaging, bronkoskopi dan pemeriksaan sitologi dan histopatologi
76 3.6. Identifikasi Variabel
a. Jenis kelamin
b. Umur
c. Pekerjaan
d. Pendidikan
e. Status gizi
f. Gejala klinis
g. Foto thoraks dan CT Scan
h. Sitologi dan Histopatologi
i. Darah lengkap
j. Faal Hemostasis dan D-dimer
k. Tumor marker
3.7. Pengolahan Data. 3.7.1. Sumber Data
Data diperoleh melalui pemeriksaan laboratorium terhadap responden atau
sampel penelitian yang telah mendapatkan informasi penelitian dan telah
menandatangani inform consent. Dimana semua informasi yang diberikan ke pasien berupa informasi lisan dan pasien harus betul-betul mengerti
tentang tujuan dari penelitian ini.
3.7.2. Teknik Pengumpulan Data
Data pasien yang dikumpulkan berupa data pribadi berupa nama, umur,
pekerjaan,dll.
Diagosis kanker paru bukan sel kecil ditegakkan berdasarkan keluhan,
pemeriksaan fisik, foto thorak, CT Scan dengan Kontras, Bronkoskopi,
TTNA, Open Biopsy. Kemudian hasil diatas dikonfirmasi dengan hasil sitologi dan histopatologi jaringan.
Pasien direncanakan mendapatkan kemoterapi lini pertama. Prosedur
pemeriksaan awal seperti perhitugan status performa, faal hati dan faal
ginjal, faal hemostasis dan tumor marker dilakukan setiap 7 hari sebelum
dilakukan kemoterapi dimana 1 siklus kemoterapi dilakukan selama 21
hari.
Selanjutnya pengambilan sampel dilakukan setelah 4 siklus kemoterapi
(bulan ke-4) ataupun setelah akhir siklus kemoterapi lini pertama (bulan
ke-6)
Serum pasien diambil dengan mengunakan spuit 3cc. Sampel darah
disimpan dengan menggunakan tabung berisi antikoagulan Sitras. Dan
dilakukan pemeriksaan faal hemostasis dan tumor marker mengunakan
78 Hasil pemeriksaan faal hemostasis D-dimer dan Tumor Marker akan
dicatat dan dianalisa berdasarkan diagosa, stadium tumor dan status klinis
pasien.
3.7.3. Analisa Data
Data yang berhasil dikumpulkan, diolah dan dianalisis dengan
menggunakan program komputer menggunakan perangkat lunak statistik.
Data akan dianalisa secara deskriptif untuk melihat distribusi frekuensi
variabel, selanjutnya diilakukan analisa data dengan uji beda untuk
mengalisa variabel faal hemostasis dan tumor marker sebelum dan sesudah
kemoterapi. Untuk menilai hubungan faal hemostasis dengan tumor marker
pada pasien kanker paru bukan sel kecil dengan kemoterapi dan seberapa
kuat tingkat hubungan keduanya diigunakan uji korelasi.
3.8. Kerangka Operasional
KANKER PARU
DarahRutin
PT
APTT
TT
TUMOR MARKERS SIKLUS 4/6
KEMOTERAPI/TARGET TERAPI
KEMOTERAPI LINI PERTAMA
SEBELUM
KEMOTERAPI/TARGET TERAPI
80 3.9. Jadwal Penelitian
No Kegiatan
Bulan
I-III IV-VI VII-X X-VI XVII
1 Persiapan √
2 Pengumpulan Data √ √ √ √ √
3 Pengolahan data √ √ √
4 Penyusunan laporan √ √ √
5 Seminar hasil √
3.10. Biaya Penelitian
a. Pengumpulan data Rp 2.000.000,-
b. Pembuatan proposal Rp 2.000.000,-
c. Seminar proposal Rp 2.500.000,-
d. Pelaksanaan Rp 6.500.000,-
e. Pembuatan laporan penelitian Rp 2.000.000,-
f. Tim pendukung penelitian Rp 2.000.000,-
g. Seminar hasil penelitian Rp 3.000.000,-
Rp 20.000.000,-
BAB 4
HASIL PENELITIAN DAN PEMBAHASAN
4.1. Hasil Penelitian
Penelitian ini dilakukan di RS Haji Adam Malik Medan dalam kurun waktu 17
bulan dimulai pada tanggal 1 januari 2015 sampai dengan 31 mei 2016. Adapun
subjek penelitian adalah sebanyak 41 orang penderita kanker paru bukan sel kecil
yang ditegakkan berdasarkan anamnesis, pemeriksaan fisik, gambaran foto toraks dan
pemeriksaan CT scan toraks dengan kontras yang kemudian dilakukan pemeriksaan
sitologi maupun histopatologi melalui tindakan bronkoskopi untuk mendapatkan
sediaan sel yang nantinya akan menentukan jenis kanker paru.
Seluruh sampel akan dilakukan pemeriksaan darah sebelum kemoterapi pertama
sekali (sebelum bulan pertama kemoterapi) dan pada akhir kemoterapi bulan ke-4
atau bulan ke-6, pemeriksaan darah yang akan dilakukan berupa pemeriksaan faal
hemostasis dan tumor marker kanker paru jenis sel kanker bukan sel kecil yaitu PT,
INR, APTT, TT, D-dimer dan NSE, Cyfra 21-1, CEA.
Hasil penelitian dianalisis dengan perangkat lunak, data akan dilakukan uji
normalitas terlebih dahulu kemudian akan dilakukan uji komparatif data sebelum
kemoterapi dan setelah kemoterapi selanjutnya data akan dilakukan uji korelasi.
Dengan uji diatas akan diketahui apakah data-data diatas memiliki asosiasi ataupun
82 4.1.1. Karakteristik Subjek Penelitian
Total jumlah sampel studi pada pasien ini adalah 41 orang, berdasarkan jenis
kelamin, sampel laki-laki lebih banyak dari perempuan yaitu sebanyak 35 orang
(85,4%) laki-laki dibanding dengan 6 orang wanita (14,6%). Usia rata-rata sampel
adalah 56,7 tahun, dimana tidak ada sampel dengan usia dibawah 40 tahun, 29 orang
(70,7%) dengan usia 40 sampai dengan 60 tahun, dan 12 pasien (29,3%) dengan usia
diatas 60 tahun Dari penelitian ini diperoleh 25 % dari seluruh sampel kanker
berjenis sel skuamous dan 75% sisanya adalah adeno karsinoma, dengan stage I-II
berjumlah 3 (7,3%) orang, stage III berjumlah 15 (36,6%) orang, dan stage IV dengan
23 (56,1%) orang.
Terdapat 35 orang (85,5%) sebelumnya pernah merokok dan, 6 orang (14,6%)
tidak pernah merokok, dengan Indeks Brinkman sedang berjumlah 3(7,3%) orang dan
Indeks Brinkman berat berjumlah 32 (78,1%) orang. Jenis rokok yang terbanyak
adalah rokok kretek pada 36 ( 87,8%) orang. Jenis kemoterapi yang dipakai pada
penelitian ini adalah kemoterapi lini pertama dengan platinum based therapy dengan Gembitabin dan Karboplatin pada 27 orang (65,9%) pasien, dengan Paklitaksel dan
Karboplatin pada 10 orang (24,4%) pasien, dan dengan Vinorelbin dan Karboplatin
pada 4 orang (9,8%) pasien.
Setelah kemoterapi pasien dilakukan follow up dalam waktu 1 bulan setelah
kemoterapi dan 12 bulan setelah kemoterapi. Dimana dari follow-up 1 bulan diperoleh 2 (4,9%) pasien tanpa keluhan, 14 (34,1%) pasien dengan keluhan berupa
disabilitas motorik dan sisanya 25 pasien (61,0%) meninggal dunia. Pada follow-up 1
tahun setelah kemoterapi diperoleh 2 (4,9%) orang tanpa keluhan, 3 orang pasien
(7,3%) dengan disabilitas motorik, dan sisanya 36 (87,8%) pasien meninggal dunia.
Tampak pada tabel 4.1.
Tabel 4.1. Distribusi Frekuensi pasien berdasarkan karakteristik
Kategori n %
Karsinoma sel skuamous
31
Tidak pernah merokok Jenis Rokok
Gemsitabin dan Karboplatin
Paklitaksel dan Karboplatin
Vinorelbin dan Karboplatin
84
Follow up pasien 1 bulan post kemoterapi
Tidak ada keluhan
Disabilitas Motorik Follow up pasien 12 bulan post
kemoterapi
Tidak ada keluhan
Disabilitas Motorik
Dari pemeriksaan parameter hemostasis sebelum kemoterapi diperoleh nilai
rata-rata PT pasien adalah 13.59 (min 10,5:max 19,5), nilai rata-rata INR pasien
adalah 0.98 (min 0,77; max 1,49), nilai rata-rata APTT pasien adalah 30,51 (min
24,70; max 37,50), nilai rata-rata TT pasien adalah 14,55 (min 11.9; max 24,5), nilai
rata-rata D-dimer pasien adalah 714,73 (min 100; max 4995), nilai rata-rata CEA
pasien adalah 42,11 (min 0,84; max 803,9), nilai rata-rata Cifra 21.1 pasien adalah
20,01 (min 1,34; max 150,8), nilai rata-rata NSE pasien adalah 33,96 (min 9,01; max
189,9).
Dari pemeriksaan hemostasis parameter setelah kemoterapi di peroleh nilai
rata-rata PT pasien adalah 16,63 (min 10,0: max 80.0), nilai rata-rata INR pasien
adalah 1,19 (min 0,72; max 6,00), nilai rata-rata APTT pasien adalah 30,98 (min
16.50; max 44,30), nilai rata-rata TT pasien adalah 15,43 (min 12,4; max 29,8), nilai
rata-rata D-dimer pasien adalah 584,82 (min 100; max 2800), nilai rata-rata CEA
pasien adalah 24,83 (min 0,61; max 207,00), nilai rata-rata Cifra21.1 pasien adalah
19,84 (min 0,50; max 138,73), nilai rata-rata NSE pasien adalah 35,67 (min 6,40;
max 147,50). Tampak pada tabel 4.2
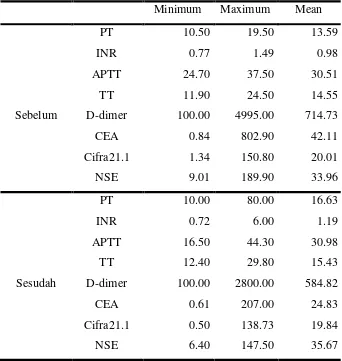
Tabel 4.2. Distribusi Sampel Sebelum dan Sesudah Kemoterapi
Minimum Maximum Mean
PT 10.50 19.50 13.59
INR 0.77 1.49 0.98
APTT 24.70 37.50 30.51
TT 11.90 24.50 14.55
Sebelum D-dimer 100.00 4995.00 714.73
CEA 0.84 802.90 42.11
Cifra21.1 1.34 150.80 20.01
NSE 9.01 189.90 33.96
PT 10.00 80.00 16.63
INR 0.72 6.00 1.19
APTT 16.50 44.30 30.98
TT 12.40 29.80 15.43
Sesudah D-dimer 100.00 2800.00 584.82
CEA 0.61 207.00 24.83
Cifra21.1 0.50 138.73 19.84
NSE 6.40 147.50 35.67
4.1.2 Uji Normalitas
Sebelum dilakukan uji korelasi, sampel harus di uji dengan uji normalitas data.
86
penelitian berasal dari populasi yang berdistribusi normal atau tidak. Model regresi
yang baik adalah yang datanya berdistribusi normal atau mendekati normal
Tabel 4.3. Uji Normalitas
One-Sample Kolmogorov-Smirnov Test
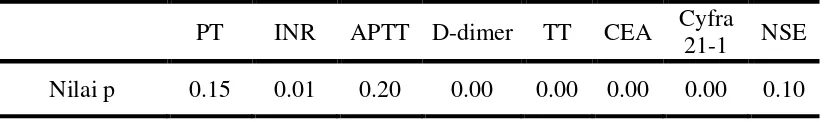
Dari uji One-Sample Kolmogorov-Smirnov Test diperoleh nilai test distribusi
variabel faal hemostasis dan serum tumor marker adalah tidak normal. Dimana pada
test ini diperoleh PT dengan nilai p 0.15, INR dengan nilai p 0.01, APTT dengan nilai
p 0.20 D-dimer dengan Nilai P 0.00, TT dengan Nilai P 0.00, CEA dengan Nilai p
0.00, Cyfra 21-1 dengan Nilai P 0.00, NSE dengan nilai p 0.10 berada pada nilai P <
0.05 yang memberikan kesimpulan bahwa variabel-variabel tersebut tidak
berdistribusi normal. Dari hasil ini maka dapat disimpulkan data pada penelitian ini
tidak berdistribusi normal.
4.1.3. Distribusi Sampel Pre Kemoterapi dan Post Kemoterapi.
Pada penelitian ini diperoleh data dengan dua kali pengambilan sampel darah,
pertama pemeriksaan dilakukan sebelum pasien mendapatkan kemoterapi dan yang
kedua adalah sesudah pasien menjalani 4 siklus atau 6 siklus kemoterapi. Pada
penilaian pada penilaian terhadap parameter hemostasis adalah PT, INR, APTT, TT PT INR APTT D-dimer TT CEA Cyfra
21-1 NSE
Nilai p 0.15 0.01 0.20 0.00 0.00 0.00 0.00 0.10
dan D-dimer, dan penilaian pada nilai serum marker kanker paru adalah CEA, Cyfra
21-1 dan NSE.
Dari pemeriksaan parameter hemostasis sebelum kemoterapi diperoleh nilai
rata-rata PT pasien adalah 13,3, nilai rata-rata INR pasien adalah 0.96, nilai rata-rata
APTT pasien adalah 30.3, nilai rata-rata TT pasien adalah 14.56, nilai rata-rata
D-dimer pasien adalah 763.6, nilai rata-rata CEA pasien adalah 62.66, nilai rata-rata
Cyfra 21-1 pasien adalah 29.51, nilai rata-rata NSE pasien adalah 27.90.
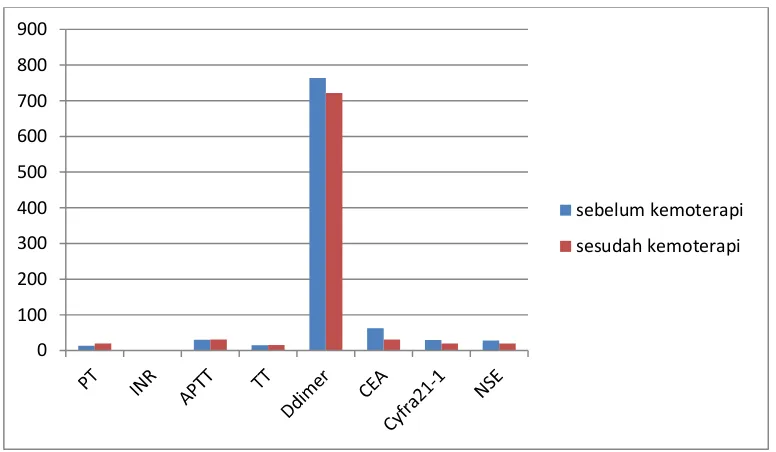
Gambar 4.1. Perbandingan Nilai Parameter Hemostasis dan Serum Tumor Marker
sebelum dan sesudah kemoterapi.
Dari pemeriksaan hemostasis parameter setelah kemoterapi di peroleh nilai
rata-rata PT pasien adalah 14.9, nilai rata-rata INR pasien adalah 1.06, nilai rata-rata
APTT pasien adalah 30.6, nilai rata-rata TT pasien adalah 15.4, nilai rata-rata
D-dimer pasien adalah 721.6, nilai rata-rata CEA pasien adalah 30.56, nilai rata-rata
0 100 200 300 400 500 600 700 800 900
sebelum kemoterapi
88
Cyfra 21-1 pasien adalah 19.2, nilai rata-rata NSE pasien adalah 19.84, perbandingan
nilai parameter hemostasis dan serum tumor marker dapat dilihat pada gambar 4.1.
4.1.4. Perbedaan Nilai Parameter Hemostsasis dan Tumor Marker Sebelum dan Sesudah Kemoterapi
Untuk mengetahui apakah ada perbedaan yang terjadi pada variabel sebelum
kemoterapi dengan variabel sesudah kemoterapi maka variabel ini dapat dilakukan uji
beda. Dalam penelitian ini dilakukan uji beda yang dilakukan pada faal hemostsasis
dan tumor marker sebagai variabel dependent terhadap kemoterapi sebagai variabel
independent adalah ujimann whitney.
Dari Uji Mann Whitney dibawah diperoleh nilai P pada PT terhadap kemoterapi
adalah 0.019, nilai p pada INR terhadap kemoterapi adalah 0.026, nilai p pada APTT
terhadap kemoterapi adalah 0.827, nilai p pada TT terhadap kemoterapi adalah 0.284,
nilai P pada D-dimer terhadap kemoterapi adalah 0.044, nilai p pada CEA terhadap
kemoterapi adalah 0.853, nilai p pada Cyfra 21.1 terhadap kemoterapi adalah 0.697,
dan nilai p pada NSE terhadap kemoterapi adalah 0.025.
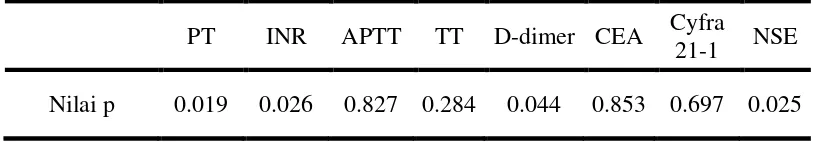
Tabel 4.4. Perbedaan Nilai parameter Hemostsasis dan Tumor Marker Sebelum dan
Sesudah Kemoterapi
PT INR APTT TT D-dimer CEA Cyfra
21-1 NSE
Nilai p 0.019 0.026 0.827 0.284 0.044 0.853 0.697 0.025
Uji Mann Whitney
Dari hasil diatas diketahui masing-masing variabel dependent PT, INR,
D-dimer dan NSE memiliki nilai p terhadap kemoterapi dibawah 0.05 yang memberikan
informasi bahwa terdapat perbedaan yang signifikan dari nilai masing-masing
variabel dependen sebelum melakukan kemoterapi dengan nilai sesudah melakukan
kemoterapi, variabel dependent APTT. TT, CEA, Cyfra 21-1 memiliki nilai p pada
terhadap kemoterapi diatas 0.05 yang memberikan informasi bahwa tidak ada
perbedaan yang signifikan dari nilai masing-masing variabel dependen sebelum
melakukan kemoterapi dengan nilai sesudah melakukan kemoterapi.
4.1.5. Korelasi antara Nilai Parameter Hemostasis terhadap Tumor Marker pada Pasien Kanker Paru Bukan Sel Kecil dengan Kemoterapi
Pada akhirnya dalam menilai adakah korelasi antara nilai parameter hemostasis
sesudah kemoterapi dan nilai tumor marker sesudah kemoterapi dilakukan Uji
Korelasi Spearman. Uji ini dilakukan dengan cara menguji korelasi 1 (satu) variabel
parameter hemostasis dengan nilai tumor marker satu persatu sampai ditemukan nilai
korelasi pada seluruh sampel yang dinilai.
Dari uji korelasi spearman diperoleh bahwa nilai koefisien korelasi variabel faal
hemostasis PT terhadap CEA adalah - 0.233 nilai p 0.143. Nilai koefisien korelasi
variabel faal hemostasis PT terhadap NSE adalah -0,298 dengan nilai p 0.059. Nilai
koefisien korelasi variabel faal hemostasis PT terhadap Cyfra 21-1 adalah -0,480
90
Nilai koefisien korelasi variabel faal hemostasis INR terhadap CEA adalah
-0,237 dengan nilai p 0.136. Nilai koefisien korelasi variabel faal hemostasis INR
terhadap NSE adalah -0,228 dengan nilai p 0.152. Nilai koefisien korelasi variabel
faal hemostasis INR terhadap Cyfra 21-1 adalah 0,010 dengan nilai p 0.951.
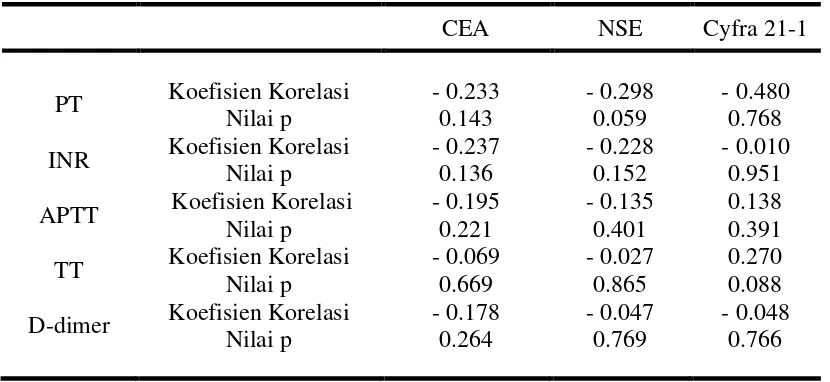
Tabel 4.5. Korelasi antara Nilai Parameter Hemostasis terhadap Tumor Marker pada
Pasien Kanker Paru Bukan Sel Kecil dengan Kemoterapi
CEA NSE Cyfra 21-1
Nilai koefisien korelasi variabel faal hemostasis APTT terhadap CEA adalah
-0,195 dengan nilai p 0.221. Nilai koefisien korelasi variabel faal hemostasis APTT
terhadap NSE adalah - 0.135 dengan nilai p 0.401. Nilai koefisien korelasi variabel
faal hemostasis APTT terhadap Cyfra 21-1 adalah 0.138dengan nilai p 0.391.
Nilai koefisien korelasi variabel faal hemostasis TT terhadap CEA adalah
-0,069 dengan nilai p 0.669. Nilai koefisien korelasi variabel faal hemostasis TT
terhadap NSE adalah -0.027 dengan nilai p 0.865. Nilai koefisien korelasi variabel
faal hemostasis TT terhadap Cyfra 21-1 adalah 0.270dengan nilai p 0.088.
Nilai koefisien korelasi variabel faal hemostasis D-dimer terhadap CEA adalah
-0,178 dengan nilai p 0,264. Nilai koefisien korelasi variabel faal hemostasis
D-dimer terhadap NSE adalah -0.047 dengan nilai p 0.769. Nilai koefisien korelasi
variabel faal hemostasis D-dimer terhadap Cyfra 21-1 adalah -0.048 dengan nilai p
0.766.
4.2. Pembahasan Penelitian
Pada penelitian ini ditemukan dari 41 sampel dengan tumor paru di RSUP
HAM yang menjalani kemoterapi 85 % berjenis kelamin laki-laki dan memiliki usia
rata-rata ± 57 tahun. Hal ini sesuai dengan beberapa literatur dan penelitian
sebelumnya yang menyebutkan prevalensi tumor paru juga lebih tinggi pada laki-laki
dan memiliki rata-rata usia diatas 40 tahun. (Faruk Tas et al, 2012). PDPI
menyebutkan pada pertengahan tahun 1990-an adenokarsinoma menjadi tipe histologi
kanker paru yang paling banyak pada laki-laki di Amerika Serikat. (Pdpi,2011).
Pada penelitian ini diperoleh jenis sel kanker adenokarsinoma mencapai 75%
dari seluruh sampel, dan 25 % lainnya adalah kanker jenis sel skuamous. Hal ini
sesuai dengan beberapa literatur dan penelitian sebelumnya juga melaporkan jenis
kanker paru terbanyak adalah adenokarsinoma. (Berna Komurcuoglu et al, 2011).
PDPI juga menyebutkan prevalensi jenis kanker sel adeno lebih tinggi dari sel
92
terbanyak yang dihisap pasien adalah kretek dengan isapan dalam, disebutkan bahwa
rokok kretek memiliki kandungan cengkeh, tar dan nikotin yang lebih tinggi dari
rokok putih, dan kebanyakan rokok kretek belum memiliki filter. Dengan kandungan
senyawa yang lebih banyak dan kebiasaan merokok dengan isapan dalam, maka
kecendrungan mendapatkan keganasan paru pada bagian bronkus bagian perifer
seperti adenokarsinoma semakin besar.
Dari follow-up 1 bulan pertama setelah kemoterapi diperoleh 2 (4,9%) pasien tanpa keluhan, 14 (34,1%) pasien dengan keluhan berupa disabilitas motorik dan
sisanya 25 pasien (61,0%) meninggal dunia. Pada follow-up 1 tahun setelah kemoterapi diperoleh 2 (4,9%) orang tanpa keluhan, 3 orang pasien (7,3%) dengan
disabilitas motorik, dan sisanya 36 (87,8%) pasien meninggal dunia. berdasarkan data
diatas diperoleh 1-year survival rate adalah 12,2 % Dalam sebuah penelitian yang dilakukan Salah Abbasi dan Ahmed Badheed di jordania menyebutkan pasien kanker
paru bukan sel kecilyang tidak diobati memiliki 1-year survival rate sebesar 10%, dengan kemoterapi angka ini meningkat menjadi 19-32%. Hasil yang berbeda ini
disebabkan karena pada penelitian tersebut pasien yang diikutkan pada peneliatian
tersebut datang dengan stage yang lebih rendah dan jenis obat kemoterapi yang digunakan yang terbanyak adalah docetaxel + platinum based dan docetaxel
monoterapi. (Salah Abbasi dan Ahmed Badheed, 2010)
Pada penelitian ini, disebutkan PT, INR, D-dimer dan NSE memiliki perbedaan
yang signifikan antara nilai sebelum kemoterapi dibandingkan dengan nilai variabel
ini setelah kemoterapi (nilai p < 0.05), dan tidak adanya perbedaan nilai yang
signifikan pada nilai sebelum dan sesudah kemoterapi pada variabel APTT, TT, CEA
dan Cyfra 21-1 (nilai p > 0.05). Sebuah penelitian yang dilakukan di Turki
menyebutkan nilai faal hemostasis PT, INR, APTT meningkat pada pasien kanker
paru yang jenis kelamin laki-laki dibandingkan dengan kelamin wanita, tetapi nilai ini
tidak berlaku pada nilai serum D-dimer. (Faruk Tas et al, 2012)
Pada penelitian ini diperoleh korelasi antara PT dengan tumor marker
memberikan hubungan terbalik yang lemah pada nilai CEA, NSE dan hubungan yang
moderat pada Cyfra 21-1 dengan nilai p yang tidak signifikan, hal ini menunjukkan
bahwa tidak ada hubungan yang nyata antara nilai PT dengan nilai tumor marker
pasien sebelum dan sesudah kemoterapi. Hasil ini sesuai dengan penelitian oleh
Faruk tas pada pasien dengan kanker yang menjalani kemoterapi menyebutkan PT
akan memanjang pada keadaan stadium lanjut (Faruk Tas et al,2012) dan sebagai
respon kemoterapi serum tumor marker akan menurun.(R Molina et al, 2003)
Korelasi antara INR dengan tumor marker memberikan hubungan terbalik yang
lemah pada nilai CEA, NSE, Cyfra 21-1 dengan nilai p yang tidak signifikan, hal ini
menunjukkan bahwa tidak ada hubungan yang nyata antara nilai INR dengan nilai
tumor marker pasien sebelum dan sesudah kemoterapi. Hasil ini sesuai dengan
penelitian oleh Faruk tas pada pasien dengan kanker yang menjalani kemoterapi
menyebutkan INR akan memanjang pada keadaan stadium lanjut dan sebagai respon
kemoterapi serum tumor marker akan menurun. (Faruk Tas et al, 2012), dan
94
kemoterapi lini pertama pada pasien-pasien kanker payudara. (Anthony Letai and
David J Kuter, 1999)
Pada penelitian ini diperoleh korelasi antara APTT dengan tumor marker
memberikan hubungan terbalik yang lemah pada nilai CEA, dan NSE dengan nilai p
yang tidak signifikan, hal ini menunjukkan bahwa tidak ada hubungan yang nyata
antara nilai APTT dengan nilai tumor marker pasien sebelum dan sesudah
kemoterapi. Hasil ini sesuai dengan penelitian sebelumya pada pasien dengan kanker
yang menjalani kemoterapi menyebutkan APTT akan memanjang pada keadaan
stadium lanjut (Faruk Tas et al, 2012, Slavica kvolik, 2010) dan sebagai respon
kemoterapi serum tumor marker akan menurun.(R Molina et al, 2003)
Korelasi APTT dengan Cyfra 21-1 memberikan hubungan lurus yang lemah
dengan nilai p yang tidak signifikan hal ini dimungkinkan karena diketahui bahwa
Cyfra 21-1 adalah marker yang kuat terhadap kanker paru tetapi marker ini tidak
memiliki nilai korelasi yang kuat pada salah satu jenis histologi kanker paru, tetapi
ada penelitian lain menyebutkan marker ini memiliki korelasi pada jenis histologi
karsinoma sel skuamous. Pada penelitian ini disebutkan bahwa jenis karsinoma
skuamous sel cukup sedikit. (R Molina et al, 2003, P.P. Mumbarkar et al, 2006)
Pada penelitian ini diperoleh korelasi antara TT dengan tumor marker
memberikan hubungan terbalik yang kurang berarti pada nilai CEA, dan NSE, dengan
nilai p yang tidak signifikan, hal ini menunjukkan bahwa tidak ada hubungan yang
nyata antara nilai TT dengan nilai tumor marker pasien sebelum dan sesudah
kemoterapi. Hasil ini sesuai dengan penelitian sebelumnya pada pasien dengan
kanker yang menjalani kemoterapi menyebutkan TT akan memanjang pada keadaan
stadium lanjut dan sebagai respon kemoterapi serum tumor marker akan menurun.
(Faruk Tas et al, 2012)
Korelasi TT dengan Cyfra 21-1 memberikan hubungan lurus yang lemah
dengan nilai p yang tidak signifikan dimana diketahui bahwa Cyfra 21-1 adalah
marker yang kuat terhadap kanker paru tetapi marker ini tidak memiliki nilai korelasi
yang kuat pada salah satu jenis histologi kanker paru, tetapi ada penelitian lain
menyebutkan marker ini memiliki korelasi pada jenis histologi karsinoma sel
skuamous. Pada penelitian ini disebutkan bahwa jenis karsinoma skuamous sel cukup
sedikit. (R Molina et al, 2003, P.P. Mumbarkar et al, 2006)
Pada penelitian ini diperoleh korelasi antara D-dimer dengan tumor marker
memberikan hubungan terbalik yang lemah pada nilai CEA, dan hubungan yang
kurang berarti dengan NSE, Cyfra 21-1 dengan nilai p yang tidak signifikan, hal ini
menunjukkan bahwa tidak ada hubungan yang nyata antara nilai D-dimer dengan
nilai tumor marker pasien sebelum dan sesudah kemoterapi. Hasil ini sesuai dengan
penelitian di Turki pada pasien dengan kanker yang menjalani kemoterapi
menyebutkan D-dimer akan memanjang pada keadaan stadium lanjut dan bila
ditemukannya adanya tanda-tanda metastasis (Berna Komurcuoglu et al, 2011) dan
sebagai respon kemoterapi serum tumor marker akan menurun. (R Molina et al,
96
Pasien kanker yang menjalani kemoterapi akan beresiko meningkatnya kejadian
koagulasi 16%,dan komplikasi tromboemboli akan meningkat pada 3 bulan pertama
kemoterapi. (Paolo Prandoni et al, 2005) Beberapa literatur juga menyebutkan bahwa
kemoterapi akan memperpanjang PT, APTT dan meningkatkan D-dimer setelah
kemoterapi dan membaik setelah 7 hari dan kembali seperti sebelum terapi 2 bulan
setelah siklus kemoterapi selesai. Penurunan sintesa antikoagulan oleh hati dan
penurunan fibronolisis oleh beberapa jaringan dapat terjadi selama kemoterapi.
(Slavica kvolik, 2010).
CEA, Cyfra 21-1, NSE telah lama digunakan untuk mengevaluasi terapi pada
kanker paru bukan sel kecil. Sebuah penelitian di china tahun 2011 oleh Hongbing
Liu dan kolega menyebutkan serum CEA akan secara signifikan berkurang setelah
dua siklus kemoterapi pada pasien dengan kanker paru bukan sel kecil. CEA dan NSE
memiliki korelasi yang lemah terhadap jenis kanker adenokarsinoma tetapi tidak
dengan Cyfra 21-1, walau ada beberapa penelitian menyebutkan Cyfra 21-1
berkorelasi lemah dengan karsinoma sel skuamous. (Hobgbing Liu, 2011)
Melihat respon variabel ini terhadap kemoterapi dapat disimpulkan adanya
hubungan terbalik pada kedua variabel ini dan hal ini juga ditemukan pada penelitian
ini. Dapat dimungkinkan nilai salah satu variabel dapat memprediksi nilai dari
variabel lainnya, hal ini dapat membantu para klinisi dalam menangani pasien kanker
paru bukan sel kecil di berbagai rumah sakit termasuk rumah sakit yang belum
memadai pemeriksaan penunjangnya dalam menilai prognostik pasien
BAB 5
KESIMPULAN DAN SARAN 5.1. Kesimpulan
Karakteristik 41 pasien kanker paru bukan sel kecil yang dilakukan kemoterapi
di Rumah Sakit Umum Pusat Haji Adam Malik Medan
1. Jenis Kelamin terbanyak adalah laki laki sebanyak 35 orang (85,4%)
2. Usia rata-rata sampel adalah 56,7 tahun, dimana 29 orang (70,7%) dengan
usia 40 sampai dengan 60 tahun,
3. Jenis Histologi terbanyak adalah adalah adeno karsinoma dengan 31 orang
(75%).
4. Tiga puluh lima orang (85,5%) adalah perokok.
5. Jenis kemoterapi terbanyak yang digunakan adalah kemoterapi lini pertama
dengan platinum based therapy dengan Gemsitabin dan Karboplatin pada 27 orang (65,9%).
6. Dari follow-up 1 bulan diperoleh 2 (4,9%) pasien tanpa keluhan, 14 (34,1%) pasien dengan keluhan berupa disabilitas motorik dan sisanya 25 pasien
(61,0%) meninggal dunia. Pada follow-up 1 tahun setelah kemoterapi diperoleh 2 (4,9%) orang tanpa keluhan, 3 orang pasien (7,3%) dengan
disabilitas motorik, dan sisanya 36 (87,8%) pasien meninggal dunia.
7. Tidak terdapat perbedaan yang signifikan dari nilai parameter hemostasis dan
98
ada peningkatan nilai PT, INR, APTT, TT, NSE sebelum dan sesudah
kemoterapi siklus 4 atau 6.
8. Terdapat korelasi negatif yang tidak bermakna pada nilai faal hemostasis dan
serum tumor marker.
9. Hasil yang berbeda terlihat antara APTT dengan Cyfra 21-1 dan TT dengan
Cyfra 21-1 dan NSE dimana terdapat korelasi positif yang bermakna.
5.2. Saran.
Masih dibutuhkan penelitian baru yang mampu menjelaskan korelasi parameter
hemostasis terhadap tumor marker berdasarkan jenis kelamin, usia, jenis histologi sel
dan jenis kemoterapi.