PENGARUH VARIASI METANOL DALAM SINTESIS MATERIAL SILIKA MENGGUNAKAN TETRAETILORTOSILIKAT (TEOS) DAN
TEMPLATE METIL ESTER RISINOLEAT
SKRIPSI
JESSICA MARDELA PAKPAHAN 140802067
PROGRAM STUDI S1 KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
MEDAN 2019
PENGARUH VARIASI METANOL DALAM SINTESIS MATERIAL SILIKA MENGGUNAKAN TETRAETILORTOSILIKAT (TEOS) DAN
TEMPLATE METIL ESTER RISINOLEAT
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
JESSICA MARDELA PAKPAHAN 140802067
PROGRAM STUDI KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
MEDAN 2019
PENGESAHAN SKRIPSI
Judul : Pengaruh Variasi Metanol Dalam Sintesis Material Silika Menggunakan Tetraetilortosilikat (TEOS) dan Template Metil Ester Risinoleat
Kategori : Skripsi
Nama : Jessica Mardela Pakpahan
NomorIndukMahasiswa : 140802067 Program Studi : Sarjana Kimia
Fakultas : MIPA - Universitas Sumatera Utara
Disetujui di Medan, Januari 2019
Ketua Program Studi Pembimbing
Dr. Cut Fatimah Zuhra, M.Si Dr.Andriayani, M.Si
NIP. 197404051999032001 NIP. 196903051999032001
PERNYATAAN ORISINALITAS
PENGARUH VARIASI METANOL DALAM SINTESIS MATERIAL SILIKA MENGGUNAKAN TETRAETILORTOSILIKAT (TEOS) DAN
TEMPLATE METIL ESTER RISINOLEAT
SKRIPSI
Saya menyatakan bahwa skripsi ini adalah hasil karya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Januari 2019
Jessica Mardela Pakpahan 140802067
PENGARUH VARIASI METANOL DALAM SINTESIS MATERIAL SILIKA MENGGUNAKAN TETRAETILORTOSILIKAT (TEOS) DAN
TEMPLATE METIL ESTER RISINOLEAT
ABSTRAK
Telah dilakukan sintesis material silika dengan menggunakan tetraetilortosilikat (TEOS) sebagai sumber silika, metil ester risinoleat sebagai template, 3- aminopropiltrimetoksisilana sebagai co-structure directing agent (CSDA), dan campuran deionized water dengan variasi massa metanol sebagai pelarutnya. Sintesis material silika dibuat dengan memvariasikan massa metanol yang dicampurkan dengan deionized water yaitu 1,2 g, 2,4 g, 3,6 g, 4,8 g dan 6 g. Campuran TEOS dan APMS dimasukkan kedalam campuran metil ester risinoleat, HCl 0,1 M, metanol dan deionized water lalu diaduk pada suhu kamar selama 2 jam. Campuran tersebut kemudian dimatangkan didalam oven pada suhu 80oC selama 72 jam. Pemisahan produk dilakukan dengan sentrifugasi, padatan yang dihasilkan dikeringkan lalu dikalsinasi pada suhu 550oC selama 6 jam. Hasil analisa XRD produk menunjukkan puncak difraksi yang melebar pada 12o sampai 38o yang menunjukkan bahwa material yang dihasilkan bersifat amorf. Spektrum FT-IR menunjukkan adanya gugus Si-OH dan Si-O-Si yang merupakan karakteristik material silika. Hasil analisa SEM menunjukkan adanya partikel berongga dengan ukuran yang tidak seragam seiring bertambahnya massa metanol. Adsorpsi desorpsi isoterm nitrogen (BET) menunjukkan kurva isoterm tipe IV dan hyteresis loop tipe H3 dengan ukuran pori dominan berturut-turut adalah 7,91 nm, 8,00 nm, 7,991 nm, 7,991 nm, dan 7,999 yang tergolong kedalam ukuran mesopori.
Kata kunci : APMS, mesopori silika, metanol, metil ester risinoleat, TEOS
THE EFFECT OF METHANOL VARIATION IN SILICA MATERIAL SYNTHESIS USE TETRAETHYLORTOSILICATE (TEOS) AND METHYL ESTER
RICINOLEIC AS TEMPLATE
ABSTRACT
Silica material has been synthesized with using tetraethylortisilicate (TEOS) as a silica source, methyl ester ricinoleic as template, 3-aminopropyltrimetoxysilane (APMS) as co-structure directing agent (CSDA), and a mixture of deionized water with methanol as a solvent. The synthesis of silica material was made with variation weight of methanol i.e. 1,2 g, 2,4 g, 3,6 g, 4,8 g and 6 g which mixtured with deionized water. A mixture of TEOS and APMS was added to a mixture of methyl ester ricinoleic, HCl o,1 M, methanol and deionized water then stirred at room temperature for 72 hours. For product separation was used with centrifugation, then the solids was dried and calcined at 550oC for 6 hours. The XRD analysis showed wide diffraction peak at 12oto 38o which indicated the material was amorphous. The FT-IR spectrum showed the Si-OH and Si-O-Si groups which indicated silica material characteristics. SEM analysis showed hollow particles with irregular size by increasing weight of methanol.
Adsorption desorption nitrogen isotherm (BET) showed an isotherm type IV curve and hysteresis loop type H3 with dominant pore size 7,91 nm, 8,00 nm, 7,991 nm, 7,991 nm, and 7,999 respectively and included to mesophorous size.
Keyword : APMS, methanol, methyl ester risinoleic, silica mesophorous, TEOS
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa dengan limpah karunia-Nya penulis dapat menyelesaikan penyusunan skripsi ini dengan judul Pengaruh Variasi Metanol Dalam Sintesis Material Silika Menggunakan Tetraetilortosilikat (TEOS) dan Template Metil Ester Risinoleat.
Dengan rasa hormat, penulis menyampaikan terima kasih kepada Ibu Dr.
Andriayani, S.Pd, M.Si selaku dosen pembimbing yang telah banyak membimbing dan memberi arahan kepada penulis selama penyusunan skripsi ini. Terimakasih kepada Ibu Dr. Cut Fatimah Zuhra, M.Si dan Ibu Dr. Sovia Lenny, M.Si selaku Ketua dan Sekretaris Program Studi Kimia FMIPA USU Medan, Dekan dan Wakil Dekan FMIPA USU, seluruh staf dan dosen bidang kimia anorganik, pegawai FMIPA USU, rekan- rekan kuliah dan terkhusus kepada rekan-rekan asisten laboratorium kimia anorganik.
Akhirnya tidak terlupakan kepada ayah W. Pakpahan dan ibu N. Tambun beserta seluruh keluarga yang selama ini memberikan bantuan yang diperlukan. Semoga Tuhan Yang Maha Esa membalasnya.
Medan, Januari 2019
Jessica Mardela Pakpahan
DAFTAR ISI
Halaman
PENGESAHAN SKRIPSI i
PERNYATAAN ORISINALITAS ii
ABSTRAK iii
ABSTRACT iv
PENGHARGAAN v
DAFTAR ISI vi
DAFTAR TABEL viii
DAFTAR GAMBAR ix
DAFTAR LAMPIRAN x
BAB 1 PENDAHULUAN 1.1 Latar Belakang 1
1.2 Permasalahan 3
1.3 Tujuan Penelitian 3
1.4 Manfaat Penelitian 3
1.5 Metodologi Penelitian 4
BAB 2 TINJAUAN PUSTAKA 2.1 Minyak Jarak 5
2.2 Ekstraksi 6
2.3 Esterifikasi 7
2.4 Metil Ester Risinoleat 8
2.5 Silika 9
2.6 Material Mesopori Silika 10
2.7 Karakteristik Mesopori Silika 11
2.7.1 Spektroskopi FT-IR (Fourier Transform Infrared) 11
2.7.2 Difraksi Snar-X (XRD) 12
2.7.3 Brunauer Emmet Teller (BET) Surface Area Analyzer 14
2.7.4 Metode Barret-Joyner-Halenda (BJH) 17
BAB 3 METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian 19
3.2 Alat dan Bahan 19
3.2.1 Alat 19
3.2.2 Bahan 19
3.3 Bagan Penelitian 21
3.3.1 Isolasi Minyak Jarak 21
3.3.2 Esterifikasi Minyak Jarak 22
3.3.3 Pembuatan Material Mesopori Silika 23
BAB 4 HASIL DAN PEMBAHASAN
4.1 Pembuatan Material Mesopori Silika 24
4.2 Karakterisasi Material Silika 26
4.2.1 Difraksi Sinar-X (XRD) 26
4.2.2 Spektrum FT-IR 27
4.2.3 Adsorpsi Desorpsi Isoterm Nitrogen (BET) 29
4.2.4 Mikroskop Elektron Skaning (SEM) 31
BAB 5 KESIMPULAN DAN SARAN
5.1 Kesimpulan 33
5.2 Saran 33
DAFTAR PUSTAKA 34
LAMPIRAN 38
DAFTAR TABEL Nomor
Tabel Judul Halaman
2.1 Sifat-sifat Silika 9
4.1 Massa Material Silika Setelah Kalsinasi 25
4.2 Luas Permukaan, Volume Pori dan Ukuran Pori Rata-rata
Material Silika 31
DAFTAR GAMBAR Nomor
Gambar Judul Halaman
2.1 Struktur Metil Ester Risinoleat 9
2.2 Refleksi Sinar X Pada Hukum Bragg 13
2.3 Klasifikasi Isoterm Adsorpsi 16
2.4 Klasifikasi Hysteresis Loop Adsorpsi 17
4.1 Material Silika Setelah Dikalsinasi dengan Variasi
Penambahan Metanol 24
4.2 Difraktogram XRD Material Silika 26
4.3 Spektrum FT-IR Tetraetilortosilikat 27
4.4 Spektrum FT-IR Metil Ester Risinoleat 28
4.5 Spektrum FT-IR Material Silika 28
4.6 Grafik Adsorpsi Desorpsi Isoterm Nitrogen 29
4.7 Grafik Distribusi Ukuran Pori 30
4.8 SEM Material Silika 32
DAFTAR LAMPIRAN Nomor
Lampiran
Judul Halaman
1 Difraktogram XRD Material Mesopori Silika MS Me 2 38
2 Difraktogram XRD Material Mesopori Silika MS Me 5 39
3 Data Analisa BET Material Mesopori Silika MS Me 1 40
4 Data Analisa BET Material Mesopori Silika MS Me 2 43
5 Data Analisa BET Material Mesopori Silika MS Me 3 46
6 Data Analisa BET Material Mesopori Silika MS Me 4 49
7 Data Analisa BET Material Mesopori Silika MS Me 5 52
8 Spektrum FT-IR Material Silika MS Me 2 55
9 Spektrum FT-IR Material Silika MS Me 5 56
10 Daftar Gambar-Gambar Penelitian 57
BAB 1 PENDAHULUAN
1.1 Latar Belakang
Material berpori menurut IUPAC dapat diklasifikasikan ke dalam 3 (tiga) kategori berdasarkan diameter porinya: (i) mikropori (d < 2 nm), (ii) mesopori ( 2 nm <
d < 50 nm), (iii) makropori ( d > 50 nm) (Kleitz et al., 2003; Lalena dan Clearly, 2005), sedangkan material berpori dengan diameter > 7500 nm disebut megapori (Vasant, et al., 1995).Ukuran molekul yang dilewatkan pada pori dan adsorpsi molekul yang masuk kedalam celah akan mempengaruhi peningkatan dan penurunan porositas, densitas, luas permukaan spesifik atau ukuran pori dan distribusi ukuran pori pada padatan berpori (Schubert and Hushing, 2006).
Sintesis material berpori dilakukan dengan penggabungan komponen anorganik dan komponen organik sebagai template berupa surfaktan kemudian dilakukan kalsinasi untuk menghilangkan komponen organiknya (Larsen, 2000).Template dipakai sebagai cetakan (pembantu dan pengarah) dalam pembentukan pori, dimana partikel koloidal primer akan mengisi celah-celah diantara susunan template, sehingga ketika template dihilangkan dari partikel silika, akan terbentuk partikel yang berongga (Yang, 2011).
Selain template pelarut juga dapat mempengaruhi karakteristik material silika, dimana semakin larut prekursor silika dalam pelarut yang digunakan makan laju hidrolisis dan kondensasi silika akan semakin baik (Anderson, 1998).
Penelitian tentang sintesis material silika dengan menggunakan pelaruttelah banyak dilakukan. Anderson, dkk (1998) mensintesis silika mesopori dengan template CTAB menggunakan campuran air dengan pelarut lainnya, yaitu dietil eter, etil asetat, THF, tetraglim, metilen klorida, 2-propanol, aseton, etanol, metanol, etilen glikol, asetonitril, gliserol, formamida, dan n-metil formamida. Hasilnya menjelaskan bahwa pelarut protik menurunkan ukuran partikel dan pelarut aprotik meningkatkan ukuran partikel.
Sadarsivan, dkk (1998) menggunakan 1-butanol, etanol, 2-propanol dan 1- propanol.Hasilnya menunjukkan bahwa ukuran partikel silika meningkat dengan meningkatnya berat molekul pelarut.Liu, dkk (2003) menggunakan template C16TMABr danetanoldenganvariasikonsentrasi. Hasilnya menunjukkan semakin tinggi konsentrasi etanol maka akan menghasilkan partikel berbentuk spherical. Lim, dkk (2012) menggunakanetanol, propanol, metanol dancampurannya.Hasilnya menunjukkan bahwa silika nanopartikel dihasilkan dengan menggunakan perbandingan pelarut etanol dengan metanol. Shokuhfar, dkk (2012) melakukan penelitian tentang pengaruh kadar etanol terhadap sifat nanostruktur dari silika lapis tipis dengan proses sol-gel. Hasilnya mengindikasikan bahwa dengan meningkatnya kadar etanol maka porositas lapisan silika akan meningkat serta semakin padat sekitar 3-4%.
Bao, dkk (2017) telah mensintesis silika dari TEOS dengan menggunakan template CTAB, menggunakan variasi etanol : air sebagai pelarutnya. Hasilnya menunjukkan diameter silika meningkat dan morfologi silika dari padat menjadi berongga dengan meningkatnya ratio etanol dalam air.Andriayani, (2013) menggunakan natrium risinoleat sebagai template dalam sintesis material mesopori silika. Hasilnya diperoleh material mesopori silika dengan distribusi ukuran pori dari 2,8-3,8 nm.
Dari uraian diatas peneliti tertarik untuk melakukan penelitian tentang pengaruh variasi metanol dalam sintesis material silika menggunakan tetraetilortosilikat (TEOS) danmetil ester risinoleat sebagai template. Metil ester risinoleat merupakan metil ester yang diperoleh dari hasil esterifikasi minyak jarak, dimana kandungan utama dari minyak jarak adalah asam risinoleat (Hosamani, 2003), yang memiliki gugus hidroksil pada atom C-12nya (Shombe, 2015). Ukuran pori dari silika dapat dimodifikasi dengan cara menambahkan template yang mengandung karbon (Sukalyan, 2008). Kepolaran pelarut juga mempengaruhi struktur material yang dihasilkan (Sinkó, 2010).Sumber silika seperti tetrametilortosilikat (TMOS) akan larut lebih baik dalam metanol, etanol, dan asetonitril dibandingkan dengan air. Sehingga akan mempengaruhi laju hidrolisis dan kondensasinya (Anderson, 1998).
Dalam penelitian ini digunakan tetraetilortosilikat sebagai sumber silika, metil ester risinoleat sebagai template, 3-aminopropiltrimetoksisilana (APMS) sebagai co- structure directing agent (CSDA), HCl 0,1 M dan campuran deionized water dengan variasi massa metanol sebagai pelarut. Selanjutnyauntukmenghilangkantemplate, material silika dikalsinasipadasuhu 550oC. Hasilnya diharapkan, mendapatkan material mesopori silika dengan keseragaman dan distribusi ukuran pori yang merata.
1.2 Permasalahan
Keseragaman dandistibusiukuranpori yang meratadari suatu material silika merupakan hal yang penting. Ukuran pori dari suatu material silika dapat dimodifikasi dengan penambahan template dan menggunakan pelarut. Berdasarkan penelitian terdahulu, penambahan pelarut ternyata dapat mempengaruhi karakteristik material silika yang dihasilkan.
Adapun permasalahan adalah sebagai berikut:
1. Bagaimana pengaruh variasi metanol dengan menggunakan metil ester risinoleat sebagai template terhadap sintesis material mesopori silika
2. Bagaimana karakteristik material mesopori silika yang diperoleh dari variasi metanol dengan menggunakan metil ester risinoleat sebagai template.
1.3 Tujuan Penelitian
1. Untuk mengetahui pengaruh variasi metanol dengan menggunakan metil ester risinoleat sebagai template terhadap sintesis material mesopori silika 2. Untuk mengetahui karakteristik material mesopori silika yang diperoleh dari
variasi metanol dengan menggunakan metil ester risinoleat sebagai template.
1.4 Manfaat Penelitian
Pemanfaatan metil ester risinoleat hasil esterifikasi minyak jarak dalam sintesis material mesopori silika.
1.5 Metodologi Penelitian
Kedalam beaker glass dimasukkan metil ester risinoleat dengan air demineralisasi. Kemudian ditambahkan metanol dan HCl 0,1 M lalu diaduk pada suhu kamar selama 30 menit. Dibuat campuran tertraetilortosilikat (TEOS) dan 3- aminopropiltrimetoksisilana (APMS) diaduk selama 10 menit, lalu campuran tertraetilortosilikat (TEOS) dan 3-aminopropiltrimetoksisilana (APMS) ditambahkan kedalam beaker glass yang berisi campuran metil ester risinoleat, metanol, HCl dan air demineralisasi sambil diaduk pada suhu kamar selama 2 jam. Dilakukan pematangan didalam oven (aging) pada suhu 80oC selama 72 jam. Produk dipisahkan pelarutnya dengan cara disentrifugasi lalu dicuci dan dikeringkan yang kemudian dikalsinasi pada suhu 550oC selama 6 jam. Dilakukan beberapa kondisi reaksi yaitu variasi penambahan metanol. Material silika yang dihasilkan dikarakterisasi menggunakan FT-IR, XRD, BET dan SEM.
BAB 2
TINJAUAN PUSTAKA
2.1 Minyak Jarak
Tanaman Jarak (Ricinus comunis Linn) termasuk dalam famili Euphorbiaceae, merupakan tanaman tahunan yang terdapat di daerah tropik maupun subtropik dan dapat tumbuh pada ketinggian 0-800 m diatas permukaan laut. Minyak jarak (castor oil) merupakan suatu senyawa trigliserida yang dapat dibedakan dengan gliserida lainnya dari komposisi asam lemaknya, viskositas, bilangan asetil dan kelarutannya dalam alkohol yang sangat tinggi. Biji jarak (Ricinus comunis Linn) mengandung 54% minyak yang disusun oleh beberapa jenis asam lemak sebagai trigliserida diantaranya asam risinoleat (75-87,5%), oleat (7-15%), linoleat (3,5-8%), asam palmitat (2-5%), asam stearat (0,5-2%), asam linolenat (0,5-2%) (Ketaren, 2008).
Minyak jarak berwarna kuning pucat, tetapi setelah dilakukan proses refining dan bleaching warna tersebut hilang sehingga menjadi hampir tidak berwarna. Minyak jarak ini dapat disimpan dan tidak mudah menjadi tengik. Kelarutannya dalam alkohol relatif tinggi, begitu juga di dalam eter, koloform, dan asam asetat glasial. Minyak jarak tidak larut dalam minyak mineral kecuali kalau dicampur dengan minyak tumbuhan lain.
Minyak jarak hampir keseluruhan berada dalam bentuk trigliserida, terutama risinolenin dengan asam risinoleat sebagai komponen asam lemaknya (Weiss, 1983).
Minyak jarak adalah minyak non edible yang memiliki potensi untuk menjadi bahan baku dalam bidang industri farmasi dan pertanian. Di samping itu, minyak jarak yang diperoleh dari biji Ricinus comunis merupakan sumber penting dalam produksi biodiesel. Biji jarak dapat menghasilkan 40-60% minyak jarak. Minyak jarak adalah minyak yang unik di antara minyak nabati karena satu-satunya sumber asam lemak terhidroksilasi (asam risinoleat) (Salihu, 2012).
Minyak jarak biasanya diperoleh melalui cara pengepresan atau ekstraksi pelarut terhadap biji tanaman jarak. Minyak jarak juga mempunyai sedikit sifat racun. Racun
tersebut terdapat dalam bentuk risin (suatu protein), risinin (suatu alkaloid) dan heat- stable allergen yang dikenal dengan CB-IA. Kandungan asam lemak esensialnya juga sangat rendah sehingga tidak dapat digunakan sebagai minyak makan dan bahan pangan (Kusumaningsih, 2006).
Asam risinoleat merupakan komposisi utama dari trigliserida minyak jarak yang memiliki struktur yang unik dibandingkan dengan asam lemak lainnya, yaitu turunan asam oleat (C18:1) yang jada posisi ɷ-7 memiliki gugus hidroksil serta mengandung ikatan π pada posisi ɷ-9 (Miller, 1984).
2.2 Ekstraksi
Ekstraksi adalah suatu proses pemisahan senyawa atau zat dari campurannya dengan menggunakan pelarut yang sesuai. Prinsip metode ini didasarkan pada distribusi zat terlarut dengan perbandingan tertentu antara dua pelarut yang tidak saling bercampur. Ekstraksi merupakan metode yang paling populer diantara berbagai jenis metode pemisahan karena metode ini dapat dilakukan baik dalam tingkat makro maupun mikro. Pada ekstraksi bertahap, setiap tahap ekstraksi digunakan pergantian pelarut sampai ekstraksi selesai. Jenis ekstraksi ini menggunakan alat berupa corong pisah (Yazid, 2005).
Proses ekstraksi dapat dilakukan dengan berbagai metode yaitu:
1. Maserasi
Maserasi merupakan cara penyarian sederhana yang dilakukan dengan cara merendam sampel dalam cairan penyari dan pengadukan pada temperatur kamar.
Cairan penyari akan menembus dinding sel atau masuk kedalam rongga sel yang mengandung zat aktif. Zat aktif tersebut akan larut karena adanya perbedaan konsentrasi antara larutan zat aktif didalam sel dengan yang diluar sel. Larutan yang lebih cepat (didalam sel) didesak keluar sel masuk kedalam larutan diluar sel. Peristiwa tersebut berulang sehigga terjadi kesetimbangan konsentrasi antara larutan diluar sel dan didalam sel. Keuntungan cara penyarian dengan maserasi adalah pekerjaan dan peralatan yang digunakan cukup sederhana.
2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang baru dan umumnya dilakukan pada temperatur ruangan. Prinsip perkolasi adalah serbuk ditempatkan dalam suatu bejana silinder yang bagian bawahnya diberi skat berpori. Cairan penyari dialirkan dari atas kebawah melalui serbuk kemudian melarutkan zat aktif dari sel yang dilalui sampai mencapai keadaan jenuh.
3. Sokletasi
Sokletasi adalah suatu metode pemisahan komponen dengan cara penyaringan berulang menggunakan pelarut sehingga semua komponen yang diinginkan akan terisolasi. Metode sokletasi berlangsung secara kontinu dengan jumlah pelarut relatif konstan dengan adanya pendingin balik.
4. Refluks
Metode refluks umumnya digunakan untuk sintesa senyawa anorganik dengan menggunakan pelarut senyawa yang volatil. Prinsip dari metode refluks ini adalah pelarut volatil mudah menguap pada temperatur yang tinggi, tetapi bila didinginkan dengan kondensor, pelarut yang tadi menguap akan mengembun pada kondensor dan turun lagi kedalam wadah reaksi sehingga pelarut akan tetap ada selama reaksi berlangsung (Sarker, 2006).
2.3 Esterifikasi
Esterifikasi adalah salah satu jenis reaksi dimana reaksi tersebut untuk menghasilkan ester. Ester merupakan sebuah hidrokarbon yang diturunkan dari asam karboksilat. Sebuah asam karboksilat mengandung gugus –COOH, dan pada sebuah ester, hidrogen di gugus ini digantikan oleh sebuah gugus hidrokarbon dari beberapa jenis. Reaksi langsung antara alkohol dengan asam karboksilat secara umum dibantu dengan katalis asam dapat berlangsung baik jika dilakukan pada suhu tinggi (Otera, 2003).
Reaksi esterifikasi akan berjalan lambat jika dilakukan tanpa menggunakan katalis. Untuk mendapatkan konversi yang tinggi dengan waktu yang relatif singkat
perlu adanya bantuan katalis. Reaksi dapat dijalankan dengan adanya katalis asam, katalis basa maupun enzimatik (Kimmel, 2004).
Reaksi transesterifikasi merupakan reaksi dari minyak atau lemak dengan alkohol untuk membentuk ester dan gliserol. Transesterifikasi tersiri dari tiga reaksi reversibel yaitu konversi trigliserida menjadi digliserida, digliserida menjadi monogliserida dan monogliserida menjadi metil ester dan gliserol (Frank, 2004).
Transesterifikasi dari minyak nabati menjadi metil ester asam lemak secara umum dapat menggunakan katalis basa seperti NaOH, KOH, dan alkoksidanya. Katalis basa mempunyai banyak keuntungan yaitu tidak korosif, ramah lingkungan dan menghasilkan sedikit masalah pembuangan. Sementara itu, lebih mudah memisahkannya dari larutan produk dan dapat dirancang untuk memberikan aktivitas tertinggi, selektivitas dan katalis dengan daya tahan yang lebih lama (Viswanathan, 2005).
2.4 Metil Ester Risinoleat
Asam risinoleat (asam 12-hidroksi-9-cis-oktadekanoat) merupakan salah satu asam lemak tak jenuh yang dapat diperoleh dari minyak biji tanaman jarak. Biji tanaman jarak dapat mengandung 40-60% minyak jarak dengan kandungan utama asam risinoleat hampir 90% (Salihu, 2012). Sumber lain asam risinoleat terdapat pada tanaman Alternanthera sessilis (Linn) R. Dengan kandungan sekitar 22,1% (Hosamani, 2003).
Tidak seperti asam lemak lainnya, asam risinoleat memiliki gugus fungsional hidroksil pada C-12 yang membuatnya lebih polar daripada kebanyakan asam lemak (Shombe, 2015). Untuk memisahkan asam risinoleat dengan asam lemak lainnya yang masih berada dalam bentuk trigliseridanya maka terlebih dahulu minyak jarak dimetilesterkan secara esterifikasi maupun interesterifikasi (Bailey’s, 1996).
Metil ester merupakan bahan yang dihasilkan dari reaksi kimia antara minyak nabati atau lemak hewani dengan alkohol.Alkohol yang paling banyak digunakan adalah metanol dan etanol. Reaksi yang melibatkan katalis umumnya basa kuat seperti natrium dan kalium hidroksida dan menghasilkan senyawa kimia baru disebut dengan metal ester yang kemudian dikenal sebagai biodiesel (Meher, 2004).
Metil risinoleat merupakan produk antara yang dapat diproses lebih lanjut untuk berbagai kegunaan dalam industri. Untuk mendapatkan metil risinoleat tersebut perlu dilakukan esterifikasi lemak/minyak. Esterifikasi dapat dilakukan dengan cara mereaksikan trigliserida atau asam lemak dengan alkohol (alkoholisasi) dengan bantuan katalis asam atau basa (Eckey, 1956).
Gambar 2.1 Struktur Metil Ester Risinoleat (Xu, 2015)
2.5Silika (SiO2)
Silika terdiri dari satu atom Si dan dua atom O, dimana Si memiliki nomor atom 14 dengan konfigurasi elektron [Ne] 3s23p2 sedangkan atom O memiliki nomor atom 8 dengan konfigurasi elektron 1s22s22p4 (Sudirham dan Utari, 2010).
Tabel 2.1. Sifat – sifat Silika (Iler, 1979)
Sifat Hasil
Berat Jenis (g/cm3) Bentuk
Daya larut dalam air
Titik cair (°C) ; Titik didih (°C) Kekerasan (Kg/mm2)
Kekuatan tekuk (MPa) Kekuatan tarik (MPa) Modulus elastisitas (GPa) Resistivitas (m)
Koordinasi geometri Struktur kristal
2,6 Padat Tidak larut 1610 ; 2230 650
70 110 73 - 75
>1014 Tetrahedral
Kristobalit, Tridimit, Kuarsa
Silika terbentuk melalui ikatan kovalen yang kuat serta memiliki struktur berupa empat atom oksigen yang terikat pada posisi sudut tetrahedral di sekitar atom pusat atom silikon (Cestari, 2000). Silika tersedia melimpah di bumi berupa senyawa murni maupun terikat pada oksida membentuk silikat. Dalam variasi bentuk amorf, silika sering digunakan sebagai desiccant, adsorben, filler, dan komponen katalis. Silika merupakan baha baku utama pada industri gelas, keramik, dan industri refraktori dan bahan baku yang penting untuk produksi larutan silikat, silikon dan alloy (Kirk-Othmer, 1967).
Silika juga dapat dibentuk dengan mereaksikan silikon dengan oksigen atau udara pada suhu tinggi (Iler, 1979).
2.6 Material Mesopori Silika
Material mesopori pertama sekali ditemukan oleh Kuroda Group dan Mobil Company awal tahun 1990 yaitu mensintesis material zeolit tunggal dengan melarutkan molekul organik dan ion logam sebagai pola (template) (Wang and Zhao, 2007).
Material yang dihasilkan menarik perhatian bagi peneliti-peneliti lain. Hal ini disebabkan ukuran pori melebihi zeolit konvensional dan dapat digunakan dalam berbagai bidang seperti katalisis dalam reaksi senyawa organik dan lain-lain.
Material mesopori silika untuk pertama kalinya disintesis pada tahun 1992 oleh para peneliti dari Mobile Corporation. Material tersebut akhirnya diberi nama Mobile Crystalline of Materials. Karakteristik material tersebut antara lain memiliki pori berbentuk heksagonal yang seragam (Alfaruqi, 2008). Interaksi antara komponen anorganik dan organik menentukan karakteristik struktur material silika. Jenis interaksinya tergantung pada tipe surfaktan yang digunakan, dapat berupa ikatan non kovalen lemah seperti ikatan hidrogen, gaya Van der Waals, dan ikatan elektrofalen (Wang and Zhao, 2007).
Karakteristik material mesopori meliputi : (1) keteraturan mesopori yang tinggi, (2) ukuran distribusi pori yang seragam, (3) luas permukaan yang besar (~1000 m2/g) dan volume pori (~1 cm3/g), (4) komposisi kimia yang dapat didisain dan permukaan yang dapat difungsionalisasi dan (5) ukuran yang dapat diatur.
Sintesis material mesopori berdasarkan pada kimia sol-gel.Dalam sistem sintesis, bahan anorganik (seperti tetraetilortosiliat, TEOS) pertama mengalami hidrolisis dan selanjutnya mengalami kondensasi ke dalam bentuk sol silika oligomer yang diikuti dengan transisi sol-gel yang menyebabkan kondensasi yang berkelanjutan, digabung dengan self-assembly surfaktan dan bahan anorganik membentuk mesostruktur.
Digunakan katalis asam atau basa untuk hidrolisis dan kondensasi prekursor silika, sehingga secara umum reaksi ini dilakukan pada kondisi asam atau basa.Sintesis mesopori silika dapat berhasil dipengaruhi oleh pemilihan surfaktan, kounter ion prekursor anorganik dan kondisi reaksi (Vasant, 1995).
Prinsip dasar kimia dalam proses sol-gel adalah transformasi Si-OR dan Si-OH menjadi senyawa siloksan melalui reaksi kondensasi. Dalam reaksi hidrolisis gugus Si- OR akan diubah menjadi Si-OH sedangkan dalam reaksi kondensasi terjadi pelepasan alkohol dan air (Schubert and Husing, 2005).
≡Si-OR + H2O ≡Si-OH + ROH Hidrolisis
≡Si-OH + ≡Si-OR ≡Si-O-Si≡ + ROH Kondensasi
≡Si-OH + ≡Si-OH ≡Si-O-Si≡ + H2O Kondensasi
Dalam kondisi asam, atom oksigen dari gugus Si-OH atau Si-OR diprotonasi dengan cepat pada tahap pertama. Gugus lepas (air dan alkohol) dihasilkan melalui protonasi. Densitas elektron ditarik dari atom pusat silika sehingga lebih elektrofilik dan membuatnya lebih mudah diserang oleh air dalam reaksi hidrolisis atau oleh gugus silanol dalam reaksi kondensasi.
2.7 Karakterisasi Material Silika
2.7.1 Spektroskopi FT-IR (Fourier Transform Infra Red)
Spektroskopi inframerah telah digunakan untuk analisis bahan di laboratorium selama lebih dari tujuh puluh tahun. Spektrum inframerah merupakan sidik jari dari sampel dengan puncak serapan yang sesuai dengan frekuensi getaran antara ikatan atom yang membentuk materi. Karena setiap perbedaan material adalah kombinasi unik dari atom, sehingga tidak ada dua senyawa menghasilkan spektrum inframerah yang sama.
Oleh karena itu, spektroskopi inframerah dapat menghasilkan identifikasi positif
(analisis kualitatif) dari setiap jenis materi yang berbeda. Selain itu, ukuran puncak dalam spektrum merupakan indikasi langsung dari jumlah material (Setyawan, 2013).
Teknik spektroskopi IR digunakan untuk mengetahui gugus fungsional, mengidentifikasi senyawa, menentukan struktur molekul, mengetahui kemurnian dan mempelajari reaksi yang sedang berjalan. Senyawa yang dianalisa berupa senyawa organik maupun anorganik. Hampir semua senyawa dapat menyerap radiasi inframerah (Mudzakir, 2013).
Metode spektroskopi IR banyak digunakan karena : - Cepat dan relatif murah
- Dapat digunakan untuk mengidentifikasi gugus fungsional dalam molekul - Spektrum inframerah yang dihasilkan oleh suatu senyawa adalah
khas dan oleh karena itu dapat menyajikan sebuah finger print (sidik jari) untuk senyawa tersebut (Setyawan, 2013).
Pancaran infra merah pada spektroskopi infra mera terbatas di antara 4000 cm-1 dan 400 cm-1 (2,5 – 15,0 μm), diserap oleh sebuah molekul organik dan diubah menjadi energi getaran molekul. Penyerapan ini juga tercantum, namun spektrum getaran tampak bukan sebagai garis-garis melainkan berupa pita-pita. Letak pita dalam spektrum inframerah disajikan sebagai bilangan gelombang atau panjang gelombang. Satuan bilangan gelombang yaitu per sentimeter (cm-1). Penetapan secara kualitatif dapat dilakukan dengan membandingkan tinggi peak (transmitansi) pada panjang gelombang tertentu yang dihasilkan oleh zat yang diuji dan zat yang standar. Dalam ilmu material analisa ini digunakan untuk mengetahui ada tidaknya reaksi atau interaksi antara bahan- bahan yang dicampurkan. Selain itu, nilai intensitas gugus yang terdeteksi dapat menentukan jumlah bahan yang bereaksi atau yang terkandung dalam suatu campuran (Silverstein, 1986).
2.7.2 Difraksi Sinar – X (XRD)
Difraksi sinar-x (X-Ray diffraction/XRD) merupakan salah satu metode karakterisasi material. Teknik ini digunakan untuk mengidentifikasi fasa kristalin dalam material dengan cara menentukan parameter struktur kisi serta untuk mendapatkaan
ukuran partikel. Difraksi sinar-x terjadi pada hamburan elastis foton-foton sinar-x oleh atom dalam sebuah kisi periodik. Hamburan monokromatis sinar x dalam fasa tersebut memberikan interferensi yang konstruktif. Dasar penggunaan difraksi sinar-x untuk mempelajari kisi kristal adalah berdasarkan persamaan Bragg (Cullity, 1978) :
n.λ = 2.d.sin θ ; n =1,2,…
Dimana :
λ : panjang gelombang sinar-x yang digunakan d : jarak antara dua bidang kisi
θ : sudut antara sinar datang dengan bidang normal n : bilangan bulat yang disebut sebagai orde pembiasan
Berdasarkan persamaan Bragg, ketika seberkas sinar-x menumbuk sampel kristal, maka bidang kristal itu akan mendifraksi sinar-x yang memiliki panjang gelombang sama dengan jarak antar kisi dalam kristal. Semakin banyak jumlah elektron yang terdapat disekeliling atom pada suatu bidang, makin besar intensitas pantulan yang disebabkan oleh bidang tersebut dan menyebabkan makin jelas spot yang terekam pada film. Dengan menggunakan suatu metoda yang dikenal dengan nama metoda sintesis Fourier, kita dapat menghubungkan intensitas spot dengan kepekatan distribusi elektron yang terdapat dalam unit sel. Dengan mengamati kepekatan distribusi elektron dalam unit sel, kita dapat menduga letak atom dalam unit sel tersebut. Atom akan terletak pada daerah-daerah yang mempunyai kepekatan distribusi elektron maksimum (Bird, 1993).
Persamaan Bragg dapat digambarkan seperti berikut :
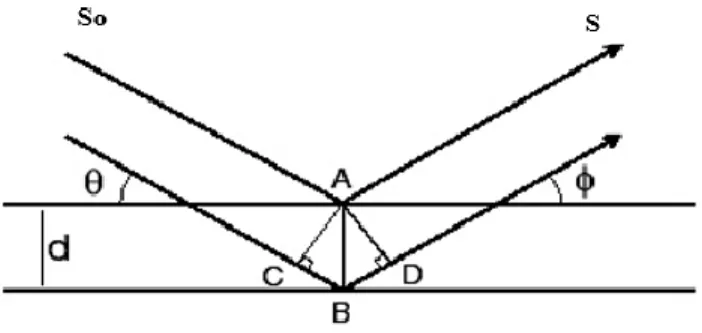
Gambar 2.2 Refleksi Sinar X pada Hukum Bragg (Eisenberg, 1979)
Dimana :
So : Sinar Datang S : Sinar Pantul A : Lapisan atas benda B : Lapisan bawah benda d : diameter benda
2.7.3 Brunauer Emmet Teller (BET) Surface Area Analyzer
Teori BET adsorpsi multilayer untuk menentukan luas permukaan (S) dikembangkan oleh Brunauer, Emmet dan Teller. Proses adsorpsi digambarkan sebagai proses lapisan dengan lapisan (layer-by-layer), permukaan secara energetik dianggap homogen, medan adsorpsi sama dalam setiap tempat permukaan, serta proses adsorpsi dianggap tidak bergerak (setiap molekul yang diadsorpsi pada sisi dasar permukaan).
Lapisan pertama molekul yang diadsorpsi memiliki energi interaksi dengan medan adsorp (Ea0) dan interaksi vertikal antara molekul setelah lapisan pertama (EL0) sama terhadap panas liqufaksi adsorbat dan molekul yang diadsorpsi tidak berinteraksi secara menyamping (Roque-Malherbe, 2007).
Metode BET tidak tepat untuk perhitungan mikropori, karena ketika metode ini diterapkan pada adsorben mikro maka akan terjadi penyerapan pada tekanan yang relatif rendah sehingga memungkinkan volume monolayer yang dihitung lebih dari satu lapisan terserap. Jika nilai ini diubah menjadi luas permukaan BET maka nilai yang dihasilkan akan lebih besar dari nilai yang sebenarnya. Meskipun metode BET tidak menggambarkan keadaan yang sebenarnya, namum metode ini yang lebih umum digunakan untuk analisa isoterm adsorpsi. Ini disebabkan metode BET relatif sederhana dan dianggap memberikan kapasitas adsorpsi yang baik dari adsorben yang digunakan (Kanellopoulos, 2011).
Untuk menentukan luas permukaan, didasarkan dari data isoterm physorption, menggunakan persamaan BET berikut ini (Gregg, 1982):
1
W[(PoP)-1)]
=
WmC1+
WmC(C-1).
ppo...(1)Dimana :
W = Berat gas yang diserap (adsorbed) pada tekanan relatif P/P0
Wm = Berat gas nitrogen (adsorbate) yang membentuk lapisan monolayer pada permukaan zat.
P = Tekanan kesetimbangan adsorb
Po = Tekanan penjenuhan adsorpsi-desorpsi cuplikan pada suhu rendaman pendingin
C = Konstanta energi
Persamaan BET (1) akan merupakan garis lurus bila dibuat grafik 1/[W(P/Po-1)]
versus P/Po. Prosedur standar multipoint BET diperlukan minimal 3 titik kisaran tekanan relatif yang tepat. Berat gas nitrogen yang membentuk lapisan tipis monolayer (Wm) dapat ditentukan dari slope (s) dan intersep (i) pada grafik BET dari persamaan (1) didapatkan :
Slope, s= C-1
WmC ...(2) Intersep, i=WmC1 ... (3)
Berat gas nitrogen yang dapat membentuk lapisan tipis (Wm) didapatkan dari menggabungkan persamaan (2) dan (3) sehingga diperoleh :
Wm= 1
s+i ... (4) Selanjutnya pada aplikasi metode BET adalah menghitung luas permukaan.
Untuk itu perlu diketahui luas permukaan cross section dari molekul gas nitrogen (adsorben), Luas permukaan total (St) dari cuplikan adalah :
St=(Wm×Nacs)
M ...(5) Dimana :
N = bilangan Avogadro (6,203 × 1023) M = berat molekul dari gas nitrogen Wm = berat gas nitrogen (gram)
acs = Cross section area untuk nitrogen
Luas permukaan spesifik (S) dapat dihitung dari luas permukaan total (St) dibagi dengan berat cuplikan (bc) sehingga didapat persamaannya sebagai berikut :
S=St
bc ...(6) Dimana :
St = Luas permukaan total (m2/g) S = Luas permukaan spesifik (m2/g) bc = Berat cuplikan (g)
Tipe adsorpsi isoterm dapat dikelompokkan menjadi enam tipe seperti yang ditunjukkan pada gambar 2.2.
Gambar 2.3 Klasifikasi Isoterm Adsorpsi
Isoterm tipe I merupakan karakteristik untuk material mikropori.Tipe II merupakan tipe untuk material nonpori, mikropori dan makropori. Tipe III menunjukkan karakteristik material yang interaksi antara adsorbat dan adsorben nya sangat lemah.
Tipe IV merupakan tipe material berpori yang mana pada tekanan yang lebih tinggi akan menunjukkan hysteresis loop. Tipe V merupakan karakteristik material yang interaksi antara adsorbat dan adsorben nya sangat lemah tetapi pada tekanan yang lebih tinggi
akan menunjukkan hysteresis loop. Tipe VI ditujukan untuk material yang adsorpsi nya terjadi pada setiap lapisan permukaan material tersebut.
Klasifikasi hysteresis loop dibagi menjadi 4 tipe seperti pada gambar 2.3
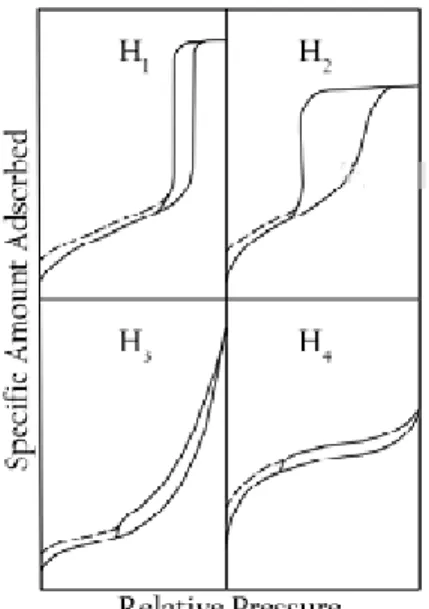
Gambar 2.4 Klasifikasi Hysteresis Loop Adsorpsi
Tipe H1 merupakan tipe untuk material dengan ukuran pori yang seragam. Tipe H2 merupakan tipe material dengan bentuk dan/atau ukuran pori yang tidak seragam, contohnya silika gel atau logam oksida. Tipe H3 menunjukkan material yang memiliki pori berbentuk celah. Hal ini dikarenakan adanya aglomerat dari partikel yang berbentuk plat. Tipe H4 hampir sama dengan H3 tetapi memiliki plat yang lebih horizontal/tipis yang artinya material tersebut merupakan mikropori (Bjork, 2013).
2.7.4 Metode Barret-Joyner-Halenda (BJH)
Metode BJH digunakan untuk menentukan distribusi ukuran pori/particle size distribution (PSD). Tekanan relatif awal proses desorpsi dalam metode Barret-Joyner- Halenda (BJH) berlangsung pada range 0,9< P/Po < 0,95 dan semua pori telah diisi fluida adsorbat. Pada tahap pertama (j=1) dalam proses desorpsi hanya melibatkan pemindahan kondensasi kapiler. Tahap berikutnya melibatkan pemindahan kondensat
dari inti pori dan penipisan multilayer dalam pori yang lebih besar (misalnya pori telah siap dikosongkan dari kondesat).
Distribusi ukuran pori Barret-Joyner-Halenda (BJH-PSD) dapat dihitung menggunakan persamaan berikut ini (Roque-Malherbe, 2007).
Vpn=( rpn
rKn+ ∆tn 2
)
2
(∆V(n)-∆tn∑ Acn-1j=1 j) ……….. (7)
Keterangan :
Vpn : volume pori pada berbagai tekanan relatif rP : jari-jari pori
rK : jari-jari inti
∆V : perubahan volume pada berbagai tekanan relatif
∆𝑡: ketebalan lapisan yang diserap Ac : area terbuka pori yang kosong
BAB 3
METODE PENELITIAN
3.1 Waktu dan Tempat Penelitian
Penelitian ini dilakukan dari bulan Maret 2018 sampai September 2018 di Laboratorium Kimia Anorganik FMIPA USU, Medan. Analisa FT-IR di lakukan di Laboratorium Organik FMIPA Universitas Gadjah Mada, Yogyakarta. Analisa BET di lakukan di Laboratorium Terpadu Universitas Islam Indonesia, Yogyakarta. Analisa XRD dan SEM dilakukan di Laboratorium Teknik Material Institut Teknologi Sepuluh November, Surabaya.
3.2 Alat dan Bahan 3.2.1 Alat
Peralatan Gelas Pyrex
Furnace 1100oC Fischer
Oven 360oC
Hotplate Stirrer
Neraca Analitis AS 220/C/2 Radwag
Kertas Saring N0. 42 Whatmann
Centrifuge
Magnetic Bar
Difraktometer Sinar-X PW 1710 Philip
Spektrofotometer FT-IR 983 Prestige 21 Shimadzu
Surface Area Meter Sorptomatic 1800
Scanning Electron Microscopy JSM-7000F JEOL
3.2.2Bahan
Minyak jarak yang diperoleh dengan cara ekstraksi maserasi langsung dari biji jarak risinus yang diperoleh dari Dolok Sanggul, Sumatera Utara
Etanol p.a Merck
Metanol p.a Merck
KOH p.a Merck
N-heksan p.a Merck
3-aminopropiltrimetoksisilana (APMS) p.a Merck
Tetraetilortosilikat (TEOS) Sigma Aldirch
HCl p.a Merck
Deionized Water HACH
3.3 Bagan Penelitian 3.3.1 Ekstraksi Minyak Jarak
3.3.2Esterifikasi Minyak Jarak dengan Metanol Menggunakan Katalis KOH
(Sembiring, 2018)
3.4.3 Pembuatan Material Silila
Dilakukan prosedur yang sama untuk variasi massa metanol : 2,4 g, 3,6 g, 4,8 g dan 6 g.
BAB 4
HASIL DAN PEMBAHASAN
4.1 Pembuatan Material Silika
Material silika yang dibuat dari tetraetilortosillikat (TEOS), metil ester risinoleat, 3-aminopropiltrimetoksisilana (APMS) dengan penambahan HCl 0,1 M dan campuran deionized water dengan metanol sebagai pelarut dilakukan dengan memvariasikan metanol mulai dari 1,2 g, 2,4 g, 3,6 g, 4,8 g, dan 6 g.
Reaksi yang terjadi adalah sebagai berikut (Andriayani, 2013) :
Produk material silika yang dihasilkan setelah dikalsinasi pada suhu 550oC berupa padatan putih yang terlihat pada gambar 4.1
a b c
CH3OH
Gambar 4.1 Material Silika Setelah Kalsinasi dengan Variasi Penambahan Metanol (a)1,2 g, (b) 2,4 g, (c) 3,6 g, (d) 4,8 g, (e) 6 g
Pada gambar 4.1 ditunjukkan hasil berupa padatan putih kering yang sudah bebas dari bahan organik (template) yaitu metil ester risinoleat dan gugus amina dari APMS setelah dilakukan kalsinasi material silika pada suhu 550oC. Material silika yang dihasilkan memiliki massa yang ringan, dan tekstur yang berbeda-beda. Berdasarkan gambar 4.1 semakin banyak jumlah metanol yang ditambahkan maka semakin banyak pula massa silika yang dihasilkan dan teksturnya semakin berbentuk bongkahan.
Tabel 4.1 Massa material mesopori silika yang dihasilkan setelah dikalsinasi pada suhu 550oC
Metanol (gram) Material Silika (gram)
1,2 1,63
2,4 1,7
3,6 1,8
4,8 2,03
6 2,1
Hal ini sesuai dengan literatur (Anderson, 1988) yaitu semakin banyak massa metanol yang ditambahkkan maka tetraetilortosilikat akan semakin larut yang menyebabkan meningkatnya laju hidrolisis dan kondendasinya sehingga jaringan silika yang terbentuk semakin banyak.
d e
4.2 Karakterisasi Material Silika
Untuk membuktikan bahwa material yang terbentuk merupakan silika, maka dilakukan beberapa karakterisasi berikut.
4.2.1 Difraksi Sinar-X (XRD)
Material silika yang dihasilkan dikarakterisasi dengan analisa XRD untuk mengidentifikasi bentuk dari material silika yang dihasilkan sehingga diperoleh pola difraksi dari silika pada sudut 2θ seperti yang terlihat pada gambar berikut.
Gambar 4.2 Difraktogram XRD Material Silika Perbandingan Metanol 2,4 g (Me 2) dengan Metanol 6 g (Me 5)
Dari gambar 4.2 dapat dilihat difraktogram XRD pada sudut 2θ yang melebar antara 12o sampai 38o. Puncak difraksi yang melebar dari material silika dengan metanol 2,4 g (Me 2) dan metanol 6 g (Me 5) berturut-turut terdapat pada sudut 22,71o dan 22,36o yang menunjukkan bahwa material yang dihasilkan merupakan silika dan
memiliki struktur amorf. Hal ini sesuai dengan data yang dijumpai pada literatur (Bao, 2017 ; Zhao, 2011).
4.2.2 Spektrum FT-IR
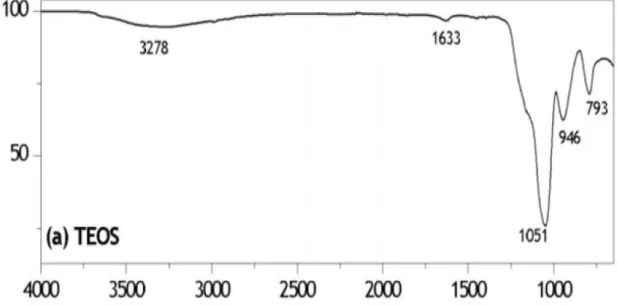
Material silika yang diperoleh dianalisis dengan FT-IR untuk mengetahui ada tidaknya terbentuk gugus fungsi yang membuktikan bahwa material yang dihasilkan adalah silika. Spektrum FT-IR dari material silika yang sudah dikalsinasi dapat dilihat pada gambar 4.5 dan untuk spektrum TEOS dan metil ester risinoleat yang digunakan sebagai senyawa pembanding dapat dilihat pada gambar 4.3 dam 4.4.
Gambar 4.3 Spektrum FT-IR Tetraetilortosilikat (Wencel, et al., 2013)
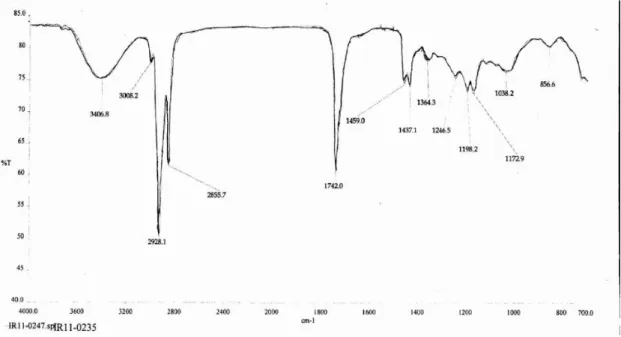
Gambar 4.4 Spektrum FT-IR Metil Ester Risinoleat (Goswami, A., 2011)
Gambar 4.5 Spektrum FT-IRMaterial Silika Perbandingan Metanol 2,4 g (Me 2) dan Metanol 6 g (Me 5)
Gambar 4.5 menunjukkan bahwa metil ester risinoleat yang digunakan sebagai template telah hilang saat dikalsinasi. Hal ini dilihat dari tidak adanya serapan C=O pada rentang 1700-1725 cm-1 dan serapan C=C pada rentang 1640-1680 cm-1 seperti yang terdapat pada gambar 4.4. Dari gambar 4.5 juga dapat dilihat puncak serapan pada bilangan gelombang 3432,6 cm-1 yang menunjukkan adanya gugus –OH (Si-OH).
Puncak serapan lain terdapat pada bilangan gelombang 1097,5 cm-1 yang menunjukkan adanya gugus asimetris Si-O-Si dan puncak pada bilangan gelombang 805,7 cm-1 yang menunjukkan adanya gugus simetris Si-O-Si. Dengan demikian, data IR material silika (Me 2 dan Me 5) sudah sesuai dengan literatur (Zhao, 2011 ; Silverstein, 1986) dan dapat disimpulkan bahwa material yang terbentuk merupakan silika.
4.2.3 Adsorpsi Desorpsi Nitrogen Isoterm
Untuk mengukur porositas dan distribusi ukuran pori material silika yang dihasilkan maka dilakukan adsorpsi desorpsi terhadap nitrogen secara isoterm dan hasilnya terlihat seperti gambar 4.6 berikut.
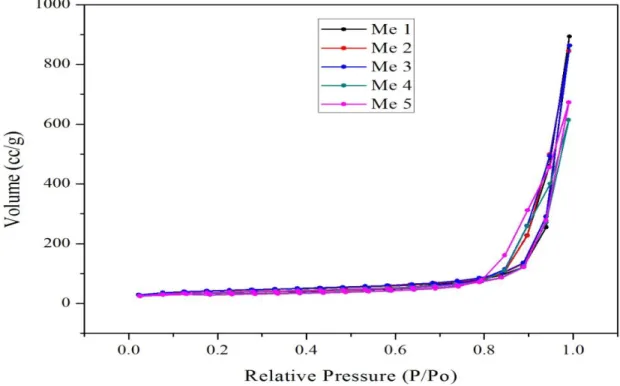
Gambar 4.6 Grafik Adsorpsi Desorpsi Isoterm Nitrogen
Grafik adsorpsi desorpsi nitrogen isoterm material silika seperti terlihat pada gambar 4.6 menunjukkan adanya pori pada variasi penambahan metanol dari 1,2 g – 6 g.
Grafik adsorpsi desorpsi isoterm pada gambar 4.6 menunjukkan material silika dengan kurva isoterm tipe IV dan hysteresis loop tipe H3, yang artinya material yang dihasilkan memiliki pori-pori berbentuk celah dari aglomerat partikel yang berbentuk plat (Bjork, 2013). Hal ini menunjukkan bahwa karakteristik material silika yang dihasilkan memiliki luas permukaan yang besar.Grafik adsorpsi desorpsi isoterm material silika dengan jumlah metanol 1,2 g (Me 1) – 4,8 g (Me 4) menunjukkan hysteresis loop pada tekanan relatif (P/P0) antara 0,837 – 0,896, sedangkan pada jumlah metanol 6 g (Me 5) menunjukkan hysteresis loop pada tekanan relatif (P/P0) antara 0,789 – 0,99.
Distribusi ukuran pori dari material silika yang dihasilkan dapat dilihat pada gambar berikut ini
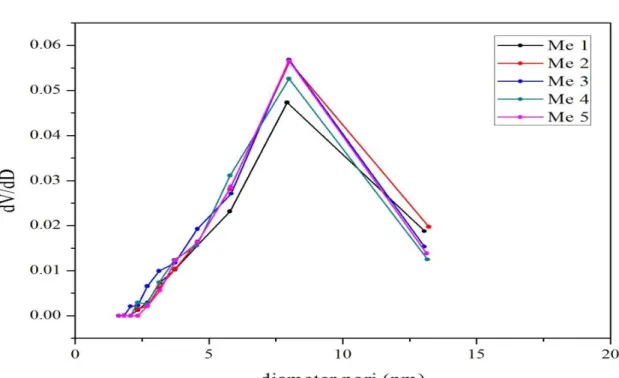
Gambar 4.7 Grafik Distribusi Ukuran Pori
Pada gambar 4.7 terlihat beberapa puncak yang hampir sama dari kelima material silika yang dihasilkan yang menandakan pori yang terbentuk cukup seragam.
Diameter ukuran pori yang dihasilkan mulai dari 1,63 nm – 13,15 nm sehingga dapat digolongkan kedalam ukuran mikropori dan mesopori. Ukuran pori yang dominan untuk variasi penambahan metanol 1,2 g, 2,4 g, 3,6 g, 4,8 g, dan 6 g berturut-turut adalah 7,91 nm, 8,00 nm, 7,991 nm, 7,991 nm, dan 7,999 yang tergolong kedalam ukuran mesopori.
Luas permukaan, volume pori dan ukuran pori rata-rata dari kelima material silika yang dihasilkan dapat dilihat pada tabel berikut.
Tabel 4.2 Luas Permukaan, Volume Pori dan Ukuran Pori Rata-Rata Material Silika Luas Permukaan
(m2/g)
Volume Pori (cc/g)
Ukuran Pori Rata-Rata (nm)
MS Me 1 (Metanol 1,2 g) 142,122 0,395 5,56
MS Me 2 (Metanol 2,4 g) 144,8 0,45 6,26
MS Me 3 (Metanol 3,6 g) 147,76 0,45 6,09
MS Me 4 (Metanol 4,8 g) 127,44 0,42 6,59
MS Me 5 (Metanol 6 g) 122,65 0,42 7,01
Berdasarkan tabel 4.2 diperoleh ukuran pori rata-rata dari kelima material silika yang dihasilkan yaitu 5,56 nm – 7,01 nm sehingga digolongkan kedalam ukuran mesopori.
4.1.4 Mikroskop Elektron Skaning (SEM)
Dari data adsorpsi desorpsi isoterm nitrogen, dapat disimpulkan bahwa material silika yang dihasilkan memiliki pori. Maka untuk mengetahui morfologi material silika dilakukan analisa foto SEM dengan perbesaran 20.000 dan 30.000 kali. Hasilnya terlihat pada gambar berikut ini.
Gambar 4.8 SEM Material silika dengan variasi metanol 2,4 g (a) 20.000 kali, (b) 30.000 kali dan metanol 6 g (c) 20.000 kali, (d) 30.000 kali
Pada gambar 4.8 (a) yaitu material silika dengan metanol 2,4 g perbesaran 20.000 kali terlihat bentuk partikel material silika yang berbentuk bulat tipis yang tersebar secara acak dan pada gambar 4.8 (b) terlihat lebih jelas bentuk partikelnya, sedangkan gambar 4.8 (c) yaitu material silika dengan metanol 6 g perbesaran 20.000 kali terlihat material silika berbentuk bulat berongga, dan pada gambar 4.8 (d) perbesaran 30.000 kali terlihat lebih jelas bentuk partikelnya. Hal ini menunjukkan bahwa semakin banyak jumlah metanol yang digunakan maka akan menghasilkan material silika yang berongga.
a b
c d
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Pengaruh variasi metanol terhadap sintesis material silika dengan menggunakan template metil ester risinoleat yaitu semakin banyak jumlah metanol yang ditambahkan maka akan semakin banyak pula massa silika yang dihasilkan. Massa silika yang dihasilkan berturut-turut adalah 1,63 g, 1,7 g, 1,8 g, 2,03 g dan 2,1 g.
2. Karakteristik material silika yang dihasilkan adalah sebagai berikut :
Difraktogram XRD pada sudut 2θ yang melebar antara 12o sampai 38o dan puncak difraksi material silika dengan metanol 2,4 g (Me 2) dan metanol 6 g (Me 5) berturut-turut terdapat pada sudut 22,71o dan 22,36o yang menunjukkan bahwa material yang dihasilkan adalah silika dan memiliki struktur amorf.
Spektrum FT-IR menunjukkan adanya gugus silanol (Si-OH) dan gugus siloksan (Si-O-Si) yang menunjukkan karakteristik silika.
Grafik adsorpsi desorpsi nitrogen menunjukkan kurva isoterm tipe IV (material yang dihasilkan merupakan mesopori) dan hysteresis loop tipe H3 (pori berbentuk celah). Ukuran pori yang dominan adalah 7,91 nm, 8,00 nm, 7,991 nm, 7,991 nm, dan 7,999 yang tergolong kedalam ukuran mesopori.
Foto SEM menunjukkan adanya partikel yang tersebar secara acak dan dengan meningkatnya jumlah metanol akan menghasilkan silika yang berongga.
5.2 Saran
Saran untuk peneliti selanjutnya untuk mencoba pelarut alkohol lain untuk melihat apakah lebih baik dalam meningkatkan laju hidrolisis dan kondensasi dari TEOS.
DAFTAR PUSTAKA
Alfaruqi, H., 2008. Teknologi Nano. Jakarta : FT UI. Halaman 1.
Anderson, M. T., Martin, J. E., Odinek, J. G., Newcomer, P. P., 1998. Surfactant- Templated Silica Mesophases Formed in Water:Cosolvent Mixtures. Chem.
Mater:1998, 10, 311-321. American Chemical Society.
Andriayani, Sembiring, S. B., Aksara, N., Sofyan, N., 2013. Synthesis of Mesoporous Silica from Tetraethylortosilicate by Using Sodium Risinoleic as a Template and 3-amonipropyltrimethoxysilane as Co-Structure Directing Agent with Volume Variation of Hydrochloric Acid 0,1 M. Advanced Materials Research Vol 789 pp 124-131. Trans Tech Publication, Switzerland.
Bailey’s, 1996. Industrial Oil and Fats Products. Vol. 1. New York : John & Wiley Sons Inc.
Bao, Y., Wang, T., Kang, Q., Shi, C., Ma, J., 2017.Micelle-template Synthesis of Hollow Silica Spheres for Improving Water Vapor Permeability of Waterbone Polyurethane Membrane. Scientific Reports.
Bird, T. 1993. Kimia Fisik Untuk Universitas. Cetakan Kedua. PT Gramedia Pustaka Utama. Jakarta.
Bjork, E. M., 2013. Mesoporous Building Blocks-Synthesis and Characterization of Mesoporous Silica Particles and Films. Sweden : Linkoping Univesity.
Cestari, A.R., Vieira, E.F.S., Simoni, J.A., Airoldi,C., 2000. Thermpchemical Investigation on the Adsorption of Some Divalent Cations on Modified Silicas Obtained feom Sol-gel Process. Thermochimica Acta. 25 – 31.
Cullity, B.D., 1978. Elements of X-Ray Diffraction. Second Edition.Canada :AddisonWesleyPublishing Company Inc.
Eckey, E. V., 1956. Esterification and Interesterification. JAOCS, 33 (11) : 575-579.
Eisenberg, D., and Crothers, D., 1979. Physical Chemistry With Application to The Life Sciences. The Benjamin/Cumming Publishing Company, Inc. California Frank, G., 2004. The Chemistry of Oil and Fats. Publish in USA and Canada.
Goswami, A., 2011. An Alternative Eco-Friendly Avenue for Castor Oil Biodiesel : Use of Solid Supported Acidic Salt Catalysts. Research Gate.
Gregg, S.J., and Sing, K.S.W., 1982. Adsorpsi, Surface and Porosity, 2 ed. London : AcademicPress
Hosamani, K. M., Ganjihal, S. S., Chavadi, D. V., 2003.,Alternanthera Triandra Seed Oil : A Moderate Source of Ricinoleic Acid And It’s Possible Industrial Utilisation. Journal Crops and Products, 19 : 133-136.
Iler, R.K., 1979. Silica Gels and Powders. New York : The Chemistry of Silica.
Kanellopoulos, N., 2011. Nanoporous Materials: Advanced Techniques for Characterization, Modelling, and Processing. CRC Press Taylor & Francis Group. New York
Ketaren, S., 2008. Pengantar Teknologi Lemak dan Minyak Pangan. Jakarta : UI- Press.
Kimmel, T., 2004. Kinetic Investigation of The Base-Catalyzed Glyserolisis of Fatty Acid Methyl Ester. Genehmigte Dissertation. Berlin : Technischen Universitat Berlin.
Kirk-Otmer. 1967.,Encyclopedia of Chemical Technology. New York. Interscience Publisher.
Kleitz, F., Liu, D., Anilkumar, G. M., Park, I. S., Solovyov, L. A., Shmakov, A. N.
And Ryoo, R., 2003. Large Cage Face-Centered-Cubic Fm3m Mesoporous Silica: Synthesis and Structure. J. Phys. Chem. B., 107 (51), 14296-14300.
Kusumaningsih, T., Pranoto, Saryoso, R., 2016. Pembuatan Bahan Bakar Biodiesel dari Minyak Jarak; Pengaruh Suhu dan Konsentrasi KOH Pada Reaksi Transesterifikasi Berbasis Katalis Basa. FMIPA Universitas Sebelas Maret (UNS). Surakarta : ISSN 0216-6887.
Lalena, J. N., and Clearly, D. A., 2005. Principles of Inorganic Design. John Wiley &
Sons Inc. 86-88.
Larsen, R. B., Polve, M., Juve, G., 2000. Granite Pegmatite Quartz from Evjelveland, Trace Element Chemostry and Implications for The Formation of High Purity Quartz. Norges Geologiske Undersogelse Bulletin 436, 57-65.
Lim, J., Ha, S., Lee, J., 2012. Precise Size-control of Silica Nanoparticles via Alkoxy ExchangeEquilibrium of Tetraethyl Orthosilicate (TEOS) in the Mixed Alcohol Solution. Bull. Korean Chem. Sic. 2012, Vol. 33, No. 3 1067.
Liu, S., Cool, P., Collart, O., Voort, P., Vansant, E. F., Lebedev, O. I., Tandeloo, G. V., Jiang, M., 2003. The Influence of the Alcohol Concentration on the StructuralOrdering of Mesoporous Silica: Cosurfactant versus Cosolvent. J.
Phys. Chem. B 2003, 107, 10405-10411. American Chemical Society.
Meher, L. C., Sagar, D. V., Naik, S. N, 2004. Technical Aspect of Biodiesel Production by Transesterification.A Review. Renew Sustain Energy Rev; 10:248-268.
Miller, A.J., and Newel, F. E., 1984. Modern Experimental Organic Chemistry.
Washington : Western Washington University-Press.
Mudzakir, A., 2013.Praktikum Kimia Anorganik (KI 425). Bandung: Jurusan Pendidikan Kimia FMIPA UPI.
Otera, J., 2013. Esterification: Methoss, Reaction and Application. Weinheim : Wiley-VCH Verlag GmbH & Co. KgaA.
Rouque-Malherbe, R.M.A., 2007. Adsorption and Diffussion in Nanoporous Material. CRC Press Taylor & Francis Group.
Sadasivan, S., Dubey A. K., Li, Y., Rasmussen, D. H., 1998.Alcoholic Solvent Effect on Silica Synthesis-NMR and DLS Investigation. Journal of Sol-Gel Science and Technology 12, 5-14. Kluwer Academic Publishers.Manufactured in The Netherlands.
Salihu, B. Z., Gana, A. K., Apuyor, B. O., 2012. Castor Oil Plant (Ricinus communis L) : Botany, Ecology and Uses. International Journal of Science and Research (IJSR). ISSN : 2319-7064
Sarker, S. D., Latif, Z., Grey, A., 2006. Method In Biotechnology, Natural Product IsolationI. Second Edition. Totowa, New Jersey : Humana Press
Schubert, U., and Husing, N., 2006. Synthesis of Inorganic Materials. Second Edition. Wiley-VCH Verlag Gmbh & Co, KgoA, Weinheim.
Sembiring, S., Bangun, N., Kaban, J., Bangun, J., 2018. Purification of Ricinoleic Acid Methyl Ester Using Mesoporous Calcium Silicate (Casio3) Adsorben.
SEMIRATA- International Conference on Science and Technology 2018. IOP Conf. Series: Journal of Physics: Conf. Series 1116 (2018) 042031
Setyawan, H., Yuwana, M., Balgis, R., 2015. PEG-Templated Mesoporous Silicas Using Silicate Precursorand Their Applications in Desiccant dehumidification Cooling Systems.Graduate School of Engineering, Hiroshima University. Japan
Shokuhfar, A., Eghdam, E., Alzamani, M., 2012.Effect of Solvent Content on the Properties of Nanostructure Silica Thin Film by Sol-Gel.Nanoscience and Nanotechnology 2012, 2(1): 22-25.
Silverstein, R.M., Bassler, G.C and Morrill, T.C. 1986. Spectrometer Identification of Organic Compound. John Willey and Sons. New York.
Sinkó, K., 2010. Influence of Chemical Conditions on the Nanoporous Structure of Silicate Aerogels. Materials ISSN 1996-1944.
Sudirham, S. Dan Utari, N. 2010. Mengenal Sifat-Sifat Material (1). Darpublic.
Bandung.
Sukalyan, D., Soumyashri, M., Sabita, T., dan Bijay, K. M., 2008. Organically Modified Silica: Synthesis and Application due to Its Surface Interaction with Organic Molecules. Advance in Colloid and Interface Science, Volume XX, Burla, Elsevier.
Vasant, E. F., Van Der Voort, P., and Vrancken, K. C., 1995. Characterization and Chemical Modification of The Silica SurfaceI. Elsevier.
Viswanathan, B., and Ramaswamy, A. V., 2005. Selection of Solid Heterogenous Catalysts for Reaction. National Centre for Catalysts Research.
Wang, Y., and Zhao, D., 2007. On The Controllable Soft-Templating Approach to Mesoporous Silicates. Chemical Rev. 107. 7. 2821-2860.
Wencel, D., Dolan, C., Barczak, M., Keyes, T.E., Mcdonagh, C., 2013.Synthesis, Tailoring and Characterizqation of Silica Nanoparticle Containing A Highly Stable Rethenium Complex. IOP Publishing.
Weiss, E. A., 1983. Oil Seed Crops. London : Longman.
Xu, W., Ge, X., Yan, X., & Shao, R., 2015. Optimization of methyl ricinoleate synthesis with ionic liquids as catalysts using the response surface methodology.
Chemical Engineering Journal, 275, 63–70.
Yang, X., S. Liao & Z. Liang, (2011). Gellatin-assisted Templating Route to Synthesize Sponge-like Meso-porous Silica with Bimodal Porosity and Iysozyme Adsorption Behavior. Microporous & Mesoporous Materials. 143, 263-268.
Yazid, E., 2005. Kimia Fisika Untuk Para Medis. Yogyakarta.
Zhao, Q., Mao, Y., Yan, L., Lu, L., Jiang, T., Yin, H., 2014.Stability and Textural Properties of Cobalt Incoporated MCM-48Mesoporous Molecular Sieves.
Applaid Surface Science, 257, 2436-2442.
Lampiran 1 Difraktogram XRD Material Mesopori Silika (MS Me 2) Measurement Conditions:
Dataset Name MS (Me 2)
File name E:\DATA PENGUJIAN\Pengujian
2018\Oktober\Mitha\Andriyani\23 oktober\MS (Me 2)\MS (Me 2).rd
Comment Configuration=Reflection-Transmission Sp Goniometer=PW3050/60 (Theta/Theta); Mini Measurement Date / Time 10/23/2018 2:32:00 PM
Peak List:
Pos. [°2Th.] Height [cts] FWHM Left [°2Th.] d-spacing [Å] Rel. Int. [%]
22.7162 46.85 0.0900 3.91133 100.00
Position [°2Theta] (Copper (Cu))
20 30 40 50 60 70 80
Counts
0 100 200
MS (Me 2)
Lampiran 2 Difraktogram XRD Material Mesopori Silika (MS Me 5) Measurement Conditions:
Dataset Name MS (Me 5)
File name E:\DATA PENGUJIAN\Pengujian
2018\Oktober\Mitha\Andriyani\23 oktober\MS (Me 5)\MS (Me 5).rd
Comment Configuration=Reflection-Transmission Sp Goniometer=PW3050/60 (Theta/Theta); Mini Measurement Date / Time 10/23/2018 1:48:00 PM
Peak List:
Pos. [°2Th.] Height [cts] FWHM Left [°2Th.] d-spacing [Å] Rel. Int. [%]
22.3659 72.36 0.0900 3.97180 100.00
55.6493 4.48 0.9792 1.65028 6.19
Position [°2Theta] (Copper (Cu))
20 30 40 50 60 70 80
Counts
0 100 200 300
MS (Me 5)
Lampiran 3 Analisa BET Material Mesopori Silika (MS Me 1) Relative Pressure, P/Po Volume Adsorbed
@STP cc/g 0.0231777 27.8265 0.0766686 34.5675 0.124899 38.0896 0.174117 40.6380 0.226884 42.8928 0.278910 44.8879 0.327539 46.8424 0.379241 48.6842 0.432421 50.7125 0.480565 52.7965 0.531893 55.1267 0.582421 57.8296 0.638019 61.3761 0.687813 65.3462 0.737582 70.9915 0.789205 79.3488 0.837280 93.0763 0.887955 123.023 0.939259 254.978 0.991912 893.568 0.946448 460.021 0.896727 227.785 0.844304 101.923 0.791739 75.1794 0.742150 63.9835 0.688430 56.5094 0.638237 51.7628 0.591367 48.5165 0.539075 45.8671 0.484835 43.1808 0.437862 41.5650 0.386265 40.1458 0.335730 39.0721 0.283884 37.9748 0.234123 37.0363 0.182563 35.8044 0.131155 34.3179 0.0758398 31.5250 0.0259612 26.3716