SMA/MA Kelas X
Hak Cipta pada Departemen Pendidikan Nasional Dilindungi Undang-undang
Kimia SMA/MA Kelas X
Penulis: Khamidinal, Tri Wahyuningsih, Shidiq Premono Editor: Munnal Hani’ah
Pembaca ahli: Susy Yunita Prabawati Desainer sampul: Aji Galarso Andoko Desainer perwajahan: Sri Basuki Ilustrator: Mukti Ali
Penata letak: Sri Basuki, Erwin Ariyanto Pengarah artistik: Sudaryanto
540.7
KHA KHAMIDINAL
k Kimia : SMA/ MA Kelas X / penulis, Khamidinal, Tri Wahyuningsih Shidiq Premono ; editor, Munnal Hani’ah ; illustrator, Mukti Al .-- Jakarta : Pusat Perbukuan, Departemen Pendidikan Nasional, 2009
vii, 202 hlm. : ilus. ; 25 cm.
Bibliografi : hlm. 196-197 Indeks
ISBN: 978-979-068-725-7 (no jilid lengkap) ISBN: 978-979-068-726-4
1. Kimia-Studi dan Pengajaran I. Judul II. Tri Wahyuningsih III. Shidiq Premono IV. Munnal Hani’ah V. Mukti Ali
Hak cipta buku ini telah dibeli oleh Departemen Pendidikan Nasional dari Penerbit Pustaka Insan Madani
Diterbitkan oleh Pusat Perbukuan Departemen Pendidikan Nasional Tahun 2009
Kata Sambutan
Puji syukur kami panjatkan ke hadirat Allah SWT, berkat rahmat dan kar-unia-Nya, Pemerintah, dalam hal ini, Departemen Pendidikan Nasional, pada tahun 2009, telah membeli hak cipta buku teks pelajaran ini dari penu-lis/penerbit untuk disebarluaskan kepada masyarakat melalui situs internet (website) Jaringan Pendidikan Nasional.
Buku teks pelajaran ini telah dinilai oleh Badan Standar Nasional Pendidikan dan telah ditetapkan sebagai buku teks pelajaran yang memenuhi syarat ke-layakan untuk digunakan dalam proses pembelajaran melalui Peraturan Men-teri Pendidikan Nasional Nomor 27 Tahun 2007 tanggal 25 Juni 2007. Kami menyampaikan penghargaan yang setinggi-tingginya kepada para penulis/penerbit yang telah berkenan mengalihkan hak cipta karyanya ke-pada Departemen Pendidikan Nasional untuk digunakan secara luas oleh para siswa dan guru di seluruh Indonesia.
Buku-buku teks pelajaran yang telah dialihkan hak ciptanya kepada
Depar-temen Pendidikan Nasional ini, dapat diunduh (down load), digandakan,
dicetak, dialihmediakan, atau difotokopi oleh masyarakat. Namun, untuk penggandaan yang bersifat komersial harga penjualannya harus memenuhi ketentuan yang ditetapkan oleh Pemerintah. Diharapkan bahwa buku teks pelajaran ini akan lebih mudah diakses sehingga siswa dan guru di seluruh Indonesia maupun sekolah Indonesia yang berada di luar negeri dapat me-manfaatkan sumber belajar ini.
Kami berharap, semua pihak dapat mendukung kebijakan ini. Kepada para siswa kami ucapkan selamat belajar dan manfaatkanlah buku ini sebaik-bai-knya. Kami menyadari bahwa buku ini masih perlu ditingkatkan mutunya. Oleh karena itu, saran dan kritik sangat kami harapkan.
Kata Pengantar
Apakah kalian menganggap kimia sebagai mata pelajaran yang rumit? Tentu tidak, bukan? Walaupun kimia mempelajari tentang pelbagai senyawa kimia, reaksi kimia, dan perhitungan kimia, tapi semuanya bisa dipelajari dengan mudah. Apalagi jika didukung dengan penggunaan buku pelajaran yang tepat. Oleh karena itu, kami menghadirkan Seri Kimia SMA/MA ini. Penyajian materi yang lengkap, interaktif, dan dengan beragam contoh kasus menarik, kami harapkan dapat menjadi bekal agar kimia mudah dipahami.
Beragam elemen dan rubrikasi di dalam buku ini antara lain
Aper-sepsi, berisi semacam pemanasan sebelum masuk ke materi pelajaran. Peta Konsep, yang memuat konsep-konsep inti yang akan diberikan pada setiap
bab. Tujuan Pembelajaran, yakni uraian singkat memuat target yang ingin
dicapai pada setiap bab. Kata Kunci, berisi kata-kata yang merupakan inti
pembahasan materi dalam bab terkait. Aktivitas, yakni praktikum yang
dilakukan siswa untuk membuktikan kebenaran materi yang sedang
dipe-lajari. Tugas, yaitu tugas yang berupa soal-soal hitungan, kegiatan mencari
materi tambahan di buku atau internet, serta proyek/penugasan jangka
panjang. Khazanah, berupa informasi tambahan yang terkait dengan
ma-teri yang sedang diulas. Tips, yaitu langkah sederhana untuk memudahkan
siswa dalam memahami soal serta penjelasan materi. Warning, yakni
peri-ngatan yang harus diperhatikan oleh siswa mengenai suatu hal penting.
Kilas Balik, berisi materi singkat untuk mengingatkan siswa tentang materi
yang telah disampaikan sebelumnya. Diskusi, yakni tugas yang harus
di-kerjakan secara berkelompok berupa kegiatan diskusi. Rangkuman, berisi
ringkasan materi satu bab. Glosarium, yakni penjelasan kata-kata asing yang
ada pada materi yang disampaikan. Uji Kompetensi, berisi soal-soal untuk
menguji kompetensi siswa yang muncul di setiap akhir subbab. Ulangan
Harian, adalah tes penguasaan materi di setiap akhir bab.
Selain rubrik-rubrik tersebut, masih ada ulangan blok yang meliputi
Latih-an UlLatih-angLatih-an Tengah Semester, Latihan UlanganAkhir Semester, dan Latihan Ujian Kenaikan Kelas. Ketiganya berfungsi menguji ketercapaian kompetensi.
Demikianlah, buku ini telah kami upayakan agar dapat tampil dengan kualitas maksimal. Untuk itu, kami segenap Tim Penulis Kimia SMA/MA mengucapkan terima kasih kepada Fakultas Sains dan Teknologi UIN Sunan Kalijaga Yogyakarta, penerbit Pustaka Insan Madani, dan pelbagai pihak yang telah mendukung kami dalam wujud apa pun.
Kata Sambutan
iii
Kata Pengantar
iv
Daftar Isi
v
Bab I
Atom
A. Perkembangan Teori dan Struktur Atom
2
1. Teori Atom Dalton
2
2. Teori Atom Thomson
3
3. Model Atom Rutherford
3
4. Teori Atom Niels Bohr
4
B. Partikel Dasar Penyusun Atom
5
1. Elektron
5
2. Proton
6
3. Neutron
6
C. Nomor Atom, Nomor Massa, dan Lambang Atom
7
1. Nomor Atom dan Nomor Massa
7
2. Penulisan Lambang Atom
8
D. Konfigurasi Elektron dan Elektron Valensi
8
1. Konfigurasi Elektron
8
2. Elektron Valensi
9
E. Satuan Massa Atom dan Massa Atom Relatif
10
1. Massa Atom Relatif
10
2. Massa Molekul Relatif
10
Bab II
Sistem Periodik Unsur
A. Perkembangan Sistem Periodik Unsur
16
1. Pengelompokan Unsur-unsur Berdasarkan Sifat Logam dan logam
16
2. Pengelompokan Unsur-unsur Berdasarkan Hukum Triade Dobereiner
18
3. Pengelompokan Unsur-unsur Berdasarkan Hukum Oktaf Newlands
19
4. Tabel Periodik Mendeleyev
19
5. Tabel Periodik Modern
20
B. Mengenal Tabel Periodik Unsur Modern
21
1. Golongan
22
2. Periode
22
3. Sifat Periodik Unsur-unsur
23
Bab III
Ikatan Kimia
A. Kestabilan Unsur
32
B. Struktur Lewis
34
C. Ikatan Ion
36
D. Ikatan Kovalen
39
E. Ikatan Kovalen Koordinasi
41
F. Keelektronegatifan
43
G. Molekul Polar
44
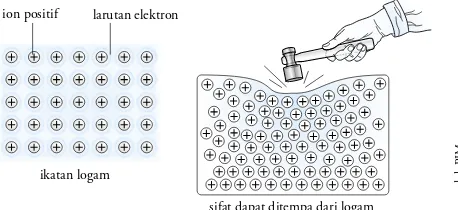
H. Ikatan Logam
47
Ulangan Tengah Semester Pertama
53
Bab IV
Tata Nama Senyawa dan Persamaan Reaksi Sederhana
A. Tata Cara Penulisan Nama Senyawa Kimia
56
1. Tata Nama Senyawa Biner dari Dua Unsur Non-logam
56
2. Tata Nama Senyawa Biner dari Unsur Logam dan Non-logam
57
3. Tata Nama Senyawa Poliatomik
59
4. Tata Nama Senyawa Asam dan Basa
60
5. Tata Nama Trivial (Perdagangan) pada Senyawa Kimia
61
B. Penulisan Persamaan Reaksi Kimia
62
Bab V
Hukum Dasar dan Perhitungan Kimia
A. Hukum Dasar Kimia
70
1. Hukum Kekekalan Massa
70
2. Hukum Perbandingan Tetap
73
3. Hukum Perbandingan Berganda
74
4. Hukum Perbandingan Volume
75
B. Perhitungan Kimia
78
1. Hukum Gay Lussac
78
2. Hukum Avogadro
79
3. Mol
81
4. Massa Molar
82
5. Volume Molar
84
6. Menentukan Rumus Empiris dan Rumus Molekul
87
7. Menentukan Kadar Air Kristal dalam Senyawa
88
8. Menentukan Kadar Zat dalam Senyawa
89
9. Menentukan Pereaksi Pembatas dalam Reaksi Kimia
90
Ulangan Akhir Semester Pertama
97
Bab VI
Larutan Elektrolit dan Non-elektrolit
A. Pengertian Larutan Elektrolit dan Non-elektrolit
102
1. Larutan Elektrolit
105
B. Pengelompokan Larutan Elektrolit Berdasarkan Kemampuannya Meng-hantarkan Listrik
106
C. Pengelompokan Larutan Elektrolit Berdasarkan Ikatannya
108
1. Senyawa Kovalen Polar
108
2. Senyawa Ion
108
Bab VII
Reaksi Oksidasi dan Reduksi
A. Pengertian dan Perkembangan Reaksi Reduksi dan Oksidasi (Redoks)
116
1. Perkembangan Konsep Reaksi Redoks
116
2. Penentuan Bilangan Oksidasi
122
3. Reaksi Redoks dan Non-redoks
123
4. Menentukan Oksidator dan Reduktor dalam Reaksi Redoks
124
5. Reaksi Autoredoks
125
B. Tata Nama Senyawa Redoks Menurut Aturan IUPAC
126
C. Penerapan Konsep Redoks dalam Mengatasi Masalah Pencemaran Ling-kungan (Lumpur Aktif )
128
1. Kualitas Air
129
2. Peranan Lumpur Aktif dalam Pengolahan Air Kotor
130
Ulangan Tengah Semester Kedua
137
Bab VIII
Senyawa Hidrokarbon
A. Kekhasan Atom Karbon
140
1. Atom Karbon dapat Membentuk Empat Ikatan Kovalen
142
2. Atom Karbon dapat Membentuk Ikatan Tunggal, Rangkap dua, dan Rangkap Tiga
143
3. Atom Karbon dapat Membentuk Rantai Karbon
143
B. Pengelompokan Senyawa Hidrokarbon
147
1. Alkana
147
2. Alkena
153
3. Alkuna
158
Bab IX
Minyak Bumi
A. Komposisi dan Pengolahan Minyak Bumi
166
1. Komposisi Minyak Bumi
166
2. Proses Terbentuknya Minyak Bumi
167
3. Pengolahan Minyak Bumi
168
B. Mutu Bensin
170
C. Penggunaan Residu Minyak Bumi dalam Industri Petrokimia
171
D. Dampak Pembakaran Bahan Bakar terhadap Lingkungan
171
E. Kegunaan Senyawa Hidrokarbon dalam Bidang Sandang, Pangan, Papan, Seni, Estetika, dan Perdagangan
173
Latihan Ujian Kenaikan Kelas
179
# B C
"UPN
*
1
FSOBILBILBMJBONBLBOCJTLVJUEFOHBODIPDPMBUFDIJQZBOHUFSTFCBSNFSBUBEJQFSNVLBBOOZB #JTLVJUZBOHMF[BUJOJUFSOZBUBNFOZFSVQBJ NPEFMBUPNZBOHEJLFNVLBLBOPMFITFPSBOHJMNVXBO#BHBJNBOBLPOTFQ NPEFMBUPNUFSTFCVU #BHBJNBOBQVMBQFSLFNCBOHBOLPOTFQBUPNTFJSJOH EFOHBOQFSLFNCBOHBOUFLOPMPHJ "HBSLBMJBOEBQBUNFOFNVLBOKBXBC BOOZBQBIBNJMBIVSBJBOCFSJLVU
EPL1
1BEB CBC JOJ LBMJBO BLBO NFNQFMBKBSJ QFSLFNCBOHBO UFPSJ BUPN NVMBJ EBSJ %BMUPO TBNQBJ /JFMT #PIS %FOHBO EFNJLJBO LBMJBO CJTB NFOHFUBIVJ QBSUJLFM QFOZVTVO BUPN FMFLUSPO QSPUPO EBO OFVUSPO LPOGJHVSBTJFMFLUSPOEBOFMFLUSPOWBMFOTJEBSJTVBUVVOTVSTFSUBIVCVOHBO LPOGJHVSBTJFMFLUSPOEFOHBOMFUBLVOTVSEBMBNUBCFMQFSJPEJL4FMBJOJUV LBMJBOKVHBCJTBNFOFOUVLBOOPNPSNBTTBEBOOPNPSBUPNTVBUVVOTVS ZBOH EJHVOBLBO VOUVL NFOHFMPNQPLLBO VOTVSVOTVS ZBOH UFSHPMPOH JTPUPQJTPCBSEBOJTPUPO
A. Perkembangan Teori dan Struktur Atom
4FKBLUBIVO4.GJMPTPG:VOBOJZBOHCFSOBNB-FVDJQVTEBO
%FNPDSJUVTUFMBINFOHFNVLBLBOUFPSJOZBUFOUBOHCBHJBOUFSLFDJMEBSJ
TVBUVNBUFSJZBOHEJTFCVUBUPN*TUJMBIBUPNCFSBTBMEBSJCBIBTB:VOBOJ
BUPNPT ZBOH CFSBSUJ AUJEBL EBQBU EJCBHJ MBHJ 1FOEBQBU %FNPDSJUVT UFOUBOH BUPN NFNVODVMLBO CFSCBHBJ QFSUFOUBOHBO EJ BOUBSB QBSB JM NVXBOBEBZBOHTFUVKVEBOBEBZBOHUJEBL,BMBOHBOZBOHUJEBLTFUVKV BOUBSB MBJO 1MBUP EBO "SJTUPUFMFT .FSFLB CFSQFOEBQBU CBIXB NBUFSJ CFSTJGBU LPOUJOV BUBV EBQBU EJCFMBI NFOKBEJ CBHJBO MFCJI LFDJM TFDBSB UFSVTNFOFSVT
4FJSJOHEFOHBOQFSLFNCBOHBOJMNVQFOHFUBIVBOUFPSJUFPSJCBSV
UFOUBOH LPOTFQ BUPN KVHB NFOHBMBNJ QFSLFNCBOHBO 1BSB JMNVXBO NFOHFNVLBLBO UFPSJOZB CFSEBTBSLBO FLTQFSJNFO ZBOH UFMBI EJMBLV LBO 1FMCBHBJ IBTJM FLTQFSJNFO UFOUBOH LPOTFQ BUPN BEBMBI TFCBHBJ CFSJLVU
5FPSJ"UPN%BMUPO
+PIO %BMUPO BEBMBI BIMJ GJTJLB EBO LJNJB EBSJ *OH HSJT*BNFOHFNVLBLBOUFPSJBUPNCFSEBTBSLBOIVLVNLFLFLBMBONBTTB EJLFNVLBLBOPMFI-BWPJTJFSZBOHNFOZBUBLBOCBIXBNBTTB[BU TFCFMVNEBOTFTVEBISFBLTJBEBMBITBNB4FMBJOIVLVNLFLFLBMBONBTTB UFPSJBUPNOZBKVHBCFSEBTBSLBOIVLVNQFSCBOEJOHBOUFUBQ EJLFNVLB LBOPMFI1SPVTUZBOHNFOZBUBLBOCBIXBQFSCBOEJOHBONBTTBUJBQ VOTVSEBMBNTFOZBXBBEBMBIUFUBQ
1BEB BXBM BCBE LF %BMUPO NFOHFNVLBLBO UFPSJOZB UFOUBOH
BUPNZBJUV
B 6OTVSUFSTVTVOBUBTQBSUJLFMZBOHUJEBLEBQBUEJCBHJMBHJZBOHEJTFCVU BUPN
C 4FNVB BUPN QFOZVTVO VOTVS ZBOH TBNB NFNJMJLJ TJGBU ZBOH TBNB VLVSBOCFOUVLEBONBTTB4FCBMJLOZBBUPNQFOZVTVOVOTVSZBOH CFSCFEBNFNJMJLJTJGBUZBOHCFSCFEBQVMB
D "UPNBUPNEBSJVOTVSZBOHCFSCFEBEBQBUNFNCFOUVLNPMFLVMEF OHBOQFSCBOEJOHBOTFEFSIBOB
E 1BEB EBTBSOZB SFBLTJ LJNJB BEBMBI TVBUV QFOZVTVOBO VMBOH LPN CJOBTJ BUPN EBSJ TFOZBXB QFSFBLTJ NFOKBEJ TVTVOBO BUPN EBMBN TFOZBXBIBTJMSFBLTJ
Kata
Kunci
• Teori atom• Elektron • Proton • Neutron
• Konfigurasi elektron • Nomor atom • Nomor massa • Isotop • Isobar • Isoton
John Dalton lahir di Eaglesfield, Cumberland, Inggris, pada tanggal 6 September 1766 dan meninggal di Manchester pada tanggal 2 Februari 1844. Karena berhasil menemukan teori atom yang ilmiah, maka Dalton dianggap sebagai salah seorang pendiri ilmu fisika modern.
+PIO@%
BMUPOEFXJLJQFEJBPSHXJLJ+
PIO@%
BMUPO
5FPSJ"UPN5IPNTPO
#FSEBTBSLBOUFPSJBUPN%BMUPOEJLFUBIVJCBIXB%BMUPOTFQFOEBQBU
EFOHBO%FNPDSJUVTLBSFOBLFEVBOZBNFOZBUBLBOCBIXBBUPNBEBMBICB HJBOUFSLFDJMEBSJTVBUVNBUFSJZBOHUJEBLEBQBUEJCBHJMBHJ NBUFSJCFSTJGBU EJTLPOUJOV1FOEBQBUJOJDVLVQMBNBCFSUBIBOIJOHHBTFPSBOHBIMJGJTJLB *OHHSJT EBQBU NFNCVLUJLBO CBIXB BUPN CVLBOMBI CBHJBO UFSLFDJM EBSJ TVBUVNBUFSJ
%FOHBOEJUFNVLBOOZBFMFLUSPOPMFI++5IPNTPOUFPSJBUPN%BMUPO
NVMBJHPZBI1BEBUBIVO++5IPNTPONFOHFNVLBLBOCBIXBBUPN NFSVQBLBOCPMBCFSNVBUBOQPTJUJGZBOHEJOFUSBMLBOPMFINVBUBOOFHBUJG FMFLUSPO ZBOH UFSTFCBS NFSBUB QBEB QFSNVLBBO CPMB UFSTFCVU5FPSJ JOJ TFSJOHEJLFOBMEFOHBOOBNBUFPSJSPUJLJTNJT QMVNQVEEJOHBUPNJD
%BSJUFPSJZBOHEJTBNQBJLBOPMFI5IPNTPOEBQBUEJLFUBIVJCBIXB
BUPNCVLBOMBICBHJBOUFSLFDJMEBSJTVBUVNBUFSJ4FCBCBUPNNBTJIUFSTV TVOPMFIQBSUJLFMQPTJUJGEBOOFHBUJG
D i s k u s i
Thomson membantah teori atom Dalton yang menyatakan bahwa atom adalah bagian terkecil dari materi. Thomson berpendapat bahwa atom tersusun atas partikel positif dan nega-tif. Diskusikan dengan teman-teman kalian mengenai kelebihan dan kekurangan teori atom Dalton dan Thomson. Kemudian, presentasikan hasil diskusi di depan kelas.
.PEFM"UPN3VUIFSGPSE
1BEBUBIVO&SOFTU3VUIFSGPSE NFMBLVLBOQFOH
VKJBOUFSIBEBQNPEFMBUPN5IPNTPOEFOHBONFOHHVOBLBOIBNCVSBO TJOBSBMGBZBOHEJUFNCBLLBOQBEBMBQJTBOMPHBNFNBTUJQJT
.FOVSVU3VUIFSGPSEKJLBNPEFMBUPN5IPNTPOCFOBSTFMVSVITJOBS
BMGBBLBOEJUFSVTLBOUBOQBBEBZBOHEJCFMPLLBO1BEBLFOZBUBBOOZBTJOBS BMGBBEBZBOHEJCFMPLLBOCBILBOBEBKVHBZBOHEJQBOUVMLBONFNCFOUVL TVEVUBOUBSBo
3VUIFSGPSENFOZBUBLBOCBIXBNVBUBOQPTJUJGTVBUVBUPNUJEBLUFSTF
CBSNFSBUBEJTFMVSVIBUPNNFMBJOLBOCFSLVNQVMQBEBQVTBUBUPN1VTBU UFNQBUCFSLVNQVMOZBNVBUBOQPTJUJGEJLFOBMTFCBHBJJOUJBUPN&MFLUSPO
CFSNVBUBOOFHBUJGCFSHFSBLNFOHFMJMJOHJJOUJBUPNTFQFSUJCFSFEBSOZB QMBOFUNFOHFMJMJOHJNBUBIBSJ
Gambar 1.1
Model atom Thomson me-nyerupai kue kismis dengan elektron menyebar di seluruh permukaan bola yang ber-muatan positif.
Gambar 1.2
(a) Eksperimen Rutherford (b) Model Atom Rutherford (a) (b)
Ernest Rutherford (1871-1937) adalah seorang fisikawan dari New Zealand yang meraih Nobel di bidang kimia pada tahun 1908.
FSOFTU@S
VUIFS
GPS
EXXX
W
BOEFS
LS
PHU
www.batan.go.id
EPL1
*.
EPL1
5FPSJ"UPN/JFMT#PIS
4VBUV LFNBKVBO EBSJ UFPSJ 3VUIFSGPSE BEBMBI EJUFNVLBOOZB JOUJ
BUPN .FTLJQVO EFNJLJBO UFPSJ BUPN 3VUIFSGPSE NBTJI NFNJMJLJ LFMFNBIBO .FOVSVU UFPSJ GJTJLB LMBTJL KJLB TVBUV QBSUJLFM CFSNVBUBO CFSHFSBLNFOHFMJMJOHJQBSUJLFMMBJOEFOHBONVBUBOCFSMBXBOBONBLBTF NBLJOMBNBQBSUJLFMJUVBLBOKBUVILFQVTBUOZB1BEBIBMFMFLUSPOUFSTFCVU UJEBLQFSOBIUFSUBSJLLFJOUJBUPN
4FPSBOH GJTJLBXBO %FONBSL/JFMT #PIS NFMBLVLBO
QFSDPCBBO EFOHBO NFOHBNBUJ TQFLUSVN BUPN NFOHHVOBLBO VOTVS IJESPHFO )BTJM QFOHBNBUBO NFOVOKVLLBO CBIXB TQFLUSVN IJESPHFO NFSVQBLBOHBSJTHBSJTZBOHUFSQJTBINFOVSVUBUVSBOUFSUFOUV(BSJTHBSJT UFSQJTBIJUVNFSVQBLBOMJOUBTBOFMFLUSPOEFOHBOUJOHLBUFOFSHJUFSUFOUV
#FSEBTBSLBOIBTJMQFOHBNBUBOOZB#PISNFOZVTVOUFPSJBUPNTFC
BHBJCFSJLVU
B "UPNUFSEJSJBUBTJOUJBUPNCFSNVBUBOQPTJUJGEBOFMFLUSPOCFSNVBUBO OFHBUJGZBOHCFSHFSBLNFOHFMJMJOHJJOUJBUPN
C &MFLUSPO CFSHFSBL NFOHFMJMJOHJ JOUJ BUPN QBEB KBSBL UFSUFOUV ZBOH EJTFCVUMJOUBTBOFMFLUSPO
D 4FMBNBCFSHFSBLNFOHFMJMJOHJJOUJBUPNFMFLUSPOUJEBLNFNBODBSLBO NBVQVONFOZFSBQFOFSHJ
E &MFLUSPOEBQBUCFSQJOEBILFMJOUBTBOZBOHMFCJIUJOHHJEFOHBONF OZFSBQFOFSHJEBOEBQBUQVMBCFSQJOEBILFMJOUBTBOZBOHMFCJISFOEBI EFOHBONFNBODBSLBOFOFSHJ
D i s k u s i
Teori atom Bohr memiliki persamaan dan perbedaan dengan teori atom Rutherford. Buatlah tabel persamaan dan perbedaan antar kedua teori tersebut. Lalu, diskusikan dengan teman-teman tentang kelebihan dan kekurangan teori atom Rutherford dan Bohr.
U j i K o m p e t e n s i
Jawablah pertanyaan-pertanyaan berikut.
1. Jelaskan teori atom yang dikemukakan Dalton. 2. Mengapa Thomson tidak sependapat dengan
teori atom yang disampaikan Dalton?
3. Berdasarkan percobaan dengan hamburan sinar alfa, Rutherford menyempurnakan teori atom yang disampaikan Thomson. Terangkan kelemahan model atom Thomson.
4. Model atom Rutherford ternyata bertentangan dengan teori fisika klasik. Jelaskan pertentang-an teori tersebut.
5. Jelaskan teori atom menurut Bohr. 6. Partikel apa yang menyusun inti
atom? Jelaskan jawaban kalian.
Gambar 1.3 Model Atom Bohr
Niels Bohr adalah seorang ilmuwan Denmark yang menerima hadiah Nobel di bidang fisika pada tahun 1922. Pada PD II, Bohr bekerja di New Mexico untuk mengem-bangkan bom atom.
/
JFMT#PIS@XXX
QIRNVMBDUJG
www.batan.go.id
EPL1
B. Partikel Dasar Penyusun Atom
1FOEBQBUZBOHNFOZBUBLBOCBIXBBUPNNFSVQBLBOCBHJBOUFSLFDJM
EBSJ NBUFSJ UFSOZBUB UJEBL CFOBS )BM JUV CJTB EJCVLUJLBO EFOHBO QF OFNVBO FMFLUSPO PMFI5IPNTPO EBO QFOFNVBO JOUJ BUPN ZBOH UFSEJSJ BUBTQSPUPOEBOOFVUSPOPMFI3VUIFSGPSE#BILBO#PISKVHBNFOZBUBLBO CBIXB FMFLUSPO ZBOH EJUFNVLBO PMFI5IPNTPO NFOHFMJMJOHJ JOUJ BUPN EBONFOFNQBUJMJOUBTBOQBEBUJOHLBUFOFSHJUFSUFOUV%FOHBOEFNJLJBO EJLFUBIVJCBIXBBUPNUFSTVTVOBUBTQSPUPOOFVUSPOEBOFMFLUSPO
&MFLUSPO
1BEBUBIVO++5IPNTPONFOHBNBUJQFMBULBUPEBEBOQFMBU
BOPEB EBMBN UBCVOH IBNQB VEBSB ZBOH EJBMJSJ MJTUSJL UFHBOHBO UJOHHJ
5IPNTPONFOFNVLBOCBIXBQFMBULBUPEB FMFLUSPEBOFHBUJGNFNBODBS
LBOTJOBSZBOHCFSHFSBLNFOVSVUHBSJTMVSVTNFOVKVQFMBUBOPEB FMFLUSPO QPTJUJG4FMBJOCFSHFSBLMVSVTTJOBSLBUPEBKVHBNFNJMJLJTJGBUZBOHVOJL ZBJUVEBQBUEJCFMPLLBOPMFINFEBONBHOFUBUBVNFEBOMJTUSJLNFOVKVLF LVUVCQPTJUJG1FSDPCBBOJOJNFNCVLUJLBOCBIXBTJOBSEBSJQFMBULBUPEB
NFSVQBLBOQBSUJLFMQFOZVTVOBUPNCFSNVBUBOOFHBUJGZBOHEJTFCVUFMFL
USPO
1FOZJNQBOHBOTVBUVQBSUJLFMCFSNVBUBOEBMBNNFEBONBHOFUBUBV
NFEBOMJTUSJLUFSOZBUBTFCBOEJOHEFOHBONVBUBOOZB FEBOCFSCBOEJOH UFSCBMJLEFOHBONBTTBOZB N%BMBNQFSDPCBBOMFCJIMBOKVU5IPNTPO NFOFNVLBOCBIXBBOHLBCBOEJOHBOUBSBNVBUBO
MJTUSJL EBO NBTTB FMFLUSPO FN BEBMBI
$LHo6OUVLNVBUBOFMFLUSPO3".JMJLBO
NFMBLVLBOQFSDPCBBOEFOHBONFOHHVOBLBOUFUFT NJOZBLEBONFOEBQBULBOIBSHBNVBUBOFMFLUSPO
TFCFTBS o o$ 4FIJOHHB EBSJ QFSDPCBBO
5IPNTPO EBO .JMJLBO EJQFSPMFI NBTTB FMFLUSPO
NF oLHBUBV oHS
Gambar 1.4 Struktur atom
QSPUPO OFVUSPO FMFLUSPO
Gambar 1.6
Percobaan tetes minyak Milikan Gambar 1.5
(a) Sinar dari pelat katoda merambat lurus menuju pelat anoda. (b) Sinar dari pelat katoda dapat dibelokkan oleh medan listrik.
(a) (b)
EPL1
*.
EPL1
1SPUPO
1BEB LFBEBBO EBTBS TVBUV BUPN UJEBL CFSNVBUBO OFUSBM 5FUBQJ
TFUFMBI EJLFUBIVJ CBIXB QBSUJLFM EBTBS QFOZVTVO BUPN BEBMBI FMFLUSPO ZBOH CFSNVBUBO OFHBUJG IBM JOJ NFOJNCVMLBO EVHBBO CBIXB QBSUJLFM EBTBSQFOZVTVOBUPNKVHBNFOHBOEVOHNVBUBOQPTJUJG
4FPSBOH BIMJ GJTJLB EBSJ +FSNBO &VHFOF (PMETUFJO NFMBLVLBO
FLTQFSJNFO NFOHHVOBLBO UBCVOH IBNQB CFSNVBUBO MJTUSJL EFOHBO NFOHHVOBLBO MFNQFOH LBUPEB ZBOH CFSMVCBOH %BSJ QFSDPCBBO JOJ EJLFUBIVJ BEBOZB TJOBS ZBOH CFSHFSBL CFSMBXBOBO BSBI EFOHBO TJOBS LBUPEB 4FIJOHHB EBQBU EJTJNQVMLBO CBIXB TJOBS UFSTFCVU NFSVQBLBO QBSUJLFMCFSNVBUBOQPTJUJGZBOHEJTFCVUTJOBSBOPEB
#FTBSOZB BOHLB CBOEJOH BOUBSB NVBUBO MJTUSJL EFOHBO NBTTB TJOBS BOPEBUFSOZBUBCFSWBSJBTJUFSHBOUVOHQBEBKFOJTHBTQFOHJTJUBCVOHIBNQB "OHLBCBOEJOHUFSTFCVUTFMBMVMFCJILFDJMEBSJIBSHBFNFMFLUSPO4FNFO UBSBJUVNBTTBTJOBSBOPEBUFSLFDJMEJQFSPMFIKJLBHBTQFOHJTJUBCVOHOZB BEBMBIIJESPHFOZBOHNFNJMJLJIBSHBFNQBMJOHCFTBS
-BJOIBMOZBEFOHBO&VHFOF(PMETUFJO3VUIFSGPSENFMBLVLBOQFSDP
CBBOEFOHBONFOHHVOBLBOIBNCVSBOTJOBSBMGB%BSJIBTJMQFSDPCBBOOZB 3VUIFSGPSE NFOFNVLBO CBIXB QBSUJLFM QPTJUJG UFSQVTBU QBEB JOUJ BUPN
ZBOHEJLFOBMTFCBHBJQSPUPOEFOHBONBTTB oHSBN
/FVUSPO
.FTLJQVO QBSUJLFM EBTBS QFOZVTVO BUPN UFMBI EJLFUBIVJ OBNVO
3VUIFSGPSENFOFNVLBOCBIXBNBTTBBUPNIBOZBTFLJUBSTFUFOHBIEBSJ NBTTB BUPN SFMBUJG ZBOH EJLFUBIVJ TFCFMVNOZB 1BEBIBM NBTTB FMFLUSPO TBOHBU LFDJM CJMB EJCBOEJOHLBO EFOHBO NBTTB QSPUPO #FSEBTBSLBO IBM UFSTFCVU QBEB UBIVO 3VUIFSGPSE CFSQJLJS CBIXB EJ EBMBN BUPN UFSEBQBUQBSUJLFMOFUSBMZBOHCFSNBTTBTBNBEFOHBOQSPUPO
1BEBUBIVO+BNFT$IBEXJDLTFPSBOHBIMJGJTJLBEBSJ*OHHSJT
NFMBLVLBO TVBUV FLTQFSJNFO ZBOH NFNCVLUJLBO EVHBBO 3VUIFSGPSE +BNFT$IBEXJDLNFMBLVLBOQFSDPCBBOEFOHBODBSBNFOFNCBLLBOTJOBS BMGBCFSNVBUBOOFHBUJGLFBUPNCFSJMJVN1FSDPCBBOJOJNFOEFUFLTJBEB
OZBQBSUJLFMUJEBLCFSNVBUBOZBOHEJTFCVUOFVUSPO.BTTBOFVUSPOZBJUV
oHS
Gambar 1.7
Percobaan sinar anoda
JamesChadwick
(1891-1974) adalah seorang ilmuwan asal Inggris. Pada tahun 1935, ia mampu membuktikan keberadaan neutron se-hinga memeroleh hadiah Nobel.
Profil James Chadwick
hal 411 buku konsep
fisika modern edisi
keempat.
XXXMBQQ
JOQ
id.wikipedia.org
EPL1
#FSEBTBSLBO QFOFNVBO QBSUJLFMQBSUJLFM BUPN EBQBU EJTJNQVMLBO CBIXBQBSUJLFMEBTBSQFOZVTVOBUPNBEBMBIQSPUPOOFVUSPOEBOFMFL USPO"HBSLBMJBOMFCJINVEBINFNBIBNJVSBJBOEJBUBTQFSIBUJLBO5BCFM CFSJLVU
5BCFM.BTTBEBO.VBUBO1BSUJLFM%BTBS1FOZVTVO"UPN
1BSUJLFM -BNCBOH .BTTB HSBN UFSIBEBQ1SPUPO.BTTB3FMBUJG .VBUBO DPVMPNC UFSIBEBQ1SPUPO.VBUBO3FMBUJG
1SPUPO Q o o
/FVUSPO O o
&MFLUSPO −F o o o
1FOHFUBIVBO UFOUBOH QBSUJLFMQBSUJLFM QFOZVTVO BUPN TBOHBU QFOUJOH EJLVBTBJ LBSFOB MFUBL BUPN EBMBN UBCFM QFSJPEJL EJUFOUVLBO PMFI KVNMBI FMFLUSPOOZBTFEBOHLBOTJGBUTJGBUBUPNEJQFOHBSVIJPMFIKVNMBIQSPUPOOZB
U j i K o m p e t e n s i
Jawablah pertanyaan-pertanyaan berikut.
1. Mengapa sinar katoda dapat dibelokkan oleh medan listrik atau medan magnet?
2. Jelaskan proses penemuan elektron, proton, dan neutron.
3. Mengapa ada anggapan bahwa partikel pe-nyusun atom mengandung muatan positif?
4. Mengapa massa proton terkecil diperoleh jika gas pengisi tabung adalah
hidrogen? Jelaskan jawaban kalian.
C. Nomor Atom, Nomor Massa, dan Lambang Atom
4FUJBQVOTVSNFNJMJLJQFSCFEBBOKVNMBIQSPUPOOFVUSPOEBOFMFL
USPOZBOHEBQBUEJHVOBLBOVOUVLNFOFOUVLBOTJGBUEBOMFUBLTVBUVVOTVS EBMBN UBCFM QFSJPEJL 0MFI LBSFOB JUV LBMJBO IBSVT NFNBIBNJ OPNPS BUPNEBOOPNPSNBTTBUFSMFCJIEBIVMV
/PNPS"UPNEBO/PNPS.BTTB
/PNPSBUPN ;NFOVOKVLLBOKVNMBIFMFLUSPOZBOHUFSEBQBUQBEB BUPN1BEBBUPNOFUSBMKVNMBIFMFLUSPOTBNBEFOHBOKVNMBIQSPUPO4F IJOHHBOPNPSBUPNKVHBNFOVOKVLLBOKVNMBIQSPUPOZBOHUFSEBQBUQBEB JOUJBUPN
-BJOIBMOZBEFOHBOBUPNZBOHNFOFSJNBBUBVNFMFQBTFMFLUSPOLF
BUPNMBJO4FIJOHHBKVNMBIFMFLUSPOOZBCFSVCBITFEBOHLBOKVNMBIQSP UPOEBOOFVUSPOUFUBQ
/PNPSNBTTBBUPN "NFOVOKVLLBOKVNMBIQSPUPOEBOOFVUSPO ZBOHUFSEBQBUQBEBJOUJBUPN4FNVBVOTVSNFOHBOEVOHLFUJHBQBSUJLFM UFSTFCVULFDVBMJVOTVSIJESPHFOZBOHUJEBLNFNJMJLJOFVUSPOEBOIBOZB NFNJMJLJTBUVQSPUPO
#SBEZ
1FOVMJTBO-BNCBOH"UPN
4VBUVVOTVSEBQBUEJMBNCBOHLBOEFOHBO
;
"9 ,FUFSBOHBO
9MBNCBOHBUPN
"OPNPSNBTTBBUPN
;OPNPSBUPN
C o n t o h
5FOUVLBOOPNPSBUPNOPNPSNBTTBFMFLUSPOQSPUPOEBOOFVUSPOEBSJ
VOTVS/B
+BXBC
-BNCBOHBUPNEJBUBTNFOVOKVLLBO /B MBNCBOHVOTVS/BUSJVN
OPNPSBUPN NFOVOKVLLBOKVNMBIFMFLUSPO
OPNPSNBTTBBUPN NFOVOKVLLBOKVNMBIQSPUPOEBOOFVUSPO 1BEBBUPNOFUSBMKVNMBIQSPUPOTBNBEFOHBOKVNMBIFMFLUSPO +BEJQBEBBUPNOBUSJVNUFSEBQBU
FMFLUSPO F OFVUSPO O"o;o
QSPUPO Q
T u g a s
Tentukan nomor atom, nomor massa, elektron, proton, dan neutron dari unsur 21
4 2Mg.
D. Konfigurasi Elektron dan Elektron Valensi
1BEB TVCCBC TFCFMVNOZB LBMJBO UFMBI NFNQFMBKBSJ TUSVLUVS BUPN
ZBOHUFSEJSJBUBTQSPUPOOFVUSPOEBOFMFLUSPO&MFLUSPOFMFLUSPONFOHF MJMJOHJ JOUJ BUPN EFOHBO NFOFNQBUJ MJOUBTBO UFSUFOUV #BHBJNBOB DBSB FMFLUSPONFOHFMJMJOHJJOUJBUPN %FOHBONFNBIBNJVSBJBOCFSJLVULB MJBOBLBONFOHFUBIVJKBXBCBOOZB
,POGJHVSBTJ&MFLUSPO
,BMJBO UFMBI NFOHFUBIVJ CBIXB TFUJBQ BUPN UFSEJSJ BUBT JOUJ BUPN ZBOH EJLFMJMJOHJ PMFI CFCFSBQB LVMJU BUPN *OUJ BUPN NFSVQBLBO QVTBU NBTTBBUPNZBOHUFSTVTVOBUBTQSPUPOEBOOFVUSPO4FNFOUBSBJUVFMFL USPOCFSQVUBSNFOHFMJMJOHJJOUJBUPNEFOHBONFOFNQBUJMJOUBTBOUFSUFOUV -JOUBTBOFMFLUSPOJOJEJOBNBLBOLVMJUBUPN
4FUJBQLVMJUBUPNEJUFNQBUJPMFITFKVNMBIFMFLUSPO1FOFNQBUBOFMFL
USPO QBEB UJBQ LVMJU BUPN EJTFCVU LPOGJHVSBTJ FMFLUSPO .FOVSVU 1BVMJ KVNMBI NBLTJNVN FMFLUSPO ZBOH NFOFNQBUJ UJBQUJBQ LVMJU NFOHJLVUJ
SVNVTO1FSIBUJLBO5BCFMCFSJLVU
Dalam tabel periodik, biasanya suatu unsur dilambangkan dengan:
atau atau Nomor atom (Z) = jumlah elektron = jumlah proton
X
Z
A X
Z
A X
Z A
5BCFM+VNMBI&MFLUSPO.BLTJNVNZBOH.FOFNQBUJ5JBQ,VMJU"UPN /PNPSLVMJU O /BNBLVMJU +VNMBIFMFLUSPONBLTJNVN O
,
-
.
/
#FSEBTBSLBO BUVSBO "VGCBV QFOHJTJBO FMFLUSPO EJNVMBJ EBSJ LVMJU ZBOH NFNJMJLJ UJOHLBU FOFSHJ SFOEBI NFOVKV UJOHLBU FOFSHJ ZBOH MFCJI UJOHHJ5JOHLBUFOFSHJUFSFOEBIEJNJMJLJPMFILVMJU,4FNBLJOKBVIMFUBL LVMJUEBSJJOUJFOFSHJZBOHEJNJMJLJTFNBLJOUJOHHJ1FSIBUJLBO5BCFM CFSJLVU
5BCFM,POGJHVSBTJ&MFLUSPO#FCFSBQB6OTVS 6OTVS /BNB6OTVS +VNMBI
FMFLUSPO ,VMJU, ,VMJU- ,VMJU. ,VMJU/
)F )FMJVN
#F #FSJMJVN
# #PSPO
0 0LTJHFO
/F /FPO
/B /BUSJVN
"M "MVNJOJVN
$B ,BMTJVN
4F 4FMFOJVN
1E 1BMBEJVN
&MFLUSPO7BMFOTJ
#BOZBLOZBFMFLUSPOZBOHNFOFNQBUJLVMJUUFSMVBSEJTFCVUFMFLUSPO
WBMFOTJ &MFLUSPO WBMFOTJ NFOFOUVLBO TJGBU LJNJB EBO TJGBU GJTJLB TVBUV VOTVS4FMBJOJUVFMFLUSPOWBMFOTJKVHBCFSQFSBOQFOUJOHEBMBNQFNCFO UVLBOJLBUBOQBEBNPMFLVMEBOSFBLTJSFBLTJLJNJB1FSIBUJLBO5BCFM CFSJLVU
5BCFM&MFLUSPO7BMFOTJ#FCFSBQB6OTVS
6OTVS /BNB6OTVS +VNMBI&MFLUSPO ,VMJU, ,VMJU- ,VMJU. ,VMJU/ &MFLUSPO7BMFOTJ
) )JESPHFO
)F )FMJVN
-J -JUJVN
$
$
Gambar 1.8
Inti atom dikelilingi oleh beberapa kulit atom
Gambar 1.9
Konfigurasi atom He, O, dan Al
4VLBS
EKPIMN
4VLBS
EKPIMN
4ZVLSJIMN
EPL1
*.
EPL1
,POGJHVSBTJFMFLUSPOEJHVOBLBOVOUVLNFOFOUVLBOMFUBLTVBUVVO TVSEBMBNUBCFMQFSJPEJL+VNMBIFMFLUSPOWBMFOTJNFOVOKVLLBOOPNPS HPMPOHBOTVBUVVOTVSTFEBOHLBOKVNMBILVMJUNFOVOKVLLBOQFSJPEFOZB
"HBSMFCJIUFSBNQJMEBMBNNFOFOUVLBOLPOGJHVSBTJVOTVSLFSKBLBO
6KJ,PNQFUFOTJCFSJLVU
U j i K o m p e t e n s i
Tentukan konfigurasi elektron dan elektron valensi dari unsur-unsur berikut. a. 7N c. 12Mg
b. 9F d. 25Mn
e. 33As g. 42Mo i. 54Xe
f. 39Y h. 49In
E. Satuan Massa Atom dan Massa Atom Relatif
,BMJBOUFMBINFNQFMBKBSJOPNPSBUPNEBOOPNPSNBTTBQBEBTVCCBC
TFCFMVNOZB4FQFSUJZBOHUFMBILBMJBOLFUBIVJNBTTBBUPNNFOVOKVLLBO KVNMBIQSPUPOEBOOFVUSPOZBOHUFSEBQBUQBEBJOUJBUPN6OUVLNFN QFSMVBTXBXBTBOLBMJBOUFOUBOHOPNPSNBTTBBUPNTJNBLMBIVSBJBOZBOH NFOKFMBTLBONBTTBBUPNSFMBUJGEBONBTTBNPMFLVMSFMBUJGCFSJLVU
.BTTB"UPN3FMBUJG "S
.BTTBBUPNSFMBUJGNFSVQBLBOSBUBSBUBEBSJNBTTBJTPUPQTFUJBQVO TVSCFSEBTBSLBOGSBLTJLFMJNQBIBOOZBEJBMBN*TPUPQBEBMBIVOTVSTFKFOJT ZBOHNFNQVOZBJOPNPSBUPNTBNBUFUBQJOPNPSNBTTBOZBCFSCFEB*TP UPQKVHBEJBSUJLBOTFCBHBJVOTVSTFKFOJTZBOHNFNQVOZBJKVNMBIQSPUPO TBNBUFUBQJKVNMBIOFVUSPOOZBCFSCFEB
1BEB UBIVO *61"$ *OUFSOBUJPOBM 6OJPO PG 1VSF BOE "QMJFE $IFNJTUSZNFOFUBQLBOBUPN$TFCBHBJTUBOEBSQFOFOUVBONBTTBBUPN
BUPNZBOHMBJO)BMJOJCFSEBTBSLBOLFTUBCJMBOBUPN$CJMBEJCBOEJOH
LBOEFOHBOEVBJTPUPQLBSCPOMBJOOZB $EBO$
.BTTB.PMFLVM3FMBUJG .S
.BTTBNPMFLVMSFMBUJGNFSVQBLBOKVNMBINBTTBBUPNSFMBUJGVOTVS VOTVSQFOZVTVOOZB5JBQUJBQVOTVSEJLBMJLBOEFOHBOKVNMBIBUPNVOTVS EBMBNTBUVNPMFLVM"HBSMFCJIKFMBTQFSIBUJLBODPOUPICFSJLVU
#F #FSJMJVN
# #PSPO
$ ,BSCPO
1 'PTGPSVT
4 #FMFSBOH
#S #SPN
,S ,SJQUPO
Massa atom relatif suatu unsur tidak sama persis dengan nomor massanya, kecuali atom 12C .
C o n t o h
)JUVOHMBINBTTBNPMFLVMSFMBUJG)0 BJS
1FOZFMFTBJBO
%JLFUBIVJ
4FOZBXB)0UFSCFOUVLEBSJBUPN)EBOBUPN0
4FIJOHHBNBTTBNPMFLVMSFMBUJGTFOZBXB)0BEBMBI
.S)0 "S) "S0
#FSEBTBSLBOUBCFMQFSJPEJLEJQFSPMFINBTTBBUPNSFMBUJGVOTVS)EBO0 TFCBHBJCFSJLVU
"S)
"S0
%JUBOZBLBO
.BTTBNPMFLVMSFMBUJG)0
+BXBC
.S)0 "S) "S0
R a n g k u m a n
1. Sejarah perkembangan teori atom meliputi: a. Teori John Dalton, yaitu atom merupakan
bagian terkecil dari materi yang sudah tidak dapat dibagi.
b. Teori Joseph John Thomson, yaitu atom merupakan bola padat bermuatan po-sitif dengan elektron yang tersebar di seluruh permukaannya.
c. Teori Ernest Rutherford, yaitu muatan positif suatu atom terpusat pada inti atom, sedangkan elektron bergerak mengelilingi inti atom.
d. Teori Niels Bohr, yaitu elektron menge-lilingi inti atom pada suatu lintasan de-ngan tingkat energi tertentu.
2. Partikel-partikel dasar penyusun atom terdiri atas:
a. Elektron (partikel bermuatan negatif) b. Proton (partikel bermuatan positif) c. Neutron (partikel yang tidak bermuatan
atau netral)
3. Nomor atom (Z) menunjukkan jumlah proton (elektron) yang terdapat pada atom. Sedang-kan nomor massa (A) menunjukSedang-kan jumlah proton dan neutron yang terdapat pada inti atom.
4. Konfigurasi elektron menggambarkan pe-nempatan elektron pada tiap kulit atom, dengan jumlah maksimum elektron pada tiap-tiap kulit = 2n2 ( n = nomor kulit ).
5. Elektron valensi menunjukkan banyaknya elektron yang menempati kulit terluar.
Konfigurasi Elektron Sebaran elektron di sekeliling inti atom yang membentuk susunan teratur dan tertentu, bergantung pada nomor atom unsur itu.
Partikel Bagian dari materi yang ukurannya paling kecil dan merupakan penyusun materi tersebut
Sinar alfa Berkas sinar yang terpancar dari inti atom 24He
Spektrum Radiasi elektromagnet yang terurai dan tersusun menurut perubahan karakter tertentu
Struktur Atom Susunan dan sebaran partikel penyusun atom (inti atom dan elektron yang mengitarinya) di dalam sebuah atom netral.
G l o s a r i u m
U
l a n g a n
H a r i a n
A Pilihlah jawaban yang tepat.
'JMPTPG :VOBOJ ZBOH NFOHFNVLBLBO UFPSJ UFOUBOH CBHJBO UFSLFDJM EBSJ TVBUV NBUFSJ BEBMBIy
" +PIO%BMUPO
# -FVDJQQVTEBO%FNPDSJUVT $ ++5IPNQTPO
% &SOFTU3VUIFSGPSE & /JFMT#PIS
1BSUJLFMUFSLFDJMTVBUVNBUFSJZBOHTVEBIUJ EBLEBQBUEJCBHJNFOKBEJCBHJBOZBOHMFCJI LFDJMEJTFCVUy
" TFOZBXB # BUPN $ JPO % QSPUPO & OFVUSPO
5FPSJBUPNZBOHEJLFNVLBLBOPMFI%BMUPO CFSEBTBSLBOBUBTy
" )VLVN5SJBEF # )VLVN0LUBG
$ )VLVN,FLFLBMBO.BTTB % )VLVN,FLFLBMBO&OFSHJ & IBNCVSBOTJOBSBMGB
1FSDPCBBOZBOHEJMBLVLBOPMFI3VUIFSGPSE NFOHHVOBLBOIBNCVSBOTJOBSy
" BMGB # CFUB $ HBNNB % TJHNB & UFUB
"EBOZBJOUJBUPNQBEBTFCVBIBUPNEJLF NVLBLBOPMFIy
" /JFMT#PIS # &SOFTU3VUIFSGPSE $ 'BSBEBZ
% +PTFQI+PIO5IPNTPO & +PIO%BMUPO
.BTTBFMFLUSPOBEBMBITFCFTBSyLH
" o
# o
$ o
% o
& o
+VNMBIQSPUPOZBOHUFSEBQBUQBEBJOUJBUPN TFCBOEJOHEFOHBOKVNMBIy
% FMFLUSPO & NPMFLVM
/PNPS NBTTB BUPN NFOVOKVLLBO KVNMBI QBSUJLFMy
" FMFLUSPO # QSPUPO $ OFVUSPO
% FMFLUSPOEBOOFVUSPO & QSPUPOEBOOFVUSPO
6OTVS"M NFNJMJLJKVNMBIOFVUSPOTFCB
OZBLyCVBI " # $ % &
#JMBTVBUVVOTVS9NFNQVOZBJOPNPSBUPN EBOOPNPSNBTTBNBLBEBQBUEJUVMJT LBOEFOHBOy
" 9
# 9
$ 9
% 9
& 9
+VNMBI FMFLUSPO NBLTJNVN ZBOH NFOFN QBUJLVMJU.BEBMBIy
" # $ %
&
1FOHJTJBO FMFLUSPO EJNVMBJ EBSJ LVMJU ZBOH NFNJMJLJ UJOHLBU FOFSHJ SFOEBI NFOVKV UJOHLBUFOFSHJZBOHMFCJIUJOHHJEJLFNVLB LBOPMFIy
" /JFMT#PIS # +BNFT$IBEXJDL $ ++5IPNTPO % "VGCBV
& &VHFOF(PMETUFJO
,VMJU BUPN ZBOH NFNJMJLJ FOFSHJ UFSFOEBI BEBMBIy
" LVMJU, # LVMJU-$ LVMJU. % LVMJU/ & LVMJU0
6OTVS9NFNQVOZBJOPNPSBUPNNBLB LPOGJHVSBTJFMFLUSPOOZBBEBMBIy
" 9
# 9
$ 9
% 9
& 9
6OTVS9NFNQVOZBJOPNPSNBTTBEBO FMFLUSPO ,POGJHVSBTJ FMFLUSPO VOTVS 9 UFSTFCVUBEBMBIy
" 9
# 9
$ 9
% 9
& 9
,POGJHVSBTJ FMFLUSPO VOUVL VOTVS EFOHBO OPNPS NBTTB EBO KVNMBI OFVUSPO BEBMBIy
" 9
# 9
$ 9
% 9
& 9
6OTVSVOTVSCFSJLVUZBOHNFNQVOZBJKVN MBIFMFLUSPOWBMFOTJUFSCBOZBLBEBMBIy " 0
# .H
$ 1
% $M
& 4
&MFLUSPOWBMFOTJVOTVS"BEBMBIyCVBI "
# $ % &
" # $ % &
6OTVS ZBOH EJHVOBLBO TFCBHBJ TUBOEBS QFOFOUVBO NBTTB BUPNBUPN MBJO BEBMBI y " $
# /
$ 0
% /B
& .H
B Jawablah pertanyaan-pertanyaan berikut.
+FMBTLBO LFMFCJIBO NPEFM BUPN 5IPNTPO EJCBOEJOHLBONPEFMBUPN%BMUPO
5FSBOHLBOQFSDPCBBOZBOHEJMBLVLBO#PIS VOUVLNFOFOUVLBONPEFMBUPN
(BNCBSLBONPEFMBUPNZBOHEJLFNVLBLBO PMFI
B +PTFQI+PIO5IPNTPO C &SOFTU3VUIFSGPSE D /JFMT#PIS
+FMBTLBOQSPTFTQFOFNVBOFMFLUSPOPMFI++ 5IPNTPO
-FOHLBQJMBIUBCFMCFSJLVU
6OTVS 0
/B
4
"S
"T
/PNPS BUPN /PNPS NBTTB 1SPUPO
/FVUSPO
&MFLUSPO
+FMBTLBOBUVSBO"VGCBVZBOHCFSIVCVOHBO EFOHBOQFOHJTJBOFMFLUSPOQBEBLVMJUBUPN 5FOUVLBOLPOGJHVSBTJFMFLUSPOEBOFMFLUSPO
WBMFOTJ EBSJ VOTVSVOTVS CFSJLVU 4FMBOKVU OZB UFOUVLBO QVMB VOTVS ZBOH DFOEFSVOH NFNCFOUVLJPOQPTJUJG
B 3C
C #S
D $B
6OTVS9NFNJMJLJKVNMBIFMFLUSPOEBO KVNMBI OFVUSPO 5FOUVLBO LPOGJHVSBTJ FMFLUSPO FMFLUSPO WBMFOTJ EBO MBNCBOH VOTVSUFSTFCVU
6OTVS:NFNQVOZBJKVNMBIFMFLUSPOQBEB LVMJU,LVMJU-LVMJU.EBO LVMJU / +JLB EJLFUBIVJ OPNPS NBTTB BUPN BEBMBI CFSBQBLBI OPNPS BUPN FMFLUSPOWBMFOTJEBOKVNMBIOFVUSPOOZB 1FSIBUJLBOCFCFSBQBVOTVSCFSJLVU
B /B
C ,
D (F
E 1
F "T
5FOUVLBOVOTVSVOTVSZBOHUFSMFUBLEBMBN
4JTUFN1FSJPEJL6OTVS
,
BMJBOUFOUVQFSOBINFNQFMBKBSJLMBTJGJLBTJIFXBOTFXBLUVLFMBT7**CVLBO )FXBO EBQBU EJLMBTJGJLBTJLBO NFOKBEJ IFXBO CFSUVMBOH CFMBLBOH WFSUFCSBUBEBOUJEBLCFSUVMBOHCFMBLBOH BWFSUFCSBUB7FSUFCSBUB NBTJI EBQBU EJLFMPNQPLLBO MBHJ CFSEBTBSLBO LFNJSJQBO TJGBUOZB 4BMBI TBUVOZBZBJUVLFMBTNBNBMJB,FSBEBOPSBOHVUBONFSVQBLBONBNBMJBZBOH NFNJMJLJLFNJSJQBOTJGBUZBLOJNFNJMJLJLFMFOKBSTVTVEBOCFSBNCVU #FHJUV QVMB EFOHBO VOTVS 6OTVSVOTVS EJLFMPNQPLLBO CFSEBTBSLBO LFNJSJQBOTJGBUTFIJOHHBQFMCBHBJVOTVSEBQBUEJTVTVOEBMBNUBCFMZBOH EJTFCVUUBCFMQFSJPEJLVOTVS#BHBJNBOBTJGBUTJGBUQFSJPEJLQFMCBHBJVOTVS UFSTFCVU 5FNVLBOKBXBCBOOZBEBMBNVSBJBOCFSJLVU
# B C
**
XXX
+BSJKBSJBUPNNFSVQBLBOTBMBITBUVTJGBUVOTVSZBOHCJTBEJQFMBKBSJ EBSJUBCFMQFSJPEJLVOTVS4FMBJOKBSJKBSJBUPNLBMJBOKVHBCJTBNFOHF UBIVJCFTBSOZBFOFSHJJPOJTBTJBGJOJUBTFMFLUSPOEBOLFFMFLUSPOFHBUJGBO UJBQVOTVS
1BEB CBC JOJ LBMJBO KVHB BLBO EJLFOBMLBO EFOHBO QFSLFNCBOHBO
TJTUFNQFSJPEJLVOTVSZBOHEJLFNVLBLBOPMFICFCFSBQBJMNVXBO%FOHBO EFNJLJBOLBMJBONBNQVNFOFOUVLBOQFSJPEFEBOHPMPOHBOUJBQVOTVS EBMBNTJTUFNQFSJPEJLVOTVS
A. Perkembangan Sistem Periodik Unsur
+JLBLBMJBOQFSOBIQFSHJLFLFCVOCJOBUBOHLBMJBOBLBONFMJIBUCBI
XBTJOHBEBOIBSJNBVCFSBEBEBMBNTBUVCMPLTFEBOHLBOCFSCBHBJKFOJT CVSVOHCFSBEBEJCMPLMBJO#JOBUBOHCJOBUBOHUFSTFCVUEJLFMPNQPLLBO CFSEBTBSLBOQFSTBNBBOTJGBUOZB
#FHJUV QVMB EFOHBO VOTVSVOTVS ZBOH BEB EJ BMBN 1BSB JMNVXBO
CFSVTBIB NFOHFMPNQPLLBOOZB BHBS NVEBI EJLFOBMJ EBO EJQFMBKBSJ 1F OHFMPNQPLBOVOTVSEJMBLVLBOBOUBSBMBJOCFSEBTBSLBOQFSCFEBBOXVKVE QBEBTVIVLBNBSZBJUVQBEBUDBJSEBOHBT.JTBMOZBCFTJ 'FCFSXVKVE QBEBUBJSCFSXVKVEDBJSEBOVBQBJSCFSXVKVEHBT
4FMBJOXVKVEVOTVSVOTVSKVHBEJLFMPNQPLLBOCFSEBTBSLBOTJGBUEBO
NBTTBVOTVSTFIJOHHBVOTVSVOTVSEBQBUEJTVTVOEBMBNUBCFMZBOHEJTF CVUUBCFMQFSJPEJL%FOHBONFOHHVOBLBOUBCFMQFSJPEJLEBQBUEJLFUBIVJ TJGBUTJGBUVOTVSEBMBNTBUVHPMPOHBONBVQVOTBUVQFSJPEF
#BHBJNBOB QFSLFNCBOHBO TJTUFN QFOHFMPNQPLBO VOTVSVOTVS 4J NBLVSBJBOCFSJLVU
1FOHFMPNQPLBO6OTVSVOTVS#FSEBTBSLBO4JGBU-PHBN
EBO/POMPHBN
1BEB BXBMOZB QBSB JMNVXBO NFOHFMPNQPLLBO VOTVSVOTVS TFDBSB
TFEFSIBOBCFSEBTBSLBOQFSCFEBBOTJGBUGJTJTOZB.JTBMOZBEFOHBODBSBNF MJIBULFNBNQVBOTVBUVVOTVSEBMBNNFOHIBOUBSLBOQBOBTBUBVMJTUSJL
6OTVS ZBOH NBNQV NFOHIBOUBSLBO QBOBT EJTFCVUVOTVS MPHBN
DPOUPI UFNCBHB CFTJ EBO QMBUJOVN TFEBOHLBO VOTVS ZBOH UJEBL
NBNQVNFOHIBOUBSLBOQBOBTEJTFCVUVOTVSOPOMPHBN DPOUPIPLTJHFO
Kata
Kunci
• Sistem periodikunsur • Jari-jari atom • Energi ionisasi • Afinitas elektron • Keelektronegatifan
Gambar 2.1
Pengelompokan binatang berdasarkan persamaan sifat.
Gambar 2.2
Wujud padat, cair, dan gas
XXX
GPDVTNNDP
VL1
"@XXX
HTQ
DD
EPL1
OJUSPHFOEBOIJESPHFO"HBSLBMJBOEBQBUNFNCFEBLBOVOTVSMPHBNEBO OPOMPHBNEFOHBOUFQBUQFSIBUJLBO5BCFMCFSJLVU
5BCFM4JGBU4JGBU'JTJT6OTVS-PHBNEBO/POMPHBN 6OTVS-PHBN 6OTVS/PO-PHBN
,POEVLUPS *TPMBUPS .FOHJMBQ 5JEBLNFOHJMBQ #FSTJGBUFMFLUSPQPTJUJG #FSTJGBUFMFLUSPOFHBUJG 0LTJEBOZBCFSTJGBUCBTB 0LTJEBOZBCFSTJGBUBTBN ,FSBQBUBOUJOHHJ ,FSBQBUBOSFOEBI
1BEBU 3BQVI
%FOHBO NFNBIBNJ QFOKFMBTBO EJ BUBT LBMJBO EBQBU NFNCFEBLBO
VOTVS MPHBN EBO OPOMPHBN 6OUVL NFOHVKJ QFNBIBNBO EJTLVTJLBO KBXBCBOQFSUBOZBBOCFSJLVU
D i s k u s i
Tentukan unsur-unsur yang termasuk unsur logam dan non-logam pada tabel berikut dengan memberi tanda ( ).
No Nama Unsur Lambang Unsur Sifat Unsur Logam Non-logam 1. Kalium K
2. Natrium Na 3. Oksigen O 4. Mangan Mg 5. Belerang S 6. Nitrogen N 7. Kalsium Ca
Untuk memperluas pengetahuan, carilah referensi dari buku-buku di perpustakaan dan internet mengenai sifat-sifat logam dan non-logam pada tujuh unsur di atas. Selanjutnya, diskusikan dengan teman-teman dan presentasikan hasil diskusi di depan kelas.
5FSOZBUBTFMBJOVOTVSMPHBNEBOOPOMPHBNNBTJIEJUFNVLBOCF
CFSBQBVOTVSZBOHNFNJMJLJTJGBUMPHBNEBOOPOMPHBN VOTVSNFUBMPJE NJTBMOZB VOTVS TJMJLPO BOUJNPO EBO BSTFO +BEJ QFOHHPMPOHBO VOTVS NFOKBEJVOTVSMPHBNEBOOPOMPHBNNBTJINFNJMJLJLFMFNBIBO
Gambar 2.3
Contoh unsur metaloid, yaitu (a) Antimon; (b) Arsen.
Unsur-unsur metaloid secara fisik memiliki bentuk seperti logam, tapi warna gelapnya agak berbeda jika dibandingkan dengan unsur logam.
(a) (b)
KNCSBEZ
FEKMEIBM
#SBEZ
IMN
Unsur-unsur metaloid memiliki sifat semikon-duktor yang spesifik, yaitu dapat menghan-tarkan listrik, tapi tidak seperti unsur logam. Sifat semikonduktor ini sangat berguna dalam industri elektronik, karena memungkinkan alat-alat mikroelektronik diperoleh dalam ukuran kecil, misalnya chip komputer (yang terbuat dari si-likon) dan kalkulator. Jika tidak dapat menghantar-kan listrik, unsur metaloid lebih bersifat non-logam.
XXX
GPDVTNNDP
VL
1FOHFMPNQPLBO6OTVS6OTVS#FSEBTBSLBO)VLVN5SJBEF
%PCFSFJOFS
1BEBCBCLBMJBOUFMBINFNQFMBKBSJNBTTBBUPN.BTTBBUPNBEBMBI
CBOZBLOZB KVNMBI QSPUPO EBO OFVUSPO ZBOH UFSEBQBU QBEB JOUJ BUPN .BTTBBUPNNFSVQBLBOTBMBITBUVTJGBULIBTZBOHEJNJMJLJPMFIVOTVS
1FOHFMPNQPLBO VOTVS CFSEBTBSLBO QFSCFEBBO NBTTB BUPNOZB
QFSUBNB LBMJ EJMBLVLBO PMFI+8 %PCFSFJOFS *B NFOZBUBLBO CBIXB
TFUJBQHPMPOHBOUFSEJSJBUBTUJHBVOTVSEBOVOTVSZBOHUFSMFUBLEJUFOHBI NFNQVOZBJNBTTBBUPNZBOHCFTBSOZBNFOEFLBUJSFSBUBNBTTBBUPNEBSJ VOTVSQFSUBNBEBOLFUJHB0MFILBSFOBJUVQFOFNVBO%PCFSFJOFSEJLFOBM
EFOHBO)VLVN5SJBEF
#BHBJNBOBQFOFSBQBO)VLVN5SJBEF "HBSMFCJINVEBINFNBIBNJ
IVLVNUFSTFCVUQFSIBUJLBODPOUPICFSJLVU
C o n t o h
6OTVS .BTTBBUPN 3FSBUBNBTTBBUPNVOTVSQFSUBNBEBOLFUJHB
6OTVSQFSUBNB -J
+
6OTVSLFEVB /B
6OTVSLFUJHB ,
6OTVS .BTTBBUPN 3FSBUBNBTTBBUPNVOTVSQFSUBNBEBOLFUJHB
6OTVSQFSUBNB #F
+
6OTVSLFEVB .H
6OTVSLFUJHB $B
6OTVS .BTTBBUPN 3FSBUBNBTTBBUPNVOTVSQFSUBNBEBOLFUJHB
6OTVSQFSUBNB "M
+
6OTVSLFEVB (B
6OTVSLFUJHB *O
1BEBDPOUPIEBOUFSMJIBUCBIXBSFSBUBNBTTBBUPNVOTVSQFS
UBNBEBOLFUJHBNFOEFLBUJNBTTBBUPNVOTVSLFEVB,BSFOBTJGBUJOJMBI VOTVSVOTVSUFSTFCVUEJLFMPNQPLLBOEBMBNTBUVLFMPNQPLZBOHEJTFCVU 5SJBEF
"HBSLBMJBOMFCJINVEBINFNCFEBLBOVOTVSZBOHNFNFOVIJEBO
UJEBLNFNFOVIJ)VLVN5SJBEFLFSKBLBOUVHBTEJSVCSJL%JTLVTJ
Walaupun Hukum Triade bisa diterapkan, ternyata bagi beberapa unsur, hu-kum Triade tidak berlaku.
D i s k u s i
Dengan menggunakan tabel periodik modern, carilah tiga unsur yang memenuhi dan tidak memenuhi Hukum Triade. Untuk men-dukung jawaban kalian, sertakan hasil perhitungan sesuai contoh 1, 2, dan 3. Kemudian, diskusikan dengan kelompok kalian dan presenta-sikan di depan kelas. Jangan lupa, konsultapresenta-sikan hasil diskusi kepada guru.
1FOHFMPNQPLBO6OTVS6OTVS#FSEBTBSLBO)VLVN0LUBG
/FXMBOET
,BSFOBUJEBLTFNVBVOTVSNFNFOVIJ)VLVN5SJBEFQBSBJMNVXBO
UFSVTNFODPCBVOUVLNFOFNVLBONFUPEFMBJOEBMBNQFOHFMPNQPLBOVO
TVS1BEBUBIVO+PIO"MFYBOEFS3FJOB/FXMBOET
TFPSBOH BIMJ LJNJB CFSLFCBOHTBBO *OHHSJT NFOZVTVO TVBUV UBCFM CFSEBTBSLBO LFOBJLBO NBTTB BUPNOZB5BCFM JOJ NFOVOKVLLBOLFNJSJQBO TJGBU ZBOH CFSVMBOH TFUJBQ EFMBQBOVOTVS+BEJVOTVSZBOHLFEFMBQBONFNJMJLJLFNJ SJQBOTJGBUEFOHBOVOTVSQFSUBNB4FEBOHLBOVOTVSLFEVB NFNJMJLJ LFNJSJQBO TJGBU EFOHBO VOTVS LFTFNCJMBO EBO TFUFSVTOZB4VTVOBOVOTVSVOTVSUFSTFCVUEJLFOBMTFCBHBJ
)VLVN0LUBG/FXMBOET
6OUVLMFCJIKFMBTOZBTJNBL5BCFM
T u g a s
Dengan memahami Tabel 2.2, kalian tentu dapat mengelompokkan unsur-unsur berdasarkan Hukum Oktaf, bukan? Nah, tugas kalian adalah mengelompokkan unsur-unsur dalam sistem periodik mo-dern berdasarkan Hukum Oktaf, kecuali unsur-unsur yang sudah dijelaskan pada Tabel 2.2. Kerjakan tugas pada buku tugas, lalu konsultasikan dengan guru.
5BCFM1FSJPEJL.FOEFMFZFW
4JTUFNQFSJPEJLVOTVSUFSVTNFOHBMBNJQFSLFNCBOHBO1BEBUBIVO
JMNVXBO EBSJ +FSNBO+VMJVT -PUIBS .FZFS EBO%NJUSZ .FO
EFMFZFW EBSJ 3VTJB NFOHFNCBOHLBO)VLVN 0LUBG /FXMBOETZBOH CFSLBJUBOEFOHBOQFOHVMBOHBOTJGBUVOTVSTFDBSBQFSJPEJL
1FOHHPMPOHBOVOTVSNFOVSVU.FOEFMFZFWNBTJICFSEBTBSLBOTJGBUTJGBU
LJNJBVOTVS6OTVSVOTVSEFOHBOTJGBUZBOHNJSJQEJMFUBLLBOQBEBTVBUVLP MPNZBOHEJTFCVUHPMPOHBO4FMBJOCFSEBTBSLBOLFNJSJQBOTJGBU.FOEFMFZFW KVHBNFOFOUVLBOVSVUBOVOTVSCFSEBTBSLBOLFOBJLBONBTTBBUPN
.FOEFMFZFWCFSQFOEBQBUCBIXBVSVUBOVOTVSCFSEBTBSLBOLFNJSJQBO
TJGBUMFCJIVUBNBEBSJQBEBLFOBJLBONBTTBBUPNOZB%FOHBOEFNJLJBO UBCFM.FOEFMFZFWNFNJMJLJLFMFNBIBOZBJUVVOTVSZBOHNFNJMJLJNBTTB BUPNMFCJICFTBSUFSMFUBLTFCFMVNVOTVSZBOHNFNJMJLJNBTTBBUPNMFCJI
5BCFM1FOHHPMPOHBO6OTVS
6OTVS.FOVSVU)VLVN0LUBG 6OTVS /PNPSBUPN 6OTVS /PNPSBUPN
) '
-J /B
#F .H
# "M
$ 4J
/ 1
0 4 4VLBS
EKPIMN
Dmitry Mendeleyev
(1834-1907) adalah seorang ahli kimia dari kekaisaran Rusia. Ia pernah menjadi guru besar kimia di Universitas St.Petersburg, Rusia.
Dmitri Mendeleev Buku konsep fisika modern edisii ke-empat hal 252.
GSXJLJQFEJB
LFDJM .JTBMOZB NBTTB BUPN EBSJ VOTVS UFMMVSJVN 5F EBO JPEJVN * EJEVHBEBOV6OTVS5FEBO*EJTVTVOUFSCBMJL NFOVSVUNBTTB BUPNLBSFOBTJGBUTJGBUUFMMVSJVNNBTVLEBMBNHPMPOHBO7*EBOTJGBUTJGBU JPEJVNNBTVLEBMBNHPMPOHBO7**
#BHBJNBOBVSVUBOVOTVSQBEBUBCFMQFSJPEJL.FOEFMFZFW 1FSIBUJLBO
5BCFMCFSJLVU
5BCFM1FSJPEJL.PEFSO
.FTLJQVO TJTUFN QFSJPEJL .FOEFMFZFW NBTJI NFNJMJLJ CFCFSBQB
LFMFNBIBO OBNVO TJTUFN QFSJPEJLOZB KBVI MFCJI CBJL EJCBOEJOHLBO TJTUFN QFOHFMPNQPLBO VOTVS NFOVSVU %PCFSFJOFS EBO /FXMBOET
4FMBOKVUOZBTFPSBOHJMNVXBONVEBCFSLFCBOHTBBO*OHHSJT)FOSZ.PTF
MFZNBNQVNFOZFNQVSOBLBOTJTUFNQFSJPEJL.FOEFMFZFW
1BEB UBIVO .PTFMFZ NFOZFMJEJLJ TFDBSB TJTUFNBUJT TQFLUSVN
TJOBS 9 EBO NFOHFUBIVJ BEBOZB IVCVOHBO BOUBSB QBOKBOH HFMPNCBOH TJOBS 9 EFOHBO OPNPS BUPNOZB %BSJ IBTJM QFOZFMJEJLBOOZB .PTFMFZ NFNPEJGJLBTJUBCFMQFSJPEJL.FOEFMFZFWEBONFOZVTVOVOTVSVOTVSCFS EBTBSLBOLFOBJLBOOPNPSBUPNOZB5BCFMQFSJPEJLJOJMBIZBOHLJUBQBLBJ
TBNQBJTFLBSBOHZBOHEJTFCVU5BCFM1FSJPEJL.PEFSO
T u g a s
Kalian telah mempelajari dasar pengelompokan unsur yang dikemuka-kan oleh Dobereiner, Newlands, Mendeleyev, dan Moseley. Banding-kan kelebihan dan kekurangan tiap-tiap pengelompoBanding-kan unsur terse-but. Carilah referensi dari buku-buku di perpustakaan dan internet. Selanjutnya, diskusikan dengan teman-teman dan presentasikan di depan kelas.
(SVQ* (SVQ** (SVQ*** (SVQ*7 (SVQ7 (SVQ7* (SVQ7** (SVQ7***
)
-J #F # $ / 0 '
/B .H "M 4J 1 4 $M
, $B o 5J 7 $S .O 'F$P
/J$V
$V ;O o o "T 4F #S
3C 4S :U ;S /C .P o 3V3I
1E"H
"H $E *O 4O 4C 5F *
$T #B %J $F o o o oo
oo
o o o o o o o
o o &S -B 5B 8 o 0T*S
1U"V
"V )H 5M 1C #J o o
o o o 5I o 6 o oo
oo
5BCFM5BCFM1FSJPEJL.FOEFMFZFW
#SBEZ
IMN
Henry Moseley (1887-1915) pada tahun 1913, ia memperkenalkan kon-sep nomor atom. Selain itu, ia juga menjelaskan sistem periodik unsur berdasarkan kenaikan nomor atom.
Profil Henry Moseley Konsep fisika modern edisi keempat hal 274
XXX
DIFNTPD
)BTJMQFOZVTVOBO4JTUFN1FSJPEJL.PEFSOPMFI.PTFMFZEBQBUEJMJ IBUQBEB5BCFMCFSJLVU
5BCFM5BCFM1FSJPEJL.PEFSO
U j i K o m p e t e n s i
Jawablah pertanyaan-pertanyaan berikut.
1. Jelaskan dasar pengelompokan unsur-unsur. 2. Terangkan pengelompokan unsur menurut
Do-bereiner. Agar lebih jelas, berilah contohnya. 3. Mengapa pengelompokkan unsur menurut
Newlands disebut Hukum Oktaf?
4. Jelaskan kelemahan tabel periodik Mendeleyev.
5. Terangkan pengelompokan unsur menurut Moseley.
B. Mengenal Tabel Periodik Unsur Modern
5BCFM1FSJPEJL.PEFSONFSVQBLBOUBCFMQFSJPEJLZBOHQBMJOHNVEBI
EJQBIBNJEBOEJQFMBKBSJEJCBOEJOHLBOUBCFMQFSJPEJLZBOHEJTVTVOPMFI .FOEFMFZFW5BCFM1FSJPEJL.PEFSOUFSEJSJBUBTMBKVSIPSJ[POUBMZBOHEJTF CVUQFSJPEFEBOMBKVSWFSUJLBMZBOHEJTFCVUHPMPOHBO6OUVLQFNBIBNBO MFCJIMBOKVUQFMBKBSJCBJLCBJLVSBJBOCFSJLVU
*" -PHBN
BMLBMJ UBOBI **"
/PNPS"UPN -BNCBOH6OTVS .BTTB"UPN3FMBUJG
***" *7" 7*" 7*" )BMPHFO
7**" (BT.VMJB
7***"
-PHBN #VLBO-PHBN -PHBNMPHBNUSBOTJTJEBMBN
-PHBNBMLBMJ
-PHBN .FUBMPJE #VLBO -PHBN
-BOUBOJEB "LUJOJEB "OHLBEBMBNUBOEBLVSVOHNFSVQBLBO OPNPSNBTTBJTPUPQQBMJOHTUBCJM
-PHBNMPHBNUSBOTJTJEBMBN
***# *7# 7# 7*# 7**# 7***# *# *#
#SBEZ
(PMPOHBO
4VBUVVOTVSEBMBNTJTUFNQFSJPEJLEJTVTVOCFSEBTBSLBOLPOGJHVSBTJ
FMFLUSPOOZB LBSFOB UJBQ VOTVS NFNJMJLJ LPOGJHVSBTJ FMFLUSPO ZBOH CFS CFEB%BSJLPOGJHVSBTJFMFLUSPOKVNMBILVMJUEBOFMFLUSPOWBMFOTJTVBUV VOTVSCJTBEJLFUBIVJ
"EBQVO VOTVSVOTVS ZBOH NFNJMJLJ LFTBNBBO KVNMBI FMFLUSPO
WBMFOTJEJTVTVOEBMBNTBUVMBKVSWFSUJLBMZBOHEJTFCVUHPMPOHBO6OTVS VOTVSZBOHCFSBEBEBMBNTBUVHPMPOHBOUFSTFCVUNFNJMJLJLFNJSJQBOTJGBU LJNJBEBOTJGBUGJTJLB
5BCFM1FSJPEJL.PEFSOUFSEJSJBUBTHPMPOHBOVUBNB HPMPOHBO"
EBOHPMPOHBOUSBOTJTJ HPMPOHBO#(PMPOHBOHPMPOHBOUFSTFCVUEJOB NBJTFTVBJEFOHBOOPNPSLFMPNQPLOZBTFQFSUJHPMPOHBO*"**"*#EBO TFUFSVTOZB #BILBO HPMPOHBO VUBNB NFNJMJLJ OBNB LIVTVT NJTBMOZB HPMPOHBO*"EJOBNBJHPMPOHBOBMLBMJEBOHPMPOHBO7***"EJOBNBJHPMPOHBO HBTNVMJB
4FNVB VOTVS HPMPOHBO USBOTJTJ NFSVQBLBO VOTVS MPHBN TFIJOHHB
CJBTBEJTFCVUMPHBNMPHBNUSBOTJTJ1BEBHPMPOHBOUSBOTJTJUFSEBQBUVOTVS VOTVSUSBOTJTJEBMBN(PMPOHBOUSBOTJTJEBMBNUFSEJSJBUBTVOTVSMBO UBOJEB UFSMFUBLTFUFMBIVOTVSMBOUBOJVNEBOVOTVSBLUJOJEB UFSMFUBL TFUFMBIVOTVSBLUJOJVN
1FSJPEF
%BMBN4JTUFN1FSJPEJL.PEFSOEBSJBUBTLFCBXBIUFSEBQBUMBKVS
IPSJ[POUBMZBOHEJTFCVUQFSJPEF%JOBNBLBOQFSJPEFLBSFOBTJGBUTJGBUZBOH EJNJMJLJVOTVSVOTVSEBMBNTBUVQFSJPEFCFSVMBOHTFDBSBQFSJPEJL6OTVS VOTVSZBOHNFNJMJLJKVNMBILVMJUZBOHTBNBEJTVTVOEBMBNTBUVQFSJPEF
+VNMBIVOTVSEBMBNUJBQQFSJPEFCFSCFEBZBJUV
1FSJPEFUFSEJSJBUBTVOTVSZBJUVIJESPHFOEBOIFMJVN 1FSJPEFUFSEJSJBUBTVOTVS
1FSJPEFUFSEJSJBUBTVOTVS 1FSJPEFUFSEJSJBUBTVOTVS 1FSJPEFUFSEJSJBUBTVOTVS 1FSJPEFUFSEJSJBUBTVOTVS
1FSJPEFNBTJICFMVNMFOHLBQVOTVSVOTVSOZBOBNVOTBBUJOJUFS EJSJBUBTVOTVS
%BMBNUBCFMQFSJPEJLVOTVSVOTVSUSBOTJTJEBMBNEJMFUBLLBOEJCB
HJBOCBXBIBHBSQFSJPEFEBONBLTJNBMCFSJTJVOTVS4FMBOKVUOZB CBHBJNBOBDBSBNFOFOUVLBOHPMPOHBOEBOQFSJPEFTVBUVBUPN 1FSIBUJ LBODPOUPICFSJLVU
C o n t o h
5FOUVLBOHPMPOHBOEBOQFSJPEFEBSJVOTVS/B$MEBO$B
+BXBC
/B HPMPOHBO*"QFSJPEF
$M HPMPOHBO7**"QFSJPEF
$B HPMPOHBO**"QFSJPEF
K i l a s
B A L I K
Elektron valensi adalah elektron yang terletak pada kulit terluar suatu atom.
Golongan Utama Golongan Nama
Golongan IA Alkali IIA Alkali tanah IIIA Aluminium IVA Karbon VA Nitrogen VIA Khalkogen VIIA Halogen VIIIA Gas mulia
T u g a s
Tentukan konfigurasi atom, golongan, dan periode dari unsur 13X,
33Y, dan 51Z. Tuliskan jawaban kalian pada buku tugas, lalu kon-sultasikan dengan guru kalian.
4JGBU1FSJPEJL6OTVSVOTVS
1BEB QFNCBIBTBO UFSEBIVMV LBMJBO UFMBI NFOHFUBIVJ CBIXB LPO
GJHVSBTJFMFLUSPOEBOFMFLUSPOWBMFOTJCFSQFSBOQFOUJOHEBMBNQFOFOUVBO TJGBUTJGBUTVBUVVOTVS1BEBUBCFMQFSJPEJLTJGBUTJGBUVOTVSCFSVMBOHTFDBSB QFSJPEJLTFIJOHHBEJTFCVUTJGBUQFSJPEJLVOTVS4JGBUTJGBUQFSJPEJLNFMJQVUJ KBSJKBSJ BUPN FOFSHJ JPOJTBTJ BGJOJUBT FMFLUSPO EBO LFFMFLUSPOFHBUJGBO 1FOKFMBTBOMFCJISJODJNFOHFOBJTJGBUTJGBUVOTVSBLBOEJCBIBTQBEBVSBJBO CFSJLVU
B +BSJKBSJ"UPN
"UPNUFSTVTVOBUBTJOUJEBOLVMJUBUPN+BSBL
BOUBSBJOUJEFOHBOLVMJUUFSMVBSTVBUVBUPNEJOB
NBLBO KBSJKBSJ BUPN 5BCFM NFOVOKVLLBO
KBSJKBSJBUPNCFCFSBQBVOTVSZBOHUFSEBQBUEBMBN UBCFMQFSJPEJL
%BSJ5BCFMEJLFUBIVJCBIXBKBSJKBSJBUPN
EBSJBUBTLFCBXBIEBMBNTBUVHPMPOHBOTFNBLJO CFTBS )BM JOJ EJTFCBCLBO KVNMBI LVMJU BUPNOZB TFNBLJOLFCBXBITFNBLJOCFTBSTFIJOHHBKBSBL EBSJJOUJLFLVMJUUFSMVBSOZBKVHBTFNBLJOCFTBS
6OUVLVOTVSZBOHCFSBEBEBMBNTBUVQFSJPEF
TFNBLJOLFLBOBOKBSJKBSJBUPNOZBTFNBLJOLFDJM )BMJOJUFSKBEJLBSFOBEBMBNTBUVQFSJPEFTFUJBQ VOTVSNFNJMJLJKVNMBILVMJUZBOHTBNBTFEBOH LBOKVNMBIFMFLUSPOWBMFOTJOZBTFNBLJOCBOZBL 4FIJOHHB HBZB UBSJLNFOBSJL BOUBSB QSPUPO EBO FMFLUSPOOZBTFNBLJOLVBUEBONFOZFCBCLBOKBSBL EBSJJOUJBUPNLFLVMJUUFSMVBSTFNBLJOLFDJM
-J
#F # $ / 0 '
/B
.H "M 4J 1 4 $M
,
$B (B (F "T 4F #S
3C
4S *O 4O 4C 5F *
$T
#F 5M 1C
5BCFM+BSJKBSJ"UPN#FCFSBQB6OTVS EBMBNTBUVBO"OHTUSPN
Gambar 2.4 Kecenderungan jari-jari atom
.&/*/(,"5
.&/*/(,"
5
4VLBS
EKPIMN
Jari-jari atom dipenga-ruhi oleh:
• Jumlah kulit • Jumlah elektron
D i s k u s i
Diketahui nomor atom dari unsur A, B, C, dan D masing-masing adalah 2, 8, 19, dan 20. Tentukan periode dan golongan dari tiap-tiap unsur tersebut. Kemudian, buatlah urutan kecenderungan kenaikan jari-jari atom. Diskusikan jawaban pertanyaan di atas dengan teman-teman, lalu konsultasikan dengan guru.
C&OFSHJ*POJTBTJ
1BEBLFBEBBOOFUSBMKVNMBINVBUBOQPTJUJGTVBUVBUPNTBNBEFOHBO
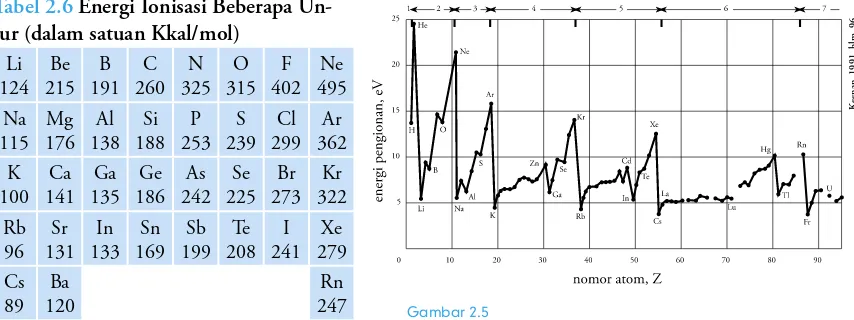
KVNMBINVBUBOOFHBUJGOZB4VBUVBUPNEBQBUNFNCFOUVLJPOQPTJUJGEF OHBODBSBNFMFQBTLBOFMFLUSPOQBEBLVMJUUFSMVBSOZB6OUVLEBQBUNF MFQBTLBOFMFLUSPOBUPNNFNFSMVLBOTFKVNMBIFOFSHJ&OFSHJNJOJNVN ZBOHEJQFSMVLBOPMFIBUPNOFUSBMEBMBNLFBEBBOHBTVOUVLNFMFQBTLBO TBUVCVBIFMFLUSPOQBEBLVMJUUFSMVBSOZBEJTFCVUFOFSHJJPOJTBTJ&OFSHJ JPOJTBTJCFCFSBQBVOTVSEBQBUEJMJIBUQBEB5BCFMEJCBXBI
%BSJ5BCFM EBQBU EJCVBU TVBUV HSBGJL IVCVOHBO BOUBSB FOFSHJ
JPOJTBTJEFOHBOOPNPSBUPNOZBTFCBHBJCFSJLVU
1FSIBUJLBO(BNCBS5BNQBLCBIXBVOTVSVOTVSQBEBQFSJPEF
NVMBJEBSJ-JTBNQBJ/FFOFSHJJPOJTBTJOZBTFNBLJOCFTBS%FNJLJBOKVHB VOUVLQFSJPEFZBOHMBJO%BMBNTBUVQFSJPEFEBSJLJSJLFLBOBOFOFSHJ JPOJTBTJOZBTFNBLJOCFTBS)BMJOJUFSKBEJLBSFOBEBMBNTBUVQFSJPEFTF NBLJOLFLBOBOKBSJKBSJBUPNTFNBLJOLFDJMTFIJOHHBHBZBUBSJLNFOBSJL BOUBSBQSPUPOQBEBJOUJBUPNEFOHBOFMFLUSPOQBEBLVMJUUFSMVBSOZBTFNB LJOCFTBS(BZBUBSJLZBOHTFNBLJOCFTBSNFOZFCBCLBOFMFLUSPOQBEBLV MJUUFSMVBSTVMJUVOUVLEJMFQBTLBO"LJCBUOZBFOFSHJJPOJTBTJKVHBTFNBLJO CFTBS
%BMBN TBUV HPMPOHBO EBSJ BUBT LF CBXBI FOFSHJ JPOJTBTJ BUPN TF NBLJO LFDJM )BM JOJ KVHB EJQFOHBSVIJ PMFI KBSJKBSJ BUPN %BMBN TBUV HPMPOHBOTFNBLJOLFCBXBIKBSJKBSJBUPNTFNBLJOCFTBS"LJCBUOZBHBZB
5BCFM&OFSHJ*POJTBTJ#FCFSBQB6O TVS EBMBNTBUVBO,LBMNPM
-J
#F # $ / 0 ' /F /B
.H "M 4J 1 4 $M "S ,
$B (B (F "T 4F #S ,S 3C
4S *O 4O 4C 5F * 9F $T
#B 3O Gambar 2.5
Grafik hubungan antara energi ionisasi dengan nomor atom
Semakin kecil jari-jari atom, energi ionisasinya semakin besar.
Sukardjo, 1990, hlm.381
,
FFOBOIMN
#
SBEZ
UBSJLNFOBSJLBOUBSBQSPUPOQBEBJOUJBUPNEFOHBOFMFLUSPOQBEBLVMJU UFSMVBSTFNBLJOMFNBITFIJOHHBFOFSHJJPOJTBTJOZBTFNBLJOLFDJM
Gambar 2.6 Kecenderungan energi ionisasi
.&/*/(,"5
.&/*/(,"
5
D i s k u s i
Bentuklah kelompok kecil yang terdiri atas 3 orang, lalu berdis-kusilah untuk menjawab pertanyaan berikut.
Tentukan urutan unsur yang memiliki energi ionisasi paling besar: Be, Mg, atau Ca?
Tuliskan hasil diskusi kalian disertai alasan secara lengkap, lalu presen-tasikan di depan kelas.
D "GJOJUBT&MFLUSPO
4VBUV VOTVS EBQBU NFNCFOUVL JPO QPTJUJG NF
MFQBTLBO FMFLUSPO EBO JPO OFHBUJG NFOFSJNB FMFL USPO#FSLFCBMJLBOEFOHBOQSPTFTQFMFQBTBOFMFLUSPO QSPTFT QFOFSJNBBO FMFLUSPO BLBO NFMFQBTLBO FOFSHJ &OFSHJ ZBOH EJCFCBTLBO PMFI BUPN OFUSBM EBMBN LF BEBBOHBTVOUVLNFOFSJNBTBUVCVBIFMFLUSPOEJTFCVU
BGJOJUBT FMFLUSPO "GJOJUBT FMFLUSPO CFCFSBQB VOTVS EBQBUEJMJIBUQBEB5BCFM
%BMBN TBUV QFSJPEF EBSJ LJSJ LF LBOBO IBSHB
BGJOUBT FMFLUSPO DFOEFSVOH TFNBLJO OFHBUJG )BM JOJ NFOZFCBCLBOTVBUVVOTVSTFNBLJONVEBINFOFSJNB FMFLUSPO4FCBMJLOZBEBMBNTBUVHPMPOHBOEBSJBUBTLF CBXBIIBSHBBGJOJUBTFMFLUSPOTFNBLJOQPTJUJGTFIJOHHB TFNBLJOTVMJUVOUVLNFOFSJNBFMFLUSPO
Gambar 2.7 Kecenderungan afinitas elektron
.&/*/(,"5
.&/*/(,"
5
5BCFM"GJOJUBT&MFLUSPO#FCFSBQB 6OTVS EBMBNTBUVBOL+NPM
-J #F # $ / 0 '
/B .H "M 4J 1 4 $M
, $B (B (F "T 4F #S 3C 4S *O 4O 4C 5F *
#SBEZ
IMN
EPL1
*.
EPL1
D i s k u s i
Berdasarkan Tabel 2.7, diketahui bahwa unsur golongan IA, IIIA, IVA, VA, VIA, dan VIIA memiliki afinitas elektron bertanda negatif. Sedangkan unsur golongan IIA memiliki afinitas elektron bertanda positif. Diskusikan alasan penggunaan tanda negatif dan positif pada harga afinitas elektron dengan teman-teman kalian. Selanjutnya, pre-sentasikan hasil diskusi di depan kelas.
E ,FFMFLUSPOFHBUJGBO
,FFMFLUSPOFHBUJGBO BEBMBI VLVSBO LFNBNQVBO TVBUV BUPN VOUVL
NFOBSJL QBTBOHBO FMFLUSPO EBMBN TVBUV JLBUBO,FFMFLUSPOFHBUJGBOEJ OZBUBLBO EBMBN 4LBMB 1BVMJOH EJ NBOB IBSHB LFFMFLUSPOFHBUJGBO ZBOH UFSCFTBSEJCFSJTLBMBTFEBOHLBOZBOHUFSLFDJMEJCFSJTLBMB1FSIBUJ LBO5BCFMCFSJLVU
5BCFM)BSHB,FFMFLUSPOFHBUJGBO#FCFSBQB6OTVS 4LBMB1BVMJOH
) -J
#F # $ / 0 ' /B
.H "M 4J 1 4 $M ,
$B 4D 5J 7 $S .O 'F $P /J $V ;O (B (F "T 4F #S 3C
4S : ;S /C .P 5D 3V 3I 1E "H $E *O 4O 4C 5F * $T
#B -B )G 5B 8 3F 0T *S 1U "V )H 5M 1C #J 1P "U 'S
3B "D -BOUIBOJEFTo"DUJOJEFTo
%BSJ5BCFMEBQBUEJLFUBIVJCBIXBEBMBNTBUVQFSJPEFEBSJLJSJLF
LBOBOIBSHBLFFMFLUSPOFHBUJGBOOZBTFNBLJOCFTBS)BMJOJUFSKBEJLBSFOB TJGBUMPHBNOZBTFNBLJONFOVSVO4FEBOHLBOVOUVLVOTVSVOTVSEBMBN TBUVHPMPOHBOEBSJBUBTLFCBXBIIBSHBLFFMFLUSPOFHBUJGBOOZBTFNBLJO NFOVSVO
Gambar 2.8 Kecenderungan keelektronegatifan atom
.&/*/(,"5
.&/*/(,"
5
Semakin besar jari-jari atom, keelektronegatif-annya semakin kecil.
Sukardjo, 1990, hlm.381
Logam timah (Sn) di Indonesia banyak dite-mukan di Pulau Bangka, Belitung dan Singkep. Logam nikel (Ni) terdapat di sekitar Danau Matana, Danau Towuti dan di Kolaka.
Logam tembaga (Cu) terdapat di Wonogiri, Muara Simpeng, dan Tembagapura. Sedan-gkan logam emas (Au) dan perak (Ag) banyak terdapat di Tembagapu-ra, Tasikmalaya, Simau, Logos, dan Meulaboh.
Sumber: www.chem-is-try.org
#SBEZ
IMN
EPL1
D i s k u s i
Mengapa unsur yang memiliki harga keelektronegatifan terbe-sar adalah fluorin?
Diskusikan jawaban pertanyaan di atas dengan teman-teman, lalu presentasikan di kelas.
U j i K o m p e t e n s i
Jawablah pertanyaan-pertanyaan berikut.
1. Jelaskan dasar penyusunan unsur-unsur dalam satu periode dan satu golongan.
2. Bandingkan besarnya harga jari-jari atom dari ion positif dengan ion negatif.
3. Sebutkan unsur yang memiliki energi ionisasi terbesar dan terkecil dalam tabel periodik. 4. Mengapa suatu unsur yang memiliki afinitas
elektron dengan harga positif semakin sulit
untuk menerima elektron? Jelaskan jawaban kalian.
5. Apakah yang dimaksud dengan keelektro-negatifan? Bagaimana
kecenderungannya dalam satu periode?
R a n g k u m a n
1. Sejarah perkembangan sistem periodik unsur meliputi:
2. Unsur-unsur yang memiliki kesamaan elektron valensi terletak pada satu golongan.
3. Unsur-unsur yang memiliki kesamaan jumlah kulit atom terletak pada satu periode.
4. Sifat-sifat periodik unsur meliputi:
a. Jari-jari atom adalah jarak antara inti dengan kulit terluar suatu atom. Jari-jari
atom meningkat dari atas ke bawah dan dari kanan ke kiri.
b. Energi ionisasi adalah energi minimum yang diperlukan oleh atom netral dalam keadaan gas untuk melepaskan satu buah elektron pada kulit terluarnya. Energi ionisasi meningkat dari bawah ke atas dan dari kiri ke kanan.
c. Afinitas elektron adalah energi yang dibebaskan oleh atom netral dalam keadaan gas untuk menerima satu buah elektron. Afinitas elektron meningkat da-ri bawah ke atas dan dada-ri kida-ri ke kanan. d. Keelektronegatifan adalah ukuran
kemampuan suatu atom untuk menarik pasangan elektron dalam suatu ikatan. Keelektronegatifan me-ningkat dari bawah ke atas dan dari kiri ke kanan. Hukum Triade
Dobereiner
Hukum Oktaf Newlands
Sistem Periodik Mendeleyev
Sistem Periodik Modern
Pengelompokan ber-dasarkan sifat logam dan non logam
Afinitas Daya tarik atau daya gabung suatu zat dengan zat lainnya
Ionisasi Peristiwa atau proses pembentukan ion dari atom atau molekul netral
Metaloid Nama lainnya adalah semilogam, yaitu unsur yang sifatnya cenderung mirip logam, namun dalam hal lain memperlihatkan sifat non-logam
Sistem Periodik Unsur Sistem pengelompo-kan unsur berdasarpengelompo-kan hukum periodik, men-cakup golongan dan periode yang keduanya saling berhubungan dan menentukan keperio-dikan sifat unsur, dan disajikan dalam bentuk tabel yang disebut Tabel Periodik Unsur.
G l o s a r i u m
A Pilihlah jawaban yang tepat.
4JGBUCFSJLVUZBOHUFSNBTVLTJGBUVOTVSMP HBNBEBMBIy
" TVLBSNFOHIBOUBSLBOQBOBT # CFSTJGBUJTPMBUPS
$ XBSOBOZBNFOHJMBQ
% CFSXVKVEHBTQBEBTVIVLBNBS & TVLBSEJUFNQB
4JGBUCFSJLVUZBOHUFSNBTVLTJGBUVOTVSOPO MPHBNBEBMBIy
" LPOEVLUPSZBOHCBJL # EBQBUEJUFNQB $ LFSBQBUBOUJOHHJ % NFOHJMBQ
& PLTJEBOZBCFSTJGBUBTBN
6OTVSZBOHNFNJMJLJTJGBUMPHBNEBOOPO MPHBNBEBMBIy
" QFSBL # BJSSBLTB $ IJESPHFO % TJMJLPO & IFMJVN
U
l a n g a n
H a r i a n
1FOHHPMPOHBO VOTVS CFSEBTBSLBO LFOBJLBO NBTTBBUPNSFMBUJGEJLFNVLBLBOPMFI " /FXMBOET
# -BWPJTJFS $ %PCFSFJOFS % .FOEFMFZFW & 3VUIFSGPSE
1FOHFMPNQPLBOVOTVSZBOHUFSEJSJBUBTUJHB VOTVSEFOHBOLFNJSJQBOTJGBUEJLFNVLBLBO PMFI
" 5IPNTPO # %PCFSFJOFS $ .FOEFMFZFW % /FXMBOET & $IBEXJDL
*MNVXBOZBOHNFNFMPQPSJQFOHFMPNQPLBO VOTVSEFOHBONFNFSIBUJLBOLFNJSJQBOTJ GBUEBMBNTBUVLPMPNWFSUJLBMBEBMBI " %BMUPO
4FTVBJEFOHBOIVLVNPLUBG/FXMBOETVO TVSEFOHBONBTTBBUPNSFMBUJGNFNQVOZBJ LFNJSJQBOTJGBUEFOHBOVOTVSZBOHNFNJMJLJ NBTTBBUPN
" # $ % &
4JTUFN 1FSJPEJL .PEFSO EJTVTVO CFSEBTBS LBO
" LFOBJLBONBTTBBUPN # LFOBJLBOOPNPSBUPN $ FOFSHJJPOJTBTJ
% KBSJKBSJBUPN & LFFMFLUSPOFHBUJGBO
1FODFUVT TJTUFN QFSJPEJL VOTVS NPEFSO BEBMBI
" +PIO%BMUPO # %PCFSFJOFS $ )FOSZ.PTFMFZ % %NJUSJ.FOEFMFZFW & -PUIBS.FZFS
1FOHHPMPOHBO VOTVSVOTVS NFOVSVU .FO EFMFZFWEJTVTVOCFSEBTBSLBO
" OPNPSBUPN # OPNPSNBTTB $ TJGBUVOTVS % JTPUPQ & FMFLUSPO
(PMPOHBOZBOHEJTFCVUHPMPOHBOHBTNVMJB BEBMBI
" *" # ***" $ 7" % 7**" & 7****"
6OTVS ZBOH CFSBEB EBMBN TBUV HPMPOHBO NFNJMJLJQFSTBNBBO
" KVNMBIFMFLUSPOWBMFOTJ # KVNMBIQSPUPO
$ TJGBULFFMFLUSPOFHBUJGBO % KBSJKBSJBUPN
& IBSHBQPUFOTJBMJPOJTBTJ
/BNBHPMPOHBO7**"EBMBNTJTUFNQFSJPEJL NPEFSOBEBMBI
" BMLBMJ # BMLBMJUBOBI $ HBTNVMJB % IBMPHFO & USBOTJTJEBMBN
4VBUV VOTVS EFOHBO LPOGJHVSBTJ FMFLUSPO UFSMFUBLQBEBQFSJPEFy
" # $ % &
6OTVSVOTVS ZBOH UFSEBQBU QBEB HPMPOHBO HBTNVMJBCFSTJGBUTUBCJMLBSFOBKVNMBIFMFL USPOQBEBLVMJUUFSMVBSOZBBEBMBI "
# $ % &
6OTVS GMPVS EFOHBO OPNPS BUPN EBMBN UBCFMQFSJPEJLVOTVSVOTVSUFSMFUBLQBEB " HPMPOHBO*"QFSJPEF
# HPMPOHBO***"QFSJPEF $ HPMPOHBO7"QFSJPEF % HPMPOHBO7**"QFSJPEF & HPMPOHBO7***"QFSJPEF
1BEBQFSJPEFLBMJVNNFNQVOZBJKBSJKBSJ BUPNUFSCFTBSIBMJOJEJTFCBCLBOPMFI " VOTVS,CFSTJGBUMPHBN
# VOTVS,NFNJMJLJKVNMBIFMFLUSPOWB MFOTJQBMJOHCBOZBL
$ VOTVS,NFNJMJLJKVNMBIFMFLUSPOQB MJOHCBOZBL
% VOTVS,CFSTJGBUSFBLUJG
& VOTVS,NFNJMJLJLFSBQBUBOZBOHLFDJM %J BOUBSB VOTVS CFSJLVU VOTVS NBOBLBI
ZBOHNFNJMJLJFOFSHJJPOJTBTJUFSCFTBS " #
% 0 & '
6OTVSZBOHNFNJMJLJBGJOJUBTFMFLUSPOUFSLF DJMBEBMBIy
" $M # 4 $ 1 % 4J & "M
6SVUBOVOTVSCFSJLVUZBOHNFOHBMBNJQF OJOHLBUBOLFFMFLUSPOFHBUJGBOBEBMBIy " #$EBO/
# /0EBO# $ $/EBO# % #/EBO$ & $'EBO/
B Jawablah pertanyaan-pertanyaan berikut.
5FSBOHLBOQFSLFNCBOHBOEBTBSQFOHFMPN QPLBOVOTVSVOTVSTFDBSBTJOHLBU
+FMBTLBO QFSCFEBBO TJGBU VOTVS MPHBN EBO OPOMPHBN "HBS MFCJI KFMBT CFSJMBI DPO UPIOZBNBTJOHNBTJOH
+FMBTLBO LFMFCJIBO EBO LFLVSBOHBO QFOHF MPNQPLBOVOTVSPMFI%PCFSFJOFSEBO0LUBG /FXMBOET
+FMBTLBO TJTUFN QFSJPEJL VOTVS NFOVSVU .PTFMFZ
5FOUVLBO QFSJPEF EBO HPMPOHBO QBEB VO TVSVOTVSCFSJLVU
B 9
C :
D ;
+FMBTLBOTJGBUTJGBUVOTVSEBMBNTJTUFNQFSJP EJL
+FMBTLBO IVCVOHBO KBSJKBSJ BUPN EFOHBO KVNMBILVMJUQBEBTVBUVBUPN
+FMBTLBO LFDFOEFSVOHBO FOFSHJ JPO JTBTJ EBMBN TBUV QFSJPEF EBO TBUV HPMPOHBO .FOHBQB BGJOJUBT FMFLUSPO EBMBN TBUV
HPMPOHBOEBSJBUBTLFCBXBITFNBLJOLFDJM +FMBTLBOKBXBCBOLBMJBO
1
FSOBILBILBMJBONFNFSIBUJLBOPSBOHZBOHTFEBOHNFOBSJEBOTBMJOH CFSQFHBOHBOUBOHBO 4BNBIBMOZBEFOHBOQFOBSJTFCBHJBOCFTBSVO TVSZBOHBEBEJBMBNKVHBNFNJMJLJiUBOHBOwZBOHTBMJOHCFSJLBUBO6OTVS VOTVSUFSTFCVUCFSJLBUBOVOUVLNFODBQBJLFTUBCJMBO/BIBQBTBKBVOTVS VOTVSZBOHEBQBUCFSJLBUBO #BHBJNBOBLBIJLBUBOZBOHUFSKBEJ 4JNBLMBI VSBJBOCFSJLVUVOUVLNFOHFUBIVJKBXBCBOOZBXXX
NJOBIBTBHP
JE
# B C
***
4FCBHJBOCFTBSVOTVSZBOHBEBEJBMBNNFNQVOZBJLFDFOEFSVOHBO VOUVLCFSJOUFSBLTJ CFSJLBUBOEFOHBOVOTVSMBJO)BMJUVEJMBLVLBOLBSF OBVOTVSUFSTFCVUJOHJONFODBQBJLFTUBCJMBO*OUFSBLTJZBOHUFSKBEJBOUBS VOTVSEJTFCBCLBOPMFIJLBUBOJPOJLBUBOLPWBMFO UVOHHBMSBOHLBQEVB EBOSBOHLBQUJHBJLBUBOLPPSEJOBTJTFSUBJLBUBOMPHBN
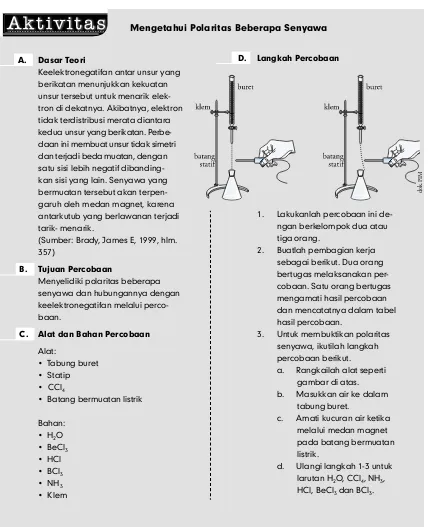
,BMJBO CJTB NFOFOUVLBO KFOJT JLBUBO ZBOH UFSKBEJ BOUBS VOTVS
EFOHBO CFSCBHBJ DBSB BOUBSB MBJO EFOHBO NFOHFUBIVJ TJGBU GJTJTOZB NFOFOUVLBO TVTVOBO FMFLUSPO EJ LVMJU UFSMVBSOZB FMFLUSPO WBMFOTJ NFOZFMJEJLJQPMBSJUBTUJBQVOTVSTFSUBNFOHIVCVOHLBOOZBEFOHBOTJGBU LFFMFLUSPOFHBUJGBONFMBMVJQFSDPCBBO
A. Kestabilan Unsur
4FCBHJBOCFTBSVOTVSEJBMBNJOHJONFODBQBJTVBUVLFTUBCJMBO,F
TUBCJMBOEJQFSPMFIEFOHBODBSBCFSHBCVOHEFOHBOVOTVSMBJOMBMVNFN CFOUVLTVBUVNPMFLVMBUBVTFOZBXBZBOHTUBCJM,FNBNQVBOCFSHBCVOH UFSTFCVU UFSKBEJ LBSFOB HBZB UBSJLNFOBSJL BOUBS VOTVS BUPN %FOHBO EFNJLJBOTFUJBQBUPNBUBVVOTVSEBQBUNFNCFOUVLTFOZBXBZBOHLIBT EBOCFSCFEBLBSFOBLFLVBUBOEBZBUBSJLNFOBSJLBOUBSBUPNNFNFOHB SVIJTJGBUTFOZBXBZBOHUFSCFOUVL%BZBUBSJLNFOBSJLBOUBSBUPNZBOH
NFOZFCBCLBOTVBUVTFOZBXBLJNJBEBQBUCFSTBUVEJTFCVUJLBUBOLJNJB
*LBUBO LJNJB EJUFNVLBO QFSUBNB LBMJ PMFI JMNVXBO BTBM "NFSJLB
4FSJLBUCFSOBNB(JMCFSU/FXUPO-FXJTQBEBUBIVO,POTFQJLBUBO
LJNJBZBOHEJLFNVLBLBOPMFILFEVBOZBTFCBHBJCFSJLVU
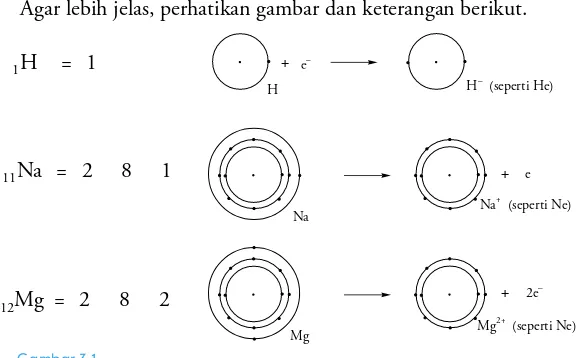
(BTNVMJB )F/F"S9FEBO3OTVLBSNFNCFOUVLTFOZBXBLBSF OBHBTNVMJBNFNJMJLJTVTVOBOFMFLUSPOZBOHTUBCJM UJEBLNFMFQBT EBONFOFSJNBFMFLUSPOEJLVMJUUFSMVBSOZBTFIJOHHBEJTFCVUJOFSU 4FUJBQBUPNJOHJONFNJMJLJTVTVOBOFMFLUSPOZBOHTUBCJMEFOHBODBSB
NFMFQBTLBOBUBVNFOBOHLBQFMFLUSPO
4VTVOBO FMFLUSPO ZBOH TUBCJM EJDBQBJ EFOHBO DBSB CFSJLBUBO BOUBS BUPNMBJO
,FTUBCJMBOBUPNUFSCFOUVLKJLBBUPNNFNJMJLJBUBVFMFLUSPOEJ
LVMJUUFSMVBSOZB6OTVSHBTNVMJBUFSNBTVLHPMPOHBOZBOHQBMJOHTUBCJM EBMBN TJTUFN QFSJPEJL VOTVS "HBS LBMJBO MFCJI NFNBIBNJ LFTUBCJMBO BUPN QFSIBUJLBO TVTVOBO LPOGJHVSBTJ FMFLUSPO VOTVSVOTVS HBT NVMJB CFSJLVU
)F )FMJVN
/F /FPO
"S "SHPO
,S ,SJQUPO
9F 9FOPO
3O 3BEPO
Kata
Kunci
+JLB LBMJBO NFNFSIBUJLBO LPOGJHVSBTJ FMFLUSPO HBT NVMJB EFOHBO TBLTBNB LBMJBO BLBO NFOHFUBIVJ CBIXB TFNVB VOTVS ZBOH UFSNBTVL HPMPOHBOHBTNVMJBNFNJMJLJFMFLUSPOEJLVMJUUFSMVBSOZB PLUFULFDVBMJ VOTVS)FZBOHNFNJMJLJFMFLUSPOEJLVMJUUFSMVBSOZB EVQMFU+BEJLFTUB CJMBOVOTVSHBTNVMJBUFSKBEJLBSFOBNFNJMJLJFMFLUSPOQBEBLVMJUUFSMVBS FMFLUSPOWBMFOTJ
4FNFOUBSBJUVBEBLFUFOUVBOMBJOCBHJVOTVSVOTVSZBOHUJEBLNFNJ
MJLJFMFLUSPOQBEBLVMJUUFSMVBSOZB,BSFOBTFNVBVOTVSNFNJMJLJLFDFO EFSVOHBOVOUVLNFODBQBJLFTUBCJMBONBLBUJBQVOTVSCFSHBCVOHEFOHBO VOTVS MBJO HVOB NFNFOVIJ BUVSBO PLUFU $BSBOZB EFOHBO NFNCFOUVL JLBUBOLJNJBZBJUVUJBQVOTVSTBMJOHCFSUVLBSFMFLUSPOVOUVLNFNFOVIJ FMFLUSPOQBEBLVMJUUFSMVBSOZB
C o n t o h
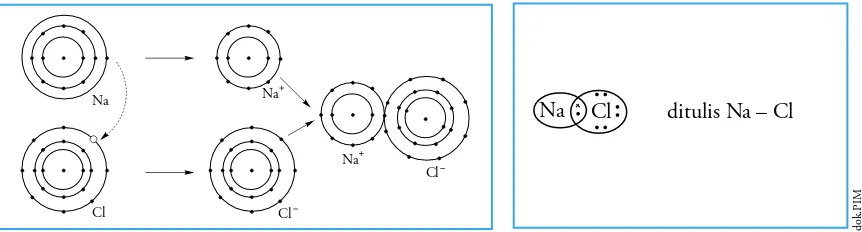
+FMBTLBOTFDBSBTJOHLBUUFSCFOUVLOZBJLBUBOQBEBTFOZBXB/B$M +BXBC
4VTVOBOFMFLUSPOQBEBVOTVSOBUSJVN /BEBOLMPS $MZBJUV
/B
$M
1FSIBUJLBOKVNMBIFMFLUSPOQBEBLVMJUUFSMVBSVOTVS/BEBO$M6OUVL NFODBQBJBUVSBOPLUFUVOTVS/BNFMFQBTLBOFMFLUSPOQBEBLVMJUUFS MVBSOZBTFEBOHLBOVOTVS$MNFOFSJNBBUBVNFOBOHLBQFMFLUSPOVOUVL NFODBQBJ BUVSBO PLUFU +BEJ BOUBS VOTVS /B EBO $M NFMBLVLBO TFSBI UFSJNBFMFLUSPOVOUVLNFNCFOUVLTFOZBXB/B$M
D i s k u s i
Jelaskan terjadinya pelepasan dan penerimaan elektron pada senyawa-senyawa berikut.
a. BeCl3 c. MgCl2 e. KCl b. CaCl3 d. HCl
Agar jawaban kalian lebih tepat, diskusikan dengan teman-teman.
Kemudian, konsultasikan kepada guru untuk menguji kebenaran jawaban kalian.
#FSEBTBSLBO DPOUPI TPBM EJ BUBT LBMJBO UFMBI NFOHFUBIVJ CBIXB
VOTVS/BNFNJMJLJLFDFOEFSVOHBOVOUVLNFMFQBTLBOFMFLUSPOTFIJOHHB CFSTJGBUMFCJIQPTJUJGBUBVFMFLUSPQPTJUJG6OTVSZBOHCFSTJGBUFMFLUSPQPTJUJG
EJMBNCBOHLBOEFOHBO9OEFOHBO9TFCBHBJVOTVSUFSTFCVUONFOVOKVL
C o n t o h
5FOUVLBOLPOGJHVSBTJFMFLUSPOEBSJVOTVSZBOHCFSTJGBUFMFLUSPQPTJUJGCFSJLVU
.BHOFTJVN "MVNJOJVN
/BUSJVN #FSJMJVN
+BXBC
.H .H
/B /B
"M "M
#F #F
4FNFOUBSBJUVVOTVS$MNFNJMJLJLFDFOEFSVOHBONFOZFSBQFMFLUSPO
TFIJOHHBCFSTJGBUMFCJIOFHBUJGBUBVFMFLUSPOFHBUJG6OTVSZBOHCFSTJGBUFMFL
USPOFHBUJGEJMBNCBOHLBOEFOHBOTJNCPM9OoEFOHBOOBEBMBIKVNMBIFMFL
USPOZBOHEJTFSBQEBOTJNCPMoVOUVLNFOVOKVLLBOTJGBUFMFLUSPOFHBUJG
6OUVLNFNQFSNVEBIQFOFOUVBOVOTVSZBOHCFSTJGBUFMFLUSPOFHBUJG
QFSIBUJLBODPOUPICFSJLVU
C o n t o h
5FOUVLBOLPOGJHVSBTJFMFLUSPOEBSJVOTVSZBOHCFSTJGBUFMFLUSPOFHBUJGCFSJLVU
0LTJHFO *PE #SPN
'MVPS ,MPS
+BXBC
0 0o
' 'o
* *o
$M $Mo
#S #So
U j i K o m p e t e n s i
Jawablah pertanyaan-pertanyaan berikut.
1. Bagaimana cara suatu unsur mencapai kesta-bilan? Jelaskan beserta contohnya.
2. Jelaskan konsep ikatan kimia yang dikemuka-kan oleh Gilbert Newton Lewis dan Albrecht Kossels.
3. Tentukan notasi penulisan sifat keelektronega-tifan untuk setiap unsur golongan A.
4. Jelaskan alasan suatu unsur ber-sifat:
a. elektropositif b. elektronegatif
B. Struktur Lewis
"OUBS VOTVS TBMJOH CFSJOUFSBLTJ EFOHBO NFOFSJNB EBO NFMFQBTLBO FMFLUSPO EJ LVMJU UFSMVBSOZB (BNCBSBO UFSKBEJOZB JOUFSBLTJ BOUBS VOTVS
4USVLUVS-FXJTEJMBNCBOHLBOEFOHBONFNCFSJLBOTFKVNMBIUJUJLZBOH NFOHFMJMJOHJBUPNOZB CJBTBOZBEJMBNCBOHLBOEFOHBO BUBVt4FUJBQUJUJL
NFXBLJMJTBUVFMFLUSPOZBOHBEBQBEBLVMJUUFSMVBSBUPNUFSTFCVU
1FSIBUJLBO 5BCFM UFOUBOH 4USVLUVS -FXJT CFSEBTBSLBO TVTVOBO
FMFLUSPOWBMFOTJEBSJVOTVSHBTNVMJB HPMPOHBO7***"ZBOHNFNFOVIJ BUVSBOPLUFUBUBVEVQMFUCFSJLVU
5BCFM4USVLUVS-FXJT6OTVS(PMPOHBO7***"
6OTVS &MFLUSPO7BMFOTJ 4USVLUVS-FXJT
)F )FMJVN )F
/F /FPO /F
"S "SHPO