6 II TINJAUAN PUSTAKA
2.1 Tandan Kosong Kelapa Sawit (TKKS)
Pohon kelapa sawit (elaeis guneensis jacq.) termasuk jenis tumbuhan gramineae, kelas monocotyledonae, famili aracaceae ordo cocoideae (Tomlinson,1961). Bagian terpenting dari pohon kelapa sawit tersebut adalah tandan buah segar (TBS). Setiap tandan mengandung 62 – 70 % buah sawit sebagai sumber produksi minyak sawit sedang sisanya adalah tandan kosong kelapa sawit (TKKS) yang mencapai 23-30 % . Dalam proses produksi minyak sawit, TKKS merupakan limbah padat dalam jumlah yang cukup besar. Komponen utama TKKS adalah selulosa, hemiselulosa dan lignin sehingga TKKS disebut limbah lignoselulosa. Potensi limbah lignoselulosa cukup besar dan secara umum semua limbah lignoselulosa termasuk TKKS mempunyai sifat fisika dan kimia yang hampir sama, sehingga proses pengolahan dan pemanfaatannya juga sama, hanya saja kondisi optimum untuk bahan satu dan lainnya akan berbeda (Fauzi dkk, 2002).
TKKS dapat dimanfaatkan melalui biokonversi yaitu dapat dijadikan substrat (bahan dasar) dalam pembuatan asam-asam organik, pelarut aseton, butanol, etanol, protein sel tunggal, dan zat antibiotika (Darnoko, 1992). Selain itu arah pengembangan TKKS juga dapat dimanfaatkan sebagai bahan baku produk berbasis selulosa seperti pulp dan kertas, serta produk berbahan baku lignin seperti lignosulfonat. Untuk mendapatkan selulosa dan lignin isolat masing-masing dengan kemurnian tinggi diperlukan pelarut yang tepat dan selektif, alkali merupakan pelarut lignin disamping berfungsi sebagai agen penggembung (swelling agent) untuk selulosa. Pengolahan selulosa dengan cara hidrolisis dan fermentasi, sedang pengolahan lignin dengan cara hidrogenolisis, hidroalkilasi dan sulfonasi (Darnoko et al,1995 dan David et al, 1996)
Gambar visual tandan kosong kelapa sawit (TKKS), disajikan pada Gambar 2.1
Gambar 2.1 Tandan kosong kelapa sawit (TKKS). 6
Hasil dari beberapa penelitian, komposisi kimia TKKS dapat dilihat pada Tabel 2.1
Tabel 2.1 Komposisi kimia TKKS (% bobot kering)
Komposisi Azemi dkk.*) 1994 Darnoko dkk. 1995 Selulosa 40 38,76 Lignin 21 22,23 Hemiselulosa 24 32,42 Abu 15 6,59
*) diacu dalam Fauzy dkk, 2002.
2.2 Lignin
Lignin adalah zat organik polimer yang komplek, merupakan komponen kimia dan morfologi dari jaringan tumbuhan seperti kayu daun jarum (gimnosperm) , kayu daun lebar (dikotil angiosperm), dan rerumputan/gramineae (monokotil angiosperm) dimana ia terdapat dalam jaringan vaskuler yang khusus untuk pengangkutan cairan dan kekuatan mekanik. Monomer lignin adalah fenilpropana, sedangkan unit pembentuk lignin adalah p-koumaril alkohol, koniferil alkohol dan sinapsil alkohol merupakan senyawa induk (prekursor) primer lignin seperti disajikan pada Gambar 2.2
Menurut Fengel and Wegener (1995), lignin dapat dibagi menjadi dua kelompok berdasarkan unsur-unsur strukturnya yaitu: Lignin guaiasil : terdapat
CH OH HC CH OH OCH3 CH2OH HC CH OH OCH3 CH3O CH2OH HC 1 2 3 CH2OH
Gambar 2.2 Unit pembentukan lignin (1) p-koumaril alkohol, (2) koniferil alkohol, (3) sinapsil alkohol.
8 pada kayu daun jarum, sebagian besar merupakan produk polimerisasi dari koniferil alkohol; lignin guaiasil-siringil : terdapat khas kayu daun lebar, merupakan kopolimer dari koniferil alkohol dan sinapil alkohol. Jumlah kandungan lignin yang terdapat dalam tumbuhan yang berbeda sangat bervariasi, kandungan lignin dalam spesies kayu berkisar antara 20 – 40%, sedangkan spesies non kayu kandungan ligninya lebih rendah.
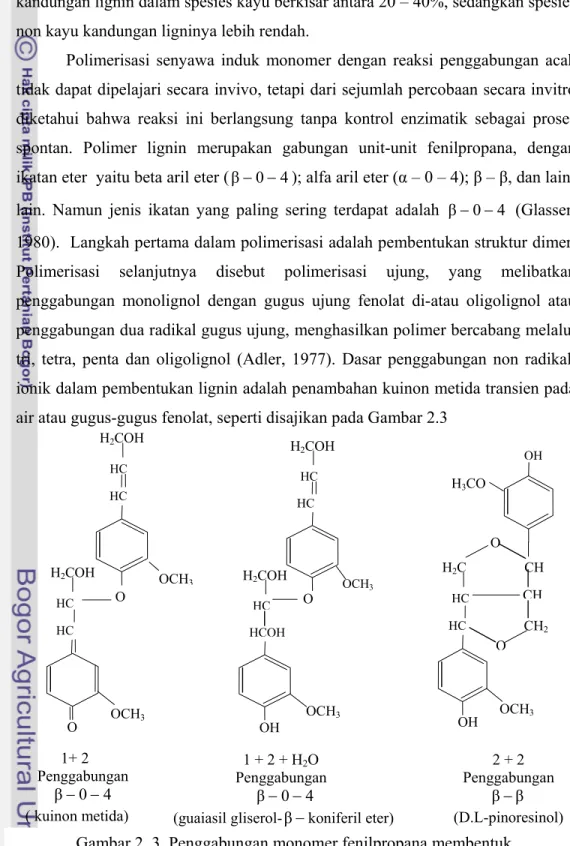
Polimerisasi senyawa induk monomer dengan reaksi penggabungan acak tidak dapat dipelajari secara invivo, tetapi dari sejumlah percobaan secara invitro diketahui bahwa reaksi ini berlangsung tanpa kontrol enzimatik sebagai proses spontan. Polimer lignin merupakan gabungan unit-unit fenilpropana, dengan ikatan eter yaitu beta aril eter (β−0−4); alfa aril eter (α – 0 – 4); β – β, dan lain-lain. Namun jenis ikatan yang paling sering terdapat adalah β−0−4 (Glasser, 1980). Langkah pertama dalam polimerisasi adalah pembentukan struktur dimer. Polimerisasi selanjutnya disebut polimerisasi ujung, yang melibatkan penggabungan monolignol dengan gugus ujung fenolat di-atau oligolignol atau penggabungan dua radikal gugus ujung, menghasilkan polimer bercabang melalui tri, tetra, penta dan oligolignol (Adler, 1977). Dasar penggabungan non radikal, ionik dalam pembentukan lignin adalah penambahan kuinon metida transien pada air atau gugus-gugus fenolat, seperti disajikan pada Gambar 2.3
Gambar 2. 3 Penggabungan monomer fenilpropana membentuk polimer fenilpropana (Adler, 1977).
1+ 2 Penggabungan β−0−4 ( kuinon metida) 1 + 2 + H2O Penggabungan β−0−4
(guaiasil gliserol-β−koniferil eter)
2 + 2 Penggabungan β β− (D.L-pinoresinol) OH H3CO OH OCH3 O HC HC H2C CH CH CH2 O OCH3 O HC HC H2COH OCH3 HCOH HC H2COH OH O HC OCH3 HC H2COH O OCH3 HC HC H2COH
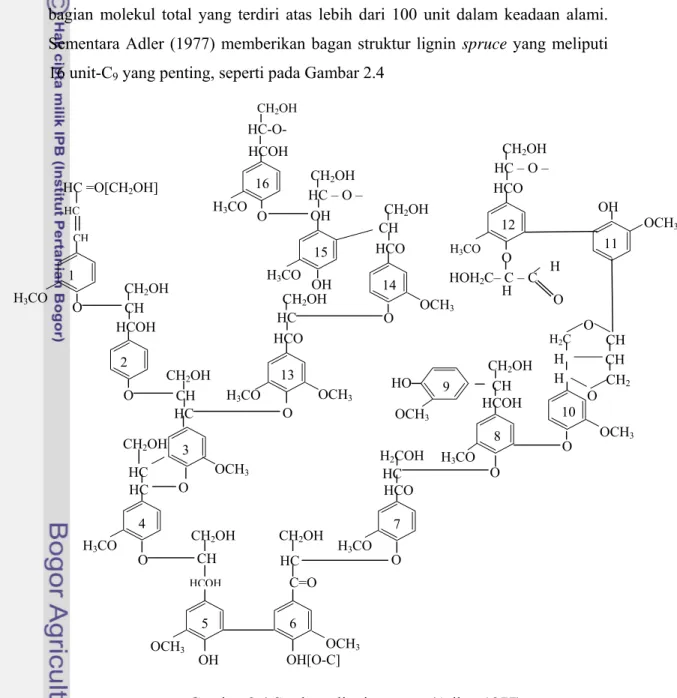
Karena makro molekul lignin tidak dapat dilukiskan dengan penggabungan satu atau beberapa unit monomer fenilpropana, maka struktur lignin masih merupakan model-model. Model lignin pertama dikemukakan oleh Freudenberg (1968) diacu dalam Fengel dan Wegener (1995), didasarkan pada konsep polimerisasi dehidrogenatif dan dipenuhinya semua data analitik, dengan bagan lignin kayu daun jarum (spruce) meliputi 18 unit fenilpropana sebagai bagian molekul total yang terdiri atas lebih dari 100 unit dalam keadaan alami. Sementara Adler (1977) memberikan bagan struktur lignin spruce yang meliputi 16 unit-C9 yang penting, seperti pada Gambar 2.4
Gambar 2.4 Struktur lignin spruce (Adler, 1977). HCOH CH OCH3 OH 5 CH2OH C=O HC HC OH[O-C] 6 CH2OH OCH3 H3CO O 4 HC OCH3 O 3 HC CH2OH HCO OCH3 O 13 H3CO CH CH2OH HCOH O 2 CH CH2OH CH HC O 1 HC =O[CH2OH] H3CO HC CH2OH HCO OCH3 O 14 CH CH2OH OH OH 15 HC – O – CH2OH H3CO HCOH O 16 H3CO HC-O- CH2OH HCO H3CO O 7 HC H2COH HCOH H3CO O 8 CH CH2OH 9 OCH3 HO OCH3 10 O O H CH2 H CH CH H2C O 11 OH OCH3 HCO O 12 CH2OH HC – O – HOH2C– C – C H O H H3CO
10 2.2.1 Karakteristik Lignin dan Turunan Lignin
2.2.1.1 Komposisi Kimia dan Bobot Molekul Lignin
Karakterisasi kimia pertama lignin yaitu penentuan gugus metoksil, sedang karakterisasi analitik lebih lanjut adalah penentuan kandungan gugus fungsional lain meliputi gugus fenolat dan hidroksil alifatik, gugus karbonil dan karboksil, yang menunjukkan perubahan-perubahan unsur lignin yang disebabkan oleh prosedur isolasi atau perlakuan kimia. Degradasi lignin dan reaksi kondensasi dapat juga dibuktikan dengan menentukan bobot molekul rata-rata atau disebut distribusi bobot molekul (Goring 1971). Nilai analitik lignin menunjukkan bahwa kandungan karbon lignin kayu daun jarum adalah 60 – 65 %, pada umumnya lebih tinggi dari kayu daun lebar yaitu 56 – 60 %. Hal ini disebabkan oleh kandungan oksigen lignin kayu daun lebar yang lebih tinggi, yang disebabkan oleh kandungan metoksil yang lebih tinggi yaitu 18 – 22 % bila dibandingkan dengan kandungan metoksil pada kayu daun jarum yaitu berkisar antara 12 – 16 %. Sedangkan sampel lignin gramineae mempunyai kandungan metoksil dengan kisaran diantara lignin kayu daun jarum dan kayu daun lebar. Lignin asam keduanya menunjukkan kandungan metoksil yang rendah, kemungkinan karena pengaruh kimia yang keras selama proses isolasi.
Degradasi lignin dan reaksi kondensasi akibat prosedur isolasi atau perlakuan kimia dapat juga mempengaruhi distribusi bobot molekul rata-rata. Hal ini menyebabkan distribusi bobot molekul lignin merupakan salah satu kriteria yang dapat dipakai sebagai parameter untuk pengontrolan kualitas lignin tersebut. Bobot molekul merupakan salah satu sifat dasar suatu polimer lignin seperti sifat alir, sifat optik, sifat listrik dan sifat mekanik. Suatu polimer pada umumnya memiliki panjang rantai yang berbeda-beda sehingga pengukuran bobot molekul hanya menghasilkan bobot molekul rata-rata. Ada beberapa jenis bobot molekul rata-rata diantaranya adalah:
: w
M bobot molekul rata-rata berat (weight –average molecular weight) :
n
M bobot molekul rata-rata jumlah (number-average molecular weight) :
v
w
M atau bobot molekul rata-rata berat dapat ditentukan dengan cara sedimentasi dengan ultra sentrifugal dan penghamburan cahaya oleh larutan polimer. Mnatau bobot molekul rata-rata jumlah dapat ditentukan dengan cara penentuan jumlah gugus ujung kimia dan penentuan tekanan osmotik. Mv atau bobot molekul rata-rata viskositas dapat ditentukan dengan beberapa cara antara lain dengan pengukuran viskositas larutan, penentuan tekanan osmotik dan penghamburan cahaya oleh larutan polimer. Hubungan bobot molekul dengan viskositas untuk polimer yang berstruktur linier maka berlaku hubungan empiris berikut ini yang dikenal dengan persamaan Mark-Houwink.
[ ]
a v M k = η Keterangan: [η] : viskositask dan a : adalah tetapan. Kedua tetapan ini tergantung pada sistem polimer, pelarut dan temperatur.
v
M : bobot molekul rata-rata viskositas
Hubungan nilai k dengan viskositas suatu bahan polimer akan mempengaruhi viskositas larutan tersebut, dimana bahan polimer yang memiliki nilai k tinggi dalam sistem pengenceran larutan akan menghasilkan viskositas tinggi pula, dan bahan polimer yang memiliki nilai k rendah dalam sistem pengenceran larutan akan menghasilkan viskositas rendah. Nilai k suatu bahan polimer dapat ditentukan dengan cara pengukuran viskositas larutannya dan dihitung dengan menggunakan
persamaan “ Fikentcher” yang ditulis secara empiris sebagai berikut: C ) (k x10 x10 k.C 1,5 1 x10 k 75 η log 3 3 6 2 r ⎥ ⎦ ⎤ ⎢ ⎣ ⎡ + ⎟⎟ ⎠ ⎞ ⎜⎜ ⎝ ⎛ + = − − − Keterangan: r η : viskositas relatif
C : konsentrasi dinyatakan dalam gram per desiliter (gr/dl, gram/100 ml)
2.2.1.2 Derajat Polidispersitas
Polidispersitas merupakan sifat yang dimiliki semua lignin isolat apakah diperoleh dengan prosedur analitik maupun teknik. Untuk melihat besaran
12 polidispersitas memerlukan nilai bobot molekul rata-rata jumlah (Mn ) dan nilai bobot molekul rata-rata berat (Mw). Derajat polidispersitas dinyatakan sebagai nisbah dari nilai bobot molekul rata berat terhadap nilai bobot molekul rata-rata jumlah (Mw/Mn) (Vollmert B., 1973). Metode yang sering digunakan meliputi osmometri, teknik hamburan sinar dan ultrasentrifugasi serta yang lebih mutakhir adalah kromatografi permeasi gel (GPC) dam kromatografi cair bertekanan tinggi (HPLC) yang digabung dengan kalibrasi kolom dengan standar yang cocok atau dengan pengukuran ultrasentrifugasi fraksi-fraksi yang terpisah. Derajat polidispersitas untuk lignin kayu spruce yang digiling sebesar (Mw/Mn = 3,1), sedangkan untuk kayu pinus (Mw/Mn = 3,4)
2.2.1.3 Sifat-sifat Spektroskopi Infrared (IR) dan Ultraviolet (UV) Lignin. Spektroskopi infra merah (IR) lignin dan turunan lignin dilakukan untuk karakterisasi secara kualitatif dan mengevaluasi pita-pita serapan khusus secara kuantitatif. Penentuan lignin secara kuantitatif dengan menentukan pita vibrasi cincin aromatis pada bilangan gelombang 1505 dan 1600 cm-1 yang dilakukan terhadap senyawa model lignin kayu yang digiling. Spektra IR lignin menunjukkan sejumlah pita serapan utama yang dapat diperuntukkan secara empiris bagi gugus-gugus struktural baik dari senyawa model maupun lignin. Pita-pita IR khas lignin yang paling mungkin tercantum dalam Tabel 2.2
Tabel 2.2 Pita serapan penting infra merah lignin menurut Hergert, 1971
Bilangan gelombang, cm-1 Pita serapan asal
3450 – 3400 Rentangan OH
2940 – 2820 Rentangan OH pada gugus metil dan metilena 1715 - 1710 Rentangan C=O tak terkonjugasi dengan cincin
aromatik
1675 – 1660 Rentangan C=O terkonjugasi dengan cincin aromatik 1605 – 1600 Vibrasi cincin aromatik
1515 – 1505 Vibrasi cincin aromatik 1470 – 1460 Deformasi C-H (asimetri) 1430 – 1425 Vibrasi cincin aromatik 1370 – 1365 Deformasi C-H (simetri) 1330 – 1325 Vibrasi cincin siringil 1270 – 1275 Vibrasi cincin guaiasil 1085 – 1030 Deformasi C-H, C-O
Peruntukan suatu pita serapan tidak dapat dideduksi dari spektrum tunggal, tetapi harus dikaji dengan pengukuran turunan senyawa model lignin dan sampel lignin, jadi dengan menggeser kedudukan pita serapan unsur struktural atau eliminasi pita-pita serapannya. Pita serapan inframerah lignin yang paling karakteristik terdapat pada sekitar 1510 dan 1600 cm-1(vibrasi cincin aromatik) dan antara 1470 dan 1460 cm-1 (deformasi C-H dan vibrasi cincin aromatik). Metoda-metoda derivatisasi yang cocok adalah metilasi, asetilasi, reduksi, sulfonasi atau pengubahan menjadi garam, yang memungkinkan penentuan gugus fungsional, misal gugus hidroksil atau karbonil (Hergert, 1971)
Sementara serapan (absorpsi) ultraviolet (UV) merupakan alat yang digunakan secara luas untuk identifikasi lignin dan turunannya baik secara kualitatif maupun kuantitatif, serta karakterisasi perubahan struktur dan sifat-sifat lignin dan turunannya. Serapan lignin yang nyata dalam kisaran ultra violet didasarkan pada sifat aromatiknya, yaitu jumlah unit fenilpropana, dan pada sejumlah unsur-unsur struktur kromofor seperti gugus hidroksil fenolat, gugus karbonil dan sebagainya. Spektra khas lignin meliputi maksimum 280 nm diikuti dengan lereng ke arah panjang gelombang yang rendah dengan pundak yang jelas pada daerah 230 nm. Perubahan-perubahan kecil namun terukur dalam perilaku spektroskopi UV disebabkan oleh berbagai jumlah gugus kromofor. Karakterisasi lignin kebanyakan terbatas pada perbandingan lignin-lignin yang berbeda, evaluasi sejumlah gugus fungsional khusus, serta penentuan perubahan struktur akibat perlakuan reaksi kimia.
2.2.2 Penggunaan Lignin Teknis
Penggunaan lignin pada saat sekarang dan masa mendatang merupakan bidang yang sangat luas dan semakin meningkat kepentingannya, suatu alasan untuk pengembangan lignin karena sifat-sifat dan jumlah yang cukup besar barasal dari proses pembuatan pulp seluruh dunia (sekitar lebih dari 50 juta ton pertahun) serta dapat dilihat dari pengetahuan tentang bahan mentah yang dapat diperbaharui. Lignin sebagai bahan mentah masih perlu dilakukan proses lanjut untuk meningkatkan penggunaan yang lebih intensif. Bidang-bidang kegunaan lignin dapat dibagi menjadi beberapa kelompok umum yaitu:
14
¾ Lignin sebagai bahan bakar
¾ Lignin sebagai produk polimer
¾ Lignin sebagai sumber bahan kimia berbobot molekul rendah.
Penggunaan utama lignin saat ini masih sebagai sumber energi. Kebanyakan lignin kraft digunakan untuk tujuan energi karena pemilihan bahan-bahan kimia proses didasarkan pada pembakaran dari lindi hitam bekas pakai. Nilai kalori dari lindi bekas pakai adalah 23,4 MJ/kg merupakan harga ekonomi yang penting dikaitkan dengan tingginya kenaikan harga gas dan minyak. Penggunaan lignin sebagai bahan polimer dengan sifat-sifat yang cocok untuk banyak tujuan teknis, namun pasaran lignin atau produk-produk lignin masih sangat kecil, jika dikaitkan dengan besarnya potensi. Diantara sebab sebab yang membatasinya jika dibandingkan dengan produk-produk sintesis dari minyak bumi dan gas bumi adalah sebagai berikut:
¾ Struktur kimia lignin dan turunan lignin yang kompleks
¾ Ketidak seragaman polidispersitas lignin
¾ Kandungan sulfonat yang cukup besar dalam lignin kraft dan lignin sulfonat, namun untuk lignin organosolv bebas sulfur (S)
¾ Biaya yang tinggi untuk isolasi dan pemurnian lignin.
Proses isolasi lignin, setelah melalui pelarutan dengan garam dan pengendapan ulang dengan asam sulfat encer maka lignin yang dihasilkan menjadi larut hanya dalam larutan alkali dan tidak larut dalam air. Sifat larut lignin yang dimiliki disebabkan karena kekuatan ikatan hidrogen dan kerapatan energi kohesifnya, menyebabkan lignin tidak larut dalam air, namun larut dalam dimetil formamida (DMF) dan tetrahidrofuran (THF). Pelarut lignin yang bagus lainnya adalah asetil bromida dalam asam asetat serta hexachloropropanol (Fengel and Wegener, 1995). Sifat tersebut merupakan hambatan yang berat untuk penggunaan lignin secara teknis. Untuk menghindari kerugian karena ketidak larutannya dalam air, maka lignin-lignin alkali dapat dimodifikasi menjadi sulfonat-sulfonat yang larut dalam air dengan proses sulfonasi. Modifikasi lignin umumnya bertujuan membentuk lignin sulfonat atau lignosulfonat melalui proses sulfonasi dan garamnya, menjadi garam lignosulfonatyang memiliki kemampuan sebagai surfaktan
2.3 Modifikasi Lignin Isolat Menjadi Garam Lignosulfonat
Modifikasi lignin isolat biasanya melalui proses sulfonasi dan garamnya menjadi garam lignosulfonat. Sebagai agen penyulfonasi dapat digunakan asam sulfat, oleum, natrium bisulfit maupun natrium thiosulfat. Sulfonasi dimaksudkan untuk mengubah sifat hidrofilisitas lignin yang kurang polar (tidak larut air) menjadi garam ligosulfonat yang memiliki sifat hidrofilisitas yang lebih polar (larut air), dengan cara memasukkan gugus sulfonat (SO3-) dan garamnya ke dalam gugus hidroksil (OH-) lignin. Prinsip inilah yang menggambarkan garam lignosulfonat berperan sebagai surface active agent atau surfaktan. Selain proses sulfonasi, lignin dapat dimodifikasi melalui proses hidrogenolisis, hidroalkilasi, metilasi, asetilasi, reduksi, atau pengubahan menjadi garam lignosulfonat (David et al, 1996). Modifikasi lignin dilakukan untuk mengubah karaktertistik yang dikehendaki, melalui beberapa proses tergantung dari fungsi yang akan dicapai dalam aplikasinya. Sebagai contoh modifikasi sulfonasi lignin menjadi surfaktan natrium lignosulfonat (NLS) mempunyai beberapa fungsi yaitu :
1) Sebagai “bahan pendispersi” pada berbagai sistem dispersi partikel, yaitu membantu memperluas penyebaran pada pasta gipsum akibat turunnya viskositas dan sedimentasi pasta gipsum, juga berfungsi sebagai aditif jenis water reducing admixtures (WRA) pada pasta semen.
2) Sebagai “bahan perekat” yaitu membantu memperbesar sifat kepaduan (cohesiveness) dalam industri keramik.
3) Sebagai “ bahan pengemulsi” yaitu penstabil emulsi dua zat yang tidak saling larut seperti emulsi aspal, pelumas, pigmen dan cat.
4) Sebagai pelarut warna pada industri tekstil.
Pada beberapa penggunaan lainnya, lignosulfonat juga dapat dimodifikasi dengan mengubah gugus hidroksil (-OH) yang terdapat dalam lignin dengan garamnya seperti kalsium, natrium, ammonium maupun seng membentuk garam lignosulfonat. Garam lignosulfonat tersebut termasuk produk garam lignosulfonat komersial yakni ammonium lignosulfonat; kalsium lignosulfonat; natrium lignosulfonat dan seng lignosulfonat (Wesco Technology,1995). Produk tersebut
16 dijual dalam bentuk bubuk maupun cair. Karakteristik garam lignosulfonat disajikan pada Tabel 2.3
Tabel 2.3 Karakteristik garam lignosulfonat komersial
Jenis garam lignosulfonat Karakteristik Ammonium Lignosulfonat Kalsium lignosulfonat Natrium lignosulfonat Seng lignosulfonat Lignosulfonat, % 57 80 80 42 Gula pereduksi, % 24 7 7 - Sulfur, % 6,8 6,6 6,6 - Kalsium , % 0,4 5,0 0,5 0,2 Natrium, % 0,2 0,2 7 4,3 Nitrogen, % 4,7 0,1 0,1 - Abu, % 1,0 20 22 - Kadar air, % 52 5 < 6 52 pH (10 % larutan) 4 – 5 4,5 7,5 4 – 5 Viskositas, (20 % larutan), cps 800 900 1000 100 Bobot jenis, kg/m3 368,42 368,42 368,42 173
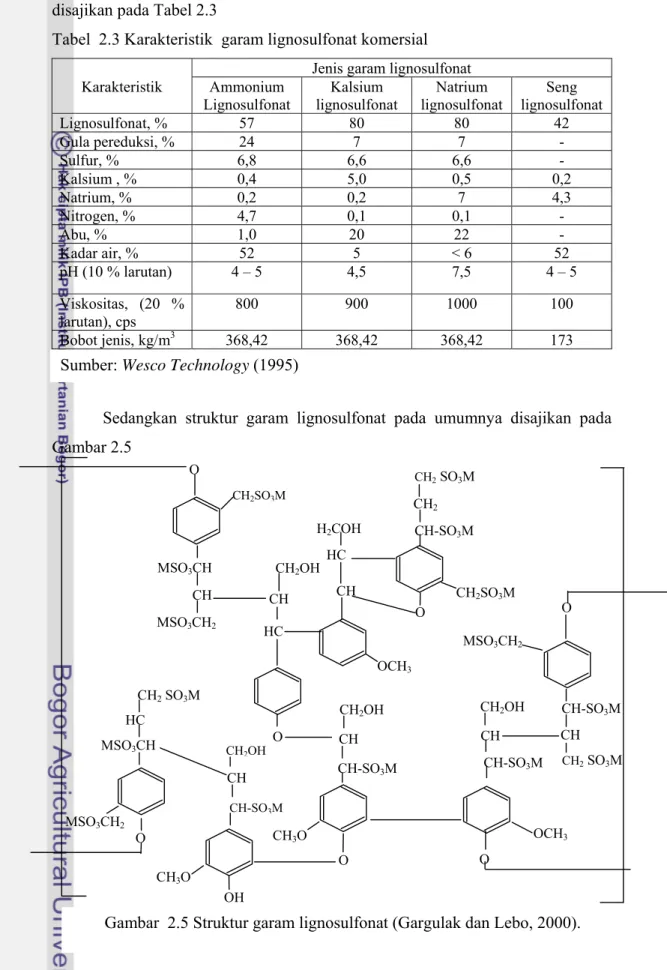
Sedangkan struktur garam lignosulfonat pada umumnya disajikan pada Gambar 2.5
Gambar 2.5 Struktur garam lignosulfonat (Gargulak dan Lebo, 2000). O CH2OH CH2 SO3M O CH-SO3M CH CH2OH OCH3 CH CH-SO3M MSO3CH2 O O CH3O OH CH-SO3M CH O MSO3CH2 MSO3CH HC CH2 SO3M CH2OH CH3O CH CH-SO3M HC CH CH2OH CH MSO3CH2 O MSO3CH CH2SO3M O CH-SO3M CH2 CH2 SO3M CH2SO3M HC OCH3 H2COH CH Sumber: Wesco Technology (1995)
Beberapa penelitian modifikasi lignin yang telah dilakukan antara lain:
1) Dilling, 1989 (US patent 5,043,435) melakukan sulfonasi lignin menggunakan oleum (xH20 ySO3) menjadi lignosulfonat. Lignin disulfonasi dengan oleum, pada suhu dibawah 40 oC selama 4 jam pada tekanan atmosfir, dan proses berlangsung pada pH 6,3 – 7.
2) Gargulak, 2001 (US Patent No. 6,238,475), memodifikasi lignin menjadi ammonium lignosulfonat melalui reaksi oksidasi dengan ammonium hidroksida, serta sulfonasi. Ammonium lignosulfonat berfungsi sebagai bahan pendispersi, dengan efek memperlambat ikatan pada beton dan mengatur gelembung udara dalam beton (set retarding and air entraining).
3) Syahmani (2001) melakukan sulfonasi dan asetilasi lignin dari TKKS pada suhu 100 OC dan pH 5, yang berfungsi sebagai bahan perekat partikel urea untuk memperbaiki sifat anti-craking dan anti-dusting.
4) Yasuda dan Matsushita (2004) melakukan sulfonasi lignin dengan asam sulfat dan phenol (proses hidrolisis) membentuk lignosulfonat dan mengevaluasi lignosulfonat sebagai bahan pendispersi pada pasta gipsum
2.4 Surfaktan Natrium Lignosulfonat (NLS)
Surfaktan merupakan senyawa organik yang didalam molekulnya memiliki sedikitnya satu gugus hidrofilik dan satu gugus hidrofobik. Molekul surfaktan dapat divisualisasikan seperti berudu ataupun raket mini yang terdiri atas bagian kepala dan ekor. Bagian kepala bersifat hidrofilik (suka air), merupakan bagian yang sangat polar, sedangkan bagian ekor bersifat hidrofobik (benci air), merupakan bagian non polar. Kepala dapat berupa anionik, kationik, nonionik dan amphoterik sedangkan ekor berupa rantai linier hidrokarbon atau cabang hidrokarbon. Konfigurasi kepala-ekor tersebut membuat surfaktan memiliki fungsi yang lebih luas dan beragam di dalam industri (Hui, 1996 ; Hasenhuiellt, 1997). Beberapa contoh struktur molekul surfaktan yaitu surfaktan anionik seperti: sulfat (-OSO2O-), sulfonat (-SO2O-), dan karboksilat (-COO-); surfaktan kationik seperti: ammonium (-NH3+), pyridinium (–NC6H5+); surfaktan nonionik seperti: digliserida {-CH2CH(O-)CH2OH}, dietanolamida {-N(CH2CH2OH)2} dan surfaktan amphoter seperti: amin oksida (-N+-O-), sulfobetain
{-18 N+(CH2)xCH2SO3-}. Gambaran struktur molekul surfaktan pada peristiwa penurunan tegangan permukaan dan antar muka disajikan pada Gambar 2.6 (Rosen dan Dahanayake, 2000).
Karakteristik dan kinerja surfaktan dapat digolongkan dalam beberapa jenis yaitu sebagai wetting dan waterproofing yang bekerjanya karena terjadinya penurunan tegangan permukaan dan antar muka; foaming yang menimbulkan pembusaan pada detergen; emulsifikasi yang bekerja pada cairan yang saling tidak larut sehingga menjadi saling larut; dispersi yang bekerja sebagai penyebar pada sistem dispersi partikel seperti pada pasta gipsum dan pasta semen. Aplikasi surfaktan sebagai bahan aditif yang penting untuk beberapa industri seperti industri sabun dan deterjen, industri tekstil, industri karet dan plastik, industri kosmetik, industri pangan, bahan perekat untuk papan gipsum, sebagai bahan pendispersi pada industri bahan konstruksi, dan lain-lain (Rosen dan Dahanayake, 2000). Dengan banyaknya kebutuhan dan penggunaan surfaktan untuk berbagai keperluan industri sehingga surfaktan memiliki nilai jual yang tinggi. Persentase pasar surfaktan untuk berbagai aplikasi didunia adalah sebagai produk pembersih sebesar 52,9 %, tekstil dan kulit 8,4 %, konstruksi 5,5 %, perminyakan 5,1 % , polimerisasi emulsi 3,4 %, pangan 2,3 %, peptisida 2,3 %, industri cat 1,9 %,
Gambar 2.6 a) Orientasi dari molekul surfaktan teradsorpsi pada antar muka (air dan udara). b) Orientasi dari molekul surfaktan teradsorpsi antara larutan nonpolar dan
industri kertas 1,4 %, industri plastik 0,5 % , bahan peledak 0,1 % serta lainnya 6,2 % (sumber: www.chemsoc.org)
Natrium lignosulfonat (NLS) termasuk surfaktan anionik karena memiliki gugus sulfonat dan garamnya (-NaSO3-) yang merupakan anion (kepala) dan gugus hidrokarbon merupakan ekor. Struktur inilah yang menyebabkan meningkanya sifat hidrofilitas NLS sehingga mudah larut dalam air. Menurut ASTM Standard C 494-79 ( spec for water reducing admixtures for concrete), natrium lignosulfonat (NLS) adalah bahan tambahan kimia termasuk jenis water reducing admixture (WRA) atau plasticizer. Prinsip dari komponen aktif bahan tambahan kimia jenis WRA adalah sebagai surfaktan anionik yang memiliki kemampuan sebagai bahan pendispersi (dispersant) pada berbagai sistem dispersi partikel (pasta semen dan gipsum). Pemberian NLS dalam sistem partikel akan menghasilkan pembatas elektrik yang mencegah bersatunya partikel-partikel (pasta semen dan gipsum) tersebut, sehingga sistem dispersi berlangsung sempurna. Pengurangan atau penghilangan pambatas elektrik menyebabkan terjadinya flokulasi (Rosen dan Dahanayake, 2000). Penambahan NLS sebagai bahan pendispersi (dispersant) pada pasta gipsum maupun pasta semen tersebut menyebabkan penurunan viskositas, sehingga luas permukaan menjadi besar (terdispersi) dan meningkatkan kelecakan/slam (slump) tanpa penambahan air sehingga mempercepat pengerjaan (setting time) dan kuat tekan (strength) akan lebih tinggi (Neville, 1981). Neville menggambarkan pasta gipsum terflokulasi (tanpa NLS) dan pasta gipsum terdispersi (dengan NLS) disajikan pada Gambar 2.7 dan Gambar 2.8
Gambar 2.8 Pasta gipsum terdispersi (dengan NLS).
Gambar 2.7 Pasta gipsum terflokulasi (tanpa NLS).
20 Sedang gambaran pasta semen terflokulasi (tanpa NLS) (kiri) dan pasta semen terdispersi (dengan NLS) (kanan) disajikan pada Gambar 2.9
Lignin Institute (2001), menyatakan bahwa kinerja natrium lignosulfonat (NLS) dapat mengurangi nilai faktor air/semen (f a s) lebih rendah hingga 15 sampai 25%. Dengan menambahkan surfaktan NLS sebagai WRA, kekentalan pasta semen dibuat sama namun nilai f a s lebih rendah, atau nilai f a s dibuat sama namun kekentalan pasta semen menjadi lebih encer. Persentase pengurangan kebutuhan air pasta semen terhadap kadar NLS seperti disajikan pada Tabel 2.4 Tabel 2.4 Hubungan penambahan NLS dalam pasta semen terhadap
pengurang-an kebutuhpengurang-an air
Kadar NLS dalam pasta semen, (%, w/w)
Pengurangan kebutuhan air (%) 0,1 5 0,2 15 0,3 20 0,5 25 0,6 33
Gambar 2.9 Pasta semen terflokulasi (tanpa NLS) (kiri) dan pasta semen terdispersi (dengan NLS) (kanan).
2.5 Perancangan
Perancangan merupakan suatu kegiatan penerapan ilmu pengetahuan dan teknologi untuk menghasilkan nilai, produk, dan/atau proses produksi serta sistem, dengan mempertimbangkan keterpaduan sudut pandang dan/atau konteks teknikal, fungsional, bisnis, sosial budaya serta estetika (Johnston et a1. 1999). Tahapan perancangan diawali melalui penemuan/gagasan awal (invensi) yang melahirkan inovasi. Tahapan berikutnya adalah perancangan untuk menghasilkan suatu produk, proses atau sistem baru yang dapat dijembatani melalui penelitian ilmiah, agar rancangan yang dihasilkan dapat dipertanggung jawabkan kebenaran dan kualitasnya. Dengan menggunakan prinsip dan metodologi ilmiah, informasi teknis dan imajinasi untuk menentukan suatu struktur, mesin, proses atau sistem baru yang memenuhi fungsi yang diinginkan dengan nilai ekonomis, efektif dan efisiensi tinggi, sehingga keluaran perancangan atau rancangan merupakan gambaran riil yang pada umumnya dapat langsung dimanfaatkan oleh manusia (Johnston et a1. 1999).
Seider et al. (1999), mengemukan perancangan pabrik dijalankan melalui beberapa tahapan yaitu :
¾ Proses penciptaan dan pengembangan kasus dasar
¾ Sintesis proses
¾ Perancangan secara lengkap, pengukuran peralatan, perkiraan biaya kapital, analisis keuntungan, dan optimasi
¾ Penilaian kemampuan kontrol skala industri
¾ Gambaran riil perancangan proses (dalam bentuk laporan tertulis) dan evaluasi kelayakan investasi finansial, sehingga diperoleh perancangan akhir berupa:
• Gambar peralatan • Diagram pipa
• Diagram instrumentasi • Tata letak alat
• Konstruksi model skala penuh • Penawaran/pemasaran
¾ Selanjutnya sampai ke tahap konstruksi, startup dan operasi industri kimia
22
Apakah proses masih menjanjikan?
Gambar 2.10 Tahapan perancangan pabrik (Seider et al., 1999).
Potensi/Peluang dan Permasalahan
Apakah proses masih menjanjikan?
Perancangan secara lengkap, Pengukuran peralatan, Perkiraan biaya kapital,
Analisis keuntungan, dan Optimasi
Penilaian kemampuan kontrol skala industri
Sintesis kualitatif dari stuktur kontrol
Analisis kemampuan kontrol diagram alir
Simulasi dinamik
Apakah proses layak?
Laporan tertulis perancangan proses dan presentasi
Perancangan akhir:
¾ Gambar peralatan
¾ Diagram pipa
¾ Diagram instrumentasi
¾ Tata letak alat
¾ Konstruksi model skala penuh
¾ Penawaran/pemasaran
Pendugaan awal Peralatan tambahan Simulasi dinamik
¾ Analisa realibilitas dan keamanan
¾ Pengujian Lab. dan pilot plant
¾ Analisa HAZOP
Konstruksi Startup Operasi
Membuat formulasi masalah sederhana
Studi literatur
Membuat basisdata awal
Percobaan
Pembuatan proses awal Reaksi, pemisahan Operasi perubahan T-P Seleksi-alat-alat yang sesuai
Ada keuntungan kotor ? tolak Proses penciptaan /kreasi
Pengembangan kasus dasar
Pembuatan diagram alir proses
Integrasi proses
Pembuatan basisdata secara detail
Modifikasi diagram alir untuk
pilot plant
Persiapan model simulasi
Sintesis proses secara detail dengan metode algoritma
Sintesis jalur pemisahan
Analisa hukum termodinamika ke 2 Integrasi panas dan tenaga tdk ya tidak ya tolak Tidak tidak ya ya
Tahap perancangan proses mengacu pada Seider (1999), yaitu sampai ke perancangan lengkap. Secara garis besar perancangan proses dapat didekati menjadi 3 tahap yaitu 1) Analisis peluang dan permasalahan, 2) Sintesis proses, serta 3) pengembangan proses
2.5.1 Analisis Peluang dan Permasalahan
Proses inovasi diawali dengan adanya peluang sehingga menciptakan suatu gagasan/ide yang merupakan aktivitas kreatif yang paling utama oleh seorang insinyur teknik proses. Adapun gagasan/ide diperoleh dari timbulnya kreativitas, penelitian pemasaran, masukan dari pengguna, produk pesaing, bahan baku/komponen baru, serta hasil penelitian awal. Selain hal tersebut juga adanya masalah yang lazim untuk dipecahkan, adanya tantangan serta adanya kemampuan (Johnston et al., 1999).
Dalam beberapa kasus nyata Douglas (1988), menyatakan bahwa gagasan baru diperlukan untuk:
¾ menghasilkan produk baru,
¾ mengubah limbah menjadi produk yang berharga,
¾ menciptakan bahan/produk yang sama sekali baru (bioproses),
¾ menemukan cara baru untuk memproduksi produk yang telah ada (katalis baru, alternatif bioproses),
¾ menerapkan teknologi baru (rekayasa genetik, sistem pakar),
¾ menggali bahan konstruksi baru (operasi suhu atau tekanan tinggi, polimer khusus)
2.5.2 Sintesis Proses
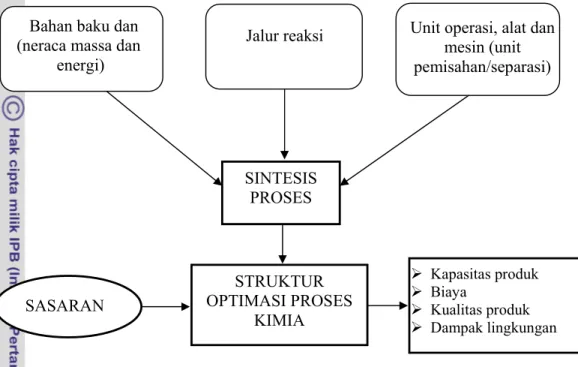
Hartmann dan Kaplick (1990), mengemukakan sintesis suatu sistem adalah pengubahan input yang ada menjadi output, merupakan elemen perancangan kompleks, interkoneksi dan model fungsi. Sintesis proses meliputi alokasi bahan pereaksi, jalur proses (sistem reaktor), unit atau makro proses (unit separasi). Sasaran yang dicapai adalah kondisi optimum suatu proses kimia untuk menghasilkan produk yang diterima. Metode yang digunakan dalam sintesis proses adalah kuantitatif (algoritma dan prosedural) serta kualitatif dengan
24 menggunakan metode heuristik (dari pengalaman). Sintesis proses merupakan metoda transformasi kimia maupun fisik, seperti disajikan pada Gambar 2.11
Misalkan pakar proses menemukan satu reaksi baru untuk membuat produk yang sudah ada, dan perancang proses bermaksud untuk menciptakan suatu proses baru, maka perancang harus mengetahui tentang mekanisme reaksi, kondisi reaksi, serta informasi ketersediaan bahan baku dan produk dari lembaga-lembaga pemasaran terkait. Untuk memasok kesenjangan informasi tersebut , pada umumnya mengembangkan beberapa anggapan (asumsi) berkaitan dengan jenis satuan proses yang harus digunakan, dan rangkaian satuan-satuan tersebut, serta kondisi proses yang akan diterapkan. Pola kegiatan yang berurutan dan terpadu tersebut merupakan suatu “ Sintesis”. Sintesis adalah kegiatan yang tidak mudah, oleh karena tersedia banyak cara yang dapat dipertimbangkan untuk mancapai tujuan yang ditetapkan yaitu sintesis proses dengan metode algoritma. Dalam beberapa kasus dapat mengikuti kaidah umum (heuristik) untuk mengurangi pilihan proses tertentu untuk pertimbangan lebih lanjut, seperti kapasitas produksi optimum yang memberikan keuntungan maksimum atau biaya
Gambar 2.11 Sintesis proses kimia (Hartmann dan Kaplick 1990). Unit operasi, alat dan
mesin (unit pemisahan/separasi) SINTESIS PROSES Jalur reaksi STRUKTUR OPTIMASI PROSES KIMIA ¾ Kapasitas produk ¾ Biaya ¾ Kualitas produk ¾ Dampak lingkungan
Bahan baku dan (neraca massa dan
energi)
produksi minimum, keamanan, serta memenuhi persyaratan lingkungan dan mudah mengoperasikannya.
Rudd et al, (1973) mengemukakan tahapan sintesis proses meliputi: 1) Pemilihan jalur reaksi atau proses
2) Alokasi bahan atau pereaksi
3) Pertimbangan teknik pemisahan atau proses hilir 4) Pemilihan operasi pemisahan
5) Pemaduan atau integrasi rancangan 1 sampai 4
Proses yang diterapkan untuk mengubah bahan dasar menjadi produk, selain proses utama juga melibatkan operasi pemisahan baik yang dilakukan pada persiapan, jalur proses maupun pemurnian produk. Agar dapat menerapkan pemisahan secara ekonomis, maka perancang proses harus dapat menciptakan lingkungan tersebut agar diketahui berdasarkan sifat fisika dan kimiawi bahan yang terlibat dalam proses. Berdasarkan perbedaan yang sangat nyata antar bahan-bahan tersebut, dapat dipilih suatu alternatif pemisahan yang ekonomis. Terdapat banyak ragam teknik pemisahan yang dapat diterapkan dalam suatu proses, dan dapat dikelompokkan menjadi beberapa kelompok besar yaitu:
a) Pemisahan berdasarkan peristiwa kesetimbangan fasa (equilibrium seperation process), meliputi: evaporasi, distilasi, ekstraksi, penyerapan (absorpsi), kristalisasi, penjerapan (adsorpsi), pengeringan, pencucian, osmosis, fraksinasi, flotasi (pengapungan), pemisahan magnetik, kromatografi, pengeringan beku, filtrasi gel.
b) Pemisahan yang terjadi sebagai akibat laju (rate governed separation), meliputi: difusi gas, difusi termal, spektrometri massa, dialisis, elektroforesis, permeasi gas, elektrodialisis, ultrasentrifugasi, osmosis balik (reverse osmosis), ultrafiltration, dan distilasi molekuler
c) Pemisahan secara mekanik, meliputi : filtrasi, pengendapan, siklon dan pengendapan elektrostatis.
2.5.3 Pengembangan Proses
Pengembangan proses merupakan tahapan untuk menuju perancangan lengkap. Menurut Seider (1999), sebelum melangkah ke pengembangan proses
26 terlebih dahulu dilakukan perhitungan keuntungan kasar yang melibatkan biaya produksi (input) dan nilai penjualan (output), apabila terdapat keuntungan kasar/kotor maka pengembangan proses dapat dilanjutkan. Pengembangan proses dimaksudkan adalah menggunakan basis data yang dapat diterapkan untuk penggandaan skala (scale up). Penggandaan skala dapat dilakukan baik melalui penelitian lebih lanjut di tingkat scale up maupun melalui pemodelan yaitu menentukan model matematik yang menghubungkan antara reaksi kimia dan kapasitas reaktor atau yang disebut kinetika reaksi. Setiap reaksi tertentu memiliki model kinetika tertentu dan dapat ditentukan melalui penelitian yang akurat. Untuk sampai ke perancangan lengkap suatu proyek komoditi tertentu, beberapa tahap perlu dilakukan yaitu menentukan kapasitas optimum yang dapat memberikan keuntungan maksimum atau biaya produksi total minimum serta menentukan peralatan yang sesuai. Untuk menyelesaikan model dan simulasi pada berbagai kapasitas digunakan fasilitas program seperti ASPEN PLUS, HYSYS dan sebagainya. Data-data dasar serta data pengembangan proses diintegrasikan dalam process engineering flow diagram (PEFD). Untuk menentukan proyek tersebut perlu dikembangkan atau tidak maka perlu dilakukan analisis kelayakan finansial. Perancangan lengkap suatu proyek komoditi tertentu sudah mendapatkan gambaran riil, yang dapat dijadikan alat bantu dalam pengambilan keputusan untuk pengembangan sampai ke perancangan akhir.
2.5.3.1 Pengembangan Proses Untuk Penggandaan Skala (Scale Up)
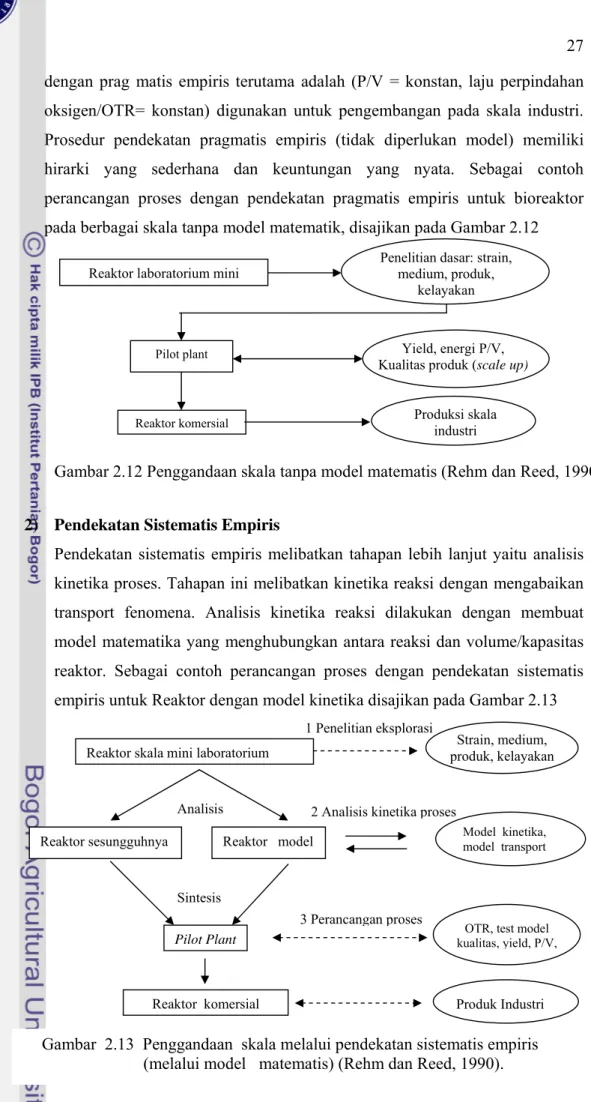
Menurut Rehm dan Reed (1990), pengembangan perancangan proses untuk penggandaan skala (scale up), didekati dengan dua cara yaitu pendekatan pragmatis empiris (tanpa model) dan pendekatan sistematis empiris (pemodelan) 1) Pendekatan Pragmatis Empiris.
Pendekatan pragmatis empiris didekatkan pada contoh perancangan reaktor mikrobia skala pilot plant. Pengembangan dilakukan dengan perhitungan ekonomi seperti pemakaian energi P/V, menghitung perpindahan neraca massa dan neraca panas, dan tujuan lain untuk mendapatkan produk dengan jumlah (yield) dan kualitas yang sesuai dengan yang diinginkan. Kriteria yang dipilih
dengan prag matis empiris terutama adalah (P/V = konstan, laju perpindahan oksigen/OTR= konstan) digunakan untuk pengembangan pada skala industri. Prosedur pendekatan pragmatis empiris (tidak diperlukan model) memiliki hirarki yang sederhana dan keuntungan yang nyata. Sebagai contoh perancangan proses dengan pendekatan pragmatis empiris untuk bioreaktor pada berbagai skala tanpa model matematik, disajikan pada Gambar 2.12
2) Pendekatan Sistematis Empiris
Pendekatan sistematis empiris melibatkan tahapan lebih lanjut yaitu analisis kinetika proses. Tahapan ini melibatkan kinetika reaksi dengan mengabaikan transport fenomena. Analisis kinetika reaksi dilakukan dengan membuat model matematika yang menghubungkan antara reaksi dan volume/kapasitas reaktor. Sebagai contoh perancangan proses dengan pendekatan sistematis empiris untuk Reaktor dengan model kinetika disajikan pada Gambar 2.13 Gambar 2.12 Penggandaan skala tanpa model matematis (Rehm dan Reed, 1990).
Reaktor komersial
Reaktor laboratorium mini
Pilot plant
Penelitian dasar: strain, medium, produk,
kelayakan
Yield, energi P/V, Kualitas produk (scale up)
Produksi skala industri
Gambar 2.13 Penggandaan skala melalui pendekatan sistematis empiris (melalui model matematis) (Rehm dan Reed, 1990).
Reaktor skala mini laboratorium
Analisis
Reaktor sesungguhnya Reaktor model
Sintesis
Pilot Plant
Reaktor komersial
OTR, test model kualitas, yield, P/V,
1 Penelitian eksplorasi
2 Analisis kinetika proses
3 Perancangan proses Strain, medium, produk, kelayakan Model kinetika, model transport Produk Industri
28 2.5.3.2 Pemodelan
Model matematik merupakan hubungan fungsional antara variabel bebas dan variabel tak bebas, dengan bentuk umum model matematik adalah y = f(b,x). Pengembangan model matematik didasarkan pada 2 (dua) hal, yaitu: 1) berdasarkan teori fisik, misalnya neraca massa, neraca energi, temodinamika, kinetika reaksi kimia, yang dapat dikembangkan untuk beberapa ukuran sistem sekalipun sistem belum dikonstruksi; 2) Berdasarkan diskripsi empiris, model ini digunakan jika model teori fisik tidak dapat dikembangkan karena batasan waktu dan sumber. Data input dan output diperlukan untuk mengetahui koefisien yang tidak diketahui dalam model lain. Penggolongan model secara teoritis maupun empiris dapat juga didasarkan kepada : a) linier-nonlinier, b) steady state-unstady state, c) peubah kontinyu – diskret.
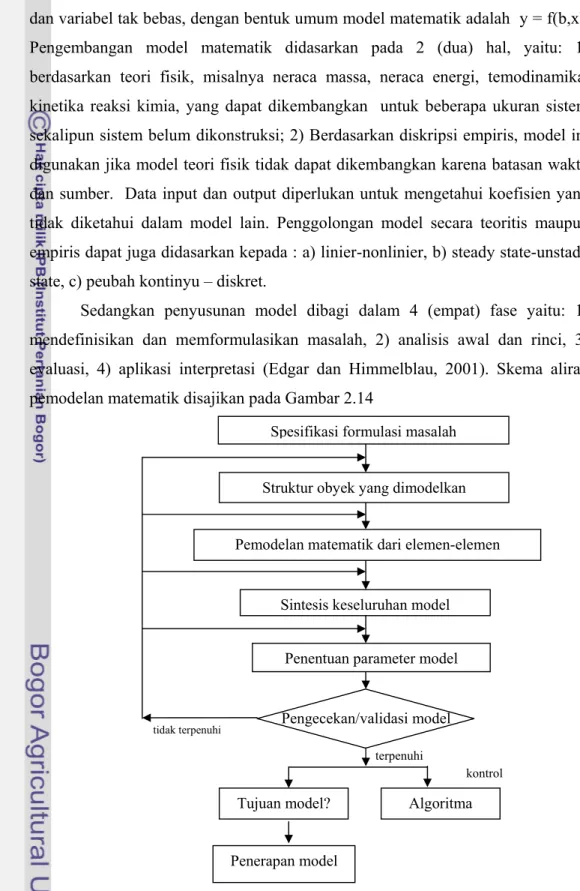
Sedangkan penyusunan model dibagi dalam 4 (empat) fase yaitu: 1) mendefinisikan dan memformulasikan masalah, 2) analisis awal dan rinci, 3) evaluasi, 4) aplikasi interpretasi (Edgar dan Himmelblau, 2001). Skema aliran pemodelan matematik disajikan pada Gambar 2.14
Gambar 2.14 Skema aliran pemodelan (Edgar dan Himmelblau, 2001).
terpenuhi
Spesifikasi formulasi masalah
Struktur obyek yang dimodelkan
Pemodelan matematik dari elemen-elemen
Sintesis keseluruhan model
Penentuan parameter model
Pengecekan/validasi model
tidak terpenuhi
Tujuan model? Algoritma
kontrol
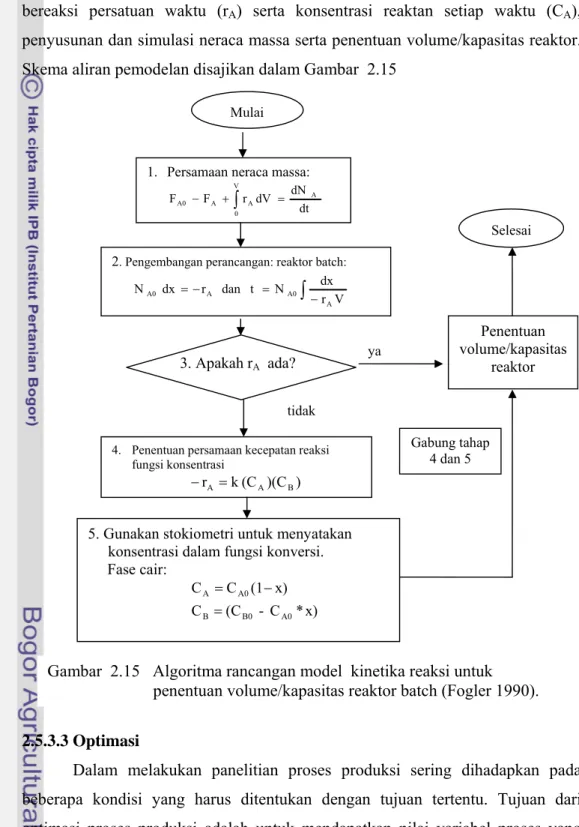
Dalam kasus pemodelan kinetika reaksi proses sulfonasi lignin menjadi natrium lignosulfonat (NLS) dilakukan berdasarkan data eksperimental yang melibatkan konversi atau mol reaktan bereaksi (x), laju reaksi atau mol reaktan bereaksi persatuan waktu (rA) serta konsentrasi reaktan setiap waktu (CA), penyusunan dan simulasi neraca massa serta penentuan volume/kapasitas reaktor. Skema aliran pemodelan disajikan dalam Gambar 2.15
2.5.3.3 Optimasi
Dalam melakukan panelitian proses produksi sering dihadapkan pada beberapa kondisi yang harus ditentukan dengan tujuan tertentu. Tujuan dari optimasi proses produksi adalah untuk mendapatkan nilai variabel proses yang
Gambar 2.15 Algoritma rancangan model kinetika reaksi untuk penentuan volume/kapasitas reaktor batch (Fogler 1990).
ya 2. Pengembangan perancangan: reaktor batch:
N dx =−r dan t =N
∫
−dxr V A A0 A A0 Mulai1. Persamaan neraca massa:
dt dN dV r F F V A 0 A A A0 − +
∫
= tidak4. Penentuan persamaan kecepatan reaksi fungsi konsentrasi ) )(C (C k rA = A B −
5. Gunakan stokiometri untuk menyatakan konsentrasi dalam fungsi konversi. Fase cair: x) * C -C ( C x) (1 C C A0 B0 B A0 A = − = Penentuan volume/kapasitas reaktor Selesai Gabung tahap 4 dan 5 3. Apakah rA ada?
30 menghasilkan nilai terbaik dari kriteria kinerja yang ada. Beberapa metode optimasi adalah dengan cara linier least square, non linier least square dengan penyelesaian numerik menggunakan metode Quasi Newton, Newton, Secant, Hooke-Jeeves atau simplex. Teknik matematika yang lain adalah dengan cara lagrange, steepest ascent atau desent, dan response surface method (RSM) (Peters dan Timmerhaus, 2000). Penyelesaian optimasi dapat dilakukan baik dengan program yang dibuat sendiri dengan menggunakan bahasa program misalnya Turbo Basic, Visual Basic, Delphi, Matlab dan sebagainya atau dengan paket program yang telah ada.
Teknik Optimasi
Teknik optimasi pada model matematis, diselesaikan secara analitis maupun grafis, baik digunakan untuk optimasi model satu peubah maupun lebih dari satu peubah. Pada model satu peubah, penentuan kondisi optimum secara grafis didapatkan dari titik maksimum atau minimum suatu kurva. Kemiringan kurva menunjukkan nilai nol pada titik optimum. Nilai optimum dapat juga ditentukan secara analitis dengan menurunkan persamaan respon CT terhadap peubah x sehingga nilai turunan pertama sama dengan nol, selanjutnya ditentukan nilai x optimum.
Misal ; CT = f(x), maka 0 dx dCT
=
,
Pada model dua peubah, misalnya CT =f(x,y) , dimana persamaan untuk CT adalah : CT = a x + b x y + c y + d, maka optimasi dapat diselesaikan dengan cara:
1) Cara grafis, yaitu hubungan antara CT, x dan y ditunjukkan sebagai kurva tiga dimensi dengan nilai minimum/maksimum. CT terjadi pada nilai optimum x dan y. Faktor yang akan dioptimasi diplot terhadap salah satu peubah bebas dan peubah lain (y) dipertahankan pada nilai yang tetap. 2) Cara analitis, yaitu metode penentuan nilai optimum x pada titik dimana
(∂CT/∂x) memberikan nilai nol, begitu juga sebaliknya nilai optimum y didapatkan jika (∂CT/∂y) memberikan nilai nol
2.6 Perancangan industri NLS Berbahan Dasar TKKS
Setelah melakukan analisis peluang yaitu melimpahnya TKKS sebagai bahan berlignoselulosa yang merupakan sumber lignin dan lignosulfonat yang potensial, serta menganalisis permasalahan yaitu mengurangi kebutuhan akan lignosulfonat import, maka perlu dikaji perancangan proses sulfonasi lignin menjadi natrium lignosulfonat (NLS). Beberapa penelitian sulfonasi lignin telah dilakukan oleh Syahmani (2001) dan Yasuda et al. (2004).
Penelitian Syahmani (2001) berjudul “Isolasi, Sulfonasi dan Asetilasi Lignin dari TKKS dan Studi Pengaruhnya Terhadap Proses Pelarutan Urea”. Sintesa proses awal meliputi isolasi lignin dari lindi hitam TKKS. Isolasi dilakukan dengan metode Kim (1987), dilanjutkan dengan sulfonasi lignin menjadi natrium lignosulfonat (NLS), dengan kondisi operasi pada nisbah pereaksi lebih dari 100% (b/b), suhu 100 OC dan pH 5. Uji kinerja NLS diaplikasikan sebagai binder urea. Mengingat struktur lignin yang sangat komplek dan kepastian struktur lignin tidak diketahui maka reaksi sulfonasi menurut Fengel dan Wegener (1995) seperti terlihat pada Gambar 2.16
Penelitian yang dilakukan oleh Yasuda et al. (2004) dengan judul “Preparation and evaluation of lignosulfonat as a dispersant for gypsum paste from acid hydrolysis lignin”, melakukan sulfonasi lignin dengan asam sulfat (H2SO4) konsentrasi 72% membentuk guaiasil sulfuric acid lignin (SAL),
Gambar 2.16 Reaksi Sulfonasi terhadap 1,2 – diguaiasilpropana – 1,3 – diol.
Natrium 1,2 – diguaiasil propana α– γ - disulfonat 1,2 – diguaiasil propana – 1,3 diol OCH3 HCSO3Na HC H2 CSO3Na OCH3 OH OH OCH3 2 NaHSO3 - 2 H2O HCOH HC H2 COH OH OCH3 OHH
32 kemudian direaksikan dengan phenol pada suhu 60 OC selama 6 jam membentuk phenolized SAL (P-SAL). Reaksi dilanjutkan dengan menambahkan Na-hidroksimetilsulfonat (HOCH2SO3Na) dengan kondisi proses pada suhu 100 sampai 150OC selama 2 jam membentuk sulfometilation (SAL). Uji kinerja M-SAL diaplikasikan sebagai bahan pendispersi pasta gipsum. Mekanisme reaksi sulfonasi lignin guaiasil, disajikan pada Gambar 2.17
2.6.1 Sintesis Proses Sulfonasi Lignin Isolat TKKS
Untuk menghasilkan bahan baku lignin isolat TKKS dan produk NLS yang baik, terlebih dahulu menentukan pemilihan jalur pemasakan/pulping TKKS dan pemilihan teknik isolasi lignin yang tepat, serta proses sulfonasi lignin isolat menjadi natrium lignosulfonat (NLS). Masing-masing proses dapat dilakukan melalui beberapa cara, dan masing-masing proses memiliki kelebihan dan kekurangan yang perlu dianalisis dan disintesis.
Gambar 2.17 Reaksi sulfonasi lignin guaiasil. CH3O CH HC-O- H2COH OH Phenolasi OCH3 SAL Sulfometilasi 72% H2SO4 CH3O OH HCOH HC-O- H2COH OH n CH3O CH HC-O- H2COH CH3O OH HCOH HC-O- H2COH Lignin (guaiasil) OH CH HC-O- H2COH P-SAL OH CH3O OH CH2SO3Na OH CH HC-O- H2COH CH2SO3Na CH2SO3Na M-SAL
2.6.1.1 Proses Pemasakan/Pulping TKKS
Proses pemasakan/pulping diartikan sebagai proses pelarutan lignin (delignifikasi), sehingga lignin terpisah dari serat-serat selulosa. Menurut Syöström (1995) selama berlangsungnya proses pulping tidak hanya lignin yang terpisah dari serat-serat selulosa, tetapi juga komponen-komponen lainya, seperti polisakarida dan sedikit hemiselulosa. Proses pemasakan/pulping dapat dilakukan dengan tiga cara yaitu proses mekanik, kimia dan proses semi kimia. Untuk memperoleh hasil pemisahan lignin dari serat selulosa secara sempurna dilakukan dengan cara kimia yaitu dengan menambahkan sejumlah bahan kimia ke dalam tempat pemasakan (digester). Bahan kimia yang digunakan dapat berupa asam atau alkali. Terdapat beberapa jenis pelarutan lignin yang dikenal dalam proses pemasakan/pulping menggunakan pelarut/pemasak bahan kimia yaitu proses kraft dan proses soda, proses organosolv serta proses semi kimia yaitu proses sulfit atau netral sulfit semi chemical (NSSC).
A. Proses Kraft dan Proses Soda
Pada umumnya pembuatan pulp untuk pelarutan lignin menggunakan proses sulfat/kraft dan proses soda, merupakan dua teknik pokok pembuatan pulp alkalis dan merupakan dasar untuk sejumlah proses alkalis yang dimodifikasi. Pada proses soda, bahan yang akan di dimasak ke dalam digester yang berisi larutan soda api (NaOH). Selama berlangsungnya proses pemasakan, lignin akan terdegradasi dan kemudian larut dalam air. Larutnya lignin disebabkan oleh terjadinya transfer ion hidrogen dari gugus hidroksil pada lignin ke ion hidroksil (Gilligen, 1974). pH larutan selama berlangsung-nya pemasakan dapat mencapai 13 – 14, dengan suhu 170 oC, sedang tekanannya antara 7 – 7,7 atm.
Pada proses pulp sulfat/kraft, natrium hidroksida (NaOH) merupakan bahan kimia pemasak utama sedangkan natrium sulfida (Na2S) merupakan komponen aktif tambahan. Saat ini proses kraft merupakan proses pembuatan pulp alkalis yang paling penting karena diperoleh rendemen pulp yang lebih tinggi dan sifat-sifat pulp yang lebih unggul bila dibandingkan dengan pulp soda. Proses-proses pembuatan pulp dilakukan pada suhu 160 – 170oC pada tekanan antara 7 samapai 11 bar, waktu pemasakan 4 – 6 jam, sedangkan
34 proses cepat yang sinambung menggunakan suhu 190 – 200 oC, dan hanya membutuhkan waktu 15 – 30 menit.
Proses pulping/delignifikasi akan terpisah berupa larutan kaya akan lignin yang biasa disebut lindi hitam (black liquor). Menurut Bronges dkk (2005), kandungan bahan organik dan anorganik pada lindi hitam proses kraft disajikan pada Tabel 2.5
Tabel 2.5 Kandungan bahan organik dan anorganik pada lindi hitam (black liquor), proses proses kraft
No Komposisi Persentase (%, bk)
I Komponen organik:
a. Lignin 37,5
b. Asam sakarin (hemiselulosa) 22,6 c. Asam alifatik (karbohidrat) 14,4 d. Lemak dan resin (ekstraktif) 0,5
e. Polisakarida (selulosa ) 3,0 II Komponen anorganik: a. NaOH 2,4 b. NaHS 3,6 c. Na2CO3 dan K2CO3 9,2 d. Na2SO4 4,8 e. Na2S2O dan Na2S 0,5 f. NaCl 0,5
g. Lain-lain (Ca, Si, Mn, Mg dll) 0,2
Meskipun sampai saat ini lebih dari 80 % pulp kimia yang dihasilkan di dunia adalah pulp kraft, namun proses kraft masih memilki beberapa sisi kelemahan yaitu karena terdapat gas-gas berbau tidak enak yaitu senyawa-senyawa belerang dan kebutuhan bahan kimia pengelantangan yang tinggi pada pulp-pulp kraft kayu lunak, namun perkembangan terkhir diharapkan bahwa modifikasi baru akan membawa perbaikan perbaikan halam hal lingkungan.
Selama tahun-tahun terakhir perhatian yang meningkat telah dipusatkan pada pengurangan pencemaran dan hemat energi dalam industri pulp. Pada industri pulp sangat sulit memulihkan sama sekali belerang dioksida , namun pencemaran ini tidak dapat diterima karena akan menyebabkan pengaruh
lingkungan yang serius. Dan kerugiannya adalah terjadinya senyawa-senyawa belerang organik yang mudah menguap.
B.Proses Organosolv
Proses organosolv adalah suatu proses pemasakan/pulping pada suhu pemasakan tertentu dengan menggunakan pelarut organik yang berfungsi sebagai media reaksi seperti metanol, etanol, asam asetat, kelompok amina dengan atom C yang rendah. Penggunaan pelarut organik dimaksudkan untuk mengurangi tegangan permukaan larutan pemasak pada suhu tinggi, mempercepat penetrasi ke dalam serpih dan difusi dari hasil pemutusan lignin dalam kayu ke dalam larutan pemasak (Marton dan Granzow, 1982). Delignifikasi pada proses organosolv disebabkan oleh terputusnya ikatan eter, yaitu α–aril eter (α-O-4) dan aril gliserol-β-aril eter (β-O-4) dalam molekul lignin. Sherrard (1991) diacu dalam Heradewi (2007), menyatakan bahwa proses organosolv dengan menggunakan etanol sebagai bahan pemasak dengan kekuatan pulp kayu daun lebar sama dengan proses kraft. Suhu pemasakan yang paling efektif untuk delignifikasi berkisar pada selang antara 135-175°C. Katalisator sangat penting dalam proses pemasakan pulp. Fungsi katalis dalam hal ini selain berfungsi untuk mempercepat proses delignifikasi, juga berfungsi untuk mengembangkan struktur kayu sehingga memudahkan penetrasi larutan pemasak kedalam serpih dan penggunaan suhu pemasakan yang lebih rendah karena selama ini proses pulping organosolv dalam kondisi netral berlangsung pada suhu yang tinggi (175-210°C) untuk mencapai proses delignifikasi. Katalis yang digunakan dalam pulping organosolv terdapat dua jenis proses, yaitu proses organosolv asam (menggunakan katalis H2SO4 dan HCl) dan proses organosolv basa yang umumnya menggunakan NaOH atau Na2S.
Selama berlangsungnya proses pemasakan dalam digester yang berisi larutan soda api (NaOH), polimer lignin akan terdegradasi dan kemudian larut dalam air. Larutnya lignin ini disebabkan oleh terjadinya transfer ion hidrogen dari gugus hidroksil pada lignin ke ion hidroksil (Gambar 2.18) . Reaksi proses pulping organosolv sama dengan proses kraft maupun proses soda. Alkali tidak
36 mampu melarutkan selulosa alam, hanya sebagian selulosa yang terdepolime-risasi dengan derajat polimeterdepolime-risasi rendah dapat larut dalam alkali (NaOH).
Proses organosolv memiliki beberapa keuntungan seperti dampak terhadap lingkungan rendah karena proses ini tidak mengandung sulfur, memberikan produk-produk sampingan karena mudahnya pemisahan lignin sebagai bahan padat dan karbohidrat sebagai bahan gula. Menurut penelitian Rofiah (1993), proses pulping organosolv cocok untuk jenis kayu lunak dan non kayu dan tidak cocok untuk proses pulping dengan campuran dari beberapa jenis kayu keras . Delignifikasi TKKS dengan proses organosolv menghasilkan serpih TKKS yang lunak yang disebut pulp dan lindi hitam atau black liquor sebagai sisa larutan pemasak. Menurut Sherrad (1991) diacu dalam Heradewi (2007), di dalam lindi hitam proses organosolv menghasilkan lignin dengan bobot molekul rendah, gula-gula, dan hemiselulosa merupakan komponen paling banyak, diikuti oleh alkohol, furfural serta campuran fenol.
C.Proses Sulfit (NSSC)
Pulping proses sulfit disebut juga proses NSSC (netral sulfit semi chemical), pada umumnya digunakan untuk memproduksi pulp dari kayu daun lebar dengan rendemen tinggi. Pada proses ini delignifikasi tidak berlangsung dengan sempurna dan hanya sebagian lignin yang terpisahkan dari selulosa. Selama berlangsungnya proses pulping sulfit, lignin dari fase padat diubah menjadi sulfonat, sehingga kandungan lindi hitam proses sulfit adalah lignosulfonat, hemiselulosa dan ekstraktif. Pada proses sulfit lignin akan bereaksi dengan asam sulfit (H2SO3). Reaksi ini akan menyebabkan terlepasnya gugus hidroksil pada lignin dan terikatnya ion sulfit dari asam
larut dalam air
+ H2O
Gambar 2.18 Reaksi lignin dengan gugus hidroksil dari NaOH selama berlang-sungnya “pulping” proses kraft , soda maupun organosolv (Gilligan, 1974). CH3O HO
-
OH CH3OH -O C H C H C + H C H C H C Hsulfit ke dalam lignin (Gambar 2.19). Terlepasnya gugus hidroksil menyebabkan lignin terpisah dari selulosa dan kemudian larut dalam air (Gilligan, 1974)
2.6.1.2Teknik Isolasi/pemisahan Lignin
Isolasi lignin adalah proses pemisahan lindi hitam atau black liquor hasil proses pulping. Beberapa proses yang sudah dikembangkan dalam isolasi lignin antara lain isolasi lignin dari lindi hitam pabrik pulp kertas dan pirolisis serabut serta tandan kosong kelapa sawit. Secara teori proses dari keduanya mempunyai perlakuan sama dalam mengisolasi (mengambil) ligninnya. Menurut Sjöström (1995), isolasi lignin dibedakan pada tiga metode yaitu isolasi dengan pengasaman yang menggunakan pereaksi organik seperti H2SO4 pekat dan HCl pekat, isolasi dengan cellulolytic lignins (CEL), dan milled wood lignin (MWL)
Pengendapan lignin terjadi sebagai akibat terjadinya reaksi kondensasi pada unit-unit penyuling lignin (para-koumaril alkohol, koniferil alkohol dan sinapsil alkohol). Reaksi kondensasi pada unit-unit penyusun lignin dapat terjadi sebagai akibat penambahan asam. Penambahan asam kuat pada lindi hitam dapat menyebabkan terjadinya degradasi polisakharida, dekomposisi kompleks lignin-karbohidrat dan meningkatnya bobot molekul lignin, karena adanya reaksi polimerisasi. Menurut Sjöström (1995), kecepatan reaksi kondensasi akan meningkat dengan semakin meningkatnya keasaman. Proses isolasi dengan metode pengasaman (presipitasi asam) banyak digunakan untuk mendapatkan lignin dengan kemurnian tinggi (Kim et al., 1987). Urutan prosesnya adalah sebagai berikut: a) Pengendapan lignin dengan asam sulfat; b) Pelarutan endapan lignin dengan menggunakan NaOH; c) Pengendapan lagi dengan menggunakan asam sulfat; d) Pencucian dengan air; e) Pengeringan padatan lignin.
OH OCH3
+ HSO3
-SO3 - OCH3
+ H2O
larut dalam air
Gambar 2. 19 Reaksi antara lignin dengan ion hidrogen sulfida selama berlangsungnya “pulping” proses sulfit (Gilligan, 1974).
38 Metode lainnya adalah metode ekstraksi pelarut yang digunakan didasarkan pada perbedaan kelarutan lignin dan kelarutan zat ekstraktif, atau pembentukan senyawa-senyawa lignin yang larut. Salah satu pelarut yang digunakan adalah deoksan dan dapat dikristalkan dalam air dingin. Metode ini menghasilkan rendemen yang tidak terlalu tinggi, disamping itu bahan ekstraksi dioksan merupakan bahan yang relatif mahal.
2.6.1.3 Sulfonasi Lignin Isolat TKKS Menjadi Surfaktan Natrium Lignosul-fonat (NLS)
Natrium lignosulfonat (NLS) merupakan hasil reaksi sulfonasi lignin dengan bahan penyulfonasi seperti asam sulfat, oleum, natrium bisulfit (NaHSO3) maupun natrium thiosulfat. Tujuan dilakukan sulfonasi adalah memasukkan gugus sulfonat ke dalam lignin, sehingga mampu mengubah sifat hidrofilisitas lignin yang kurang polar (tidak larut air) menjadi NLS yang lebih polar (larut air). Dengan memasukkan gugus sulfonat dan garamnya (NaSO3-) ke dalam gugus hidroksil (OH-) lignin, mampu meningkatkan sifat hidrofilitasnya yang menyebabkan NLS mudah larut dalam air. Prinsip inilah yang menggambarkan NLS berperan sebagai surface active agent atau surfaktan. Dalam penelitian ”proses sulfonasi lignin isolat TKKS menjadi surfaktan natrium lignosulfonat (NLS), dilakukan dengan mengkombinasi penelitian Syahmani (2001) dan Yasuda et al. (2004). Dari penelitian Syahmani dan Yasuda perlu dilakukan perbaikan-perbaikan untuk mendapatkan kualitas produk NLS yaitu mendapatkan konversi (lignin bereaksi) tinggi serta kemurnian NLS tinggi . Disamping itu NLS yang dihasilkan memenuhi karakteristik sebagai bahan pendispersi pada sistem dispersi pertikel (pasta gipsum). Untuk meningkatkan sifat hidrofilitas NLS dan efisiensi terhadap kebutuhan bahan penyulfonasi natrium bisulfit NaHSO3, serta penanganan dalam pemurnian produk NLS, dilakukan dengan menambahkan katalis NaOH sekaligus sebagai pengatur pH sehingga tidak perlu menggunakan bahan penyulfonasi NaHSO3 yang berlebih.
Reaksi sulfonasi lignin menjadi NLS menggunakan katalis NaOH, berlangsung serupa dengan sulfonasi terhadap 1,2,diguaiasilpropana-1,3-diol (Gambar 2.20). Langkah pertama berlangsung melalui pembentukan kuinon
metida dengan pemecahan gugus α-hidroksil (eliminasi air). Reaksi adisi elektrofilik terhadap kuinon metida oleh bisulfit menghasilkan natriun 1,2-diguasilpropana-α-sulfonat (eliminasi air) dan diikuti adisi elektrofilik yang menghasilkan natrium 1,2-diguasilpropana-α, γ-disulfonat (Fengel dan Wegner, 1995). Reaksi sulfonasi lignin menjadi surfaktan NLS seperti disajikan pada Gambar 2.20
2.6.1.3.1 Optimasi Kondisi Proses Sulfonasi Menggunakan Metode Permu-kaan Respon
Untuk menentukan kondisi proses sulfonasi yang optimum digunakan metode permukaan respon atau response surface method (RSM). Menurut Montogomery (1992), RSM adalah suatu kumpulan dari teknik-teknik statistik dan matematika yang berguna untuk menganalisis permasalahan tentang beberapa variabel bebas yang mempengaruhi variabel tak bebas atau respon, serta bertujuan untuk mengoptimumkan respon tersebut. Pada dasarnya analisa permukaan respon adalah serupa dengan analisa regresi yaitu menggunakan prosedur pendugaan parameter fungsi respon berdasarkan metode kuadrat terkecil (least square method) dan diperluas dengan menerapkan teknik matematika untuk menentukan titik-titik optimum agar dapat ditemukan respon yang optimum (maksimum atau minimum).
Gambar 2.20 Reaksi Sulfonasi terhadap 1,2 – diguaiasilpropana – 1,3 – diol dengan katalis NaOH.
2 NaHSO3 -2H 2O Natrium 1,2 – diguaiasil propana α– γ - disulfonat 1,2 – diguaiasil
propana – 1,3 diol Kuinon metida
OCH3 Katalis NaOH HCOH HC H2 COH OH OCH3 OH OCH3 HCSO3Na HC H2CSO3Na OCH3 OH OH OCH3 O HC HC OCH3 OH H2COH
40 Pada penelitian proses produksi NLS belum diketahui bentuk hubungan antara respon dan variable-variabel bebas yang dispesifikasikan, maka langkah-langkah yang dilakukan adalah:
¾ menentukan variabel respon dan variabel bebas yang berpengaruh terhadap variabel respon dan menentukan interval variabel dari masing-masing variabel bebas;
¾ membuat model persamaan pada orde pertama dan uji kesahihan model dengan mengetahui ada tidaknya lack of fit dengan menggunakan analisa varians dan dilanjutkan dengan membuat rancangan pada orde ke dua;
¾ membuat dan menguji model orde ke dua;
¾ pemeriksaan dan pengujian asumsi terhadap model;
¾ menentukan kondisi optimum dari model yang sesuai;
¾ menganalisis kanonik untuk mempermudah penggambaran kontur dari permukaan respon .
Dari kasus penelitian yang dilakukan diatas dapat diketahui nantinya bahwa fungsi respon untuk k > 2 akan dicirikan oleh permukaan-permukaan respons konstan yang diharapkan. Analisis untuk menduga fungsi respons ini disebut sebagai analisis permukaan respons atau sering disebut teknik permukaan respon. Biasanya pada tahap awal dirumuskan model regresi polinomial dengan ordo yang rendah yaitu berordo satu yang tidak lain merupakan model regresi linear : ∈ + + + + + = o X X kXk Y
β
β
1 1β
2 2 ...β
Jika terdapat lengkungan dalam sistem, maka model polinomial dengan derajat lebih tinggi dapat dirumuskan. Rumusan model matematis untuk model polinomial ordo kedua adalah sebagai berikut :
∈ + + + + =
∑
∑
∑∑
< = = i j j i ij k i i ii k i i i o X X X X Y β β β β 1 2 1Untuk menentukan kondisi operasi optimum pada orde ke dua diperlukan rancangan komposit terpusat (central composite design) dalam pengumpulan data percobaan. Rancangan komposit terpusat (CCD) adalah rancangan faktorial 2k atau faktorial sebagian (fractional factorial), yang diperluas melalui penambahan
titik-titik pengamatan pada pusat agar memungkinkan pendugaan koefisien parameter permukaan ordo kedua (kuadratik).
Penentuan kondisi optimum proses dilakukan dengan menggunakan analisis kanonik (canonical analysis) dan analisa plot kontur permukaan respon. Analisis kanonik dalam metode permukaan respon adalah mentransformasikan permukaan respon dalam bentuk kanonik. Pada analisis ini akan diperoleh titik stasioner yaitu berupa titik dari respon maksimum, titik dari respon minimun maupun titik pelana (sadle point). Plot kontur adalah suatu seri garis atau kurva yang mengidentifikasi nilai-nilai peubah uji pada respon yang konstan sehingga plot kontur memegang peranan penting dalam mempelajari analisis permukaan respon. Pengujian model pada metode permukaan respon digunakan untuk mengetahui ketepatan model berdasarkan atas uji penyimpangan model atau lack of fit, R-kuad-rat (koefisien determinan), uji signifikansi model dan uji asumsi residual (Box et al, 1987; Box dan Draper, 1987; Gaspersz, 1995).
Kriteria utama dalam menentukan ketepatan model adalah bila uji simpangan dari model (lack of fit) bersifat tidak nyata secara statistik, serta model dianggap tidak tepat apabila uji penyimpangan dari model (lack of fit) bersifat nyata secara statistik, meskipun kriteria yang lain cukup memuaskan.
η2 X1 X2 η1 η3 X3 η4 η5 X4 X5
42 2.6.2 Pengembangan Proses Melalui Pendekatan Sistematis Empiris
(Pemodelan) , Simulasi, Optimasi serta Integrasi Proses Tahapan pengembangan proses ini meliputi:
1) Menyusun model kinetika reaksi yaitu menentukan model persamaan laju reaksi (rA) proses sulfonasi lignin isolat TKKS menjadi NLS, dan menentukan tetapan laju reaksi (k) dan parameternya: faktor frekuensi tumbukan (A), dan energi aktivasi (E),
2) Menyusun neraca massa dan neraca energi untuk mengetahui distribusi kebutuhan bahan baku, kebutuhan bahan pembantu dan simulasi neraca massa untuk berbagai kapasitas produk NLS,
3) Menyusun persamaan biaya produksi total (tc) sebagai fungsi kapasitas produksi NLS (P),
4) Melakukan optimasi untuk menentukan kapasitas optimum produksi NLS,
5) Menentukan perkiraan harga peralatan (purchased equipment cost), 6) Integrasi process engineering flow diagram (PEFD) proses sulfonasi
lingin dengan paket program HYSYS,
7) Analisis kelayakan finansial pendirian industri NLS.
2.6.2.1 Kinetika Reaksi
Kinetika reaksi merupakan ilmu yang mempelajari tentang kecepatan reaksi kimia secara kuantitatif serta faktor-faktor yang mempengaruhi kecepatan reaksi kimia tersebut. Pada kinetika kimia selain mempelajari kecepatan reaksi juga mempelajari : 1) Mekanisme reaksi, yaitu perubahan struktur atom dalam molekul zat pereaksi selama reaksi berlangsung, untuk membentuk zat hasil reaksi (produk reaksi). 2) Menentukan konstanta kecepatan reaksi (k). 3) Pengaruh variabel-variabel pada kecepatan reaksi.
Dalam kaitannya dengan perancangan proses, kinetika reaksi mempunyai beberapa fungsi utama yaitu: 1) Menentukan mekanisme reaksi kimia. (2) mengumpulkan data percobaan untuk kecepatan/laju reaksi. 3) Merancang volume/kapasitas reaktor yang sesuai. 4) Menetapkan kondisi operasi, cara pengontrolan dan alat-alat bantunya (Walas, 1981). Kecepatan reaksi
didefinisikan sebagai perubahan reaksi atau produk dalam satu satuan reaksi. Selain itu kecepatan reaksi (laju reaksi) didefinisikan juga sebagai laju berkurangnya konsentrasi suatu pereaksi atau laju bertambahnya suatu produk.
Model kinetika sederhana yang sering dipakai yaitu: -rA = k(t) CAa CBb
Keterangan :
k : konstanta kecepatan reaksi (fungsi dari temperatur) CA, CB : konsentrasi A dan B di dalam larutan
a : orde reaksi terhadap A b : orde reaksi terhadap B
Berdasarkan perhitungan-perhitungan disain reaktor yang sering digunakan maka persamaan laju reaksi dibedakan atas 2 tipe yaitu : 1) reaksi sederhana (single reaction). 2) reaksi kompleks (multiple reaction). Kecepatan reaksi tidak dapat diukur secara langsung, tetapi melalui pengukuran jumlah salah satu komponen reaksi pada setiap saat dengan cara sebagai berikut: 1) dengan mengukur konsentrasi. 2) dengan mengukur sifat-sifat fisik (daya hantar listrik, induksi bias dan viskositas). 3) dengan mengukur perubahan teknik pada sistem yang mempunyai volume tetap. 4) dengan mengukur perubahan volume pada sistem yang mempunyai tekanan tetap.
Pada umumnya untuk percobaan tersebut dilakukan pada reaktor batch dengan kondisi operasi volume dan temperatur tetap, hal ini akan sangat memudahkan untuk diinterpretasikan. Dalam menganalisis data yang diperoleh dari percobaan tersebut, untuk memperoleh persamaan kecepatan reaksi, ada 3 metode yang digunakan : 1) Metode integral. Untuk menguji persaman hasil integrasi dari data percobaan tersebut, ada 3 cara yaitu : cara grafik, cara waktu paruh, cara tabulasi. 2) Metode differensial dan 3) Cara isolasi.
Adapun tujuan analisis data kinetik tersebut adalah untuk mendapatkan nilai orde reaksi-reaksi konstanta laju reaksi. Berdasarkan perhitungan desain reaktor yang sering digunakan maka persamaan laju reaksi dibedakan atas 2 tipe yaitu: 1) reaksi sederhana (single reaction) : reaksi searah (irreversible) dan reaksi bolak-balik (reversible), 2) reaksi kompleks (multiple reaction).
44 Kinetika reaksi berdasar data reaktor batch adiabatis:
Proses sulfonasi lignin menjadi natrium lignosulfonat (NLS) dengan reaksi sebagai berikut:
[H2C(OH)R’R”]n + nNaHSO3 [H2C(SO3Na)R’R’’]n + nH2O Lignin Natrium bisulfit Natrium lignosulfonat Air
(NLS) atau bisa diwakili dengan persamaan berikut:
a A + b B → c C + d D
Neraca massa lignin (A) Dalam Reaktor adalah:
Kec. massa masuk - kec. massa keluar - kec. massa reaksi = kec. massa akumulasi dt ) (V.C d C . k V. 0 0 n A A = Volume reaktor dianggap tetap maka:
n A A A k .C dt ) (C d r =− =−
Penyelesaian untuk menghitung harga k dan orde reaksi digunakan cara integral. Jika reaksi sederhana:
Dibuat grafik hubungan antara konsentrasi zat pereaksi kunci/key component (lignin) dengan waktu reaksi
Dicari harga ( ) dt dCA
) pada t0; t1; t2; t3; t4;... seperti terlihat pada gambar dibawah ini
Persamaaan kecepatan reaksi yang terjadi A A A k C dt dC r - =− = ...1) ∫ − = ∫ − C t dtk C C dC 0 A A A 0 A ...2) k t ) C C ( ln ) C C ( ln A A A A 0 0 − = = − ...3) kt e C C atau kt e C C 0 0 A A A A = − = − ...4) Jika dinyatakan dalam konversi A = xA
ln (1 x ) k t...5) ) x 1 1 ( ln ] ) x (1 C C [ ln ) C C ( ln ) x (1 C C A A A A A A A A A A 0 0 0 0 = − − = − = − = − =
Jika reaksi tingkat dua:
Persamaan reaksi: A B A B A dt k C C dC dt dC r =− =− = − …………...6) Jika konversi A = xA, dan konsentrasi awal A dan B, berturut-turut
CA0 CA 0 t,, waktu mol bertambahnya C = rC mol berkurangnya A = -rA
46 CA0 dan CB0, maka : ) x C )(C x (1 kC dt dx C dt ) x (1 dC ) r ( A A A B A A A A A A 0 0 0 0 0 − = = − − − = − ...7) Jika konsentrasi awal CB0 = M CA0 atau (CB0/CA0) = M, maka :
(
)
kC (1 x )(M x ),dt dx C
rA = A0 A = 2A0 − A − A
− jika diintegralkan menjadi,
∫ = ∫ − − t 0 dt k C x 0 (1 x )(M x ) x d 0 A A A A A ………...8)
Setelah diintegralkan dan diubah kembali ke CA dan CB, diperoleh:
maka 9, dan 8 persamaan subtitusi #1, M Jika ) 9 .... ... ... C M C ln C C C C ln ) x (1 M x M ln x 1 x 1 ln A B A B A B A A A B 0 0 = = − − = ⎟⎟ ⎠ ⎞ ⎜⎜ ⎝ ⎛ − − atau 11) . ... ... ... ... ... k t ) C (C M C C ln atau ..10) ... ... ... k t ) C (C k t 1) (M C ) x (1 M x M n 0 0 0 0 0 A B A B A B A A A − = − = − = − − 12) .. ... ... ... ... M ln k t ) C (C C C ln B0 A0 A B = − + Tetapan Arrhenius :
)
13
...
...
...
...
...
...
...
...
e
k
-E/RTA
=
Keterangan:k : tetapan laju reaksi
A : faktor frekuensi tumbukan E : energi aktivasi reaksi T : suhu reaksi
R : tetapan gas
Dengan mengetahui konsentrasi lignin awal (CA0) dan konsentrasi natrium bisulfit awal (CB0) serta mengetahui konsentrasi masing-masing setiap fungsi waktu (CA dan CB) atau konversi lignin NLS setiap fungsi waktu, diperoleh harga