commit to user
UJI AKTIVITAS ANTIBAKTERI EKSTRAK DAUN PEPAYA
(Carica papaya L.) TERHADAP Streptococcus mutans
SECARA In vitro
SKRIPSI
Untuk Memenuhi Persyaratan
Memperoleh Gelar Sarjana Kedokteran
Muhamad Muamar
G.0008132
FAKULTAS KEDOKTERAN
UNIVERSITAS SEBELAS MARET
Surakarta
commit to user
PENGESAHAN SKRIPSI
Skripsi dengan judul :Uji Aktivitas Antibakteri Ekstrak Daun Pepaya
(Carica papaya L.) terhadap Streptococcus mutans Secara In vitro
Muhamad Muamar, NIM : G.0008132, Tahun : 2011 Telah diuji dan sudah disahkan di hadapan Dewan Penguji Skripsi
Fakultas Kedokteran Universitas Sebelas Maret Pada Hari Kamis, Tanggal 22 September Tahun 2011
Pembimbing Utama
Nama : Hudiono, Drs., MS.
NIP : 19580206 198601 1 001 ………
Pembimbing Pendamping
Nama : Leli Saptawati, dr., Sp.MK.
NIP : 19761227 200501 2 001 .………...
Penguji Utama
Nama : Marwoto, dr., M.Sc., Sp.MK.
NIP : 19590203 198601 1 004 ………
Anggota Penguji
Nama : Dr. Pradipto Subiyantoro, drg., Sp.BM.
NIP : 19570629 198403 1 003 ………
Surakarta, …… Ketua Tim Skripsi Dekan FK UNS
commit to user
PERNYATAAN
Dengan ini menyatakan bahwa dalam skripsi ini tidak terdapat karya yang pernah diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggi, dan sepanjang pengetahuan penulis juga tidak terdapat karya atau pendapat yang pernah ditulis atau diterbitkan oleh orang lain, kecuali secara tertulis diacu dalam naskah dan disebutkan dalam daftar pustaka.
Surakarta, 22 September 2011
commit to user
ABSTRAK
Muhamad Muamar, G.0008132, 2011. Uji Aktivitas Antibakteri Ekstrak Daun
Pepaya (Carica papaya L.) terhadap Streptococcus mutans secara In vitro. Skripsi, Fakultas Kedokteran, Universitas Sebelas Maret, Surakarta.
Tujuan Penelitian: Ekstrak daun pepaya memiliki kandungan senyawa latex
yang di dalamnya terdapat enzim papain (complex mixture chemical), senyawa alkaloid karpain, polifenol, saponin, dan flavonoid. Senyawa-senyawa tersebut diduga memiliki efek antibakteri. Penelitian ini bertujuan untuk mengetahui aktivitas antibakteri ekstrak daun pepaya terhadap pertumbuhan Streptococcus mutans secara In vitro.
Metode Penelitian: Penelitian ini bersifat eksperimental laboratorik dengan the
post test only controlled group design. Subjek penelitian adalah ekstrak daun papaya (Carica papaya L.) dengan sampel penelitian adalah bakteri Streptococcus mutans yang diambil dari usap rongga mulut dan gigi pasien dengan caries dentis. Teknik sampling dengan non random incidental sampling sebanyak 20 sampel pada setiap kelompok perlakuan. Uji sensitivitas menggunakan metode difusi cakram dengan media Muller Hinton agar. Data dianalisis menggunakan uji Kruskal-Wallis dilanjutkan uji Post Hoc (Mann-Whitney) dan juga menggunakan uji-tuntuk membandingkan data sampel dengan kuman standar.
Hasil Penelitian: Hasil uji Kruskal-Wallis menunjukkan adanya perbedaan daya
hambat yang bermakna (p < 0,05) antara kontrol negatif (aquadest), ekstrak daun pepaya 50 %, 75 %, 100 % dan kontrol positif (disk penicillin). Namun, tidak dijumpai perbedaan daya hambat yang bermakna antara kontrol negatif (aquadest) dan ekstrak daun pepaya 25 %. Ekstrak daun pepaya 50 % telah memiliki daya hambat terhadap Streptococcus mutans dan peningkatan konsentrasi sebanding dengan peningkatan zona hambatan kuman. Hasil penelitian juga menunjukkan tidak adanya perbedaan daya hambat yang bermakna (p > 0,05) antara sampel penelitian dengan kuman Streptococcus mutans standar.
Simpulan Penelitian: Ekstrak daun pepaya terbukti memiliki aktifitas daya
hambat terhadap pertumbuhan Streptococcus mutans yang sudah tampak pada pemberian ekstrak daun pepaya konsentrasi 50 %. Semakin tinggi konsentrasi ekstrak daun pepaya yang digunakan, maka semakin besar daya hambat antibakterinya. Bila dibandingkan dengan efek antibakteri penicillin, ekstrak daun pepaya dosis berapapun masih lebih rendah daya hambatnya dibandingkan dengan antibiotik penicillin terhadap Streptococcus mutans.
Kata kunci: ekstrak daun pepaya (Carica papaya L.), antibakteri, Streptococcus
commit to user
ABSTRACT
Muhamad Muamar, G.0008132, 2011. The Antibacterial Activity Test of the
Papaya Leaf Extract (Carica papaya L.) Toward Streptococcus mutans In vitro. Script, Faculty of Medicine, Sebelas Maret University, Surakarta. .
Objectives: Papaya leaf extract contains compounds which are considered to have
antibacterial effects, such as the latex compounds that contain papain enzyme (complex chemical mixtures), carpain alkaloid compounds, polyphenols, saponins, and flavonoids. The aim of this study is to determine the antibacterial activity of papaya leaf extract toward the growth of Streptococcus mutans In vitro.
Methods: This experimental research used a laboratory setting with the post test
only controlled group design. Subjects were papaya leaf extract (Carica papaya L.) and the samples were Streptococcus mutans from teeth and oral cavity swabs of patients with dental caries. The non random incidental sampling was used as much as 20 samples in each treatment group. The sensitivity test was using disc-diffusion method with the Muller Hinton agar media. Data were analyzed by using the Kruskal-Wallis test followed by post hoc test (Mann-Whitney test) and also
were analyzed by using t-test to compare samples and standard bacteria. .
Result: The results of the Kruskal-Wallis test showed significant differences in
inhibitory activities (p < 0.05) between the negative controls (the distilled water), papaya leaf extracts 50 %, 75 %, 100 % and the positive controls (the penicillin disc). However, hadn’t found significant difference in inhibitory activities between the negative controls (distilled water) and papaya leaf extracts 25 %. Papaya leaf extracts 50 % had minimal inhibitory activities against Streptococcus mutans and an increase in concentration of this sample is proportional to the increase in germ barrier zone. The results didn’t show significant difference in inhibitory activities (p > 0.05) between the study sample with the standardized Streptococcus mutans. .
Conclusions: The papaya leaf extract showed to have inhibitory activities against
the growth of Streptococcus mutans which has been shown in papaya leaf extracts of a concentration of 50 %. The higher concentration of papaya leaf extracts used, the greater the antibacterial inhibitory activities. When compared to the antibacterial effect of penicillin, all doses of papaya leaf extracts against
Streptococcus mutans are still lower compared to penicillin antibiotic. .
Keyword: papaya leaf extract (Carica papaya L.), antibacterial, Streptococcus
commit to user
PRAKATA
Segala puji bagi Allah, tidak ada sesembahan yang berhak diibadahi selain Allah, dengan rahmat dan pertolongan-Nya, penulis dapat menyelesaikan skripsi yang berjudul Uji Aktivitas Antibakteri Ekstrak Daun Pepaya (Carica papaya
L.) terhadap Streptococcus mutans secara In vitro. Shalawat dan salam semoga
tercurah kepada Rasulullah Shalallahu ‘Alaihi Wa Sallam dan orang-orang yang senantiasa mengikuti sunnahnya.
Dalam penyusunan skripsi ini, penulis banyak menemui kendala dan hambatan, namun berkat bimbingan, arahan serta bantuan berbagai pihak, penulis dapat menyelesaikannya. Untuk itu dengan setulus hati penulis menyampaikan rasa terima kasih kepada:
1. Prof. Dr. Zainal Arifin Adnan, dr., Sp.PD-KR-FINASIM, selaku Dekan Fakultas Kedokteran Universitas Sebelas Maret Surakarta.
2. Muthmainah, dr., M.Kes, selaku Ketua Tim Skripsi Universitas Sebelas Maret Surakarta.
3. Tri Nugraha Susilawati, dr., M.Med., selaku Pembimbing I awal yang telah banyak memberikan bimbingan, masukan, saran dan arahan dalam penelitian ini.
4. Hudiono, Drs., MS., selaku Pembimbing I pengganti yang telah banyak memberikan bimbingan, masukan, saran dan arahan dalam penelitian ini. 5. Leli Saptawati, dr., Sp.MK, selaku Pembimbing II pengganti yang telah
banyak memberikan bimbingan, masukan, saran dan arahan dalam penelitian ini.
6. Marwoto, dr., Sp.MK., M.Sc., selaku Penguji I yang telah berkenan menguji serta memberikan saran dan masukan dalam penelitian ini.
7. Dr. Pradipto Subiyantoro, drg., Sp.BM., selaku Penguji II yang telah berkenan menguji serta memberikan saran dan masukan dalam penelitian ini.
8. Seluruh Staf Bagian Skripsi dan Staf Laboratorium Mikrobiologi Fakultas Kedokteran Universitas Sebelas Maret yang telah banyak membantu dalam penelitian ini.
9. Ibu dan Ayah tercinta, Elli Iriana, S.Pd, serta Ir. Abil Huda; atas doa, saran, dan motivasi di setiap waktu pada penulis.
10.Penyemangat utama penulis yang tiada hentinya memberikan yang terbaik bagi penulis, MAP.
11.Teman-teman yang senantiasa membantu dalam skripsi ini: Ahmad, Ali, Yasjudan, Afandi, Alfin, Tenri, Deni, Iyas, Nafika, Rifki, Tri, Wegig, dan Syamsu.
12.Semua pihak yang telah membantu dalam penyusunan skripsi ini.
Penulis berharap semoga skripsi ini dapat bermanfaat bagi yang berkepentingan khususnya dan bagi pembaca umumnya.
commit to user
E. Identifikasi Variabel Penelitian ... 31
F. Definisi Operasional Variabel Penelitian ... 32
G. Prosedur Penelitian ... 33
H. Alat dan Bahan Penelitian ... 34
I. Cara Kerja ... 36
J. Teknik Analisis Data Statistik ... 39
commit to user
DAFTAR TABEL
Tabel 1. Hasil Pengukuran Diameter Zona Hambat (mm) Pertumbuhan
Streptococcus mutans pada Berbagai Konsentrasi Ekstrak Daun Pepaya, Kontrol Positif, dan Kontrol Negatif.
Tabel 2. Perbandingan antara Rerata Zona Hambat pada 20 Sampel yang Diteliti
dengan Bakteri Streptococcus mutans Standar.
Tabel 3. Hasil Uji Normalitas Kolmogorov-Smirnov
Tabel 4. Hasil Uji Kolmogorov-Smirnov Setelah Dilakukan Transformasi Data.
Tabel 5. Hasil Uji Kruskall-Wallis.
Tabel 6. Hasil Uji Mann-Whitney.
Tabel 7. Hasil Uji Shapiro-Wilk.
commit to user
DAFTAR GAMBAR
Gambar 1. Skema Kerangka Pemikiran.
Gambar 2. Skema Prosedur Penelitian.
Gambar 3. Populasi Sampel Menurut Umur dan Jenis Kelamin.
Gambar 4. Zona Hambat Rerata Ekstrak Daun Pepaya (Carica papaya L.)
commit to user
DAFTAR LAMPIRAN
Lampiran 1. Surat Ijin Penelitian dan Pengambilan Sampel
Lampiran 2. Surat Ijin Peminjaman Alat Pemeriksaan Gilut
Lampiran 3. Surat Ijin Pembuatan Ekstrak.
Lampiran 4. Lembar Kerja Uji Ekstraksi
Lampiran 5. Ethical Clearance.
Lampiran 6. Informed consent Subjek Penelitian.
Lampiran 7. Dokumentasi Penelitian.
commit to user
BAB I
PENDAHULUAN
A. Latar Belakang Masalah
Streptococcus mutans adalah agen utama penyebab caries dentis dan dipercayai sebagai penyebab tersering terjadinya proses cariogenic (pembentukan caries dentis) dibandingkan jenis Streptococcus lain. Streptococcus mutans yang melekat pada permukaan gigi akan memetabolisme berbagai macam karbohidrat, sisa makanan, yang menempel di gigi. Dari hasil perombakan karbohidrat, bakteri ini memproduksi asam yang menyebabkan terjadinya caries dentis (Karyn, 2002).
Caries dentis adalah suatu penyakit infeksi yang disebabkan oleh adanya interaksi antara bakteri, plak, dan lapisan email gigi. Plak gigi terutama disebabkan oleh bakteri Streptococcus mutans dan Lactobacillus (Kidd dan Joyston, 1992).
Streptococcus mutans banyak menyerang penduduk di seluruh dunia. Berdasarkan penelitian di negara – negara maju terdapat 8 – 35 % penderita caries dentis yang disebabkan oleh bakteri Streptococcus mutans (Karyn, 2002). Persentase penyakit caries dentis di Indonesia tergolong tinggi, 63 % orang Indonesia menderita caries dentis aktif, dengan prevalensi usia tertinggi pada kelompok usia 11-20 tahun (Probosari dan Pradopo, 2004).
Pengetahuan tentang agen penyebab caries dentis ini merupakan suatu hal yang penting dalam melakukan tindakan preventif terhadap penyakit ini. (Kidd dan Joyston, 1992). Pencegahan caries dentis disertai peningkatan kesehatan gigi telah lama menjadi tujuan utama dalam dunia kedokteran gigi sejak diketahui bahwa plak gigi merupakan faktor yang mendominasi penyebab rusaknya gigi oleh karena cariesdentis (Da Silva dkk., 2004).
commit to user
baik untuk individu maupun populasi (Kidd dan Joyston, 1992). Secara kimiawi, bahan antibakteri telah banyak digunakan, salah satunya berupa bahan kimia dalam pasta gigi. Namun, menurut penelitian, ternyata dalam pasta gigi juga terkandung senyawa berbahaya bagi kesehatan seperti fluoride dan DEG (Diethyle Glycol). (Turner, 2007; CDC, 2002).
Berbagai antibiotik telah banyak diteliti untuk menangani masalah caries dentis ini. Erythromycin, penicillin, methicillin, lincomycin, tetracycline, vancomycin, gentamicin, streptomycin, neomycin, kanamycin,
bacitracin, dan polymyxin B merupakan jenis antibiotik yang telah banyak diujicobakan sebagai terapi antibakteri pada Streptococcus mutans. Banyak dilaporkan kasus resistensi Streptococcus mutans terhadap jenis antibiotik erythromycin (Cowan, 1999).
Dewasa ini mulai ada kecenderungan untuk menggantikan bahan-bahan kimia. Beberapa negara maju kini telah mulai menekuni gaya hidup untuk kembali ke alam (back to nature). Para peneliti di Indonesia pun giat menggalakkan program pemanfaatan tanaman obat asli Indonesia. Dengan demikian obat tradisional asli Indonesia dapat berperan aktif dalam peningkatan derajat kesehatan masyarakat (Mursito, 2000). Selain murah dan mudah didapat, obat tradisional yang berasal dari tumbuhan relatif tidak menimbulkan efek samping (Fauziah, 1997).
Penelitian terkini pada terapi antibakteri mulai dikembangkan untuk menemukan bahan-bahan baru dari alam yang memiliki potensi terhadap daya antibakteri. Hal ini didasarkan pada kenyataan telah banyaknya resistensi terhadap berbagai antibiotik.
commit to user
Penelitian ini merupakan pengembangan dari penelitian-penelitian sebelumnya dengan tujuan untuk mengetahui daya antibakteri ekstrak daun pepaya terhadap Streptococcus mutans. Hasil penelitian yang diperoleh diharapkan dapat menjadi pertimbangan dalam pengembangan ekstrak daun pepaya untuk digunakan dalam rangka peningkatan kesehatan masyarakat.
B. Perumusan Masalah
Perumusan masalah pada penelitian ini adalah:
1. Apakah ekstrak daun pepaya (Carica papaya L) memiliki aktivitas antibakteri terhadap Streptococcus mutans secara In vitro?
2. Berapa kadar ekstrak daun pepaya (Carica papaya L) yang memiliki aktivitas antibakteri terhadap Streptococcus mutans secara In vitro?
C. Tujuan Penelitian
Penelitian ini bertujuan:
1. Mengetahui aktivitas antibakteri ekstrak daun pepaya (Carica papaya L.) terhadap Streptococcus mutans secara In vitro.
2. Mengetahui kadar ekstrak daun pepaya (Carica papaya L) yang memiliki aktivitas antibakteri terhadap Streptococcus mutans secara In vitro?
D. Manfaat Penelitian
1. Manfaat Teoritis
a. Menambah pengetahuan tentang khasiat obat bahan alam
commit to user 2. Manfaat Aplikatif
commit to user
BAB II
LANDASAN TEORI
A. Tinjauan Pustaka
1. Tanaman pepaya (Carica papaya L)
a. Sistematika
Tanaman pepaya dapat diklasifikasikan sebagai berikut: Kingdom : Plantae
Divisio : Spermatophyta Sub divisio : Angiospermae Class : Dicotyledonae Ordo : Cistales Familia : Caricacecae Genus : Carica
Species : Carica papaya L. (Steenis, 2002)
b. Nama Lain
commit to user
c. Deskripsi
Tanaman pepaya merupakan tanaman semak berbentuk pohon dengan batang lurus, bulat silindris, di bagian atas bercabang atau terkadang tidak, sebelah dalam batang serupa spons dan berongga, di luar batang terdapat tanda bekas daun yang banyak, tinggi 2,5 - 10 meter.
Daun berjejal pada ujung batang dan ujung cabang, tangkai daun bulat telur, bertulang dan jemari, berdaun menjari, ujung runcing dan pangkal berbentuk jantung, garis tengah 25-75 cm, taju selalu berlekuk menyirip tidak beraturan.
Bunga hampir selalu berkelamin satu dan berumah dua, tetapi terkadang terdapat juga bunga berkelamin dua pada karangan bunga yang jantan. Bunga jantan pada tandan yang serupa malai dan bertangkai panjang, berkelopak sangat kecil, mahkota berbentuk terompet, putih kekuningan, dengan tepi yang bertaju 5 dan tabung yang panjang, langsing, taju terputar dalam kuncup, kepala sari bertangkai pendek dan dengan posisi duduk. Bunga betina kebanyakan berdiri sendiri, daun mahkota lepas atau hampir lepas, berwarna putih kekuningan, bakal buah beruang satu, kepala putik 5, posisi duduk.
Buah bulat telur memanjang atau lonjong, berdaging dan berisi cairan; biji banyak, dibungkus oleh selaput yang berisi cairan, di dalamnya berduri tempel (Steenis, 2002).
d. Kandungan kimia
commit to user
polifenol dan bijinya mengandung saponin. Polifenol dan flavonoid merupakan golongan fenol yang telah diketahui memiliki aktivitas antiseptik (Hutapea, 2000). Buah mengandung beta karoten, pektin, delta-galaktosa, lamda-arabinosa, papain, papayotimin papain, alkaloid karpain, fitokinase, vitamin
A, vitamin C (Rahardjo, 2006).
2. Tinjauan Umum Bakteri Streptococcus mutans
a. Klasifikasi
Kingdom : Monera Filum : Firmicutes Class : Bacilli
Ordo : Lactobacilalles Famili : Streptococcaceae Genus : Streptococcus
Species : Streptococcus mutans (Bergey, 1998).
b. Deskripsi
Streptococcus viridans meliputi S. mitis, S. mutans, S. salivarius, S. sanguis, dan lain-lain. Ciri khas organisme ini adalah sifat α-hemolitik, tetapi dapat juga nonhemolitik (Brooks, dkk., 2007)
commit to user
dentis. Bakteri ini pertama diuraikan oleh Clarke pada tahun 1924 (Ryan, 2004; Loesche, 1996)
Bakteri ini mensintesis polisakarida dekstran atau levans dari sukrosa dan berperan penting menyebabkan terjadinya caries dentis (Brooks, dkk., 2007). Pembentukan dekstran oleh bakteri ini hanya ketika ada sukrosa dan diperantarai oleh enzim dekstransukrase (Madigan dan Martinko, 2006). Morfologi dan sifat pembenihan Streptococcus mutans adalah kokus gram positif, terdapat berpasangan dan dalam rantai, tidak berkapsul, tidak berspora, tidak bergerak, fakultatif anaerob, dan ditemukan di plak gigi (Pelczar dan Chan, 1998)
commit to user
Bakteri aerob tumbuh di media solid pada kadar udara ruangan (10 % CO2, dan 18 - 21% O2); bakteri fakultatif anaerob dapat tumbuh sama baik pada kondisi ada atau tidak ada O2 (10 - 15 %). Bakteri mikroaerofilik tidak dapat tumbuh sama sekali atau tumbuh dengan buruk pada kadar ruangan, tetapi, dapat tumbuh pada kadar O2 di bawah 10 %. Sedangkan bakteri anaerob dibagi menjadi dua, strict anaerob dapat tumbuh pada kadar kurang dari 0,5 % O2, dan moderate anaerob pada kadar 2 - 8 % O2. (Brooks, dkk., 2007)
Dalam keadaan fakultatif anaerob, bakteri ini memerlukan O2 dengan kadar 10 - 15%, juga memerlukan CO2 dan amonia sebagai sumber nitrogen agar dapat bertahan hidup dalam lapisan plak yang tebal (Ryan, 2004). Pertumbuhan sebagian besar Streptococcus hemolitik paling baik pada suhu 37°C (Brooks, dkk., 2007)
3. Caries Dentis
commit to user
terjadinya caries melalui bakteri rongga mulut yang mengubah sukrosa dan karbohidrat lain menjadi asam laktat yang selanjutnya akan menyerang enamel. Bakteri yang berperan paling penting dalam proses ini (cariogenic) adalah Streptococcus mutans (Tortora, dkk., 2007)
Caries dentis bersifat kronis dan dalam perkembangannya membutuhkan waktu lama sehingga sebagian besar penderita mempunyai potensi mengalami gangguan seumur hidup (Situmorang, 2005). Prevalensi penyakit gigi dan mulut di Indonesia cukup tinggi, sekitar 63% orang Indonesia menderita caries dentis aktif sehingga perlu adanya perhatian serius untuk menanganinya (Probosari dan Pradopo, 2004).
4. Antibakteri
a. Definisi
Antibakteri adalah senyawa kimia yang digunakan untuk membasmi bakteri, khususnya bakteri yang bersifat merugikan manusia (Jawetz dkk., 2005). Kadar minimal yang digunakan untuk menghambat pertumbuhan bakteri atau membunuh masing-masing dikenal sebagai Kadar Hambat Minimal (KHM) dan Kadar Bunuh Minimal (KBM). Antibakteri tertentu aktivitasnya dapat meningkat dari bakteriostatik menjadi bakterisid bila kadar antimikrobanya ditingkatkan melebihi KHM (Gan dkk., 1997).
commit to user
kecil. Toksisitas antibiotika ada dua yaitu toksisitas selektif (membunuh mikroorganisme yang menginvasi host tanpa merusak sel host) dan toksisitas relatif (perlu kontrol konsentrasi obat secara hati-hati sehingga dapat ditolerir tubuh). Aktivitas antibiotik umumnya dinyatakan dalam satuan berat (mg) kecuali yang belum sempurna permurniannya dan terdiri dari campuran beberapa macam zat, atau karena belum diketahui struktur kimianya, aktivitasnya dinyatakan dalam satuan internasional = Internasional Unit (IU). Dasar pertimbangan (ideal) pemberian antibiotik adalah Identifikasi & sensitivitas organisme, tempat infeksi, status pasien (umur, BB, keadaan patologis, kehamilan & laktasi), keamanan antibiotik, biaya.
Dalam pemberian antibiotika harus diperhatikan :
1) Dosis : kadar obat di tempat infeksi harus melampaui MIC kuman. Untuk
mencapai kadar puncak obat dalam darah, kalau perlu dengan loading dose (ganda) dan dimulai dengan injeksi kemudian diteruskan obat oral.
2) Frekuensi pemberian : tergantung waktu paruh (t½) obat. Bila t½
pendek, maka frekuensi pemberiannya sering.
3) Lama terapi : harus cukup panjang untuk menjamin semua kuman telah
mati & menghindari kekambuhan. Lazimnya terapi diteruskan 2-3 hari setelah gejala penyakit lenyap.
Faktor-faktor yang mempengaruhi aktivitas antibakteri In vitro: a) pH Lingkungan
commit to user d) Besarnya inokulum bakteri
e) Masa pengeraman
f) Aktivitas metabolik mikroorganisme (Jawetz dkk., 2005).
b. Klasifikasi Antibiotik
Antibiotika dapat digolongkan berdasarkan aktivitas daya hambat, cara kerja, spektrum maupun struktur kimianya.
1) Berdasarkan daya hambatnya
Bakteriostatika :
a) Menahan pertumbuhan & replikasi bakteri pada kadar serum yang dapat dicapai tubuh pasien.
b) Membatasi penyebaran infeksi saat sistem imun tubuh bekerja memobilisasi & mengeliminasi bakteri patogen.
c) Misalnya : Sulfonamid, Kloramfenikol, Tetrasiklin, Makrolid, Linkomisin.
Bakterisid :
a) Membunuh bakteri serta jumlah total organisme yang dapat hidup & diturunkan.
b) Pembagian :
1) Bekerja pada fase tumbuh kuman, misalnya : Penisilin, Sefalosporin, Kuinolon, Rifampisin, Polipeptida
commit to user
2) Berdasarkan cara kerjanya
Berdasarkan cara kerjanya kerja antibiotik dapat dibedakan menjadi sebagai berikut :
a) Antibiotik menghambat sintesis dinding sel mikroba
Dinding sel bakteri menentukan bentuk karakteristik dan berfungsi melindungi bagian dalam sel terhadap perubahan tekanan osmotik dan kondisi lingkungan lainnya. Di dalam sel terdapat sitoplasma dengan membran sitoplasma yang merupakan tempat berlangsungnya proses biokimia sel (Katzung dkk., 2005).
Dinding sel bakteri terdiri dari beberapa lapisan. Pada bakteri gram positif struktur dinding selnya relatif sederhana dan gram negatif relatif lebih komplek. Dinding sel bakteri gram positif tersusun atas lapisan peptidoglikan relatif tebal, dikelilingi lapisan teichoic acid dan pada beberapa species mempunyai lapisan polisakarida. Dinding sel bakteri gram negatif mempunyai lapisan peptidoglikan relatif tipis, dikelilingi lapisan lipoprotein, lipopolisakarida, fosfolipid dan beberapa protein. Peptidoglikan pada kedua jenis bakteri merupakan komponen yang menentukan rigiditas pada gram positif dan berperanan pada integritas gram negatif. Oleh karena itu gangguan pada sintesis komponen ini dapat menyebabkan sel lisis dan dapat menyebabkan kematian sel (Katzung dkk., 2005).
commit to user
penghambatan atau membinasakan hanya dilakukan selama pertumbuhan sel dan aktivitasnya dapat ditiadakan dengan menaikkan tekanan osmotik media untuk mencegah pecahnya sel. Bakteri tertentu seperti mikobakteria dan halobakteria mempunyai peptidoglikan relatif sedikit, sehingga kurang terpengaruh oleh antibiotik grup ini. Sel selama mensintesis peptidoglikan memerlukan enzim hidrolase dan sintetase. Untuk menjaga sintesis supaya normal, kegiatan kedua enzim ini harus seimbang satu sama lain. Biosintesis peptidoglikan berlangsung dalam beberapa stadium dan antibiotik pengganggu sintesis peptidoglikan aktif pada stadium yang berlainan. Sikloserin terutama menghambat enzim racemase dan sintetase yang berperan dalam pembentukan dipeptida. Vankomisin bekerja pada stadium kedua diikuti oleh basitrasin, ristosetin dan diakhiri oleh penisilin dan sefalosporin yaitu menghambat transpeptidase (Katzung dkk., 2005).
Perbedaan antara sel mamalia dan bakteri yaitu dinding sel luar bakteri tebal dengan membran sel menentukan bentuk sel dan memberi ketahanan terhadap tekanan osmotik. Karena struktur dinding sel mamalia tidak sama dengan dinding sel bakteri, maka antibiotik yang mempunyai aktivitas mengganggu sintesis inding sel mempunyai toksisitas selektif sangat tinggi. Oleh karena itu antibiotik tipe ini merupakan antibiotik yang sangat berharga (Katzung dkk., 2005).
commit to user
(1) Beta-laktam menghambat pertumbuhan bakteri dengan cara berikatan pada enzim DD-transpeptidase yang memperantarai dinding peptidoglikan bakteri, sehingga dengan demikian akan melemahkan dinding sel bakteri Hal ini mengakibatkan sitolisis karena ketidakseimbangan tekanan osmotis, serta pengaktifan hidrolase dan autolysins yang mencerna dinding peptidoglikan yang sudah terbentuk sebelumnya. Namun Beta-laktam (dan Penicillin) hanya efektif terhadap bakteri gram positif, sebab keberadaan membran terluar (outer membran) yang terdapat pada bakteri gram negatif membuatnya tak mampu menembus dinding peptidoglikan.
(2) Penicillin meliputi natural Penicillin, Penicillin G dan Penicillin V, merupakan antibiotik bakterisidal yang menghambat sintesis dinding sel dan digunakan untuk penyakit-penyakit seperti sifilis, listeria, atau alergi bakteri gram positif/Staphilococcus/Streptococcus. Namun karena Penicillin merupakan jenis antibiotik pertama sehingga paling lama digunakan telah membawa dampak resistansi bakteri terhadap antibiotik ini. Namun demikian Penicillin tetap digunakan selain karena harganya yang murah juga produksinya yang mudah.
commit to user
Staphilococcus dan Streptococcus. Adapun Polymixin B digunakan untuk bakteri gram negatif.
(4) Cephalosporin (masih segolongan dengan Beta-laktam) memiliki mekanisme kerja yang hampir sama yaitu dengan menghambat sintesis peptidoglikan dinding sel bakteri. Normalnya sintesis dinding sel ini diperantarai oleh PBP Penicillin Binding Protein (PBP) yang akan berikatan dengan D-alanin-D-alanin, terutama untuk membentuk jembatan peptidoglikan. Namun keberadaan antibiotik akan membuat PBP berikatan dengannya sehingga sintesis dinding peptidoglikan menjadi terhambat.
(5) Ampicillin memiliki mekanisme yang sama dalam penghancuran dinding peptidoglikan, hanya saja Ampicillin mampu berpenetrasi kepada bakteri gram positif dan gram negatif. Hal ini disebabkan keberadaan gugus amino pada Ampicillin, sehingga membuatnya mampu menembus membran terluar (outer membran) pada bakteri gram negatif.
commit to user
(7) Antibiotik jenis inhibitor sintesis dinding sel lainmemiliki spektrum
sasaran yang lebih luas, yaitu Carbapenems, Imipenem, Meropenem. Ketiganya bersifat bakterisidal.
b) Antibiotik mengganggu membran sel mikroba.
Di bawah dinding sel bakteri adalah lapisan membran sel lipoprotein yang dapat disamakan dengan membran sel pada manusia. Membran ini mempunyai sifat permeabilitas selektif dan berfungsi mengontrol keluar masuknya substansi dari dan ke dalam sel, serta memelihara tekanan osmotik internal dan ekskresi waste products. Selain itu membran sel juga berkaitan dengan replikasi DNA dan sintesis dinding sel. Oleh karena itu substansi yang mengganggu fungsinya akan sangat lethal terhadap sel (Katzung dkk., 2005).
commit to user
Polimiksin dapat merusak membran sel setelah bereaksi dengan fosfat pada fosfolipid membran sel. Sehingga polimiksin lebih aktif terhadap bakteri gram negatif daripada gram positif yang mempunyai jumlah fosfor lebih rendah. Antibiotik polyene hanya bekerja pada fungi tetapi tidak aktif pada bakteri. Dasar selektivitas ini, karena antibiotik bekerja berikatan dengan sterol yang ada pada membran fungi dan organisme yang lebih tinggi lainnya. Secara In vitro polyene dapat menyebabkan hemolisis, karena diduga membran sel darah merah mengandung sterol sebagai tempat aktivitas antibiotik polyene. Amfoterisin B juga dapat digunakan untuk infeksi sistemik tetapi sering disertai efek samping anemia hemolitik. Kerusakan membran sel dapat menyebabkan kebocoran sehingga komponen-komponen penting di dalam sel seperti protein, asam nukleat, nukleotida dan lain-lain dapat mengalir keluar. Diduga struktur membran ini ada pada mamalia, oleh karena itu antibiotik ini mempunyai toksisitas selektif relatif kecil dibanding antibiotik yang bekerja pada dinding sel bakteri, sehingga dalam penggunaan sistemik antibiotik ini relatif toksik; untuk mengurangi toksisitasnya dapat digunakan secara topikal (Katzung dkk., 2005).
c) Antibiotik menghambat sintesis protein mikroba
commit to user
(1) Ribosom 80s, terdapat pada sel eukariot. Partikel ini terdiri dari subunit 60s dan 40s.
(2) Ribosom 70s, didapatkan pada sel prokariot dan eukariot. Partikel ini terdiri dari subunit 50s dan 30s.
(3) Ribosom 55s, hanya terdapat pada mitokondria mamalia dan menyerupai ribosom bakteri baik fungsi maupun kepekaannya terhadap antibiotik.
Untuk memelihara kelangsungan hidupnya, sel mikroba perlu mensintesis protein yang berlangsung di dalam ribosom bekerja sama dengan mRNA dan tRNA; gangguan sintesis protein akan berakibat sangat fatal dan antimikroba dengan mekanisme kerja seperti ini mempunyai daya antibakteri sangat kuat (Katzung dkk., 2005).
Yang termasuk ke dalam golongan ini adalah Macrolide, Aminoglycoside, Tetracycline, Chloramphenicol, Kanamycin,
Oxytetracycline.
commit to user
(2) Aminoglycoside meliputi Streptomycin, Neomycin, dan Gentamycin, merupakan antibiotik bakterisidal yang berikatan dengan subunit 30s/50s sehingga menghambat sintesis protein. Namun antibiotik jenis ini hanya berpengaruh terhadap bakteri gram negatif.
(3) Tetracycline merupakan antibiotik bakteriostatis yang berikatan dengan subunit ribosomal 16S-30S dan mencegah pengikatan aminoasil-tRNA dari situs A pada ribosom, sehingga dengan demikian akan menghambat translasi protein. Namun antibiotik jenis ini memiliki efek samping yaitu menyebabkan gigi menjadi berwarna dan dampaknya terhadap ginjal dan hati.
(4) Chloramphenicol merupakan antibiotik bakteriostatis yang menghambat sintesis protein dan biasanya digunakan pada penyakit akibat kuman Salmonella. (Katzung dkk., 2005)
d) Antibiotik menghambat sintesis asam nukleat mikroba
commit to user
umumnya kurang selektif dalam membedakan sel bakteri dan sel mamalia. Antimikroba ini umumnya bersifat sitotoksik terhadap sel mamalia. Sehingga penggunaan antimikroba jenis ini harus hati-hati dan selektif yaitu yang sifat sitotoksiknya masih dapat diterima. Seperti asam nalidiksat dan rifampisin, karena aktivitasnya sangat kuat dalam menghambat pertumbuhan, maka antimikroba dengan mekanisme seperti ini sering digunakan sebagai anti-tumor. (Katzung dkk., 2005)
Antimikroba yang mempengaruhi sintesis asam nukleat dan protein mempunyai mekanisme kegiatan pada tempat yang berbeda, antara lain: (1) Antimikroba mempengaruhi replikasi DNA, seperti bleomisin,
phleomisin, mitomisin, edeine, porfiromisin.
(2) Antimikroba mempengaruhi transkripsi, seperti aktinomisin, kromomisin, ekonomisin, rifamisin, korisepin, streptolidigin.
(3) Antimikroba mempengaruhi pembentukan aminoacyl-tRNA, seperti borrelidin.
(4) Antimikroba mempengaruhi translasi, antara lain kloraphenikol, streptomisin, neomisin, kanamisin, karbomisin, crytromisin, linkomisin,
fluidic acid, tetrasiklin.
commit to user
e) Antibiotik mengganggu metabolisme sel mikroba.
Yang termasuk ke dalam golongan ini adalah Sulfa atau Sulfonamide, Trimetophrim, Azaserine.
(1) Pada bakteri, Sulfonamide bekerja dengan bertindak sebagai inhibitor kompetitif terhadap enzim dihidropteroate sintetase (DHPS). Dengan dihambatnya enzim DHPS ini menyebabkan tidak terbentuknya asam tetrahidrofolat bagi bakteri. Tetrahidrofolat merupakan bentuk aktif asam folat, di mana fungsinya adalah untuk berbagai peran biologis di antaranya dalam produksi dan pemeliharaan sel serta sintesis DNA dan protein. Biasanya Sulfonamide digunakan untuk penyakit Neiserria meningitis.
(2) Trimetophrim juga menghambat pembentukan DNA dan protein melalui penghambatan metabolisme, hanya mekanismenya berbeda dari Sulfonamide. Trimetophrim akan menghambat enzim dihidrofolate reduktase yang seyogyanya dibutuhkan untuk mengubah dihidrofolat (DHF) menjadi tetrahidrofolat (THF).
commit to user
5. Antibakteri Ekstrak Daun Pepaya
Daya antibakteri ekstrak daun pepaya disebabkan oleh adanya kandungan senyawa latex yang di dalamnya terdapat enzim papain (complex mixture chemical), senyawa alkaloid karpain, polifenol, saponin, dan flavonoid (Hutapea, 2000).
Enzim papain dapat mendenaturasi protein sel dengan mekanisme memproduksi senyawa koagulan yang mampu mengimobilisasi mikroorganisme sehingga sel fagosit dapat menghancurkan bakteri. Senyawa alkaloid karpain mampu mengganggu sintesis DNA bakteri. Polifenol mampu mendenaturasi protein dan merusak membran sel. Mekanisme kerjanya dengan memproduksi enzim inhibisi dari senyawa yang dioksidasi, kemungkinan melalui reaksi sulfihidril atau interaksi nonspesifik dengan protein sel. Proses ini mengakibatkan struktur tiga dimensi protein berubah dan berubah dan terbuka menjadi struktur acak tanpa adanya kerusakan pada stuktur kerangka kovalen, sehingga protein terdenaturasi. Deret asam amino tersebut tetap utuh setelah denaturasi, namun aktivitas biologisnya menjadi rusak sehingga protein tidak dapat melakukan fungsinya (Cowan, 1999)
commit to user
6. Uji Aktivitas Antibakteri
Penentuan kepekaan bakteri patogen terhadap antimikroba dapat dilakukan dengan salah satu dari dua metode pokok yakni dilusi atau difusi. Penting dalam menggunakan metode standar untuk mengendalikan semua faktor yang mempengaruhi aktivitas antibakteri (Jawetz dkk., 2005).
a. Metode Dilusi
Metode ini menggunakan antibakteri dengan kadar yang menurun secara bertahap, baik dengan media cair atau padat. Kemudian media diinokulasi bakteri uji dan dieramkan. Tahap akhir metode ini, antibakteri dilarutkan dalam kadar yang menghambat atau mematikan. Uji kepekaan cara dilusi cukup memakan waktu dan penggunaannya dibatasi pada keadaan tertentu saja. Uji kepekaan cara dilusi cair dengan menggunakan tabung reaksi, tidak praktis dan jarang dipakai. Namun, kini ada cara yang lebih sederhana dan banyak dipakai, yakni menggunakan microdilution plate (Jawetz dkk., 2005).
b. Metode Difusi
commit to user
molekular dan stabilitas obat). Meskipun demikian, standardisasi faktor-faktor tersebut memungkinkan melakukan uji kepekaan dengan baik (Jawetz dkk., 2005).
Beberapa faktor yang dapat mempengaruhi ukuran zona penghambatan dan harus dikontrol adalah :
1) Konsentrasi bakteri pada permukaan medium. Semakin tinggi konsentrasi mikroba maka zona penghambatan akan semakin kecil.
2) Kedalaman medium pada cawan petri. Semakin tebal medium pada cawan petri maka zona penghambatan akan semakin kecil.
3) Nilai pH dari medium. Beberapa antibiotika bekerja dengan baik pada kondisi asam dan beberapa basa kondisi alkali/ basa.
4) Kondisi aerob/ anaerob. Beberapa antibakterial kerja terbaiknya pada kondisi anaerob dan yang lainnya pada kondisi aerob (Cowan, 1999)
7. Metode Penyarian
commit to user
karbohidrat, dan lemak (Cowan, 1999). Adapun pada penelitian ini metode penyarian yang dipakai adalah metode maserasi.
a. Tujuan Ekstraksi
Tujuan ekstraksi adalah untuk menarik semua komponen kimia yang terdapat dalam simplisia. Ekstraksi ini didasarkan pada perpindahan masa komponen zat padat ke dalam pelarut di mana perpindahan mulai terjadi pada lapisan antarmuka, kemudian berdifusi masuk ke dalam pelarut.
Secara umum, terdapat empat situasi dalam menentukan tujuan ekstraksi: 1) Senyawa kimia telah diketahui identitasnya untuk diekstraksi dari
organisme. Dalam kasus ini, prosedur yang telah dipublikasikan dapat diikuti dan dibuat modifikasi yang sesuai untuk mengembangkan proses atau menyesuaikan dengan kebutuhan pemakai.
2) Bahan diperiksa untuk menemukan kelompok senyawa kimia tertentu, misalnya alkaloid, flavanoid atau saponin, meskipun struktur kimia sebetulnya dari senyawa ini bahkan keberadaannya belum diketahui. Dalam situasi seperti ini, metode umum yang dapat digunakan untuk senyawa kimia yang diminati dapat diperoleh dari pustaka. Hal ini diikuti dengan uji kimia atau kromatografik yang sesuai untuk kelompok senyawa kimia tertentu
commit to user
harus dicontoh semirip mungkin jika ekstrak akan melalui kajian ilmiah biologi atau kimia lebih lanjut, khususnya jika tujuannya untuk memvalidasi penggunaan obat tradisional.
4) Sifat senyawa yang akan diisolasi belum ditentukan sebelumnya dengan cara apapun. Situasi ini (utamanya dalam program skrining) dapat timbul jika tujuannya adalah untuk menguji organisme, baik yang dipilih secara acak atau didasarkan pada penggunaan tradisional untuk mengetahui adanya senyawa dengan aktivitas biologi khusus.
Proses pengekstraksian komponen kimia dalam sel tanaman yaitu pelarut organik akan menembus dinding sel dan masuk ke dalam rongga sel yang mengandung zat aktif, zat aktif akan larut dalam pelarut organik di luar sel, maka larutan terpekat akan berdifusi keluar sel dan proses ini akan berulang terus sampai terjadi keseimbangan antara konsentrasi cairan zat aktif di dalam dan di luar sel.
b. Prinsip ekstraksi Maserasi
commit to user
Selama proses maserasi dilakukan pengadukan dan penggantian cairan penyari setiap hari. Endapan yang diperoleh dipisahkan dan filtratnya dipekatkan.
commit to user Streptococcus mutans secara In vitro.
Complex
Gambar 1. Skema Kerangka Pemikiran
commit to user
BAB III
METODE PENELITIAN
A. Jenis Penelitian
Penelitian ini bersifat eksperimental laboratorik menggunakan rancangan the post test only with control group design dengan pendekatan cross sectional.
B. Lokasi Penelitian
Penelitian dilaksanakan di Laboratorium Mikrobiologi Fakultas Kedokteran Universitas Sebelas Maret Surakarta, Poliklinik Kesehatan Gigi dan Mulut Medical Center Universitas Sebelas Maret Surakarta, dan Instalasi Bagian Gigi dan Mulut RSUD dr. Moewardi Surakarta.
C. Subjek Penelitian
Subjek penelitian adalah ekstrak daun pepaya (Carica papaya L) yang diuji aktivitasnya dengan bakteri Streptococcus mutans secara In vitro.
D. Teknik Sampling
commit to user
Pengambilan sampel dilakukan pada bulan April - Juli 2011. Dalam penelitian ini digunakan 20 bakteri Streptococcus mutans sebagai sampel berdasarkan rumus Federer :
(k-1)(n-1) ≥15 k = kelompok perlakuan (6-1)(n-1) ≥ 15 n = jumlah tiap kelompok 5(n-1) ≥ 15
5n ≥ 15 + 5
n ≥ 4 à 20 ≥ 4
E. Identifikasi Variabel Penelitian
1. Variabel Bebas
Konsentrasi ekstrak daun pepaya (Carica papaya L.). 2. Variabel Terikat
Daya antibakteri terhadap Streptococcus mutans. 3. Variabel Luar
a. Variabel luar yang dapat dikendalikan
Proses ekstraksi, suhu, kelembaban, pH, aerogenesis. b. Variabel luar yang tidak dapat dikendalikan
commit to user
F. Definisi Operasional
1. Ekstrak daun pepaya (Carica papaya L.)
Ekstrak daun pepaya diperoleh dan diproses dengan metode maserasi di Lembaga Penelitiaan dan Pengembangan Terpadu Universitas Gajah Mada. Ekstrak daun pepaya diencerkan dengan aquadest steril, menggunakan perbandingan massa (gr) tiap ml pelarut aquadest steril. Konsentrasi ekstrak daun pepaya (Carica papaya L.) yang digunakan adalah 25 %, 50 %, 75 %, dan 100 %. Sedangkan antibiotik yang digunakan sebagai kontrol positif adalah Penicillin.
2. Streptococcus mutans
Bakteri Streptococcus mutans didapatkan dari usap rongga mulut pada subjek yang menderita caries dentis dan diidentifikasi dengan uji biokimia di Laboratorium Mikrobiologi Fakultas Kedokteran Universitas Sebelas Maret Surakarta. Pada penelitian ini dibutuhkan 20 isolat sampel.
3. Daya antibakteri terhadap Streptococcus mutans
commit to user
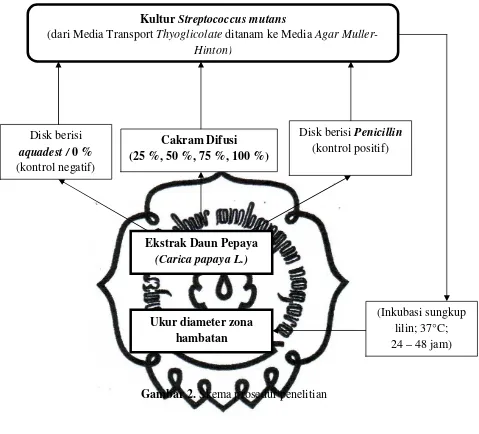
Kultur Streptococcus mutans
(dari Media Transport Thyoglicolate ditanam ke Media Agar Muller-Hinton)
G. Prosedur penelitian
Sampel dari swab rongga mulut
Streptococcus mutans
Medium transport Thyoglicolate (inkubasi sungkup lilin; 37°C; 24-48 jam)
24 – 48 jam)
Uji identifikasi S.mutans
Pengecatan Gram
Media Agar Darah (Inkubasi sungkup lilin; 37°C; 24 – 48 jam)
Tes Katalase
Gram (+) Katalase (-)
Uji Hemolise Tes Optochin
Hemolise sebagian Resisten pada uji
commit to user
(dari Media Transport Thyoglicolate ditanam ke Media Agar Muller-Hinton)
Gambar 2. Skema prosedur penelitian
H. Alat dan Bahan Penelitian
1. Alat Penelitian
a. Oshe kolong b. Pipet
c. Piring petri sedang d. Tabung reaksi e. Kaca objek f. Kapas lidi
Cakram Difusi (25 %, 50 %, 75 %, 100 %)
Disk berisi Penicillin (kontrol positif) Disk berisi
aquadest / 0 %
(kontrol negatif)
(Inkubasi sungkup lilin; 37°C; 24 – 48 jam)
Ukur diameter zona hambatan Ekstrak Daun Pepaya
commit to user h. Toples (sungkup lilin)
i. Lampu spiritus
j. Lilin (diameter 3,5 cm, tinggi 4 - 5 cm) k. Inkubator
l. Mikroskop m.Disk kosong n. Jangka sorong
2. Bahan Penelitian
a. Ekstak daun pepaya (Carica papaya L.) b. Aquadest
c. Cat Gram d. H202 0,3%
e. Disk antibiotik optochin f. Medium Thyoglicolate g. Media Agar Darah h. Muller-Hinton Agar
commit to user
I. Cara Kerja
1. Persiapan awal
Alat-alat yang diperlukan dicuci bersih kemudian dikeringkan dan disterilkan dalam autoklaf pada suhu 121°C selama 15 menit.
2. Isolasi Streptococcus mutans
Spesimen diambil dari usap rongga gigi dan mulut penderita caries dentis dengan menggunakan kapas lidi steril, sebelumnya penderita diminta untuk berkumur terlebih dahulu. Sampel yang telah diambil kemudian dimasukkan ke dalam medium thyoglicolate dan diinkubasi dalam sungkup lilin (37°C) selama 24-48 jam. Apabila tampak pertumbuhan bakteri pada medium thyoglycolate, kemudian dilakukan kultur pada media agar darah. Sisa koloni bakteri pada media thyoglicolate digunakan untuk uji identifikasi S. mutans dengan pengecatan Gram dan tes Katalase.
commit to user
3. Identifikasi Streptococcus mutans
a. Tes Hemolise
Spesimen ditanam pada media agar darah. Streptococcus mutans akan menunjukkan zona kehijauan di sekitar koloni dan akan menghemolisis sebagian (parsial) karena merupakan tipe α-hemoliticus (viridans).
b. Pengecatan Gram
Streptococcus mutans merupakan bakteri gram positif sehingga dengan pengecatan gram bakteri Streptococcus mutans akan terlihat berwarna ungu di bawah mikroskop.
c. Tes Katalase
1) Pijarkan oshe pada lampu spiritus, biarkan agak dingin, ambil 2-3 oshe larutan NaCl 0,9 %, letakkan pada kaca objek.
2) Pijarkan oshe pada lampu spiritus, biarkan agak dingin, ambil 2-3 oshe koloni Streptococcus mutans, campurkan pada larutan NaCl tadi
3) Teteskan larutan H202 0,3 % 1-2 tetes pada campuran bakteri dan larutan NaCl
4) Amati hasilnya
commit to user d. Skrining dengan antibiotik optochin
Antibiotik optochin adalah antibiotik yang digunakan untuk skrining bakteri Streptococcus mutans, digunakan dalam bentuk disk antibiotik dan akan menghasilkan hasil yang resisten terhadap bakteri Streptococcus mutans.
4. Persiapan ekstrak daun pepaya
Konsentrasi ekstrak daun pepaya (Carica papaya L.) 25 %, 50 %, 75 %, dan 100 %. Ekstrak daun pepaya (Carica papaya L.) diencerkan dengan menggunakan aquadest steril, dengan memakai perbandingan masa ekstrak daun pepaya (Carica papaya L.) tiap ml pelarut aquadest steril. Ekstrak ini adalah ekstrak steril yang telah disterilkan dalam autoklaf pada suhu 121°C selama 15 menit. Kemudian ekstrak digoreskan pada media agar darah dan mc concey untuk memastikan tidak ada koloni yang terbentuk akibat ekstrak yang tidak steril.
5. Persiapan disk ekstrak daun pepaya
Disk kertas saring ditetesi dengan ekstrak daun pepaya (Carica papaya L.) sesuai dengan konsentrasi masing-masing hingga jenuh, kemudian dibiarkan selama 10 menit dalam cawan petri steril dan diulang sekali lagi.
6. Pelaksanaan uji daya hambat bakteri
commit to user
dipersiapkan yaitu disk dengan ekstrak daun pepaya dan disk kontrol diletakkan di atas media tersebut. Disk kertas saring ditekan ringan dengan menggunakan pinset sehingga tidak melukai permukaan media. Jarak antara setiap disk diatur sedemikian rupa sehingga tidak akan mengganggu pengamatan hasil. Kemudian cawan petri tersebut dimasukkan ke dalam sungkup lilin lalu di inkubasi 37°C selama 24 – 48 jam. Zona hambatan yang terbentuk diukur dengan jangka sorong dalam satuan milimeter.
J. Teknik Penyajian Data
commit to user BAB IV
HASIL PENELITIAN
A. Hasil Penelitian
Hasil penelitian daya hambat ekstrak daun pepaya (Carica papaya L.)
terhadap pertumbuhan Streptococcus mutans dilakukan sebanyak 20 sampel,
dapat dilihat pada tabel berikut:
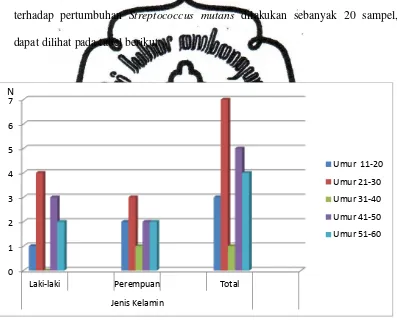
Gambar 3. Populasi Sampel Menurut Umur dan Jenis Kelamin
Gambar 3 menyajikan populasi sampel menurut umur dan jenis kelamin. Data
ditampilkan dalam bentuk jumlah dan presentase sehingga dapat dilihat sebaran
variasi sampel pada 20 sampel yang terdapat bakteri Streptococcus mutans.
commit to user
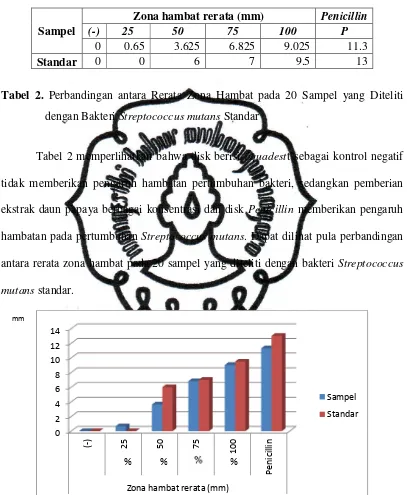
Streptococcus mutans pada Berbagai Konsentrasi Ekstrak Daun
Pepaya, Kontrol Positif, dan Kontrol Negatif
Tabel 1 menyajikan diameter zona hambatan pertumbuhan Streptococcus
mutans pada berbagai konsentrasi ekstrak daun papaya, kontrol positif (Penicillin),
dan kontrol negatif (aquadest) sangatlah bervariasi pada 20 sampel yang diteliti.
Tampak pula diameter zona hambat pertumbuhan bakteri Streptococcus mutans
commit to user
Tabel 2 memperlihatkan bahwa disk berisi aquadestt sebagai kontrol negatif
tidak memberikan pengaruh hambatan pertumbuhan bakteri, sedangkan pemberian
ekstrak daun papaya berbagai konsentrasi dan disk Penicillin memberikan pengaruh
hambatan pada pertumbuhan Streptococcus mutans. Dapat dilihat pula perbandingan
antara rerata zona hambat pada 20 sampel yang diteliti dengan bakteri Streptococcus
mutans standar.
Gambar 4. Zona Hambat Rerata Ekstrak Daun Pepaya (Carica papaya L.) terhadap
commit to user B. Analisis Data
Data yang diperoleh dari hasil penelitian, pertama kali diuji apakah ada
perbedaan rata-rata diameter aktivitas antibakteri yang bermakna antara keenam
kelompok dengan uji One-Way ANOVA. Analisis data dilakukan dengan
menggunakan program komputer Statistical Product and Service Solution
(SPSS) 16.0 for Windows.
Syarat menggunakan uji One-Way ANOVA:
1. Variabel data berupa variabel numerik/ kontinu/ rasio. Data pada penelitian ini
adalah diameter aktivitas antibakteri ekstrak daun pepaya terhadap
Streptococcus mutans yang dinyatakan dengan skala rasio.
2. Sebaran data harus normal, dibuktikan dengan nilai uji Kolmogorov-Smirnov
atau Saphiro-Wilk yang memiliki nilai p lebih besar daripada nilai alfa. Misal,
alfa = 0,05 maka nilai p untuk uji sebaran data harus > 0,05.
3. Varians data harus sama. Hal ini dapat diketahui dengan menggunakan uji
Homogeneity of Variances, di mana untuk varians data yang sama akan
memiliki nilai p > nilai alfa.
4. Jika ketiga syarat di atas tidak terpenuhi maka dapat digunakan uji hipotesis
alternatif yaitu berupa uji hipotesis non-parametrik Kruskall-Wallis (Dahlan,
2008).
Metode analisis yang dapat digunakan untuk menentukan sebaran data
normal atau tidak normal adalah uji Kolmogorov-Smirnov
commit to user
menggunakan total 120 sampel dengan jumlah 20 sampel tiap kelompok
perlakuan, maka digunakan uji Kolmogorov-Smirnov untuk menentukan apakah
sebaran data normal atau tidak. Hasil uji Kolmogorov-Smirnov dapat dilihat pada
lampiran 8, tabel 3.
Dari hasil uji Kolmogorov-Smirnov Didapatkan nilai p = 0.000. Dikatakan
bermakna atau memiliki distribusi yang normal bila nilai p > 0.05. Karena pada
penelitian ini nilai p uji normalitas < 0.05, maka data berdistribusi tidak normal.
Maka perlu dilakukan transformasi data agar data dapat berdistribusi normal.
Setelah dilakukan transformasi data didapatkan nilai p = 0.000, maka data
tetap berdistribusi tidak normal, maka uji one way Anova tidak dapat dilakukan.
Uji alternatif yang digunakan adalah uji Kruskal-Wallis. Hasil uji Kruskal-Wallis
dapat dilihat pada lampiran 8, tabel 5.
Dari hasil Uji Kruskal-Wallis, diperoleh p (Asymp sig) < 0.05, yaitu p =
0.000. Dapat disimpulkan bahwa terdapat perbedaan antara berbagai variabel
bebas terhadap daya hambat bakteri. Untuk mengetahui kelompok mana yang
memiliki perbedaan, maka harus dilakukan uji Post Hoc. Alat untuk melakukan
analisis Post Hoc untuk uji Kruskal-Wallis adalah dengan uji Mann-Whitney.
Data yang dibandingkan adalah Penicillin dengan aquadest, Penicillin
dengan kelompok 1 (ekstrak 25 %), Penicillin dengan kelompok 2 (ekstrak 50
%), Penicillin dengan kelompok 3 (ekstrak 75 %), Penicillin dengan kelompok 4
(ekstrak 100 %); aquadest dengan kelompok 1, aquadest dengan kelompok 2,
commit to user
kelompok 2, kelompok 1 dengan kelompok 3, kelompok 1 dengan kelompok 4;
kelompok 2 dengan kelompok 3, kelompok 2 dengan kelompok 4; kelompok 3
dengan kelompok 4.
Uji statistik kemudian dilanjutkan dengan uji Mann-Whitney yang dapat
dilihat pada lampiran 8, tabel 6. Hasil uji Mann-Whitney didapatkan :
a. Nilai p antarkelompok kontrol positif (Penicillin) - kontrol negatif (aquadest)
= 0,000; lebih kecil dari alfa (0,05).
b. Nilai p antarkelompok kontrol positif (Penicillin) - kelompok 1 (ekstrak 25 %)
= 0,000; lebih kecil dari alfa (0,05).
c. Nilai p antarkelompok kontrol positif (Penicillin) - kelompok 2 (ekstrak 50 %)
= 0,000; lebih kecil dari alfa (0,05).
d. Nilai p antarkelompok kontrol positif (Penicillin) - kelompok 3 (ekstrak 75 %)
= 0,000; lebih kecil dari alfa (0,05).
e. Nilai p antarkelompok kontrol positif (Penicillin) - kelompok 4 (ekstrak 100
%) = 0,016; lebih kecil dari alfa (0,05).
f. Nilai p antarkelompok kontrol negatif (aquadest) - kelompok 1 (ekstrak 25 %)
= 0,152; lebih besar dari alfa (0,05).
g. Nilai p antarkelompok kontrol negatif (aquadest) - kelompok 2 (ekstrak 50 %)
= 0,000; lebih kecil dari alfa (0,05)
h. Nilai p antarkelompok kontrol negatif (aquadest) - kelompok 3 (ekstrak 75 %)
commit to user
i. Nilai p antarkelompok kontrol negatif (aquadest) - kelompok 4 (ekstrak 100
%) = 0,000; lebih kecil dari alfa (0,05)
j. Nilai p antarkelompok 1 (ekstrak 25%) - kelompok 2 (ekstrak 50 %) =
0,003; lebih kecil dari alfa (0,05)
k. Nilai p antarkelompok 1 (ekstrak 25 %) - kelompok 3 (ekstrak 75 %) =
0,000; lebih kecil dari alfa (0,05)
l. Nilai p antarkelompok 1 (ekstrak 25 %) - kelompok 4 (ekstrak 100 %) =
0,000; lebih kecil dari alfa (0,05)
m. Nilai p antarkelompok 2 (ekstrak 50 %) - kelompok 3 (ekstrak 75 %) =
0,001; lebih kecil dari alfa (0,05)
n. Nilai p antarkelompok 2 (ekstrak 50 %) - kelompok 4 (ekstrak 100 %) =
0,000; lebih kecil dari alfa (0,05)
o. Nilai p antarkelompok 3 (ekstrak 75 %) - kelompok 4 (ekstrak 100 %) =
0,005; lebih kecil dari alfa (0,05)
Hasil ini menunjukkan bahwa:
1) Terdapat perbedaan daya hambat bakteri antara kelompok kontrol positif
(Penicillin) dengan kelompok kontrol negatif (aquadest)
2) Terdapat perbedaan daya hambat bakteri antara kelompok kontrol positif
(Penicillin) dengan ekstrak daun pepaya kelompok 1 (Ekstrak 25 %)
3) Terdapat perbedaan daya hambat bakteri antara kelompok kontrol positif
commit to user
4) Terdapat perbedaan daya hambat bakteri antara kelompok kontrol positif
(Penicillin) dengan ekstrak daun pepaya kelompok 3 (Ekstrak 75 %)
5) Terdapat perbedaan daya hambat bakteri antara kelompok kontrol positif
(Penicillin) dengan ekstrak daun pepaya kelompok 4 (Ekstrak 100 %)
6) Tidak terdapat perbedaan daya hambat bakteri antara kelompok kontrol
negatif (aquadest) dengan ekstrak daun pepaya kelompok 1 (Ekstrak 25 %)
7) Terdapat perbedaan daya hambat bakteri antara kelompok kontrol negatif
(aquadest) dengan ekstrak daun pepaya kelompok 2 (Ekstrak 50 %)
8) Terdapat perbedaan daya hambat bakteri antara kelompok kontrol negatif
(aquadest) dengan ekstrak daun pepaya kelompok 3 (Ekstrak 75 %)
9) Terdapat perbedaan daya hambat bakteri antara kelompok kontrol negatif
(aquadest) dengan ekstrak daun pepaya kelompok 4 (Ekstrak 100 %)
10) Terdapat perbedaan daya hambat bakteri antara ekstrak daun pepaya
kelompok 1 (Ekstrak 25 %) dengan ekstrak daun pepaya kelompok 2 (Ekstrak
50 %)
11) Terdapat perbedaan daya hambat bakteri antara ekstrak daun pepaya
kelompok 1 (Ekstrak 25 %) dengan ekstrak daun pepaya kelompok 3 (Ekstrak
75 %)
12) Terdapat perbedaan daya hambat bakteri antara ekstrak daun pepaya
kelompok 1 (Ekstrak 25 %) dengan ekstrak daun pepaya kelompok 4 (Ekstrak
commit to user
13) Terdapat perbedaan daya hambat bakteri antara ekstrak daun pepaya
kelompok 2 (Ekstrak 50 %) dengan ekstrak daun pepaya kelompok 3 (Ekstrak
75 %)
14) Terdapat perbedaan daya hambat bakteri antara ekstrak daun pepaya
kelompok 2 (Ekstrak 50 %) dengan ekstrak daun pepaya kelompok 4 (Ekstrak
100 %)
15) Terdapat perbedaan daya hambat bakteri antara ekstrak daun pepaya
kelompok 3 (Ekstrak 75 %) dengan ekstrak daun pepaya kelompok 4 (Ekstrak
100 %)
16) Ekstrak daun pepaya dosis 1 (25 %) tidak memiliki daya hambat bakteri yang
bermakna. Daya hambat bakterinya sama dengan aquadest.
17) Semakin tinggi kadar daun pepaya, semakin baik daya hambatnya terhadap
bakteri.
18) Penicillin lebih baik daya hambatnya terhadap bakteri dibandingkan dengan
ekstrak daun pepaya dengan dosis berapa pun.
Kemudian dilakukan uji perbandingan antara bakteri sampel dengan
bakteri standar American Type Culture Collection (ATCC) untuk mengetahui
karakteristik bakteri yang digunakan. Uji yang digunakan adalah uji-t tidak
berpasangan. Salah satu syarat uji-t tidak berpasangan adalah data harus
berdistribusi normal. Uji normalitas yang digunakan adalah Shapiro-Wilk karena
uji analitis ini lebih sensitif dan objektif dibandingkan uji yang lain. Kemudian
commit to user
dibandingkan kurang dari 50, yakni 12 yang merupakan penjumlahan dari 6
kelompok data bakteri usap dan 6 kelompok data bakteri standar. Hasil uji
Shapiro-Wilk dapat dilihat pada lampiran 8, tabel 7.
Dari hasil uji Shapiro-Wilk didapatkan p > 0.05 pada bakteri usap maupun
bakteri standar, yaitu p = 0.628 pada data bakteri usap dan p = 0.508 pada data
bakteri standar. Karena nilai p > 0.05, dapat disimpulkan bahwa distribusi daya
hambat bakteri pada kelompok bakteri usap maupun kelompok bakteri standar
berdistribusi normal.
Selanjutnya dilakukan uji-t tidak berpasangan untuk mengetahui
karakteristik bakteri sampel yang digunakan dibandingkan bakteri standar. Hasil
uji-t tidak berpasangan dapat dilihat pada lampiran 8, tabel 8.
Dari hasil uji-t tidak berpasangan didapatkan pada kotak Levene’s Test
(nama uji hipotesis untuk menguji varians), nilai p (sig) = 0.926. Karena nilai p >
0.05, maka varians data kedua kelompok adalah sama. Oleh karena varians sama,
maka untuk melihat hasil uji-t tidak berpasangan memakai baris pertama atau
baris equal variances assumed. Angka signifikansi baris pertama adalah p (sig 2
tailed) = 0.814 (tidak signifikan), dengan perbedaan rerata (mean difference)
sebesar -0,68. Nilai IK 95% adalah antara -6.96 sampai 5.60. Karena nilai 0
tercakup dalam rentang IK 95%, maka tidak signifikan atau tidak ada perbedaan
yang bermakna. Karena p > 0.05 atau IK 95% mencakup nilai 0, maka dapat
disimpulkan tidak terdapat perbedaan daya hambat bakteri pada jenis bakteri usap
commit to user
memiliki kesamaan karakter dengan bakteri standar, atau tidak memiliki
perbedaan yang bermakna. Maka dalam penelitian ini secara umum, karakteristik
kuman usap yang dipakai sebagai sampel tidak memiliki perbedaan bermakna
commit to user BAB V
PEMBAHASAN
Telah dilakukan penelitian uji aktivitas antibakteri ekstrak daun
pepaya (Carica papaya L.) terhadap pertumbuhan bakteri Streptococcus mutans.
Penelitian dilakukan dengan ekstrak daun pepaya konsentrasi 25 %, 50 %, 75 %,
dan 100 %. Aquadest digunakan sebagai kontrol negatif, dan disk Penicillin
sebagai kontrol positif.
Gambar 3 menunjukkan gambaran umur dan jenis kelamin 20
responden yang ikut serta dalam penelitian. Berdasarkan data yang diperoleh,
diketahui bahwa Streptococcus mutans banyak ditemukan pada kelompok umur
21-30 tahun baik laki maupun perempuan, terutama pada jenis kelamin
laki-laki. Hal tersebut dapat disebabkan oleh perilaku pada usia remaja hingga dewasa
muda yang sebagian besar kurang menjaga kebersihan gigi dan mulut. Pola
makan, merokok, meminum alkohol, dan lain sebagainya merupakan faktor
penyebab terjadinya caries dentis pada kelompok umur tersebut, di samping
faktor komponen gigi dan air ludah, mikroorganisme penghasil asam, dan waktu
(Julianti, dkk., 2008).
Tabel 1 menggambarkan rerata diameter zona hambatan pertumbuhan
bakteri pada tiap konsentrasi. Hal tersebut sesuai dengan hipotesis bahwa ekstrak
daun pepaya mempunyai daya hambat terhadap pertumbuhan Streptococcus
commit to user
pertumbuhan Streptococcus mutans pada berbagai konsentrasi ekstrak daun
papaya pada kontrol positif, dan kontrol negatif. Pada konsentrasi ekstrak daun
pepaya sebesar 25%, ternyata belum menunjukkan daya hambat yang bermakna
terhadap Streptococcus mutans, hanya 2 dari total 20 sampel ini yang
menunjukkan efek antibakteri. Hasil dari kelompok pada konsentrasi tersebut
relatif sama dengan kontrol negatif. Perbedaan daya hambat antibakteri ekstrak
daun pepaya pada konsentrasi 25 %, 50 %, 75 % dan 100 % tampak signifikan
dan aktifitas antibakterinya berbanding lurus dengan peningkatan kadar ekstrak.
Pada kelompok daun papaya 100 % hasilnya mendekati kontrol positif disk
antibiotik Penicillin. Hal ini menunjukkan bahwa dengan konsentrasi ekstrak
daun pepaya 100 % memiliki khasiat yang mendekati kekuatan disk Penicillin
yang dibuktikan dengan nilai p = 0,016; lebih kecil dari alfa (0,05). Berdasarkan
penelitian sebelumnya, yaitu penelitian Oladimeji dkk., tahun 2007, didapatkan
hasil ekstrak daun pepaya memiliki efek antibakteri, tetapi masih di bawah efek
antibakteri penicillin.
Berdasarkan data pada tabel 2, rerata diameter zona hambat yang
terbentuk pada ekstrak daun papaya 25 % adalah 0,65 mm, 50 % adalah 3,63 mm,
75 % adalah 6,83 mm, 100 % adalah 9,03 mm, dan kontrol positif adalah 11,3
mm. Rerata diameter zona hambatan kelompok sampel hampir sama dengan
rerata diameter zona hambatan pada kuman standar. Pada kuman standar
didapatkan diameter zona hambatan ekstrak daun papaya 25 % adalah 0 mm, 50
commit to user
adalah 13 mm. Berdasarkan hasil uji-T tidak berpasangan pada lampiran 8, tabel
8, bakteri usap pada penelitian ini tidak memiliki perbedaan yang bermakna.
Maka dalam penelitian ini, karakteristik kuman usap yang dipakai sebagai sampel
tidak memiliki perbedaan bermakna dengan karakteristik kuman standar.
Gambar 4 menunjukkan bahwa konsentrasi ekstrak daun papaya 25 %
belum memberikan efek hambatan terhadap Streptococcus mutans dan
peningkatan konsentrasi ekstrak daun papaya mengakibatkan peningkatan
diameter zona hambat. Hal ini menunjukkan adanya hubungan dosis-respon
(dose-response relationship). Temuan ini memperkuat simpulan hubungan kausal
antara pemberian ekstrak daun pepaya (Carica papaya L.) dengan pertumbuhan
Streptococcus mutans. (Dahlan, 2008)
Penelitian ini pada mulanya akan dianalisis dengan menggunakan uji
One Way ANOVA untuk mengetahui apakah ada perbedaan rerata hitung yang
signifikan pada semua kelompok perlakuan, tetapi karena data tidak memenuhi
syarat distribusi normal dan varians yang sama, maka dilakukan transformasi data
agar berdistribusi normal dan varians sama. Namun, karena data tetap tidak
memenuhi syarat, uji analisis yang digunakan menjadi uji Kruskal Wallis. Setelah
dilakukan uji Kruskal Wallis didapatkan p < 0,05 hampir pada semua sampel
perlakuan, atau dengan kata lain terdapat perbedaan yang signifikan pada
perlakuan-perlakuan tersebut. Terdapat 1 data perbedaan yang tidak signifikan