UNSUR, SENYAWA & CAMPURAN
.
Unsur
.
Unsur adalah zat tunggal yang tidak dapat diuraikan lagi menjadi zat yang lebih sederhana. Ada banyak cara untuk menggabungkan elemen dengan berbagai macam bahan berbeda di dunia ini untuk mengubah satu kombinasi unsur menjadi suatu persenyawaan yang lain. Meskipun kombinasi unsur dapat berubah, unsur tidak dapat dibuat atau dihancurkan. Biarpun besi bekas berkarat dan berubah bentuk, tetapi jumlah besinya tidak berubah. Cahaya, panas, dan suara adalah bentuk energi. Energi adalah kemampuan untuk menghasilkan perubahan. Setiap kali terjadi perubahan dalam bentuk apa pun, pasti melibatkan energi, dan setiap kali bentuk energi diubah ke bentuk lain, itu adalah bukti bahwa perubahan sedang atau telah terjadi.
Berikut adalah daftar unsur dalam tabel unsur periodik.
No Simbol Nama bentuk Grup Periode Blok Berat Atom(Da)
Kepadatan (g/cm3)
Titik lebur (k)
Titik didih (k)
Kapasitas kalor (J/g · K)
Keelektrone gatifan
Kelimpahan unsur (mg/kg)
1 H Hidrogen Gas 1 1 S 1,008 0,00008988 14,01 20,28 14,304 2,20 1400
2 He Helium Gas 18 1 S 4,0026 0,0001785 0,95 4,22 5,193 – 0,008
3 Li Lithium Padat 1 2 S 6,94 0,534 453,69 1560 3,582 0,98 20
4 Be Beryllium Padat 2 2 S 9,0122 1,85 1560 2742 1,825 1,57 2,8
5 B Boron Padat 13 2 P 10,81 2,34 2349 4200 1,026 2,04 10
6 C Carbon Padat 14 2 P 12,011 2,267 >4000 4300 0,709 2,55 200
7 N Nitrogen Gas 15 2 S 14,007 0,0012506 63,15 77,36 1,04 3,04 19
8 O Oxygen Gas 16 2 P 15,999 0,001429 54,36 90,20 0,918 3,44 461000
9 F Fluorine Gas 17 2 P 18,998 0,001696 53,53 85,03 0,824 3,98 585
10 Ne Neon Gas 18 2 S 20,180 0,0008999 24,56 27,07 1,03 – 0,005
11 Na Sodium Padat 1 3 S 22,990 0,971 370,87 1156 1,228 0,93 23600
12 Mg Magnesium Padat 2 3 S 24,305 1,738 923 1363 1,023 1,31 23300
13 Al Aluminium Padat 13 3 P 26,982 2,698 933,47 2792 0,897 1,61 82300
14 Si Silicon Padat 14 3 P 28,085 2,3296 1687 3538 0,705 1,9 282000
15 P Phosphorus Padat 15 3 P 30,974 1,82 317,30 550 0,769 2,19 1050
16 S Sulfur Padat 16 3 P 32,06 2,067 388,36 717,87 0,71 2,58 350
17 Cl Chlorine Gas 17 3 P 35,45 0,003214 171,6 239,11 0,479 3,16 145
18 Ar Argon Gas 18 3 S 39,95 0,0017837 83,80 87,30 0,52 – 3,5
19 K Potassium Padat 1 4 S 39,098 0,862 336,53 1032 0,757 0,82 20900
20 Ca Calcium Padat 2 4 S 40,078 1,54 1115 1757 0,647 1,00 41500
21 Sc Scandium Padat 3 4 D 44,956 2,989 1814 3109 0,568 1,36 22
22 Ti Titanium Padat 4 4 F 47,867 4,54 1941 3560 0,523 1,54 5650
23 V Vanadium Padat 5 4 F 50,942 6,11 2183 3680 0,489 1,63 120
24 Cr Chromium Padat 6 4 S 51,996 7,15 2180 2944 0,449 1,66 102
25 Mn Manganese Padat 7 4 S 54,938 7,44 1519 2334 0,479 1,55 950
26 Fe Iron Padat 8 4 D 55,845 7,874 1811 3134 0,449 1,83 56300
27 Co Cobalt Padat 9 4 F 58,933 8,86 1768 3200 0,421 1,88 25
28 Ni Nickel Padat 10 4 F 58,693 8,912 1728 3186 0,444 1,91 84
29 Cu Copper Padat 11 4 S 63,546 8,96 1357,77 2835 0,385 1,90 60
No Simbol Nama bentuk Grup Periode Blok Berat Atom(Da)
Kepadatan (g/cm3)
Titik lebur (k)
Titik didih (k)
Kapasitas kalor (J/g · K)
Keelektrone gatifan
Kelimpahan unsur (mg/kg)
30 Zn Zinc Padat 12 4 S 65,38 7,134 692,88 1180 0,388 1,65 70
31 Ga Gallium Padat 13 4 P 69,723 5,907 302,914 2673 0,371 1,81 19
32 Ge Germanium Padat 14 4 P 72,630 5,323 1211,40 3106 0,32 2,01 1,5
33 As Arsenic Padat 15 4 S 74,922 5,776 1090 887 0,329 2,18 1,8
34 Se Selenium Padat 16 4 P 78,971 4,809 453 958 0,321 2,55 0,05
35 Br Bromine Cair 17 4 P 79,904 3,122 265,8 332,0 0,474 2,96 2,4
36 Kr Krypton Gas 18 4 S 83,798 0,003733 115,79 119,93 0,248 3,00 1×10−4
37 Rb Rubidium Padat 1 5 S 85,468 1,532 312,46 961 0,363 0,82 90
38 Sr Strontium Padat 2 5 S 87,62 2,64 1050 1655 0,301 0,95 370
39 Y Yttrium Padat 3 5 D 88,906 4,469 1799 3609 0,298 1,22 33
40 Zr Zirconium Padat 4 5 F 91,224 6,506 2128 4682 0,278 1,33 165
41 Nb Niobium Padat 5 5 D 92,906 8,57 2750 5017 0,265 1,6 20
42 Mo Molybdenum Padat 6 5 S 95,95 10,22 2896 4912 0,251 2,16 1,2
43 Tc Technetium Padat (buatan) 7 5 S 97 11,5 2430 4538 – 1,9 ~ 3×10−9
44 Ru Ruthenium Padat 8 5 F 101,07 12,37 2607 4423 0,238 2,2 0,001
45 Rh Rhodium Padat 9 5 F 102,91 12,41 2237 3968 0,243 2,28 0,001
46 Pd Palladium Padat 10 5 S 106,42 12,02 1828,05 3236 0,244 2,20 0,015
47 Ag Silver Padat 11 5 S 107,87 10,501 1234,93 2435 0,235 1,93 0,075
48 Cd Cadmium Padat 12 5 S 112,41 8,69 594,22 1040 0,232 1,69 0,159
49 In Indium Padat 13 5 P 114,82 7,31 429,75 2345 0,233 1,78 0,25
50 Sn Tin Padat 14 5 P 118,71 7,287 505,08 2875 0,228 1,96 2,3
51 Sb Antimony Padat 15 5 S 121,76 6,685 903,78 1860 0,207 2,05 0,2
52 Te Tellurium Padat 16 5 P 127,60 6,232 722,66 1261 0,202 2,1 0,001
53 I Iodine Padat 17 5 P 126,90 4,93 386,85 457,4 0,214 2,66 0,45
54 Xe Xenon Gas 18 5 S 131,29 0,005887 161,4 165,03 0,158 2,60 3×10−5
55 Cs Caesium Padat 1 6 S 132,91 1,873 301,59 944 0,242 0,79 3
56 Ba Barium Padat 2 6 S 137,33 3,594 1000 2170 0,204 0,89 425
57 La Lanthanum Padat n/a 6 D 138,91 6,145 1193 3737 0,195 1,1 39
58 Ce Cerium Padat n/a 6 G 140,12 6,77 1068 3716 0,192 1,12 66,5
No Simbol Nama bentuk Grup Periode Blok Berat Atom(Da)
Kepadatan (g/cm3)
Titik lebur (k)
Titik didih (k)
Kapasitas kalor (J/g · K)
Keelektrone gatifan
Kelimpahan unsur (mg/kg)
59 Pr Praseodymium Padat n/a 6 I 140,91 6,773 1208 3793 0,193 1,13 9,2
60 Nd Neodymium Padat n/a 6 I 144,24 7,007 1297 3347 0,19 1,14 41,5
61 Pm Promethium Padat (buatan) n/a 6 H 145 7,26 1315 3273 – 1,13 2×10−19
62 Sm Samarium Padat n/a 6 F 150,36 7,52 1345 2067 0,197 1,17 7,05
63 Eu Europium Padat n/a 6 S 151,96 5,243 1099 1802 0,182 1,2 2
64 Gd Gadolinium Padat n/a 6 D 157,25 7,895 1585 3546 0,236 1,2 6,2
65 Tb Terbium Padat n/a 6 H 158,93 8,229 1629 3503 0,182 1,2 1,2
66 Dy Dysprosium Padat n/a 6 I 162,50 8,55 1680 2840 0,17 1,22 5,2
67 Ho Holmium Padat n/a 6 I 164,93 8,795 1734 2993 0,165 1,23 1,3
68 Er Erbium Padat n/a 6 H 167,26 9,066 1802 3141 0,168 1,24 3,5
69 Tm Thulium Padat n/a 6 F 168,93 9,321 1818 2223 0,16 1,25 0,52
70 Yb Ytterbium Padat n/a 6 S 173,05 6,965 1097 1469 0,155 1,1 3,2
71 Lu Lutetium Padat 3 6 D 174,97 9,84 1925 3675 0,154 1,27 0,8
72 Hf Hafnium Padat 4 6 F 178,49 13,31 2506 4876 0,144 1,3 3
73 Ta Tantalum Padat 5 6 F 180,95 16,654 3290 5731 0,14 1,5 2
74 W Tungsten Padat 6 6 D 183,84 19,25 3695 5828 0,132 2,36 1,3
75 Re Rhenium Padat 7 6 S 186,21 21,02 3459 5869 0,137 1,9 7×10−4
76 Os Osmium Padat 8 6 D 190,23 22,61 3306 5285 0,13 2,2 0,002
77 Ir Iridium Padat 9 6 F 192,22 22,56 2719 4701 0,131 2,20 0,001
78 Pt Platinum Padat 10 6 D 195,08 21,46 2041,4 4098 0,133 2,28 0,005
79 Au Gold Padat 11 6 S 196,97 19,282 1337,33 3129 0,129 2,54 0,004
80 Hg Mercury Cair 12 6 S 200,59 13,5336 234,43 629,88 0,14 2,00 0,085
81 Tl Thallium Padat 13 6 P 204,38 11,85 577 1746 0,129 1,62 0,85
82 Pb Timbal Padat 14 6 P 207,2 11,342 600,61 2022 0,129 2,33 14
83 Bi Bismuth Padat 15 6 S 208,98 9,807 544,7 1837 0,122 2,02 0,009
84 Po Polonium Padat 16 6 P 209 9,32 527 1235 – 2,0 2×10−10
85 At Astatine Padat 17 6 P 210 7 575 610 – 2,2 3×10−20
86 Rn Radon Gas 18 6 S 222 0,00973 202 211,3 0,094 2,2 4×10−13
87 Fr Francium Padat 1 7 S 223 1,87 281 890 – >0,79 ~ 1×10−18
No Simbol Nama bentuk Grup Periode Blok Berat Atom(Da)
Kepadatan (g/cm3)
Titik lebur (k)
Titik didih (k)
Kapasitas kalor (J/g · K)
Keelektrone gatifan
Kelimpahan unsur (mg/kg)
88 Ra Radium Padat 2 7 S 226 5,5 973 2010 0,094 0,9 9×10−7
89 Ac Actinium Padat n/a 7 D 227 10,07 1323 3471 0,12 1,1 5,5×10−10
90 Th Thorium Padat n/a 7 F 232,04 11,72 2115 5061 0,113 1,3 9,6
91 Pa Protactinium Padat n/a 7 K 231,04 15,37 1841 4300 – 1,5 1,4×10−6
92 U Uranium Padat n/a 7 L 238,03 18,95 1405,3 4404 0,116 1,38 2,7
93 Np Neptunium Padat (buatan) n/a 7 L 237 20,45 917 4273 – 1,36 ≤ 3×10−12
94 Pu Plutonium Padat (buatan) n/a 7 F 244 19,84 912,5 3501 – 1,28 ≤ 3×10−11
95 Am Americium Padat (buatan) n/a 7 S 243 13,69 1449 2880 – 1,13 –
96 Cm Curium Padat (buatan) n/a 7 D 247 13,51 1613 3383 – 1,28 –
97 Bk Berkelium Padat (buatan) n/a 7 H 247 14,79 1259 2900 – 1,3 –
98 Cf Californium Padat (buatan) n/a 7 I 251 15,1 1173 1743 – 1,3 –
99 Es Einsteinium Padat (buatan) n/a 7 I 252 8,84 1133 1269 – 1,3 –
100 Fm Fermium tidak diketahui n/a 7 H 257 9,7 1800 – – 1,3 –
101 Md Mendelevium tidak diketahui n/a 7 F 258 10,3 1100 – – 1,3 –
102 No Nobelium tidak diketahui n/a 7 S 259 9,9 1100 – – 1,3 –
103 Lr Lawrencium tidak diketahui 3 7 P 266 15,6 1900 – – 1,3 –
104 Rf Rutherfordium tidak diketahui 4 7 F 267 23,2 2400 5800 – – –
105 Db Dubnium tidak diketahui 5 7 D 268 29,3 – – – – –
106 Sg Seaborgium tidak diketahui 6 7 D 269 35,0 – – – – –
107 Bh Bohrium tidak diketahui 7 7 D 270 37,1 – – – – –
108 Hs Hassium tidak diketahui 8 7 D 269 40,7 – – – – –
109 Mt Meitnerium tidak diketahui 9 7 D 278 37,4 – – – – –
110 Ds Darmstadtium tidak diketahui 10 7 D 281 34,8 – – – – –
111 Rg Roentgenium tidak diketahui 11 7 D 282 28,7 – – – – –
112 Cn Copernicium tidak diketahui 12 7 D 285 14,0 283 340 – – –
113 Nh/Uut Nihonium tidak diketahui 13 7 P 286 16 700 1400 – – –
114 Fl/Uuq Flerovium tidak diketahui 14 7 P 289 9,928 200 380 – – –
115 Mc/Uup Moscovium tidak diketahui 15 7 P 288 13,5 700 1400 – – –
116 Lv/Uuh Livermorium tidak diketahui 16 7 P 293 12,9 700 1100 – – –
117 Ts/Uus Tennessine tidak diketahui 17 7 P 294 7,2 700 883 – – –
118 Og/Uuo Oganesson tidak diketahui 18 7 P 294 13,65 325 320 - 380 – – –
Penamaan unsur ada beberapa macam aturan, seperti penamaan berdasarkan nama lokasi, nama benda astronomi, nama orang, ataupun berdasarkan sistem penomoran tertentu. Contoh nama unsur berdasarkan nama tempat, antara lain:
No Nama unsur Simbol Nomor
urut unsur Lokasi
1 Europium Eu 63 Europe
2 Magnesium Mg 12 Magnesia, Yunani 3 Manganese Mn 25 Magnesia, Yunani 4 Beryllium Be 4 Belur, India
5 Indium In 49 India (indicum/indigo)
6 Copper Cu 29 Siprus
7 Francium Fr 87 Perancis
8 Gallium Ga 31 Perancis (Galia) 9 Lutetium Lu 71 Paris (Lutetia)
10 Germanium Ge 32 Germany
11 Hassium Hs 108 Hassia, Jerman 12 Darmstadtium Ds 110 Darmstadt, Jerman 13 Rhenium Re 75 Sungai Rhein, Swiss
14 Strontium Sr 38 Vila Strontian, Skotlandia
15 Scandium Sc 21 Scandinavia
16 Hafnium Hf 72 Copenhagen (Hafnia), Denmark 17 Thulium Tm 69 Thule, Greenland, Denmark 18 Holmium Ho 67 Stockholm (Holmia), Swedia 19 Yttrium Y 39 Vila Ytterby, Swedia
20 Terbium Tb 65 Vila Ytterby, Swedia 21 Erbium Er 68 Vila Ytterby, Swedia 22 Ytterbium Yb 70 Vila Ytterby, Swedia
23 Polonium Po 84 Polandia
24 Ruthenium Ru 44 Rusia (Ruthenia) 25 Moscovium Mc 115 Oblast Moskwa, Rusia
26 Dubnium Db 105 Dubna, Rusia
27 Americium Am 95 Amerika
28 Californium Cf 98 California, Amerika
29 Berkelium Bk 97 Berkeley, California, Amerika
No Nama unsur Simbol Nomor
urut unsur Lokasi
30 Livermorium Lv 116 Laboratorium Nasional Lawrence Livermore, Amerika
31 Tennessine Ts 117 Tennessee, Amerika 32 Nihonium Nh 113 Japan (Nihon)
Contoh nama unsur berdasarkan nama benda astronomi, antara lain:
No Nama unsur Simbol Nomor
urut unsur Nama benda astronomi
1 Helium He 2 Matahari
2 Mercury Hg 80 Planet Merkurius
3 Selenium Se 34 Bulan
4 Palladium Pd 46 Asteroid Pallas
5 Tellurium Te 52 Planet Bumi
6 Cerium Ce 58 Planet Ceres
7 Uranium U 92 Planet Uranus
8 Neptunium Np 93 Planet Neptunus 9 Plutonium Pu 94 Planet Pluto
Contoh nama unsur berdasarkan nama orang, antara lain:
No Nama unsur Simbol Nomor
urut unsur Nama Orang Asal Negara
1 Samarium Sm 62 Vasili Samarsky Rusia
2 Gadolinium Gd 64 Johan Gadolin Finlandia
3 Americium Am 95 Amerigo Vespucci Italia
4 Curium Cm 96 Marie Curie
Pierre Curie Polandia–Prancis Perancis
5 Berkelium Bk 97 George Berkeley Irlandia
6 Einsteinium Es 99 Albert Einstein Jerman–Swiss
7 Fermium Fm 100 Enrico Fermi Italia–Amerika
8 Mendelevium Md 101 Dmitri Mendeleev Rusia
9 Nobelium No 102 Alfred Nobel Orang Swedia
10 Lawrencium Lr 103 Ernest Lawrence Amerika
11 Rutherfordium Rf 104 Ernest Rutherford Selandia Baru–Inggris
12 Seaborgium Sg 106 Glenn T. Seaborg Amerika
No Nama unsur Simbol Nomor
urut unsur Nama Orang Asal Negara
13 Bohrium Bh 107 Niels Bohr Denmark
14 Meitnerium Mt 109 Lise Meitner Austria–Swedia
15 Roentgenium Rg 111 Wilhelm Röntgen Jerman
16 Copernicium Cn 112 Nicolaus Copernicus Polandia–Jerman
17 Flerovium Fl 114 Georgy Flyorov Rusia
18 Livermorium Lv 116 Robert Livermore Inggris–Meksiko
19 Oganesson Og 118 Yuri Oganessian Rusia
Nama unsur ada juga yang berdasarkan nomor urut atom. Kamus angkanya adalah sebagai berikut:
Nil = 0 Pent = 5
Un = 1 Hex = 6
Bi = 2 Sept = 7
Tri = 3 Okt = 8
Quad = 4 Enn = 9
Sistem penamaan unsur berdasarkan nomor urut atom biasanya menggunakan rumus:
kamus angka + ium.
Contoh nama unsur berdasarkan nomor urut atom, antara lain:
No Nama unsur Simbol Nomor urut
unsur 1 Ununtrium (Nihonium) Uut (Nh) 113 2 Ununquadium (Flerovium) Uuq (Fl) 114 3 Ununpentium (Moscovium) Uup (Mc) 115 4 Ununhexium (Livermorium) Uuh (Lv) 116 5 Ununseptium (Tennessine) Uus (Ts) 117 6 Ununoctium (Oganesson) Uuo (Og) 118
Senyawa
.
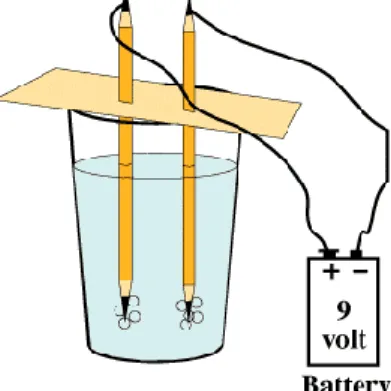
Senyawa adalah zat tunggal yang masih dapat dipecah atau diuraikan lagi sesuai dengan unsur pembentuknya. Air dapat dipisahkan menjadi oksigen dan hidrogen dengan cara elektrolisis. Gula pasir akan terurai menjadi karbon jika direaksikan dengan asam sulfat.
Gambar elektrolisis terhadap air. Gambar pemisahan gula menjadi arang.
Rumus senyawa merupakan gabungan lambang unsur yang menunjukkan jenis unsur pembentuk senyawa dan jumlah atom masing-masing unsur. Beberapa contoh senyawa pada kehidupan keseharian manusia, antara lain:
No Nama Senyawa Rumus Kegunaan
1 Asam asetat CH₃COOH Cuka makan
2 Amoniak NH₃ Pupuk
3 Asam askorbat C₆H₈O₆ Vitamin C
4 Kalsium karbonat CaCO₃ Kalsit (Bahan Bangunan)
5 Karbon dioksida CO₂ Penyegar Minuman
Sukrosa mempunyai rumus C₁₂H₂₂O₁₁. Rumus tersebut menunjukkan bahwa sukrosa tersusun dari 12 atom karbon (C), 22 atom hidrogen (H) dan 11 atom oksigen (O). Urea merupakan pupuk yang telah lama digunakan.
Urea mempunyai rumus senyawa CO(NH₂)₂. Dari rumus senyawa tersebut dapat ditunjukkan bahwa urea tersusun dari unsur 1 atom karbon (C), 1 atom oksigen (O₂), 2 atom nitrogen (N) dan 4 atom hidrogen (H).
Campuran
.
Campuran adalah sebuah materi yang terbuat karena dua zat atau lebih yang saling gabung tanpa adanya reaksi kimia dan atom molekul tidak menempel satu sama lain seperti senyawa. Contoh campuran adalah udara yang dihirup makhluk hidup yang mana terdiri atas oksigen, hidrogen, nitrogen, dll dimana semuanya tercampur tetapi tidak saling terikat antar atom molekulnya. Campuran dibagi menjadi 2, yaitu : campuran homogen dan campuran heterogen.
Campuran homogen.
Campuran homogen adalah dua atau lebih campuran unsur atau senyawa pembentuknya larut merata dan hasil campuran yang terbentuk terlihat seragam. Contoh: campuran air dan garam, campuran air dan cuka, dll. Nama lain dari campuran homogen adalah larutan.
Campuran heterogen.
Campuran heterogen adalah dua atau lebih campuran unsur atau senyawa pembentuknya tidak larut secara merata dan unsur atau senyawanya masih terlihat jelas pada campuran yang terbentuk. Contoh: campuran air dan pasir.
ASAM, BASA DAN GARAM
.
Perbedaan mendasar asam, basa dan garam adalah rasa. Asam memiliki rasa asam kecut, basa memiliki rasa pahit, sedangkan garam memiliki rasa asin. Meskipun begitu membedakan rasa melalui lidah bukanlah langkah yang aman, karena asam dan basa pada zat kimia tertentu dapat merusak tubuh, dalam kondisi parah bahkan bisa menyebabkan kanker.
Contoh asam:
No Nama Asam Contoh
1 Asam asetat Cuka makan
2 Asam askorbat Vitamin C
4 Asam karbonat Minuman bersoda
5 Asam borat Larutan tetes mata
6 Asam klorida Asam lambung di perut
7 Asam laktat Keju
Contoh basa:
No Nama Basa Contoh
1 Alumunium hidroksida Deodoran, antasid 2 Kalsium hidroksida Mortar dan plester
3 Natrium hidroksida sabun
Sifat dari asam, basa atau garam apabila dilarutkan dalam air akan menghasilkan ion-ion.
Ion adalah zat atau partikel yang bermuatan listrik. Larutan yang memiliki muatan listrik dinamakan larutan elektrolit. Sifat lain dari asam, basa atau garam adalah bersifat korosif.
Reaksi antara asam dan basa akan menghasilkan garam dan air. Jadi reaksi asam dengan basa bisa disebut juga dengan penggaraman. Garam dapur (NaCl) merupakan salah satu contoh garam hasil reaksi antara asam klorida dan natrium hidroksida.
Contoh garam:
No Nama Garam Rumus Contoh
1 Natrium klorida NaCl Garam dapur
2 Natrium bikarbonat NaHCO₃ Baking soda
3 Kalsium karbonat CaCO₃ Kalsit
4 Kalium nitrat KNO₃ Pupuk, bahan peledak
5 Kalium karbonat K₂CO₃ Potash
6 Natrium fosfat Na₃PO₄ Deterjen
7 Amonium klorida NH₄Cl Baterai kering
Identifikasi asam, basa dan garam
.
Cara penentuan senyawa bersifat asam, basa atau netral dapat menggunakan kertas lakmus, larutan indikator atau indikator alami. Sedangkan untuk menentukan nilai dari suatu zat asam atau basa, digunakan yang namanya pH (Power of Hydrogen) meter. Untuk kertas lakmus, terdapat standarisasi warna dimana warna tertentu menunjukkan nilai terhadap suatu zat asam atau basa. Suatu zat netral memiliki nilai pH 7, asam memiliki nilai kurang dari 7, sedangkan basa memiliki nilai pH lebih dari 7. Secara kimia, jika dilarutkan kedalam air maka zat asam melepaskan ion hidrogen (H⁺) sedangkan zat basa melepaskan ion hidroksida (OH⁻).
Untuk mengidentifikasi asam, basa dan garam menggunakan kertas lakmus, maka perlu kertas lakmus dua warna digunakan sebagai pembanding, yaitu kertas lakmus merah dan biru. Zat asam akan cenderung mengubah warna kertas lakmus menjadi merah, sedangkan zat basa akan cenderung mengubah kertas lakmus menjadi biru.
Adapun zat yang netral tidak akan merubah kertas lakmus baik kertas lakmus yang merah ataupun kertas lakmus yang biru.
Berikut tabel perubahan warna kertas lakmus.
Indikator Zat Netral Zat asam Zat basa
Lakmus merah Merah Merah Biru
Lakmus biru Biru Merah Biru
Mengidentifikasi asam atau basa menggunakan larutan indikator, yang sering digunakan adalah fenolftalin, metil merah, metil violet, metil jingga dan bromcresol hijau.
Adapun tabel perubahan warnanya adalah sebagai berikut:
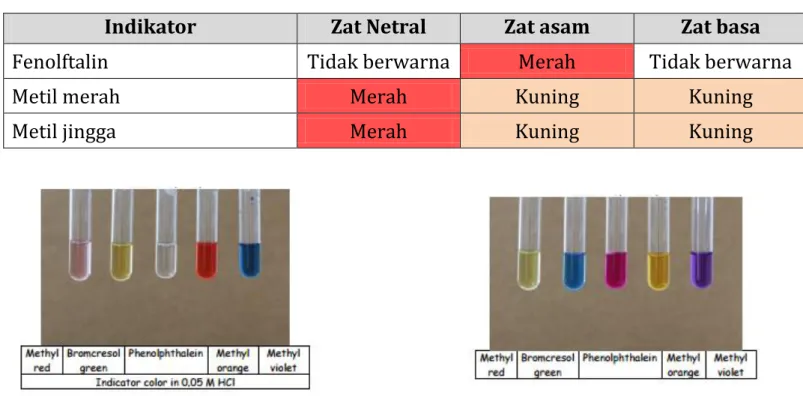
Indikator Zat Netral Zat asam Zat basa
Fenolftalin Tidak berwarna Merah Tidak berwarna
Metil merah Merah Kuning Kuning
Metil jingga Merah Kuning Kuning
Gambar perubahan warna pada uji coba asam klorida Gambar perubahan warna pada uji coba sodium hidroksida
Mengidentifikasi asam atau basa menggunakan indikator alami adalah suatu metode identifikasi menggunakan ekstrak tumbuhan, seperti: bunga sepatu, bunga pacar air, kunyit, kubis ungu, dll.
Adapun tabel perubahan warnanya adalah sebagai berikut:
Indikator Zat asam Zat basa
Bunga sepatu Kuning Merah
Bunga pacar air Kuning Merah
Kunyit Merah Kuning
Kubis ungu Kuning Merah tua