PLANAR KROMATOGRAFI
KARYA ILMIAH YANG TIDAK DI PUBLIKASIKAN
IYAN SOPYAN, M.Si, Apt
UNIVERSITAS PADJADJARAN
FAKULTS FARMASI
I. Pendahuluan
Kromatografi merupakan suatu metode umum yang sudah biasa digunakan dalam laboratorium baik untuk kepentingan analisis kualitatif ataupun kuantitatif walau ada beberapa asumsi bahwa untuk keperluan kuantitatif metode planar kromatografi kurang representatif namun dengan perkembangan penemuan dan pengembangan instumentasi, metode kromatografi planar juga cukup representatif untuk keperluan kuantitatif bahkan tidak hanya terbatas pada bahan atau material yang sederhana akan tetapi pada materi yang lebih komplek misalnya suatu cairan biologis dari serum manusia.
Pada dasarnya yang kromatografi planar adalah suatu instrumen yang terdiri dari dua komponen yang penting yang pertama adalah fase diam (stationary phase) dan fase gerak (mobile phase) modifikasi pada dua komponen inilah yang mendasari perkembangan instumen dari planar kromatografi sehingga menghasilkan pemisahan yang diharapkan lebih baik, selain pada sistem deteksinya dengan perkembangan pada instrumen detektornya yang sangat variatif, yang disesuaikan dengan keperluan analisis dan akurasi hasil.
Prinsip pemisahan pada kromatografi sendiri bisa terjadi secara adsorbsi atau partisi. Fase gerak pada planar kromatografi pada dasarnya merupakan suatu sistem pelarut atau cair walaupun kadang bisa menggunakan gas, dan umumnya analit adalah analit yang akan dianalisis dengan metode planar kromatografi merupakan molekul yang tidak mengaup dan stabil di udara terbuka, sementara fase diam (solid phase) bisa berupa suatu padatan atau suatu larutan yang ditempelkan pada suatu penunjang. Modifikasi dari fase solid ini sangat menentukan sekali terhadap efisiensi pemisahan dan merupakan modifikasi yang paling banyak dilakukan dalam perkembangan instrumen yang termasuk didalamnya HPTLC (high perfomance thin layer chromatograpy) sementara kromatografi elektroforesis merupakan modifikasi yang dilakukan karena sifat dari analit atau sampel yang akan di uji dan disini akan lebih melibatkan instumen lain karena berhubungan dengan muatan listrik(elektroda), ukuran molekul atau BM atau sistem polarisasi dari analit.
I. Pembagian Instrumentasi pada Planar Kromatografi
a. Kertas Kromatografi (Paper chromatography)
Kromatografi ini adalah suatu metode pemisahan yang didasarkan atas perbedaan mobolitas dalam suatu fase stasioner yang diberikan. Jika ada substansi campuran, kromatografi dalam memungkinkan pemisahan dari substansi tersebut. Sebagai contoh, tinta, yang biasanya disusun atas beberapa pewarna, denga kromatografi planar kita dapat memisahkannya dan kemudian menganalisis dan mengidentifikasi nya. Kromatografi juga digunakan untuk memperoleh kadar murni dari substanasi. Ada banyak metode dari kromatografi. Diantarnya kromatografi kertas,
kromatografi, liquid kromatografi, dan kromatografi kolom. Biasanya campuran dari senyawa dapat dipisahkan dimasukan ke dalam suatu pelarut. Jenis larutan pengembang dan fase diam dapat dipilih dalam kisaran yang lebar dari kemungkinannya. biasanya, pilihan ini membuat disesuaikan dengan molekul yang akan dipisahkan. Disesuaikan dengan keadaan, yang dapat memanfaatkan perbedaan ukuran molekul, afinitas kimia terhadap penunjang, derajat ionisasi pH, solubilitas dalam air, dan lain-lain. Percobaan ini untuk di rumah atau sekolah dimana kita dapat menggunakan pelarut dan penunjang yang mudah diperoleh. Test pipa sering digunakan untuk memuat uap pelarut, manjaga kertas dari kekeringan dan tidak yang tidak membahayakan penguji. (Chamberlain J, 1995)
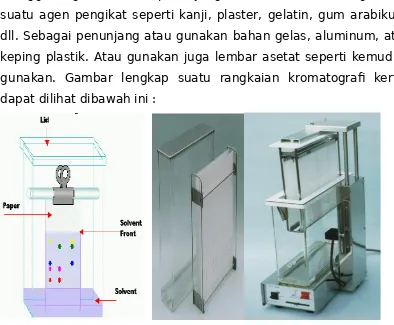
untuk TLC harus dibuat sendiri. Uintuk sekup ini gunakan serbuk alumina, kalsium karbonat, silika gel, magnesium silikat, dll. Untuk menggabungkan bahan penunjang dari suatu serbuk, gunakan suatu agen pengikat seperti kanji, plaster, gelatin, gum arabikum, dll. Sebagai penunjang atau gunakan bahan gelas, aluminum, atau keping plastik. Atau gunakan juga lembar asetat seperti kemudian gunakan. Gambar lengkap suatu rangkaian kromatografi kertas dapat dilihat dibawah ini :
Gambar. 1. kiri tradisional, kanan automatic sampler
b. Kromatografi Lapis Tipis (TLC)
Medium pemisahannya merupakan lapisan setebal 0.1-0.3 mm yang merupakan zat padat absorben yang dilekatkan pada penunjang seperti pelat seng atau kaca, plastik, alumunium, lempeng berukuran lazim berukuran 20X5 cm zat padat yang digunakan biasanya berupa alumina, silika gel atau selulosa. Dulu peneliti menyiapkan lempeng sendiri dengan menyalut kaca dengan suspensi air dari zat padat tersebut. yang biasanya mangandung zat pengikat seperti plester paris dan kemudian mengeringkannya dalam oven, dan kemudian setelah kering lempeng-lempeng alumunium, kaca atau plastik tersebut dapat dipotong-potong sesuai dengan ukuran yang diminati, dan ini biasa digunakan oleh peneliti-peneliti di laboratorium sekarang ini.
Gambar. 2
http://www.CAMAG.com
c. HPTLC
High perferpomance thin layer chromatography (HPTLC) adalah suatu metode kromatografi yang merupakan pegembangan dari TLC, hal yang dikembangkan adalah fase diam atau stationary phase dari dari instrumen, yang diharapkan menghasilkan daya pisah yang lebih baik dari TLC baik dilihat dari hasil, efisiensi waktu dan biaya.
HPTLC dari sisi peralatan tidak terlalu jauh berbeda dengan TLC hanya biasanya pada fase diam ukuran pori dari fase penyerap lebih kecil sehingga diharapkan terjadi pemisahan yang lebih baik karena terjadi interaksi antara analit dengan absorbent pada permukaan yang lebih luas, kemudian ukuran dari lempeng lebih kecil karena menggunakan suatu absorbent dengan pori yang lebih kecil hal ini akan berpengaruh terhadap waktu pengembangan yang memungkinkan lebih pendek atau singkat.
Dari profil hasil kromatogram yang diperoleh dari HPTLC lebih baik dari TLC karena pada HPTLC, HETP atau efisiensi dari teori keping lebih baik dari pada TLC hal ini disebabkan permukaan dari absorbent ukuran porinya lebih kecil dari absorben0 dari TLC sehingga permukaan interaksi analit dengan stationary fase lebih luas. HPTLC mempunyai beberapa kelebihan di banding dengan TLC dalam hal:
Tebal, keseragaman manghasilkan garis dasar stabil dalam densitometry
Jarak pengembangan dan waktu lebih singkat
Pita difusi rendah manghasilkan keterpaduan pita sampel
Mikrosample (nanograms dan picogram) dapat dianalisis
(Day. R.A, et,. al. 1997)
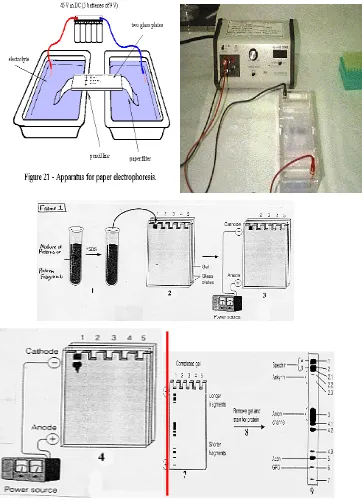
d. Kromatografi Elektroforesis Kertas
berdasarkan muatan listriknya atau polaritasnya dan ukuran dari BMnya. Gambaran sederhana dari kromatografi elektroforesis dapat dilihat pada gambar di bawah ini :
II. Instrumentasi Utama pada Kromatografi Planar
a. Fase Diam/Stationary Phase/Sorbent 1. Kromatografi Kertas
Pada kromatografi kertas dapat digunakan sebagian fase diam adalah kertas, kertas yang digunakan mulai dari kertas selulosa biasa atau kertas dengan spesifikasi Whatman dengan berbagai ukuran atau nomor; berikut dapat dilihat gambar kertas yang digunakan sebagai fase diam :
Gambar. 4 Paper for Chromatography
2. Fase Diam/Sorbent TLC dan HPTLC
agent dan sebab itu dapat diaplikasikan secara universal. Pemisahan optimum (migration) jarak pada lempeng TLC adalah 12–15 cm. Jika hanya sedikit sampel yang akan dipisahkan pada waktu lempengnya sama, format yang lebih kecil seperti 10 cm × 20 cm atau 5 cm × 20 cm (20 cm dalam pengembangan secara langsung), yang juga memungkinkan perpindahan jarak optimum, terjadi. Jika efisiensi pemisahan optimum sesungguhnya kurang penting (sebagai contoh, jika sample mangandung hanya satu atau sangat banyak komponen), Jarak pengembangan dapat dikurangi sampai kira-kira 8 cm dan lempeng format 20 cm × 10 cm (atau lempeng fraksional sekecil 2.5 cm × 10 cm) mungkin kurang.
Gambar. 5 Silika gel untuk TLC
Gambar. 6 lempeng silika gel untuk HPTLC (lebih kecil dari TLC) (WWW.LUMEX.RU)
Spesifikasi dari masing-masing sorbent :
Silika gel - untuk pemisahan polarisasi lamah sampai kuat
High purity silika gel -asam washed untuk pemisahan dari aflatoxins
Sellulosa - untuk kromatografi partisi
Sellulosa PEI - untuk pemisahan dari anion lemah (amino acids, peptides)
Aluminum oxida – alumina dasar, untuk pemisahan hormone and antibiotika
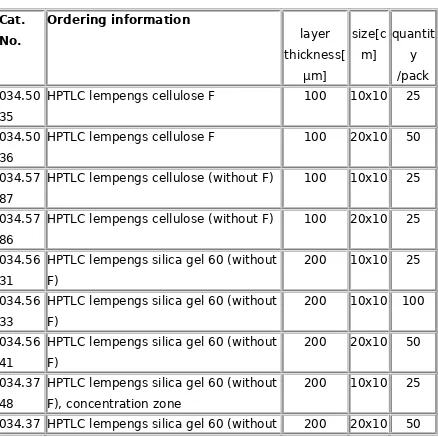
Dibawah ini daftar beberapa spesifikasi sorbent yang dapat digunakan sebagai fase stationary yang sekarang biasa digunakan :
Tabel. 3
HPTLC lempengs cellulose F 100 10x10 25
034.50 36
HPTLC lempengs cellulose F 100 20x10 50
034.57 87
HPTLC lempengs cellulose (without F) 100 10x10 25
034.57 86
HPTLC lempengs cellulose (without F) 100 20x10 25
034.56 31
HPTLC lempengs silica gel 60 (without F)
200 10x10 25
034.56 33
HPTLC lempengs silica gel 60 (without F)
200 10x10 100
034.56 41
HPTLC lempengs silica gel 60 (without F)
200 20x10 50
034.37 48
HPTLC lempengs silica gel 60 (without F), concentration zone
200 10x10 25
49 F), concentration zone 034.56
28
HPTLC lempengs silica gel 60 F 254 200 10x10 25
034.56 29
HPTLC lempengs silica gel 60 F 254 200 10x10 100
034.55 64
HPTLC lempengs silica gel 60 F 254 GLP
200 10x10 25
034.56 42
HPTLC lempengs silica gel 60 F 254 200 20x10 50
034.17 64
HPTLC lempengs silica gel 60 F 254, extra thin layer
100 20x10 25
034.37 27
HPTLC lempengs silica gel 60 F 254, concentration zone
200 10x10 25
034.37 28
HPTLC lempengs silica gel 60 F 254, concentration zone
200 20x10 50
034.56 13
HPTLC lempengs silica gel 60 F 254 GLP
200 20x10 25
034.15 52
HPTLC lempengs silica gel WR 60 F 254s
200 20x10 25
034.54 45
HPTLC lempengs LiChrospher® Si 60 F 254s
180 20x10 25
034.55 47
HPTLC aluminium sheets silica gel 60 (without F)
200 20x20 25
034.55 48
HPTLC aluminium sheets silica gel 60 F 254
200 20x20 25
034.55 43
HPTLC aluminium sheets silica gel 60 F 254s, RAMAN
034.37 25
HPTLC lempengs RP-8 F 254s 200 10x10 25
034.42 96
HPTLC lempengs RP-18 W (without F) 200 20x10 25
034.31 24
HPTLC lempengs RP-18 W F 254s
200 10x10 25
HPTLC lempengs CN F 254s 200 10x10 25
034.25 71
HPTLC lempengs CN F 254s 200 20x10 25
034.25 72
HPTLC lempengs NH2 (without F) 200 20x10 25
034.31 92
HPTLC lempengs NH2 F 254s 200 20x10 25
034.56 47
HPTLC lempengs NH2 F 254s 200 10x10 25
034.26 68
HPTLC lempengs Diol F 254 200 10x10 25
034.56 36
HPTLC lempengs MERCK Diol F 254 200 20x10 25
034.56 07
UTLC silica gel 60 w/o F 254 10 6x3.6 25
(WWW.LUMEX.RU.com)
SILICA GEL 60 G F SILICA GEL 60 G F254254
• Adalah Silica Gel dengan : • Ukuran pori : 60 Å
• G = CaSO4.½ H2O sebagai binder/gypsum
• F = bahan fluorescen / fosforescen yg ditambahkan • 254 = dituliskan sesudah F atau UV utk
menandakan panjang gelombang eksitasi bahan fluorescent atau fosforescen yang
ditambahkan (Snyder, et al, 1997) b. Chamber / Ruang Pengembang
Pada dasarnya chamber atau tempat untuk pengembangan dari kromatografi planar tidak terlalu spesifik untuk masing-masing jenis kromatografi, yang membedakan chamber yang digunakan adalah ukuran dari chamber, dimana ukuran dapat disesuaikan dengan kebutuhan:
Gambar. 7 Glass Chamber
atau bahkan dalam suatu plastik seperti gambar dibawah ini :
Untuk kromatografi elektroforesis dalam chamber di bagi dua bagian yang kedalam masing-masing chamber dimasukan satu ujung dari kertas dan pada masing-masing chamber dihubungkankan dengan suatu muatan listrik yang berbeda yaitu muatan positif dan negatif, sehingga akan terjadi pemisahan, pada kedua chamber tersebut dimasukan suatu suatu larutan elektrolit agar bisa menghantarkan muatan pada kertas sebagai fase diam dan larutan elektrolit disini sekaligus bertindak sebagai fase gerak dari proses kromatografi. (Suherman, M. Mulja. 1995)
IV. Instrumen Pendukung / Tambahan a. Sprayer
Gambar. 8 Sprayer
Berikut beberapa derivating agent yang bisa di gunakan :
a. Scaner
Scaner merupakan suatu alat yang dimaksudkan untuk memperjelas suatu spot pada saat mengamati, bisanya pada alat ini disertai dengan lampu baik itu lampu UV atau yang lainya yang dapat memendarkan cahaya dari spot-spot analit setelah disemprot dengan larutan penampak noda (derivating agent), berikut beberapa gambar alat scaner :
Gambar.9 UV Scaner 254 nm dan 366 nm
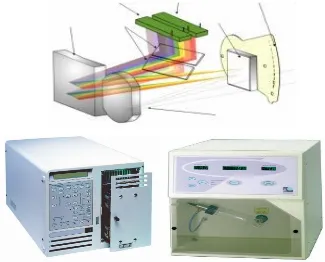
b. Detektor
Detektor yang bisa di gunakan pada analisis kromatografi planar adalah adalah detektor photon, diamana sifat dari analit dapat dibuat atau di derivatisasi dengan senyawa yang membuat senyawa tersebut berflourisensi dan dapat di deteksi atau di scanning dengan detektor yang sesuai.
Detektor yang umum digunakan dalah detektor UV atau flourisensi detektor berikut gambar dari beberapa detektor yang terkait erat dengan kromatografi planar: beberpa UV detektor yang bisa digunakan dalam deteksi spot hasil kromatogram dari planar kromatografi.
2. Germanium Photodiodes 3. InGaAs Photodiodes
4. Extended InGaAs Photodiodes
Prinsip kerjanya secara umum adalah lempeng yang terdapat spot didalamnya dikenai sinar dan nanti akan berflourisensi kemudian flourisensinya akan ditangkap oleh detektor kemudian intensitasnya akan terukur dan akan sebanding dengan kadarnya.
Gambar. 10 UV- detektor 254 nm dan 366 nm
C. Alat Penderivatisasi
Gambar. 11 Derivating tool
D. Spray Cabinet
Alat ini untuk sebagai ruang untuk menyemprot spot dengan zat penampak noda/zat penderivatisasi
Gambar. 12 Spray Kabinet
E. Lempeng heater
Alat ini untuk memanaskan lempeng sebelum dipakai atau untuk mengaktifkan dengan cara menguapkan uap air yang dikandungnya selain dengan menggunakan oven biasa:
Gambar. 13 Plate
F. Lempeng Coater
Gambar. 14 Coater Plate
G. Pipet sampel/drods/Penetes Sampel
Adalah suatu kapiler dengan ukuran tertentu yang berguna untuk meneteskan sampel pada lempeng atau fase diam, berikut dapat dilihat alah satunya ;
Gambar. 15 Droper/Penetes Sampel
IV. Aplikasi.
Penggunaan dari kromatografi planar secara umum dapat kelompokan untuk dua keperluan yang pertama adalah untuk keperluan kualitatif dan kuantitatif. Keperluan secara kualitatif biasanya menggunakan parameter dari Rf (Range Factor) dimana nilai ini dihasilkan dari perbandingan antara jarak tempuh relatif dari spot-spot tertentu terhadap jarak tempuh dari larutan pengembang atau larutan pengembang. Yang merupakan angka
relatif dan dibandingkan dengan Rf standard pada kondisi yang sama (instrument, pengembang dan deteksi) jika sama maka dapat ditentukan dengan zat tertentu atau di scanning sehingga menghasilkan suatu kromatogram yang dapat di bandingkan dengan standard. Jika spot yang dihasilkan masing bertumpuk atau masih lebih dari satu spot atau berekor ini menandakan masih belum murni, jika ini terjadi maka dapat dilakukan pengembangan dua arah dengan arah tegak lurus (900) sehingga yang spot yang menumpuk terpisahkan dengan baik. Hal ini apat dilihat pada gambar dibawah ini :
Gambar. 16
Gambar. 17
Gambar 18 . Kromatogram dari planar Kromatografi (Snyder, et al, 1997)
VI. Kesimpulan
Kromatografi planar merupakan kronmatografi yang sangat praktis dan mudah untuk dipraktekan, kromatografi ini meliputi : kromatografi kertas, kromatografi lapis tipis (KLT), atau high performance thin layer kromatografi (HPTLC) dan kromatografi elektroforesis, masing-masing kromatografi ini mempunyai kelebihan dan kekurangan yang dapat berupa efisiensi (biaya dan waktu), dan hasil dari kromatogram,
Kromatografi ini juga dibedakan juga berdasarkan fungsi pemisahan terhadap subastansinya, apakah itu sederhana atau lebih komplek misalkan elektroforesis lebih difokuskan atau digunakan untuk suatu substansi yang mempunyai polaritas atau muatan misalnya asam amino dalam serum dan lain-lain.
Untuk keperluan analisis baik kuantitatif atau kualitatatif metode ini dapat digunakan seiring dengan perkembangan instrumentasi sampai dengan sekarang ini. Secara umum alat kromatografi planar dapat dikelompokan menjadi bebrrapoa bagian yang penting antara lain:
1. fase diam (stationary phase) 2. ruang pengembang (chamber)
3. penyemprot penampak Noda (sprayer) 4. drops penetes sampel (micro pipet) 5. scaner (panampak spot)
yang masing-masing dapat dikembangkan sehingga kromatografi planar juga dapat representatif untuk keperluan analisis kuantitatif, selain metode-metode pemisahan lain.
Pustaka
1. Chamberlain J, 1995, The Analysis Drugs in Biological Fluids, Second Edition, CRC press, NewYork, P 105-117.. 2. Day. R.A, and Underwood, A.L. 1996. Analisis Kimia
Kuantitatif, Edisi kelima, Erlangga press, Jakarta. P 551-554
Pennsylvania 18042, Analytical Chemistry, Vol. 76, No. 12, June 15,
4. Snyder, R.L., Kirkland, J.J., and Glajch, J.L., 1997, Practical HPLC method development, 2nd edition, p.686-697, John Wiley & Son, Inc., New York
5. Suherman, M. Mulja. 1995. Analisis Instrument. Airlangga University Press, Surabaya, P 223-234.