BAB 2
TINJAUAN PUSTAKA
2.1. Tumbuhan Temulawak
Temulawak merupakan tanaman obat berupa tumbuhan rumpun berbatang semu. Di daerah Jawa Barat temulawak disebut sebagai koneng gede sedangkan di Madura disebut sebagai temu lobak. Kawasan Indo-Malaysia merupakan tempat dari mana temulawak ini menyebar ke seluruh dunia. Saat ini tanaman ini selain di Asia Tenggara dapat ditemui pula di Cina, IndoCina, Bardabos, India, Jepang, Korea, di Amerika Serikat dan beberapa Negara Eropa.
Klasifikasi ilmiah tanaman temulawak adalah sebagai berikut: Divisi : Spermatophyta
Sub divisi : Angiospermae Kelas : Monocotyledonae Ordo : Zingiberales Keluarga : Zingiberaceae Genus : Curcuma
Spesies : Curcuma xanthorrhiza ROXB.(Rahmat,1995)
2.1.1. Deskripsi Temulawak
Tanaman temulawak berbatang semu dengan tinggi hingga lebih dari 1m tetapi kurang dari 2m, berwarna hijau atau coklat gelap. Akar rimpang terbentuk dengan sempurna dan bercabang kuat, berwarna hijau gelap. Tiap batang mempunyai daun 2 – 9 helai dengan bentuk bundar memanjang sampai bangun lanset, warna daun hijau atau coklat keunguan terang sampai gelap, panjang daun 31 – 84 cm dan lebar 10 – 18 cm, panjang tangkai daun termasuk helaian 43 – 80 cm. Perbungaan lateral, tangkai ramping dan sisik berbentuk garis, panjang tangkai 9 – 23 cm dan lebar 4 – 6 cm, berdaun pelindung banyak yang panjangnya melebihi atau sebanding dengan
mahkota bunga. Kelopak bunga berwarna putih berbulu, panjang 8 – 13 mm, mahkota bunga berbentuk tabung dengan panjang keseluruhan 4.5 cm, helaian bunga berbentuk bundar memanjang berwarna putih dengan ujung yang berwarna merah dadu atau merah, panjang 1.25 – 2 cm dan lebar 1cm.
Gambar 2.1. Tanaman Temulawak (Rahmat, 1995) 2.1.2. Manfaat Tanaman
Di Indonesia satu – satunya bagian yang dimanfaatkan adalah rimpang temulawak untuk dibuat jamu godog. Rimpang ini mengandung 48-59, 64 % zat tepung, 1,6-2,2 % kurkumin dan 1,48-1,63 % minyak asiri dan dipercaya dapat meningkatkan kerja ginjal serta anti inflamasi. Manfaat lain dari rimpang tanaman ini adalah sebagai obat jerawat, meningkatkan nafsu makan, anti kolesterol, anti inflamasi, anemia, anti oksidan, pencegah kanker, dan anti mikroba (Rahmat, 1995).
2.1.3. Kandungan Kimia Temulawak
Komponen – komponen yang terkandung dalam temulawak dapat digolongkan menjadi 2 golongan, yaitu minyak atsiri dan golongan kurkuminoid. Minyak atsiri atau minyak menguap merupakan komponen dalam temulawak yang memberikan bau karateristik, sedangkan kurkuminuid terdiri dari beberapa zat warna kuning (Oei dkk, 1985).
xantorizol. Selanjutnya dibuktikan bahwa ketiga senyawa tersebut yaitu : α -kurkumen, ar-turmeron dan xantorizol, mempunyai khasiat anti-tumor.
Ueraha (1989, 1990) berhasil mengidentifikasi tujuh senyawa seskuiterpenoid bisabolon dari fraksi larutan klorofom rimpang temulawak, setelah dideterminasi berdasarkan data spektral, konversi kimia, dan kristalografi sinar-X. Ketujuh senyawa tersebut adalah bisacuron, bisacumol, bisacurol, bisacuron epoksida, bisacuron A, bisacuron B, dan bisacuron.
Kandungan kimia minyak atsiri temulawak
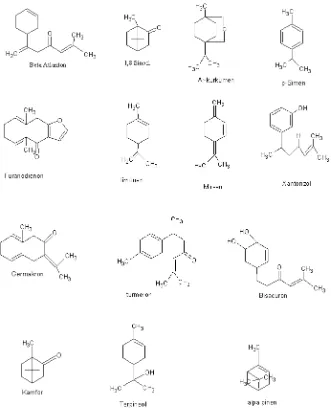
Alto-Aromadendre, β–Atlanton, α–Bergamoten, β-Bisabolol, Bisacumol, Bisacuron, Bisacuron A, Bisacuron B, Bisacuron C, Bisacuron epoksida, Borneol, Isoborneol, Kamfen, Kamfor, 1,8 Sineol, Ar-kurkumen, α- kurkumen, β- kurkumen, Kurkufenol , Kurzeren, Kurzerenon, P- Sinem, 2-(1,5-Dimetilheks-4-enil) 4 metilfenol, β– Elemen, δ – Elemen, γ – Elemen, β- Famesen, Furanodienon, Germakonm, Isofuranogermakren, Limonen, Linalol, Mirsen, α- Pinen, β- Pinen, Sabinen, β-Seskuifelandren, α- Terpineol, Trisiklen, Turmerol, Ar-turmeron, α-Turmeron, β
Gambar 2.2. Berbagai rumus kimia minyak atsiri temulawak (Purnomowati,Yoganingrum,1997)
2.2. Senyawa Terpen
terpen merupakan kerangka penyusun sejumlah senyawa penting bagi makhluk hidup. Sebagai contoh, senyawa-senyawa
terpene) diambil dari produk getah
tusamturpentine).
Terpen dan terpenoid menyusun banyak tumbuhan. Kandungan minyak atsiri memengaruhi penggunaan produk rempah-rempah, baik sebagai bumbu, sebagai wewangian, serta sebagai bahan pengobatan, kesehatan, dan penyerta upacara-upacara ritual. Nama-nama umum senyawa golongan ini seringkali diambil dari nama minyak atsiri yang mengandungnya. Lebih jauh lagi, nama minyak itu sendiri diambil dari nama (nama latin) tumbuhan yang menjadi sumbernya ketika pertama kali diidentifikasi. Sebagai misal adal diambil dari minyak yang diambil dariCitrus). Contoh lain adala diambil dari minyak yang dihasilkan olEugenia aromatica).
Terpenoid disebut juga isoprenoid. Hal ini dapat dimengerti karena kerangka penyusun terpena dan terpenoid adala5H8).
Terpen memiliki rumus dasar (C5H8)n, dengan n merupakan penentu kelompok tipe terpen. Modifikasi terpen (disebut terpenoid, berarti "serupa dengan terpena") adalah senyawa dengan struktur serupa tetapi tidak dapat dinyatakan dengan rumus dasar. Kedua golongan ini menyusun banyak minyak atsiri.
Tabel 2.1. Klasifikasi Terpen
Nama Rumus Sumber
Monoterpen C10H16 Minyak Atsiri
Seskuiterpen C15H24 Minyak Atsiri
Diterpen C20H32 Resin Pinus
Triterpen C30H48 Saponin, Damar
Tetraterpen C40H64 Pigmen, Karoten
Politerpen (C5H8)n n 8 Karet Alam
2.3. Minyak Atsiri
Dalam tumbuhan, kebanyakan senyawa-senyawa yang beraroma dihasilkan melalui jalur metabolisme sekunder. Terpen merupakan persenyawaan hidrokarbon tidak jenuh yang molekulnya tersusun dari unit isoprene (C5H8). Unit Isopren berkondensasi dengan persambungan kepala ke ekor isopentenil pirofosfat dan dimetil pirofosfat menghasilkan terpen dalam tumbuhan.
Isoprene (C5) Satuan isopenten
pewangi. Monoterpen dan seskuiterpen dapat dipilah-pilah berdasarkan kepada kerangka karbon dasarnya. Yang umum adalah asiklik (misalnya graniol dan fanesol), monosiklik (misalnya limonene dan bisabolena), bisiklik (misalnya α dan β-pinena). Dalam setiap golongan monoterpen dan seskuiterpen bisa terdapat senyawa hidrokarbon tak jenuh atau keton.
Minyak atsiri dapat diperoleh melalui ekstraksi tumbuh – tumbuhan yakni dari daun, bunga, akar, dan kulit kayu. Biasanya tumbuhan penghasil minyak atsiri tumbuh liar atau dibudidayakan dan biasanya tumbuhan itu berarti wangi.
Minyak atsiri merupakan minyak yang mudah menguap pada suhu kamar tanpa mengalami dekomposisi, mempunyai rasa getir (pungent taste), beraroma wangi sesuai dengan aroma tumbuhan penghasilnya. Umumnya larut dalam pelarut organic dan tidak larut dalam air.Minyak atsiri itu berupa ciran jernih,tidak berwarna, tetapi selama penyimpanan akan mengental dan berwarna kekuningan atau kecoklatan. Hal tersebut terjadi karena adanya pengaruh oksidasi dan resinifikasi (berubah menjadi dammar atau resin). Untuk mencegah atau memperlambat proses oksidasi dan resinifikasi tersebut, minyak atsiri harus dilindungi dari pengaruh sinar matahari yang dapat merangsang terjadinya oksidasi dan oksigen udara yang akan mengoksidasi minyak atsiri, (Koensoemardiyah,2010).
2.3.1. Sumber Minyak Atsiri
Tabel 2.2. Sumber-sumber Minyak Atsiri Nama Minyak Tanaman Penghasil Bagian
Tanaman
Negara Asal
Sereh wangi Cymbopogon nardus R Daun Srilanka
Nilam (patchouli) Pogostemon cablin Benth
Cymbopogon citrates Daun Madagaskar, Guetemala
Lada (pepper) Piper nigrum L Daun/buah India Timur,
Cina,
Cengkeh (clove) Caryophyllus Bunga Zanzibar,
Indonesia, Madagaskar
Lavender Lavandula offcinalis
Chaix
Bunga Perancis,
Rusia
Mawar (rose) Rosa alba L Bunga Bulgaria,
Turki
Melati (jasmine) Jasminumofficinale Bunga Perancis
selatan Kapolaga
(cardamom)
Elettaria cardamomun Biji India, amerika Seledri (celery seed) Apium graveolen L Biji Inggris, India
Sitrun (lemon) Citrus medica Buah/Kulit
Buah
Kalifornia
Adas (fennel) foeniculum fulgares Mill
Kunyit (Turmeric) Curcuma longa Akar/rhizoma Amerika
selatan Jahe (ginger) Zingiber officinale
Roscoe
Akar/rhizoma Jamaika
“Camphor” Cinnamomun
Camphora L
Batang/kulit buah
2.3.2. Penggunaan Minyak Atsiri
Penggunaan minyak atsiri dan bahan kimia volatil untuk tujuan pengobatan, kosmetik serta wangi – wangian telah dikenal dalam masyarakat sejak zaman purba. Dan kini ada kecenderungan untuk kembali ke penggunaan bahan – bahan alam, antara lain karena minyak atsiri dapat larut dalam lemak yang terdapat pada kulit, dapat diabsorbsi kedalam aliran darah, dan mempunyai kompabilitas dengan lingkungan (dapat mengalami biodegradasi dan merupakan bagian dari kesetimbangan ekosistem selama ribuan tahun) (Rojat, dkk, 1996).
Minyak atsiri merupakan sumber dari aroma kimia alami yang dapat digunakan sebagai komponen flavor dan fragrance alami dan sebagai sumber yang penting dari struktur stereospsesifik enansiomer murni yang biosintesisnya lebih murah dibandingkan dengan proses sintesis (Lawrence dan Reynold, 1992).
Minyak atsiri digunakan sebagai bahan baku dalam berbagai industri, misalnya industri parfum, kosmetik, “essence”, industri farmasi dan “flavoring agent”. Dalam pembuatan parfum dan wangi-wangian, minyak atsiri tersebut berfungsi sebagai zat pengikat bau (fixative) dalam parfum, misalnya minyal nilam, minyak akar wangi dan minyak cendana. Minyak atsiri yang berasal dari rempah-rempah, misalnya minyak lada, minyak kayu manis, minyak jahe, minyak cengkeh, minyak ketumbar, umumnya digunakan sebagai bahan penyedap (flavoring agent) dalam bahan pangan dan minuman (Ketaren, 1985).
Minyak atsiri ini selain memberikan aroma wangi yang menyenangkan juga dapat membantu pencernaan dengan merangsang system saraf skresi, sehingga akan meningkatkan skresi getah lambung yang mengandung enzim hanya oleh stimulus aroma dan rasa bahan pangan. Selain itu juga dapat merangsang keluar cairan getah sehingga rongga mulut dan lambung menjadi basah.
2.3.3. Cara Memproduksi Minyak Atsiri
Komponen minyak atsiri dalam tumbuhan terdapat dalam jumlah yang sangat kecil, sehingga diperlukan bahan awal yang besar jumlahnya untuk memperoleh minyak atsiri yang memadai jumlahnya untuk diteliti. Ada beberapa metode untuk mendapatkan minyak atsiri antara lain:
a. Metode Penyulingan (Destilasi)
Bahan yang mengandung minyak atsiri dapat diperoleh dengan metode penyulingan (Bradesi, dkk, 1997). Bahan untuk penyulingan biasanya diambil pada pagi hari secepat mungkin setelah embun menghilang (Douglas, 1979). Ada tiga metode penyulingan yang digunakan dalam industry minyak atsiri, yaitu:
1. Penyulingan dengan air (hydrodistillation)
2. Penyulingan dengan air dan uap (hydro and steam distillation) 3. Penyulingan dengan uap langsung (steam distillation)
Perbedaan antara distilasi uap langsung dengan hidrodistilasi adalah pada distilasi uap langsung tidak terjadi kontak langsung antara sampel dengan air, sedangkan hidrodistilasi sampelnya dicelupkan ke dalam air mendidih (Chalchat dan Garry, 1997).
Dalam setiap metode penyulingan bahan tumbuhan, baik dengan penyulingan uap, penyulingan air dan uap atau penyulingan air minyak atsiri hanya dapat diuapkan jika kontak langsung dengan uap panas. Minyak dalam jaringan tumbuhan mula-mula terekstraksi dari kelenjar tanaman dan selanjutnya terserap pada permukaan bahan melalui peristiwa osmosis (Guenther, 1987). Lamanya penyulingan yang dilakukan pada setiap tumbuhan tidak sama satu dengan yang lain tergantung pada mudah atau tidaknya minyak atsiri tersebut menguap, dua sampai delapan jam tersebut secara maksimal.
berpenetrasi kedalam bahan, uap hanya akan menguapkan minyak atsiri yang terdapat dipermukaan gumpalan. Tetapi metode penyulingan ini juga mempunyai kelemahan, yaitu adanya penggunaan suhu yang tinggi (Pino, dkk, 1997) yang dapat mengakibatkan dekomposisi minyak (hidrolisis ester, polimerisasi dll).
b. Maserasi dengan Lemak/Minyak
Kebanyakan bahan flavor bersifat larut dalam lemak atau minyak, tetapi mempunyai range polaritas yang lebar. Minyak dapat bertindak sebagai pelarut dan merupakan medium yang dapat melindungi bahan yang mudah menguap. Lemak/minyak mempunyai daya absorbsi yang tinggi dan jika dicampur dan kontak dengan bunga yang beraroma wangi, maka lemak akan mengabsorbsi minyak yang dikeluarkan oleh bunga tersebut. Pada akhir proses, minyak dari bunga tersebut diekstraksi dari lemak dengan menggunakan alkohol dan selanjutnya alkohol dipisahkan (Guenter, 1987).
c. Ekstraksi dengan Pelarut Menguap
Metode lain yang dapat digunakan untuk mengisolasi minyak atsiri adalah dengan menggunakan metode ekstraksi pelarut menguap. Contoh pelarut yang digunakan adalah dietil eter untuk mengekstraksi daun Citrus aurantium. Dan pelarut ini juga digunakan dalam mengekstraksi minyak Rhizome dari Curcuma ochrorhiza Val dan lain-lain.
Jika dibandingkan dengan mutu minyak bunga hasil penyulingan, maka minyak hasil ekstraksi dengan menggunakan pelarut lebih mendekati aroma bunga alamiah, namun demikian metode ini juga mempunyai kelemahan yaitu kesulitan penghilang residu pelarut dari ekstrak (Pino, dkk, 1997).
d. Ekstraksi dengan Karbon Dioksida Superkritis
CO2 dimasukkan kedalam ekstraktor berupa labu yang diberi tekanan dan temperatur yang telah diatur, kemudian CO2 dipompa kedalam separator pada tekanan dan temperatur yang rendah, yang kemudian masuk kedalam tangki ekstraksi. Kelebihan CO2 dimurnikan kembali didalam bejana terisi arang (Charcoal trap).
Keuntungan dari metode ini antara lain adalah tidak menggunakan pelarut yang beracun, biaya murah, mampu mengisolasi senyawa termolabil tanpa diikuti denaturasi karena dilakukan pada temperatur rendah, juga kemungkinan untuk memperoleh produk baru dengan komposisi yang biasanya diperoleh dengan teknik destilasi ( Pino, 1997 ). Namun demikian metode ini juga mempunyai kekurangan yaitu dalam hal penentuan kondisi untuk ekstraksi minyak atsiri dari tumbuhan tertentu (Boelens dan Boelens, 1997).
2.3.4. Penyimpanan Minyak Atsiri
Pada proses penyimpanan minyak atsiri dapat mengalami kerusakan yang diakibatkan oleh berbagai proses, baik secara kimia maupun secara fisika. Biasanya kerusakan disebabkan oleh reaksi-reaksi yang umum seperti oksidasi, resinifikasi, polimerisasi, hidrolisis ester dan interaksi gugus fungsional. Proses tersebut dipercepat (diaktivasi) oleh panas, adanya udara (oksigen), kelembaban, serta dikatalis oleh cahaya dan pada beberapa kasus kemungkinan dikatalis oleh logam (Guenther, 1987).
Minyak atsiri yang mengandung kadar terpen tinggi mudah mengalami kerusakan oleh proses oksidasi terutama oleh proses esterifikasi. Terpen dan turunannya biasanya mengandung atom karbon tidak jenuh, karena itu dengan adanya oksigen bisa menyebabkan pemecahan atau penataulangan dari terpen.
dari cahaya. Penyimpanan minyak dalam jumlah yang kecil sangat baik dilakukan memakai botol atau gelas berwarna gelap, sedangkan dalam jumlah yang besar dapat disimpan dalam drum yang dilapisi dengan timah atau bahan yang tidak bereaksi dengan minyak atsiri. Penyemprotan gas karbon dioksida atau nitrogen kedalam drum sebelum ditutup akan menghilangkan gas oksigen dari permukaan minyak, sehingga minyak terlindungi dari kerusakan akibat oksidasi (Guenther, 1987).
2.4. Kromatografi Gas – Spektrometri Massa (GC-MS)
Spektrometer massa memiliki 3 fungsi yang sangat penting, pertama molekul molekul ditembaki oleh elektron – electron berenergi tinggi membentuk ion – ion. Ion – ion di aselerasi dalam suatu medan elektrik. Kedua, ion – ion yang di aselerasi dipisahkan berdasarkan perbandingan massa mereka terhadap muatan di dalam medan magnet atau medan elektrik. Selanjutnya ion – ion tertentu dengan perbandingan massa terhadap muatan di deteksi oleh suatu peralatan yang mampu menghitung jumlah ion ion yang terpisah. Hasilnya di deteksi oleh detektor dan di rekam dalam rekorder. Hasil dari rekorder adalah suatu spektrum massa yakni grafik dari sejumlah partikel partikel yang di deteksi sebagai suatu fungsi perbandingan massa terhadap muatan (Donald,et al,1979).
2.4.1. Kromatografi Gas
Kromatografi gas adalah metode kromatografi pertama yang dikembangkan pada zaman instrumen dan elektrokimia yang telah merevolusikan keilmuan selama lebih dari tiga puluh tahun.
suatu campuran, semakin banyak komponen yang terdapat dalam suatu campuran maka waktu yang diperlukan semakin lama. Komponen campuran dapat diidentifikasi berdasarkan waktu tambat (waktu retensi) yang khas pada kondisi yang tepat. Waktu tambat adalah waktu yang menunjukkan berapa lama suatu senyawa tertahan dalam kolom (Gritter J, et al, 1985).
a. Memilih Sistem
Dalam kromatografi gas terdapat empat peubah utama yaitu gas pembawa, jenis kolom dan fase diam dan suhu untuk pemisahan.
Gas Pembawa
Faktor yang mempengaruhi suatu senyawa bergerak melalui kolom kromatografi gas ialah keatsirian yang merupakan sifat senyawa itu dan aliran gas melalui kolom. Nitrogen, helium, argon, hydrogen dan karbon dioksida merupakan gas yang sering digunakan sebagai gas pembawa karena tidak reaktif serta dapat dibeli dalam keadaan murni dan kering dalam tangki bervolume besar dan bertekanan tinggi.
Detektor
Detektor pilihan pertama untuk kromatografi gas adalah Detektor Ionisasi Nyala (DIN) yang memiliki kepekaan yang tinggi untuk beberapa jenis senyawa. Fase Cair Diam
Dua segi fase harus diketahui, pertama, bagaimana cairan ditahan dalam kolom yaitu cairan itu disaputkan pada permukaan serbuk padat dalam kolom, dan yang kedua yaitu sifat kimia dari cairan itu.
b. Sistem Suhu Kolom
dalam kromatografi gas. Suhu kolom berkisar -100o C – 400oC tergantung sifat bahan. Secara umum, pemisahan yang baik diperoleh pada suhu rendah. Sebagai patokan dapat dipakai bahwa setiap kenaikan suhu 30oC waktu tambat menjadi setengahnya.
Gas Pembawa
Laju aliran gas tergantung pada diameter kolom. Aliran berbanding lurus dengan penampang kolom dan penampang bergantung pada jari-jari pangkat dua (πr2
). Misalnya jika pemisahan yang baik dengan kolom 2 mm pada aliran 20 ml/menit, maka untuk menghasilkan hasil yang sama dengan kolom 4 mm diperlukan aliran 80 ml/menit. Untuk mendapatkan sistem kolom yang optimal yaitu dengan cara mengatur laju aliran gas dan menghasilkan tingkat puncak yang maksimum.
Kolom
Ada dua kolom dalam kromatografi gas yaitu: kolom kemas, terdiri atas fase cair berdiameter 1-3 mm dan panjangnya 2 m, kolom kapiler; berdiameter 0,02 - 0,2 mm dan panjangnya 15-25 m, yang berfungsi sebagai penyangga lembam untuk fase diam cair.
Detektor
Detektor adalah gawai yang ditempatkan pada ujung kolom kromatografi gas yang menganalisis aliran gas yang keluar dan memberikan data kepada perekam data yang menyajikan hasil kromatogram secara grafis. DHB (Detektor hantar bahang); didasarkan pada bahang dipindahkan dari benda panas dengan laju yang bergantung pada susunan gas yang mengelilingi benda panas. Daya hantar ini merupakan fungsi dari laju pergerakan molekul gas. Gas yang mempunyai bobot molekul yang rendah mempunyai daya hantar paling tinggi.
Penanganan Sinyal
Data Kualitatif; data kromatografi gas biasanya terdiri atas waktu tambat berbagai komponen campuran. Waktu tambat diukur mulai dari titik penyuntikan sampai ketitik maksimum puncak dan sangat khas untuk senyawa tertentu dan pada kondisi tertentu. Komponen tertentu didalam campuran dapat dipisahkan dengan cara spiking jika tersedia senyawa murninya. Senyawa murni ditambahkan kedalam cuplikan yang diduga mengandung senyawa itu dan cuplikan dikromatografi.
Data Kuantitatif; Pengukuran sebenarnya yang dilakukan pada kertas grafik ialah pengukuran luas puncak. Jika puncak itu simetris atau berupa kurva Gauss tinggi puncak dapat dipakai untuk mengukur luas puncak.
2.4.2. Spektrum Massa
Spektrum massa biasa diambil pada suatu berkas sinar sebesar 70 elektron volt. Kejadian tersederhana ialah tercampaknya satu atom dari satu molekul dalam fasa gas oleh sebuah elektron dalam berkas atom dan membentuk suatu ion molekul yang merupakan suatu kation radikal (M+).
Suatu massa elektron menyatakan massa – massa bermuatan positif terhadap (konsentrasi) nisbinya. Puncak paling kuat (tinggi) pada atom disebut puncak dasar (base peak), dinyatakan dengan nilai 100 % dan kekuatan (tinggi x kepekaan) puncak – puncak lain, termasuk puncak ion molekulnya, dinyatakan sebagai persentasi puncak dasar tersebut.
Puncak ion molekul biasanya merupakan puncak – puncak dengan bilangan massa tertinggi, kecuali jika terdapat puncak-puncak isotop. Puncak – puncak isotopnya yang biasa.
a. Penentuan Rumus Molekul
Misalnya suatu senyawa mengandung 1 atom karbon. Maka untuk tiap 100 molekul yang mengandung satu atom 12C, sekitar 1,08 % molekul mengandung satu atom 13C. Karenanya molekul-molekul ini akan menghasilkan sebuah puncak M + 1 yang besarnya 1,08 % kuat puncak ion molekulnya; sedangkan atom-atom 2H yang akan memberikan sumbangan tambahan yang amat lemah pada puncak M + 1 itu. Jika suatu senyawa mengandung sebuah atom sulfur, puncak M + 2 akan menjadi 4,4 % puncak induk.
b. Pengenalan Puncak Ion Molekul
Ada dua hal yang menyulitkan pengidentifikasian puncak ion molekul yaitu: 1. Ion molekul tidak nampak atau amat lemah. Cara penanggulangannya ialah
mengambil spectrum pada kepekaan maksimum, jika belum diketahui dengan jelas dapat juga dilihat berdasarkan pola pecahnya.
2. Ion molekul nampak tetapi cukup membingungkan karena terdapatnya beberapa puncak yang sama atau lebih menonjol. Dalam keadaan demikian, pertama – tama soal kemurnian harus dipertanyakan. Jika senyawa memang sudah murni, masalah yang lazim ialah membedakan puncak ion molekul dari puncak M – 1 yang lebih menonjol. Satu cara yang bagus ialah dengan mengurangi berkas penembak mendekati puncak penampilan.
Kaidah Umum untuk Mengenali Puncak-Puncak dalam Spektra
Sejumlah kaidah umum untuk mengenali puncak-puncak menonjol dalam dampak electron dapat ditulis dan dipahami dengan konsep-konsep buku kimia fisik:
1. Tinggi nisbi puncak ion molekul terbesar bagi senyawa rantai lurus dan akan menurun jika derajat percabangan bertambah.
2. Tinggi nisbi puncak ion molekul biasanya makin kecil dengan bertambahnya bobot molekul deret homolog; kecuali untuk ester lemak. 3. Pemecahan/pemutusan cenderung terjadi pada karbon terganti gugus alkil;
makin terganti gugus, makin mudah terputus. Hal ini merupakan akibat lebih mantapnya karboksasi tersier daripada sekunder yang lebih mantap daripada yang primer.
4. Adanya ikatan rangkap, struktur lingkar dan terlebih – lebih cincin aromatik (heteroatom) memantapkan ion molekul hingga meningkatkan pembentukannya.
5. Ikatan rangkap mendukung pemecahan alil dan menghasilkan ion karbonium alil.
6. Cincin jenuh denderung melepas rantai samping pada ikatan-α. Hal ini tidak lain daripada kejadian khusus percabangan. Muatan positif cenderung menyertai sibir cincin. Cincin tak jenuh dapat mengalami reaksi Retro-Diels-Alder.
7. Dalam senyawa aromatik terganti gugus alkil, pemecahan paling mungkin terjadi pada ikatan berlokasi beta terhadap cincin menghasilkan ion benzyl talunan termantapkan atau iontropilium.
8. Ikatan C-C yang bersebelahan dengan heteroatom cenderung terpecah, meninggalkan muatan pada sibiran yang mengandung heteroatom yang electron tak- ikatannya menciptakan kemantapan talunan.
sulfida, hidrogen sianida, merkaptan, ketena atau alkohol. (Silverstein, 1981).
2.4.3. Spektroskopi Inframerah
Penggunaan spektrofotometri infra merah untuk maksud analisa lebih banyak ditujukan untuk identifikasi suatu senyawa.Hal ini disebabkan spectrum infra merah senyawa organik bersifat khas, artinya senyawaan yang berbeda akan mempunyai spectrum yang berbeda pula. Selain dari senyawaan isomer-optik, tidak satu pun antara dua senyawaan yang mempunyai kurva serapan infra merah yang identik.
Alat spektrofotometer infra merah pada dasarnya terdiri dari komponen komponen pokok yang sama dengan alat spektrofotometer ultra lembayung dan sinar tampak,yaitu terdiri sumber sinar, monokromator berikut alat alat optic seperti cermin dan lensa, sel tempat cuplikan, detector, amplifier, dan alat dengan skala pembacaan atau alat perekam spectrum (recorder).
Sumber sinar infra merah pada umumnya berupa zat padat inert yang dipanaskan dengan listrik, sehingga mancapai suhu antara 1.500 – 2.000o K.Akibat pemanasan ini akan dipancarkan sinar kontinu yang menyerupai sinar yang dipancarkan oleh benda hitam.
Daerah penyerapan terpenting dalam spectrum infra merah adalah: a. Daerah vibrasi regang hydrogen 3700 – 2700 cm-1
Ditemukan puncak puncak serapan maksimum di daerah ini hanya disebabkan oleh vibrasi regang antara hydrogen dengan suatu atom lain.
b. Daerah vibrasi regang ikatan ganda tiga, 2700 – 1850 cm-1.
Gugus fungsional yang menyerap di daerah ini terbatas, karena itu ada atau tidak adanya serapan tersebut dalam suatu molekul dapat segera di lihat.
c. Daerah ikatan ganda dua, 1950 – 1550 cm-1.
d. Daerah sidik jari “ finger-print “ , 1500 – 700 cm-1.
Di daerah ini perbedaan sedikit saja dari molekul, adanya subtitusi denga gugus fungsional yang berbeda akan menyebabkan perubahan yang menyolok pada distribusi puncak serapannya (Noerdin.D, 1986).
2.4.4. Sensitivitas Antimikrobial
Banyak zat kimia dapat menghambat atau mematikan mikroorganisme berkisar dari unsur logam berat seperti perak dan tembaga sampai kepada molekul organic yang kompleks seperti persenyawaan ammonium kwartener. Berbagai substansi tersebut menunjukkan efek antimikrobialnya dalam berbagai cara dan terhadap permukaan benda atau bahan juga berbeda-beda; ada yang serasi dan ada yang bersifat merusak.
2.4.5. Bakteri Escherichia coli
Escherichia coli, atau biasa disingkat E. coli, adalah salah satu jenis spesies utam ditemukan dalam
Gambar 2.3. Bakteria Escherichia coli
makanan. Dari sekian ratus strain E. coli yang teridentifikasi, hanya sebagian kecil bersifat pathogen, misalnya strain O157 : H7. Bakteri yang namanya berasal dari sang penemu Theodor Escherich yang menemukannya di tahun 1885 ini merupakan jenis bakteri yang menjadi salah satu tulang punggung dunia bioteknologi. Hampir semua rekayasa genetika di dunia bioteknologi selalu melibatkan E. coli akibat genetikanya yang sederhana dan mudah untuk direkayasa. Riset di E. coli menjadi model untuk aplikasi ke bakteri jenis lainnya. Bakteri ini juga merupakan media cloning yang paling sering dipakai. Teknik recombinant DNA tidak dapat tanpa bantuan bakteri ini. Banyak industri kimia mengaplikasikan teknologi fermentasi yang memanfaatkan E. coli. Misalnya dalam produksi obat-obatan (insulin, antiobiotik), high value chemicals (1-3 propanediol, lactate). Secara teoritis, ribuan jenis produk kimia yang dihasilkan oleh bakteri ini asal genetikanya sudah direkayasa sedemikian rupa guna menghasilkan jenis produk tertentu yang diinginkan. Jika mengingat besarnya peranan ilmu bioteknologi dalam aspek-aspek kehidupan manusia, maka tidak dapat dipungkiri juga betapa besar manfaat E. coli bagi kita.(Levinson,2008).
2.4.6. Bakteri Salmonella
Salmonella adalah suat
tongkat yang menyebabka
spesies Salmonella dapat bergerak bebas dan menghasilka
Salmonella dinamai dari
sebenarnya, rekannya yang pertama kali menemukan bakteri ini t
adalah penyebab utama darifoodborne
diseases). Pada umumnya
kandungannya serta orang lanjut usia. Hal ini disebabkan karena kekebalan tubuh mereka yang menurun. Kontaminasi Salmonella dapat dicegah dengan mencuci tangan dan menjaga kebersihan makanan yang dikonsumsi. Penyebab penyakit Typus (Hepatitis A atau dulu orang menyebutnya sebagai penyakit kuning karena seluruh tubuh si penderita berwarna kekuningan) adalah bakteri bernama Salmonella typhi. Sumber penyebab hepatitis, lebih banyak disebabkan kuman yang menempel di bekas cucian gelas, sendok, piring dan sebagainya dengan kondisi air cucian yang tak diganti, tangan yang kotor. Bakteri ini umumnya terdapat dalam makanan yang sudah basi, daging mentah, maupun kotoran.
2.4.7. Bakteri Shigella
Shigella adalah
berbentuk-tongkat yang berhubungan dekat deng
Shigella merupakan penyebab dari penyakit
Shigella juga menyebabkan penyakit pada
lainnya.
Gambar 2.4. Bakteri Shigella
ketidakmampuannya meragikan laktosa. Shigella mempunyai susunan antigen yang kompleks. Terdapat banyak tumpang tindih dalam sifat serologic berbagai spesies dan sebagian besar kuman ini mempunyai antigen O yang juga dimiliki oleh kuman enterik lainnya. Antigen somatic O dari Shigella adalah lipopolisakarida. Kekhususan serologiknya tergantung pada polisakarida. Terdapat lebih dari 40 serotipe. Klasifikasi Shigella didasarkan pada sifat-sifat biokimia dan antigenik.
Disentri merupakan penyakit yang sangat sering kita jumpai di masyarakat. Umumnya penyakit disentri ini menyerang masyarakat menengah ke bawah dimana tingkat pengetahuannya tentang sanitasi dan kebersihan lingkungan sangatlah terbatas. Disentri adalah suatu infeksi yang menimbulkan luka yang menyebabkan tukak di usus besar bagian tengah yang disebut colon ditandai dengan gejala khas yang disebut sebagai sindroma disentri, yakni: sakit di perut yang sering disertai dengan berak-berak, dan tinja mengandung darah dan lendir. Adanya darah dan lekosit dalam tinja merupakan suatu bukti bahwa kuman penyebab disentri tersebut menembus dinding kolon dan bersarang di bawahnya. Dulu dikenal hanya dua macam disentri berdasarkan penyebabnya, yakni disentri basiler yang disebabkan oleh Shigella spp. dan disentri amuba yang disebabkan oleh Entamoeba histolytica.
2.4.8. Bakteri Staphylococcus aureus
Staphylococcus aureus (S. aureus) adal
menghasilkan pigmen kuning, bersifat aerob fakultatif, tidak menghasilka tidak motil, umumnya tumbuh berpasangan maupun berkelompok, dengan diameter sekitar 0,8-1,0 µm. S. aureus tumbuh dengan optimum pada suhu 37oC dengan waktu
pembelahan 0,47 jam. S. aureus merupaka
luka, atau perlakuan menggunaka sehingga terjadi pelemahan inang.
Gambar 2.5. Bakteria Staphylococcus aureus
Klasifikasi S. aureus Kingdom : Monera Divisio : Firmicutes Class : Bacilli Order : Bacillales
Family : Staphylococcaceae Genus : Staphilococcus
Species : Staphilococcus aureus