BAB 2
TINJAUAN PUSTAKA
2.1. Serbuk Minuman Rasa Jeruk
2.1.1.Definisi
Serbuk Minuman Rasa Jeruk adalah produk yang merupakan campuran
tepung, gula pasir dengan cita rasa jeruk (alami, identik alami, tiruan) dan bahan
tambahan makanan lainnya yang di izinkan (SNI 01-3722-1995). Pengendalian
mutu air sangatlah penting terutama untuk minuman ringan minuman ini pada
hakekatnya adalah air maka rasa atau bau apapun yang kurang menyenangkan
yang ada didalam air akan mempengaruhi rasa produk akhir. Kejernihan yang
tinggi dari sebagian besar minuman ringan merupakan faktor penting dari segi
pemasaran (Buckle, 1985).
Umumnya warna yang ditambahknan disesuaikan dengan cita rasa produk yang
akan dibuat. Misalnya untuk rasa jeruk diberi warna orange. Warna dan rasa
ditambahkan agar ada kesan dari buah asli.
Bahan pewarna sintesis yang boleh digunakan untuk minuman harus dibatasi
jumlahnya karena pada dasarnya setiap benda sintesis yang masuk kedalam tubuh
kita akan mempengaruhi kesehatan jika digunakan dalam dosis tertentu dalam
jangka waktu tertentu, untuk itu kita harus memperhatikan ADI. ADI dinyatakan
dalam mg/kg berat badan jumlah zat kimia yang masuk dalam setiap harinya
2.2 Bahan Tambahan Pangan
Penentuan mutu bahan pangan pada umumnya sangat bergantung pada
beberapa faktor seperti cita rasa, tekstur, nilai gizinya juga sifat mikrobiologisnya.
berdasarkan sumbernya dikenal dua jenis zat pewarna yang temasuk dalam
golongan Bahan Tambahan Pangan (BTP), yaitu pewarna alami dan pewarna
sintetis (Cahyadi, 2009).
Bahan tambahan pangan yang digunakan hanya dapat dibenarkan apabila :
1. Dimakasudkan untuk mencapai masing-masing tujuan penggunaan dalam
pengolahan
2. Tidak digunakan untuk menyembunyikan penggunaan bahan yang salah
atau yang tidak memenuhi persyaratan.
3. Tidak digunakan untuk menyembunyikan cara kerja yang bertentangan
dengan cara produksi yang baik untuk pangan
4. Tidak digunakan untuk menyembunyikan kerusakan bahan pangan
Pengertian Bahan Tambahan Pangan dalam Peraturan Menteri Kesehatan
RI No. 772/Menkes/Per/IX/88No.1168/menkes/PER/X/1999 secara umum
adalah bahan yang biasanya tidak digunakan sebagai makanan dan
biasanya bukan merupakan komponen khas makanan, mempunyai atau
tidak mempunyai nilai gizi, yang sengaja ditambahkan kedalam makanan
untuk maksud teknologi pada pembuatan, pengolahan, penyiapan,
perlakuan, pengepakan, pengemasan dan penyimpanan.
Terdiri dari golongan BTP yang diizinkan diantaranya sebagai berikut.
1. Antioksidan (antioxidant)
3. Pengatur keasaman (acidity regulator)
4. Pemanis buatan (artificial sweetener)
5. Pemutih dan pematang telur (flour treatment agent)
6. Pengemulsi, pemantap dan pengental (emulsifier, stabilizer, thickener)
7. Pengawet (preservative)
8. Pengeras (firming agent)
9. Pewarna (colour)
10. Penyedap rasa dan aroma, penguat rasa (flavor, flavor enhancer)
11. Sekuestran (sequestrant)
Tujuan Penggunaan bahan tambahan pangan adalah dapat meningkatkan
atau mempertahankan nilai gizi dan kualitas daya simpan, membuat bahan pangan
lebih mudah dihidangkan, serta mempermudah preparasi bahan pangan lebih
mudah dihidangkan, serta mempermudah preparasi bahan pangan. Pada umumnya
bahan tambahan pangan dapat dibagi menjadi dua golongan besar, yaitu sebagai
berikut
1. Bahan tambahan pangan yang ditambahkan dengan sengaja kedalam
makanan, dengan mengetahui komposisi bahan tersebut dan maksud
penambahan itu dapat mempertahankan kesegaran, cita rasa, dan
membantu pengolahan , sebagai contoh pengawet, pewarna, dan pengeras.
2. Bahan tambahan pangan yang tidak sengaja ditambahkan, yaitu bahan
yang tidak mempunyai fungsi dalam makanan tersebut, terdapat secara
tidak sengaja, baik dalam jumlah sedikit atau cukup banyak akibat
ditambahkan untuk tujuan produksi bahan mentah atau penanganannya
yang masih terus terbawa kedalam makanan yang akan dikonsumsi.
(Cahyadi, 2006).
2.3 Pewarna Pangan
Pewarna makanan banyak digunakan untuk berbagai jenis makanan dan
minuman, terutama berbagai produk jajanan pasar serta berbagai makanan dan
minuman olahan yang dibuat oleh industri kecil ataupun industri rumah tangga
meskipun pewarna buatan juga ditemukan pada berbagai jenis makanan yang
dibuat oleh industri besar. Yang terakhir ini biasanya sengaja dilakukan oleh
pabrik untuk membuat makanan atau minuman berkalori rendah yang ditujukan
untuk penderita diabetes melitus. Hampir setiap makanan dan minuman olahan
telah dicampur dengan pewarna sintetis. Penggunaannya secara terus menerus
(berlebihan) dapat membahayakan kesehatan. Penggunaan pewarna sebenarnya
boleh saja selama dalam jumlah terbatas. Namun demikian, apabila pewarna yang
digunakan adalah pewarna nonmakanan, misalnya pewarna tekstil atau kertas
ataupun pewarna makanan, tetapi dalam jumlah yang berlebihan, tentulah akan
membahayakan kesehatan konsumen (Yuliarti, 2007).
Warna merupakan salah satu aspek yang penting terhadap kualitas suatu
produk makanan. Kualitas warna dianggap menunjukkan kualitas rasa dan tekstur
dari suatu makanan agar makanan tersebut dapat diterima di masyarakat. Warna
juga mengindikasikan bahwa telah terjadi reaksi kimia pada makanan (Deman,
Ada lima sebab yang dapat menyebabkan suatu bahan makanan berwarna, yaitu :
1. Pigmen yang secara alami terdapat pada tanaman dan hewan. Misalnya
klorofil berwarna hijau, karoten berwarna jingga, dan mioglobin
menyebabkan warna merah pada daging.
2. Reaksi karamelisasi yang timbul bila gula dipanasknan membentuk warna
cokelat. Misalnya warna cokelat pada kembang gula karamel atau roti yang
dibakar.
3. Warna gelap yang timbul karena adanya reaksi Mailard, yaitu antara gugus
aminoprotein dengan gugus karbonil gula pereduksi. Misalnya susu bubuk
yang disimpan lama akan berwarna gelap.
4. Reaksi antara senyawa organik dengan udara akan menghasilkan warna
hitam atau cokelat gelap. Reaksi oksidasi ini dipercepat oleh adanya logam
serta enzim, mislanya warna gelap permukaan apel atau kentang yang
dipotong.
5. Penambahan zat warna, baik zat warna alami maupun zat warna sintetik,
yang termasuk dalam golongan bahan aditif makanan (Winarno, 1992).
2.3.1.Tujuan Penggunaan Pewarna Pangan
Berdasarkan survai yang telah dilakukan Walford (1980), ada beberapa
tujuan penggunaan pewarna pangan, yaitu :
1. Untuk memberikan penampilan yang menarik dari produk makanan yang
telah berubah warna ketika proses pembuatan.
2. Untuk memeberikan warna kepada produk makanan sesuai dengan sifat
3. Untuk menguatkan warna suatu produk makanan yang memiliki warna yang
lemah.
4. Untuk memastikan keseragaman suatu bets dari sumber yang berbeda
(Walford, 1980).
2.3.2.Klasifikasi Zat Pewarna Makanan 2.3.2.1Pewarna Alami
Zat pewarna yang termasuk dalam uncertified color ini adalah zat
pewarna alami (ekstrak pigmen dari tumbuh-tumbuhan) dan zat pewarna mineral,
walaupun ada juga beberapa zat pewarna seperti β -karoten dan kantaxantin yang
telah dapat dibuat secara sintetik. Untuk penggunaannya, zat pewarna ini bebas
dari prosedur sertifikasi dan termasuk daftar yang telah tetap (Winarno, 1992).
Banyak warna cemerlang yang dipunyai oleh tanaman dan hewan dapat
digunakan sebagai pewarna untuk makanan. Beberapa pewarna alami yang
berasal dari tanaman dan hewan, diantaranya adalah klorofil, mioglobin dan
hemoglobin, antosianin, flavonoid, tannin, quinon dan xanton, serta karotenoid
(Cahyadi, 2009)
Berikut beberapa contoh zat pewarna alami yang biasa digunakan untuk
mewarnai makanan
• Karoten menghasilkan warna jingga sampai merah. Biasanya digunakan
mewarnai produk-produk minyak dan lemak seperti minyak goreng dan
margarine. Dapat diperoleh dari wortel, papaya, dan sebagainya.
• Biksin, memberikan warna kuning seperti mentega, biksin diperoleh
digunakan untuk mewarnai mentega, margarine, minyak jagung, dan
salad dressing.
• Karamel berwarna cokelat gelap dan merupakan hasil dari hidrolisis
(pemecahan) karbohidrat, gula pasir, laktosa dan sirup malt. Karamel
terdiri dari 3 jenis, yaitu karamel tahan asam yang sering digunakan
untuk minuman berkarbonat, caramel cair untuk roti dan dan biscuit,
serta caramel kering. Gula kelapa yang selain berfungsi sebagai
pemanis, juga memberikan warna merah kecoklatan minuman es kelapa
ataupun es cendol.
• Klorofil, mengahsilkan warna hijau, diperoleh dari daun. Banyak
digunakan untuk makanan. Saat ini bahkan mulai digunakan pada
berbagai produk kesehatan. pigmen klorofil banyak terdapat pada
dedaunan seperti suji, pandan, dan daun katuk dan sebagainya.
• Antosianin, penyebab warna merah, orange, ungu dan biru banyak
terdapat pada bunga dan buah-buahan. Penggunaan zat pewarna alami,
misalnya pigmen antosianin masih terbatas pada beberapa produk
makanan, seperti produk minuman
• Kurkumin berasal dari kunyit sebagai salah satu bumbu dapur sekaligus
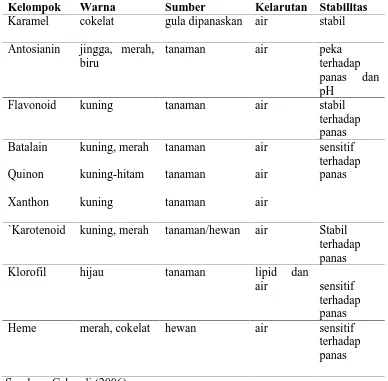
Tabel 1.Sifat-sifat Bahan Pewarna Alami
Kelompok Warna Sumber Kelarutan Stabilitas
Karamel cokelat gula dipanaskan air stabil
Antosianin jingga, merah, biru
tanaman air peka
terhadap panas dan pH
Flavonoid kuning tanaman air stabil
terhadap panas Batalain Quinon Xanthon kuning, merah kuning-hitam kuning tanaman tanaman tanaman air air air sensitif terhadap panas
`Karotenoid kuning, merah tanaman/hewan air Stabil terhadap panas
Klorofil hijau tanaman lipid dan
air sensitif
terhadap panas
Heme merah, cokelat hewan air sensitif
terhadap panas
Sumber : Cahyadi (2006)
Banyak sekali bahan alami yang dapat digunakan sebagai pewarna
makanan, umumnya pewarna alami aman untuk digunakan dalam jumlah yang
bear sekalipun, berbeda dengan pewarna sintesis yang demi keamanan
penggunaanya harus dibatasi dengan melihat ADI-nya (Yuliarti, 2007)
Zat pewarna ditambahkan kedalam makanan bertujuan untuk menarik
selera dan keinginan konsumen. Zat-zat Pewarna alam yang sering digunakan
misalnya, karoten, kunyit dan daun-daun pandan. Dibandingkan dengan bahan
pewarna alami, maka bahan pewarna buatan mempunyai banyak kelebihan yaitu
penyimpanannya lebih mudah dan lebih tahan lama. Selain daripada itu
bahan pewarna alami biasanya warnanya jarang yang sesuai dengan warna yang di
ingini. (Winarno, 1980)
Tabel 2.Kestabilan Beberapa Pewarna Sintetis
Perwarna Nomor Indeks Warna
(C.I.No)
Batas Maksimum Penggunaan
Amaran Amaranth: CI Food
Red 9
16185
Secukupnya
Biru Berlian
Brilliant Blue FCF: CI
42090
Secukupnya
Eritrosin Food red 2
Eritrosin: CI
45430
Secukupnya
Hijau FCF
Food red 14 Fast green FCF: CI
42053 Secukupnya
Hijau S
Food green 3 Green S: CI Food
44090 Secukupnya
Indigotin
Green 4 Indigotin: CI Food
73015 Secukupnya
Ponceau 4R
Blue I
Ponceau 4R: CI
16255
Secukupnya
Kuning
Food red 7 74005
Secukupnya
Karmoisin Carmoisine; CI Food Red 3;
14720
2.3.2.2 Pewarna Sintetis
Pewarna sintetik adalah pewarna yang dibuat melalui sintesis secara
kimia. Berdasarkan kelarutannya, dikenal dua macam pewarna sintetis, yaitu dyes
dan lakes. Penggunaan bahan pewarna buatan yang tidak direkomondasikan oleh
Depkes RI atau oleh FDA dapat menimbulkan gangguan kesehatan, seperti
Timbulnya kanker usus dan pancreas . Hal ini disebabkan oleh kandungan arsen
melebihi 0,00014% dan timbal melebihi 0,001%. Batas konsumsi bahan pewarna
buatan yang direkomondasikan oleh Depkes berkisar 1,25-1,5 mg/Kg berat badan
(untuk warna merah 25 mg/Kg berat badan (untuk warna biru) 12,5 mg/Kg berat
badan untuk (warna hijau), dan 5-7,5 mg/Kg berat badan (untuk warna kuning).
(Budiyanto, 2001).
Banyak warna cemerlang yang dipunyai oleh tanaman dan hewan dapat
digunakan sebagai pewarna makanan. Beberapa pewarna alami ikut
menyumbangkan nilai nutrisi memberikan bumbu atau pemberi rasa ke bahan
olahannya. Dewasa ini ada beberapa bahan pewarna alami yang digunakan untuk
menggantikan pewarna sintetik.. Pewarna alami juga dapat memberikan fungsi
tambahan sebagai antioksidan, antimikroba, dan fungsi lainnya.
Hal ini menyebabakan pertumbuhan penggunaan pewarna alami
cenderung menjadi dua kali lipat bila dibandingkan dengan pewarna sintetis,
terutama di negara-negara maju. Meskipun pewarna alami ini jauh lebih aman
untuk dikonsumsi, akan tetapi penggunaan pewarna alami belum dapat dilakukan
secara menyeluruh, sebab beberapa kendala, seperti rasa yang kurang sedap,
Di Indonesia, peraturan mengenai penggunaan zat pewarna yang diizinkan
dan dilarang untuk pangan diatur melalui SK Menteri Kesehatan RI Nomor
722/Menkes/Per/IX/88 mengenai Bahan Tambahan Pangan (BTP). Akan tetapi,
seringkali terjadi penyalahgunaan pemakaian zat pewarna untuk sembarang bahan
pangan, misalnya zat pewarna untuk tekstil dan kulit dipakai untuk mewarnai
bahan pangan. Hal ini jelas sangat berbahaya bagi kesehatan karena adanya residu
logam berat pada zat pewarna tersebut (Yuliarti, 2007).
Umumnya pewarna alami diperoleh dari ekstrak kasar dari suatu
tumbuhan yang pada dasarnya tidak stabil. Jelas terlihat stabilitas warna pada
beberapa makanan dari penggunaan pewarna alami ini. Sebagai contoh adalah
antosianin. Antosianin dapat digunakan pada beberapa produk, akan tetapi variasi
warna yang ada terlalu sempit penggunaannya. Hal ini disebabkan ketidakstabilan
antosianin terhadap pH tertentu, terutama pH asam (Walford, 1984).
Tabel3.Kestabilan Beberapa Pewarna Sintetis
Pewarna Kestabilan terhadap
Cahaya Oksidasi pH
Eritrosin Sangat baik Rendah Sangat rendah
Merah
Allura
Sangat baik Rendah Baik
Kuning
FCF
Sedang Rendah Baik
Hijau FCF Rendah Sangat rendah Baik
Biru Berlian Rendah Sangat rendah Baik
Indigotin Sangat rendah Sangat rendah Baik
Zat warna yang termasuk golongan dyes telah melalui prosedur sertifikasi
yang ditetapkan oleh US-FDA. Sedangkan zat pewarna lakes yang hanya terdiri
dari satu warna, tidak merupakan campuran, juga harus mendapat sertifikat.
Dalam certified colour terdapat spesifikasi yang mencantumkan keterangan yang
penting mengenai zat pewarna tertentu, misalnya bentuk garam, kelarutan, dan
residu yang terdapat didalamnya. Pada umumnya pewarna sintetis lebih stabil
terhadap pH, cahaya, dan faktor lainnya selama pengolahan dan penyimpanan
(Cahyadi, 2008).
Tabel 4.Golongan Pewarna Sintetik
Golongan Contoh Pewarna
Azo Dyes Allura Red (Merah Allura)
Amaranth, Azorubin (Carmoisin), Briliant
Black, Brown FK, Brown HT, Litol Rubin BK,
Ponceau 4R, Merah 2G, Sunst Yellow,
Tartrazine
Triarylmethane Dyes Briliant Blue FCF, Fast Green FCF, Green S,
Patent Blue V
Quinophthalon Dyes Quinoline Yellow (Kuning Kuinelin)
Xanthene Dyes
Indigo Dyes
Erythrosine (Eritrosin)
Tabel 5. Pewarna Sintetik yang diizinkan dan yang dilarang di Indonesia Pewarna yang Diizinkan
Pewarna Nomor Indeks Warna (C.I. No)
Amaran 16185
Biru Berlian 42090
Eritrosin 45430
Hijau FCF 42053
Hijau S 44090
Indigotin 73015
Ponceau 4R 16255
Kuning Kuinelin 15980
Sunset Yellow 15985
Tartrazin 19140
Carmoisin 14720
Pewarna yang Dilarang
Citrus Red 12156
Ponceau 3R 16155
Ponceau SX 14700
Rhodamin B 45170
Buinea Green B 42085
Magentha 42510
Chrysoidine 11270
Butter Yellow 11020
Sudan I 12055
Methanil Yellow 13065
Auramine 41000
Oil Orange SS 12100
Oil Orange XO 12140
Oil Yellow AB 11380
Oil Yellow OB 11390
Sumber : Cahyadi (2008)
Menurut Winarno (1992), ada dua macam yang tergolong certified color
yaitu dye dan lake. Keduanya adalah zat pewarna buatan. Zat warna yang
juga harus mendapat sertifikat. Dalam certified color terdapat spesifikasi yang
mencantumkan keterangan yang penting mengenai zat pewarna tertentu, misalnya
bentuk garam, kelarutan dan residu yang terdapat didalamnya.
1. Dye
Dye adalah zat pewarna yang umumnya bersifat larut dalam air, sehingga
larutannya menjadi berwarna dan dapat digunakan untuk mewarnai bahan. Pelarut
yang dapat digunakan selain air adalah propilen glikol, gliserin atau alkohol,
sedangkan dalam semua jenis pelarut organik, dye tidak dapat larut. Dye terdapat
dalam bentuk bubuk, butiran, pasta maupun cairan. Penggunaannya tergantung
dari kondisi bahan, kondisi proses dan zat pewarnaannya sendiri. Zat pewarna dye
terbagi menjadi empat kelompok, yaitu azo dye, tryphenylmethane dye,
fluorescein dan sulfonated indigo (Winarno, 1992). Pada umumnya penggunaan
dye dilakukan untuk mewarnai roti dan kue, produk-produk susu, minuman
ringan, minuman berkarbonat dan lain-lain. Konsentrasi pemakaian tidak dibatasi
secara khusus, tetapi di Amerika Serikat disarankan agar digunakan dengan
memperhatikan Good Manufacturing Practices (GMP), yang pada prinsipnya
dapat digunakan dalam jumlah yang tidak melebihi keperluan untuk memperoleh
efek yang diinginkan.
2. Lake
Zat pewarna ini merupakan gabungan dari zat warna dye dengan radikal
basa (Al atau Ca) yang dilapisi dengan aluminium hidrat (alumina). Lapisan
alumina ini tidak larut dalam air, sehingga lake ini tidak larut pada hampir semua
pelarut. Lake stabil pada pH 3,5-9,5 dan diluar selang tersebut lapisan alumina
Kandungan dye dalam lake disebut pure dyes contents (pdc). Lakes
umumnya mengandung 10-40% dye murni. Sesuai dengan sifatnya yang tidak
larut dalam air, maka zat pewarna ini digunakan untuk produk-produk yang tidak
boleh kena air. Dibandingkan dengan dye, maka lake pada umumnya bersifat
lebih stabil terhadap cahaya, kimia dan panas sehingga harga lake umumnya lebih
mahal daripada harga dye (Cahyadi, 2006).
2.4. Efek Bahan Pewarna Terhadap Kesehatan
Sejumlah makanan yang kita konsumsi tidak mengandung zat berbahaya
menurut daftar zat warna yang dinyatakan sebagai bahan berbahaya (Peraturan
Menteri Kesehatan Republik Indonesia Nomor 722/Menkes/Per/IX/88). Namun
demikian, penggunaan pewarna tersebut hendaknya dibatasi karena meskipun
relatif aman, penggunaannya dalam jumlah yang besar tetap dapat membahayakan
kesehatan masyarakat. Menurut Cahyadi (2009), zat warna diabsorbsi dari dalam
saluran pencernaan makanan dan sebagian dapat mengalami metabolisme oleh
mikroorganisme dalam usus. Dari saluran pencernaan dibawa langsung ke hati,
melalui vena portal atau melalui sistem limpatik ke vena superior. Zat warna yang
dimetabolisme dan dikonjugasi di hati, selanjutnya ada juga yang ke empedu
memasuki jalur sirkulasi enterohepatik. Zat warna azo yang larut dalam air
diekskresi secara kuantitatif melalui empedu, sedangkan yang larut dalam lemak
diabsorpsi sempurna tanpa metabolisme dalam usus, melainkan dimetabolisme
dalam hati oleh azo-reduktase membentuk amin primer yang sesuai, atau dapat
juga dihidrolisis, atau diikat oleh protein-protein hati. Senyawa yang merupakan
Efek kronis yang disebabkan oleh zat warna azo yang dimakan dalam
jangka waktu lama menyebabkan kanker hati. Selain senyawa-senyawa azo lain
mengakibatkan kanker walaupun efeknya lebih kecil dan waktunya lebih lama.
Para ilmuwan pada umumnya mempergunakan zat warna azo dalam
penelitiannya, karena hampir 90% dari bahan pewarna pangan terdiri dari zat
warna azo (Cahyadi, 2006).
Zat-zat yang berbahaya bagi kesehatan disebut zat beracun. Banyak zat-zat
kimia yang beracun pada dosis besar dan tidak beracun pada dosis yang kecil.
Kecenderungan zat-zat berbahaya yang menyebabkan kanker pada manusia
menjadi perhatian publik pada saat ini (Hughes, 1987).
Khususnya yang dijual di pinggir jalan, rentan terhadap polusi, debu
maupun asap knalpot. Sering kali makanan tersebut tidak disiapkan secara
higienis atau juga mempergunakan bahan-bahan yang berbahaya seperti zat
pewarna karena alas an harganya murah. (Khomsan, 2003).
2.5 Analisis Zat Pewarna Sintetis Secara Kromatografi Kertas
Pada laboratorium analisis pewarna pangan sudah rutin dilakukan dengan
berbagai metode, tehnik dan cara. Sebagian besar analisis berdasarkan suatu
prinsip kromatografi ataupun menggunakan alat spektrofotometer. Cara tersebut
digunakan untuk mendeteksi zat pewarna secara teliti, karena itu minimal
diperlukan fasilitas cukup serta cukup tersedianya pelarut organik yang biasanya
cukup mahal harganya dan tehnik ini memerlukan waktu yang cukup lama
2.5.1 Kromatografi
Berbagai jenis pemisahan yang sederhana dengan kromatografi kertas telah
dikerjakan dimana proses dikenal sebagai analisa kapiler. Mula-mula telah
dilakukan pemisahan asam-asam amino dan peptida yang merupakan hasil
hidrolisa protein wool dengan suatu cara dimana kolom yang berisi bubuk diganti
dengan lembaran kertas dan kemudian diletakkan dalam bejana tertutup yang
berisi uap jenuh larutan. Dimana fase tetap adalah air, disokong oleh
molekul-molekul selulosa dari kertas, dan fase gerak biasanya merupakan campuran dari
satu atau lebih pelarut-pelarut organik dan air. (Sastrohamidjojo, 1991).
Kromatografi Kertas dan Kromatografi Lapis Tipis merupakan metode
kromatografi yang sederhana. Kromatografi Kertas merupakan jenis kromatografi
partisi, dimana fasa diam adalah air yang disokong oleh molekul-molekul selulosa
dari kertas, dan fasa gerak merupakan campuran dari satu atau lebih
pelarut-pelarut organik dan air. Kromatografi Kertas sudah sering digunakan untuk
mengidentifikasi pewarna sintetik pada makanan. Bahkan metode ini hingga saat
ini masih digunakan oleh Balai Besar Pengawas Obat dan Makanan (POM)
(Gritter, 1991).
Prosedur penyiapan sampel dari kedua metode kromatografi ini sama
yakni, sejumlah cuplikan ditambahkan asam asetat encer kemudian masukkan
benang wool bebas lemak secukupnya, lalu dipanaskan diatas nyala api kecil
selama 30 menit sambil diaduk. Benang wool dicuci dengan air hingga bersih.
Pewarna dilarutkan dari benang wool dengan penambahan ammonia 10% diatas
juga totolkan baku pembanding. Elusi dengan eluen yang sesuai pada suhu kamar
(Cahyadi, 2009).
Mekanisme pemisahan dengan kromatografi kertas prinsipnya sama
dengan mekanisme pada kromatografi kolom. Adsorben dalam kromatografi
kertas adalahkertas saring, yakni selulosa. Sampel yang akan dianalisis ditotolkan
ke ujung kertas yang kemudian digantung dalam wadah. Kemudian dasar kertas
saring dicelupkan kedalam pelarut yang mengisi dasar wadah. Fasa mobil
(pelarut) b dapat saja beragam.Air, etanol, asam asetat atau campuran zat-zat ini
dapat digunakan.Kromatografi kertas diterapkan untuk analisis campuran asam
amino dengan sukses besar. Karena asam amino memiliki sifat yang sangat mirip,
dan asam-asam amino larut dalam air dan tidak mudah menguap (tidak mungkin
didestilasi), pemisahan asam amino adalah masalah paling sukar yang dihadapi
kimiawan di akhir abad 19 dan awal abad 20. Jadi penemuan kromatografi kertas
merupakan berita sangat baik bagi mereka. Kimiawan Inggris Richard Laurence
Millington Synge (1914-1994) adalah orang pertama yang menggunakan metoda
analisis asam amino dengan kromatografi kertas.Saat campuran asam amino
menaiki lembaran kertas secara vertikal karena ada fenomena kapiler, partisi asam
amino antara fasa mobil dan fasa diam (air) yang teradsorbsi pada selulosa
berlangsung berulang-ulang. Ketika pelarut mencapai ujung atas kertas proses
dihentikan. Setiap asam amino bergerak dari titik awal sepanjang jarak
tertentu.Dari nilai R, masing-masing asam amino diidentifikasi. Kromatografi
kertas dua-dimensi (2D) menggunakan kertas yang luas bukan lembaran kecil,
dan sampelnya diproses secara dua dimensi dengan dua pelarut ( www.Indigo.
Menurut Sastrohamidjojo, H (1991) menyatakan bahwa apabila akan
melakukan pemisahan dengan kromatografi kertas maka hal-hal seperti berikut
perlu mendapatkan perhatian.
2.5.1.1. Metode Pemisahan
Ada beberapa metode dalam pemisahan dengan kromatografi kertas
diantaranya :
- Metode penurunan yaitu berupa bejana yang terbuat dari gelas, platina atau
logam tahan karat yang di atasnya ditutup untuk mencegah dari pelarut. Untuk
menyangga agar kertas tak lepas perlu diberi penahan dari batang gelas. Untuk
beberapa centimeter pelarut mengalir oleh gaya kapiler dan mengalir oleh
gravitasi setelah permukaan pelarut melintasi batang gelas.
- Metode penaikan. Bejana yang digunakan untuk kromatografi penaikan sama
seperti untuk kromatografi penurunan, tetapi pelarut diletak dibagian bawah
bejana dan kertas dicelupkan di atasnya.
- Metode mendatar. Dalam cara ini kertas dibentuk bulat ditengahnya diberi
lubang sebagai tempat untuk meletakkan sumbu yang terbuat baik dari gulungan
kertas atau dari benang dimana melalui ini pelarut akan naik yang kemudian akan
membesahikertas untuk kemudian mengembang, melingkar, membawa senyawa
yang dipisahkan.
2. 5.1.2. Kertas
Kromatografi kertas menggunakan kertas saring whatman no. 1 dan
sampai saat ini masih dipakai.Kertas dalam pemisahan terutama mempunyai
hidroksil dimana ini kemungkinan sangat penting dan sejumlah kecil dari gugus
karboksil dalam selulosa dapat menaikkan terhadap efek-efek pertukaran ion.
Kecepatan aliran naik dengan penurunan kekentalan dari pelarut (dengan kenaikan
dalam suhu), tetapi aliran pelarut pada suhu yang tertentu, ditentukan oleh
kerapatan dan tebalnya kertas.
2.5.1.3. Pelarut
Fase bergerak biasanya merupakan campuran yang terdiri atas satu
komponen organik yang utama, air dan berbagai tambahan seperti asam-asam,
basa atau pereaksi-pereaksi kompleks untuk memperbesar kelarutan dari beberapa
senyawa atauuntuk mengurangi yang lainnya. Anti oksida sering digunakan juga
dan harus didapati dengan kemurnian yang tinggi. Pelarut harus sangat mudah
menguap, karena terlampau cepat mengadakan kesetimbangan, pada keadaan
yang lain volalitas yang tinggi mengakibatkan lebih cepat hilang meninggalkan
lembaran kertas setelah bergerak. Kecepatan bergeraknya harus tidak cepat
dipengaruhi oleh perubahanperubahan suhu. Contoh penggunaan dari pelarut yang
dipilih untuk senyawa- senyawa organik yang polar akan lebih mudah larut dalam
air dari pada dalam zat–zat cair organic akan terjadi gerakan-gerakan yang lambat
jika fase bergerak anhidrida digunakan, penambahan air terhadap pelarut akan
menyebabkan senyawa-senyawa tersebut untuk bergerak. Jadi n-butanol bukan
merupakan suatu pelarut untuk asam-asam amino jika tidak dijenuhkan dengan air
penambahan asam cuka disertai dengan pemberian lebih banyak air akan menjadi
baik, yaitu akan menaikkan kelarutan dari asam-asam amino terutama yang
bersifat basa, campuran tiga komponen ini sangat baik untuk senyawa senyawa
2.5.1.4.Cara Penempatan Cuplikan Pada Kertas
Larutan campuran yang akan dipisahkan ditempatkan pada kertas yang
berupa noda. Biasanya dibiarkan untuk berkembang membentuk suatu bulatan.
Bagian kertas yang ditetesi dibiarkan dalam keadaan mendatar, sehingga larutan
pada keadaan kompak dalam bentuk bulatan. Dan jangan biarkan kertas tersentuh
zat-zat yang lain. Biasanya diameter dari noda yang digunakan adalah 0,5 cm
(Sastrohamidjojo, 1991).
2.5.1.5.Identifikasi Dari Senyawa-Senyawa
Menurut Sastrohamidjojo, H (1991) menyatakan bahwa dalam
mengidentifikasi nodanodadalam kertas sangat lazim menggunakan harga Rf
(retordation factor) yang didefenisikan sebagai :
Rf =
Nilai maksimum Rf adalah 1 dan ini dicapai ketika solut mempunyai
perbandingan distribusi dan faktor retensi sama dengan 0 yang berarti senyawa
bermigrasi dengan kecepatan yang sama dengan fase gerak. Nilai minimum Rf
adalah 0 dan ini teramati jika senyawa tertahan pada posisi titik awal dipermukaan
fase diam (Rohman, 2007).
Ada beberapa faktor yang menentukan harga Rf yaitu diantaranya adalah :
1. Pelarut, disebabkan pentingnya koefisien partisi, maka perubahan-perubahan
yang sangat kecil dalam komposisi pelarut dapat menyebabkan
perubahan-perubahan harga Rf.
2. Suhu, perubahan dalam suhu merubah koefisien partisi dan juga kecepatan
3. Ukuran dari bejana, volume dari bejana mempengaruhi homogenitas dari
atmosfer jadi mempengaruhi kecepatan penguapan dari komponen-komponen
pelarut dari kertas.
4. Kertas. Pengaruh utama kertas pada harga Rf timbul dari perubahan ion dan
serapan, yang berbeda untuk macam-macam kertas. Kertas mempengaruhi
kecepatan aliran.ia akan juga mempengaruhi pada kesetimbangan partisi.
5. Sifat dari campuran. Berbagai senyawa mengalami partisi dan antara
volume-volume yang sama dari fase tetap dan bergerak. Mereka hampir selalu
mempengaruhi karakteristik dari kelarutan satu terhadap yang lainnya hingga