210
MAKALAH
PARALEL
PARALEL C
ISBN :978-602-73159-8
ISOLASI, IDENTIFIKASI DAN UJI ANTIOKSIDAN SENYAWA
ASAM FENOLAT DARI RIMPANG LENGKUAS MERAH (
Alpinia
purpurata
K. Schum)
Siti Nurhasanah
1*, Dra. Dewi Kusrini, M.Si
1, dan Dra. Enny Fachriah, M.Si
1 1Departemen Kimia, Fakultas Sains dan Matematika, Universitas Diponegoro,Jl. Prof. Soedarto, Tembalang, Kota Semarang, Jawa Tengah 50275, Indonesia
1 Departement of Chemistry, Faculty of Science and Mathematics, University of Diponegoro
Prof. Soedarto street, Tembalang, Semarang, Central Jawa 50275, Indonesia
* Untuk korespondensi: Telp: 082110506088, e-mail: snurhasanahf@gmail.com
ABSTRAK
Telah dilakukan penelitian tentang identifikasi dan penentuan kadar asam fenolat dari rimpang lengkuas merah (Alpinia purpurata K Schum). Penelitian ini bertujuan untuk mengidentifikasi asam fenolat pada ekstrak etanol rimpang lengkuas merah, menentukan kadar asam fenolat dan uji aktivitas antioksidan. Metode yang digunakan pada peneitian ini adalah isolasi asam fenolat dengan hidrolisis asam, hidrolisis basa dan tanpa hidrolisis, penentuan kadar asam fenolat dengan instrument TLC Scanner dan uji aktivitas antioksidan dengan metode DPPH. Berdasarkan identifikasi menggunakan TLC dan TLC Scanner, bahwa dari fraksi hidrolisis asam (HA), hidrolisis basa (HB) dan tanpa hidrolisis (TH) ekstrak etanol rimpang lengkuas merah diduga mengandung senyawa asam ferulat. Dari hasil kuantitatif menggunakan TLC Scanner diketahui kadar asam ferulat pada fraksi HA, HB dan TH masing-masing 16,25%; 5%; dan 4,9%. Hasil penelitian menunjukkan pada fraksi HA menghasilkan kadar asam ferulat lebih tinggi dibanding fraksi HB dan TH. Pada uji aktivitas antioksidan yang dilakukan secara kualitataif menunjukkan bahwa isolat asam ferulat yang terkandung pada ketiga fraksi aktif meredam radikal DPPH.
Kata kunci: Alpinia purpurata, asam fenolat, TLC Scanner, DPPH
ABSTRACT
This research is conducted about the identification and determination of phenolic acids in red galangal rhizomes (Alpinia purpurata K Schum). The main purpose of this research is to identify phenolic acids in ethanol extract of the red galangal rhizomes, to determine the levels of phenolic acids and to test the antioxidant activities. The methods used in this research are the isolation of phenolic acids with hydrolysis acids hydrolysis bases and non-hydrolysis, the determination of phenolic acids is using TLC Scanner instrument and the test of antioxidant activity using DPPH method. Based on the identification using TLC and TLC Scanner, from the fraction of acid hydrolysis (HA), base hydrolysis (HB) and non-hydrolysis (TH), the ethanol extract of the red galangal rhizomes contain ferulic acids. The quantitative result using TLC Scanner, the levels of ferulic acids in HA, HB and TH fractions are 16.25%; 5%; and 4.9%. The result of the research shows in which HA fraction produces more ferulic acids than HB and TH fractions. In the antioxidant activity test conducted by qualitative explains that ferulic acid isolate contained in three active fractions reduce the DPPH radical.
PENDAHULUAN
Dewasa ini penggunaan obat herbal memiliki kemajuan yang pesat, tidak hanya masyrakat kalangan bawah yang
menggunakan melainkan masyarakat
kalangan atas juga menggunakan
pengobatan herbal yang dinilai berkhasiat dan tidak menimbulkan efek samping yang berlebih.
Salah satu obat tradisional yang sudah dikonsumsi oleh banyak orang adalah berasal dari tanaman lengkuas merah (Alpinia purpurata K. Schum). Beberapa penelitian melaporkan bahwa lengkuas
merah memiliki aktivitas antioksidan,
antibakteri[1] antikanker[2] antijamur[3].
Aktivitas tersebut dimiliki oleh tanaman lengkuas merah atas peran serta dari kandungan kimia dalam tanaman tersebut. Kandungan kimia yang terkandung didalam tanaman lengkuas merah adalah flavonoid, saponin, tannin, fenolik[4] sineol, sinamat,
kamfer, d-pinen, galangin dan eugenol[5].
Asam fenolat yang terkandung di dalam tanaman alpinia meliputi asam galat, asam ellagat [6].
Asam fenolat dalam beberapa tanaman ada tiga bentuk yaitu asam fenolat bebas, asam fenolat yang terikat dengan ester dan asam fenolat yang terikat dengan glikosida[7]. Pengambilan asam fenolat bebas
dari ikatan ester dan ikatan glikosida dapat
dilakukan dengan memutuskan ikatan
tersebut melalu hidrolisis[7]. Oleh sebab itu,
pada penelitian ini telah dilakukan hidrolisis asam, hidrolisis basa dan tanpa hidrolisis pada ekstrak etanol rimpang lengkuas merah untuk mengindentifikasi asam fenolat serta menguji aktivitas antioksidan.
METODE PENELITIAN
Bahan. Simplisia rimpang kengkuas merah, n-heksana, etanol , akuades, amonia, amil alkohol, serbuk magnesium, anhidrida asam asetat, pereaksi Meyer, pereaksi Dragendorff, pereaksi FeCl3 1%, H2SO4 p.a,
NaOH p.a, NaHCO3 p.a, eter, HCl p.a,
metanol p.a, kloroform p.a, CH3COONa p.a,
Na2SO4 anhidrat, plat silika gel GF254,
CH3COOH p.a, pereaksi diazo p-nitroanilin,
Na2CO3 p.a, etil asetat p.a, asam galat, asam
ferulat, pirogalol, dan asam salisilat.
Alat. Peralatan Alat gelas standar penelitian, lampu UV 254 nm atau 365 nm, satu set alat maserator dan rotary evaporator Buchii, satu set alat hidrolisis, neraca analitis, botol semprot, botol vial, chamber KLT, pipet tetes, pipet ukur, pipet mikro, indikator pH dan, TLC Scanner Camag 3.
Preparasi Sampel
Sampel berupa rimpang lengkuas merah yang diperoleh di daerah Semarang Jawa Tengah. Rimpang lengkuas merah yang diperoleh dibersihkan, dikeringkan dan dihaluskan menjadi serbuk
Uji Skrinning Fitokimia. Uji Flavonoid
Serbuk rimpang lengkuas merah
sebanyak 5 gram ditambahkan 50 mL aquades kemudian dipanaskan hingga mendidih. Filtrat yang diperoleh diambil sebanyak 5 mL kemudian ditambah dengan serbuk Mg, ditambah dengan 1 mL HCl pekat, dan ditambah dengan 2 mL amil alkohol. Kemudian dikocok perlahan dan dibiarkan memisah hingga terbentuk lapisan amil alkohol. Hasil positif ditandai dengan
terbentuknya 2 lapisan. Uji Saponin.
Serbuk rimpang lengkuas merah
sebanyak 2,5 gram ditambah dengan 10 mL air panas. Kemudian didinginkan dan setelah itu dikocok kuat 10 detik. Hasil positif ditandai dengan munculnya busa dan dengan penambahan 1% HCl busa tetap stabil. Uji Fenol
Sebanyak 2,5 gram serbuk rimpang lengkuas merah didihkan dalam 10 mL air suling selama 5 menit , kemudian disaring lalu filtratnya diambil 2 mL larutan lalu ditambahkan 1 sampai 2 tetes pereaksi besi (III) klorida. Apabila terjadi warna biru atau hijau kehitaman menunjukkan adanya tanin (Farnsworth, 1966).
Uji Triterpenoid/Steroid
Sebanyak 2,5 gram Serbuk rimpang lengkuas merah dimaserasi dengan 20 mL eter selama 2 jam, kemudian disaring dan filtratnya ditempatkan pada plat tetes lalu
dibiarkan sampai kering. Selanjutnya
ditambahkan 2 tetes anhidrida asetat dan 1 tetes H2SO4 p.a ke plat tetes. Adanya steroid
ditunjukkan jika terbentuk warna biru atau ungu, sedangkan bila terbentuk warna merah menandakan adanya triterpenoid.
Isolasi Asam Fenolat
Sebanyak 1,4 kg serbuk rimpang lengkuas merah merah dimaserasi dengan n-heksana, ampasnya dikering anginkan dan dimaserasi kembali dengan etanol 96% dan
diperoleh ekstrak etanol kemudian
dievaporasi sampai mendapat ekstrak kental
dan ditimbang. Ekstrak etanol kental
dilarutkan dalam etanol selanjutnya ekstrak etanol diproses melalui tiga macam, yaitu
hidrolisis basa, hidrolisis asam, dan tanpa hidrolisis.
Hidrolisis basa
Ekstrak etanol dicampur dengan larutan NaOH 1 N pada suhu kamar dan ruang gelap selama 24 jam. Hasil hidrolisis dilakukan penambahan H2SO4
10% kemudian diekstraksi dengan eter untuk memisahkan asam fenolat dengan senyawa lain. Fraksi eter selanjutnya diuapkan dengan rotarry evaporator dan diekstraksi dengan NaHCO3 20% untuk
memisahkan asam fenolat dengan senyawa fenol lainnya. Lapisan air diasamkan dengan H2SO4 10% lalu
diekstraksi dengan eter. Fraksi eter selanjutnya diuapkan sampai kering. Residu dilarutkan dalam metanol dan
selanjutnya disebut fraksi HB
(Zadernowski dkk, 2005).
Hidrolisis asam
Ekstrak etanol dicampur dengan larutan H2SO4 2N dalam penangas air
selama 2 jam. Hasil hidrolisis lalu
diekstraksi dengan eter untuk
memisahkan asam fenolat dengan senyawa lain. Fraksi eter selanjutnya
diuapkan dengan dengan rotarry
evaporator dan diekstraksi dengan NaHCO3 20% untuk memisahkan asam
fenolat dengan senyawa fenol lainnya. Lapisan air diasamkan dengan H2SO4
10% lalu diekstraksi dengan eter. Fraksi eter selanjutnya diuapkan sampai kering. Residu dilarutkan dalam metanol dan
selanjutnya disebut fraksi HA
(Zadernowski dkk, 2005).
Ekstrak etanol diasamkan dengan
H2SO4 10% kemudian diekstraksi
dengan eter untuk memisahkan asam fenolat dengan senyawa lain. Fraksi eter selanjutnya diuapkan dengan dengan rotarry evaporator dan diekstraksi
dengan NaHCO3 20% untuk
memisahkan asam fenolat dengan senyawa fenol lainnya. Lapisan air diasamkan dengan H2SO4 10% lalu
diekstraksi dengan eter. Fraksi eter selanjutnya diuapkan sampai kering. Residu dilarutkan dalam metanol dan
selanjutnya disebut fraksi TH
(Zadernowski dkk, 2005).
Pemisahan Asam Fenolat
Pemisahan asam fenolat dilakukan
terhadap fraksi HA, HB, dan TH
menggunakan kromatografi lapis tipis (KLT) dengan plat silika gel GF254 dan eluen
campuran etil asetat kloroform dan asam asetat dengan perbandingan tertentu. Noda yang diperoleh selanjutnya dibandingkan dengan standar yaitu asam galat, asam kafeat, asam ferulat, asam pirogalol, asam salisilat. Noda tiap fraksi yang memiliki Rf sejajar dengan pembanding selanjutnya diidentifikasi dengan TLC Scanner.
Identifikasi Asam Fenolat menggunakan TLC Scanner.
Identifikasi dilakukan menggunakan TLC Scanner terhadap fraksi HA, HB dan TH, dan senyawa standar 50, 100, 250, 500 dan 1000 ppm dalam methanol. Selanjutnya masing-masing 20 µL senyawa standar dengan variasi konsentrasi, fraksi HA, HB dan TH dianalisis dan diukur luas areanya
menggunakan TLC Scanner untuk
menentukan kadar senyawa yang
terkandung dalam setiap fraksi.
Penentuan Aktivitas Antioksidan dengan metode DPPH
Penentuan aktivitas antioksidan menggunakan metode dari Molyneux (2004)
secara kualitatif yaitu dengan cara
melarutkan 19,7 mg DPPH dalam metanol 100 mL kemudian direaksikan di dalam ruangan gelap dan dipindahkan ke dalam wadah spray. Hasil isolat ferulat kemudian disemprotkan dengan larutan DPPH. Hasil positif sampel meredam radikal bebas yaitu berubah menjadi warna kuning.
HASIL DAN PEMBAHASAN
Preparasi Sampel dan Uji Skrinning Sampel rimpang lengkuas merah 15 kg didapatkan serbuk rimpang lengkuas merah sebanyak 1,46 kg dengan rendemen yang didapatkan 9.7%. Pada uji skrinning atau penapisan fitokimia didapatkan bahwa
serbuk rimpang lengkuas merah
mengandung senyawa alkaloid, flavonoid, saponin, steroid/triterpenoid, dan fenolik.
Pembuatan Ekstrak Etanol
Ekstrak etanol dibuat dengan mengekstraksi serbuk rimpang lengkuas merah melalui metode maserasi. Serbuk rimpang lengkuas merah dimaserasi dengan pelarut n-heksan untuk menghilangkan senyawa non polar, kemudian dimaserasi
kembali dengan pelarut etanol untuk
mengambil senyawa polar yang terkandung dalam rimpang lengkuas merah. Ekstrak
etanol pekat yang didapatkan sebanyak 113.96 gram sehingga rendemen yang diperoleh yaitu 7.85%.
Isolasi Asam Fenolat
Ekstrak etanol rimpang lengkuas merah diisolasi dalam tiga metode isolasi, yaitu hidrolisis basa, hidrolisis asam, dan tanpa hidrolisis. Untuk mengambil asam fenolat dari bentuk ester dilakukan dengan hidrolisis basa. Pada tahap ini digunakan NaOH 1N untuk mengambil asam fenolat dari bentuk ester karena gugus ester akan mengalami hidrolisis dengan NaOH dan air. Untuk membebaskan asam fenolat dari bentuk glikosida dilakukan hidrolisis asam. Pada tahap ini digunakan H2SO4 2N untuk
mengambil asam fenolat dari bentuk
glikosida. Isolasi asam fenolat dalam bentuk tanpa hidrolisis bertujuan untuk mengambil asam fenolat bebas. Dari ketiga hasil isolat tersebut didapatkan masing-masing secara berurutan yaitu 0.79 gram; 0.38 gram; 0,55 gram (sebelum dilarutkan dalam methanol).
Pemisahan Asam Fenolat
Pemisahan asam fenolat dilakukan dengan menggunakan KLT dengan fase diam, silika gel GF254 3x8 cm dan eluen
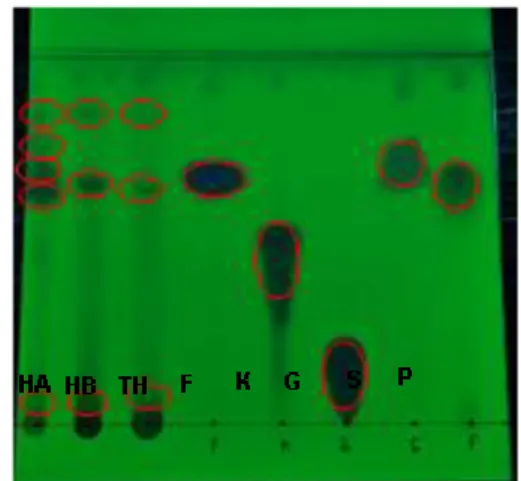
campuran etil asetat:kloroform:asam asetat (50:50:3) sebagai fase gerak. Pada tahap ini didapatkan pada fraksi HA menghasilkan 5 noda, fraksi HB 3 noda dan fraksi TH 3 noda tersaji pada Gambar 1. Hasil gambar menunjukkan bahwa ada noda pada masing-masing fraksi yang hampir dan memiliki kemiripan Rf, yang dapat disimpulkan bahwa dalam ke tiga fraksi tersebut diduga
mengandung senyawa yang sama.
Identifikasi selanjutnya dengan
membandingkan sampel dan asam fenolat standar asam kafeat, sama ferulat. Asam galat, asam salisilat, dan asam pirogalol) didapatkan bahwa dari ke tiga fraksi yang noda nodanya memiliki Rf yang sejajar sebelumnya memiliki kemiripan Rf dengan asam fenolat standar yaitu asam ferulat Rf=0,62.
Gambar 1. Hasil KLT pada fraks HA, HB dan TH.
Keterangan :
G : asam galat pembanding K : asam kafeat pembanding F : asam ferulat pembanding P : asam pirogalol pembanding S : asam salisilat pembanding HB : fraksi hidrolisis basa TH : fraksi tanpa hidrolisis HA : fraksi hidrolisis asam
Identifikasi Asam Fenolat dan TLC Scanner
Identifikasi asam fenolat dilakukan
dengan TLC Scanner pada panjang
gelombang 365 nm dan luas area sampel yang telah di KLT dan dielusi dengan fase diam silika gel dan eluen campuran etil asetat:kloroform:asam asetat (50:50:3). Dari
data TLC Scanner yang dihasilkan
menunjukkan harga Rf sampel yang
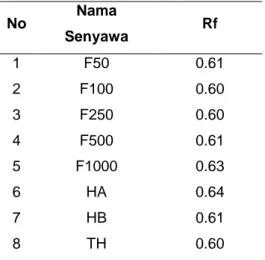
kemudian dibandingkan dengan harga Rf asam ferulat standar yang ditunjukkan dalam Tabel 1.
Tabel 1. Hasil Analisis TLC Scanner
Pada hasil tersebut dapat disimpulkan bahwa Rf asam ferulat standar memiliki kemiripan dengan salah satu Rf dari masing-masing fraksi tersebut yaitu 0.61 Sehinga dapat disimpulkan bahwa ke tiga fraksi tersebut terbukti mengandung asam ferulat. Struktur asam ferulat dapat dilihat pada gambar 2.
Gambar 2. Struktur Asam Ferulat
TLC Scanner juga dapat digunakan sebagai analisis kuantitatif (kadar dalam
senyawa tersebut). Penetapan kadar
dilakukan dengan bantan persamaan linier kurva standar yang diperoleh dari korelasi
berat senyawa dan luas area senyawa standar. Kurva korelasi kosentrasi dan area senyawa standar yaitu senyawa asama ferulat dapat dilihat pada Gambar 3. Dan didapatkan persamaan y= 5.2532x + 16296 selanjutnya digunakan untuk menentukan berat senyawa dalam setiap sampel. Dari berat senyawa tersebut dapat digunakan untuk menentukan kadar senyawa asam ferulat dari ketiga fraksi dan didapatkan masing-masing pada fraksi HA 16,25%; fraksi HB 5%; dan fraksi TH 4,9%. Dapat disimpulkan bahwa fraksi HA yang memiliki kadar asam ferulat terbesar.
Gambar 3. Grafik kurva kalibrasi asam ferulat
Aktivitas Antioksidan dengan Metode DPPH
Uji aktivitas antioksidan secara
kualitatif digunakan untuk mengetahui
kemampuan suatu senyawa atau ekstrak dalam meredam radikal bebas. Hasil penyemprotan isolat ferulat dengan DPPH
adalah positif yaitu ditandai dengan
perubahan warna pada noda KLT menjadi kuning. Hal ini sesuai dengan reaksi peredaman radikal bebas pada senyawa DPPH oleh molekul pendonor H dari suatu senyawa dapat disajikan pada gambar 4.
No Nama Senyawa Rf 1 F50 0.61 2 F100 0.60 3 F250 0.60 4 F500 0.61 5 F1000 0.63 6 HA 0.64 7 HB 0.61 8 TH 0.60
KESIMPULAN
Dari hasil analisis TLC dan TLC Scanner terhadap fraksi HA, HB dan TH diduga mengandung senyawa asam ferulat. Kadar asam ferulat didapatkan dari ketiga fraksi tersebut yaitu fraksi HA 16,25%; HB 5%; dan TH 4.9%. Uji aktivitas antioksidan secara kualitatif terbukti positif isolat ferulat mampu meredam radikal bebas.
UCAPAN TERIMA KASIH
Atas selesainya penelitian ini ucapan terimakasih disampaikan kepada
Dosen-dosen Departemen Kimia FSM
Universitas Diponegoro khususnya bidang Kimia Organik atas bimbingan dan arahan selama penelitian ini berlangsung, serta teman-teman riset Laboratorium Organik atas semangat dan dukungan sehingga penelitian ini dapat terlaksana dengsn lancar.
DAFTAR RUJUKAN
[1] Wei, E., Chan, C., & Wong, S. K. (2015). Review Phytochemistry and pharmacology of ornamental gingers
, Hedychium coronarium and Alpinia purpurata : a review. Journal of Integrative Medicine, 13(6), 368– 379. http://doi.org/10.1016/S2095-4964(15)60208-4
[2] Raj, C. A., Ragavendran, P., Sophia, D., Rathi, M. A., & Gopalakrishnan, V. K. (2012). Evaluation of in vitro antioxidant and anticancer activity of Alpinia purpurata. Chinese Journal of Natural Medicines, 10(4), 263–268.
http://doi.org/10.1016/S1875-5364(12)60053-3
[3] Hezmela, R. 2006. Daya Antijamur Ekstrak Lengkuas Merah (Alpinia purpurata K. Schum) dalam Sediaan Shampo. Skripsi. TIN. FATETA. IPB. Bogor.
[4] Screening, P., Vieill, P.,
Subramanian, V., & Suja, S. (2011). Phytochemical Screening of Alpinia Purpurata (Vieill). Research Journal of Pharmaceutical, Biological and Chemical Sciences Phytochemical, 2(3), 866–871.
[5] Darwis, S.N., M. Indo dan S.
Hasiyah. 1991. Tumbuhan Obat
Famili Zingiberaceae. Pusat
Penelitian dan Pengembangan
Tanaman Industri. Bogor.
[6] Nampoothiri, S. V, Esakkidurai, T., & Pitchumani, K. (2015). Identification and Quantification of Phenolic Compounds in Alpinia galanga and Alpinia calcarata and its Relation to Free Radical Quenching Properties : A Comparative Study. Journal of Herbs, Spices & Medicinal Plants,
(Ungu) (Kuning)
Gambar 4. Mekanisme peredaman radikal bebas (Molyneux, 2004)
N N NO2 NO2 O2N N N NO2 NO2 O2N
1,1-dif enil-2-pikrilhidrazil (radikal bebas) 1,1-dif enil-2-pikrilhidrazin (bukan radikal)
Pendonor atom H
21(2), 140–147.
http://doi.org/10.1080/10496475.201 4.923358
[7] Orak, H.H, 2006, EJPAU., 9.
[8] Zademowski, R., Naczk, M.,
Czaplicki, S., Rubinskiene, M., dan Sza ‘Ikiewicz M., 2005 JAOCS; 8,3.
[9] Molyneux, P., 2004, The Use of the
Stable Free Radical
Diphenylpicrylhydrazyl (DPPH) for Estimating Antioxidant Activity, J. Sci. Technol., 26, 211-219