Empulur Sagu
Tanaman sagu termasuk tumbuhan monokotil dari famili Palmae, sub famili Calamoideae, genus Metroxylon, spesies Eumetroxylon. Tanaman ini banyak ditemukan di hutan hujan dan toleran terhadap pH tanah yang asam dan mengandung unsur Al, Fe dan Mn yang tinggi. Fase vegetatif tanaman ini berada pada 7-15 tahun setelah penanaman dan selama masa inilah pati diakumulasi pada batang. Pati sagu akan maksimum pada saat sebelum tahap berbuah (10-13 tahun setelah penanaman). Ukuran dari batang sagu dan kandungan patinya bergantung pada jenis sagu, umur dan habitat pertumbuhannya.
Sagu (Metroxylon sp.) dikenal sebagai tanaman penghasil karbohidrat. Sebagai sumber karbohidrat, tanaman sagu memiliki keunggulan dibandingkan dengan tanaman penghasil karbohidrat lain karena relatif sudah tersedia lahan yang telah ditanami sehingga dapat langsung dimanfaatkan, berkembang biak dengan anakan sehingga panen dapat berkelanjutan tanpa melakukan peremajaan ataupun penanaman ulang, dapat dipanen dan diolah tanpa musim, resiko terkena hama penyakit tanaman kecil, dan tingkat pemanfaatannya masih sedikit (Bustaman 2008).
Areal sagu Indonesia sangat luas yaitu sekitar 1,128 juta ha (Bustaman 2008). Setiap satu batang pohon sagu rata-rata mengandung 200-400 kg pati sagu (Safitri et al. 2009). Pati sagu diisolasi dari batang sagu. Batang sagu bagian dalam disebut empulur. Pada saat ekstraksi, empulur sagu yang digunakan harus segar dan segera diproses, karena jika ditunda akan mengakibatkan pati menjadi kecoklatan akibat aktivitas enzim katalisis reaksi oksidasi senyawa polifenol menjadi kuinon (Onsa et al. 2000).
Empulur sagu kering didominasi pati (81.51-84.72%) dan serat (3.20-4.20%). Bagian tengah batang sagu mengandung pati lebih tinggi dibandingkan bagian luar (Tabel 1). Batang sagu yang diekstraksi patinya akan menyisakan ampas sebagai limbah. Konversi langsung empulur sagu menjadi glukosa akan menghemat penggunaan air dan energi untuk ekstraksi dan pengeringan pati, sekaligus sebagai salah satu cara pemanfaatan limbah.
Tabel 1. Komposisi empulur sagu kering Empulur Utuh (%) Bagian Luar (%) Bagian Tengah (%) Bagian dalam (%) Pati 83.50 81.51 83.20 84.72 Lemak Kasar 0.38 0.49 0.38 0.31 Serat Kasar 3.32 4.20 3.33 3.20 Abu 3.80 4.00 3.50 3.20 Protein 1.15 1.76 1.27 1.06 Pentosan 2.87 Asam organik (sebagai asam malat)
1.02
Air 9.79 12.03 12.74 12.67
Sumber : Fujii et al. (1986), data dalam % basis kering, kecuali kadar air
Pati
Pati sagu umumnya berwarna putih, bersifat tidak larut dalam air, tidak berasa dan tidak berbau. Granula pati sagu berbentuk elips agak terpotong, permukaannya datar, dan berukuran 15-65 μm. Granula pati terdiri atas bagian kristalin yang dibentuk oleh amilopektin dan amilosa, serta daerah amorf yang mengandung titik percabangan dari amilopektin (Zhang et al. 2006), yang ditunjukkan oleh Gambar 1.
Gambar 1 Struktur granula pati
Pati mengandung dua komponen utama yaitu 20%-30% amilosa dan 70%-80% amilopektin, yang keduanya merupakan polimer dengan konformasi glukosa pada 4C1. Pati merupakan homopolimer glukosa dengan ikatan α-glikosidik. Pati terdiri atas dua fraksi yang dapat dipisahkan dengan air panas, fraksi terlarut disebut amilosa dan fraksi tidak terlarut disebut amilopektin. Tabel 2 berikut adalah karakteristik dari amilosa dan amilopektin.
Daerah kristalin Daerah amorf
Tabel 2 Karakteristik amilosa dan amilopektin
Karakteristik Amilosa Amilopektin
Struktur dasar Linear Bercabang
Stabilitas dalam larutan Retrodegradasi Stabil
Derajat polimerisasi 103 104-10
Panjang rantai rata-rata
5
103 20-25
Hidrolisis oleh β-amilase 87% 54%
λmaks kompleks iodin 650 nm 550 nm
Sumber: Aiyer (2005)
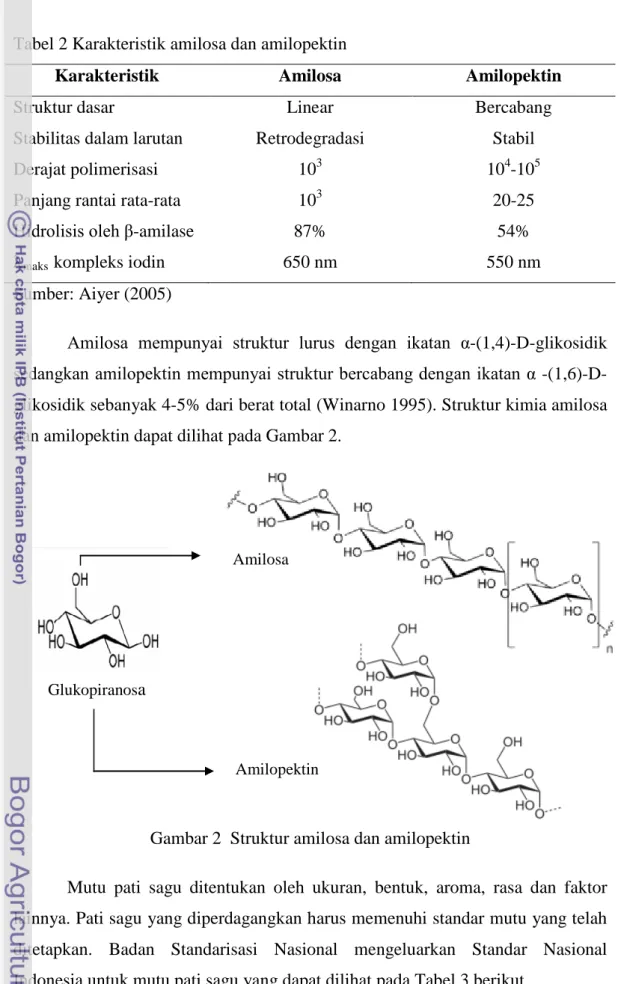
Amilosa mempunyai struktur lurus dengan ikatan α-(1,4)-D-glikosidik sedangkan amilopektin mempunyai struktur bercabang dengan ikatan α -(1,6)-D-glikosidik sebanyak 4-5% dari berat total (Winarno 1995). Struktur kimia amilosa dan amilopektin dapat dilihat pada Gambar 2.
Gambar 2 Struktur amilosa dan amilopektin
Mutu pati sagu ditentukan oleh ukuran, bentuk, aroma, rasa dan faktor lainnya. Pati sagu yang diperdagangkan harus memenuhi standar mutu yang telah ditetapkan. Badan Standarisasi Nasional mengeluarkan Standar Nasional Indonesia untuk mutu pati sagu yang dapat dilihat pada Tabel 3 berikut.
Glukopiranosa
Amilosa
Tabel 3 Standar mutu pati sagu (SNI 01-3729-1995)
Karakteristik Kriteria
Kadar air (% b/b) Maks. 13
Kadar abu (% b/b) Maks. 0.5
Kadar serat kasar (% b/b) Maks. 0.11
Derajat asam (ml NaOH 1N/100g) Maks. 4
Kadar SO2 (mg/kg) Maks. 30
Kehalusan (lolos ayakan 100 mesh) % b/b Min. 95
Total Plate Count (koloni/g) Maks. 10
Jenis pati lain selain pati sagu
6 Tidak boleh ada Sumber: Dewan Standarisasi Nasional (1995)
Lignoselulosa
Komponen lain dari empulur sagu yaitu serat (selulosa, hemiselulosa, dan lignin). Selulosa merupakan polimer glukosa yang membentuk rantai linier dan dihubungkan oleh ikatan β-1,4-glikosidik. Struktur linier ini menyebabkan selulosa bersifat kristalin. Molekul-molekul selulosa memiliki kecenderungan membentuk ikatan hidrogen intramolekul dan intermolekul. Hidrolisis sempurna selulosa menghasilkan glukosa, sedangkan hidrolisis tidak sempurna menghasilkan selobiosa dan oligosakarida. Struktur selulosa dapat dilihat pada Gambar 3.
Gambar 3 Struktur selulosa
Hemiselulosa merupakan rantai polimer bercabang dari berbagai jenis monomer gula-gula anhidro yang dapat dikelompokkan berdasarkan penyusunnya, yaitu heksosa (glukosa, mannosa, galaktosa), pentosa (xilosa, arabinopiranosa, arabinofuranosa), asam heksuronat (glukoronat, metil glukoronat, galakturonat) dan deoksi heksosa (rhamnosa dan fruktosa). Struktur hemiselulosa berupa rantai bercabang, amorf, dengan ikatan yang lebih lemah dan
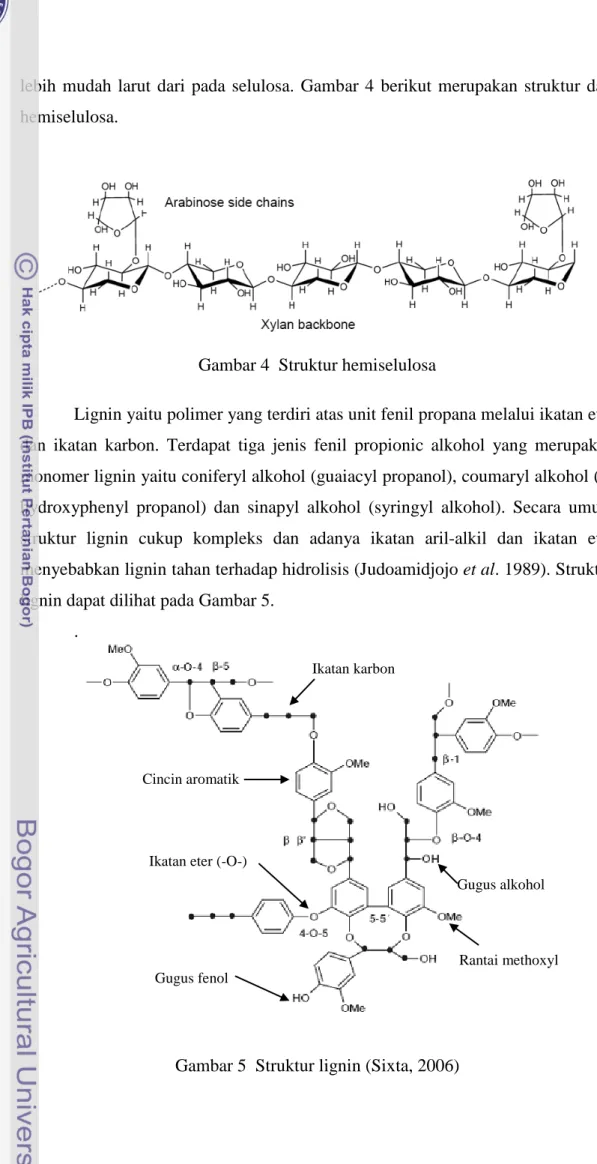
lebih mudah larut dari pada selulosa. Gambar 4 berikut merupakan struktur dari hemiselulosa.
Gambar 4 Struktur hemiselulosa
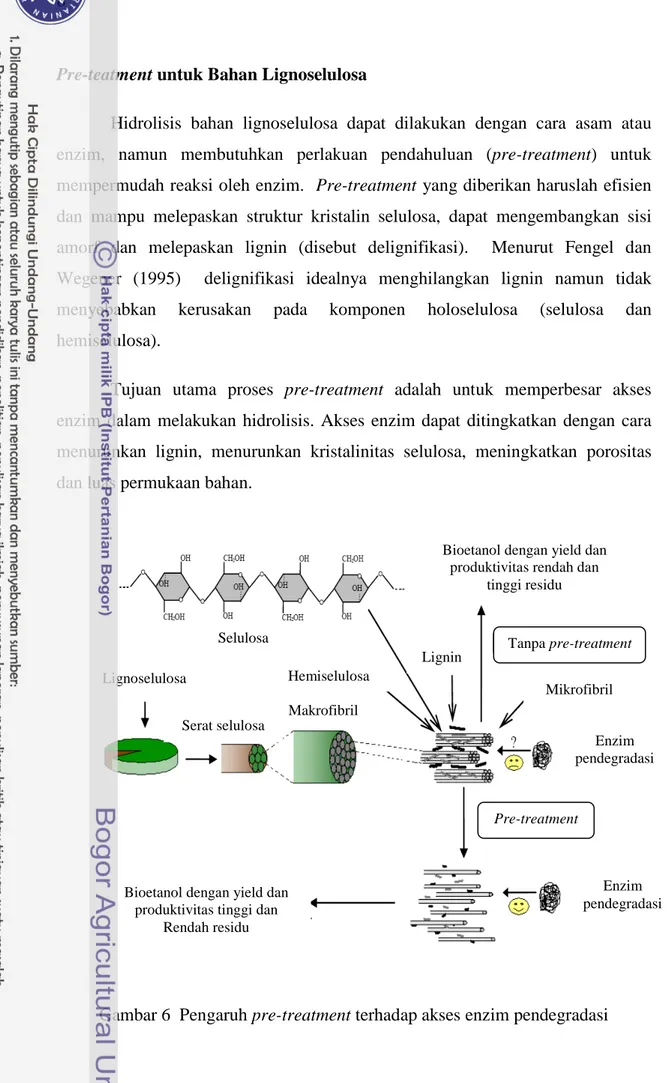
Lignin yaitu polimer yang terdiri atas unit fenil propana melalui ikatan eter dan ikatan karbon. Terdapat tiga jenis fenil propionic alkohol yang merupakan monomer lignin yaitu coniferyl alkohol (guaiacyl propanol), coumaryl alkohol (p-hydroxyphenyl propanol) dan sinapyl alkohol (syringyl alkohol). Secara umum struktur lignin cukup kompleks dan adanya ikatan aril-alkil dan ikatan eter menyebabkan lignin tahan terhadap hidrolisis (Judoamidjojo et al. 1989). Struktur lignin dapat dilihat pada Gambar 5.
.
Gambar 5 Struktur lignin (Sixta, 2006)
Rantai methoxyl Gugus fenol
Cincin aromatik
Gugus alkohol Ikatan eter (-O-)
Pre-teatment untuk Bahan Lignoselulosa
Hidrolisis bahan lignoselulosa dapat dilakukan dengan cara asam atau enzim, namun membutuhkan perlakuan pendahuluan (pre-treatment) untuk mempermudah reaksi oleh enzim. Pre-treatment yang diberikan haruslah efisien dan mampu melepaskan struktur kristalin selulosa, dapat mengembangkan sisi amorf dan melepaskan lignin (disebut delignifikasi). Menurut Fengel dan Wegener (1995) delignifikasi idealnya menghilangkan lignin namun tidak menyebabkan kerusakan pada komponen holoselulosa (selulosa dan hemiselulosa).
Tujuan utama proses pre-treatment adalah untuk memperbesar akses enzim dalam melakukan hidrolisis. Akses enzim dapat ditingkatkan dengan cara menurunkan lignin, menurunkan kristalinitas selulosa, meningkatkan porositas dan luas permukaan bahan.
Gambar 6 Pengaruh pre-treatment terhadap akses enzim pendegradasi
Bioetanol dengan yield dan produktivitas rendah dan
tinggi residu
Bioetanol dengan yield dan produktivitas tinggi dan
Rendah residu Enzim pendegradasi Tanpa pre-treatment Pre-treatment Lignoselulosa Serat selulosa Hemiselulosa Makrofibril Lignin Mikrofibril Enzim pendegradasi Selulosa
Sejumlah reaksi heterogen terjadi pada hidrolisis menggunakan asam pada konsentrasi rendah dan menyebabkan terbentuknya “hydrocellulose”, yaitu produk dengan derajat polimerisasi yang rendah namun kristalinitas yang lebih tinggi. Hidrolisis selulosa sangat dipengaruhi oleh derajat kristalinitas dan bentuk swelling selulosa. Kinetika hidrolisis selulosa secara asam sangat tergantung pada ikatan hidrogen, sehingga sangat berguna untuk memungkinkan terjadinya proses sakarifikasi biomassa. Contoh yang diberi perlakuan asam 65% mampu mengubah bentuk serat selulosa menjadi selulosa berbentuk seperti gel (Xiang et al. 2003).
Proses pre-treament dapat dilakukan melalui beberapa metode yaitu secara fisik, kimia atau fisiko kimia, dan biologis. Tabel 4 memperlihatkan metode pre-treatment dan bentuk biomassa setelah mengalami proses perlakuan pendahuluan.
Tabel 4 Pengaruh pre-treatment terhadap bentuk biomassa
Metode Proses Perubahan pada biomassa
Fisik Penggilingan Iradiasi
Lainnya seperti hidrotermal,
penggunaan tekanan tinggi dan pirolisis.
Transformasi struktur lignin Meningkatkan porositas dan luas
permukaan bahan
Menurunkan kristalinitas selulosa Menurunkan derajat polimerisasi Kimia dan fisiko-kimia Explosion Alkali Asam Gas Agen oksidasi Ekstraksi pelarut
Meningkatkan luas permukaan bahan
Delignifikasi parsial atau hampir lengkap
Menurunkan kristalinitas selulosa Menurunkan derajat polimerisasi Hidrolisis hemiselulosa parsial
atau lengkap Biologis Fungi dan Aktinomiset Delignifikasi
Mereduksi derajat polimerisasi selulosa
Hidrolisis hemiselulosa secara parsial
Sumber: Taherzadeh dan Karimi (2008)
Iradiasi Gelombang Mikro
Gelombang mikro merupakan gelombang elektromagnetik yang berada pada daerah antara infrared dan frekuensi radio. Daerahnya antara 300 MHz – 30
GHz. Microwave domestik dan industrial dioperasikan pada 900 MHz – 2,45 GHz. Jantung dari microwave disebut dengan megatron yang akan menghasilkan radiasi listrik. Pada frekuensi 2,45 GHz, energi foton yang dibawa microwave sekitar 1 joule per mol. Jika bahan yang mengandung molekul polar dan ion diradiasi oleh microwave maka radiasi ini akan mepercepat proses kimia, biologi, dan fisik (Sridar 1998). Keuntungan menggunakan microwave yaitu energi yang dibutuhkan rendah, prosesnya beragam dan selektif, dapat bekerja secara otomatis dan waktu yang dibutuhkan relatif singkat (Datta 2001).
Iradiasi microwave pada bahan akan menyebabkan dua efek yaitu efek termal dan non termal. Efek termal yaitu dengan mempercepat pemanasan dan efek non termal dengan mengintensifkan tumbukan antar partikel yang selanjutnya akan mempengaruhi laju reaksi (Keshwani 2009).
Peran Iradiasi Microwave terhadap Degradasi Pati dan Lignoselulosa
Penelitian tentang penggunaan pemanasan microwave untuk degradasi pati telah digunakan untuk bahan seperti gandum, beras, kentang dan jagung, baik dalam larutan air maupun asam. Kebanyakan kajian menggunakan microwave oven 2450 MHz. Konsentrasi pati bervariasi antara 1-50%, namun umumnya 10% pati (Yu et al. 1996 dan Kunlan et al. 2001), sedangkan pada konsentrasi yang lebih tinggi telah dilakukan oleh Khan et al. (1979), Palav dan Seetharaman (2006) dan Nikolic et al. (2008). Hanya sedikit peneliti yang mencantumkan suhu seperti Yu et al. (1996) dan Tsubaki et al. (2009). Sebagian besar hanya mencantumkan derajat power yang digunakan atau persentase dari power (Kunlan et al. 2001, Palav dan Seetharaman 2006, Nikolic et al. 2008).
Tsubaki et al. (2009) melaporkan proses pelarutan pati pada suhu tinggi, sebagian besar pati larut pada suhu 200 sampai 220 oC namun diikuti oleh dekomposisi produk menjadi produk sekunder yang memberi warna kegelapan. Waktu terlama yang telah digunakan adalah 10 menit, namun proses hidrolisis pati berjalan sempurna kurang dari 10 menit. Perlakuan pemanasan pati dengan microwave dapat menggunakan air atau asam pada konsentrasi rendah, baik HCl atau H2SO4. Namun Kunlan et al. (2001) telah melaporkan penambahan garam yang mengandung ion Cl dan SO4 dapat meningkatkan laju hidrolisis pati.
Enzim Hidrolisis
Proses hidrolisis dapat dilakukan menggunakan asam maupun secara enzimatis. Hidrolisis asam akan menghasilkan etanol dengan yield yang rendah menimbulkan masalah korosi dan menghasilkan produk samping yang dapat menghambat proses fermentasi (Safitri et al. 2009). Hidrolisis enzimatis bersifat spesifik dan ramah lingkungan. Enzim yang digunakan untuk hidrolisis pati yaitu enzim amilolitik sedangkan selulosa dihidrolisis oleh selulolitik dan hemiselulosa oleh xilanolitik.
Enzim amilolitik bekerja menghidrolisis polisakarida (pati) menjadi gula-gula sederhana. Enzim amilolitik yang digunakan untuk mendegradasi pati adalah α-amilase yang akan memecah pati menjadi maltosa. Enzim ini bekerja memutus ikatan α-(1,4)-glikosidik pada amilosa, amilopektin dan glikogen. Ikatan α-(1,6)-glikosidik tidak dapat diputus oleh α-amilase namun dapat dibuat menjadi cabang-cabang yang lebih pendek (Dordick 1991). Amiloglukosidase juga merupakan enzim amilolitik yang bekerja memecah ikatan α-(1,4), α-(1,6), α-(1,3), α-(1,2), dan (1,1) glikosidik. Enzim ini bekerja lebih lambat dibandingkan enzim α-amilase.
Enzim selulolitik bekerja mengkonversi selulosa menjadi glukosa. Enzim ini terdiri atas kompleks endo-β-1,4-glukanase, kompleks ekso- β-1,4-glukanase, dan β-1,4-glukosidase. Enzim ini dapat mengkonversi selulosa menjadi glukosa. Enzim xilanolitik terdiri dari kompleks 1,4-β-endoxilanase, β-xilosidase, α-L-arabionofuronase, α-glukoronidase, asetil xilan esterase dan asam fenolat. Enzim ini bekerja mengkonversi xilan menjadi xilosa.
Tabel 5. Karakteristik Enzim Selulolitik dan Xilanolitik dari Isolat Lokal Karakterisitk
Enzim
Selulase1) Xilanase2)
Mikroorganisme Bakteri Isolat J Streptomyces 234-P16
Suhu optimum (oC) 60 90
pH optimum 6.5 5.0
Waktu optimum (hari) 7 5
Aktivitas puncak (U/ml) 0.057 0.27
Bioetanol
Etanol (etil alkohol) merupakan cairan yang mudah menguap, mudah terbakar, tak berwarna, memiliki bau khas alkohol, dan merupakan alkohol yang paling sering digunakan dalam kehidupan sehari-hari. Etanol termasuk ke dalam alkohol rantai tunggal, dengan rumus kimia C2H5OH dan rumus empiris C2H6O dengan berat molekul 46,07 g/mol. Etanol dapat dibuat dari bahan nabati yang mengandung gula, pati atau lignoselulosa yang dikenal dengan istilah bioetanol.
Bioetanol dapat diproduksi melalui proses fermentasi oleh khamir. Khamir merupakan jamur bersel satu yang bersifat mikroskopis, tidak memiliki flagel, tetapi ada beberapa yang membentuk filamen, bersifat saprofit dan parasit. Khamir tumbuh baik pada kondisi aerobik, walaupun demikian beberapa khamir dapat tumbuh pada kondisi anaerobik. Khamir dapat tumbuh dan memfermentasi gula menjadi etanol pada pH 3.5-6.0 dan suhu 28-35 oC. Fermentasi etanol memerlukan waktu 30-72 jam dengan suhu optimum untuk fermentasi antara 25-30 o
Khamir akan mengubah gula sederhana menjadi etanol melalui jalur Embden Meyerhoff-Parnas (EMP). EMP mengubah glukosa menjadi asam piruvat melalui reaksi oksidasi-reduksi. Asam piruvat yang dihasilkan kemudian didekarboksilasi menjadi asetaldehida lalu mengalami dehidrogenasi sehingga terkonversi menjadi etanol.
C, dan kadar gula berkisar antara 10-18% (Paturau 1969).
Bioetanol dapat diproduksi dari berbagai biomassa hasil pertanian, namun secara tradisional bahan hasil pertanian yang digunakan adalah yang mengandung gula dan pati. Gula sederhana dapat langsung digunakan oleh khamir, sedangkan pati dapat dengan mudah dikonversi dahulu menjadi glukosa oleh enzim atau asam, kemudian difermentasi oleh khamir menjadi etanol. Varga et al. (2004) memproduksi etanol dari jagung, limbah jagung dan tongkol jagung dan memperlihatkan kemampuan Saccharomyces cerevisiae dalam menggunakan fraksi hemiselulosa sebagai sumber karbon untuk fermentasi etanol.