Pemisahan Ion Kromium (VI) dan Nikel dari Limbah Industri
Elektroplating dengan Proses Reverse Osmosis
Aisyah Endah Palupi
Jurusan Teknik Mesin, Fakultas Teknik, Universitas Negeri Surabaya Kampus Ketintang - Surabaya 60231
Telp. (031)82998487; Fax. (031)8292957 Email: [email protected]
Abstrak
Salah satu tahapan dari industri elektroplating adalah pembilasan, dimana pada tahap tersebut menghasilkan limbah cair yang mempunyai kandungan kromium hexavalent dan nikel yang berbahaya, beracun, dan bersifat karsinogenik. Makalah ini berisikan tentang penyisihan kromium hexavalent dan nikel menggunakan teknologi reverse osmosis. Operasi pemisahan dilakukan secara batch pada suhu kamar. Pengaruh tekanan operasi dan % recovery terhadap laju alir, TDS, dan turbiditas permeate RO dipelajari dalam penelitian ini. Reverse osmosis diobservasi sebagai proses yang paling efektif dalam penyisihan kromium hexavalent dan nikel. Dari pembelajaran dapat diketahui bahwa terjadi perubahan laju alir permeate RO pada berbagai tekanan, perubahan TDS umpan dan permeate. Pada penelitian ini dapat disimpulkan bahwa kemampuan rejeksi membran reverse osmosis dari total kromium dan nikel adalah sebesar 100 %.
Kata kunci : hexavalent kromium, nikel, elektroplating, reverse osmosis
Pendahuluan
Dalam beberapa tahun belakangan ini, kewaspadaan publik terhadap pengaruh ion logam berat yang terlarut dalam air atau limbah semakin meningkat [1]. Logam berat seperti kromium, kadmium, timah dan nikel yang terkandung dalam limbah cair industri elektroplating dapat menghasilkan polusi lingkungan dan mempunyai pengaruh negatif pada kesehatan manusia [2]. Kromium di lingkungan ditemukan dalam bentuk Cr (III) dan Cr (VI). Ion Cr (VI) mempunyai kelarutan yang sangat tinggi dalam air [3]. Para pekerja dalam industri elektroplating mempunyai resiko tinggi terkena kanker paru-paru jika terkena Cr (VI) [4]. Dalam larutan, Cr (VI) dapat menyebabkan iritasi mata, tenggorokan, dan hidung. Sebaliknya ion Cr (III) mempunyai toksisitas yang relatif rendah dan cenderung berada dalam bentuk kompleks dengan hidroksida yang tidak larut pada pH netral [3]. Sejak detoksifikasi alami tidak dapat merubah secara sempurna ion Cr (VI) menjadi Cr (III), maka perlu dilakukan pengontrolan terhadap limbah hasil elektroplating [3].
Ion nikel yang terdapat dalam limbah elektroplating dapat menyebabkan kanker paru-paru dan kanker sinus-nasal pada pekerja [4]. Nikel juga mempunyai potensi menyebabkan iritasi pada kulit yang sensitif [4].
Elektroplating atau lapis listrik atau penyepuhan merupakan deposisi lapisan tipis pelindung (biasanya logam) ke dalam permukaan logam yang telah dipersiapkan menggunakan proses elektrokimia [5]. Benda yang dikenai pelapisan harus merupakan konduktor [6]. Proses elektroplating terdiri dari pretreatment (pencucian,
degreasing, dll), pelapisan, pembilasan, passivating, dan pengeringan. Dalam proses elektroplating, objek yang akan dilapisi biasanya digunakan sebagai katoda pada tangki elektrolit [5]. Jenis larutan elektrolit yang sering digunakan adalah asam, basa, dan ion kompleks seperti sianida. Skematik sel elektroplating dapat dilihat pada Gambar 1. Pelapisan nikel dan kromium secara umum bertujuan untuk membuat benda mempunyai permukaan yang lebih keras, mengkilap dan tahan terhadap korosi-karat [4]. Jasa plating krom pada kendaraan bermotor dan mobil dilakukan untuk skala kecil dan menengah. Skala industri besar dilakukan untuk sektor produksi seperti kursi, suku cadang kendaraan bermotor dan mobil, dan lain-lain [6].
Suatu industri elektroplating di Purbalingga mengalami kesulitan dalam mengolah limbah yang mengandung kromium dan nikel. Teknik pengolahan limbah konvensional seperti presipitasi dan filtrasi akan menghasilkan limbah padat, sedangkan proses elektrokimia juga digunakan untuk penyisihan logam berat tetapi efisiensinya kurang dan tidak ekonomis. Pada masa lalu, aplikasi Reverse Osmosis dalam industri elektroplating terbatas [7]. Teknik separasi RO menawarkan lingkup dan potensial yang tinggi, seperti kemudahan operasional, kebutuhan energi yang lebih sedikit dan selektifitas yang tinggi [8].
Reverse Osmosis merupakan teknik pemisahan air dari larutan dengan mendorong larutan melalui membran semipermeabel menggunakan tekanan. Aliran produk murni membran disebut permeate dan aliran pekat yang mengandung konsentrasi garam terlarut yang tinggi disebut konsentrat. Sistim membran RO cross-flow filtration membiarkan aliran konsentrat menyapu molekul yang tertahan dan untuk mencegah permukaan membran dari clogging atau fouling [7]. Membran RO merupakan penghalang semua garam terlarut dan molekul anorganik/organik dengan berat molekul >100. Garam terlarut tertahan 95% hingga lebih dari 99% [9]. RO digunakan dalam industri elektroplating untuk penyisihan logam berat sekaligus untuk pemurnian air [10].
Berdasarkan Peraturan Pemerintah Indonesia no.18 Tahun 1999, limbah elektroplating yang mengandung ion kromium dan nikel adalah termasuk kategori limbah bahan berbahaya dan beracun (B3) [11]. Dalam penelitian ini dipelajari pengaruh tekanan dan % recovery terhadap laju alir permeate dan total dissolved solid (TDS) pada limbah elektroplating selama proses reverse osmosis, sehingga dapat memenuhi syarat baku mutu limbah keluaran elektroplating dari pemerintah Indonesia.
Gambar 1. Skematik Sel Elektroplating
Gambar 2. Reverse Osmosis Cross-flow Filtration
Eksperimental Bahan
Umpan asli yang digunakan adalah 10 L limbah cair elektroplating yang mengandung nikel dan kromium hexavalent. Larutan HCl dan NaOH digunakan untuk pengasaman dan penetralan. Tahap reduksi menggunakan larutan sodium bisulfite (NaHSO3).
Tabel 1. Karakterisasi Limbah Elektroplating
Sifat Nilai
pH 6,9
Cr6+, ppm 16,0298
Ni, ppm 0,9874
TDS, ppm 197
Warna Kuning terang
Eksperimen
Penyisihan ion kromium hexavalent dan nikel dari limbah elektroplating melalui 4 tahap, yaitu : Mo Mn+ (+) (-) Sumber Arus DC Larutan elektrolit PERMEATE PERMEATE KONSENTRAT UMPAN BERTEKANAN Membran
Tahap reduksi (tahap 1).
Proses reduksi dimaksudkan untuk mengubah Cr (VI) menjadi Cr (III). Larutan yang digunakan untuk mereduksi adalah sodium bisulfite (NaHSO3) menurut reaksi berikut :
Cr6+ + 3e Cr3+
Tahap reduksi bisa berlangsung pada kisaran pH 2-3 dengan penambahan larutan HCl.
Tahap penetralan (tahap 2).
Tahap penetralan dilakukan dengan penambahan larutan NaOH sampai pH 8,5 untuk menghasilkan endapan kromium (III) hidroksida Cr(OH)3 dan nikel hidroksida Ni(OH)2 yang tidak beracun.
Cr3+ + NaOH Cr(OH)3 Ni2+ + NaOH Ni(OH)2 Tahap ultrafiltrasi (tahap 3).
Larutan hasil penetralan merupakan umpan membran ultrafiltrasi. Tahap ultrafiltrasi dimaksudkan untuk meningkatkan efisiensi dan umur dari sistim membran reverse osmosis. Pemilihan ultrafiltrasi akan memaksimalkan efisiensi dan umur membran dengan meminimalkan fouling, kerak, dan degradasi membran.
Tahap reverse osmosis (tahap 4).
Permeate membran ultrafiltrasi diumpankan ke dalam membran reverse osmosis. Penelitian dilakukan pada tekanan 3 dan 5 bar. Operasi reverse osmosis dilakukan dengan mengembalikan aliran konsentrat ke dalam tangki umpan. Setiap penambahan recovery 10 % dilakukan pengukuran laju alir permeate, TDS, dan COD.
Gambar 3. Skema Tahapan Penelitian Analisa
Analisa laboratorium yang diberikan pada akhir proses adalah sebagai berikut : Total Dissolved Solid (TDS)
Pengukuran TDS dilakukan dengan menggunakan alat TDS meter (TDS-3 HM Digital).
Konsentrasi nikel dan total kromium
Konsentrasi nikel dan total kromium dalam sampel dianalisa dengan menggunakan AAS.
NaHSO3
HCl
NaHSO3 NaOH
1 2 3 4
Tahap Reduksi, pH 2-3 Tahap Netralisasi, pH 8,5 Ultrafiltrasi Reverse osmosis
1 4 3 2 Retentat Permeat Keterangan : 1. Tangki feed 2. Pompa 3. Modul membran 4. Tangki umpan Feed
Chemical Oxygen Demand (COD)
COD digunakan sebagai pengukuran oksigen yang ekuivalen dengan kandungan organik dari sampel yang rentan terhadap oksidasi oleh oksidan kimia kuat. Metode yang digunakan dalam analisa ini adalah Standard Methode.
Gambar 4. Rangkaian Alat
Hasil dan Pembahasan Laju Alir Permeate.
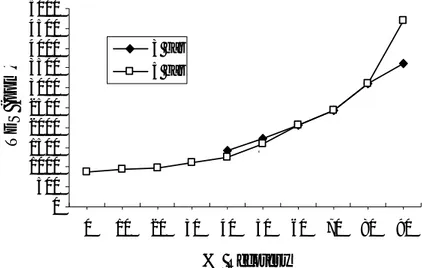
Penelitian dilakukan dengan mengumpankan limbah elektroplating dari tahap 3 menuju membran reverse osmosis. Pengukuran laju alir dilakukan setiap penambahan 10 % recovery. Tekanan diaplikasikan untuk mendorong larutan, air, dan molekul lain yang mempunyai berat molekul rendah untuk dapat melewati membran mikropori RO [7]. Pengaruh tekanan operasi dan % recovery terhadap laju umpan telah dipelajari dalam penelitian ini. Hasil tersebut diperlihatkan oleh gambar 5.
Pada % recovery yang sama, laju alir permeate tekanan 3 bar lebih kecil dibandingkan laju alir permeate tekanan 5 bar. Tekanan yang lebih tinggi menyebabkan suatu larutan mempunyai kemampuan yang lebih untuk melewati membran sebagai permeate sehingga laju alir permeate juga semakin besar.
0 2 4 6 8 10 12 14 0 10 20 30 40 50 60 70 80 90 % Recovery J ( L /j a m ) 3 bar 5 bar
Pada tekanan yang sama setiap kenaikan 10 % recovery, maka laju alir permeate menurun dan suatu saat akan berhenti pada nilai dimana tekanan osmotik konsentrat mempunyai nilai yang sama dengan tekanan umpan [9]. Didalam sistim membran, umpan limbah elektroplating akan terpisah menjadi dua aliran yaitu aliran produk murni atau permeate dan aliran garam konsentrasi tinggi atau konsentrat. Aliran konsentrat yang dikembalikan ke dalam umpan akan menaikkan konsentrasi garam dalam umpan. Dengan menggunakan daya dorong yang sama kemampuan rejeksi garam membran menurun sehingga laju alir permeate menurun [9].
Pada akhir operasi, penurunan laju alir permeate signifikan. Konsentrasi garam yang sangat tinggi dalam umpan menyebabkan kemampuan larutan untuk melewati membran menjadi sangat rendah dengan menggunakan daya dorong yang sama.
Konsentrasi Garam Terlarut
Penelitian ini dilakukan dengan mengumpankan limbah elektroplating dari tahap ultrafiltrasi menuju membran reverse osmosis. Pengukuran TDS umpan dan permeate dilakukan setiap kenaikan 10 % recovery.
Dalam sistim membran RO, proses pemisahan didasarkan pada perbedaan ukuran partikel. Reverse osmosis dapat digunakan untuk memisahkan solute dengan berat molekul rendah seperti ion dan garam terpisah dari solventnya [10].
Pengaruh perubahan tekanan operasi terhadap TDS umpan RO dapat dilihat pada gambar 6. Pada tekanan yang sama, konsentrasi garam dalam umpan semakin tinggi seiring bertambahnya % recovery umpan. Aliran konsentrat yang dikembalikan ke dalam umpan akan menaikkan konsentrasi garam dalam umpan.
Pada % recovery yang sama, konsentrasi garam dalam umpan untuk tekanan 5 bar lebih besar dibandingkan dengan tekanan 3 bar. Tekanan yang lebih tinggi menyebabkan kemampuan umpan untuk melewati membran semakin besar, garam yang tertahan di permukaan membran semakin banyak sehingga kandungan garam dalam konsentrat yang dimasukkan kembali ke dalam umpan semakin besar. Laju ion menembus membran dapat menyeimbangi perpindahan ion dan garam membran akibat tekanan operasi.
0 500 1000 1500 2000 2500 3000 3500 4000 4500 5000 0 10 20 30 40 50 60 70 80 90 % Recovery T DS ( p p m ) 3 bar 5 bar
Gambar 6. Pengaruh Perubahan Tekanan Operasi dan Faktor Recovery Terhadap TDS Umpan RO
Gambar 7 merupakan grafik pengaruh tekanan operasi terhadap TDS permeate RO. Pada % recovery yang sama, konsentrasi garam dalam permeate semakin naik. Selama proses reverse osmosis berlangsung, konsentrasi garam dalam umpan semakin tinggi. Dengan kemampuan rejeksi garam yang sama rata-rata sebesar 93,4 % maka konsentrasi garam yang lolos ke dalam aliran produk permeate juga semakin besar.
Dari grafik tersebut juga dapat dilihat bahwa pada akhir operasi daya rejeksi membran RO menurun sebesar 86,3 %. Garam yang tertahan di permukaan membran dapat menyebabkan pore blocking pada permukaan membran sehingga menghambat proses penyisihan. 0 100 200 300 400 500 600 700 0 10 20 30 40 50 60 70 80 90 % Recovery T D S ( p p m ) 3 bar 5 bar
Gambar 7. Pengaruh Perubahan Tekanan Operasi dan Faktor Recovery Terhadap TDS Permeate RO
Analisa Laboratorium.
Hasil analisa permeate RO mengenai kandungan ion total kromium, nikel dan COD ditunjukkan oleh Tabel 2.
Dari hasil analisa diatas dapat dilihat bahwa membran reverse osmosis mempunyai kemampuan rejeksi terhadap Cr total 100 % dan Ni 100 %. Sebagian besar ion kromium total telah tertahan di permukaan membran UF sebelum tahap RO karena ion kromium total dan ukuran endapan Cr(OH)3 lebih besar dibandingkan Ni(OH)2. Membran RO dapat menahan semua ion dan garam terlarut dengan berat molekul > 100. Ion kromium dan nikel serta endapan Cr(OH)3 dan Ni(OH)2 yang lolos dari tahap ultrafiltrasi dapat dipisahkan dalam membran RO. Dari data tersebut diatas dapat diketahui bahwa penggunaan RO dalam pengolahan limbah elektroplating lebih efisien dibandingkan dengan UF, penggunaan UF disini dimaksudkan sebagai tahap pretreatment yang bertujuan untuk memperpanjang umur membran RO. Produk dari RO telah memenuhi syarat baku mutu limbah dari pemerintah sehingga aman untuk dibuang atau digunakan kembali sebagai rinse water
Tabel 2. Hasil Analisa Kandungan Zat Dalam Permeate RO
Parameter Hasil analisa RO Hasil analisa UF Baku mutu PP
no.18 Th 1999
Kromium total, ppm Tidak terdeteksi 0,0693 0,25
Nikel, ppm Tidak terdeteksi 0,1274 -
COD, ppm 8,64 8,64 100
Warna Jernih tidak
berwarna
Jernih tidak berwarna
Jernih tidak berwarna
Parameter Hasil analisa RO Hasil analisa UF Baku mutu PP
no.18 Th 1999
Kromium total, ppm Tidak terdeteksi 0,0693 0,25
Nikel, ppm Tidak terdeteksi 0,1274 -
COD, ppm 8,64 8,64 100
Warna Jernih tidak
berwarna Jernih tidak berwarna Jernih tidak berwarna Penutup
Kinerja sebuah sistem reverse osmosis untuk proses pengolahan limbah elektroplating telah diobservasi. Studi ini dilakukan untuk skala laboratorium. Proses reverse osmosis ini dioperasikan secara batch. Parameter operasi volume umpan 10 L telah diteliti dan dioperasikan pada tekanan 3 dan 5 bar. Semua pengujian dilakukan pada temperatur kamar. Hasil menunjukkan bahwa komponen total ion kromium dan nikel dapat dipisahkan dengan teknik reverse osmosis sebanyak 100 % dan laju alir permeate berubah. Produk RO telah memenuhi syarat baku mutu limbah elektroplating oleh PP No.18 tahun 1999, sehingga aman untuk dibuang atau digunakan kembali sebagai rinse water. Sebaiknya dilakukan pengontrolan pH 2-3 pada tahap reduksi Cr(VI) menjadi Cr(III) dan pH 8,5 pada tahap netralisasi agar semua Cr(OH)3 dan Ni(OH)2 mengendap sempurna.
Daftar Pustaka
1. Edris Bazrafshan. (2006). Performance Evaluation of Electrocoagulation Process for Removal of Chromium (VI) from Synthetic Chromium Solutions Using Iron and Aluminium Electrodes. Iran.
2. Choi, D.W. and Kim, Y.H., (2003). Cadmium Removal Using Hollow Fiber Membrane with Organic Extractants, Korean J. Chem. Eng., 20(4), 768-771. 3. G. Muthuraman, Teng Tjoon Tow*, Leh Cheu Peng, Norli Ismail. (2008).
Removal of Hexavalent Chromium from Plating Wastewater by Bulk Liquid Membrane, Malaysia.
4. Electroplating : A Focus on Chrome Plating
5. Environmental Guidelines for Electroplating Industry
6. Huda Syamsul, Purwanto. (2005). Teknologi Industri Elektroplating. Semarang : UNDIP
7. Reverse Osmosis Apllications for Metal Finishing Operations
8. S. Saravanan, K.M. Meera Sheriffa Begum, N. Anantharman. (2006). Removal Of Hexavalent Chromium By Emulsion Liquid Membrane Technique
9. Dow. FILMTECTM Reverse Osmosis Membran.
10.Mulder, Marcel., (1996). Basic Principles of Membrane Technology, Kluwer Academic Publisher, Dordrecht. Boston. London
EFEK PENAMBAHAN ABU SEKAM PADI TERHADAP SEBARAN BESI DARI PIGMEN ANORGANIK ALAMI DALAM BATA MERAH
Akhmad Jamila, Irmina Kris Murwanib
a
Program Magister Kimia, Institut Teknologi Sepuluh Nopember, Surabaya b
Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Teknologi Sepuluh Nopember, Surabaya
Abstrak. Telah dilakukan penelitian dan karakterisasi terhadap sebaran besi dari
pigment anorganik alami batu merah terhadap sistem bata merah yang terdiri dari Lempung Pejaten-Abu sekam padi-Batu merah Tajun dengan optimasi menggunakan metode Triaxial Blend. Bata merah yang dihasilkan dikarakterisasi dengan XRD, DTA/TGA, dan uji sifat fisik yang terdiri dari susut total, kuat tekan, porositas, penyerapan air dan uji garam terlarut. Sedangkan studi sebaran besi menggunakan sofware color detector. Hasil penelitian menunjukkan bahwa 15 komposisi memenuhi SII. Dengan suhu pembakaran 800°C diperoleh komposisi optimum dengan komposisi 80% lempung, 15% abu sekam padi dan 5% batu merah dengan susut total 5.48%, kuat tekan 363.62 N/mm2, porositas 46.66%, penyerapan air 27.36%, dan garam terlarut 10.73%.
Kata kunci : Lempung, batu merah, abu sekam padi, homogenitas warna, dan sebaran besi.
1. PENDAHULUAN
Bata merah sebagai bahan konstruksi sampai saat ini masih sangat dibutuhkan, mengingat batako sebagai pengganti bata merah masih sangat mahal harganya dibandingkan dengan harga bata merah. Penggunaan bata merah di Bali mempunyai fungsi ganda yaitu sebagai bahan konstruksi sekaligus sebagai ornamen dalam arsitektur Bali tradisional maupun modern. Seperti pada pura, gapura, rumah, perkantoran, hotel, taman kota, pasar dan sebagainya. Penggunaan bata merah yang banyak di Bali seperti tersebut di atas menjadikan penting untuk memproduksi bata merah menjadi lebih, baik dari segi kuantitas maupun kualitas.
Material utama dalam penelitian ini digunakan lempung dari desa Pejaten Badung Bali, karena selama ini bata merah sudah diproduksi di sana, namun bata merah yang dihasilkan masih memberikan warna merah yang kurang homogen. Warna merah pada bata selain dipengaruhi oleh suhu pembakaran juga jumlah kadar besi dari lempung. Untuk meningkatkan jumlah kadar besi dilakukan dengan penambahan pigmen anorganik alami dalam pembuatan bata merah. Pigmen anorganik alami yang digunakan adalah batu merah yang berasal dari Desa Tajun Kec Kubutambahan Buleleng Bali karena batu merah memiliki kadar besi yang tinggi.
Selain homogenitas warna dari produk akhir bata merah yang penting adalah kuat tekan dan penyerapan air. Kuat tekan dan penyerapan air dapat diperbaiki dengan menambahkan abu sekam padi (Rahman, 1998). Dari beberapa penelitian (Harsono, 2002) yang telah dilakukan menunjukkan bahwa abu sekam padi banyak mengandung silika. Carty & Senapati (1998), menjelaskan bahwa silika berfungsi sebagai pengisi bahan yang dapat mengurangi susut selain itu dapat mendifusikan pigmen besi dari batu merah pada pembakaran.
LANDASAN TEORI
Melimpahnya lempung mendorong studi lebih lanjut tentang pembuatan bata yang berkualitas. Pemakaian bahan tambahan dalam produksi bata tergantung pada karakteristik produk yang dihasilkan. Untuk membuat bata merah minimal diperlukan lempung sebagai komponen plastis. Bahan tambahan ditambahkan untuk memperbaiki sifat mekanik produk dari bata merah. Penambahahan abu sekam padi sebagai komponen filler akan meningkatkan modulus patah dan mengurangi susut kering maupun susut bakar (Rahman MA, 1998). Penambahan pigment anorganik alami yang berupa batu merah dilakukan untuk mencapai homogenitas warna merah yang maksimal (Johnson 1963).
METODE PENELITIAN
Eksperimen menggunakan metode segitiga terner. Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah lempung Pejaten Tabanan Bali, dan sebagai bahan aditif digunakan batu Merah Tajun Buleleng Bali, dan abu sekam padi dari Prambon.
Peralatan yang digunakan meliputi : papan pengering, saringan 80 mesh, timbangan analitis, pot mill, Electric Kiln (Nabertherm N50), alat pengukur modulus patah (SNI 0256-1989-A), DTA/TGA model TA dengan perangkat lunak Thermal Analyst 1750 (Setaram Setsys-1750), XRF (Minipal 4), XRD 6000 Tube = Cu Kα 1,5406 Ǻ, dan
FTIR (Shimadzu, 8400S). Prosedur Kerja
Bahan baku dianalisis dengan XRF untuk menentukan kadar SiO2, Al2O3, Fe2O3, TiO2, MgO, CaO, K2O, Na2O. XRD untuk mengetahui kandungan mineralogi. Kemudian dibuat 15 komposisi dengan segitiga terner. Preparasi meliputi pengurangan ukuran partikel dan pencampuran bahan baku yang telah dikeringan.
Campuran bahan baku sesuai prosentase masing-masing titik di milling, dikeringkan kembali untuk digerus kemudian diayak, selanjutnya ditambahkan air secukupnya sampai diperoleh campuran plastis sehingga siap dicetak dengan ukuran (7x3x1) cm3 sebanyak 15 batang setiap komposisi.
Karakterisasi meliputi susut, modulus patah, porositas dan penyerapan air setelah dibakar pada suhu sintering yang ditentukan dengan alat DTA/TGA. Susut total diamati dengan mengukur panjang sampel, modulus patah diukur dengan alat modulus patah. XRD dilakukan untuk mengamati transformasi unsur/mineral pada suhu pembakaran 800oC.
HASIL DAN PEMBAHASAN Optimasi Matriks Bata Merah
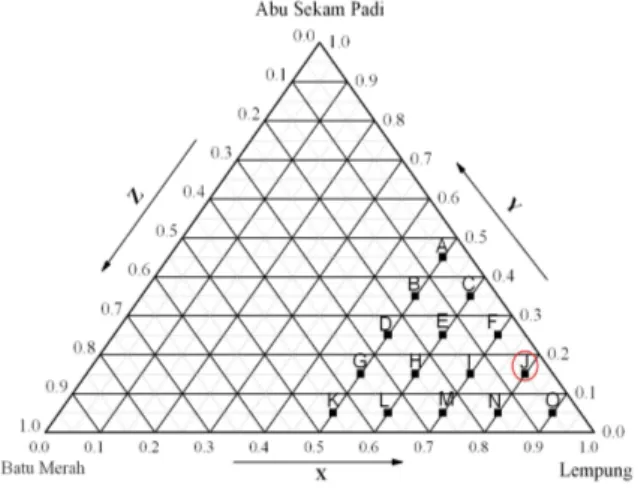
Hasil analisis kimia terhadap msing-masing bahan baku yang digunakan terlihat pada Tabel 1, sedangkan hasil kaarakterisasi dengan XRD nampak pada Gambar 1. Optimasi dengan metode segitiga terner untuk campuran yang terdiri dari 3 bahan (lempung, kuarsa, feldspar) dalam Gambar 2, dibuat 15 formula yang ditandai dengan
titik berkode A, B, C, ... , O sehingga komposisi dari setiap formula disusun dalam histogram Gambar 3.
Tabel 1. Komposisi Oksida Bahan Baku
Prosentase (%) Senyawa Senyawa
Lempung Batu Merah Abu Sekam Padi
SiO2 49,50 46,70 93,90 Al2O3 19,80 14,20 0,00 Fe2O3 23,99 22,99 0,53 TiO2 1,91 2,37 0,04 CaO 1,83 8,21 1,44 MgO 0,00 0,00 0,00 Na2O 0,00 0,00 0,00 K2O 0,65 2,99 2,73 LOI 2,29 2,59 1,33 SiO2/Al2O3 2,50 3,29 -- (a) (b) (c)
Gambar 1. Difraktogram Sinar-X bahan baku (a) Lempung Pejaten, (b) Batu Merah Tajun, (c) Abu Sekam Padi.
Gambar 3. Histogram Matriks Bata Merah
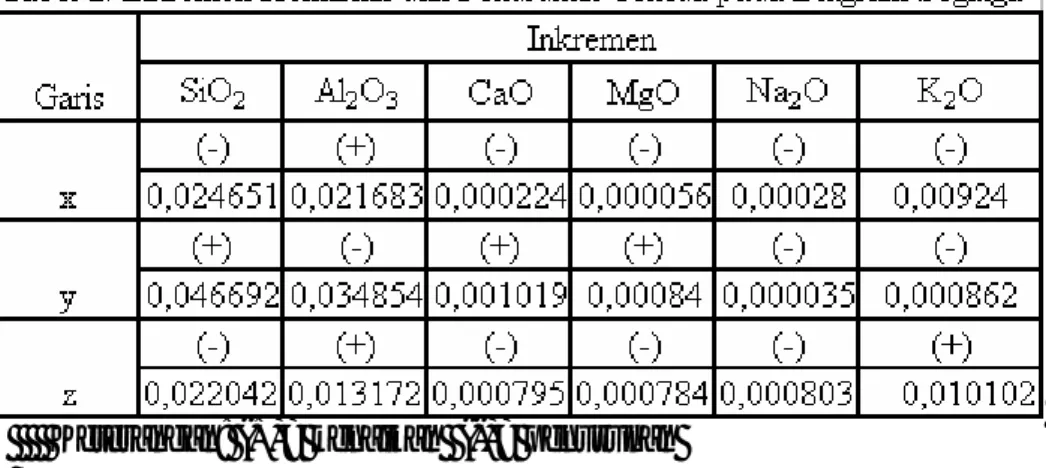
Prosentase senyawa/oksida yang terdapat dalam setiap formula mengikuti keteraturan kenaikan atau penurunan dari bahan baku, tampak pada, Tabel 2. Tabel 4.2 Inkremen Kenaikan/Penurunan Oksida pada Segitiga Terner
Inkremen Garis
SiO2 Al2O3 Fe2O3 TiO2 CaO K2O MgO Na2O
(+) (+) (+) (-) (-) (-) X 0.0028 0.005 0.001 0.0005 0.01 0.0023 0 0 (+) (-) (-) (-) (-) (+) Y 0.0444 0.019 0.024 0.0019 0.0004 0.0021 0 0 (-) (+) (+) (+) (+) (+) Z 0.0472 0.014 0.023 0.0023 0.0104 0.0003 0 0 Ketengan : (+) : kenaikan, (-) : penurunan
Penentuan Suhu Pembakaran
Hal yang terpenting dari pembuatan bata merah adalah pembakaran, yaitu pada suhu sintering. Penentuan suhu sintering dilakukan uji termal dengan metode DTA/TGA.
Gambar 4. Termogram DTA/TG
Dari termogram DTA/TG pada Gambar 4. dapat diketahui reaksi yang terjadi selama pembakaran bata merah dan besarnya hilang berat. Reaksi yan terjadi selama pembakaran ditunjukkan oleh puncak-puncak endotermis A, B, dan C dan puncak eksotermis D. ∆m1, ∆m2 dan ∆m3 menunjukkan besarnya kehilangan berat sampel. Pada puncak endotermis A terjadi pada suhu 126ºC dengan hilang berat ∆m1 sebesar 6,534%. Pada suhu ini reaksi penghilangan air yang terabsorbsi secara fisik. Puncak
endotermis B terjadi pada suhu 226,42ºC diikuti hilang berat sebesar ∆m2 0,671%. Pada suhu ini terjadi reaksi penghilangan air kristal. Puncak endotermis C terjadi pada suhu 503,045ºC yang diikuti dengan kehilangan berat ∆m3 sebesar 5,455%. Pada suhu ini terjadi dehidrasi Ca(OH)2 menjadi CaO dan H2O serta dekomposisi bahan-bahan organik.
Paama et al. (1999), menjelaskan bahwa pada sekitar suhu 100ºC terjadi penghilangan air yang terabsorpsi secara secara fisik, sedangkan air kristal hilang pada suhu sekitar 200–350ºC dan dehidrasi Ca(OH)2 terjadi pada rentang suhu 400-520ºH. Sedangkan Sousa & Holanda (2005) menyatakan bahwa penghilangan air kristal terjadi pada suhu 225ºC. Reed (1988), Boke at al. (2006), juga melaporkan bahwa senyawa-senyawa organik dalam lempung umumnya teroksidasi pada suhu antara 200-700ºC. Pada suhu 785,400ºC yaitu puncak D, terjadi reaksi eksotermis memberikan informasi terjadinya prsoses sintering, pada suhu ini sudah tidak diikuti oleh hilang berat, sehingga bata merah yang terdiri dari campuran lempung Pejaten, batu merah Tajun dan abu sekam padi dapat dibakar minmal pada suhu 785,400ºC.
Perubahan Fase pada Suhu 800C
Perubahan fase ini dapat diamati dengan menggunakan difraksi sinar-X pada bata mentah dan bata yang telah dibakar pada suhu 800ºC. Matriks bata merah yang diamati adalah matriks J karena dianggap mewakili sistem yang diteliti.
Gambar 5. Difraktogram Sinar-X Perubahan Fase Bata Merah ( : Quartz)
Pada Gambar 5. terdapat perubahan puncak-puncak selama peningkatan suhu pembakaran. Pada suhu 800ºC dapat diamati puncak anorthite maupun maghemit sudah tidak nampak dan puncak baru yang diidentifikasi sebagai puncak-puncak kuarsa. Merujuk termogram DTA/TGA Gambar 4. pada suhu 700-800°C tidak terjadi kehilangan berat, hal ini menunjukkan bahwa hanya terjadi perubahan fase kristal bahan mentah menjadi fase kuarsa. Fase kuarsa ini menunjukkan bahwa telah terjadi vitrifikasi (penggelasan) pada bata merah yang menjadikan bata merah menjadi kuat dan keras. Sebagaimana dilaporkan oleh Astuti, (1997) yang menyatakan bahwa unsur pembentuk gelas pada suhu tinggi akan mencair kemudian menjadi gelas dan kalau didinginkan akan menjadi keras.
Karakterisasi Sifat Fisik Bata Merah
Sistem bata merah dengan segitiga terner yang tersusun dari lempung, batu merah, dan abu sekam padi mempunyai karakter yang saling mendukung selama proses pembuatan dan produk yang dihasilkan. Lempung pembawa sifat plastis, abu sekam
merah. Karakter tersebut antara lain kemampuan bentuk dan batas plastis pada tahap preparasi, penyusutan selama tahap pengeringan dan pembakaran, porositas, penyerapan air, kekuatan mekanik (Conrad, 1980).
Susut
Gambar 6. Prosentase Susut Kering Selama Waktu Pengeringan Hasil penelitian menunjukkan bahwa lempung murni menunjukkan susut kering paling besar yaitu 6,93%, sedangkan pada komposisi matriks bervariasi yaitu antara 3,88-6,65%, matriks O menunjukkan susut kering paling besar yaitu 6,65%. Hal ini disebabkan matriks O pembawa sifat plastis (lempung 90%) lebih besar dibandingkan pembawa sifat non-plastis (abu sekam padi 5% dan batu merah 5%). Hal ini menunjukkan bahwa penambahan material non-plastis (abu sekam padi dan batu merah) dapat mengurangi susut kering sesuai dengan komposisi matriks bata merah (Das et al., 2005).
Dari diagram terner didapat bahwa penurunan susut kering sepanjang sumbu y seiring dengan menurunnya Al2O3 dan meningkatnya SiO2, sedangkan kenaikan susut kering sesuai dengan sumbu x dan z ditandai dengan meningkatnya Al2O3 dan menurunnya SiO2. Dengan menurunnya Al2O3 berarti menurunnya kadar air yang terikat sehingga susutnya kecil, dan bertambahnya SiO2 mengakibatkan susut akan mengecil hal ini sesuai dengan laporan Norton (1952); Carty & Senapati (1998) melaporkan bahwa keberadaan SiO2 akan membentuk kerangka matriks sehingga mengurangi susut.
Pada proses pembakaran bata mentah akan mengalami susut bakar yang disebabkan oleh saling mendekatnya partikel-partikel penyusun matriks bata. Hal ini berlangsung karena perubahan komposisi bata mentah selama pemanasan sehingga terjadi pengecilan ukuran pori yang memisahkan partikel-partikel, penyusutan kristal penyusun bata, dan terbentuknya fase baru pada suhu tinggi. Perhitungan susut bakar dilakukan dengan membandingkan antara panjang kering dan panjang setelah dibakar, sedang susut total dihitung dengan membandingkan panjang plastis dengan panjang setelah dibakar (Richerson, 1982). Hasil susut total terlihat pada Gambar 7.
Gambar 7. Prosentase Susut Total Matriks Bata Merah pada Suhu 800ºC Modulus Patah
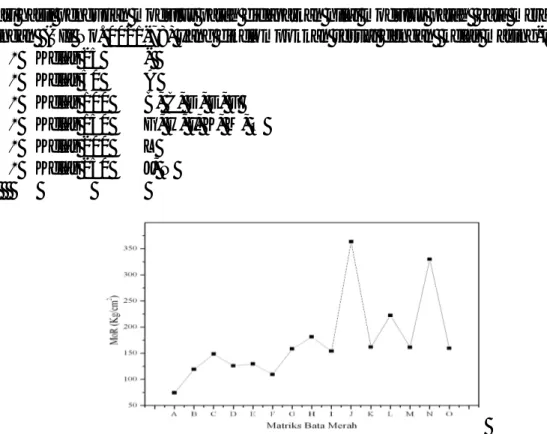
Dari hasil pengujian modulus patah didapatkan nilai modulus patah bata merah sesuai dengan (SII No. 0021-78) yang dikelompokkan sesuai dengan kelas masing-masing :
Kelas 25 - Kelas 50 A Kelas 100 B, C, D, E, F Kelas 150 G, H, I, K, M, O Kelas 200 L Kelas 250 J, N
Gambar 8. Modulus Patah Matriks Bata Merah pada Suhu 800°C
Merujuk pada segitiga terner pada Gambar 2. dapat diketahui bahwa kecenderungan modulus patah sepanjang sumbu x dan z, serta penurunan sesuai dengan sumbu y. Kenaikan dan penurunan modulus patah dipengaruhi oleh kenaikan dan penurunan Al2O3 dan Fe2O3. Hal ini sesuai dengan laporan Abadir et al., (2002) yang mengatakan bahwa penggunaan alumina selalu meningkatkan kekuatan, sedangkan Iqbal & Lee (2000) menjelaskan bahwa pembentukan kristal Al2O3 maupun mullit merupakan faktor utama kekuatan.
Dari tabel 3. terlihat bahwa sampel J memiliki harga modulus patah terbesar diantara sampel yang lain. Sehingga dapat dikatakan bahwa sampel J dengan komposisi lempung 80%, abu sekam padi 15% dan batu merah 5% atau dengan kadar SiO2 56,02%; Al2O3 15,93%; Fe2O3 37,66% (Si/Al = 3,5158) menghasilkan harga modulus patah yang maksimum.
Porositas dan Penyerapan Air
Gambar 9. Porositas dan Penyerapan Air Setelah dibakar Suhu 800C
Dari hasil pengukuran porositas, penyerapan air, susut dan kekuatan mekanik pada suhu 800C menunjukkan bahwa pada pembakaran suhu sintering berbanding lurus dengan nilai susut dan kekuatan mekaniknya dan berbanding terbalik dengan porositas dan penyerapan airnya. Hal ini sesuai yang dilaporkan oleh Vieira et al
(2005) bahwa susut linear dan kekuatan mekanik akan semakin meningkat sedangkan penyerapan air dan porositas akan menurun yang disebabkan mekanisme sintering dan proses pemadatan (densification). Meningkatnya susut menyebabkan mengecilnya porositas sehingga kemampuan untuk menyerap air semakin kecil dan kekuatan akan semakin besar.
Karakteristik Tampak Luar
Karakteristik yang diukur dari hasil pembakaran bata dilakukan berdasarkan Standar Industri Indonesia No. 0021-78 adalah meliputi kenampakan fisik luar (bentuk dan warna) spesimen bata merah yang dihasilkan. Hasil dari pengamatan secara visual ditabelkan sebagai berikut :
Tabel 4. Tampak Luar
Bentuk Kode
Sampel Kerataan Bidang Siku Rapuh Warna
A Rata Tajam Tidak Merah kekuning-kuningan B Rata Tajam Tidak Merah kekuning-kuningan C Rata Tajam Tidak Merah kekuning-kuningan
D Rata Tajam Tidak Merah Muda
E Rata Tajam Tidak Merah Muda
F Rata Tajam Tidak Merah Muda
G Rata Tajam Tidak Merah Muda
H Rata Tajam Tidak Merah Muda
I Rata Tajam Tidak Merah
J Rata Tajam Tidak Merah
K Rata Tajam Tidak Merah Gelap
L Rata Tajam Tidak Merah Gelap
M Rata Tajam Tidak Merah Gelap
N Rata Tajam Tidak Merah
Warna merah pada bata diakibatkan oleh FeO yang mengalami oksidasi pada suhu tinggi menjadi Fe2O3, dan mengakibatkan kekuatan mekanis akan lebih tinggi. Warna dari hasil produksi disamping tergantung dari pembakaran, juga tergantung dari perbandingan banyaknya antara Fe2O3 dan (CaO + Al2O3). Semakin banyak Fe2O3, makin merah warnanya dan sebaliknya makin banyak (CaO + Al2O3) makin pucat warnanya (Sukandarrumidi, 1999). Nilai maksimum hasil perbandingan antara Fe2O3 dan (CaO + Al2O3) adalah 2,09 pada komposisi J, sehingga J mempunyai warna merah yang paling baik.
Uji Garam yang dapat Larut
Pengujian terhadap garam yang dapat larut dilakukan sesuai dengan SII No. 0021-78, Dari hasil uji garam terlarut prosentase lapisan putih berkisar antara 1,98% - 11,65% dari permukaan bata. Komposisi B mempunyai prosentase tertinggi yaitu 11,65%, sedangkan komposisi O mempunyai prosentase terendah yaitu 1,98%. Tidak ada matriks bata merah yang mempunyai prosentase garam terlarut lebih dari 50%.
KESIMPULAN
Karakterisasi sistem bata merah lempung Pejaten-batu merah Tajun-abu sekam padi dengan segitiga terner diperoleh komposisi yang optimum 80% lempung, 15% abu sekam padi dan 5% batu merah. Bata merah ini pada pembakaran 800oC mempunyai susut total 5,479%, modulus patah 363,526 Kg/cm2 dan penyerapan air sebesar 27,363% yang telah memenuhi SII.
Daftar Pustaka
Astuti, A., (1997), Pengetahuan Keramik, Gadjah Mada University Press, Yogyakarta.
Carty, M.W., and Senapati, U. (1998), “Porcelain-Raw Material, Processing, Phase Evolution, and Mechanical Behavior”, J.Am.Ceram.Soc., Vol. 81, hal. 3-20. Das, Kr.S & Dana, K., Sing, N., Sarkar, R., (2005), “Shrinkage and Strength behavior
of quartzitic and kaolinitic clays in wall tile compositions”, Apllied Clay Science, Vol.29, hal.137-143.
Ismunandar, (2004), Padatan Oksida Logam : Struktur, Sintesis dan Sifat-sifatnya,
Institut Teknologi Bandung, Bandung.
Iqbal, Y., and Lee, W.E. (2000), “Microstructural Evolution in Triaxial Porcelain”,
J.Am.Ceram.Soc., Vol. 83, hal. 3121-3127
Johnson, Stanley S. (1963), “Iron And Titanium Mineral Pigments In Virginia”,
Virginia Minerals, Vol. 10, No. 03, hal. 1-12.
Kamseu, E., Leonelli, C., Bocaccini, D.N., Veronesi, P., Miselli, P., Pellacani, G., Melo, U.C., (2007), “Characterisation of porcelain composition using two china clay from Cameron”, Ceram.Int.J., Vol. 33, hal. 851-857.
Karaman S., Gunal H., Ersahin S., (2006), “Assesment Of Clay Bricks Compressive Strength Using Quantitative Values Of Colour Components”, Construction and Building Materials, Vol. 20, Hal. 348–354
Kumar, S, (2003), Brick and Ceramics Sector, Regional Energy Resources Information Center (RERIC) Asian Institute of Technology Pathumthani, Thailand.
Paama, Lilli., Pitkanen, Ilkka., Peramaki, Paavo., (2000),”Analysis Of Archaeological Samples And Local Clays Using ICP-AES, TG–DTG and FTIR Techniques”, Talanta Vol. 51., Hal. 349–357
Rahman, M.A. (1998), “Effect Of Rice Husk Ash On The Properties Of Bricks
Made From Fired Lateritic Soil-Clay Mix”, J. Materials and Structures/Materiaux et Constructions.,Vol. 21, hal. 222-227.
Reed, J.S, (1988), Introduction to the Principle of Ceramic Processing, John Wiley & Sons, New York.
Richerson, D.W, (1982), Modern Ceramic Engineering, Marcel Dekker Inc. NY. Standar Industri Indonesia (1978), Mutu dan Cara Uji Bata Merah Pejal, SII
0021-78, Departemen Perindustrian, RI.
Sukandarrumidi, (1999), Bahan Galian Industri, Gajah Mada University Press, Yogyakarta.
Sulistya, R., Hartanto, Dj., Murwani, Irmina K., (2006), “Karakterisasi dan Studi Sebaran Kobalt Sistem Badan Keramik Lempung Bojonegoro-Feldspar-Kuarsa”, Indo.J.Chem., Vol.6, hal. 138-143.
Vieira, C.M.F., da Silva, P.R.N., da Silva, F.T., Capitaneo, J.L., Monteiro, S.N., (2005), “Microstructural Evaluation and Properties of a Ceramic Body for Extruded Floor Tile”, Revista Materia, Vol. 10, hal. 526-536.
KAJIAN KARAKTERISASI SISTEM BADAN KERAMIK
LEMPUNG BANGKA-KUARSA-FELDSPAR SESUAI SNI
Amin Makmuna, Irmina Kris Murwanib a
Program Magister Kimia, Institut Teknologi Sepuluh Nopember, Surabaya b
Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Teknologi Sepuluh Nopember, Surabaya
Abstrak. Telah dilakukan penelitian karakterisasi dan studi sebaran kobalt terhadap sistem badan keramik yang terdiri atas Lempung Bangka-Kuarsa-Feldspar dengan optimasi menggunakan metode Triaxial Blend. Badan keramik yang dihasilkan dikarakterisasi dengan XRD,DTA/TGA dan uji sifat fisik yang terdiri dari susut total, kuat tekan, porositas dan penyerapan air. Hasil penelitian menunjukkan bahwa dari 15 komposisi diperoleh 4 komposisi yang memenuhi SNI. dengan suhu optimum pembakaran untuk badan keramik dan glasir pada 1150oC. Diperoleh sistem badan keramik optimum dengan komposisi 44,00% lempung, 11,50% kuarsa dan 45,10% feldspar dengan susut total 7,25%, modulus patah 15,29N/mm2, porositas 27,98% dan penyerapan air 16,83%.
Kata kunci : Lempung Bangka, kuarsa, feldspar, badan keramik, susut, modulus patah, dan penyerapan air .
1. PENDAHULUAN
Melimpahnya bahan tambang mineral keramik di Indonesia seperti lempung, feldspar, pasir kuarsa, bentonit, kapur dan lain-lain, merupakan aset yang berharga bagi industri keramik. Oleh karena itu diperlukan suatu penelitian yang mendalam dan secara simultan terhadap kelimpahan lempung dan pasir kuarsa Bangka agar diperoleh suatu produk keramik yang memiliki kualitas yang tinggi dan pada akhirnya akan memiliki nilai jual yang tinggi pula, dan juga bisa menjadi produk unggulan mengingat Bangka menjadi propinsi sendiri.
Propinsi Bangka merupakan salah satu daerah penghasil mineral-mineral keramik seperti lempung, kuarsa, feldspar dan kapur. Meskipun keberadaannya sudah banyak yang digunakan oleh para pengrajin keramik dan industri, namun penelitian dan publikasi dari karakterisasi dan optimasi campuran lempung Bangka, Feldspar, dan Pasir kuarsa masih sedikit dilakukan (Sukandarrumidi, 1999).
2. LANDASAN TEORI
Untuk membuat keramik tile minimal diperlukan 3 komponen yaitu (1)
clay/lempung sebagai komponen plastis, (2) feldspar sebagai komponen fluxing, dan (3) kuarsa sebagai komponen filler (Conrad, 1980; Correia et al, 2004).Lempung mengandung silika, alumina dan sedikit feldspar. Silika (SiO2) berfungsi sebagai pengisi atau pembentuk badan keramik sehingga mengurangi susut. Alumina (Al2O3) mengontrol dan mengimbangi pelelehan sehingga memberikan kekuatan pada badan keramik. Feldspar terdiri dari mineral-mineral kalium, natrium dan kalsium yang berfungsi sebagai pelebur sehingga menurunkan suhu bakar keramik. Oleh karena itu lempung merupakan bahan dasar dalam pembuatan keramik tradisional (Barsoum, 2003).
3. METODE PENELITIAN
Eksperimen menggunakan metode segitiga terner (Triaxial Blend) Bahan dan Alat
Bahan-bahan yang digunakan adalah lempung lokal yang didatangkan dari daerah Bangka Belitung, kuarsa dari Bangka Belitung dan feldspar dari Lodoyo Blitar yang merupakan bahan baku pembuatan produk kerajinan keramik di BPTIK Malang. Alat-alat yang digunakan dalam penelitian ini antara lain : Gelas ukur 50 ml, pipet tetes, gelas kimia 100 ml, alu dan lumpang besi, ember plastik, papan pengering, saringan 80 mesh, timbangan analitis, pot mill untuk mencampur dan menggiling pada proses reduksi ukuran bahan baku, cetakan terbuat dari besi berbentuk balok persegi panjang dengan ukuran (7x3x1) cm3, Alat pembakaran Electric Kiln (Nabertherm N50), alat pengukur modulus patah
di BPTIK Malang, alat petrografi di BPPTK Yogyakarta, instrumen DTA/TGA model TA dengan perangkat lunak Thermal Analyst 1750 (Setaram Setsys-1750) untuk mempelajari reaksi termal mineral-mineral dalam sistem badan keramik di Laboratorium Balai Besar Kereamik Bandung, Spektroskopi Serapan Atom (SSA) Shimadzu untuk mengetahui kompoaiai oksida-oksida bahan baku di Laboratorium FMIPA Unibraw, Difraksi sinar-X (XRD 6000 Shimadzu, Tube = Cu Kα 1,5406 Ǻ)
untuk identifikasi secara kualitatif mineral-mineral bahan baku dan transformasi mineral di Laboratorium Dasar Bersama Unair.
Prosedur Kerja
Bahan baku dianalisis dengan metode gravimetri untuk menentukan kadar SiO2, volumetri untuk menentukan kadar Al2O3 dan spektroskopi serapan atom untuk mengetahui kadar Fe2O3, TiO2, MgO, CaO, K2O, Na2O. XRD untuk mengetahui kandungan mineralogi. Kemudian dibuat 15 komposisi dengan segitiga terner. Preparasi meliputi pengurangan ukuran partikel dan pencampuran bahan baku yang telah dikeringan. Campuran bahan baku sesuai prosentase masing-masing titik di
milling, dikeringkan kembali untuk digerus kemudian diayak, selanjutnya ditambahkan air secukupnya sampai diperoleh campuran plastis sehingga siap dicetak dengan ukuran (7x3x1) cm3 sebanyak 30 batang setiap komposisi.
Karakterisasi meliputi susut, modulus patah, porositas dan penyerapan air setelah dibakar pada suhu sintering yang ditentukan dengan alat DTA/TGA. Susut total diamati dengan mengukur panjang sampel, modulus patah diukur dengan alat modulus patah. XRD dilakukan untuk mengamati transformasi unsur/mineral pada suhu pembakaran 600, 900, 1000 dan 1100oC.
4. HASIL DAN PEMBAHASAN Optimasi Matriks Keramik
Hasil analisis komposisi kimia terhadap masing-masing bahan baku yang digunakan terlihat pada Tabel 1, sedangkan hasil karakterisasi dengan XRD dalam Gambar 1. Optimasi dengan metode segitiga terner untuk campuran yang terdiri dari 3 bahan (lempung, kuarsa, feldspar) dalam Gambar 2, dibuat 15 formula yang ditandai dengan titik berkode A, B, C, ... , O sehingga komposisi dari setiap formula disusun dalam histogram Gambar 3.
Tabel 1 Komposisi Kimia Lempung Bangka, Kuarsa dan Feldspar Prosentase Senyawa (%)
Senyawa
Lempung Kuarsa Feldspar
SiO2 55,050 96,740 77,060 Al2O3 31,430 0,310 12,070 Fe2O3 1,000 0,110 0,160 CaO 0,180 1,090 0,380 MgO 0,000 0,750 0,050 TiO2 0,350 0,000 0,250 K2O 0,900 0,130 9,150 Na2O 0,080 0,049 0,330 LOI 0,990 0,680 0,600 SiO2/Al2O3 1,7515 312,0645 6,3844 Gambar 1 Difraktogram Sinar-X Lempung Bangka, Kuarsa dan Feldspar
(Ka=kaolinit,Al=albit, Mc=muskovit, Qz= kuarsa, Or=ortoklas)
Gambar 2. Diagram Terner,
Gambar 3. Histogram Komposisi Matriks Badan Keramik Z
Y
Keterangan: (+)= kenaikan (-)= penurunan Penentuan Suhu Pembakaran
Uji termal ini dilakukan pada kondisi atmosfir gas oksigen sampai suhu 1400°C dengan kecepatan pemanasan 10°C/menit pada sampel I dengan komposisi 55,2% lempung, 22,7% kuarsa, dan 22,7% feldspar diperolah kurva termogram DTA/TGA pada Gambar 4. Berdasarkan hasil uji termal dapat teridentifikasi ada empat puncak . Tiga puncak endotermis (A,B, dan C), dan satu puncak eksotermis (D). Dua puncak A
dan B ditunjukkan dengan penurunan berat pertama (Δm1) dan puncak C ditunjukkan dengan penurunan berat kedua (Δm2).
Gambar 4. Termogram Sampel I
Puncak endotermis A terjadi pada suhu 113°C dan puncak endotermis B terjadi pada suhu 216°C, dan dari kedua puncak tersebut diikuti oleh penurunan berat (Δm1=
0,799%). Reaksi yang terjadi pada puncak endotermis A terkait dengan reaksi pelepasan air absorpsi pada badan keramik, sedangkan pada puncak endotermis B berkaitan dengan reaksi oksidasi bahan organik (Carbajal et al. 2007; Escardino et al. 1993). Besarnya penurunan berat pada kedua reaksi ini tergantung dari besarnya daya absorpsi mineral penyusun dan impuriti karbon yang terkandung dalam badan keramik.
Puncak endotermis C terjadi pada suhu 539°C, memberikan informasi yang berkaitan dengan reaksi dehidroksilasi kaolinit menjadi metakaolinit yang disertai
dengan penurunan berat sebesar (Δm2= 5,961%). Menurut Escardino et al (1993);
Iqbal & Lee (2000); Carty & Senapati, (1998); Lopez & Rodriguez (2007) menyatakan bahwa reaksi dehidroksilasi kaolinit menjadi metakaolinit biasanya
terjadi pada rentangan suhu 500°C - 600°C dengan persamaan reaksi : Al2O3•2SiO2•2H2O Al2O3•2SiO2 + 2H2O
Kaolinit metakaolin
Chen et al (2004) memaparkan lebih jauh tentang dehidroksilasi kaolinit tersebut, bahwa dehidroksilasi dihasilkan karena adanya gangguan terhadap gugus hidroksi (OH) luar yang terdapat pada lembar oktahedral (AlO,OH)6 , tetapi tidak banyak berpengaruh terhadap gugus hidroksi (OH) luar yang terdapat pada lembar tetrahedral SiO4 selama pemanasan. Metakaolin merupakan senyawa antara menuju senyawa berikutnya (mullit). Kinetika dehidroksilasi dipercaya sebagai reaksi orde satu, menghasilkan laju dehidroksilasi secara langsung, proporsional dengan luas area kaolin (Carty & Senapati, 1998).
Puncak eksotermis D yang terjadi pada suhu 997°C, memberikan informasi pembentukan fase kristalin dari metakaolin. Menurut Carty & Senapati (1998) perubahan metakaolin menjadi struktur spinel dan amorphous silika bebas terjadi pada ~ 950-1000ºC. Sedangkan Vieira et al (2005) mempelajari evolusi fase kaolinit sampai suhu 1300ºC dan menemukan bahwa mullit dan fase spinel kemungkinan terbentuk pada 980ºC, hal ini sesuai dengan pendapat Chen et al., (2004) yang menyatakan bahwa pembentukan fase spinel atau silikon yang mengandung γ-alumina terjadi pada suhu 980ºC.
Perubahan Fase pada Kenaikan Suhu Pembakaran
Pada penelitian ini, matriks badan keramik yang dipilih adalah matriks I karena dianggap mewakili. Perubahan fase yang terjadi diamati dengan membandingkan data hasil pola difraksi sinar-X dari badan keramik mentah dan badan keramik yang dibakar pada suhu 600, 900, 1000, 1150 dan 1200°C dari hasil analisis DTA/TGA. Pemilihan rentang suhu pembakaran tersebut berdasarkan pada; setelah reaksi dehidroksilasi kaolinit, sebelum terjadi sintering, setelah sintering, dan pembentukan mullit, sehingga dapat dijelaskan perubahan karakter badan keramik selama terjadinya peningkatan suhu.
Pada Gambar 5 terlihat perubahan puncak-puncak selama terjadinya proses kenaikan suhu. Pada suhu 600°C dapat diamati puncak kaolinit talah hilang(*). Hal ini dapat dijelaskan bahwa reaksi dehidroksilasi kaolinit menjadi metakaolinit telah berlangsung secara sempurna. Merujuk pada hasil DTA/TGA (Gambar 4) reaksi dehidroksilasi kaolinit menjadi metakaolinit terjadi pada suhu 539ºC, sehingga dapat dikatakan suhu 600°C telah melampui suhu reaksi dehidroksilasi kaolinit, dan puncak-puncak yang lain tidak banyak berubah.
Pada suhu 900 dan 1000°C puncak feldspar (albit dan K-feldspar) mengalami penurunan intensitas dan menghilang pada suhu 1150°C(), hal ini sesuai dengan laporan Braganca (2003) bahwa mineral feldspar melebur pada suhu 1100°C. Sedangkan puncak kuarsa mengalami kenaikan intensitas karena terbentuk fase kristalin dari kuarsa dan pada suhu 1150 sampai 1200ºC mengalami penurunan intensitas yang signifikan karena terjadi pelarutan kuarsa oleh leburan feldspar untuk membentuk massa yang lebih padat sehingga menambah kekuatan badan keramik (Lopez et al, 2007).
Gambar 5. Difraktogram Badan Keramik pada berbagai Suhu; a) Bahan Baku; b) 600; c) 900; d) 1000 dan e) 1100oC
Selain terjadinya penghilangan fase dan penurunan intensitas mineral-mineral penyusun badan keramik, terlihat juga pada data termogram sinar-X terbentuknya fase baru mullit dan kenaikan intensitas dari mullit (M) yang mulai terdeteksi pada suhu 1150°C dan intensitasnya semakin naik pada suhu 1200ºC. Menurut Chen et al (2003) terbentuknya mullit meningkat dengan peningkatan suhu pembakaran dari 1050 sampai 1300ºC. Sedangkan menurut Iqbal & Lee (2000) kehadiran mullit terdeteksi pada 1100°C dan jumlahnya meningkat maksimum sampai suhu pembakaran 1400ºC dan menurun karena mengalami pelarutan pada suhu yang lebih tinggi.
Karakterisasi Sifat Fisik Badan Keramik 1. Kemampuan Bentuk dan Batas Plastis
Dalam penelitian ini, terdapat 15 komposisi dalam terner (A sampai O) dengan variasi prosentase penambahan air 22,5-35%. Komposisi (A, B, D, G, K) dengan prosentase lempung 32,8% tidak layak cetak pada kondisi plastis karena kesenjangan massa plastis yang signifikan, sehingga menyebabkan partikel-partikel penyusun badan keramik tidak terikat satu sama lainnya. Sampel badan keramik A, B, D, G , K memiliki komposisi lempung sebagai pembawa sifat plastis dengan prosentase yang tetap 32,8% sedangkan komposisi pembawa sifat non-plastis bervariasi. Komposisi kuarsa dengan variasi 11,5-56,3% dan komposisi feldspar 11,5-56,3% secara bergantian. Adanya kesenjangan yang signifikan antara komposisi pembawa sifat plastis (lempung) dan komposisi pembawa sifat non-plastis (kuarsa dan feldspar) membuat campuran semakin tidak homogen yang berakibat berkurangnya kemampuan partikel-partikel lempung untuk mengikat air . Komposisi (C, E, F, H, I, J, L, M, N, O) dengan variasi prosentase lempung 44-77,6%, prosentase kuarsa 11,5-45,1%, dan prosentase feldspar 11,5-45,1% layak cetak pada kondisi plastis karena komposisi lempung sebagai pembawa sifat plastis bervariasi sehingga homogenitas campuran tetap terjaga.
Melihat diagram terner (Gambar 2) maka kadar air dan keplastisan sesuai dengan sumbu x dan z dengan meningkatnya mineral Al2O3 dan menurunnya mineral SiO2, meningkatnya Al2O3 berarti meningkatnya kandungan mineral kaolinit yang memiliki struktur lembaran 1:1 yaitu lembaran oktahedral Al-O.OH yang bermuatan positif bersama dengan lembaran tetrahedral (Si2O5)2- yang bermuatan negatif, sehingga proses penyerapan air yang bersifat polar berjalan dengan cepat (Barsoum, 1997). Sedangkan sumbu y dengan menurunnya Al2O3 dan meningkatnya SiO2 berarti menurunnya kandungan mineral kaolinit sebagai pembawa sifat plastis dan naiknya
kandungan mineral SiO2 sebagai pembawa sifat non-plastis. Kenyataan ini juga didukung dari hasil analisis XRD lempung, kuarsa dan feldspar (Gambar 1) bahwa mineral Al2O3 tidak ada yang berada dalam keadaan bebas tetapi berada dalam bentuk mineral kaolinit.
2. Karakteristik Pengeringan dan Susut
Hasil penelitian, matriks badan keramik O memiliki prosentase air plastis 35% dengan kandungan mineral 77,60% lempung, 11,50% kuarsa, dan 11,50% feldspar terjadi susut terbesar mencapai 3,75%. Sedangkan susut terkecil dimiliki oleh matriks badan keramik C mencapai 1,00% dengan kandungan mineral 44,00% lempung, 45,10% kuarsa, dan 11,50% feldspar dengan prosentase air plastis 30%. Melihat perbedaan yang ekstrim dari matriks badan keramik C dan O dapat dijelaskan bahwa besarnya kadar air plastis berbanding lurus dengan besarnya kadar lempung dan besarnya susut berbanding terbalik dengan besarnya besarnya kadar kuarsa (filler) (Dondi, 2007)
Merujuk pada diagram terner, maka peningkatan susut kering sesuai dengan sumbu x dan z karena nilai Al2O3 meningkat dan nilai SiO2 berkurang. Sedangkan penurunan susut kering sesuai dengan sumbu y karena nilai Al2O3 berkurang dan nilai SiO2 bertambah. Hal ini dapat dijelaskan bahwa dengan meningkatnya Al2O3 berarti meningkatnya kadar air, karena selama proses pengeringan banyak ruang kosong yang ditinggalkan oleh molekul air ditempati oleh partikel-partikel penyusun badan keramik yang pada akhirnya menyebabkan susut. Sebaliknya dengan meningkatnya SiO2 berarti keplastisan dan susut berkurang karena SiO2 memberikan struktur terbuka sehingga memudahkan gas-gas menguap dan bertindak sebagai kerangka sehingga mencegah terjadinya perubahan bentuk (Hartono, 1993). Sedangkan keberadaan oksida CaO, MgO dalam keadaan bebas akan mempercepat pengeringan dan mengurangi susut kering (Hartono, 1993) hal ini sesuai dengan sumbu y dimana terjadi peningkatan CaO dan MgO menyebabkan susut kering mengalami penurunan. K2O, dan Na2O tidak dapat dijelaskan adanya pengaruh terhadap susut pengeringan karena pada diagram terner tidak ditemukan keteraturan pada sumbu x, y, dan z. Hal ini juga diperkuat oleh penelitian Sulistya dkk (2006) yang melaporkan bahwa Na2O dan K2O tidak berpengaruh terhadap susut kering badan keramik.
Gambar 6. Prosentase susut kering selama pengeringan
Tahap selanjutnya adalah proses pembakaran matriks badan keramik. Terjadinya susut selama proses pembakaran disebabkan oleh penghilangan air fisis, oksidasi material organik, dan pelepasan air kristal yang terikat secara kimia karena reaksi dehidroksilasi kaolinit menjadi metakaolinit yang terjadi pada suhu 539°C, terjadinya peleburan mineral feldspar pada suhu 1100ºC yang menyebabkan jarak pori-pori
membentuk massa larutan yang mengisi pori membentuk massa yang padat dan kuat. Susut pembakaran dihitung dengan membandingkan antara panjang kering dengan panjang setelah dibakar, sedangkan susut total dapat dihitung dengan membandingkan panjang plastis dengan panjang setelah dibakar (Richerson, 1982). Pengukuran susut total dari berbagai suhu pembakaran dapat dilihat pada Gambar 7.
Gambar 7. Susut total pada berbagai suhu pembakaran
Melihat data di atas, matriks badan keramik C memiliki susut terkecil dan matriks badan keramik O memiliki susut terbesar pada hampir semua rentang suhu pembakaran. Berdasarkan tabel komposisi matriks badan keramik C memiliki prosentase kuarsa paling besar dan lempung paling kecil dibandingkan matriks badan keramik O dengan prosentase feldspar yang sama. Hal ini menunjukkan bahwa yang memberikan perbedaan nilai susut dari kedua matriks badan keramik adalah lempung dan kuarsa. Namun demikian nilai susut bakar semua matriks badan keramik yang dibakar pada suhu 1150ºC sesuai SNI.
Pada diagram terner gambar.4.4 peningkatan susut sesuai dengan x dan z yaitu terjadi peningkatan Al2O3 dan penurunan SiO2 sehingga nilai Si/Al kecil, sedangkan penurunan susut sesuai dengan y yaitu terjadi penurunan Al2O3 dan peningkatan SiO2 sehingga nilai Si/Al besar.
Merujuk pada hasil analisis DTA/TGA (Gambar 4) dan analisis XRD (Gambar 5) bahwa terjadinya susut pembakaran pada suhu 600ºC disebabkan adanya reaksi pelepasan air fisis, oksidasi material organik, dan dehidroksilasi kaolinit menjadi metakaolinit. Sedangkan susut yang terjadi pada suhu 900 sampai 1200ºC disebabkan terjadinya proses peleburan feldspar yang melarutkan kuarsa sehingga terjadi penggelasan dari mineral-mineral penyusun keramik yang bergerak mengisi pori-pori yang pada akhirnya badan keramik menjadi lebih padat sehingga terjadi susut total yang semakin besar. Menurut Braganca et al (2003) fase gelas dalam komponen pembakaran terbentuk karena peleburan feldspar yang berinteraksi dengan fase kristalin. Hal ini dapat dilihat dari hasil analisis XRD bahwa mulai terjadinya penurunan fase dari mineral pelebur pada suhu 900ºC dan akhirnya hilang pada suhu 1150ºC, karena terjadi peleburan feldspar dengan melarutkan kuarsa yang ditandai dengan penurunan intensitas kuarsa. Sehingga dapat disimpulkan bahwa terjadinya proses penggelasan dimulai pada suhu sintering 997ºC dari data DTA/TGA dan diperkuat dengan data analisis XRD.
3. Modulus Patah
Pada diagram terner Gambar 2 kecenderungan kenaikan modulus patah sesuai dengan sumbu x dan z dengan meningkatnya Al2O3 dan menurunnya SiO2. Bernando et al (2007) menyatakan bahwa peningkatan modulus patah sesuai dengan
peningkatan kandungan Al2O3 dalam badan keramik. Selain itu Iqbal & Lee (2000) menjelaskan bahwa pembentukan kristal Al2O3 dan mullit merupakan faktor utama kekuatan badan keramik, sedangkan Carty & Senapati (1998) menjelaskan bahwa keberadaan kristal Al2O3 juga berfungsi sebagai filler menggantikan kuarsa untuk menghindari terjadinya inversi kuarsa dan dengan demikian meningkatkan sifat-sifat mekanik badan keramik. Berdasarkan data hasil analisis XRD (Gambar 5) pada suhu 1150ºC mulai terdeteksi adanya puncak mullit dan intensitasnya semkin meningkat pada suhu 1200ºC. Hal ini sesuai dengan laporan Lopez & Rodriguez (2007) yang menyatakan bahwa mullit mulai terdeteksi pada 1050ºC dan jumlahnya meningkat pada suhu yang lebih tinggi. Sedangkan Iqbal & Lee (2000) menyatakan bahwa mullit telah terdeteksi pada 1100ºC dan jumlahnya meningkat maksimum pada 1400ºC, dengan demikian maka semakin meningkatnya Al2O3 (lempung dan feldspar) maka akan menyebabkan modulus patah meningkat karena meningkatnya mullit seiring meningkatnya kenaikan suhu pembakaran. Hal ini sesuai dengan laporan Carbajal et al (2007) yang menyatakan bahwa kekuatan badan keramik semata-mata tergantung pada interlocking dari mullit, dan mengindikasikan bahwa kekuatan mekanik dengan peningkatan kandungan mullit.
Gambar 8. Modulus Patah pada berbagai Suhu Pembakaran 4. Porositas
Berdasarkan Gambar 9 terdapat penurunan porositas seiring sumbu x dan z yaitu dengan naiknya Al2O3 dan turunnya SiO2., dan mengalami peningkatan porositas sesuai sumbu y yaitu dengan turunnya Al2O3 dan naiknya SiO2. Merujuk pada Tabel 1 dan hasil analisis difraksi sinar-X (Gambar 1) keberadaan oksida Al2O3 dan K2O tidak berada dalam bentuk bebas tetapi dalam bentuk mineral kaolinit dan feldspar, sehingga dengan naiknya suhu pembakaran menyebabkan terjadinya penurunan porositas karena terjadi proses peleburan feldspar dengan melarutkan kuarsa dan mineral-mineral lain sehingga terjadi penggelasan dari mineral penyusun keramik dan bergerak mengisi pori-pori dan akhirnya memadat.
Gambar 9 Porositas Matriks Badan Keramik Setelah Dibakar pada Berbagai Suhu
KESIMPULAN
Komposisi optimum sistem badan keramik lempung Nagara-kuarsa-feldspar adalah 43,15% lempung, 22,84% kuarsa dan 34,01% feldspar. Badan keramik ini pada pembakaran 1100oC mempunyai susut total 8,71%, modulus patah 184,8 kg/cm2 dan penyerapan air sebesar 12,21% yang telah memenuhi SNI.
PUSTAKA
Alexander, B., (2000), Kamus Keramik, Milenia Populer, Bali Indonesia. Barsoum, M. (2003). Fundamental of Ceramics, Mc-Graw-Hill International.
Braganca, S.R., and Bergmann, C.P., (2003), “Traditional and Glass Powder Porcelain: Technical and Microstructure Analysis” , J. Ceram. Int. Vol. 24, hal. 2383-2388.
Chan, C.F., and Ko, Y.C., (1998), “Effect of CaO on the Hot Strength of Alumina-Spinel Castables in the Temperature Range of 1000o to 1500oC”,
J.Am.Ceram.Soc, Vol. 81, hal. 2957-2960.
Carbajal, L., Rubio-Marcos, F., Bengochea, M.A., Fernandez, J.F., (2007), “Properties Related Phase Evolution in Porcelain Ceramics”, J. Europe. Ceram. Soc, Vol. 27, hal. 4065-4069.
Carty, M.W., Senapati, U., (1998), “Porcelein-Row Material, Procesing, Phase Evolution, Ang Mechanical Behavior”, J. Am. Ceram. Soc, Vol. 81, No. 1, hal. 3-20.
Correia, S.L., Curto, K.A.S., Hotza, D., Segadaes, A.M., (2004), “Using statistical techniques to model the flexure strength of dried triaxial ceramic bodies”,
J.Eur.Ceram.Soc., Vol. 24, hal. 2813-2818.
Das, Kr.S & Dana, K., (2003), “Differences in densification behavior of K-and Na-Feldspar-containing porcelain bodies”, Thermochimica acta, Vol. 406, hal. 199-206.
Hartono, Y.M.V., (1993), Pengendalian Bahan Mentah Keramik, Balai Besar Industri Keramik Bandung.
Iqbal, Y., and Lee, W.E. (2000), “Microstructural Evolution in Triaxial Porcelain”,
J.Am.Ceram.Soc., Vol. 83, hal. 3121-3127.
Lopez, S.R., and Rodriguez. S., (2007), “Characterization of Microstructure in Experimental Triaxial Ceramic body”. J. Adv. in Tech. of Mat. and Mat. Proc,
Vol. 9, No. 2, hal 173-178.
Sukandarrumidi., (1999), Bahan Galian Industri, Gajah Mada University Press, Yogyakarta.
Sulistya, R., Hartanto, Dj., Murwani, Irmina K., (2006), “Karakterisasi dan Studi Sebaran Kobalt Sistem Badan Keramik Lempung Bojonegoro-Feldspar-Kuarsa”,Indo.J.Chem, Vol. 6, hal. 138-143.
Velde, B., (1992), Introduction to Clay Minerals, Chapman & Hall, London.
Vieira, C.M.F., da Silva, P.R.N., da Silva, F.T., Capitaneo, J.L., Monteiro, S.N., (2005), “Microstructural Evaluation and Properties of a Ceramic Body for Extruded Floor Tile”, Revista Materia, Vol.10, hal. 526-536.
Studi Tentang Kinetika Adsorpsi Ion Hg2+ Pada Elektroda Pasta Karbon Termodifikasi Bentonit (EPKTB)
Oleh
Asep Supriatna, Agus Setiabudi, Ali Kusrijadi Abstrak
Telah dilakukan kajian tentang kinetika adsorpsi ion Hg2+ pada elektroda pasta karbon termodifikasi bentonit (EPKTB) yang didasarkan pada kerja sensor amperometrik, dilakukan melalui dua tahap kegiatan yaitu pembuatan dan uji kinerja EPKTB dan uji analisis terhadap larutan ion Hg2+ sebagai dasar kajian terhadap kinetika adsorpsi ion Hg2+ dalam EPKTB. Kajian data optimasi penggunaan EPKTB terhadap larutan Cd2+ memperlihatkan tegangan listrik optimum sebesar 0,6 volt dan waktu kontak yang dibutuhkan sebesar 360 detik. Respon arus yang diberikan EPKTB terhadap larutan model meunjukkan peningkatan dengan bertambahnya konsentrasi larutan. Penggunaan EPKTB pada larutan uji Hg2+ memperlihatkan respon arus menurun sejalan dengan lamanya waktu interaksi EPKTB dengan larutan uji. Hal ini menunjukkan lambatnya terjadi kesetimbangan proses adsorpsi dan reduksi dari analit. Waktu optimum yang diperlukan pada analisis larutan uji sebesar 30 detik dengan batas konsentrasi analisis 4 ppm. Didasarkan pada perbandingan kadar Karbon-Bentonit dalam EPKTB, menunjukkan semakin besar perbandingan kadar Bentonit terhadap karbon semakin tinggi daya adsorpsi EPKTB. Kajian kinetika adsorpsi Hg2+ oleh EPKTB mengikuti model Freunlich, hal ini sesuai dengan karakter situs pengadsorps yang tidak seragam dalam EPKTB dan interaksi yang diramalkan berupa adsorpsi kimia dan fisik.
Kata Kunci : Kinetika adsorpsi, EPKTB, Model Freunlich
PENDAHULUAN
Electroda pasta karbon (EPK) merupakan elektroda yang relatif mudah dimodifikasi secara kimia dengan wilayah aplikasi yang luas. EPK adalah campuran serbuk grafit dengan cairan pemasta dan modifier. Salah satu material yang dapat digunakan sebagai modifier adalah lempung Bentonite. Bentonit menunjukan sifat adsorpsi yang baik terhadap ion-ion logam berat. Sifat adsorpsi ini disebabkan oleh adanya kandungan montmorillonit dalam bentonite; yaitu sekitar (60%). Montmorillonite, yang tergolong lempung kationik, memiliki struktur berlapis dengan ion positif pada fasa inter-layer. Kation interlayer inilah yang menjadikan montmorillonite memiliki sifat adsorpsi.
Beberapa studi tentang sifat adsorpsi bentonite dan zeolit telah dilakukan oleh pengusul dan kelompok peneliti pengusul. Studi tersebut adalah: studi adsorpsi limbah vinase pada bentonit (Supriatna, 2005), adsorpsi pengotor dalam Crude Palm
Oil..(CPO) dan Coconut Oil (CNO) oleh bleching earth bentonit teraktivasi (Supriatna, 2005), Pengkajian kapasitas pertukaran ion dan kinetika adsorpsi lempung terhadap ion Pb2+, menunjukkan kecenderungan terjadinya adsorpsi isotermis model Langmuir dengan tingkatan kapasitas adsorpsi optimum sebesar 80 % (Degsy, 2006).
Adsorpsi ion Hg2+ pada Elektroda Pasta Karbon Termodifikasi Bentonite (EPKTB), merupakan proses yang penting untuk digunakan sebagai komponen peralatan sensor Hg2+. Pengetahuan tentang kinetika adsorpsi ion oleh elektroda Pasta Karbon dapat memberikan informasi tentang batas kinerja EPKTB sebagai sensor Hg2+. Batas kinerja dimaksud, misalnya,: Potensial prekonsentrasi optimum , konsentrasi maksium dan waktu.
TINJAUAN PUSTAKA
Sensor Kimia dan Sensor Elektrokimia
Sensor kimia adalah alat yang digunakan untuk mendeteksi atau mengukur sesuatu yang digunakan untuk mengubah variasi mekanis, magnetis, panas, sinar, dan kimia menjadi beda potensial dan arus listrik (Petruzella, 2002). Sensor kimia merupakan miniatur perlengkapan analitis yang dapat memberikan informasi adanya senyawa atau ion tertentu dalam suatu sampel. Biasanya proses pengenalan terhadap analit dengan cara mengubah informasi kimia ke dalam sinyal listrik atau sinyal optik. Sensor kimia dapat juga digunakan sebagai sensor elektroaktif yang menimbulkan sifat selektif dan spesifik terhadap suatu analit tertentu.
Sensor amperometrik dan sensor potensiometrik adalah bagian dari sensor elektrokimia, yaitu sensor yang prinsip kerjanya didasarkan pada reaksi elektrokimia. Biasanya sensor jenis ini memiliki tiga buah elektroda yaitu sensing electrode, working electrode dan reference electrode. Sensor amperometrik mengukur arus yang dihasilkan dari reaksi elektrokimia yang melibatkan analit di mana arus ini sebanding dengan konsentrasi analit. Sedangkan sensor potensiometri mengukur konsentrasi analit dengan cara mengukur potensial yang dihasilkan dari reaksi elektrokimia yang melibatkan analit.
Adsorpsi
Adsorpsi adalah proses penyerapan suatu zat (adsorbat) pada permukaan suatu bahan penyerap (adsorben). Berdasarkan mekanismenya, adsorpsi dibagi dua jenis,
1). Adsorpsi secara fisika
Interaksi antara adsorben dengan adsorbat pada prinsipnya adalah gaya elektrostatik, termasuk interaksi dipol-dipol, interaksi dispersi, dan ikatan hidrogen. Adsorbat dapat diserap karena adanya gaya tarik menarik yang relatif lemah dengan permukaan adsorben. Adsorbat tidak tertarik secara kuat sehingga adsorbat dapat bergerak dari suatu bagian permukaan ke bagian permukaan lain. Adsorpsi ini berlangsung cepat, reversibel, dan kalor adsorpsinya rendah.
2). Adsorpsi secara kimia
Pada adsorpsi secara kimia pendekatannya adalah atraksi antara adsorben dengan adsorbat ikatan kimia kovalen atau elektrostatik antara atom-atom yang memiliki ikatan yang lebih pendek dengan ikatan yang berenergi lebih tinggi. Adsorpsi secara kimia tidak reversibel, terjadi pada suhu tinggi, dan kalor adsorpsinya juga tinggi.
Mekanisme terserapnya adsorbat pada adsorben terjadi melalui empat tahap, yaitu: Berpindahnya solut dari larutan menuju lapisan sekitar adsorben (bulk transport),.Solut terdifusi melalui lapisan tipis (film diffusion), Difusi solut melalui pori atau kapiler menuju sisi adsorben (diffusion pore)., Penyerapan solut pada permukaan adsorben.
Adsorpsi Isotherm
Terdapat beberapa jenis model adsorpsi isotherm yang dihubungkan dengan jenis adsorpsi yang terjadi.
Langmuir Kemisorpsi pada permukaan ideal
Freundlich Kemisorpsi dan adsorpsi fisik
Temkin Kemisorpsi
Brunauer-Emmett-Teller Adsorpsi fisik multilayer
Persamaan adsorpsi Model Langmuir adalah sebagai berikut
(1 )
KC KC
= fraksi permukaan (EPKTB) yang tetutupi adsorbat
K = konstanta yang sebanding dengan kads/kdes dan tergantung pada temperatur C = konsentrasi adsorbat dalam larutan
Penggunaan Model adsorpsi Langmuir didasarkan pada beberap asumsi : a. Situs adsorpsi bersifat eqivalen
b. Interaksi antara molekul yang terikat dengan situs pengadsorp kuat
c. Hanya satu molekul adsorbat yang dapat terikat pada satu situs pengadsorp Oleh karena itu model ini bersifat ideal dan jenis adsorpsinya didasarkan pada interaksi kimiawi antara adsorbat dan pengadsorp.
Persamaan adsorpsi Model Adsorpsi Freunlich adalah sebagai berikut
b
aC
= fraksi permukaan (EPKTB) yang tetutupi adsorbat a, b = konstanta
C = konsentrasi adsorbat dalam larutan
Model adsorpsi Freunlich lebih sesuai dengan situs aktif pengadsorp dari permukaan yang tidak seragam. Oleh karea itu interaksi material pengadsorps dengan zat adsorbat dapat bersifat interaksi kimiawi maupun fisik.
Persamaan adsorpsi Model Adsoprsi Tempkin adalah sebagai berikut ln
r sC
= fraksi permukaan (EPKTB) yang tetutupi adsorbat r, s = konstanta
C = konsentrasi adsorbat dalam larutan
Model adsorpsi Tempkin lebih sesuai dengan situs aktif pengadsorp dari permukaan yang tidak seragam. Namun interaksi material pengadsorps dengan zat adsorbat hanya bersifat interaksi kimiawi .
METODE PENELITIAN Desain Penelitian
Penelitian ini diawali dengan pembuatan EPK dan EPKTB dari karbon yang dipastakan dan dicampur dengan mineral bentonit. Selanjutnya dilakukan aplikasi penggunaan EPKTB terhadap larutan Hg2+, data yang dihasilkan digunakan untuk mengkaji mekanisme dan kinetika adsorpsi Hg2+ oleh EPKTB.