1. PENDAHULUAN
1.1 Latar Belakang.
Pada dasarnya serangkaian proses di dalam IPAM utamanya adalah untuk menurunkan kadar kekeruhan air baku. Proses koagulasi-flokulasi diperlukan sebagai tahap awal dalam menurunkan kekeruhan air baku. Dimana zat padat yang terdapat di dalam air berukuran sangat kecil dan tidak dapat mengendap dengan cepat, sehingga diperlukan suatu zat pembantu untuk memperbesar ukurannya agar dapat mengendap dengan cepat.
Untuk mengatasi kesulitan bilamana kualitas air baku tidak baik, maka proses koagulasi dilakukan dengan menggunakan bantuan bahan kimia. Supaya proses berjalan dengan efektif, maka perlu dilakukan yang diantaranya adalah tahap preklorinasi dan Jar test.
Jar test adalah suatu metode untuk mengevaluasi proses-proses koagulasi-flokulasi. Apabila percobaan dilakukan secara tepat, maka informasi yang diperoleh akan berguna untuk membantu operator instalasi dalam mengoptimalkan proses-proses koagulasi-flokulasi dan penjernihan, serta bagi para ahli teknik ( engineer ) dalam merancang bangunan IPA yang baru atau memperbaiki instalasi yang ada.
Jar test akan memberikan data mengenai kondisi optimum untuk parameter-parameter proses, seperti :
• Dosis koagulan dan koagulan pembantu.
• pH.
• Metode pembubuhan bahan kimia :
o Pada atau di bawah permukaan air.
o Pembubuhan beberapa bahan kimia secara bersamaan atau berurutan.
o Lokasi pembubuhan relatif terhadap peralatan pengadukan, dll.
• Kepekatan larutan kimia.
• Waktu penjernihan.
Terpisah dari parameter-parameter di atas, yang juga harus dimonitor adalah :
• Temperatur air di dalam beaker glass.
• Kekeruhan, warna, alkalinitas air baku dan air yang telah diolah.
• Metode pengeluaran air sample.
• Peralatan percobaan laboratorium dan prosedur analisa laboratorium.
1.2 Tujuan Praktikum.
Setelah melakukan praktikum, diharapkan mahasiswa mampu :
• Memahami kegunaan proses preklorinasi.
• Menentukan dosis kaporit pada proses preklorinasi.
• Menghitung debit pembubuhan kaporit.
• Melakukan Jar test.
• Menentukan dosis optimum koagulan.
• Menghitung debit pembubuhan koagulan.
2. DASAR TEORI
2.1 Koagulasi-flokulasi
Koagulasi adalah proses destabilisasi koloid dengan penambahan koagulan melalui pengadukan cepat hingga terbentuk mikroflok. Sedangkan flokulasi adalah proses pengadukan lambat untuk memberi waktu mikroflok bertumbukan dan bersatu membentuk makroflok.
Faktor-faktor yang mempengaruhi efisiensi proses koagulasi-flokulasi, antara lain :
• Zat Anorganik; akan mempengaruhi proses flokulasi dengan
koagulan-flokulan, sebab secara kimiawi akan membentuk senyawa sebagai endapan hidroksida misalnya ion fosfat, sulfat, kalsium, dan magnesium. Dengan demikian jangkauan pH optimum untuk pengendapan hidroksida metal secara kimiawi diperluas. Selain itu secara langsung dipengaruhi oleh konsentrasi CO2 atau kapasitas dapar /
buffer karena berpengaruh terhadap pH sebelum dan sesudah koagulasi, jika tidak dilakukan penetapan pH dengan asam atau basa untuk proses stabilisasi.
• Zat Organik; alami terlarut atau sintetis yang terkandung di dalam air
yang akan diolah sangat mempengaruhi proses koagulasi-flokulasi, selain adsorpsi di atas permukaan zat padat yang menyebabkan efek stabilitas, juga terjadi pembentukan molekul kompleks dengan zat koagulan-flokulan yang menurunkan efisiensi koagulan-flokulan menyebabkan kebutuhan koagulan-flokulan menjadi lebih besar.
• pH; jenis koagulan memiliki range pH optimum tertentu dan pada pH
lebih besar dari 7,8 ion aluminat Al(OH)4 yang terbentuk bermuatan
negatif dan larut dalam air, selama koagulasi pengaruh pH air terhadap ion H+ dan OH- adalah sangat penting dalam menentukan muatan hasil
dan HPO42- dapat diganti dengan ion-ion OH- dalam kompleks, oleh
karena itu dapat berpengaruh terhadap sifat-sifat endapan. 2.2 Koagulan
Koagulan adalah zat kimia yang menyebabkan destabilisasi muatan negatif partikel di dalam suspensi. Zat ini merupakan donor muatan positif yang digunakan untuk mendestabilisasi muatan negatif partikel, dalam pengolahan air sering dipakai garam dari aluminium ( Al3+ ) atau garam dari
besi ( Fe2+ dan Fe 3+ ).
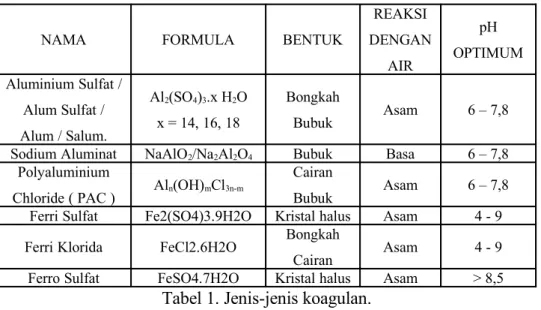
Jenis-jenis koagulan yang umumnya sudah dikenal dan digunakan :
NAMA FORMULA BENTUK
REAKSI DENGAN AIR pH OPTIMUM Aluminium Sulfat / Alum Sulfat / Alum / Salum. Al2(SO4)3.x H2O x = 14, 16, 18 Bongkah Bubuk Asam 6 – 7,8
Sodium Aluminat NaAlO2/Na2Al2O4 Bubuk Basa 6 – 7,8
Polyaluminium
Chloride ( PAC ) Aln(OH)mCl3n-m
Cairan
Bubuk Asam 6 – 7,8
Ferri Sulfat Fe2(SO4)3.9H2O Kristal halus Asam 4 - 9
Ferri Klorida FeCl2.6H2O Bongkah
Cairan Asam 4 - 9
Ferro Sulfat FeSO4.7H2O Kristal halus Asam > 8,5
Tabel 1. Jenis-jenis koagulan. 2.3 Preklorinasi
Preklorinasi adalah tahap pertama desinfeksi yang bertujuan untuk mempertahankan kandungan sisa klor sebesar 0,2 – 0.4 mg/L pada seluruh unit pengolahan dalam suatu system ( bersamaan dengan oksidasi ).
Manfaat preklorinasi khususnya diproses koagulasi-flokulasi, antara lain :
• Mengurangi kandungan zat organik dalam air baku.
• Menurunkan kadar kekeruhan air baku.
• Dengan preklorinasi kerja koagulan akan lebih efektif.
Preklorinasi dilakukan sebelum pembubuhan koagulan, bilamana kualitas air baku tidak baik, kekeruhan tinggi, dan kandungan zat organiknya besar.
2.4 Daya Pengikat Klor ( DPK ).
DPK adalah kebutuhan klor dengan waktu kontak yang sudah pasti ( tertentu ) untuk mendapatkan sisa klor yang tersedia cukup efektif untuk desinfeksi, DPK secara tidak langsung menyatakan oksidasi zat organik secara lengkap.
DPK terutama digunakan dalam kasus dimana air mempunyai kualitas yang tidak baik ( mengoksidasi Fe2+ dan Mn2+, menghilangkan rasa, mencegah pertumbuhan bakteri dalam filter, memperpanjang waku penyaringan dan mencegah tumbuhnya alga ).
2.5 Jar Test
Jar test adalah suatu metode untuk mengevaluasi proses-proses koagulasi-flokulasi, yang memberikan data mengenai kondisi optimum untuk parameter-parameter proses.
Kegunaan Jar test :
• Bagi operator instalasi; membantu dalam mengoptimalisasi proses-proses koagulasi, flokulasi, dan penjernihan.
• Bagi ahli teknik ( engineer ); membantu dalam merancang bangunan IPA yang baru atau memperbaiki instalasi yang ada.
Evaluasi :
Dengan mengulangi percobaan-percobaan dengan dosis yang sedikit lebih tinggi dan sedikit lebih rendah dari dosis optimum yang diperoleh dari seri percobaan awal, maka akan didapat lebih banyak data yang akurat mengenai dosis-dosis bahan kimia dan batas-batas pH optimum.
3.1 Pengukuran pH, Temperatur, dan kekeruhan pada air sample murni
NO NAMA ALAT UKURAN
( mL )
JUMLAH
( buah ) NAMA BAHAN
VOLUME ( mL )
1 Beaker glass 100 3 Air Sample 300
2 pH Meter - 1 Aquadest ?
3 Termometer - 1
4 Turbidy Meter - 1
Tabel 2. Peralatan & Bahan Prosedur percobaan :
a. Pengukuran pH dan Temperatur :
• Siapkan alat ukur.
• Masukan air sample ke dalam beaker glass hingga tanda batas.
• Bilas elektroda alat ukur dengan aquadest.
• Celupkan elektroda ke dalam air sample ( jangan menyentuh dasar atau dinding beaker glass ).
• Tunggu sampai penunjukan angka pada monitor stabil.
• Catat hasil pengukuran pada tiap beaker glass, lalu rata-ratakan. b. Pengukuran kekeruhan :
• Kocok sample dengan sempurna, tunggu sampai tidak ada gelembung udara.
• Ambil air sample, masukan ke kuvet hingga tanda batas.
• Bersihkan bagian luar kuvet dengan tissue.
• Tekan “ON”, masukan kuvet 0 NTU lalu tekan “READ”, tunggu hingga monitor menunjukan “0”.
• Keluarkan kuvet 0 NTU, masukan kuvet yang berisi air sample.
• Tekan “READ”, tunggu hingga pembacaan stabil.
• Catat hasil pembacaan alat, tekan “Off” lalu keluarkan kuvet. 3.2 Uji kadar klor aktif
NO NAMA ALAT UKUR AN ( mL ) JUMLAH ( buah ) NAMA
BAHAN KONSENTRASI VOLUME
1 Pipet ukur 10 1 K2Cr2O7 0,025 N 25 mL
2 Pipet filler - 1 Aquadest - 25 mL
3 Erlenmeyer 250 1 KI serbuk - 2 Gr
4 Gelas ukur 100 1 HCL pekat - 8 mL
5 Neraca - 1 Na2S2O3 - 50 mL
6 Spatula - 1 Amylum - 3 mL
7 Klem statis - 1
8 Corong - 1
9 Buret 50 1
Tabel 3. Peralatan & Bahan Prosedur percobaan :
• Pipet 25 mL larutan K2Cr2O7, masukan ke dalam erlenmeyer.
• Tambahkan 25 mL aquadest dan 2 gr KI, aduk hingga larut.
• Tambahkan 8 mL HCL pekat.
• Titrasi dengan larutan Na-thiosulfat sampai warna kuning muda.
• Tambahkan 3 mL larutan amylum.
• Lanjutkan titrasi sampai warna biru tepat hilang. b. Penentuan kadar klor aktif dalam kaporit.
NO NAMA ALAT UKUR AN ( mL ) JUMLAH ( buah ) NAMA
BAHAN KONSENTRASI VOLUME
1 Pipet ukur 10 1 Kaporit 0,1 % 10 mL
2 Pipet filler - 1 Aquadest - 90 mL
3 Erlenmeyer 250 1 KI serbuk - 1 Gr
4 Labu ukur 100 1 CH3COOH - 3 mL
5 Neraca - 1 Na2S2O3 - 50 mL 6 Spatula - 1 Amylum - 3 mL 7 Klem statis - 1 8 Corong - 1 9 Buret 50 1 10 Btl.semprot 500 1
Tabel 4. Peralatan & Bahan Prosedur percobaan :
• Pipet 10 mL larutan kaporit 0,1 %, masukan ke labu ukur 100 mL.
• Tambahkan aquadest hingga tanda batas meniskus ( 100 mg/L ).
• Pindahkan larutan ke erlenmeyer, tambahkan 1 gr KI lalu aduk rata.
• Titrasi dengan larutan Na-thiosulfat sampai warna kuning muda.
• Tambahkan 3 mL larutan amylum, lanjutkan titrasi sampai warna biru tepat hilang (hasil titrasi = A ).
Analisa larutan blanko :
• Masukan aquadest ke dalam labu ukur 100 mL, pindahkan ke erlenmeyer lalu tambahkan 1 gr KI dan aduk hingga larut.
• Tambahkan 3 mL larutan amylum, titrasi dengan larutan Na-thiosulfat ( jika tidak terbentuk warna biru , maka B = 0 ).
3.3 Penentuan DPK NO NAMA ALAT UKUR AN ( mL ) JUMLAH ( buah ) NAMA
BAHAN KONSENTRASI VOLUME
1 Beaker
glass 100 1 Air sample - 1000 mL
2 Pipet ukur 10 1 Larutan
kaporit 0,1 % 3 mL
3 Pipet filler - 1 Tablet DPD
No.1 - 1 biji
4 Pengaduk - 1
5 Komparator - 1
Tabel 5. Peralatan & Bahan Prosedur percobaan :
• Masukan 1000 mL sample ke dalam beaker glass.
• Tambahkan 3 mL larutan kaporit 0,1 %, aduk rata.
• Simpan beaker di tempat yang terlindung dari cahaya selama 20 menit.
• Uji sisa klor bebas selama waktu kontak yang dipilih menggunakan Komparator LOVIBOND. misal a mg/L Cl 2.
• Tentukan kadar klor aktif dalam kaporit., misal s %
• Hitung dosis kaporit .
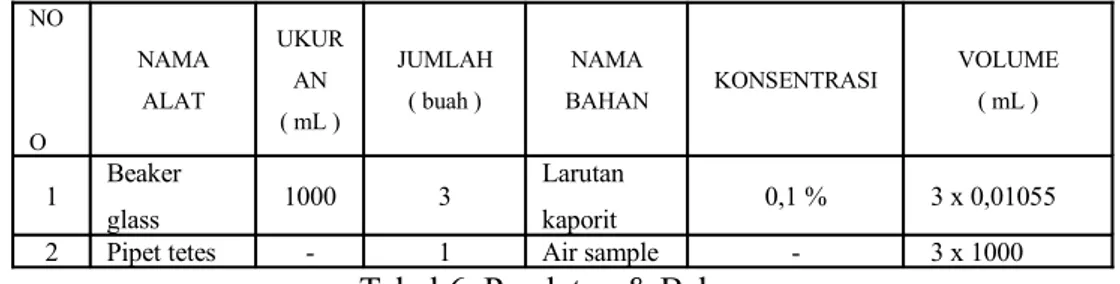
3.4 Pengukuran pH, Temperatur, dan kekeruhan setelah proses preklorinasi NO O NAMA ALAT UKUR AN ( mL ) JUMLAH ( buah ) NAMA BAHAN KONSENTRASI VOLUME ( mL ) 1 Beaker glass 1000 3 Larutan kaporit 0,1 % 3 x 0,01055
2 Pipet tetes - 1 Air sample - 3 x 1000
Tabel 6. Peralatan & Bahan Prosedur percobaan proses preklorinasi :
• Masukan air sample ke beaker glass 1000 mL hingga tanda batas.
• Tambahkan larutan kaporit 0,1 % ( dosis sesuai perhitungan DPK ). Prosedur percobaan pengukuran pH, temperatur, dan kekeruhan sama dengan di halaman 6 ( catatan : sample + DPK ).
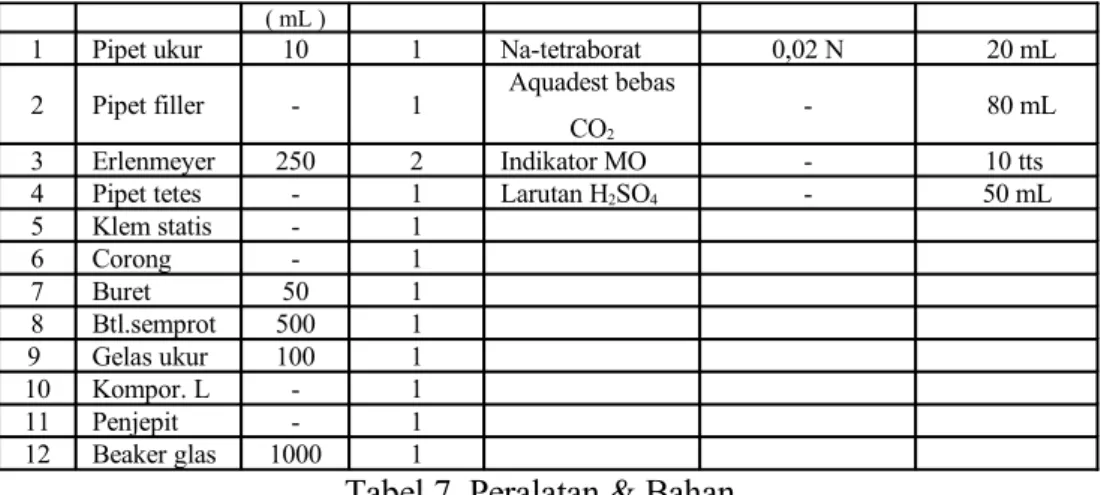
3.5 Pengukuran alkalinitas setelah proses klorinasi. a. Standarisasi larutan H2SO4 : 0,02 N NO NAMA ALAT UKUR AN JUMLAH ( buah ) NAMA BAHAN KONSENTRASI VOLUME
( mL )
1 Pipet ukur 10 1 Na-tetraborat 0,02 N 20 mL
2 Pipet filler - 1 Aquadest bebas
CO2
- 80 mL
3 Erlenmeyer 250 2 Indikator MO - 10 tts
4 Pipet tetes - 1 Larutan H2SO4 - 50 mL
5 Klem statis - 1 6 Corong - 1 7 Buret 50 1 8 Btl.semprot 500 1 9 Gelas ukur 100 1 10 Kompor. L - 1 11 Penjepit - 1 12 Beaker glas 1000 1
Tabel 7. Peralatan & Bahan
Prosedur percobaan :
• Pipet 20 mL larutan Na-tetraborat 0,02 N, masukan ke erlenmeyer.
• Tambahkan 30 mL aquadest bebas CO2 dan 5 tetes indikator MO.
• Titrasi dengan larutan H2SO4 sampai terjadi perubahan warna dari
kuning menjadi jingga / orange .
• Catat pemakaian H2SO4, masukan kedalam perhitungan.
• Buat larutan pembanding untuk mempermudah TAT, sbb :
o Masukan 50 mL aquadest bebas CO2 ke dalam erlenmeyer.
o Tambahkan 5 tetes indikator MO dan 1-2 tetes larutan H2SO4.
b. Penentuan alkalinitas ( untuk sample dengan pH > 8,2 ) NO NAMA ALAT UKUR AN ( mL ) JUMLAH ( buah ) NAMA
BAHAN KONSENTRASI VOLUME
1 Gelas ukur 100 1 Air sample - 100 mL
2 Btl.semprot - 1 Indikator PP - 5 tts
3 Erlenmeyer 250 2 Indikator MO - 5 tts
4 Pipet tetes - 1 Larutan H2SO4 - 50 mL
5 Klem statis - 1
6 Corong - 1
Tabel 8. Peralatan & Bahan Prosedur percobaan :
• Ukur 100 mL sample, masukan ke dalam erlenmeyer.
• Tambahkan 2-3 tetes indikator PP, titrasi dengan larutan H2SO4
sampai warna merah tepat hilang ( masukan mL pemakaian larutan H2SO4 ke dalam perhitungan sebagai Palk ).
• Tambahkkan 5 tetes indikator MO, lanjutkan titrasi sampai terjadi perubahan warna indikator.
• Catat pemakaian larutan H2SO4 total, masukan ke dalam perhitungan
sebagai Talk.
3.6 Jar Test
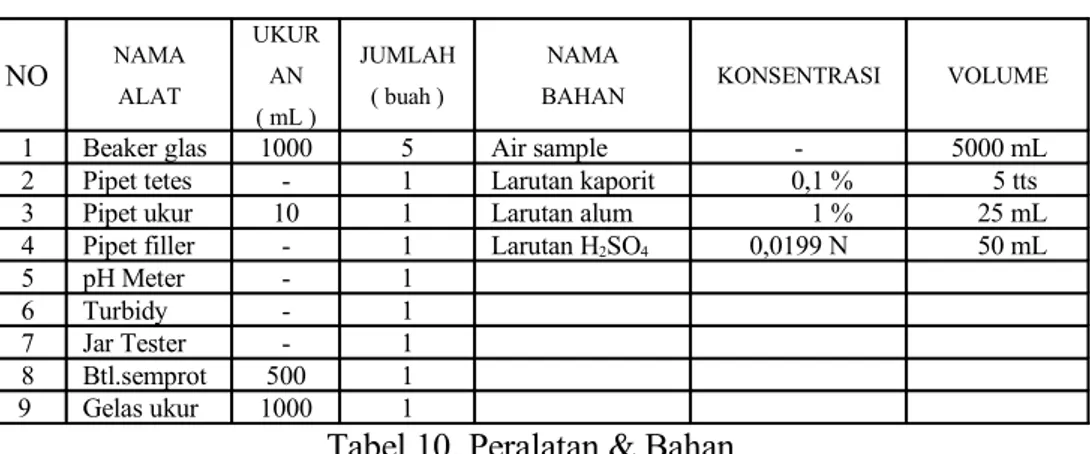
a. Penentuan dosis optimum NO NAMA ALAT UKUR AN ( mL ) JUMLAH ( buah ) NAMA
BAHAN KONSENTRASI VOLUME
1 Beaker glas 1000 5 Air sample - 5000 mL
2 Pipet tetes - 1 Larutan kaporit 0,1 % 5 tts
3 Pipet ukur 10 1 Larutan alum 1 % 15 mL
4 Pipet filler - 1 5 pH Meter - 1 6 Turbidy - 1 7 Jar Tester - 1 8 Btl.semprot 500 1 9 Gelas ukur 1000 1
Tabel 9. Peralatan & Bahan Prosedur percobaan :
• Siapkan 5 buah beaker glass, ke dalam masing-masing beaker glass masukan 1000 mL air sample.
• Tambahkan 1 tetes larutan kaporit 0,1 % ke tiap beaker glass.
• Letakan tiap beaker glass di bawah rotor jar tester, turunkan tiap rotor hingga kedalaman 10 cm dari permukaan air sample.
• Masukan larutan alum 1 % ke dalam beaker glas masing-masing 1 mL, 2 mL, 3 mL, 4 mL,dan 5 mL.
• Karena pH sample terklorinasi > 7 , maka tidak direkomendasikan penambahan NaOH.
• Atur kecepatan rotor pada 150 rpm untuk pengadukan cepat selama 30-60 detik, amati dan catat pertama kali flok terbentuk..
• Lalu atur kecepatan rotor pada 50 rpm untuk pengadukan lambat selama 15-20 menit. ( amati dan catat ukuran flok pada masing-masing beaker setiap 5 menit pengadukan dengan Gambar Ukuran Flok sebagai pembanding.
• Setelah itu diamkan flok mengendap selama 20-30 menit.
• Ukur pH dan kekeruhan setelah waktu pengendapan di tiap beaker glass ( untuk masing-masing dosis koagulan ), lalu buat grafik dan kurva antara Dosis Koagulan Vs Kekeruhan ( posisi dosis koagulan di sumbu X dan kekeruhan di sumbu Y ).
• Tentukan dosis optimum, dengan cara :
o Tarik garis Tangen = 1 atau sudut = 45o.
o Buat garis yang sejajar dengan garis Tangen = 1 sampai ada yang menyinggung kurva di satu titik.
o Dari titik singgung, tarik garis lurus menuju sumbu X sehingga akan menunjukan nilai dosis alum yang optimum.
b. Penentuan pH optimum NO NAMA ALAT UKUR AN ( mL ) JUMLAH ( buah ) NAMA
BAHAN KONSENTRASI VOLUME
1 Beaker glas 1000 5 Air sample - 5000 mL
2 Pipet tetes - 1 Larutan kaporit 0,1 % 5 tts
3 Pipet ukur 10 1 Larutan alum 1 % 25 mL
4 Pipet filler - 1 Larutan H2SO4 0,0199 N 50 mL
5 pH Meter - 1
6 Turbidy - 1
7 Jar Tester - 1
8 Btl.semprot 500 1
9 Gelas ukur 1000 1
Tabel 10. Peralatan & Bahan Prosedur percobaan :
• Siapkan 5 buah beaker glass, ke dalam masing-masing beaker glass masukan 1000 mL air sample.
• Tambahkan 1 tetes larutan kaporit 0,1 % ke tiap beaker glass.
• Letakan tiap beaker glass di bawah rotor jar tester, turunkan tiap rotor hingga kedalaman 10 cm dari permukaan air sample.
• Ke dalam masing-masing beaker glass tambahkan larutan H2SO4
masing-masing : 8, 9, 10, 11, dan 12 mL, lalu masukan 5 mL larutan alum 1 %.
• Atur kecepatan rotor pada 150 rpm untuk pengadukan cepat selama 30-60 detik, amati dan catat pertama kali flok terbentuk..
• Lalu atur kecepatan rotor pada 50 rpm untuk pengadukan lambat selama 15-20 menit. ( amati dan catat ukuran flok pada masing-masing beaker setiap 5 menit pengadukan dengan Gambar Ukuran Flok sebagai pembanding.
• Setelah itu diamkan flok mengendap selama 20-30 menit.
• Ukur pH dan kekeruhan setelah waktu pengendapan di tiap beaker glass ( untuk masing-masing dosis koagulan ), lalu buat grafik dan kurva antara pH Vs Kekeruhan ( posisi pH di sumbu X dan kekeruhan di sumbu Y ).
• Tentukan pH optimum, dengan cara :
o Tarik garis yang sejajar dengan sumbu X pada grafik untuk nilai kekeruhan 2 NTU dan 5 NTU ( akan didapat 2 titik singgung ).
o Dari masing-masing titik singgung tarik garis lurus menuju sumbu X ( ke bawah ), sehingga akan didapat 2 nilai pH yang menjadi batas-batas pH optimum.
c. Perhitungan volume endapan. NO NAMA ALAT UKUR AN ( mL ) JUMLAH ( buah ) NAMA
BAHAN KONSENTRASI VOLUME
Imhof
2 Pewaktu - 1 Larutan kaporit 0,1 % 1 tts
3 Beaker glas 1000 1 Larutan alum 1 % 5 mL
4 Jar Tester - 1 Larutan H2SO4 0,0199 N 9 m L
Tabel 11. Peralatan & Bahan Prosedur percobaan :
• Masukan air yang telah diolah ( hasik koagulasi dengan dosis koagulan optimum dan pH optimum ) ke dalam Kerucut Imhof.
• Biarkan semua flok mengendap, catat waktu total pengendapan.
• Ukur volume endapan, masukan kedalam perhitungan. 4. HASIL
4.1 Data pengamatan
* Pengukuran pH, Temperatur,dan kekeruhan pada air sample murni :
Beaker Glass pH Temperatur
( oC ) Kekeruhan ( NTU ) I 8,40 28 II 8,36 29 519 III 8,37 29
Tabel 12. Hasil praktikum 1 * Uji kadar klor aktif :
Analisa Pemakaian
Na-thiosulfat Standarisasi larutan Na-Thiosulfat 30,1 mL Penentuan kadar klor aktif dalam kaporit 0,5 mL
Tabel 13. Hasil praktikum 2 * Penentuan DPK :
Analisa Hasil
Sisa klor bebas ( a ) a = 0,1
Kadar klor aktif dalam kaporit ( s % ) s = 3,685 Tabel 14. Hasil praktikum 3
* Pengukuran pH, Temperatur, dan kekeruhan setelah proses preklorinasi ( air sample + DPK ) :
Beaker Glass pH Temperatur ( oC ) Kekeruhan ( NTU ) I 8,35 28 II 8,35 28 348 III 8,35 29
Tabel 15. Hasil praktikum 4 * Pengukuran alkalinitas setelah proses preklorinasi
Analisa Pemakaian H2S04
Standarisasi larutan H2SO0,02 N 20 mL
Penentuan alkalinitas 8 mL
Tabel 16. Hasil praktikum 5
* Jar Test
- Penentuan dosis optimum koagulan Data air baku :
• pH : 8,377 • Kekeruhan : 519 NTU • Konsentrasi alum : 1 % ( 1 mL ≈ 10 mg ) DOSIS KOAGULAN ( mg/L Al2(SO4)3 . x H2O ) PARAMETER 10 20 30 40 50 Sample + DPK
Pertama kali flok
terbentuk ( detik ) - - -
-Ukuran flok dalam
5 menit A B C C C
-Ukuran flok dalam
10 menit A B C C D
-Ukuran flok dalam
15 menit A B C D D
-Waktu endapan 10
cm ( menit ) - - -
Kekeruhan (NTU) 141 97 42,96 25,49 10,36 348
Dosis Optimum √
Tabel 17. Hasil praktikum 6 - Penentuan pH optimum
Data :
• Dosis alum optimum : 50 mg/L
• Bahan alkali yang digunakan : H2SO4
• Konsentrasi larutan : 0,0199 N DOSIS H2SO4 ( mL ) PARAMETER 8 9 10 11 12 Sample + DPK
Pertama kali flok
terbentuk ( detik ) - - -
-Ukuran flok dalam
5 menit A A A A A
-Ukuran flok dalam
10 menit B B B B B
-Ukuran flok dalam
15 menit B B B B B -Waktu endapan 10 cm ( menit ) - - - -pH 7,52 6,91 6,89 6,52 6,29 8,35 Kekeruhan (NTU) 17,92 17,15 23,89 22,23 34,17 348 pH Optimum √
Tabel 18. Hasil praktikum 7 - Volume endapan ( kadar Lumpur )
Data :
• Kadar klor aktif dalam kaporit : 3,685 %
• Waktu kontak : 20 menit.
• DPK : 0,01055 mg/L Cl2 Kadar Lumpur ( mL ) Volume Air ( mL ) Lama Pengendapan ( menit ) 10,1 900 41
Tabel 19. Hasil praktikum 8
4.2 Perhitungan
* Pengukuran sample :
o pH rata-rata = ( 8,40 + 8,36 + 8,37 ) / 3 = 8,377
o T rata-rata = ( 28,0 + 29,0 + 29,0 ) / 3 = 28,67 oC
o Kekeruhan = 519 NTU. * Uji kadar klor aktif :
- Standarisasi Natrium Thiosulfat :
N Na-thiosulfat = ( V x N )K2Cr2O7 / VNa-thiosulfat
= ( 25 x 0,025 ) / 30,1 = 0,021 N
- Kandungan klor aktif :
mg/L Cl2 = [ 1000 x ( A-B ) x N Na thiosulfat x 35,43 ] / V dititrasi
= [ 1000 x ( 0,5 - 0 ) x 0,021 x 35,43 ] / 100 = 3,72
- Kadar klor aktif dalam kaporit :
s % = mg/L Cl2 x 100 % / Konsentrasi kaporit
= 3,72 x 100 % / 100 = 3,72 %
- Sisa klor bebas = 0,1 mg/L Cl2 → ( menggunakan komparator ) - DPK : mg/L Cl2 = ( 3 s / 100 ) – a = ( 3 x 3,72 / 100 ) – 0,1 = 0,0116 - Volume kaporit : Vkaporit = 0,0116 x 1 / 10 = 0,00116 mg/L Cl2 ≈ 1 tetes.
* % penurunan kekeruhan setelah preklorinasi :
% = ( Sebelum – Sesudah ) x 100 % / Sebelum = ( 519 – 348 ) x 100 % / 519
= 32,95 %
* Pengukuran alkalinitas sample + DPK : - Standarisasi larutan H2SO4 0,02 N :
NH2SO4 = ( 1000 x W x A ) / ( 190,685 x B x C )
= ( 1000 x 0,95 x 20 ) / ( 190,685 x 20 x 250 ) = 0,0199 N
- Penentuan alkalinitas :
mg/L CaCO3 = 1000 x E x NH2SO4 x 50 / Vsample
= 1000 x 8 x 0,0199 x 50 / 100 = 79,6
* Perhitungan dari hasil Jar Test : - Penentuan dosis alum optimum :