GAMBARAN HISTOLOGIS GINJAL MENCIT (
Mus musculus
L.) STRAIN DDW SETELAH PEMBERIAN EKSTRAK
N-HEKSAN BUAH ANDALIMAN (
Zanthoxylum acanthopodium
DC.)
SKRIPSI
MIDUK ULIARTA SIANIPAR
080805042
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN
ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
GAMBARAN HISTOLOGIS GINJAL MENCIT (
Mus musculus
L.) STRAIN DDW SETELAH PEMBERIAN EKSTRAK
N-HEKSAN BUAH ANDALIMAN (
Zanthoxylum acanthopodium
DC.)
SKRIPSI
Penelitian ini diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains pada Fakultas Matematika dan Ilmu bengetahuan Alam
Universitas Sumatera Utara
MIDUK ULIARTA SIANIPAR
080805042
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN
ALAM
2014
PERSETUJUAN
Judul : GAMBARAN HISTOLOGIS GINJAL MENCIT
(Mus musculus L.) STRAIN DDW SETELAH
PEMBERIAN EKSTRAK N-HEKSAN BUAH ANDALIMAN (Zanthoxylum acanthopodium DC.)
Kategori : SKRIPSI
Nama : MIDUK ULIARTA SIANIPAR
Nomor Induk Mahasiswa : 080805042
Program Studi : SARJANA (S-1) BIOLOGI Departemen : BIOLOGI
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Komisi Pembimbing
Pembimbing 2
Diluluskan di
Medan, Agustus 2014
:
Pembimbing 1
Dr. Salomo Hutahaean, M.Si Dra. Emita Sabri, M.Si NIP. 19651011 199501 1 001 NIP. 19560712 198702 2 002
Diketahui/Disetujui Oleh
Departemen Biologi FMIPA USU Ketua,
PENGHARGAAN
Puji dan syukur penulis panjatkan ke hadirat Tuhan Yang Maha Esa karena atas berkat dan karunia-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul “GAMBARAN HISTOLOGIS GINJAL MENCIT (Mus musculus L.) STRAIN DDW SETELAH PEMBERIAN EKSTRAK N-HEKSAN BUAH ANDALIMAN (Zanthoxylum acanthopodium DC.)” yang merupakan syarat untuk melengkapi dan memenuhi syarat mencapai gelar Sarjana Sains di Departemen Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara.
Pada kesempatan ini penulis mengucapkan terima kasih kepada Ibu Dra. Emita Sabri, M.Si selaku Dosen Pembimbing I dan Bapak Dr. Salomo Hutahaean, M.Si selaku dosen pembimbing II yang telah banyak memberikan dorongan, bimbingan, dan arahan, waktu serta perhatian yang besar selama penulisan dan penyusunan hasil penelitian ini. Ucapan terima kasih juga penulis sampaikan kepada Bapak Prof. Dr. Syafruddin Ilyas, M. Biomed dan Ibu Dra. Elimasni, M.Si selaku Dosen Penguji yang telah banyak memberikan arahan dan saran dalam penyempurnaan penulisan hasil penelitian ini. Penulis juga mengucapkan terima kasih kepada Ibu Dr. Nursahara Pasaribu, M.Sc selaku Ketua Departemen Biologi FMIPA USU, Bapak Drs. Kiki Nurtjahja, M.sc selaku sekretaris Departemen Biologi FMIPA USU sekaligus Dosen Pembimbing Akademik yang telah banyak memberikan arahan dan motivasi mulai dari awal perkuliahan sampai penyusunan hasil penelitian ini, Bapak Dr. Sutarman, M.Sc selaku Dekan FMIPA USU, Ibu Mizarwati, S.Si selaku Ketua Panitia Seminar Departemen Biologi FMIPA USU, Ibu Nurhasni Muluk yang selalu setia membantu penulis dalam melengkapi peralatan dan bahan saat penelitian, Abang Erwin, dan Ibu Roslina Ginting selaku staf pegawai Departemen Biologi FMIPA USU.
Teristimewa penulis sampaikan rasa terima kasih yang sebesar-besarnya kepada orangtua saya tercinta: A. Sianipar dan H. Br. Sitompul yang dengan sabar dan tiada mengenal lelah untuk mendukung pendidikan penulis mulai dari kecil hingga sekarang, yang tulus memberikan doa, dana dan kasih sayang yang luar biasa sehingga penulis bisa menyelesaikan skripsi ini. Terima kasih juga penulis ucapkan kepada adik-adikku yang memberikan motivasi dan kasih sayang yang begitu besar kepada penulis.
Kepada sahabat-sahabatku tersayang (Michimelnaztha) Azmi, Chister, Mela, Ina, dan Agnez, there is nothing too hard when we’re together, fighting!. Kepada kakak asuhku Deni Simarmata, dan adik asuhku Sandi Sianturi dan Sri Hasianna Sinaga, yang telah banyak memberikan bantuan, dukungan dan motivasi kepada penulis. Kepada tim PKM Adi Gunawan, Mela, dan Rahmad Jaiz keep moving, keep moving, for better future!. Kepada seluruh asisten Laboratorium Struktur Hewan dan Laboratorium Fisiologi Hewan atas kekompakan dan kerjasamanya. Terimakasih juga kepada adik junior stambuk 2009, stambuk 2010 (seluruh adik asuh tercinta), stambuk 2011, stambuk 2012 dan stambuk 2013 yang selalu memberikan semangat.
Akhirnya, dengan segala kerendahan hati penulis menyadari bahwa skripsi ini masih jauh dari sempurna. Oleh karena itu, penulis mengharapkan kritik dan saran demi kesempurnaan hasil penelitian ini. Penulis berharap karya yang sederhana ini dapat bermanfaat bagi semua pihak, bagi penulis pada khususnya dan para pembaca serta bermanfaat bagi bagi perkembangan ilmu pengetahuan. Sebelum dan sesudahnya penulis mengucapkan terima kasih. Semoga Kasih-Nya beserta kita, Amin.
Medan, Agustus 2014
GAMBARAN HISTOLOGIS GINJAL MENCIT (Mus musculus L.) STRAIN DDW SETELAH PEMBERIAN EKSTRAK N-HEKSAN BUAH
ANDALIMAN (Zanthoxylum acanthopodium DC.)
ABSTRAK
Penelitian dilakukan untuk mengetahui efek dari ekstrak N-heksan buah andaliman (Zanthoxylum acanthopodium DC.) terhadap struktur histologis ginjal mencit (Mus musculus L.) strain DDW. Percobaan yang dilakukan menggunakan Rancangan Acak Lengkap (RAL) dengan 5 perlakuan dan 6 ulangan. Perlakuan terdiri dari kontrol blank (P0), kontrol pelarut 1% CMC (P1), Ekstrak N-hekan buah andaliman (2% = P2), (4%=P3) dan (6%=P4). Semua perlakuan diberikan secara oral dengan menggunakan jarum gavage (0,1 ml/10g/bb) mulai dari hari pertama sampai hari kesepuluh kebuntingan. Hasil menunjukkan bahwa ekstrak N-heksan buah andaliman memberikan pengaruh yang signifikan terhadap struktur histologis ginjal mencit (P < 0,05).
Keywords: histologis ginjal, ekstrak buah andaliman, tubulus proksimal, N-heksan
THE HISTOLOGICAL APPEARANCE OF DDW MICE’S KIDNEY (Mus
muscullus L.) AFTER THE ADMINISTERING OF ANDALIMAN FRUIT
EKSTRACT (Zanthoxylum acanthopodium DC.)
ABSTRACT
The research has been conducted to study the effect of N-hexane extract of the andaliman fruit (Zanthoxylum acanthopodium DC.) to the histologic structure of mice kidney (Mus musculus L.) strain DDW. Experiment was carried out using Completely Randomized Design (CDR) with 5 treatments and 6 replication. Treatments consist of untreated control (T0), solvent control 1 % of CMC (T1), N-hexane extract of andaliman fruit (2%= T2), (4%=T3) and (6%=T4). All treatments were given by oral gavage (0,1 ml/10g/bw) start from 1st day to 10th days of gestation. The result showed that N-hexane extract of the andaliman fruit give significant effect to the histologic structure of mice kidney (p < 0,05).
DAFTAR ISI 2.1 Tanaman Andaliman (Zanthoxylum acanthopodium DC.) 6
2.2 Ginjal (Ren) 9
3.3.2 Hewan Percobaan 15
3.3.3 Rancangan Penelitian 16
3.3.4 Pemberian Perlakuan 16
3.3.5 Penimbangan Berat Ginjal 17 3.3.6 Pembuatan Preparat Ginjal Mencit dengan 17
Metode Parafin 3.4 Parameter Pengamatan
3.4.1 Pengamatan Berat Ginjal 19
3.4.2 Pengamatan Kerusakan Tubulus Proksimal Ginjal 19 3.4.3 Pengamatan Diameter Tubulus Proksimal yang 19
BAB 5 KESIMPULAN DAN SARAN
5.1 Kesimpulan 30
5.2 Saran 30
DAFTAR PUSTAKA 31
DAFTAR TABEL
Halaman
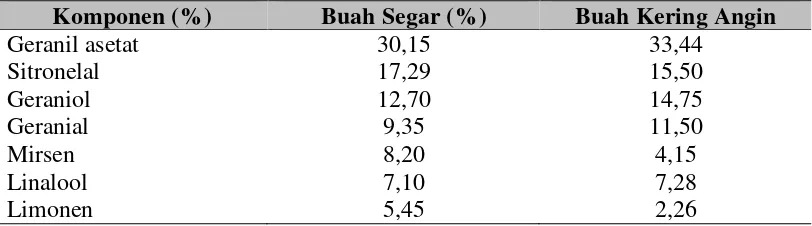
Tabel 2.1. Komponen Minyak Buah Andaliman Segar dan Kering Angin dengan Teknik Kromatografi Gas 8
DAFTAR GAMBAR
Halaman
Gambar 2.1. Tanaman Andaliman 7
Gambar 2.2.1 Gambaran Makroskopis Ginjal 9 Gambar 2.2.3.1 Ginjal dan Nefron 12
Gambar 2.2.3.2 Histologi Ginjal 12
Gambar 4.1 Diagram Berat Ginjal 21
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Data Analisis Statistik 34
Lampiran 2. Foto Pengamatan Tubulus Proksimal yang Menutup 51
GAMBARAN HISTOLOGIS GINJAL MENCIT (Mus musculus L.) STRAIN DDW SETELAH PEMBERIAN EKSTRAK N-HEKSAN BUAH
ANDALIMAN (Zanthoxylum acanthopodium DC.)
ABSTRAK
Penelitian dilakukan untuk mengetahui efek dari ekstrak N-heksan buah andaliman (Zanthoxylum acanthopodium DC.) terhadap struktur histologis ginjal mencit (Mus musculus L.) strain DDW. Percobaan yang dilakukan menggunakan Rancangan Acak Lengkap (RAL) dengan 5 perlakuan dan 6 ulangan. Perlakuan terdiri dari kontrol blank (P0), kontrol pelarut 1% CMC (P1), Ekstrak N-hekan buah andaliman (2% = P2), (4%=P3) dan (6%=P4). Semua perlakuan diberikan secara oral dengan menggunakan jarum gavage (0,1 ml/10g/bb) mulai dari hari pertama sampai hari kesepuluh kebuntingan. Hasil menunjukkan bahwa ekstrak N-heksan buah andaliman memberikan pengaruh yang signifikan terhadap struktur histologis ginjal mencit (P < 0,05).
Keywords: histologis ginjal, ekstrak buah andaliman, tubulus proksimal, N-heksan
THE HISTOLOGICAL APPEARANCE OF DDW MICE’S KIDNEY (Mus
muscullus L.) AFTER THE ADMINISTERING OF ANDALIMAN FRUIT
EKSTRACT (Zanthoxylum acanthopodium DC.)
ABSTRACT
The research has been conducted to study the effect of N-hexane extract of the andaliman fruit (Zanthoxylum acanthopodium DC.) to the histologic structure of mice kidney (Mus musculus L.) strain DDW. Experiment was carried out using Completely Randomized Design (CDR) with 5 treatments and 6 replication. Treatments consist of untreated control (T0), solvent control 1 % of CMC (T1), N-hexane extract of andaliman fruit (2%= T2), (4%=T3) and (6%=T4). All treatments were given by oral gavage (0,1 ml/10g/bw) start from 1st day to 10th days of gestation. The result showed that N-hexane extract of the andaliman fruit give significant effect to the histologic structure of mice kidney (p < 0,05).
BAB 1
PENDAHULUAN
1.1Latar Belakang
Jumlah penduduk di Indonesia dari tahun ke tahun terus mengalami peningkatan
yaitu sekitar 3 sampai 4 juta jiwa per tahun (Sabtono, 2013). Pertumbuhan
penduduk yang tinggi ini bila tidak dikendalikan akan menyebabkan masalah
yang besar. Upaya pengendalian masalah pertumbuhan penduduk dengan
penggunaan program keluarga berencana (KB) sudah dilaksanakan dengan baik
melalui pemakaian alat kontrasepsi yang pada umumnya terbuat dari hormon
sintetik, namun seringkali menimbulkan masalah serius bagi pemakainya (Sabri,
2007). Untuk itu, sedang digalakkan pemakaian alat kontrasepsi yang berasal dari
bahan alam, salah satunya tanaman andaliman (Zanthoxylum acanthopodium
DC.).
Andaliman (Zanthoxylum acanthopodium DC.) merupakan tanaman
rempah khas Sumatera Utara yang umumnya digunakan sebagai bumbu masakan
tradisional suku Batak (Siregar, 2003). Tanaman andaliman tidak hanya
ditemukan di Indonesia, tetapi juga ditemukan di negara lain seperti negara Eropa,
China, dan India. Umumnya tanaman andaliman digunakan di berbagai negara
tersebut sebagai tanaman obat-obatan bersama dengan tanaman genus
Zanthoxyllum lainnya seperti Z. piperitum, Z. simulans, Z. fagara, dan Z.
rhoifolium (Gonzaga et al., 2003 dalam Sabri, 2007). Beberapa penelitian telah
membuktikan bahwa buah andaliman juga memiliki aktivitas antioksidan dan
antimikroba (Miftakurohmah & Shinta, 2009). Sedangkan menurut Widyastuti
(2000), andaliman mengandung senyawa terpenoid, flavonoid, dan alkaloid yang
berperan sebagai antimikroba.
Penelitian yang telah dilakukan oleh Sabri et al (2005 dalam Sabri 2007),
melaporkan bahwa ekstrak andaliman dapat mempengaruhi perkembangan embrio
Penelitian selanjutnya oleh Sabri (2007) juga membuktikan bahwa ekstrak buah
andaliman bersifat embriotoksik dan fetotoksik, dimana ekstrak buah andaliman
ini mampu menurunkan secara nyata jumlah implantasi (penempelan zigot pada
dinding rahim) dan meningkatkan secara nyata jumlah kematian fetus. Potensi
inilah yang membuat andaliman dikembangkan menjadi alat kontrasepsi herbal
atau berbahan alam yang diharapkan mampu mengatasi permasalahan penduduk
tanpa menimbulkan efek samping.
Sebagian besar masyarakat berpendapat bahwa obat herbal tidak
mempunyai efek samping. Obat herbal meskipun berbahan alami bukan berarti
tidak mempunyai efek samping karena tanaman obat pun mengandung racun.
Penggunaan obat herbal selama ini hanya bersifat empiris artinya hanya
berdasarkan dosis dan efek yang didapat dari pengalaman yang bervariasi tiap-tiap
orang. Bukan berdasarkan evidence based medicine, dimana obat harus lolos
melewati uji fisik, kimiawi, farmakologis, biologis, dan uji toksisitas (Wulandari,
2010). Setiap obat pasti melewati sistem-sistem di dalam tubuh, termasuk sistem
ekskresi. Organ ekskresi utama di dalam tubuh yang dilaluinya yaitu ginjal. Ginjal
merupakan organ ekskresi utama dalam tubuh yang memiliki peranan yang sangat
penting dalam menyaring darah dan zat-zat toksik yang ikut masuk bersama
darah. Ginjal merupakan organ yang sangat sensitif terhadap kandungan yang
bersifat toksik (Cotran et al.,2007).
Ginjal berperan untuk mengeluarkan sisa-sisa metabolisme tubuh,
termasuk zat-zat toksik yang tidak sengaja masuk ke dalam tubuh. Akibatnya
ginjal menjadi salah satu organ sasaran utama dari efek toksik. Urin sebagai jalur
utama ekskresi, dapat mengakibatkan ginjal memiliki volume darah yang tinggi,
mengkonsentrasikan toksikan pada filtrat, membawa toksikan melalui sel tubulus
dan mengaktifkan toksikan tertentu (Guyton, 1995). Kerusakan ginjal karena zat
toksik dapat diidentifikasi berdasarkan perubahan struktur histologi, yaitu
necrosis tubular accute (NTA) yang secara morfologi ditandai dengan dekstruksi
epitel tubulus proksimal. Sel epitel tubulus proksimal peka terhadap anoksia dan
mudah hancur karena keracunan akibat kontak dengan bahan-bahan yang
diekskresikan melalui ginjal (Underwood, 1999). Pada NTA nefrotoksik
kongesti piramid, vakuolisasi sitoplasma sel epitel tubulus dan terbanyak di
tubulus proksimal. Gambaran mikroskopisnya tampak degenerasi tubulus
proksimal berupa edema epitel tubulus dengan lumen yang mengandung debris,
tetapi membran basalis tetap utuh (Anggriani, 2008).
Penelitian mengenai efek samping konsumsi andaliman terhadap organ
telah dilakukan oleh Prasetyawan (2013), dimana hasil penelitiannya
menunjukkan bahwa konsumsi buah andaliman pada mencit betina hamil
memberikan pengaruh negatif terhadap struktur hepar (hepatoksik) dengan
meningkatnya jumlah sel hati yang mengalami nekrosis. Sedangkan penelitian
mengenai efek samping konsumsi ekstrak buah andaliman terhadap ginjal sendiri
telah dilakukan oleh Panjaitan (2012), dimana hasil penelitiannya menunjukkan
bahwa konsumsi buah andaliman pada mencit betina virgin dapat mempengaruhi
struktur histologis ginjal yang ditunjukkan dengan adanya edema pada ginjal,
yaitu penumpukan cairan yang berlebihan pada jaringan tubulus proksimal yang
menyebabkan lumen tubulus menutup dan sel tubulus membengkak yang disebut
juga dengan necrosis tubular accute (NTA) yang merupakan kerusakan ginjal
yang paling ringan.
Perubahan struktur histologi ginjal ini tentu dipengaruhi oleh jumlah
senyawa yang masuk ke dalam tubuh. Untuk itu perlu dilakukan penelitian
mengenai pengaruh pengkonsumsian andaliman terhadap organ ginjal dengan
dosis yang bertingkat. Pada penelitian Panjaitan (2012) uji efek konsumsi buah
andaliman telah dilakukan dengan menggunakan ekstrak etanol buah andaliman.
Namun, pada penelitian ini akan digunakan ekstrak n-heksan buah andaliman
karena n-heksan merupakan pelarut non-polar yang diharapkan mampu
melarutkan lebih banyak senyawa terpenoid yang terdapat pada buah andaliman.
1.2 Perumusan Masalah
Setelah dilakukan beberapa uji kandungan diketahui bahwa andaliman terdiri dari
beberapa senyawa terpen seperti geraniol, linalool, dan limonen, yang telah
dilaporkan bersifat antimikroba dan antioksidan (Miftakurohmah & Shinta, 2009).
andaliman bersifat embriotoksik dan fetotoksik sehingga andaliman
dikembangkan menjadi alat kontrasepsi berbahan alam. Namun belum diketahui
bagaimana efek pengkonsumsian buah andaliman terhadap organ-organ vital
tubuh, terutama organ yang berkaitan langsung dengan sistem digesti dan
ekskresi.
Secara farmakokinetik, obat yang masuk ke dalam tubuh akan mengalami
absorbsi, distribusi, metabolisme, dan ekskresi. Ginjal merupakan organ ekskresi
utama yang sangat penting untuk mengeluarkan sisa-sisa metabolisme tubuh,
termasuk zat-zat toksik yang tidak sengaja masuk ke dalam tubuh (Agustie, 2006).
Buah andaliman mengandung berbagai senyawa kimia dengan sifat yang
berbeda-beda, ada kemungkinan interaksi dari senyawa-senyawa tersebut dalam tubuh.
Sejauh ini belum diketahui efek konsumsi buah andaliman secara terus-menerus
terhadap struktur ginjal sebagai organ ekskresi yang mengalami kontak dengan
senyawa-senyawa tersebut.
1.3 Tujuan Penelitian
1. Untuk mengetahui pengaruh ekstrak n-heksan buah andaliman terhadap
berat ginjal mencit
2. Untuk mengetahui pengaruh ekstrak n-heksan buah andaliman terhadap
kerusakan tubulus proksimal ginjal mencit dan dosis berapa yang telah
mampu merusaknya
3. Untuk mengetahui pengaruh ekstrak n-heksan buah andaliman terhadap
diameter tubulus proksimal
1.4 Hipotesis
1. Ekstrak n-heksan buah andaliman dapat meningkatkan berat ginjal mencit
2. Ekstrak n-heksan buah andaliman dapat merusak tubulus proksimal ginjal
mencit
3. Ekstrak n-heksan buah andaliman dapat memperbesar diameter tubulus
1.5 Manfaat
a. Untuk mengetahui apakah ekstrak Andaliman (Zanthoxylum acanthopodium
DC.) berpengaruh terhadap struktur histologis ginjal (Mus musculus L.)
b. Sebagai sumber informasi bagi masyarakat umum dan instansi yang
membutuhkannya.
BAB 2
TINJAUAN PUSTAKA
2.1 Tanaman Andaliman (Zanthoxylum acanthopodiumDC.)
Andaliman (Zanthoxylum acanthopodium DC.), adalah tanaman yang khas
dijumpai di Sumatera Utara, Indonesia. Buahnya umum digunakan sebagai bumbu
masakan tradisional suku Batak. Andaliman memiliki rasa pedas getir dan
memiliki aroma seperti jeruk (sitrus) yang dapat menghilangkan bau amis pada
masakan. Menurut Tensiska dkk., (2003), masakan yang menggunakan andaliman
biasanya lebih tahan lama dibandingkan dengan makanan yang tidak mengandung
andaliman. Hal ini disebabkan karena andaliman memiliki aktivitas antimikroba
dan antioksidan.
Adapun deskripsi andaliman menurut Siregar (2003), adalah sebagai
berikut: Semak atau pohon kecil bercabang rendah, tegak, tinggi mencapai 5 m.
Batang, cabang, dan ranting berduri, daun tersebar, bertangkai, panjang 5-20 cm
dan lebar 3-15 cm, terdapat kelenjar minyak. Rakis bersayap, permukaan bagian
atas, bagian bawah rakis, dan anak daun berduri; 3-11 anak daun, berbentuk
jorong hingga oblong, ujung meruncing, tepi bergerigi halus, paling ujung
terbesar, anak daun panjang 1-7 cm, lebar 0.5-2.0 cm. Permukaan atas daun hijau
berkilat dan permukaan bawah hijau muda atau pucat, daun muda permukaan atas
hijau dan bawah hijau kemerahan. Bunga di ketiak, majemuk terbatas, anak
payung menggarpu majemuk, kecil-kecil; dasar bunga rata atau bentuk kerucut;
kelopak 5- 7 bebas, panjang 1-2 cm, warna kuning pucat; berkelamin dua, benang
sari 5-6 duduk pada dasar bunga, kepala sari kemerahan, putik 3-4, bakal buah
apokarp, bakal buah menumpang. Andaliman merupakan tumbuhan yang
termasuk ke dalam famili Rutaceae, tumbuh perdu, dengan tinggi 3 - 8 m, batang
dan cabang merah kasar beralur, berbulu halus dan berduri. Daun berukuran kecil,
mirip daun bunga mawar. Buah andaliman tumbuh di antara duri-duri dan
warnanya cepat berubah menjadi hitam. Bentuk buah bulat dan kecil, lebih kecil
dari merica, bila digigit mengeluarkan aroma wangi dan rasa tajam yang khas, dan
dapat merangsang produksi air liur. Tumbuhan ini tersebar antara lain di India
Utara, Nepal, Pakistan Timur, Thailand, Cina. Di Indonesia, andaliman banyak
ditemukan di kawasan pegunungan Danau Toba dan beberapa daerah di Sumatera
Utara, dan biasanya tumbuh secara liar pada ketinggian 1.200 - 1.400 m dpl.
Sedangkan di Cina, dapat tumbuh sampai pada ketinggian 2.900 m dpl (Hartley,
1966; Miftakhurohmah & Shinta, 2009).
Gambar 2.1 Buah Andaliman (Zanthoxyllum
acanthopodium) (Sumber: Siregar, 2003)
Ciri lain famili Rutaceae yang terdapat pada andaliman ialah daun
majemuk, bunga majemuk berbatas dalam anak payung, mempunyai perhiasan
bunga satu lingkaran, yaitu kelopak yang disusun oleh lima daun kelopak bebas.
Lain halnya dengan anggota famili Rutaceae, berdaun tunggal, bunga majemuk
tidak terbatas, tersusun dalam bulir (lada), dan tidak memiliki perhiasan bunga
(Tjitrosoepomo, 1991). Andaliman memiliki kombinasi ciri berikut: tumbuhan
berduri, daun tersebar dan majemuk, bakal buah apokarp atau semikarp. Keempat
ciri ini ada pada andaliman. Dari satu bunga dapat terbentuk satu hingga empat
andaliman ialah epigeal. Perkecambahan di atas tanah terjadi karena
pembentangan ruas batang di bawah daun lembaga sehingga daun lembaganya
terangkat ke atas tanah (Hartley, 1966).
Beberapa penelitian telah membuktikan bahwa buah andaliman memiliki
aktivitas antioksidan dan antimikroba. Minyak atsiri dari buah andaliman terdiri
dari beberapa senyawa terpen seperti geraniol, linalool, dan limonen, yang telah
dilaporkan bersifat antioksidan. Selain itu, serbuk buah andaliman mampu
menghambat pertumbuhan Eschericia coli, Salmonella typhimurium, Bacillus
cereus, Staphylococcus aureus, dan Pseudomonas fluorescens. Aktivitas
antimikroba rempah tergantung pada satu atau beberapa komponen minyak
atsirinya. Senyawa tersebut mungkin terdapat pada berbagai jenis rempah atau
hanya khas pada jenis rempah tertentu. Analisis minyak atsiri buah andaliman
dengan teknik GC-MS menghasilkan 11 komponen, dengan 5 komponen utama
adalah alfapinen, limonen, geraniol, sitronelal, dan geranil asetat. Sedangkan
dengan teknik kromatografi gas, senyawa yang berhasil diidentifikasi sebanyak 7
komponen, yaitu geranil asetat, sitronelal, geraniol, geranial, mirsen, linalool, dan
limonene (Miftakhurohmah & Shinta, 2009).
Tabel 2.1 Komponen minyak buah andaliman segar dan kering angin dengan teknik kromatografi gas, Miftakhurohmah dan Shinta (2009)
Tanaman andaliman secara umum belum dikenal masyarakat Indonesia.
Walau telah diperdagangkan di luar daerah asalnya, namun masih hanya dikenal
dan dipergunakan oleh kalangan terbatas. Padahal melihat keunikan sensorik yang
dimiliki dan mungkin juga aktivitas fisiologi, bukan mustahil rempah ini dapat
menjadi salah satu rempah yang berpotensi merebut peluang pasar ekspor. Untuk
itu perlu ditunjang dengan informasi hasil penelitian ilmiah yang dapat
diperoleh terobosan-terobosan produk yang mempunyai nilai ekonomi lebih
(Wijaya, 1999).
2.2 Ginjal
Ginjal sering disebut buah pinggang, bentuknya seperti kacang dan
letaknya disebelah belakang rongga perut. Ginjal kiri lebih tinggi letaknya dari
ginjal kanan, berwarna merah keunguan (Irianto, 2004). Ginjal merupakan organ
terpenting dalam mempertahankan homeostatis cairan tubuh. Berbagai fungsi
ginjal untuk mempertahankan homeostatik adalah dengan mengatur volume
cairan, keseimbangan osmotik, asam basa, ekskresi sisa metabolisme, dan sistem
pengaturan hormonal (Syaifuddin, 2000).
2.2.1 Struktur Ginjal
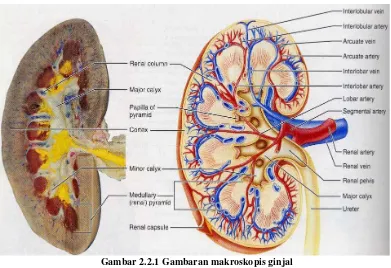
Gambar 2.2.1 Gambaran makroskopis ginjal (Sumber: Robbins & Kumar, 2005)
Struktur ginjal dilingkupi oleh selaput tipis dari jaringan fibrosa yang rapat dan
halus. Di dalamnya terdapat struktur-struktur ginjal. Terdiri atas bagian korteks
tersusun atas limabelas atau enambelas massa berbentuk piramida yang disebut
piramid ginjal. Puncaknya langsung mengarah ke hilus dan berakhir di kalises.
Kalises ini menghubungkannya dengan pelvis ginjal. Struktur halus ginjal terdiri
atas banyak nefron yang merupakan satuan-satuan fungsional ginjal dan
diperkirakan ada 1.000.000 nefron dalam setiap ginjal. Setiap nefron, mulai
sebagai berkas kapiler (Badan malphigi atau glomerulus) yang erat tertanam
dalam ujung atas yang lebar pada nefron. Tubulus ada yang berkelok-kelok ada
pula yang lurus. Bagian pertama tubulus yang berkelok dikenal sebagai tubulus
proksimal dan setelahnya terdapat lengkung Henle, kemudian tubulus itu
berkelok-kelok lagi yang dikenal dengan tubulus distal yang bersambung dengan
tubulus penampung, yang berjalan melintasi korteks dan medula, yang berakhir di
puncak salah satu piramida (Irianto, 2004).
Setiap ginjal memiliki sisi medial cekung, yaitu hilum, tempat saraf masuk
juga tempat pembuluh darah, pembuluh limfa, dan ureter keluar. Ginjal juga
memiliki sisi medial yang cembung yang di dalamnya terdapat pelvis renis, ujung
ureter yang melebar, dibagi dalam dua atau tiga kaliks mayor dan beberapa
cabang yang lebih kecil, kaliks minor, yang muncul dari setiap kaliks mayor
(Gambar 2). Dari dasar setiap piramid medula, terjulur berkas-berkas tubulus
paralel, yaitu berkas medula, yang menyusup ke dalam korteks. Setiap berkas
medula terdiri atas satu atau lebih duktus koligens bersama bagian lurus beberapa
nefron. Massa jaringan korteks yang mengelilingi setiap piramid medula
membentuk sebuah lobus renis, dan jaringan korteks juga terdapat di antara
piramid medula, struktur ini disebut kolumna Bertin (Junquiera dkk., 2005).
2.2.2 Pembuluh Darah pada Ginjal
Struktur ginjal berisi pembuluh darah (Gambar 3). Arteri renalis membawa darah
bersih dari aorta abdominalis ke ginjal. Cabang-cabang arteri beranting banyak di
dalam ginjal dan menjadi arteriola aferen yang masing-masing membentuk simpul
dari kapiler-kapiler di dalam salah satu badan malphigi, itulah glomerulus.
Pembuluh aferen kemudian tampil sebagai arteriola aferen yang
ini kemudian bergabung untuk membentuk vena renalis yang membawa darah
dari ginjal ke vena cava inferior. Oleh karena itu, darah yang beredar dalam ginjal
mempunyai dua kelompok kapiler yang bertutjuan agar darah dapat lebih lama
berada di sekitar tubulus uriniferus (Irianto, 2004).
Menurut Syaifuddin (2000), ginjal mendapat darah dari arteri renalis yang
merupakan cabang dari aorta abdominalis sebelum masuk ke dalam massa ginjal.
Arteri renalis memiliki cabang yang besar, arteri anterior dan arteri renalis
posterior. Cabang anterior memberikan darah untuk ginjal anterior dan ventral dan
cabang posterior memberikan darah untuk ginjal posterior dan bagian dorsal. Di
antara kedua cabang ini terdapat suatu garis (Brudels line) yang terdapat di
sepanjang largo lateral dari ginjal. Pada garis ini tidak terdapat pembuluh darah
sehingga kedua cabang ini akan menyebar sampai ke bagian anterior dan bagian
posterior dari colisis (kalises) sampai ke bagian ginjal, terletak diantara piramid
yang disebut dengan arteri aquarta. Pembuluh ini akan bercabang menjadi arteri
interlobularis yang berjalan tegak ke dalam korteks berakhir sebagai vasa aferen
glomerulus untuk 1-2 glomerulus, pleksus kapiler sepanjang tubulus melingkar di
dalam korteks tanpa berhubungan dengan glomerulus, dan pembuluh darah
menembus kapsula Bowman.
Darah yang membawa sisa-sisa hasil metabolisme tubuh difiltrasi di dalam
glomerulus kemudian ditubuli ginjal, beberapa zat yang masih diperlukan tubuh
mengalami reabsorbsi dan zat-zat hasil sisa metabolisme mengalami sekresi
bersama air membentuk urin. Setiap hari tidak kurang 180 liter cairan tubuh
difiltrasi di glomerulus dan menghasilkan urin 1-2 liter (Nasution, 2010).
2.2.3 Histologi Ginjal
Secara anatomis ginjal terbagi menjadi 2 bagian yaitu korteks dan medula ginjal.
Di dalam korteks terdapat berjuta-juta nefron. Sedangkan di dalam medula banyak
terdapat duktuli ginjal. Nefron terdiri atas, tubulus kontortus proksimalis, badan
malphigi, tubulus kontortus distalis, segmen tipis dan tebal ansa Henle, dan
Gambar 2.2.3.1 Ginjal dan Nefron
(Sumber: Cotran dkk, 2007)
Korteks ginjal terdiri dari pars konvulata dan pars radiata. Pars konvulata
tersusun dari korpuskuli ginjal dan tubuli yang membentuk labirin kortikal. Pars
radiata tersusun dari bagian-bagian lurus yaitu segmen lurus tubulus proksimal
dan segmen lurus tubulus distal dari nefron dan duktus koligens (Maulana, 2010).
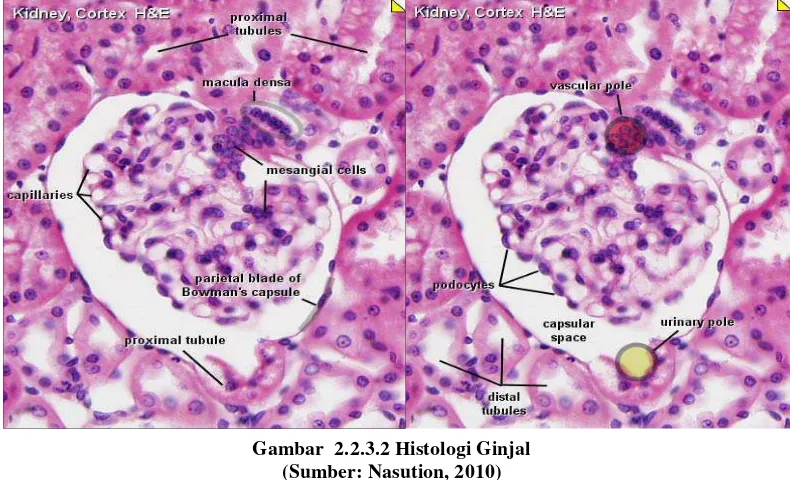
Gambar 2.2.3.2 Histologi Ginjal (Sumber: Nasution, 2010)
Badan malphigi terdiri atas glomerulus dan kapsula Bowman. Glomerulus
viseral dan kapsula Bowman merupakan lapisan parietal. Lapisan viseral
mempunyai sel yang disebut podosit, dimana dari badan selnya keluar beberapa
tonjolan primer dan dari tonjolan primer keluar banyak tonjolan sekunder.
Arteriol afferen masuk kedalam badan malphigi dan arteriol efferen keluar dari
badan malphigi. Dari arteriol afferen bercabang menjadi banyak kapiler. Antara
lapisan viseral dan lapisan parietal terdapat ruang kosong yang berisi cairan, dan
selanjutnya cairan itu dikeluarkan melalui tubulus kontortus proksimal (Junqueira
dkk, 1995). Ruangan dalam kapsula Bowman disebut ruang Bowman (ruang
urinarius) yang menampung cairan yang disaring melalui dinding kapiler dan
lapisanviseral. Glomerulus berhubungan dengan kapsula Bowman di bagian
dalam melalui lapisan viseral yang tersusun oleh modifikasi sel-sel epitel yang
disebut podosit. Dinding luar yang mengelilingi ruang Bowman tersusun oleh
sel-sel epitel skuamous simpleks yang membentuk lapisan parietal (Stevens & Lowe,
2005; Gartner & Hiatt, 2007).
Menurut Junqueira dkk (1995), tubulus kontortus proksimal keluar dari
badan malphigi, dibatasi oleh sel epitel selapis kubus. Lumennya kecil. Apeks sel
yang menghadap lumen mempunyai banyak mikrofili yang panjangnya sekitar 1
um yang membentuk brush border, sitoplasma sel granular dan sel sangat
terwarnai oleh eosin. Tubulus kontortus distal mempunyai perbedaan-perbedaan
dibandingkan tubulus kontortus proksimal. Perbedaan-perbedaannya dalam hal
ukuran lumen tubulus distal lebih besar dibandingkan tubulus proksimal. Ukuran
sel tubulus distal lebih kecil dibandingkan tubulus proksimal. Brush border pada
tubulus distal tidak ada. Sel tubulus distal kurang asidofil dibandingkan sel-sel
tubulus proksimal (kurang terwarnai oleh eosin). Lengkung Henle berbentuk
huruf U dan mempunyai segmen yang tipis dan diikuti dengan segmen yang
tebal. Bagian tipis lengkung Henle merupakan lanjutan dari tubulus kontortus
proksimal yang mempunyai garis tengah 12 um, tetapi lumennya lebar karena
dindingnya terdiri dari sel epitel gepeng yang intinya menonjol ke dalam lumen.
Urin berjalan dari tubulus kontortus distal ke tubulus koligens. Tubulus koligens
dibatasi oleh epitel kubus dan bergaris tengah sekitar 40 um. Ketika menembus
BAB 3
BAHAN DAN METODE
3.1 Waktu dan Tempat
Penelitian ini dilaksanakan dari bulan November 2011 sampai Maret 2013
di Laboratorium Struktur Hewan, Departemen Biologi, dan Laboratorium Kimia
Organik Bahan Alam, Departemen Kimia, Fakultas Matematika dan Ilmu
Pengetahuan Alam, Universitas Sumatera Utara, Medan.
3.2 Alat dan Bahan
Alat yang digunakan untuk pemeliharaan hewan uji dan pemberian perlakuan
yaitu kandang hewan, tempat makan dan minum hewan, jarum gavage, neraca
timbangan, dan alat tulis. Alat yang digunakan dalam pembuatan bahan uji yaitu
blender, kertas saring, spatula, botol, Erlenmeyer, dan rotavapor. Untuk
pembuatan sediaan mikroskopis digunakan jarum pentul, bak bedah, dissecting
set, sample cup, aluminium foil, oven, mikrotom, kuas, hot plate, gelas ukur,
beaker glass, botol zat, chamber, object glass, cover glass, kertas label dan botol
balsem. Alat yang digunakan untuk pengamatan yaitu mikroskop binokuler,
kamera digital, timbangan digital, dan alat tulis,
Bahan yang digunakan untuk pemeliharaan hewan uji dan pemberian
perlakuan yaitu mencit betina dewasa (Mus musculus L.) strain DDW yang
bunting, pakan, sekam, ekstrak andaliman 2 %, 4%, 6%, dan pelarut CMC
(carboxyl metil cellulose) 1. Bahan yang digunakan dalam pembuatan bahan uji
yaitu buah andaliman (Zanthoxzyllum acanthopodium DC.) dan pelarut n-heksan.
Bahan yang digunakan untuk pembuatan sediaan mikroskopis yaitu larutan NaCl
0,9%, larutan Bouin, alkohol 100%, 96%, 80%, 70%, 60%, 50%, 40%, 30%,
3.3 Prosedur Percobaan
3.3.1 Pembuatan Bahan Uji
Buah andaliman diperoleh dari daerah Dairi, Kabupaten Tapanuli Utara.
Buah andaliman yang masih bercampur dipisahkan untuk memperoleh buah yang
masih segar kemudian dikeringkan dalam suhu kamar sampai kering. Buah yang
telah kering diblender hingga menjadi simplisia (serbuk), kemudian dimasukkan
ke dalam stoples dan disimpan pada suhu kamar. Simplisia yang telah dihasilkan
dimaserasi dengan cara memasukkan simplisia ke dalam botol dan ditambahkan
pelarut n-heksan sampai terendam. Campuran tersebut diaduk dan dibiarkan
selama ± 1 malam. Hasil maserasi disaring dengan kertas saring dan diperoleh
filtrat. Residu yang ada direndam kembali dengan pelarut n-heksan. Hal ini
dilakukan secara berulang hingga diperoleh filtrat jernih. Kemudian filtrat yang
diperoleh dipisahkan dengan rotavapor sehingga dihasilkan ekstrak kental.
Ekstrak kental yang telah dirotavapor di tempatkan ke dalam beakerglass
dan ditutup dengan alumunium foil, lalu dimasukkan ke dalam freezer untuk
mencegah kerusakan ekstrak. Ekstrak andaliman tidak larut dalam air, maka untuk
mendapat campuran yang homogen digunakan suatu pelarut yaitu carboxyl metil
cellulosa (CMC) dengan konsentrasi 1% (1 mL CMC dilarutkan dalam 100 mL
aquadest) sehingga dihasilkan ekstrak yang diinginkan. Lalu dibuat dosis yang
telah dimodifikasi dengan cara melarutkan ekstrak buah andaliman 2% dalam 1%
CMC, 4% dilarutkan dalam 1% CMC, dan 6% dilarutkan dalam 1% CMC
(Chairul et al., 1992; Pratiwi, 2006).
3.3.2 Persiapan Hewan Uji
Penelitian ini menggunakan mencit betina (Mus musculus L.) strain DDW.
Disediakan satu ekor mencit jantan lalu ditempatkan dalam kandang yang berisi
enam ekor mencit betina yang sedang estrus selama satu malam. Sumbat vagina
menyatakan telah terjadi kopulasi atau perkawinan mencit antara mencit jantan
dan mencit betina dan ditetapkan sebagai hari ke-0 (nol) kebuntingan (Taylor,
mencit yang berumur ± tiga minggu dipisahkan dari induknya dan dipelihara
dalam kandang terpisah dengan memisahkan antara mencit jantan dan betina.
Kandang yang terbuat dari plastik yang diberi alas sekam yang dilakukan
pergantian sekam dua kali seminggu. Pemberian pakan dan minum dilakukan
setiap hari secara ad-libitum (Sabri et al, 2007). Mencit betina yang sudah
berumur ± 12 minggu dengan kisaran berat badan ± 25-30 g kemudian
dikawinkan dengan mencit jantan. Apabila terjadi sumbat vagina pada mencit
betina maka dinyatakan sebagai hari ke-0 (nol) kebuntingan (Taylor, 1986).
Mencit yang bunting dari perkawinan tersebut siap untuk diberi perlakuan.
3.3.3 Pemberian Perlakuan
Pemberian bahan uji dilakukan pada mencit betina (Mus musculus L.)
yang sedang bunting dengan menggunakan jarum gavage (Hrapkiewicz &
Medina, 2007). Pemberian dilakukan selama 10 hari kebuntingan. Volume
pemberian ekstrak sebanyak 0,3 ml/ekor/hari. Kemudian mencit dibunuh dengan
cara dislokasi leher pada saat mencapai 18 hari kebuntingan. Selanjutnya mencit
dibedah, diambil organ ginjal dan dicuci dalam larutan fisiologis (NaCl 0,9%) lalu
ditimbang, setelah itu dimasukkan ke dalam larutan Bouin.
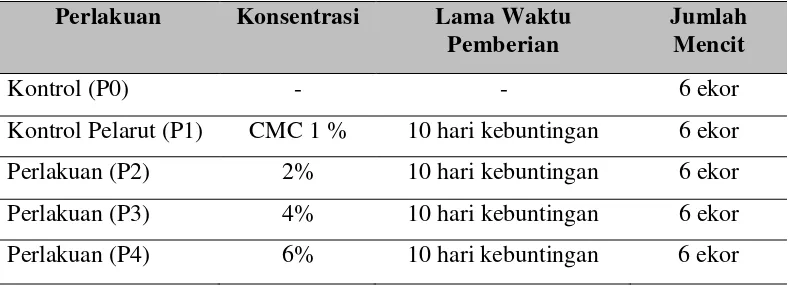
3.3.4 Rancangan Penelitian
Tabel 3.3.4 Model Rancangan Penelitian
Penelitian ini adalah penelitian eksperimental dengan rancangan acak lengkap
(RAL). Pada penelitian ini jumlah sampel yang digunakan adalah sebanyak 30
Perlakuan Konsentrasi Lama Waktu
Pemberian
Jumlah Mencit
Kontrol (P0) - - 6 ekor
Kontrol Pelarut (P1) CMC 1 % 10 hari kebuntingan 6 ekor
Perlakuan (P2) 2% 10 hari kebuntingan 6 ekor
Perlakuan (P3) 4% 10 hari kebuntingan 6 ekor
ekor mencit strain DDW yang memenuhi kriteria inklusi, yaitu umur 2-3 bulan,
berat badan 25-30 g, dan tidak terdapat abnormalitas anatomi yang tampak.
Setelah mengalami masa adaptasi selama 1 minggu, sampel secara random dibagi
menjadi lima kelompok yang terdiri atas kelompok kontrol, kelompok kontrol
pelarut dan 3 kelompok perlakuan.
Kelompok P0 (kontrol) mendapatkan pakan standar dan minum berupa air
ledeng secara ad-libitum. Kelompok Kontrol Pelarut (P1) diberi pakan standar dan
CMC 1%. Sedangkan kelompok perlakuan P2, P3, P4) masing-masing diberi
pakan standar, air ledeng dan ekstrak N-heksan andaliman dengan konsentrasi
2%, 4%, dan 6%. Setelah perlakuan, pada hari kedelapan belas mencit dibunuh
dengan cara dislokasi leher, kemudian diambil organ ginjalnya, dicuci dengan
larutan NaCl 0,9% lalu difiksasi dengan Bouin dan diproses mengikuti metode
parafin dengan pewarnaan HE. Dari setiap organ diamati di bawah mikroskop
dalam 5 lapangan pandang, yaitu pada keempat sudut dan bagian tengah preparat,
dengan perbesaran 400x. Sasaran yang dibaca adalah tubulus proksimal ginjal.
Penghitungan kerusakan tubulus proksimal menggunakan rumus (n/m) x
100%, dimana n adalah jumlah tubulus proksimal yang telah menutup dalam satu
lapangan pandang sedangkan m adalah jumlah seluruh tubulus proksimal yang
terdapat dalam satu lapangan pandang (Sihardo, 2006).
3.3.5 Penimbangan Berat Ginjal
Setelah mendapat perlakuan mencit didislokasi kemudian dibedah. Diambil
salah satu ginjal secara acak. Organ ginjal diambil dan ditimbang pada timbangan
elektronik.
3.3.6 Pembuatan Preparat Ginjal dengan Metode Parafin
Mencit (Mus musculus L.) didislokasi dan dibedah. Diambil organ ginjal,
ditimbang dan dicuci dengan larutan NaCl 0,9% kemudian difiksasi selama
seminggu dengan larutan Bouin. Setelah difiksasi, ginjal dicuci dengan alkohol
alkohol 70 % selama 1 malam. Setelah direndam semalaman dilakuan dehidrasi
dengan merendam organ ginjal sambil dishaker dengan menggunakan alkohol
bertingkat, yaitu dari alkohol 70%, 80%, 96% dan 100% (absolut) selama 1 jam
pada masing-masing konsentrasi. Setelah itu organ ginjal direndam di dalam
xylol selama 1 malam. Organ ginjal yang telah direndam 1 malam di dalam xylol
kemudian diambil dan direndam dalam xylol lagi selama 1 jam pada suhu kamar,
lalu dipindahkan lagi ke dalam xylol yang baru selama 1 jam. Setelah itu organ
ginjal direndam ke dalam parafin murni I, parafin murni II, dan parafin murni III
masing-masing selama 1 jam pada suhu 60°C.
Setelah melewati tahap-tahap tersebut barulah memasuki tahap embedding
atau penanaman organ ke dalam parafin. Parafin baru yang telah cair dituang ke
dalam kotak yang telah disediakan, kemudian ginjal ditanam dalam kotak yang
telah berisi parafin dan diatur posisinya lalu diberi label. Dibiarkan sampai dingin
sehingga membentuk blok parafin. Blok-blok tersebut selanjutnya dirapikan pada
holder yang terbuat dari kayu berukuran 3x2x3 cm yang berbentuk balok. Setelah
itu dilakukan pemotongan atau cutting dengan memotong blok-blok parafin yang
telah diholder pada mikrotum sehingga membentuk pita-pita parafin dengan
ukuran ketebalan 6 µm. Kemudian dilakukan penempelan, yaitu dengan
mengambil beberapa pita parafin, kemudian diletakkan pada object glass, dan
dicelupkan pada air dingin dan kemudian pada air hangat. Lalu diletakkan di atas
hotplate beberapa detik untuk melekatkan pita parafin pada object glass. Setelah
tahap ini selesai barulah memasuki tahap pewarnaan. Object glass dicelupkan
pada xylol sampai parafin habis kira-kira selama 5 menit. Lalu ke dalam alkohol
bertingkat dengan konsentrasi menurun, yaitu dari alkohol absolut, 96%, 80%,
70%, 60%, 50%, 40%, 30% kemudian ke dalam aquadest. Dimana
masing-masing konsentrasi dicelupkan ± 3-5 detik.
Setelah itu, sediaan dimasukkan ke dalam larutan pewarna hematoksilin
selama beberapa detik, lalu dicuci dengan air mengalir, kemudian dimasukkan ke
dalam alkohol 30%, 40 %, 50%, 60 %, dan 70%, lalu dimasukkan ke dalam
larutan pewarna eosin selama beberapa detik, dilanjutkan ke dalam alkohol 80%,,
90%, dan alkohol absolute. Setelah itu, dilap dengan kertas tisu dan dimasukkan
tisu. Kemudian preparat diberi canada balsam agar awet dan melekat pada cover
glass, diusahakan agar tidak terdapat gelembung udara saat menutup preparat
dengan cover glass. Preparat yang telah diwarnai kemudian diberi label dan
diamati kerusakannya khususnya pada tubulus proksimal di bawah mikroskop.
3.4 Parameter Pengamatan
3.4.1 Berat Ginjal
Pengamatan berat ginjal dilakukan dengan cara menimbang organ ginjal
mencit betina pada timbangan elektronik. Dari satu ekor mencit betina diambil
satu organ ginjal. Ginjal dipilih secara acak tanpa membedakan antara ginjal kiri
dan kanan. Berat ginjal dari ke enam ekor mencit pada tiap perlakuan kemudian
dirata-ratakan dan dicatat hasilnya hingga diperoleh data.
3.4.2 Kerusakan Tubulus Proksimal Ginjal
Preparat ginjal dibuat dengan metode blok parafin dengan pewarnaan HE.
Dari setiap organ ginjal yang diambil, dibuat dua preparat kemudian dilakukan
pengamatan. Setiap preparat diamati di bawah mikroskop dalam 5 lapangan
pandang, yaitu dengan menggeser preparat ke kiri atas, kiri bawah, tengah, kanan
atas, dan kanan bawah dengan perbesaran 400x. Sasaran yang dibaca adalah
tubulus proksimal ginjal yang mengalami kerusakan berupa edema atau
pembengkakan hingga lumen menutup. Pada setiap lapangan pandang dihitung
jumlah tubulus proksimal yang rusak, kemudian dirata-ratakan dan dihitung
persentase kerusakannya lalu dicatatat pada buku data.
3.4.3 Diameter Tubulus Proksimal yang Menutup
Tubulus proksimal yang menutup dari setiap preparat dipilih secara acak
sebanyak 20 buah, kemudian diukur diameternya. Ukuran diameter yang
3.5 Analisis Statistik
Data yang didapat dari setiap parameter (variabel) pengamatan, yaitu berat
ginjal, penutupan tubulus proksimal, dan diameter tubulus proksimal yang
menutup dicatat dan disusun ke dalam bentuk tabel. Data kuantitatif (variabel
dependen) yang didapatkan yaitu rerata dan standart deviasi dari berat ginjal,
penutupan tubulus proksimal, dan diameter tubulus proksimal yang menutup diuji
dengan bantuan progr statistik komputer yakni progr SPSS release 16. Urutan uji
diawali dengan uji normalitas dan uji homogenitas. Apabila data yang diperoleh
homogen dan normal (p>0,05) maka dilanjutkan dengan uji sidik ragam
(ANOVA), jika berbeda nyata (p<0,05) maka dilanjutkan dengan uji Post
Hoc-Bonferroni. Tetapi apabila hasil uji homogenitas dan normalitas menunjukkan
tidak homogen atau tidak normal, maka data tersebut ditransformasi sebanyak 3
kali. Apabila tetap tidak homogen atau tidak normal (p<0,05) maka dilanjutkan
dengan uji non parametrik (Kruskal-Wallis). Setelah itu untuk melihat perbedaan
antara 2 perlakuan (kontrol dan ekstrak andaliman) dilakukan uji Mann-Whitney
BAB 4
HASIL DAN PEMBAHASAN
4.1 Berat Ginjal Mencit
Hasil pengamatan terhadap berat ginjal mencit betina hamil dengan
perlakuan ekstrak n-heksan buah andaliman dengan perbedaan konsentrasi telah
dilakukan uji analisis statistik Dari data tersebut diperoleh bahwa rata-rata berat
ginjal mencit yang diberi perlakuan ekstrak n-heksan buah andaliman terjadi
penurunan bila dibandingkan dengan kontrol blank (P0) dan kontrol pelarut (P1).
Rata-rata berat ginjal mencit pada P0 (0,260 g) dan P1 ( 0,250 g). Sedangkan
rata-rata berat ginjal mencit pada P2 (0,230 g), pada P3 (0,220 g), dan pada P4 (0,218
g). Grafiknya dapat dilihat pada Gambar 4.1.1
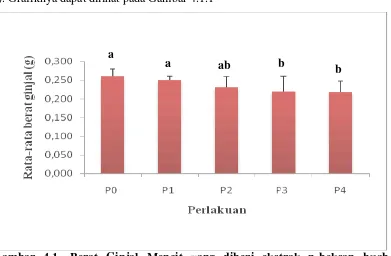
Gambar 4.1. Berat Ginjal Mencit yang diberi ekstrak n-heksan buah andaliman pada konsentrasi yang berbeda. P0= Kontrol Blank (mencit tidak diberi perlakuan apapun selain pakan); P1 = Kontrol Pelarut (pemberian CMC 1%); P2, P3 dan P4= Perlakuan dengan konsentrasi ekstrak N-heksan buah andaliman 2%, 4%, dan 6%; huruf yang berbeda pada perlakuan berbeda menunjukkan berbeda nyata; satuan dalam gram (g).
a
a ab b
Hasil analisis statistik antara kontrol blank (P0) dan kontrol pelarut (P1)
menunjukkan tidak ada perbedaan yang nyata, antara perlakuan P2 dengan P0 dan
P1 terdapat perbedaan yang tidak signifikan, namun antara perlakuan P3 dan P4
dengan perlakuan P0 dan P1 menunjukkan perbedaan yang signifikan (p<0,05).
Penurunan berat ginjal terjadi seiring dengan peningkatan konsentrasi ekstrak
pada kelompok perlakuan. Hal ini kemungkinan disebabkan oleh beberapa faktor.
Faktor pertama, kandungan minyak atsiri ekstrak n-heksan buah andaliman
mempengaruhi permeabilitas sel epitel ginjal, sehingga menyebabkan gangguan
pada proses penyerapan air, yang menyebabkan menurunnya bobot ginjal.
Menurut Cotran et al., (2007), penyerapan air kembali (reabsobsi) dilakukan oleh
seluruh pembuluh renalis, namun reabsorbsi terbesar terjadi di tubulus proksimal
dengan cara osmosis yang disebut dengan reabsorbsi obligat. Reabsorbsi air
sangat dipengaruhi oleh permeabilitas membran. Semakin tinggi permeabilitas
membran, semakin banyak air yang diserap oleh ginjal. Dan sebaliknya, semakin
rendah permeabilitas membran, semakin sedikit air yang diserap oleh ginjal.
Dalam hal ini, senyawa aktif yang terdapat dalam ekstrak n-heksan buah
andaliman mungkin mempengaruhi permeabilitas membran tubulus proksimal
terhadap penyerapan air sehingga berpengaruh terhadap berat ginjal.
Faktor kedua, pada penelitian ini ditemukan adanya jaringan tubulus
proksimal yang mengalami kematian (nekrosis), kemungkinan ada juga jaringan
lain selain tubulus proksimal yang mengalami nekrosis. Rusaknya
jaringan-jaringan pada ginjal ini akan menyebabkan bobot ginjal berkurang. Menurut
Anggriani (2008), sel epitel tubulus mudah hancur karena kontak dengan bahan
toksik yang diekskresi melalui ginjal. Perubahan struktur histologis ginjal ini
dipengaruhi oleh jumlah senyawa yang masuk ke dalam tubuh. Apabila kerusakan
yang bersifat reversible seperti necrosis tubular acute (NTA) dibiarkan dan terus
berlanjut, akan diikuti dengan proses vasokonstriksi arterial praglomerolus, yang
dapat menyebabkan iskemik. Iskemik menyebabkan berbagai perubahan struktur
dan fungsi dari sel epitel, dari kerusakan yang reversibel hingga kerusakan yang
bersifat irreversibel yang ditandai dengan terjadinya nekrosis dan apoptosis
(Sarjadi, 2003). Terjadinya kerusakan jaringan ginjal inilah yang juga mungkin
4.2 Penutupan Tubulus Proksimal
Hasil pengamatan terhadap persentase penutupan tubulus proksimal ginjal mencit
betina hamil dengan perlakuan ekstrak n-heksan buah andaliman dengan
perbedaan konsentrasi telah diuji analisis statistik. Dari data tersebut diperoleh
bahwa bahwa rata-rata persentase penutupan tubulus proksimal yang diberi
perlakuan ekstrak n-heksan buah andaliman terjadi peningkatan bila dibandingkan
dengan kontrol blank (P0) dan kontrol pelarut (P1). Rata-rata jumlah penutupan
Tubulus proksimal pada P0 (41,84 %) dan P1 (43,91 %). Sedangkan rata-rata
persentase penutupan tubulus proksimal pada P2 (61,49 %), pada P3 (80,68 %),
dan pada P4 (62,61 %). Grafik dapat dilihat pada Gambar 4.2.1.
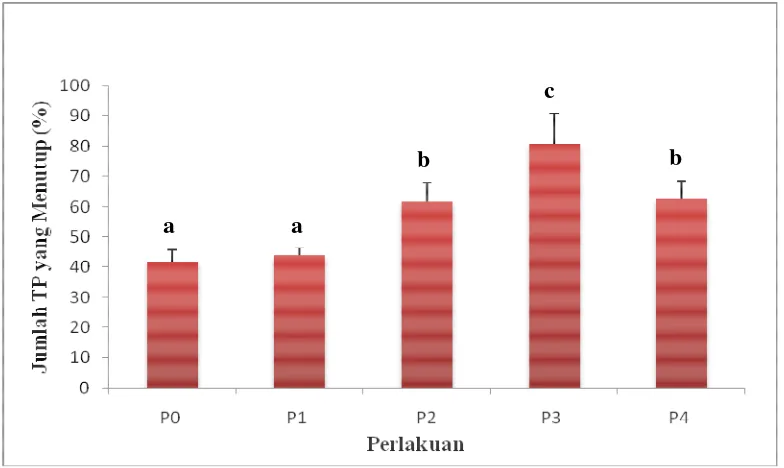
Gambar 4.2.1 Persentase Penutupan Tubulus Proksimal setelah diberi ekstrak n-heksan buah andaliman pada konsentrasi yang berbeda. P0 = Kontrol Blank (mencit tidak diberi perlakuan apapun selain pakan); P1 = Kontrol Pelarut (pemberian CMC 1%); P2, P3 dan P4= Perlakuan dengan konsentrasi ekstrak n-heksan buah andaliman 2%, 4%, dan 6%; huruf yang berbeda pada perlakuan berbeda menunjukkan berbeda nyata; satuan dalam persen (%).
Hasil analisis statistik antara perlakuan kontrol blank (P0) dengan kontrol
pelarut (P1) tidak menunjukkan adanya perbedaan yang nyata. Namun antara
perlakuan P0 dan P1 dengan perlakuan ekstrak n-heksan 2% (P2), 4% (P3), dan
6% (P4) terdapat perbedaan yang signifikan terhadap peningkatan penutupan
a a
b
c
tubulus proksimal. Demikian pula terdapat perbedaan yang nyata (P<0,05) antara
perlakuan P3 dengan perlakuan P2 dan P4. Peningkatan persentase penutupan
tubulus proksimal yang terjadi pada P3 sebesar 80,68 % sedangkan pada P2
sebesar 61,49 % dan P4 sebesar 62,61 %. Hasil pengamatan histologis tubulus
proksimal ginjal (ren) mencit dapat dilihat pada Gambar 4.2.2.
Gambar 4.2.2. Gambar Histologi Ren Mencit, Pewarnaan HE, Perbesaran 400. Keterangan: A. Kontrol: 1. Tubulus Proksimal Normal, 2. Tubulus Proksimal Menutup (Nekrosis); B. Perlakuan: 1. Tubulus Proksimal menutup (Nekrosis)
Pada kelompok kontrol dapat ditemukan tubulus proksimal normal
maupun yang menutup (Gambar 4.2.2A). Tubulus proksimal yang menutup pada
kelompok normal merupakan hal yang dapat terjadi karena setiap sel atau
jaringan pasti memiliki kontak dengan senyawa-senyawa yang masuk ke dalam
tubuh baik melalui makanan, minuman, dan lingkungan yang dapat menyebabkan
1
2
2
1
A
perubahan struktur, namun hal ini bukan merupakan masalah selama tidak atau
belum menimbulkan perubahan fungsi fisiologis jaringan. Menurut Sarjadi et al.,
(2003), pembengkakan pada tubulus proksimal merupakan gejala kerusakan
paling ringan yang disebut degenerasi albuminosa (cloudy swelling) dimana
perubahan dapat kembali menjadi normal seperti semula. Sedangkan pada
kelompok perlakuan ditemukan peningkatan jumlah tubulus proksimal yang
menutup, dapat dilihat pada Gambar 4.2.2B. Pada Gambar dapat dilihat perubahan
yang terjadi pada tubulus proksimal dimana lumen mengalami penutupan dan
terjadi pembengkakan pada sel tubulus. Peningkatan persentase penutupan lumen
pada tubulus proksimal ini diduga karena terdapat berbagai senyawa kimia seperti
terpenoid, alkaloid, dan flavonoid pada buah andaliman yang memberikan efek
toksik terhadap organ ginjal mencit sehingga menyebabkan pembengkakan pada
tubulus proksimal (Panjaitan, 2012). Terjadinya kerusakan tubulus proksimal
mencit setelah pemberian ekstrak n-heksan andaliman ini sesuai dengan teori
bahwa proses ekskresi obat yang berlangsung pada suatu organ dapat
menimbulkan dampak buruk bagi organ itu sendiri (Robbins & Kumar, 1995).
Ginjal menerima darah sebesar 20% dari curah jantung melalui arteri
renalis. Tingginya aliran darah yang menuju ginjal inilah yang menyebabkan
berbagai macam obat dan bahan kimia dalam sirkulasi sistemik dikirim ke ginjal
dalam jumlah yang besar. Faktor lain yang mungkin menyebabkan kerusakan
ginjal adalah kemampuan ginjal untuk mengkonsentrasikan substansi xenobiotik
di dalam sel. Jika suatu zat kimia disekresi secara aktif dari darah ke urin, zat
kimia terlebih dahulu diakumulasikan dalam tubulus proksimal atau jika substansi
kimia ini direabsorbsi dari urin maka akan melalui sel epitel tubulus dengan
konsentrasi tinggi. Proses pemekatan tersebut zat-zat toksik ini akan terakumulasi
di ginjal dan menyebabkan kerusakan bagi ginjal (Hodgson & Levi, 2001).
Proses ekskresi senyawa-senyawa yang bersifat toksik dapat menyebabkan
kerusakan tubulus, berupa Necrosis Tubular Accute (NTA) yang bersifat
reversibel karena sel-sel epitel tubulus proksimal kemampuan daya regenerasi
yang baik. Secara histologi kerusakan tersebut ditandai dengan destruksi sel epitel
tubulus proksimal, namun membrana basalis tubuli pada umumnya masih baik.
diekskresi melalui ginjal (Wijaya & Miranti, 2005). Sel-sel epitel tubulus
proksimal akan membengkak dengan sitoplasma granuler karena pergeseran air
ekstraselular ke dalam sel (Robbins & Kumar, 1995). Pergeseran cairan ekstra
selular ke dalam sel tubulus proksimal ini terjadi karena toksin menyebabkan
perubahan muatan listrik permukaan sel epitel tubulus, transpor aktif ion dan asam
organik, dan kemampuan untuk mengkonsentrasikannya hingga mengakibatkan
tubulus rusak, aliran kemih terganggu, tekanan intra tubulus meningkat, kecepatan
filtrasi glomerulus menurun (Wijaya & Miranti, 2005). Hal inilah yang
kemungkinan menyebabkan sel tubulus proksimal membengkak dan mengalami
penyempitan hingga menutup pada penelitian ini.
Selain tubulus yang menutup, pada pengamatan juga ditemukan adanya
kerusakan lain seperti hipertrofi, nekrosis dan serosis. Menurut Arifin et al.,
(2004), nefron ginjal akan mengalami hipertropi apabila mendapat beban kerja
yang besar. Hipertropi pada nefron ini dapat terjadi karena menggantikan fungsi
nefron lain yang telah hancur dan rusak, sehingga hemostatis tubuh tidak
terganggu meskipun sejumlah nefron yang lain telah rusak. Nekrosis ditandai
dengan penyerapan warna oleh inti yang berkurang serta terlepasnya sel-sel
tubulus kedalam lumen. Sedangkan serosis merupakan kematian sel yang bersifat
parah dan dapat meluas yang ditandai dengan hilangnya inti sel atau kekosongan
pada jaringan dimana jaringan tersebut digantikan oleh jaringan parut (jaringan
ikat) yang sebelumnya mengalami lisis dan nekrosis (Mayori et al., 2013)
Selain menimbulkan kerusakan tubulus secara langsung, zat-zat toksik
juga memiliki kemampuan untuk merusak tubulus dengan cara mempengaruhi
sistem hemodinamik. Beberapa zat toksik dapat merubah hemodinamik intrarenal
yang memicu terjadinya vasokonstriksi. Vasokonstriksi berkepanjangan
mengakibatkan hipoksia pada medula dan pada akhirnya menyebabkan kerusakan
tubulus (Pratita, 2008). Komposisi dari ekstrak buah andaliman mengandung
zat-zat toksik yang merusak ginjal (nephrotoxic agent). Zat-zat nefrotoksik ini
merusak ginjal melalui dua mekanisme yaitu merusak tubulus ginjal secara
langsung maupun perubahan hemodinamik. Kandungan apa dalam buah
andaliman yang menyebabkan kerusakan ginjal dan mekanisme mana yang lebih
4.3 Diameter Tubulus Proksimal yang Menutup
Telah dilakukan uji analisis statistik terhadap hasil pengamatan terhadap diameter
tubulus proksimal ginjal mencit betina hamil yang menutup dengan perlakuan
ekstrak n-heksan buah andaliman dan dengan konsentrasi yang berbeda-beda.
Dari data tersebut diperoleh bahwa rata-rata diameter tubulus proksimal yang
menutup pada perlakuan ekstrak n-heksan buah andaliman terjadi peningkatan
bila dibandingkan dengan kontrol blank (P0) dan kontrol pelarut (P1). Rata-rata
diameter tubulus proksimal pada P0 (12,38 µm) dan P1 (12,66 µm). Sedangkan
rata-rata diameter tubulus proksimal pada P2 (14,92 µm), pada P3 (14,09 µm) dan
pada P4 (13,83 µm). Grafik dapat dilihat pada Gambar 4.3.1.
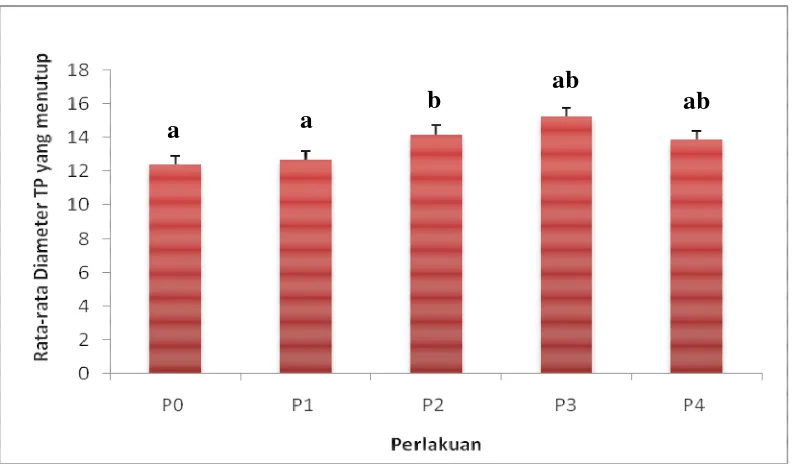
Gambar 4.3.1 Diameter Tubulus Proksimal yang Menutup setelah diberi ekstrak N-heksan buah andaliman pada konsentrasi yang berbeda. P0= Kontrol Blank (mencit tidak diberi perlakuan apapun selain pakan); P1 = Kontrol Pelarut (pemberian CMC 1%); P2, P3 dan P4= Perlakuan dengan konsentrasi ekstrak n-heksan buah andaliman 2%, 4%, dan 6%; huruf yang berbeda pada perlakuan berbeda menunjukkan berbeda nyata; satuan dalam mikrometer (µm).
Hasil analisis statistik antara perlakuan ekstrak n-heksan dan kontrol blank
(P0) dan kontrol pelarut (P1) menunjukkan adanya perbedaan yang nyata (p<0,05)
terhadap pertambahan diameter tubulus proksimal yang menutup. Pertambahan
a b
ab
diameter yang paling besar terdapat pada perlakuan P2. Berikut gambar hasil
pengamatan terhadap pertambahan diameter tubulus proksimal.
Gambar 4.3.2. Gambar Histologi Ren Mencit, Pewarnaan HE, Perbesaran 400x. Keterangan: A. Diameter Kontrol (P0); B. Diameter Perlakuan 2% (P2).
Pertambahan diameter tubulus proksimal diduga terjadi karena adanya
penumpukan cairan pada tubulus proksimal yang membuat dinding tubulus
semakin membengkak karena masuknya cairan ekstra selular ke dalam sel.
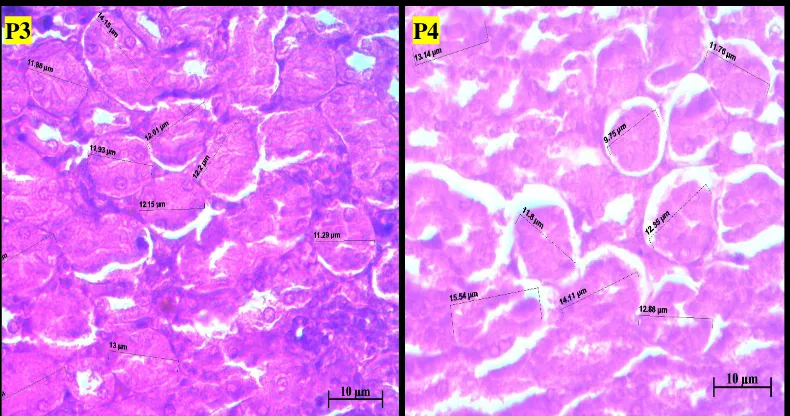
Diameter terbesar terdapat pada P2 yaitu 14.92, sedangkan pada P3 dan P4
diemeter kembali mengecil yaitu 14.09 pada P3 dan 13.83 pada P4. Namun, pada
P3 dan P4 srtuktur jaringan terlihat lebih mengalami kerusakan (Gambar 4.3.3).
Hal ini kemungkinan disebabkan oleh peningkatan konsentrasi ekstrak andaliman
yang diberikan tidak lagi hanya mempengaruhi penutupan tubulus proksimal
tetapi juga menyebabkan kerusakan jaringan ikat yang cukup parah. Tubulus
A
proksimal yang menutup kelihatan lebih kecil namun kehilangan jaringan
disekitarnya (tampak seperti ruang-ruang kosong pada gambar).
P3 P4
Gambar 4.3.3. Histologis Ren Mencit, P3 dan P4, Pewarnaan HE, Perbesaran 400x.
Menurut Robbins & Kumar (1995), edema tubulus proksimal adalah
manifestasi awal dari jejas. Gambaran mikroskopis ini berupa sel-sel epitel
tubulus proksimal yang membengkak dengan sitoplasma granuler karena terjadi
pergeseran air ekstraseluler ke dalam sel. Pergeseran cairan ini terjadi karena
toksin menyebabkan perubahan muatan listrik permukaan sel epitel tubulus,
transpor aktif ion dan asam organik, dan kemampuan mengkonsentrasikan dari
ginjal. Pembengkakan ini mendorong lumen hingga menyebabkan lumen tubulus
proksimal mengalami penyempitan dan menutup (Wijaya & Miranti, 2005)..
Menurut Robbins & Kumar (1995), gambaran mikroskopis ginjal yang
mengalami kerusakan tampak degenerasi tubulus proksimal berupa edema epitel
tubulus tetapi membrana basalis tetap utuh. Tanda awal dari nekrosis tubular akut
ditandai dengan degenerasi albuminosa dimana epitel tubulus proksimal akan
mengalami pembengkakan sehingga menutup lumen tubulus. Namun jika toksin
terus menerus masuk dapat membuat tubulus proksimal lebih mengalami
kerusakan. Kerusakan ini dapat ditandai dengan kerusakan membran basalis dan
kerusakan jaringan lainnya disekitar tubulus. Kerusakan membran basalis ini akan
menyebabkan cairan sel keluar dan sel akan menciut. Selanjutnya, hal ini akan
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
a. Pemberian ekstrak n-heksan andaliman dengan dosis bertingkat pada mencit
betina hamil selama 10 hari telah dapat menurunkan berat ginjal mencit.
b. Pemberian ekstrak n-heksan andaliman dengan dosis 4% pada mencit betina
hamil selama 10 hari sudah dapat merusak struktur atau gambaran histologis
ginjal mencit.
c. Pemberian ekstrak n-heksan andaliman dengan dosis bertingkat pada mencit
betina hamil selama 10 hari telah dapat mempengaruhi diameter tubulus
proksimal ginjal mencit.
5.2 Saran
1. Perlu pertimbangan apabila menggunakan andaliman sebagai bahan
kontrasepsi karenadari hasil penelitian ini diketahui bahwa andaliman dapat
merusak ginjal.
2. Perlu dilakukan penelitian lebih lanjut tentang kandungan Zanthoxylum
DAFTAR PUSTAKA
Agustie, M. C. 2006. Pengaruh Pemberian Rumput Mutiara (Hediotys corymbosa) dengan Dosis Bertingkat Terhadap Gambaran Histologis Ginjal Mencit Balb/C. [Artikel Penelitian]. Semarang: Universitas Diponegoro. Hlm. 6.
Anggriani, Y. D. 2008. Pengaruh Pemberian Teh Kombucha Dosis Bertingkat Per Oral Terhadap Gambaran Histologis Ginjal Mencit Balb/C. [Karya Tulis Ilmiah]. Semarang: Diponegoro. Hlm. 5.
Arifin, H., Y. S. Rahmi, dan N. Marusin. 2004. Kajian Toksisitas Ekstrak Etanol Daun Kompri (Symphytum officinale L). Jurnal Sains dan Teknologi Farmasi. 9 (1): 28-35.
Chairul, Harapini, M., dan Daryati, Y. 1992. Pengaruh Ekstrak Kencur (Kaempferia galanga L.) Terhadap Kehamilan Mencit Putih (Mus musculus L.). Seminar Nasional Indonesia V. Pokjanas. Bandung: Universitas Padjajaran, Bandung dan Laboratorium Treub Puslitbang Biologi LIPI Bogor.
Cotran R. S., Rennke H., dan Kumar V. 2007. Ginjal dan Sistem Penyalurnya. Dalam: Kumar V., Cotran R. S., Robbins S. L. Buku Ajar Patologi Robbins Volume 2. Edisi VII. Jakarta: EGC. Hlm. 572, 594.
Gartner J. P. and Hiatt J. L. 2007. Color Text Book of Histology. 3th ed. Philadelphia: Elsevier Saunders. Page 437.
Hartley TG. 1966. A revision of the Malesian species of Zanthoxylum (Rutaceae). Journal Arnold Arboretum. 47(3): 2.
Hartono, A. 1995. Prinsip Diet penyakit Ginjal. Edisi IV. Jakarta : ARCAN. Hlm. 9-10.
Hodgson, E. and Levi P.E. 2001. A textbook of modern toxicology. 2nd ed. New York: The McGraw-Hill. Pages 492-500.
Hrapkiewicz, K., dan Medina, L. 2007. Laboratory Animal. USA: Blackwell Publishing. Page. 46, 51.
Irianto, K. 2004. Struktur dan Fungsi Tubuh Manusia untuk Paramedis. Bandung: Yrama Widya. Hlm. 224-226.
Maulana, A.I. 2010. Pengaruh Ekstrak Tauge (Phaseolus Radiatus) Terhadap Kerusakan Sel Ginjal Mencit (Mus Musculus) yang Diinduksi Parasetamol. [Karya Tulis Ilmiah]. Surakarta: Fakultas Kedokteran Universitas Sebelas Maret. Hlm. 10-14.
Mayori, R., Netty, M., dan Djong, H. T. 2013. Pengaruh Pemberian Rhodamin B Terhadap Struktur Histologis GinjalMencit Putih (Mus musculus L.). Jurnal Biologi Universitas Andalas. 2(1): 3.
Miftakhuromah dan Shinta S. 2009. Potensi Andaliman sebagai bahan antioksidan dan antimikroba alami. Jurnal Warta Penelitian dan Pengembangan Tanaman Industri. 15(2): 9-10.
Nasution, A. H. 2010. Gambaran Makroskopis dan Mikroskopis Ginjal Mencit (Mus musculus) Akibat Pemberian Pb Asetat dan Rosella (Hibiscus sabdariffa). [Karya Tulis Ilmiah]. Medan: Fakultas Kedokteran Universitas Sumatera Utara. Hlm. 8-12.
Panjaitan, A.C. 2012. Efek Pemberian Ekstrak Segar dan Ekstrak Etanol Andaliman (Zanthoxyllum acanthopodium DC.) Terhadap Gambaran Histologis Ginjal Mencit (Mus musculus L.) Strain DDW. [Skripsi]. Medan: Universitas Sumatera Utara. Hlm. 45.
Prakoso, R.B. 2008. Pengaruh Pemberian Ekstrak Kunyit (Curcuma domestica) terhadap Gambaran Mikroskopis Ginjal Mencit Balb/C yang Diberi Parasetamol. [Karya Tulis Ilmiah]. Semarang: Fakultas Kedokteran Universitas Diponegoro. Hlm. 7.
Pratita, (2008). Pengaruh Pemberian Ekstrak Daun Jati Belanda (Guazuma ulmifolia Lamk.) dengan Dosis Bertingkat Terhadap Gambaran Histopatologis Ginjal Tikus Putih (Rattus norvegicus B.) Galur Wistart. [Karya Tulis Ilmiah]. Semarang: Fakultas Kedokteran Universitas Diponegoro. Hlm. 13.
Pratiwi. 2006. Pengaruh Ekstrak Buah Andaliman (Zanthoxylum acanthopodium DC.) Terhadap Perkembangan Embrio Mencit (Mus musculus L.) Strain DDW Sejak Praimplantasi Sampai Prenatal. [Skripsi]. Medan: Fakultas MIPA Universitas Sumatera Utara. Hlm. 41.
Robbins, S.L. dan Kumar, V. 1995. Buku Ajar Patologi II (Basic Pathology II). Jakarta: EGC. Hlm. 375, 379.
Sabri, E. 2007. Efek perlakuan ekstrak andaliman (Zanthoxyllum acanthopodium) pada tahap praimplantasi terhadap fertilitas dan perkembangan embrio mencit (Musmusculus L.). Jurnal Biologi Sumatera. 2(2): 4.