UIN SYARIF HIDAYATULLAH JAKARTA
ANALISIS KANDUNGAN MERKURI DAN
HIDROKUINON DALAM KOSMETIK KRIM
RACIKAN DOKTER
SKRIPSI
GIANTI
NIM: 109102000058
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
JAKARTA
UIN SYARIF HIDAYATULLAH JAKARTA
ANALISIS KANDUNGAN MERKURI DAN
HIDROKUINON DALAM KOSMETIK KRIM
RACIKAN DOKTER
SKRIPSI
Diajukan sebagai syarat untuk memperoleh gelar sarjana farmasi
GIANTI
NIM: 109102000058
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
JAKARTA
Skripsi ini adalah hasil karya saya sendiri,
dan semua sumber baik yang dikutip maupun dirujuk
telah saya nyatakan dengan benar
Nama : Gianti
NIM : 109102000058
Tanda Tangan :
Nama : Gianti
NIM : 109102000058
Program Studi : Farmasi
Judul Skripsi : Analisis kandungan merkuri dan hidrokuinon dalam
kosmetik krim racikan dokter
Disetujui Oleh:
Pembimbing I Pembimbing II
Drs. Umar Mansur, M.Sc., Apt Sabrina, M.Farm., Apt
NIP: 19790222200702001
Mengetahui,
Kepala Program Studi Farmasi
FKIK UIN Syarif Hidayatullah Jakarta
Skripsi ini diajukan oleh :
Nama : Gianti
NIM : 109102000058
Program Studi : Strata-1 Farmasi
Judul Skripsi : Analisis kandungan merkuri dan hidrokuinon dalam
kosmetik krim racikan dokter
Telah berhasil dipertahankan di hadapan Dewan Penguji dan diterima sebagai bagian persyaratan yang diperlukan untuk memperoleh gelar Sarjana Farmasi pada Program Studi Farmasi, Fakultas Kedokteran dan Ilmu Kesehatan, Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta.
DEWAN PENGUJI
Pembimbing I : Drs. Umar Mansur, M.Sc., Apt
(
)
Pembimbing II : Sabrina, M.Farm., Apt
(
)
Penguji I : Zilhadia, M.Si., Apt (
)
Ditetapkan di : Jakarta
NIM : 109102000058
Program Studi : Strata-1 Farmasi
Judul Skripsi : Analisis kandungan merkuri dan hidrokuinon dalam kosmetik krim racikan dokter
Hidrokuinon dan merkuri banyak digunakan dalam kosmetik untuk menghilangkan bercak-bercak hitam pada wajah. Kadar hidrokuinon melebihi 5% dapat menimbulkan kemerahan dan rasa terbakar pada kulit. Merkuri dalam kadar terkecil dapat bersifat racun, mulai dari perubahan warna kulit, bintik-bintik hitam, alergi serta iritasi. Pada pemakaian dosis tinggi dapat menyebabkan kerusakan permanen otak, ginjal dan gangguan perkembangan janin. Empat sampel racikan dokter yang diambil dari beberapa wilayah, dianalisis dengan menggunakan HPLC untuk mengetahui kadar hidrokunon. Kadar merkuri dianalisis dengan menggunakan mercury analyzer. Hasil pemeriksaan terhadap 4 sampel menunjukkan krim A mengandung 3,499 % hidrokuinon dan 0,1833 % merkuri, krim B mengandung 3,561 % hidrokuinon dan 0,1708 % merkuri, krim C mengandung 3,754 % hidrokuinon dan 0,1324 % merkuri, krim D mengadung 3,541 % hidrokuinon.
Kata kunci : krim, hidrokuinon, merkuri, HPLC, mercury analyzer
NIM : 109102000058
Study program : 1-strata pharmacy
Title : Determining of mercury and hydroquinone in cosmetic of doctor’s formulation.
Hydroquinones and mercury is widely used in cosmetics to eliminate black spots on the face. Levels of hydroquinones, which exceeded the 5% can cause redness and burning feeling on the skin. Meanwhile, in the levels of that a little mercury can sort of poison. Ranging from skin discoloration, dark spots, allergies, irritation, as well as on the use of high doses can cause permanent damage to the brain, kidneys and impaired fetal development.four samples of doctor’s formulations those taken from several areas, analyzed by HPLC (High Perform Liquid Chromatography) to know the levels of hydroquinone. The levels of mercury analyzed by mercury analyzer. 4 samples that analyzed ,cream A containing 3,499 % hidroquinone and 0,1833 % mercury, cream B containing 3,561 % hidroquinone and 0,1708 % mercury, cream C containing 3,754 % hidroquinone and 0,1324 % mercury and cream D containing 3,541 % hidroquinone.
Puji dan syukur kehadirat Allah SWT yang senantiasa mencurahkan segala
rahmat-Nya kepada kita semua, khususnya saya sebagai penulis sehingga dapat menyelesaikan skripsi yang berjudul “Analisis Kandungan Merkuri Dan Hidrokuinon Dalam Kosmetik Krim Racikan Dokter” ini. Shalawat serta salam
senantiasa terlimpahkan kepada junjungan kita nabi muhammad SAW, yang telah
membawa kita dari kegelapan menuju dunia yang terang benderang yang penuh
dengan ilmu pengetahuan. Semoga kita mendapat syafa’atnya di hari kiamat. amin
Skripsi ini disusun berdasarkan hasil penelitian di laboratorium penelitian II
dan laboratorium kimia obat UIN syarif hidayatullah jakarta. Skripsi ini juga
disusun berdasarkan dari berbagai sumber. Dalam menyelesaikan masa
perkuliahan sampai penulisan ini tentu banyak berbagai halangan serta kesulitan yang menyertai, sehingga penulis tidak terlepas dari do’a, dorongan, bantuan, dan bimbingan dari banyak pihak. Oleh karena itu, izinkan menulis untuk
menghaturkan ucapan terimakasih yang mendalam kepada :
1. Bapak Drs. Umar Mansur, M.Sc., Apt sebagai Pembimbing I sekaligus
sebagai ketua Program Studi Farmasi Fakultas Kedokteran Dan Ilmu
Kesehatan yang telah bersedia memberikan ilmu, waktu, tenaga, nasehat,
serta arahan selama penelitian dan penulisan skripsi ini.
2. Ibu Sabrina, M.Farm, Apt sebagai Pembimbing II sekaligus sebagai
pembimbing akademik yang telah bersedia memberikan ilmu, waktu,
tenaga, nasehat, serta arahan selama masa perkuliahan, penelitian dan
penulisan skripsi ini.
3. Ibu Zilhadia, M.Si., Apt sebagai penguji I dan ibu Lina Elfita M.Si., Apt
sebagai penguji II yang telah banyak sekali mengoreksi kesalahan saya dan
membantu saya dalam menyelesaikan skripsi ini.
4. Bapak Prof. Dr. (hc). dr. MK. Tadjudin, Sp.And selaku Dekan Fakultas
Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri (UIN) Syarif
Hidayatullah Jakarta.
5. Bapak dan Ibu staf pengajar, serta karyawan yang telah memberikan
6. Kedua orang tua tercinta, Ayahanda Tugiman dan Ibunda Boniyem yang
selalu ikhlas tanpa pamrih memberikan kasih sayang, dukungan moral,
material, nasehat-nasehat, serta lantunan doa di setiap waktu.
7. Kakanda tercinta Sarmoko S.Pdi dan ayunda tersayang Ummi kaltsum S.Pdi
yang turun mendoakan dan menuntut saya untuk lebih giat belajar demi
mencapai cita-cita yang saya inginkan.
8. Teman-teman di Program Studi Farmasi khususnya 2009 serta adik-adik
yang tidak bisa di sebutkan satu persatu.
9. Sahabat special, seperjuangan sekaligus sekamar dengan saya Astuti Puji
Utami Bachtiar yang selalu menemani saya dikala suka maupun duka.
10. Calon suami saya tercinta Omika Asnadi S.Pdi yang turut mendoakan dan
memotivasi saya untuk semangat belajar dan siap menjadi teman hidup saya
di dunia dan insha allah di akhirat
11. Semua pihak yang telah membantu penulis selama melakukan penelitian
dan penulisan yang tidak dapat disebutkan satu per satu.
Semoga semua bantuan yang telah diberikan mendapatkan balasan dari
Allah SWT. Penulis menyadari bahwa masih banyak kekurangan dalam penulisan
ini, oleh karena itu kritik dan saran sangat diharapkan demi perbaikan skripsi ini.
Dan semoga skripsi ini bisa bermanfaat bagi pengembangan ilmu pengetahuan.
Jakarta, 24 Oktober 2013
Sebagai sivitas akademik Universitas Islam Negeri (UIN) Syarif Hidayatullah
Jakarta, Saya yang bertanda tangan di bawah ini :
Nama : Gianti
NIM : 109102000058
Program studi : Farmasi
Fakultas : Fakultas Kedokteran dan Ilmu Kesehatan (FKIK)
Jenis Karya : Skripsi
Demi pengembangan ilmu pengetahuan, saya menyetujui skripsi/ karya ilmiah
saya dengan judul:
ANALISIS KANDUNGAN MERKURI DAN HIDROKUINON DALAM KOSMETIK KRIM RACIKAN DOKTER
Untuk dipublikasikan atau ditampilkan di internet atau media lain yaitu Digital Library Perpustakaan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta untuk kepentingan akademik sebatas sesuai dengan Undang-Undang Hak Cipta.
Dengan demikian persetujuan publikasi karya ilmiah ini saya buat dengan sebenarnya.
Dibuat di : Ciputat
Pada Tanggal : 24 Oktober 2013
Yang menyatakan,
HALAMAN JU
HALAMAN PERNYATAAN ORISINALITAS ... iii
HALAMAN PERSETUJUAN PEMBIMBING ... iv
HALAMAN PENGESAHAN ... v
ABSTRAK ... vii
ABSTRACT ... viii
KATA PENGANTAR ... ix
HALAMAN PERSETUJUAN PUBLIKASI KARYA ILMIAH ... x
DAFTAR ISI ... xi
2.2.3 Beberapa Data Kelarutan Komponen Dalam Krim ... 7
2.8 Tekhnik Sampling ... 22
2.8.1 Definisi Sampel dan Sampling ... 22
2.8.2 Tekhnik Pengambilan Sampel ... 22
2.9 Validasi Metode ... 23
BAB 3. KERANGKA KONSEP... 25
BAB 4. METODE PENELITIAN ... 26
4.1 Pengambilan Sampel ... 26
4.2 Tempat dan Waktu Penelitian ... 26
4.3 Alat dan Bahan ... 26
4.3.1 Alat ... 26
4.3.2 Bahan ... 27
4.4 Prosedur Penelitian ... 27
4.4.1 Analisis Hidrokuinon ... 28
4.4.2 Analisis Merkuri ... 29
BAB 5. HASIL DAN PEMBAHASAN ... 30
5.1 Hasil Percobaan ... 30
5.2 Pembahasan... 32
BAB 6. KESIMPULAN DAN SARAN ... 37
6.1 Kesimpulan ... 37
6.2 Saran ... 37
Lampiran 1. Uji Linieritas dan Pembuatan Kurva Kalibrasi Hidrokuinon ... 42
Lampiran 2. Data Parameter Uji LOD dan LOQ ... 43
Lampiran 3. Uji Perolehan Kembali ... 44
Lampiran 4. Penentuan Kadar HQ Sampel Krim Racikan Dokter ... 46
Lampiran 5. Penentuan Panjang Gelombang Maksimum Hidrokuinon ... 47
Lampran 6. Kromatogram Larutan Standar Hirokuinon ... 48
Lampiran 7. Kurva Kalibrasi Standar Hidrokuinon ... 51
Lampiran 8. Kromatogram Krim Simulasi Hidrokuinon ... 52
Lampiran 9. Kromatogram Sampel Krim Racikan Dokter ... 55
Lampiran 10. Alat HPLC ... 57
Lampiran 11. Sertifikat Analisis Standar Hidrokuinon ... 58
Lampiran 12. Kurva Kalibrasi Standar Merkuri ... 59
Lampiran 13. Data Parameter Uji LOD Dan LOQ Pada Standar Merkuri ... 60
Lampiran 14. Hasil Pengukuran Kadar merkuri ... 61
Lampiran 15. Alat Mercury Analyzer ... 62
HQ : Hidrokuinon
HPLC : High Perform Liquid Chromatography LOD : Limit of Detection
LOQ : Limit of Quantification
MA : Mercury Analyzer
RD : Racikan Dokter
CVAAS : Cold Vapour Atomic Absorbtion Spectrofotometer PPT : Part Per Triliun
PPB : Part Per Billion PPM : Part Per Million ODS : Okta Desil Silica
PG : Propilen Glikol
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Maraknya kosmetik racikan dokter yang diberikan kepada pasien dinilai
dapat membahayakan konsumen. Dua zat kimia yang sering ditambahkan
dalam kosmetik adalah hidrokuinon dan merkuri, karena kemampuan zat
tersebut untuk menghambat pembentukan melanin pada permukaan kulit dan
menjadikan kulit putih mulus dalam waktu yang relatif singkat (Syafnir et al.,
2011).
Kosmetik berbentuk krim yang mengandung hidrokuinon banyak
digunakan untuk menghilangkan bercak-bercak hitam pada wajah. Daya kerja
pemucatan hidrokuinon sangat lambat dan akan lebih cepat dengan kadar yang
lebih tinggi, tetapi kadar yang tinggi akan memberikan efek samping yang
tidak diinginkan (Ibrahim et al., 2004).
Hidrokuinon lebih dari 2% merupakan golongan obat keras yang
penggunaannya berdasarkan resep dokter. Kadar hidrokuinon yang melebihi
5% dapat menimbulkan kemerahan dan rasa terbakar pada kulit. Bahaya
pemakaian obat keras ini tanpa pengawasan dokter dapat menyebabkan iritasi
kulit, kulit kemerahan, rasa terbakar, kelainan ginjal, kanker darah dan kanker
hati. Pemakaian yang berlebih dapat menyebabkan iritasi kulit, namun jika
dihentikan seketika akan berefek lebih buruk. Kadar hidroquinon dalam krim
yang beredar di pasaran hanya diperbolehkan 2%, lebih dari itu dipergunakan
sebagai obat (BPOM RI, 2007).
Merkuri adalah unsur yang mempunyai nomor atom 80 dengan berat
molekul relatif 200,59. Merkuri diberikan simbol kimia Hg yang berasal dari
bahasa yunani hydrargyricum yang berarti cairan berwarna perak (SPU, 2007)
Dalam kosmetik krim biasanya digunakan merkuri anorganik, yaitu
ammoniated mercury, merkuri juga dapat ditemukan dalam kosmetik yang
lain, misalnya dalam produk pembersih make up mata dan maskara.
Ammoniated mercury 1-10 % digunakan sebagai bahan pemutih kulit dalam
sediaan krim karena berpotensi sebagai bahan pemucat warna kulit. Daya
ginjal, saraf dan otak sangat kuat maka pemakaiannya dilarang dalam sediaan
kosmetik (WHO, 2011).
Menurut Peraturan Mentri Keseharan RI No. 445/MENKES/PER/V/1998
tentang bahan, zat warna, substrat, zat pengawet dan tabir surya pada
kosmetik. Dalam kadar yang sidikitpun merkuri dapat bersifat racun. Mulai
dari perubahan warna kulit, bintik-bintik hitam, alergi, iritasi, serta pada
pemakaian dosis tinggi dapat menyebabkan kerusakan permanen otak, ginjal
dan gangguan perkembangan janin. Bahkan, paparan jangka pendek dalam
dosis tinggi dapat menyebabkan muntah-muntah, diare dan kerusakan
paru-paru serta merupakan zat karsinogenik (BPOM RI, 2007)
Karena masyarakat percaya sepenuhnya kepada dokter spesialis yang
menanganinya, seringkali tidak peduli apakah kosmetik yang diberikan telah
terdaftar di BPOM atau belum. Kesadaran dokter juga diperlukan sehingga
tidak hanya mendahulukan profit tapi juga keamanan. Masyarakat yang hanya
melihat hasil tanpa melihat efek juga tidak pernah tahu bahwa ternyata
kosmetik yang digunakan mengandung zat kimia yang berbahaya.
Banyaknya dokter yang memberikan kosmetik racikan untuk konsumen
yang tidak diketahui dengan jelas kandungan dalam sediaan krim kosmetik
tersebut, diduga dapat membahayakan konsumen. Hal ini diakibatkan
kecenderungan penggunaan hidrokuinon dan merkuri dalam sediaan kosmetik
racikan dokter. Untuk menghindari terjadinya efek yang tidak diinginkan,
maka peneliti menguji kosmetik racikan dokter untuk dianalisis kandungan
hidrokuinon dan merkuri dalam krimm sediaannya. Karena kedua zat tersebut
dapat membahayakan kesehatan konsumen.
Terdapat beberapa metode pada penentuan kadar merkuri. Yaitu dengan
spektrofotometri serapan atom dan titrasi ditizon (DepKes, 1995), CVAAS
(Irianto, 1998 & Parenkuan et al., 2013),dan metode kompleksometri (RAY &
Underwood, 2002).
Penetapan kadar hidrokuinon ada beberapa metode yang dapat digunakan,
diantaranya dengan Titrasi Redoks (DepKes, 1995), Spektrofotometri UV
(Pedro et al., 2007), Kolorimetri (Ibrahimet al., 2004), Thin Layer
Chromatography (BPOM, 2005), Gas Chromatography Mass
Spectrofotometry (Saito et al., 1994), Miselar Elektro Kromatografi
(Jangseokim dan Youngseong Kim, 2005) dan Capillary
Electrochromatography (Desiderio et al., 2000).
Penelitian ini dilakukan pengukuran kadar merkuri dengan alat Mercury
Analyzer karena alat ini dapat mendeteksi hingga konsentrasi ppt, spesifik
untuk merkuri, preparasi yang sederhana, dan aman (Akaojicho, 2003).
Sedangkan untuk analisis hidrokuinon menggunakan alat HPLC karena dapat
dilakukan pada suhu ruang, kolom dapat digunakan berulang, cepat, dan
mudah dioperasikan secara otomatis (Harmita, 2005).
1.2 Batasan Masalah
Pada penelitian ini, masalah hanya dibatasi pada :
1. Sampel yang diteliti adalah krim malam pada beberapa merk yang diracik
oleh dokter di wilayah Cileduk, Cirendeu, Bintaro dan Depok
2. Zat yang akan ditetapkan kadarnya adalah hidrokuinon dan merkuri
1.3 Rumusan Masalah
1. Apakah dalam 4 sampel krim racikan dokter mengandung hidrokuinon ?
2. Apakah dalam 3 sampel krim racikan dokter mengandung merkuri ?
3. Berapakah kadar hidrokuinon yang terdapat dalam 4 sampel yang diuji ?
4. Berapakah kadar merkuri yang terdapat dalam 3 sampel yang diuji ?
5. Apakah kadar hidrokuinon dan merkuri yang terdapat dalam krim racikan
dokter tersebut masih berada pada batas yang diizinkan pemerintah ?
1.4 Tujuan Penelitian
1. Menganalisis kadar hidrokuinon dalam kosmetik racikan dokter
2. Menganalisis kadar merkuri dalam kosmetik racikan dokter
3. Menilai apakah krim racikan dokter yang dianaisis masih dalam taraf
1.5 Hipotesa Penelitian
1. Diduga beberapa krim kosmetik racikan dokter yang banyak digunakan
mengandung hidrokuinon dan atau merkuri.
2. Diduga adanya kandungan hidrokuinon yang melebihi batas yang
diperbolehkan dalam krim kosmetik racikan dokter
1.6 Manfaat Penelitian 1. Manfaat umum
a. Memberi informasi pada masyarakat agar berhati-hati dalam
menggunakan kosmetik yang digunakan terutama yang tidak
teregistrasi di BPOM
b. Masyarakat lebih berhati-hati dalam menggunakan kosmetik racikan
dokter
2. Manfaat khusus
a. Memperdalam ilmu peneliti tentang analisa
b. Memberi masukan kepada pemerintah supaya lebih ketat untuk
BAB 2
TINJAUAN PUSTAKA
2.1 Kosmetik
2.1.1 Definisi Kosmetik
Kosmetik adalah sediaan atau paduan bahan yang untuk digunakan
pada bagian luar badan (kulit, rambut, kuku, bibir dan organ kelamin
bagian luar), gigi dan rongga mulut untuk membersihkan, menambah daya
tarik, mengubah penampilan, memperbaiki bau badan, melindungi atau
memelihara tubuh pada kondisi baik (BPOM RI, 2011).
2.1.2 Penggolongan Kosmetik (Iswari, 2007)
Kosmetik dapat digolongkan berdasarkan kegunaan bagi kulit :
1. Kosmetik perawatan kulit (skin-care cosmetic)
a. Kosmetik untuk membersihkan kulit (cleanser), misalnya sabun, susu
pembersih wajah dan penyegar kulit (freshner)
b. Kosmetik untuk melembabkan kulit (mouisturizer), misalnya
mouisterizer cream, night cream
c. Kosmetik pelindung kulit, misalnya sunscreen cream dan sunscreen
foundation, sun block cream/lotion
d. Kosmetik untuk menipiskan atau mengampelas kulit (peeling), misalnya
scrub cream yang berisi butiran-butiran halus yang berfungsi sebagai
pengampelas (abrasiver)
e. Kosmetik untuk membersihkan kulit (cleanser), misalnya sabun, susu
pembersih wajah dan penyegar kulit (freshner).
2. Kosmetik riasan (dekoratif atau make-up)
Jenis ini diperlukan untuk merias dan menutup cacat pada kulit sehingga
menghasilkan penampilan yang lebih menarik. Dalam kosmetik riasan, peran
zat pewarna dan zat pewangi sangat besar.
2.2 Krim
2.2.1 Definisi Krim
Krim merupakan suatu sediaan berbentuk setengah padat
bahan dasar yang sesuai, berupa emulsi kental mengandung tidak kurang
60 % air ditujukan untuk pemakaian luar (Anief, 2000).
Formulasi krim ada dua, yaitu krim air dalam minyak (A/M),
misalnya cold cream dan minyak dalam air (M/A), misalnya vanishing
cream (Yanhendri, 2012).
2.2.2 Contoh Formula Krim
Contoh krim A/M (Yahendri, 2012 dan Katsure et al., 2008)
R/ Cerae alba 5
Contoh krim M/A (Anief, 2000)
R/ acedi stearinici 15
2.2.3 Beberapa Data Kelarutan Komponen Dalam Krim
Cera alba : Praktis tidak larut dalam air, agak sukar larut dalam etanol
95% dingin, larut dalam kloroform, eter hangat, minyak
lemak dan minyak atsiri (DepKes, 1979).
Parafin liquid : Praktis tidak larut dalam air, dan etanol 95%, larut dalam
Hard paraffin : Praktis tidak larut dalam air, dan etanol 95%, larut dalam
kloroform (DepKes, 1979).
Cetaceum : Praktis tidak larut dalam air, dalam etanol 95% dingin, larut
dalam 20 bagian etanol 95% mendidih, koroform, eter,
karbon disulfida, minyak lemak dan minyak atsiri (DepKes,
1979).
Olive oil : Sukar larut dalam etanol 95%, mudah larut dalam
kloroform dalam eter dan minyak tanah (DepKes, 1979)
Triethanolamine : Mudah larut dalam air, kloroform dan etanol 95% (DepKes,
1979)
Vaselin album : Praktis tidak larut dalam air, dan etanol, larut dalam
kloroform, eter, minyak tanah (DepKes, 1979)
Asam stearat : Praktis tidak larut dalam air, larut dalam 20 bagaian etanol
95%, 2 bagian klroform dan 3 bagian eter (DepKes, 1979)
Propilen glikol : Bercampur dengan air, etanol 95% dan kloroform, larut
dalam 6 bagian eter, tidak bercampur dengan minyak tanah
dan minyak lemak (DepKes, 1979)
Setil alkohol : Tidak larut dalam air, larut dalam etanol dan eter, kelarutan
bertambah dengan naiknya suhu (DepKes, 1995)
Gliserin : Bercampur dengan air dan etanol, tidak larut dalam eter,
korofor, minyak lemak dan minyak atsiri (DepKes, 1995)
Gom arab : Larut dalam 2 bagian air, praktis tidak larut dalam etanol
dan eter (DepKes, 1979)
Karbomer : Larut dalam air, etanol dan gliserol (DepKes, 1995)
Tokoferol : Praktis tidak larut dalam air, sukar larut dalam alkali, larut
dalam etanol 95%, eter, aseton dan miyak nabati,sangat
mudah larut dalam kloroform (DepKes, 1979)
Niasin amida : Mudah larut alam air, etanol dan gliserol (DepKes, 1979)
Krim tipe A/M biasanya menggunakan surfaktan seperti, sabun polivalen,
span, adeps lannae dan cera. Sedangkan untuk krim dengan tipe M/A biasanya
stearat, amonium stearat, tween, natrium lauril sulfat, kuning telur, CMC,
emulgidum, pectinum dan gelatin (Anief, 2000).
2.3 HPLC (High Performance Liquid Chromatography) 2.3.1 Definisi HPLC
Kromatografi cair berperforma tinggi (High Performance Liquid
Chromatography, HPLC) merupakan salah satu teknik kromatografi untuk
zat cair yang disertai dengan tekanan tinggi. Dilihat dari peralatannya
HPLC termasuk kromatografi kolom karena fase diam terpacking dalam
kolom. HPLC digunakan untuk memisahkan molekul berdasarkan
perbedaan afinitasnya terhadap zat padat tertentu. Cairan yang akan
dipisahkan merupakan fasa cair dan zat padatnya merupakan fasa diam
(stasioner). Teknik ini sangat berguna untuk memisahkan beberapa
senyawa sekaligus karena setiap senyawa mempunyai afinitas selektif
antara fasa diam tertentu dan fasa gerak tertentu. Dengan bantuan detektor
serta integrator kita akan mendapatkan kromatogram. Kromatogram
memuat waktu tambat serta tinggi puncak suatu senyawa (Ketut, 2010).
2.3.2 Kelebihan HPLC (Ketut, 2010)
HPLC dapat digunakan untuk analisis kualitatif dan kuantitatif. Kelebihan
HPLC dibandingkan dengan jenis kromatografi lain adalah :
a. Dapat dilakukan pada suhu kamar
b. Kolom dan pelarut pengembang dapat digunakan berkali-kali
c. Detektor HPLC dapat divariasikan dan mempunyai banyak jenis
d. Waktu analisis pada umumnya relatif singkat
e. Ketepatan dan ketelitian relatif tinggi
f. Mudah dioperasikan secara otomatis
2.3.3 Komponen HPLC (Ketut, 2010)
Secara garis besar instrumentasi HPLC terdiri dari :
a. Pelarut
Pelarut merupakan fase gerak. Pemilihan fase gerak berdasarkan pada
b. Kolom
Kolom berisi fase diam. Fasa diam yang biasa digunakan adalah kolom
C18 yang bersifat non polar dan fasa geraknya bersifat polar. Jenis
pemisahan ini disebut dengan kromatografi partisi fasa terbalik.
Senyawa yang polar akan keluar terlebih dahulu sehingga memiliki
waktu retensi yang relatif kecil sedangkan senyawa non polar akan
ditahan lebih lama oleh fasa diamnya
c. Pompa
Pompa berfungsi untuk mengalirkan fase gerak melewati fase diam
untuk membawa sampel yang ada dalam fase diam.
d. Detektor
Detektor yang digunakan dalam HPLC adalah detektor UV, radiasi
UV, fluoresens, refraktif index dan detektor NMR yang baru
dikembangkan.
e. Injektor
Injektor HPLC yang dipakai secara umum adalah :
1. Injektor dengan memakai diafragma (septum injector)
2. Injektor tanpa memakai diafragma (septumless injection system)
3. Injektor dengan pipa dosis (loop valve)
4. Sistem injeksi otomatis (autoinjector)
2.4 Mercury Analyzer (Yusnizam, 2008) 2.4.1 Definisi
Mercury analyzer merupakan alat untuk menganalisa merkuri yang
cepat, mempunyai sensitivitas yang tinggi, dapat menentukan jumlah
merkuri pada sampel padat, cair dan gas dengan operasi yang mudah.
Merupakan metode otomatis di mana sampel disuntikkan ke dalam aliran
kontinu cairan pembawa yang mencampur dengan larutan lain yang terus
mengalir sebelum mencapai detektor. Flow injection analysis salah
satunya adalah FIMS (Flow Injection Mercury Spectrometer).
2.4.2 Prinsip Kerja
tersebut akan ditangkap oleh amalgam sehingga yang tinggal hanya uap
merkuri. Analisa dengan instrumentasi dilakukan pada panjang gelombang
253.7 nm. Gas merkuri yang dihasilkan akan dilewatkan pada cell tube
yang ditembakkan sinar/cahaya dari lampu merkuri. Besarnya konsentrasi
yang dihasilkan sebanding dengan konsentrasi merkuri yang terkandung
dalam sampel dan sebanding dengan nilai absorban yang dihasilkan.
2.5 Hidrokuinon
2.5.1 Identitas
Rumus kimia : C6H6O2 (DepKes, 1995)
Rumus bangun : (DepKes, 1995)
Gambar 1.Struktur Senyawa Hidrokuinon
Sinonim :Alpha-hydroquinone; Hydroquinol; Quinol;Benzoquinol;
1,4-Benzenediol; 1,4-Dihydroxybenzene;
p-Dihydroxybenzene; p-Hydroxyphenol; p-Dioxobenzene;
1,4-Dihydroxybenzene; Dihydroquinone; Pyrogentistic
acid; Quinnone; Aida; Tecquinol; Tenox HQ; Tequinol.
(BPOM, 2011)
BM : 110,11 (DepKes, 1995)
Golongan : Kuinon (BPOM, 2011)
2.5.2 Persyaratan Kadar
Bahan baku hidrokuinon mengandung tidak kurang dari 99% dan
tidak lebih dari 10,5% C6H4(OH)2 dihitung terhadap zat anhidrat (Depkes,
2.5.3 Data Fisikokimia
Pemerian :Berbentuk jarum halus, putih, mudah menjadi gelap
dengan adanya paparan cahaya dan udara (DepKes, 1995)
Jarak lebur :172 - 1740 C (DepKes, 1995)
Titik didih :285 0C – 287 0C (DHHS, 2009)
Kelarutan :Mudah larut dalam air, alkohol dan eter (DepKes, 1995)
Stabilitas :Stabil pada tekanan dan suhu normal stabil, tidak menyatu
dengan oksidator kuat, basa kuat, O2, Fe. Sensitif terhadap
cahaya dan udara (BPOM, 2011)
Efek samping :Efek samping hidrokinon dapat menimbulkan
Hidrokuinon merupakan suatu reduktor dengan potensial
elektrokimia E0. +268 mV. Pada titrasi oksidasi reduksi,
hidrokuinon akan melepaskan elektron (mengalami oksidasi)
sementara titran akan mengalami reduksi karena mengikat
elektron. Prosedur analisis hidrokuinon secara titrasi redoks
menurut Farmakope Indonesia edisi IV:
Timbang seksama sampel sebanyak 250 mg, larutkan dalam
campuran 100 ml air dan 10 ml asam sulfat 0,1 N, tambahkan 3
tetes difenilamin dan titrasi dengan serium IV sulfat 0,1 N
dengan 1 ml serium IV sulfat 0,1 N setara dengan 5,506 mg
C6H6O2 (DepKes, 1995).
b. Spektrofotometri UV-Vis (Garcia et al., 2007 )
Hidrokuinon memiliki gugus kromofor sehingga dapat
dianalisa dengan menggunakan alat spektrofotometri UV-Vis.
Cara yang dilakukan untuk analisa hidrokuinon dengan metode
ini adalah :
Diukur panjang gelombang secara spektrofotometri
ultraviolet pada panjang gelombang 200 - 400 nm. Sedangkan
untuk menghitung kadar hidrokuinon dalam sampel dihitung
dengan menggunakan kurva baku dengan persamaan regresi :
y = a ± bx
c. Kromatografi Lapis Tipis (Siddique et al., 2012)
Analisis hidrokuinon menggunakan fase diam yang bersifat
polar dan fase diam yang bersifat nonpolar. Kuantitas
hidrokuinon dihitung dengan membandingkan luas puncak
bercak sampel terhadap bercak standar menggunakan alat
densitometri yang diukur pada panjang gelombang
maksimumnya.
Fase gerak yang dapat digunakan adalah :
1. Metanol-kloroform (50:50) (DepKes,1995)
2. Heksana-aseton (3:2) (Siddique et al., 2012)
d. HPLC (High Permormance Liquid Chromatography)
Sistem kromatografinya merupakan kromatografi fase
terbalik. dimana fase diam bersifar non polar dengan fase gerak
bersifar polar. Berikut merupakan contoh kondisi kromatografi
untuk penetapan kadar hidrokuinon menggunakan HPLC :
Sistem kromatografi :Detektor 295 nm, kolom ODS
(Oktadesil Silika) (25cm x 4,6 mm),
laju alir 1,5 ml/menit
Kadar hidrokuinon dalam sampel diperoleh dengan
membandingkan luas puncak larutan sampel dengan standar
hidrokuinon (siddique et al., 2012) .
e. Misellar Electrokinetic Chromatography
Metode ini menggunakan surfaktan seperti SDS (Sodium
Dodesil Sulfat) dan CTAB (Cetil Trimetil Ammonium
Bromida) untuk menigkatkan resolusi dengan interaksi
hidrofobik antara inti hidrofobik dalam misel dengan analit.
Sistem kromatografinya menggunakan kolom kapiler fused
silica dengan detector UV (Jangseokminet al., 2005).
f. Capillary Electrochromatography (Desiderio et al., 2000)
Merupakan tekhnik analisis terbaru yang menggunakan
kapiler fused silica dengan kombinasi mekanisme
elektroporetik dan kromatografi. Analit dapat dipisahkan
berdasarkan perbedaan partisi dalam fase gerak dan fase diam.
Metode ini dapat digunakan untuk menganalisa analit netral
maupun analit yang bermuatan.
g. Kolorimetri (Ibrahim et al., 2004)
Metode ini menggunakan pereaksi floroglusin untuk
penentuan kadar hidrokuinon dalam krim pemucat. Kondisi
pengukuran dioptimumkan berdasarkan penentuan pengaruh
konsentrasi natrium hidroksida, penentuan pengaruh lama
pemanasan dan suhu optimum serta penentuan pengaruh
jumlah pereaksi floroglusin. Hasil yang diperoleh kemudian
diambil sebagai prosedur baku dalam reaksi warna. Teknik
kolorimetri mempunyai keunggulan karena senyawa yang
daerah ultraviolet tidak akan mengganggu pengukuran serapan
radiasi pada sinar tampak.
2.6 Merkuri 2.6.1 Identitas
No CAS :7487-94-7(MercuricChloride); 1600-27-7 (Mercuri
Acetate); 1344-48-5 (Mercuric Sulfide); 21908-53-2
(Mercuric Oxide) (EPA, 2007)
No atom : 80 (SPU, 2007)
Nama kimia : Hg/ Hydrargyrum (SPU, 2007)
Sinonim :Raksa, mercuric chloride, mercuric acetate,
mercuric sulfide, mercuric oxide, mercury bichloride,
corrosive sublimate, mercuric(II)chloride, mercury
perchloride, mercurous (I) chloride. (EPA, 2007)
2.6.2 Sifat fisikokimia
Pemerian : Cairan berat mengkilat, putih keperakan (DepKes,
1979)
Titik lebur : 234.32 K, -38.83 °C, -37.89 °F (Horas, 1985)
Titik didih : 629.88 K, 356.73 °C, 674.11 °F (Horas, 1985)
Berat jenis : 13,55 (Horas, 1985)
Kelarutan :Praktis tidak larut dalam air, etanol dan asam
klorida, larut sempurna dalam asam nitrat pekat
dan asam sulfat pekat (DepKes, 1979)
Jenis :
1. Uap merkuri (unsur merkuri), mempunyai tekanan uap yang
tinggi dan sukar larut dalam air. Paparan kronis uap merkuri
ialah akibat kontaminasi yang tidak disengaja dalam ruangan
dengan ventilasi yang buruk, misalnya dalam laboratorium
2. Merkuri anorganik (Hg2+ dan Hg22+), Hg2+ lebih reaktif yang
HgCl2 sangat larut dalam air dan sangat toksik sedangkan
HgCl tidak larut dan kurang toksik.
3. Merkuri organik, mengandung merkuri dengan satu ikatan
kovalen dengan atom karbon. Contoh ; metil merkuri.
Dianggap lebih berbahaya dan dapat larut dalam lapisan
lemak yang menyelimuti korda syaraf (Zulalfian, 2006)
2.6.3 Metode Analisis merkuri
a. AAS (Atomic Absoption Spectrophotometry)
Tekhnik AAS ini berdasarkan pada penguraian molekul
menjadi atom (atomisasi) dengan energi dari api atau arus listrik
(Harmita, 2006).
Dalam mendeteksi merkuri digunakan AAS yang khusus,
dilengkapi dengan perekam respon cepat dan dapat mengukur
radiasi yang diserap oleh uap merkuri pada garis resonansi merkuri
pada panjang gelombang 253,6 nm. berikut merupakan prosedur
menurut farmakope indonesia edisi IV.
Pasang alat erasi dan labu perangkap dalam keadaan
kosong, dan kran pada posisi langsung ke labu perangkap.
Hubungkan alat dengan sel penyerap dan atur laju aliran udara atau
nitrogen sehingga diperoleh penyerapan dan reprodusibilitas
maksimum tanpa busa berlebih dalam larutan uji. Usahakan
pembacaan garis dasar yang lurus pada 253,6 nm, sesuai petunjuk
penggunaan alat. perlakukan larutan baku dan larutan uji dengan
cara yang sama sebagai berikut : Hilangkan kelebihan permanganat
dengan penambahan tetes demi tetes larutan hidroksilamina
hidroklorida sampai larutan tidak berwarna. segera masukkan
larutan kedalam bejana aerasi, bilas dan encerkan dengan air
hingga 100 ml. tambahkan 2 ml larutan timah II klorida, dan segera
hubungkan kembali bejana dengan alat aerasi, putar kran dari
posisi langsung ke labu perangkap ke posisi aerasi dan teruskan
aerasi sampai puncak serapan telah terlampaui dan pena pencatat
alat setelah digunakan. Setelah dikoreksi dengan blanko pereaksi,
serapan larutan uji tidak boleh lebih dari larutan baku (DepKes,
1995).
b. Spektrofotometer UV-Vis (Harmita, 2006).
Sampel yang sering dianalisis dengan UV-Vis adalah
senyawa organik. Dimana senyawa organik dapat memberikan
serapan adalah senyawa yang mempunyau gugus kromofor dan
auksokrom. Gugus kromofor adalah gugus fungsional tidak jenuh
yang dapat memberikan serapan pada daerah UV atau cahaya
tampak. Hampir semua kromofor mempunyai ikatan rangkap
seperti alkena (C=C), C=O,NO2, benzene dan lain-lain. sedangkan
auksokrom adalah gugus fungsional seperti OH, NH2,X, yaitu
gugus yang mempunyai elektron nonbonding dan tidak
mengabsorbsi radiasi pada lamda diatas 200 nm, akan tetapi
mengabsorbsi sinar UV jauh.
Metode analisis kuantitatif yang menggunakan
spektrofotometer pada daerah tampak/visible (380 - 780 nm) sering
disebut dengan kalorimetri. Kalorimetri dapat didefinisikan sebagai
metode analisis kuantitatif suatu zat berdasarkan intensitas warna
yang timbul dari konsentrasi yang berbeda. Pada kalorimetri yang
ditentukan adalah serapan cahaya oleh larutan yang berwarna.
panjang gelombang dalam suatu sistem berwarna spesifik.
c. Titrasi ditizon
Untuk menentukan kadar merkuri dengan titrasi ditizon,
pertama-tama dilakukan dengan pembuatan pereaksi, lalu dibuat
larutan hidroksilamina hidroklorida, larutan baku raksa, larutan
pengekstrasi ditizon dan pembakuan titran ditizon. Setelah itu buat
larutan uji dengan menimbang 2 g, lalu masukkan kedalam labu
erlenmeyer 250 ml bersumbat kaca, tambahkan 20 ml campuran
asam nitrat spekat dan asam sulfat pekat dengan volume yang
sama, hubungkan dengan pendingin yang sesuai, refluks campuran
didihkan sampai asam nitritnya habis. Dinginkan larutan, encerkan
hati-hati dengan air, pindahkan kedalam labu 200 ml, encerkan
hingga tanda batas, campur kemudian saring. Masukkan 50 ml
larutan uji kedalam corong pisah 250 ml, ekstraksi beberapa kali
dengan sedikit kloroform pekat, sampai ekstrak kloroform terakhir
tidak berwarna. Buang ekstrak klorofrom dan tambahkan 50 ml
asam sulfat 1 N pada larutan yang tertinggal, ditambah 90 ml air, 1
ml asam asetat glasial dan 10 ml larutan hidroksilamina
hidroklorida pekat (1 dalam 5). Hitung jumlah merkuri (DepKes,
1995).
d. Kompleksometri (Day dan Underwood, 2002)
Untuk menentukan merkuri dapat dilakukan dengan metode
kompleksometri dengan cara, pertama ion Hg2 ditentukan dengan
cara titrasi kembali, larutan uji direaksikan dengan larutan natrium
EDTA berlebih dan kelebihannya dititrasi dengan larutan seng
klorida atau larutan seng sulfat. Sehingga ion merkuri yang
bervalensi dua yang ada merupakan atom pusat khelat melalui
penambahan suatu bahan terselubung didesak dari kompleks.
Dengan penambahan kalium iodida akan terjadi kompleks
tetraiodida merkurat(II) yang stabil.
Pada titrasi pertama dan kedua secara teoritis harus
digunakan jumlah larutan EDTA yang sama atau jumlahnya harus
ditentukan. perhitungan ditentukan dari larutan garam seng yang
digunakan pada titrasi kedua. Pada penentuan raksa (II) klorida
sebagai reduktor ditambahkan kalium iodida. Sedangkan untuk
penentuan raksa dalam salep presipitatum ditambahkan natrium
tiosulfat sebagai bahan penyelubung.
2.7 Kulit
2.7.1 Definisi Kulit
Kulit adalah organ terbesar pada tubuh manusia dan merupakan garis
2.7.2 Struktur Kulit ( Sloane, 2003)
Secara garis besar kulit tersusun atas 3 lapisan :
a. Lapisan epidermis
Lapisan epidermis adalah bagian terluar kulit. Tersusun dari
jaringan epitel bertingkat yang mengalami keratinasi Berdasarkan
ketebalan epidermis, dapat dibedakan kulit tebal dan kulit tipis. Turunan
epidermis meliputi rambut, kuku, kelenjar sebasea dan kelenjar keringat.
Lapisan epidermis terdiri dari stratum korneum, stratu lusidum, stratum
granulosum, stratum spinosum, stratum basal.
b. Lapisan dermis
Lapisan dermis dipisahkan dari lapisan epidermis dengan adanya
membran dasar atau lamina yang merupakan suatu lapisan jaringan ikat
yang berasal dari mesoderm, terletak di bawah lapisan epidermis dan
jauh lebih tebal dari epidermis. Lapisan ini terdiri dari lapisan elastik dan
fibrosa padat dengan elemen-elemen selular dan folikel rambut. Secara
garis besar, lapisan dermis dibagi menjadi dua bagian yaitu pars papilar
dan pars retikular. Pada lapisan ini tedapat sel-sel saraf dan pembuluh
darah.
c. Lapisan subkutis atau hipodermis
Lapisan ini terdiri atas jaringan ikat longgar yang mengikat kulit
secara longgar pada organ-organ di bawahnya, yang memungkinkan kulit
di bagian atas bergeser. Lapisan ini mengandung sel-sel lemak.
2.7.3 Jenis Kulit (Tresna, 2010)
Kulit digolongkan menjadi 4 jenis yang pokok yaitu : kulit normal,
berminyak, kering dan campuran.
a. Kulit normal
Kulit jenis ini merupakan kulit yang sehat dimana kelenjar lemak
memproduksi minyak tidak berlebihan, sehingga tidak menimbulkan
penyumbatan pada pori-pori kulit. Tanda-tanda kulit normal antara
kelihatan, tonus (daya kenyal) kulit bagus. Kulit normal biasanya
dijumpai pada anak-anak sampai menjelang remaja.
b. Kulit berminyak
Kulit berminyak disebabkan oleh sekresi kelenjar sebasea yang
berlebihan. Ciri ciri kulit berminyak adalah kulit kelihatan basah dan
mengkilat, pori-pori jelas terlihat,sering terdapat jerawat atau acne,
kulit terlihat pudar dan kusam. Kulit berminyakumumnya terdapat
pada usia remaja dan dewasa.
c. Kulit kering
Kulit kering sering terdapat pada orang dewasa dan orang-orang
yang telah lanjutusianya. Penyebabnya adalah akibat
ketidakseimbangan sekresi sebum. Ciri-ciri kulit kering antara lain:
bagian tengah muka normal, disekitar pipi dan dahi kering,tidak
lembab dan tidak berminyak, halus, tipis dan rapuh. Kulit kering cepat
menjadi tua karena kelenjar lemak tidak berfungsi dengan baik.
d. Campuran
Jenis kulit campuran, yakni bagian tengah muka (sekitar
hidung,dagu dan dahi) kadang-kadang berminyak atau normal.
Sedangkan bagian lain normal atau kering. Dapat terjadi pada semua
umur, tetapi lebih sering terdapat pada usia 35 tahun keatas.
2.7.4 Faktor Yang Mempengaruhi Jenis Kulit (Tresna, 2010)
Terdapat beberapa faktor yang dapat mempengaruhi perubahan
jenis kulit, antara lain sebagai berikut :.
1. Usia
Usia dapat mempengaruhi perubahan jenis kulit seseorang. Suatu
contoh, seseorang yang pada masa anak-anak mempunyai jenis kulit
normal setelah remaja kulitnya menjadi berminyak. Demikian pula
pada masa muda mempunyai jenis kulit berminyak setelah tua
kulitnya menjadi kering.
2. Makanan dan minuman
Perubahan jenis kulit, dapat disebabkan jenis makanan yang
minuman es dapat mengubah kulit dari normal menjadi berminyak.
Sebaliknya makan masam, minuman keras atau beralkohol dapat
mengubah kulit normal menjadi kering
3. Iklim
Iklim dapat menyebabkan perubahan jenis kulit. Pada iklim panas,
kulit bisa berubah menjadi berminyak, sedangkan pada iklim dingin
kulit bisa menjadi kering.
2.8 Tekhnik Sampling
2.8.1 Definisi Sampel dan Sampling
Sampel adalah bagian dari populasi yang menjadi sebagian dari
keseluruhan objek penelitian yang dianggap mewakili seluruh populasi.
Sedangkan sampling merupakan proses dalam menyeleksi porsi dari
populasi untuk mewakili populasi (Nasution R, 2003)
2.8.2 Tekhnik Pengambilan Sampel (Setiawan, 2005)
Teknik pengambilan sampel dibagi atas 2 kelompok besar, yaitu :
1. Random sampling atau sampel acak/probability sampling
Pada pengambikan sampel secara random, setiap unit populasinya
mempunyai kesempayan yang sama untuk diambil sebagai sampel.
keuntungan tekhnik ini adalah :
a. Derajat kepercayaan sampel dapat ditentukan
b. Beda penaksiran parameter populasi dengan statistik sampel dapat
diperkirakan
c. Besar sampel yang akan diambil dapat dihitung secara statistik
Lima cara pengambilan sampe secara random, yaitu sebagai
berikut :
1. Sampel random sederhana
Dilakukan dengan memberi kesempatan yang sama pada
setiap anggota populasi untuk menjadi anggota sampel. Cara ini
mempunyai keuntungan prosedur yang lebih mudah namun
membutuhkan daftar seluruh populasi dan biaya transportasi
2. Sampel random sistematik
Proses pengambilan sampel, setiap urutan dari titik awal
yang dipilih secara random. Pengambilan sampel dengan cara
ini membutuhkan perencanaan dan penggunaan yang mudah
karena sampel tersebar pada daerah populasi namun
membutuhkan daftar populasi yang lengkap
3. Sampel random berstrata
Populasi dibagi strata-strata (sub populasi), kemudian
pengambilan sampel dilakukan dalam setiap strata baik secara
simple random sampling maupun secara sistematik. Cara ini bisa
mendapatkan taksiran mengenai karakteristik populasi lebih
tepat namun harus membutuhkan daftar populasi setiap strata
4. Sampel random berkelompok
Dilakukan terhadap sampling unit, dimana sampling unit
terdiri dari satu kelompok (cluster) yang setiap individu dalam
kelompok yang dipilih akan diambil sebagai sampel. Cara
pengambilan sampel ini tidak memerlukan daftar populasi
namun prosedur pengambilan tergolong lebih sulit.
5. Sampel bertingkat
Proses pengambilan sampel dilakukan secara bertingkat,
bertingkat dua ataupun lebih. Cara ini hanya membutuhkan
sedikit biaya transportasi namun mempunyai prosedur kerja
yang sulit dan perencanaan yang lebih cermat
2. Non probability sampling (selected sample)
Cara ini dipergunakan apabila biaya sangat sedikit, hasil yang
diminta segera, dan tidak memerlukan ketepatan yang tinggi.
Ada 3 cara sampling ini :
1. Purposive sampling
Atas dasar pertimbangan peneliti yang menganggap unsur
unsur yang dikehendaki telah ada dalam anggota sampel yang
2. Accidental sampling
Atas dasar perandaian, tanpa direncanakan terlebih dahulu.
Jumlah sampel yang dikehendaki tidak berdasarkan pertimbangan
yang dapat dipertanggungjawabkan, asal memenuhi keperluan saja.
kesimpulan yang diperoleh bersifat kasar dan sementara.
3. Quota sampling
Berdasarkan pertimbangan peneliti, namun besar dan
kriteria sampel telah ditentukan terlebih dahulu. cara ini dilakukan
jika peneliti benar-benar mengenal daerah dan situasi dimana
penelitian akan dilakukan.
2.9 Validasi Metode (Harmita, 2004)
Validasi metoda analisis adalah suatu tindakan penilaian terhadap parameter tertentu, berdasarkan percobaan laboratorium, untuk
membuktikan bahwa parameter tersebut memenuhi persyaratan untuk
penggunaannya.
Beberapa parameter analisis yang harus dipertimbangkan dalam
validasi metode analisis diuraikan dan didefinisikan sebagaimana cara
penentuannya diantaranya adalah sebagai berikut :
1. Kecermatan (accuracy)
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan
hasil analis dengan kadar analit yang sebenarnya. Kecermatan
dinyatakan sebagai persen perolehan kembali (recovery) analit yang
ditambahkan.
Kecermatan hasil analis sangat tergantung kepada sebaran galat
sistematik di dalam keseluruhan tahapan analisis. Oleh karena itu untuk
mencapai kecermatan yang tinggi hanya dapat dilakukan dengan cara
mengurangi galat sistematik tersebut seperti menggunakan peralatan
yang telah dikalibrasi, menggunakan pereaksi dan pelarut yang baik,
pengontrolan suhu, dan pelaksanaannya yang cermat, taat asas sesuai
2. Keseksamaan (precision)
Keseksamaan adalah ukuran yang menunjukkan derajat kesesuaian
antara hasil uji individual, diukur melalui penyebaran hasil individual
dari rata-rata jika prosedur diterapkan secara berulang pada
sampel-sampel yang diambil dari campuran yang homogen.
3. Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuannya
yang hanya mengukur zat tertentu saja secara cermat dan seksama
dengan adanya komponen lain yang mungkin ada dalam matriks sampel.
Selektivitas seringkali dapat dinyatakan sebagai derajat penyimpangan
(degree of bias) metode yang dilakukan terhadap sampel yang
mengandung bahan yang ditambahkan berupa cemaran, hasil urai,
senyawa sejenis, senyawa asing lainnya, dan dibandingkan terhadap
hasil analisis sampel yang tidak mengandung bahan lain yang
ditambahkan.
4. Linearitas dan rentang
Linearitas adalah kemampuan metode analisis yang memberikan
respon yang secara langsung atau dengan bantuan transformasi
matematik yang baik, proporsional terhadap konsentrasi analit dalam
sampel. Rentang metode adalah pernyataan batas terendah dan tertinggi
analit yang sudah ditunjukkan dapat ditetapkan dengan kecermatan,
keseksamaan, dan linearitas yang dapat diterima.
5. Batas Deteksi dan Batas Kuantitasi
Batas deteksi adalah jumlah terkecil analit dalam sampel yang
dapat dideteksi yang masih memberikan respon signifikan dibandingkan
dengan blangko. Batas deteksi merupakan parameter uji batas. Batas
kuantitasi merupakan parameter pada analisis renik dan diartikan
sebagai kuantitas terkecil analit dalam sampel yang masih dapat
memenuhi kriteria cermat dan seksama.
6. Ketangguhan Metode (ruggedness)
Ketangguhan metode adalah derajat ketertiruan hasil uji yang
normal, seperti laboratorium, analisis, instrumen, bahan pereaksi, suhu,
hari yang berbeda, dan lain-lain. Ketangguhan biasanya dinyatakan
sebagai tidak adanya pengaruh perbedaan operasi atau lingkungan kerja
pada hasil uji. Ketangguhan metode merupakan ukuran ketertiruan pada
BAB 3
KERANGKA KONSEP
Kosmetik krim racikan dokter
Sampling investigatif (berdasarkan banyaknya pemakaian)
Persyaratan BPOM RI NO 445/MENKES/PER/1998 Metode HPLC dan
Mercury Analyzer
Preparasi sampel
kesimpulan Kualitas dan kuantitas hidrokuinon dan
BAB 4
METODE PENELITIAN
1.1 Tempat dan Waktu Penelitian
Penelitian dilakukan di Laboratorium kimia obat dan laboratorium penelitian II
di UIN Syarif Hidayatullah Jakarta yang berlangsung dari bulan Maret 2013
hingga bulan September 2013.
1.2 Tekhnik Pengambilan Sampel
Sampel krim kosmetik yang digunakan untuk penelitian diambil sebanyak 4
sampel secara acak. Sampel diambil dari beberapa wilayah di daerah Cirendeu,
Cileduk, Bintaro dan Depok berdasarkan kecenderungan pemakaian konsumen
yang tinggi terhadap produk tersebut.
1.3 Alat dan Bahan 1.3.1 Alat
Alat yang digunakan dalam penelitian ini adalah :
a. Analisis hidrokuinon
HPLC Dionex yang dilengkapi dengan detektor UV, volume injeksi 20 μL ,
kolom analitik ODS/C18 dengan dimensi 4,6 mm x 150 mm. waterbath
dengan temperatur 600 C, vortex, membran filter 0,2 µm, syring filter 0,2
µm, sentrifuge, spatula, pipet ukur, pipet tetes, spuit, mikro pipet 500 μL– 1
ml, batang pengaduk, timbangan analitik dan alat-alat gelas.
b. Analisis merkuri
Mercury analyzer NIC MA 3000, neraca analitik, pipet ukur, mikro pipet 20 – 200 µL , batang pengaduk, spatula, penangas listrik dan alat-alat gelas. 1.3.2 Bahan
a. Analisis hidrokuinon
Standar hidrokuinon, As.stearat, TEA, cera alba, vaselin album, PG,
b. Analisis merkuri
Standar baku merkuri, HNO3 pekat, aquades, 3 sampel krim racikan dokter.
1.4 Prosedur Penelitian 1.4.1 Analisis Hidrokuinon 1. Pembuatan fase gerak
Air : metanol (40 : 60), 60 ml metanol dicampurkan dengan 40 ml air
2. Penentuan panjang gelombang maksimum
Larutan standar hidrokuinon dengan konsentrasi 10 ppm, dibuat spektrum
serapan dari panjang gelombang 200 - 400 nm dengan spektrofotometri
UV-Vis. Tentukan panjang gelombang maksimumnya (ASEAN, 2005)
3. Pembuatan standar hidrokuinon
Sebanyak 50 mg standar hidrokuinon ditimbang dan dimasukkan kedalam
labu ukur 50 mL, ditambahkan dengan 25 mL fase gerak kemudian dikocok
dan dicukupkan volumenya hingga tanda batas. Dipipet 5 mL dari larutan
induk dimasukkan dalam 50 mL labu ukur dan ditambahkan fase gerak
hingga tanda batas. Dibuat standar dengan konsentrasi 20 ppm, 30 ppm, 40
ppm, 50 ppm dan 60 ppm. Diinjeksikan kedalam alat HPLC dengan panjang
gelombang 290 nm, laju alir 1 mL/menit dan volume injeksi 20 µL. Dibuat
kurva kalibrasinya dengan memplotkan peak area vs konsentrasi, dihitung
nilai LOD dan LOQ (ASEAN, 2005)
4. Pembuatan krim simulasi
R/ Hidrokuinon 12,5 mg
Asam stearat 229 mg
Cera alba 30 mg
Vaselin 122 mg
Propilen glikol 122 mg
TEA 23 mg
Aquades ad 1 g
Lelehkan asam stearat, cera alba dan vaselin diatas water bath
dan aquades dipanaskan sebagai fase air (M2). Campurkan M2 pada
M1, digerus hingga homogen hingga dapat membentuk massa krim
kemudian ditambakan hidrokuinon kedalam krim dan digerus hingga
homogen. (Anief, 2000)
5. Preparasi krim simulasi
Sebanyak 12,5 mg krim simulasi ditimbang kemudian dimasukkan dalam
beaker glass 25 mL. dibilas dengan fase gerak hingga tidak ada basis yang
tersisa. Larutan dimasukkan kedalam labu ukur 50 mL, divortex selama 1
menit, diletakkan diatas water bath dengan suhu 600 C selama 15 menit,
dinginkan dalam temperatur ruangan. Ditambah fase gerak hingga tanda
batas 50 mL dalam labu ukur, kemudian dikocok hingga homogen. Larutan
disentrifuge dan disaring dengan membran filter 0,2 µm kemudian
diinjeksikan kedalam alat HPLC dengan panjang gelombang 290 nm, laju
alir 1 mL/menit dan volume injeksi 20 µL. hasil yang diperoleh dianalisis
dan dihitung % perolehan kembalinya (ASEAN, 2005).
6. Preparasi sampel krim racikan dokter
Sebanyak 1 g sampel krim ditimbang kemudian dimasukkan dalam beaker
glass 25 mL, ditambahkan fase gerak hingga basis tidak ada yang tertinggal
dalam beker sambil dipanaskan. Larutan dimasukkan kedalam labu ukur 50
mL, divortex selama 1 menit, diletakkan diatas water bath dengan suhu 60 0
C selama 15 menit, dinginkan dalam temperatur ruangan. Ditambah fase
gerak hingga tanda batas 50 mL dalam labu ukur kemudian dihomogenkan.
Larutan disentrifuge selama 10 menit pada kecepatan 5000 rpm kemudian
disaring dengan membran filter 0,2 µm. Filtrat diinjeksikan kedalam alat
HPLC dengan panjang gelombang hingga 290 nm, laju alir 1 mL/menit dan
volume injeksi 20 µL. Hasil yang didapat dianalisis kadarnya. Perlakuan
1.4.2 Analisis Merkuri (Akaojicho et al, 2003) 1. Pembuatan larutan L-sistein
Timbang L-systein sebanyak 10 mg, kemudian larutkan dengan aquades 10
mL dan masukkan kedalam labu ukur 1 L, dicukupkan dengan aquades
hingga 500 mL. tambahkan asam nitrat pekat sebanyak 2 mL dan
dicukupkan dengan aquades hingga 1 L.
2. Pembuatan kurva kalibrasi
Pipet 5 mL larutan Hg(NO3) dengan konsentrasi 1000 ppm kedalam labu
ukur 50 mL, dicukupkan dengan larutan adisi L-sistein sehingga
konsentrasinya 100 ppm, encerkan larutan dari 100 ppm ke 1 ppm ke 100
ppb ke 50 ppb dan 5 ppb.
3. Pengukuran kadar merkuri pada sampel
Masing-masing sampel dimasukkan kedalam boat alat Mercury Analyzer
BAB 5
HASIL DAN PEMBAHASAN
5.1 Hasil percobaan 5.1.1 Hidrokuinon
5.1.1.1Penentuan panjang gelombang maksimum hidrokuinon
Hidrokuinon memberikan serapan maksimum pada panjang
gelombang 290 nm. Spektrum serapan larutan hidrokuinon 10 ppm
dapat dilihat pada lampiran 5.
5.1.1.2Pemilihan fase gerak dan kondisi optimum HPLC
Fase gerak yang digunakan pada penelitian ini berdasarkan
hasil orientasi yaitu metanol : air (60 : 40), dengan laju alir 1
mL/menit, volume injeksi 20 µL pada panjang geombang 290 nm,
menggunakan kolom C-18 dengan lampu detektor UV.
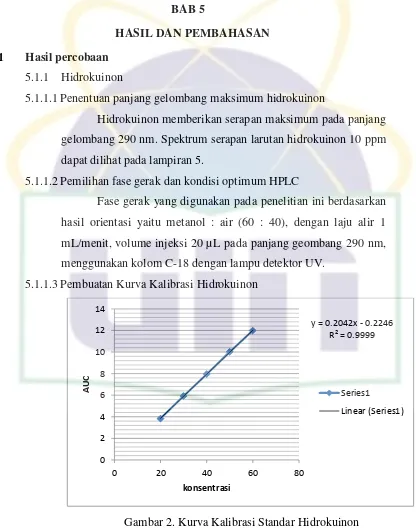
5.1.1.3Pembuatan Kurva Kalibrasi Hidrokuinon
Gambar 2. Kurva Kalibrasi Standar Hidrokuinon
Keterangan : a = -0,2246
b = 0,2042
r = 0,9999
5.1.1.4Uji Perolehan Kembali
5.1.1.5Penentuan Kadar Hidrokuinon Dalam Krim Racikan Dokter
Krim A mengandung hidrokuinon sebesar 3,51%, krim B
3,54%, krim C 3,74% dan krim D 3,47%. (Lampiran 4 dan 8)
5.1.2 Merkuri
5.1.2.1 Pembuatan Kurva Kalibrasi Merkuri
Dari konsentrasi 0 ppb, 5 ppb, 50 ppb dan 100 ppb didapat
absorbansinya sebesar 0,000010, 0,000563, 0,005525, 0,010747.
(Lampiran 12)
Gambar 3. Kurva Kalibrasi Standar Merkuri
Keterangan : a = 1,0798333
b = 1,00
r = 0,9999
5.1.2.2 Penentuan kadar merkuri pada krim racikan dokter
Dari 3 sampel yang diuji, semuanya mengandung merkuri.
Krim A mengandung merkuri sebesar 0,1833 %, sampel B
mengandung 0,1708 % dan sampel C mengandung 0,1324 %
5.2 Pembahasan 5.2.1 Hidrokuinon
Hidrokuinon merupakan senyawa kimia berupa Kristal putih
berbentuk jarum, tidak berbau, memiliki struktur kimia C6H6O2 dengan
nama kimia 1,4 benzendiol dan mengalami oksidasi terhadap cahaya dan
udara. Senyawa ini digunakan sebagai bahan pemutih dan pencegahan
pigmentasi yang bekerja menghambat enzim tirosinase yang berperan
dalam penggelapan kulit (Ibrahim et al., 2004).
Penelitian ini bertujuan untuk menganalisis kadar hidrokuinon
dalam kosmetik racikan dokter juga menilai apakah krim racikan dokter
mengandung kadar hidrokuinon yang melebihi batas. Analisa ini
menggunakan alat HPLC dengan sampel krim racikan dokter yang diambil
dengan cara sampling investigatif. Penggunaan alat HPLC untuk
penetapan kadar hidrokuinon dalam krim ini karena waktu analisis yang
relatif cepat, mempunyai ketelitian yang tinggi dan mudah.
Kondisi optimum alat yang digunakan untuk penelitian adalah
dengan menggunakan kolom ODS C18 (Oktadesil Silica), detector UV,
fase gerak air : metanol (40 : 60), dilakukan pada panjang gelombang 290
nm, dengan laju alir 1 mL/menit, dan volume injeksi 20 µL.
Penelitian dimulai dengan penentuan panjang gelombang
maksimum hidrokuinon menggunakan alat spektrofotometri UV-VIS
karena hidrokuinon selain mempunyai gugus fungsi OH juga mempunyai
gugus kromofor sehingga dapat ditentukan menggunakan alat
spektrofotometri UV-VIS (Harmita, 2006).
Berdasarkan hasil pengukuran panjang gelombang maksimum
hidrokuinon diperoleh 290,5 nm dengan konsentrasi 10 ppm. Namun pada
alat HPLC digunakan pada panjang gelombang 290 nm karena alat HPLC
tidak bisa menggunakan tanda koma.
Pembuatan kurva kalibrasi dibuat dengan lima konsentrasi yang
berbeda, yaitu 20 ppm, 30 ppm, 40 ppm, 50 ppm dan 60 ppm. Diperoleh
nilai r 0,9999 dengan menggunakan persamaan regresi linier y = -0,2246 +
besar dari 0,999 sehingga kurva kalibrasi hidrokuinon memberikan nilai
linieritas yang baik, dan penetapan kadar dengan kurva kalibrasi terjamin
kebenarannya (Mulja, 2003).
Batas deteksi untuk hidrokuinon adalah 0,396 µg/mL, sedangkan
batas kuantitasinya adalah 1,322 µg/mL. perhitungan dilakukan secara
statistik melalui garis regresi linier dari kurva kalibrasi. Batas deteksi
merupakan batas minimum suatu analit yang dapat dideteksi sedangkan
batas kuantisasi merupakan batas minimum analit yang dapat dihitung
kadarnya (Mulja, 2003).
Penentuan akurasi dapat ditentukan dengan uji perolehan kembali
menggunakan krim yang ditambahkan standar hidrokuinon yang telah
diketahui kadarnya. Lalu uji perolehan kembali diperoleh dengan
membandingkan kadar hasil analisis dengan kadar hidrokuinon yang
sebenarnya. Persen perolehan kembali yang diperoleh adalah 92,5 %.
Kriteria ini tidak masuk dalam rentang yang diperbolehkan, namun karena
pada penelitian ini menggunakan ekstraksi sehingga % perolehan
kembalinya lebih sulit didapatkan dengan sempurna. Hal ini dikarenakan
zat hidrokuinon terperangkap dalam basis yang tidak larut dalam pelarut.
Kriteria penerimaan untuk akurasi pada penetapan kadar komponen dalam
sediaan farmasi adalah 98 – 102 %. Sehingga hasil uji perolehan kembali
yang dilakukan telah memenuhi syarat (Harmita, 2006).
Hidrokuinon merupakan senyawa polar, untuk menarik senyawa
tersebut maka dapat diekstraksi dengan menggunakan senyawa polar.
Tahap preparasi sampel krim racikan dokter adalah dengan menimbang
masing-masing sampel sebanyak 1 g kemudian dimasukkan kedalam beker
glass 25 mL dan ditambah fase gerak metanol : air (60 : 40) kedalam beker
glass, diaduk merata dengan fase gerak hingga 25 mL dan kemudian
dipindahkan kedalam labu ukur 50 mL. sampel kemudian divortex selama
1 menit hingga homogen dan dipanaskan diatas water bath dengan suhu
600 C selama 15 menit. Sehingga basis krim terpisah dengan fase gerak.
Setelah dingin larutan dicukupkan dengan fase gerak hingga 50 mL dan
selama 10 menit. Diambil larutan diatas dan disaring menggunakan
membrane filter 0,45 µm kemudian filtratnya diinjeksikan kedalam alat
HPLC.
Filtrat sampel diinjeksikan sebayak 20 µL dengan waktu retensi
hingga 3 menit dan laju alir 1 mL/menit. Hasil analisa yang didapat dari
sampel dihitung kadarnya dengan menggunakan persamaan kurva
kalibrasi.
Hasil yang didapat dari pengukuran menggunakan HPLC didapat
nilai AUC untuk krim simulasi sebesar 46,9612. Sehingga didapat
konsentrasinya sebesar 231,189 ppm. Sedangkan konsentrasi krim
simulasi yang sebenarnya adalah 250 ppm. Sehingga didapat nilai UPK
sampel krim racikan dokter yang diuji semuanya masih dalam range yang
diperbolehkan selama penggunaanya dibawah pegawasan dokter (BPOM,
2007).
Hasil pengujian pada 4 sampel krim racikan dokter didapat
konsentrasi yang terlalu tinggi dari konsentrasi standar, hal ini terjadi
karena ketidaktahuan peneliti tentang kualitas dan kuantitas hidrokuinon
dalam sampel. Hasil % kadar yang didapat tersebut tidak bisa dipercayai
100 %. Sampel seharusnya diencerkan agar masuk dalam rentang kurva
kalibrasi sehingga angka bias dari hasil yang didapat relative lebih besar
dari yang sebenarnya, namun demikian tidak menutup kesimpulan jika
kadar hidrokuinon memang tinggi. Penelitian ini tidak bisa diulang karena
adanya kendala pada alat yang tidak bisa dioperasikan kembali.
Kecurangan distributor seringkali terjadi, sehingga tanpa ada izin
dari dokter konsumen dapat membeli krim secara bebas, padahal walaupun
krim yang digunakan adalah racikan dari dokter, jika penggunaannya
rasa terbakar pada kulit karena adanya kadar hidrokuinon yang tinggi
dalam krim (BPOM, 2007).
5.2.2 Merkuri
Merkuri digunakan sebagai bahan kosmetik untuk pemutih kulit.
Akan tetapi penggunaan merkuri pada sediaan krim pemutih dapat
menimbulkan berbagai hal mulai dari perubahan warna kulit yang
akhirnya dapat menyebabkan bintik-bintik hitam pada kulit, alergi,dan
iritasi kulit. Pada pemakaian dosis tinggi dapat menyebabkan kerusakan
permanen pada otak, ginjal, dan gangguan perkembangan janin (BPOM,
2007).
Untuk mengetahui adanya senyawa merkuri dalam sediaan krim
kosmetik racikan dokter dilakukan analisis penetapan kadar merkuri
dengan menggunakan alat mercury analyzer. Penggunaan alat ini karena
lebih spesifik, canggih dan cepat.
Penentuan linieritas diawali dengan pembuatan kurva kalibrasi.
Untuk pembuatan kalibrasi, mula-mula ditimbang L-sistein 10 mg
dimasukkan kedalam labu ukur 1000 mL. ditambahkan aquades hingga
500 ml dan asam nitrat pekat 2 mL. dikocok hingga L-sistein terlarut
kemudian dicukupkan dengan aquades hingga 1000 mL. pembuatan
larutan L-sistein ini digunakan sebagai larutan pengganti aquades pada
saat pembuatan larutan standar. Pada pembuatan kurva kalibrasi dibuat 3
konsentrasi. Yaitu 5 ppb, 50 ppb dan 100 ppb. Hasil plot antara
konsentrasi dan absorbansi pada pembuatan kurva kalibrasi didapat nilai r
sebesar 0,9999 dengan menggunakan persamaan regresi linier y =
1,0798333 + 1,00x. Nilai LOD didapat18 µg/L dan nilai LOQ didapat 60
µg/L.
Untuk menentukan kadar senyawa merkuri yang terdapat pada
krim racikan dokter, sampel langsung diambil dengan menggunakan tusuk
gigi dan digoreskan kedalam boat pada alat mercury analyzer. Hasil
pengukuran yang telah dilakukan, 3 sampel racikan dokter yang diperiksa
kadar merkuri 0,1833 %, sampel B mengandung 0,1708 % dan sampel C
mengandung 0,1324 %.
Menurut PP no.445/MenKes/Per/V/1998 tentang bahan, zat warna,
substrat, zat pengawet dan tabir surya pada kosmetik. Dalam kadar
sedikitpun merkuri dapat bersifat racun. Sehingga penggunaan merkuri
BAB 6
KESIMPULAN DAN SARAN
6.1 Kesimpulan
1. Hasil penetapan kadar hidrokuinon pada 4 sampel krim racikan dokter
menunjukkan adanya hidrokuinon dengan kadar 3,499 % pada krim A,
3,561 % pada krim B, 3,754 % pada krim C dan 3,541 % pada krim D
2. Dari 4 sampel krim racikan dokter yang telah dianalisis semuanya
mengandung hidrokuinon yang masih diperbolehkan penggunaanya
dalam krim (maksimal 5%)
3. Hasil penetapan kadar merkuri pada 3 sampel krim racikan dokter
menunjukkan adanya merkuri dengan kadar 0,1833 % pada krim A,
0,1708 % pada krim B dan 0,1324 % pada krim C
4. Dari data analisis yang telah dilakukan, 3 sampel krim racikan dokter
yang diuji semuanya tidak aman karena mengandung merkuri.
6.2 Saran
Perlu dilakukan penelitian lebih lanjut dengan jumlah sampel yang
representatif untuk penetapan kadar hidrokuinon dan merkuri dalam