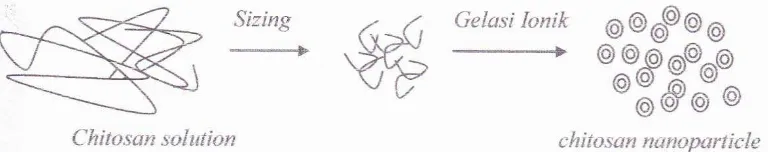PEMBUATAN EMULSI KITOSAN CANGKANG BELANGKAS
MELALUI METODE GELASI IONIK TERHADAP
KITOSAN NANO DENGAN MENGGUNAKAN
FREEZE-DRYER
TESIS
Oleh
DWI YULIANI 117006019/KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PEMBUATAN EMULSI KITOSAN CANGKANG BELANGKAS
MELALUI METODE GELASI IONIK TERHADAP
KITOSAN NANO DENGAN MENGGUNAKAN
FREEZE-DRYER
ABSTRAK
Pembuatan nano kitosan cangkang belangkas melalui proses gelasi ionik dapat dilakukan dengan mereaksikan kitosan, tripolifosfat (TPP) dan Tween 80, dengan menggunakan magnetik stirrer dan ultrasonik untuk mengecilkan ukuran. Emulsi yang dihasilkan dikeringkan menggunakan freeze-dryer dengan variasi waktu tertentu, kemudian dikarakterisasi menggunakan FTIR dan SEM. Hasil yang didapat menunjukkan kesesuaian antara spektrum IR nano kitosan yang diperoleh dengan spektrum IR kitosan standar. Variasi waktu freeze-drying tidak menunjukkan perubahan yang signifikan terhadap derajat deasetilasi, namun berpengaruh terhadap jumlah dan ukuran nano kitosan yang terbentuk. Waktu freeze-drying yang terlalu singkat (1-4 jam) mengakibatkan nano kitosan yang dihasilkan teraglomerasi kembali, sementara freeze-drying yang dilakukan selama 8-10 jam cenderung menghasilkan partikel berukuran lebih kecil dengan jumlah yang lebih banyak.
PREPARATION OF HORSESHOE CRAB SHELL CHITOSAN
EMULSION THROUGH THE IONIC GELATION METHOD
USING CHITOSAN NANO FREEZE-DRYER
ABSTRACT
Nano chitosan was produced by ionic gelation methode of chitosan, tripolyphospate (TPP), and Tween 80 with ultrasonic and magnetic stirrer as particle sizing process. The emulsion that form was dryed by various time of freeze-drying process and than the product of nano chitosan were characterize by FTIR and SEM. The conclusion showed the similarity of IR spectra between nano chitosan and chitosan standard. Although freeze-drying didn’t affect deacetilation degree of the product, its affected size and number of nano chitosan. Fast freeze-drying (1-4 hr) consequence aglomeration of nano chitosan, meanwhile freeze-drying for 8-10 hr tend to form number of smaller particles.
DAFTAR ISI
Halaman
ABSTRAK i
ABSTRACT ii
KATA PENGANTAR iii
RIWAYAT HIDUP iv
DAFTAR ISI v
DAFTAR TABEL vii
DAFTAR GAMBAR viii
DAFTAR LAMPIRAN ix
BAB 1. PENDAHULUAN
1.1. Latar Belakang 1
1.2. Perumusan masalah 3
1.3. Pembatasan Masalah 3
1.4. Tujuan Penelitian 3
1.5. Manfaat Penelitian 3
1.6. Metodologi Penelitian 4
1.7. Lokasi Penelitian 4
BAB 2. TINJAUAN PUSTAKA
2.1. Kitin dan Kitosan 5
2.1.1. Sifat Kitosan dan Parameter yang Mempengaruhinya 8
2.2. Nano Kitosan 9
2.3. Gelasi Ionik 10
2.4. Tripolifosfat (TPP) 11
2.6. Sonikasi 12
2.7. Freeze-Drying 15
2.7.1. Proses Freeze-Drying 15
2.8. Fourier Transform Infra Red (FTIR) 16
2.9. Scanning Electron Microscopy (SEM) 18
BAB 3. METODA PENELITIAN
3.1. Bahan dan Alat 20
3.1.1. Peralatan 20
3.1.2. Bahan-Bahan 20
3.2. Prosedur Penelitian ... 20 3.2.1. Pembuatan Nano Kitosan Cangkang Belangkas 20 3.2.2. Karakterisasi Nano Kitosan Cangkang Belangkas 21
3.3. Bagan Penelitian 22
BAB 4. HASIL DAN PEMBAHASAN
4.1. Analisa Spektrum Infra Merah 23
4.1.1. Analisa Kualitatif 23
4.1.2. Analisa Kuantitatif 26
4.2. Analisa Scanning Electron Microscopy (SEM) 27
BAB 5. KESIMPULAN DAN SARAN
5.1. Kesimpulan 32
5.2. Saran 32
Daftar pustaka 33
DAFTAR TABEL
Nomor Judul Halaman
2.1. Karakterisasi Kitin Belangkas 5
2.2. Serapan FTIR Karakteristik untuk Kitin dan Kitosan 7
2.3. Karakterisasi Kitosan Belangkas 7
2.4 Spesifikasi Kitosan Niaga 8
DAFTAR GAMBAR
Nomor Judul Halaman
2.1. Struktur Selulosa, Kitin, dan Kitosan 6
2.2. Larutan Kitosan dengan Gelasi Ionik menjadi Kitosan Nano 11 4.1. Spektrum Infra Merah Kitosan Nanopartikel
dengan Perlakuan 1 Jam Freeze-Drying 23
DAFTAR LAMPIRAN
Nomor Judul Halaman
Lampiran 1. Spektrum Infra Merah Kitosan Nanopartikel dengan
Perlakuan 0 Jam Freeze-Drying 37
Lampiran 2. Spektrum Infra Merah Kitosan Nanopartikel dengan
Perlakuan 2 Jam Freeze-Drying 38
Lampiran 3. Spektrum Infra Merah Kitosan Nanopartikel dengan
Perlakuan 4 Jam Freeze-Drying 39
Lampiran 4. Spektrum Infra Merah Kitosan Nanopartikel dengan
Perlakuan 6 Jam Freeze-Drying 40
Lampiran 5. Spektrum Infra Merah Kitosan Nanopartikel dengan
Perlakuan 8 Jam Freeze-Drying 41
Lampiran 6. Spektrum Infra Merah Kitosan Nanopartikel dengan
PEMBUATAN EMULSI KITOSAN CANGKANG BELANGKAS
MELALUI METODE GELASI IONIK TERHADAP
KITOSAN NANO DENGAN MENGGUNAKAN
FREEZE-DRYER
ABSTRAK
Pembuatan nano kitosan cangkang belangkas melalui proses gelasi ionik dapat dilakukan dengan mereaksikan kitosan, tripolifosfat (TPP) dan Tween 80, dengan menggunakan magnetik stirrer dan ultrasonik untuk mengecilkan ukuran. Emulsi yang dihasilkan dikeringkan menggunakan freeze-dryer dengan variasi waktu tertentu, kemudian dikarakterisasi menggunakan FTIR dan SEM. Hasil yang didapat menunjukkan kesesuaian antara spektrum IR nano kitosan yang diperoleh dengan spektrum IR kitosan standar. Variasi waktu freeze-drying tidak menunjukkan perubahan yang signifikan terhadap derajat deasetilasi, namun berpengaruh terhadap jumlah dan ukuran nano kitosan yang terbentuk. Waktu freeze-drying yang terlalu singkat (1-4 jam) mengakibatkan nano kitosan yang dihasilkan teraglomerasi kembali, sementara freeze-drying yang dilakukan selama 8-10 jam cenderung menghasilkan partikel berukuran lebih kecil dengan jumlah yang lebih banyak.
PREPARATION OF HORSESHOE CRAB SHELL CHITOSAN
EMULSION THROUGH THE IONIC GELATION METHOD
USING CHITOSAN NANO FREEZE-DRYER
ABSTRACT
Nano chitosan was produced by ionic gelation methode of chitosan, tripolyphospate (TPP), and Tween 80 with ultrasonic and magnetic stirrer as particle sizing process. The emulsion that form was dryed by various time of freeze-drying process and than the product of nano chitosan were characterize by FTIR and SEM. The conclusion showed the similarity of IR spectra between nano chitosan and chitosan standard. Although freeze-drying didn’t affect deacetilation degree of the product, its affected size and number of nano chitosan. Fast freeze-drying (1-4 hr) consequence aglomeration of nano chitosan, meanwhile freeze-drying for 8-10 hr tend to form number of smaller particles.
BAB 1
PENDAHULUAN
1.1Latar Belakang
Belangkas merupakan komoditas andalan dan bernilai ekonomis sebagai salah satu hasil perikanan utama (selain udang dan kepiting) di kota Medan, Sumatera Utara. Komoditas ini dapat dengan mudah diperoleh di Tempat Pelelangan Ikan (TPI) kawasan Bagan Deli, Belawan. Secara umum, belangkas dimanfaatkan telurnya sebagai bahan pangan, sedangkan cangkangnya biasanya terbuang begitu saja. Cangkang belangkas ini dapat memberikan nilai ekonomis bila dimanfaatkan sebagai bahan untuk menghasilkan kitosan.
Belangkas termasuk golongan hewan arthropoda yaitu crustacea yang pada cangkangnya mengandung senyawa kitin yang dapat dideasetilasi menjadi kitosan. Kitosan adalah senyawa organik turunan kitin, berasal dari biomaterial kitin yang dewasa ini banyak dimanfaatkan untuk berbagai keperluan, antara lain membersihkan dan menjernihkan air, immobilisasi enzim sel bakteri, dan pengawet bahan makanan. Kitin sebagai bahan baku kitosan ditemukan pertama kali oleh Braconnat, berkebangsaan Perancis pada tahun 1811 yang diisolasinya dari jamur.
butir kitosan menjadi lebih kecil untuk pemanfaatan yang lebih luas. Oleh karena itu, perkembangan modifikasi fisik mengarah ke bentuk nanopartikel (Wahyono, 2010).
Namun, ada hambatan yang membatasi penggunaan nanopartikel ini, yaitu ketidakstabilan fisika (aggregation/particle fusion) dan/atau ketidakstabilan kimia, hal ini harus selalu diperhatikan ketika suspensi larutan nanopartikel disimpan dalam jangka waktu yang lama. Dalam hal ini, untuk memperbaiki kestabilan fisika dan kimia dari nanopartikel, maka harus menghilangkan kandungan airnya. Freeze-drying adalah proses yang paling sering digunakan untuk mengubah larutan atau suspensi dari nanopartikel menjadi padatan sehingga menjadi stabil saat pendistribusian dan penyimpanan untuk keperluan farmasi (Abdelwahed et al., 2006).
Peneliti sebelumnya, Rachmania (2011) telah berhasil membuat nano kitosan dari cangkang udang melalui metode gelasi ionik dengan berbagai perlakuan pengecilan ukuran (sizing). Hasil yang didapat berupa nano kitosan dengan ukuran partikel sebesar 400-450 nm dengan perlakuan pengecilan ukuran (sizing) menggunakan magnetic stirrer. Sedangkan Noviary (2012) telah berhasil mensintesis kitosan dari cangkang belangkas (Tachypleus Gigas) dan memodifikasi mikropartikelnya melalui ikat silang dengan genepin. Sementara Zuhairiah (2013) telah menyelidiki pengaruh variasi waktu penyimpanan kitosan dengan berbagai berat molekul dalam larutan asam terhadap viskositasnya, hasil yang didapat yaitu viskositas kitosan akan menurun seiring dengan lamanya waktu penyimpanan dalam larutan asam. Selain itu ia juga membuat kitosan nanopartikel dan mengkarakterisasinya menggunakan FTIR dan SEM.
1.2Perumusan Masalah
Bagaimanakah proses pembuatan nano kitosan cangkang belangkas dengan metode gelasi ionik yang kemudian dikeringkan menggunakan freeze-dryer dengan variasi waktu tertentu.
1.3Pembatasan Masalah
Penelitian ini dibatasi pada pembuatan nano kitosan cangkang belangkas dengan metode gelasi ionik dengan Tripolifosfat (TPP) sebagai zat pengikat silang dan Tween 80 sebagai surfaktannya. Nano kitosan ini kemudian distabilkan menggunakan freeze-dryer dengan variasi waktu 1; 2; 4; 6; 8; dan 10 jam. Karakterisasinya
menggunakan Spektroskopi FTIR dan SEM.
1.4 Tujuan Penelitian
Tujuan dari penelitian ini adalah untuk membuat nano kitosan cangkang belangkas dengan metode gelasi ionik dengan variasi waktu pengeringan menggunakan freeze-dryer, dan melihat pengaruh variasi waktu freeze-drying terhadap nano kitosan yang
terbentuk.
1.5 Manfaat Penelitian
Diharapkan penelitian ini dapat memberikan informasi tentang pembuatan nano kitosan dari cangkang belangkas, pengeringannya melalui proses freeze-drying, pengaruh variasi waktu freeze-drying, dan karakterisasi nano kitosan tersebut.
1.6Metodologi Penelitian
dengan metode gelasi ionik dan perlakuan pengecilan ukuran (sizing) dengan magnetic stirrer dan ultrasonic bath. Kemudian ditambahkan surfaktan Tween 80
secara tetes demi tetes sambil distirer, dan didiamkan memutar selama 30 menit. Setelah itu, ditambahkan TPP yang bertujuan agar ukuran partikel yang dihasilkan tetap stabil. Kemudian distirer selama 30 menit. Nano kitosan yang diperoleh dikeringkan menggunakan freeze-dryer dan dikarakterisasi dengan FTIR dan SEM.
1.7 Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Penelitian Fakultas Matematika dan Ilmu Pengetahuan Alam (FMIPA) Universitas Sumatera Utara. Analisa FTIR dilakukan di Laboratorium Kimia Organik Universitas Gajah Mada, Yogyakarta. Dan analisa SEM dilakukan di Laboratorium Geologi Kuarter-PPPGL, Bandung.
BAB 2
TINJAUAN PUSTAKA
2.1 Kitin dan Kitosan
Kitin adalah polimer yang paling melimpah di laut. Sedangkan pada kelimpahan di muka bumi, kitin menempati posisi kedua setelah selulosa. Hal ini karena kitin dapat ditemukan di berbagai organisme eukariotik termasuk serangga, moluska, krustasea, fungi, alga, dan protista. Kata kitin berasal dari bahasa Yunani, “khiton” yang berarti “baju dari besi” karena sesuai dengan fungsinya sebagai jaket pelindung untuk hewan-hewan golongan invertebrata (Suhardi, 1993).
Kitin merupakan komponen yang membentuk struktur eksoskeleton udang, kepiting, belangkas dan sebagainya dengan kisaran relatif 30-60%. Kitin berperan sebagai suatu unsur penguat jaringan bersama-sama dengan protein (Peter, 1993 dalam Noviary, 2012). Proses deproteinasi menggunakan larutan NaOH 5% akan
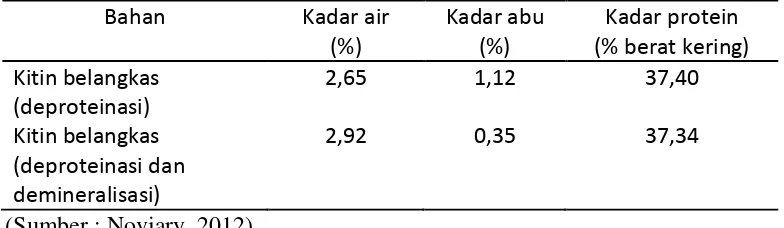
mengurangi protein dari cangkang belangkas. Kadar air, kadar abu dan kadar protein kitin dapat dilihat seperti pada Tabel 2.1.
Tabel 2.1 Karakterisasi kitin belangkas
Bahan Kadar air
(Sumber : Noviary, 2012)
dikembangkan karena aplikasinya yang luas adalah kitosan (Bhuvana, 2006). Kitosan adalah jenis polimer alami yang dihasilkan dari proses deasetilasi kitin (Sugita, 2009).
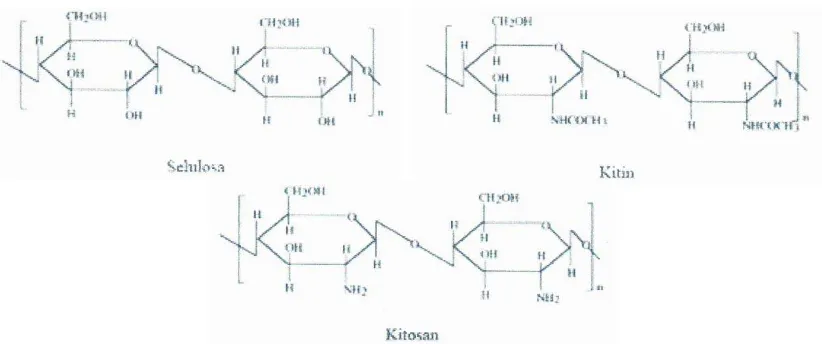
Kitosan (bahasa Inggris: Chitosan), pertama kali ditemukan oleh Rouget pada 1859, merupakan biopolimer polisakarida penting dan sangat melimpah. Kitosan dihasilkan melalui deasetilasi molekul basa N (nitrogen) parsial pada kitin, yang secara komersil diekstrak dari kulit udang dan kerang. Secara kimia, kitin dan kitosan dapat dianggap sebagai turunan selulosa dengan gugus hidroksi pada atom C-2 selulosa digantikan oleh gugus asetamida dan amina bebas. Jika gugus hidroksi pada atom C-2 selulosa digantikan oleh gugus asetamida, maka senyawa yang terbentuk adalah kitin. Tetapi jika gugus hidroksi pada atom C-2 selulosa digantikan oleh gugus amina bebas maka senyawa yang terbentuk adalah kitosan (Mia, 2007).
Gambar 2.1 Struktur Selulosa, Kitin, dan Kitosan
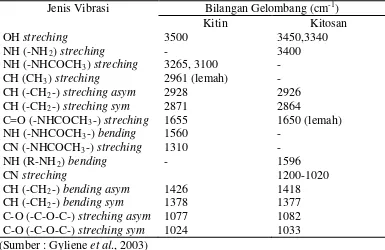
Proses deasetilasi kitin menggunakan larutan NaOH pekat bertujuan untuk mengubah gugus asetil dari kitin menjadi gugus amina pada kitosan. Perubahan ini dapat dideteksi dengan melihat perubahan spektrum IR kitin dengan hasil deasetilasinya pada panjang gelombang tertentu yang karakteristik. Gugus fungsi yang karakteristik dari spektra FTIR kitin dan kitosan dapat dilihat pada Tabel 2.2.
Jenis Vibrasi Bilangan Gelombang (cm-1)
C-O (-C-O-C-) streching asym -) bending sym C-O (-C-O-C-) streching sym
3500 (Sumber : Gyliene et al., 2003)
Karakterisasi kitosan dari cangkang belangkas seperti kadar air, kadar abu, dan kadar protein dapat dilihat pada Tabel 2.3.
Tabel 2.3 Karakterisasi kitosan belangkas
Bahan Kadar air
(Sumber : Noviary, 2012)
Kitosan (1,4)-2-amino-2-deoksi-β-D-glukosamin (Gambar 2.1) merupakan biopolimer kationik linier terdiri dari D-glukosamin dan N-asetil-D-glukosamin yang dihubungkan oleh ikatan β-(1→4) glikosidik, mempunyai nilai pKa kira-kira 6,3 pada nilai pH lebih rendah, molekulnya bersifat kation karena protonasi dari grup amino. Laporan selanjutnya, terindikasikan bahwa ketika kitosan dilarutkan dalam garam, air suling, atau media laboratorium, menunjukkan aktivitas antimikrobial melawan strain-strain berfilamen dari fungi, yeast, dan bakteri (Rhoades & Roller, 2000).
Kitosan mempunyai sifat yang khas yakni bioaktifis, biodegradasi dan tidak beracun. Selain itu juga tidak berbau, berwarna putih dan terdiri dari dua jenis polimer yaitu poli(2-deoksi,2-asetilamin,2-glukosa) dan poli(2-deoksi,2-amino glukosa) yang berikatan secara beta (1,4). Kitosan larut dalam pelarut organik, HCl encer, HNO3 encer, dan H3PO4 0,5%, tetapi tidak larut dalam basa kuat dan H2SO4
Tabel 2.4 Spesifikasi kitosan niaga
(Sugita, 2009). Menurut Knorr (1984) pelarut kitosan yang baik dan umum digunakan adalah asam asetat dengan konsentrasi 1-2%. Sifat kelarutan kitosan ini dipengaruhi oleh bobot molekul dan derajat deasetilasi. Bobot molekul kitosan beragam, bergantung pada degradasi yang terjadi selama proses deasetilasi (Sugita, 2009).
97% dalam 1% asam asetat ≤ 2,0
≤ 10,0
Tak berwarna ≥ 70,0
(Sumber : Kencana, 2009)
alkohol organik dan piridin. Kitosan larut dalam asam organik/mineral encer melalui protonasi gugus amino bebas (NH2→NH3+
Parameter lain yang berpengaruh pada sifat kitosan adalah berat molekul (BM) dan derajat deasetilasi (DD). Derajat deasetilasi menyatakan banyaknya gugus amino bebas dalam polisakarida. Kitosan merupakan kitin dengan derajat deasetilasi lebih dari 70%. Deasetilasi adalah proses pengubahan gugus asetil (-NHCOCH
) pada pH kurang dari 6,5. Pelarut yang baik untuk kitosan dalah asam format, asam asetat dan asam glutamat. Kelarutan kitosan menurun dengan bertambahnya berat molekul kitosan.
3) dan
rantai molekular kitin menjadi gugus amina lengkap (-NH2) pada kitosan dengan penambahan NaOH konsentrasi tinggi. Kemampuan kitosan bergantung pada derajat kimia reaktif yang tinggi gugus aminonya (Kusumaningsih dkk., 2004 dalam Ariesta, 2008). Penentuan derajat deasetilasi dapat dilakukan dengan beberapa metode, seperti titrimetri HBr, spektroskopi IR, FDUV-spektrofotometri, difraksi sinar-X dan spektroskopi 1
Dalam penelitian ini, kitosan yang dihasilkan dari cangkang belangkas kemudian diubah ke dalam bentuk nano.
H NMR (Khan et al., 2002).
2.2 Nano Kitosan
Nano kitosan yaitu kitosan yang memiliki partikel yang berbentuk padat dengan ukuran sekitar 10-1000 nm. Kitosan dalam bentuk nanopartikel ini pun bersifat netral, tidak toksik, dan memiliki stabilitas yang konstan (Mohanraj & Chen, 2006).
metode yang prosesnya lebih efisien dan sederhana untuk memudahkan dalam pembuatan nano kitosan.
Umumnya pembentukan ikatan silang ionik antara polikationik kitosan dengan senyawa polianion akan lebih disukai. Tripolifosfat (TPP) yang merupakan senyawa polianion merupakan zat pengikat silang yang baik. Kekuatan mekanik gel kitosan meningkat dengan menggunakan TPP karena TPP memiliki rapatan muatan negatif yang tinggi sehingga interaksi dengan polikationik kitosan akan lebih besar (Shu & Zhu, 2002).
2.3 Gelasi Ionik
Gelasi atau pembentukan gel merupakan gejala penggabungan atau pengikatan silang rantai-rantai polimer membentuk jaringan tiga dimensi yang sinambung dan dapat memerangkap air di dalamnya menjadi suatu struktur yang kompak dan kaku yang tahan terhadap aliran bertekanan (Fardiaz, 1989 dalam Latifah, 2010). Gel yang dapat menahan air dalam strukturnya disebut hidrogel (Wang et al., 2004 dalam Napthaleni, 2010). Hidrogel dapat diklasifikasikan menjadi hidrogel kimia dan hidrogel fisika. Contoh hidrogel kimia adalah hidrogel kitosan yang berikatan silang secara kovalen (Keuteur, 1996).
Larutan kitosan pada batas konsentrasi tertentu dalam asam asetat 1% dapat membentuk gel. Gel kitosan terjadi karena terbentuknya jaringan tiga dimensi antara molekul kitosan yang terentang pada seluruh volume gel yang terbentuk dengan menangkap sejumlah air di dalamnya. Sifat jaringan serta interaksi molekul yang mengikat keseluruhan gel menentukan kekuatan, stabilitas, dan tekstur gel. Untuk memperkuat jaringan di dalam gel biasanya digunakan molekul lain yang berperan sebagai pembentuk ikatan silang (Keuteur, 1996). Gel kitosan yang terbentuk dapat diperbaiki sifatnya (menurunnya waktu gelasi dan meningkatnya kekuatan mekanik gel) dengan penambahan PVA (Wang et al., 2004 dalam Wahyono, 2010).
homogenizer, ataupun magnetic stirrer. Banyak penelitian difokuskan untuk
membuat nanopartikel dari polimer yang biodegradable: kitosan, gelatin, dan sodium alginat. Salah satu contoh metode gelasi ionik ini adalah mencampurkan polimer kitosan dengan polianion sodium tripolifosfat (Na-TPP) yang menghasilkan interaksi antara muatan positif pada gugus amino kitosan dengan muatan tripolifosfat. Tripolifosfat dianggap sebagai zat pengikat silang yang paling baik (Mohanraj & Chen, 2006). Proses terbentuknya kitosan nanopartikel dengan gelasi ionik dapat dilihat pada Gambar 2.2.
Gambar 2.2 Larutan Kitosan dengan Gelasi Ionik menjadi Kitosan Nano
2.4 Tripolifosfat (TPP)
Pembentukan ikatan silang ionik salah satunya dapat dilakukan dengan menggunakan senyawa tripolifosfat. Tripolifosfat dianggap sebagai zat pengikat silang yang paling baik. Shu dan Zhu (2002) melaporkan bahwa penggunaan tripolifosfat untuk pembentukan gel kitosan dapat meningkatkan mekanik dari gel yang terbentuk. Hal ini karena tripolifosfat memiliki rapatan muatan negatif yang tinggi sehingga interaksi dengan polikationik kitosan akan lebih besar. Menurut Yongmei & Yumin (2003), pembentukan nanopartikel hanya terjadi pada konsentrasi tertentu kitosan dan TPP. Peran TPP sebagai zat pengikat silang akan memperkuat matriks nanopartikel kitosan. Dengan semakin banyaknya ikatan silang yang terbentuk antara kitosan dan TPP maka kekuatan mekanik matriks kitosan akan meningkat sehingga partikel kitosan menjadi semakin kuat dan keras, serta semakin sulit untuk terpecah menjadi bagian-bagian yang lebih kecil (Wahyono, 2010).
Penelitian nanopartikel kitosan termodifikasi menggunakan emulsifier yang merupakan senyawa pengikat silang dan surfaktan. Berdasarkan penelitian Silva et al. (2005) diketahui bahwa penambahan surfaktan dapat memperkecil ukuran partikel kitosan. Zat pengikat silang yang sering digunakan adalah glutaraldehida, sedangkan surfaktan yang banyak dipakai adalah surfaktan nonionik (Tween 80 dan Span 80). Beberapa contoh surfaktan nonionik adalah Tween 80 (polietilena sorbitan monooleat) dan Span 80 (sorbitan monooleat). Tween 80 dan Span 80 bersifat nontoksik yang umumnya digunakan sebagai emulsifier dan penstabil pada bidang pangan dan farmasi. Tarirai (2005) dalam Wahyono (2010) telah melakukan penelitian tentang pembuatan gel kitosan sebagai pembawa obat ibuprofen dengan menggunakan senyawa pengikat silang tripolifosfat dan senyawa surfaktan yang sekaligus berfungsi sebagai pengikat silang, yaitu asam oleat, sodium laurit sulfat (SLS) dan Tween 80.
2.6 Sonikasi
pembersihan, pembentukan plastik, dan yang terbaru adalah sonokimia (Mason et al., 2002 dalam Komariah 2010).
Iradiasi ultrasonik sangat berkaitan erat dengan kavitasi, yaitu pembentukan, pertumbuhan, dan pengempisan gelembung di dalam cairan. Ultrasonik intensitas tinggi dapat memberikan efek pada perubahan fisika dan kimia yang cukup luas karena memiliki energi yang cukup tinggi yang dapat diberikan pada zat lain dalam waktu yang cukup singkat dengan tekanan yang tinggi. Tekanan inilah yang akan menimbulkan kavitasi. Efek fisika dari ultrasonik intensitas tinggi salah satunya adalah emulsifikasi (Wahid, dkk, 2001 dalam Wahyono, 2010).
Suara ultrasonik yang menjalar di dalam medium cair memiliki kemampuan terus menerus membangkitkan semacam gelembung atau rongga (cavity) di dalam medium tersebut yang kemudian secepat kilat meletus. Fenomena ini lebih dikenal dengan nama kavitasi. Gelembung-gelembung yang meletus tadi bisa menghasilkan energi kinetik luar biasa besar yang berubah menjadi energi panas. Penciptaan dan luruhnya gelembung yang cepat memberikan efek transfer energi panas yang juga cepat. Gelembung-gelembung tadi bisa mencapai suhu 5000 K, bertekanan 1000 atm, dan memiliki kecepatan pemanasan-pendinginan 1010 K/s. Selama terjadinya gelembung-gelembung, kondisi fisika kimia suatu reaksi bisa berubah drastis namun suhu medium yang teramati tetaplah dingin karena proses terbentuk dan pecahnya gelembung tadi terjadi dalam skala mikroskopik.
berhasil mengubah air menjadi hidrogen peroksida. Banyak penjelasan berbeda yang diajukan untuk menjelaskan fenomena ini, tetapi semuanya berdasarkan pada keberadaan partikel tertentu atau gelembung-gelembung gas yang menurunkan gaya antarmolekul sehingga memungkinkan terbentuknya gelembung. Tahap kedua adalah pertumbuhan gelembung yang terjadi melalui difusi uap zat terlarut (solut) pada gelembung, dan tahap ketiga adalah pecahnya gelembung yang terjadi ketika ukuran gelembung mencapai nilai maksimumnya. Berdasarkan mekanisme hot-spot, ledakan gelembung tersebut menaikkan temperatur lokal hingga 5000 K dan tekanan 1000 atm. Kondisi ekstrim tersebut menyebabkan pemutusan ikatan kimia (Wahyono, 2010).
Efek kimia dari gelombang ultrasonik, tidak secara langsung berintraksi dengan molekul-molekul untuk menginduksi suatu perubahan kimiawi. Ini karena panjang gelombang ultrasonik yang terlalu panjang jika dibandingkan dengan panjang gelombang molekul-molekul. Interaksi gelombang ultrasonik dengan molekul-molekul terjadi melalui media perantara berupa cairan. Gelombang yang dihasilkan oleh tenaga listrik (lewat tranduser) diteruskan oleh media cair ke medan yang dituju melalui fenomena kavitasi akustik (Wardiyati dkk, 2004 dalam Wulandari 2010).
Pada umumnya, nanopartikel menunjukkan kestabilan yang rendah dalam jangka panjang, karena perbedaan faktor fisika dan kimia yang mungkin membuat sistem menjadi tidak stabil. Dalam peneliltian ini, gel nano kitosan yang dihasilkan akan dihilangkan kandungan airnya melalui proses freeze-drying dengan variasi waktu tertentu.
2.7 Freeze-Drying
2.7.1 Proses Freeze-Drying
Freeze-drying adalah proses yang telah digunakan secara luas untuk mengeringkan
vaksin, protein, peptida atau colloidal carriers: liposom, nanopartikel, nanoemulsi. Proses Freeze-drying dapat dibagi menjadi 3 tahapan : freezing (pengerasan), primary drying (sublimasi es) dan secondary drying (desorpsi air yang tidak dapat membeku).
A.Tahap Freezing
Freezing adalah tahapan pertama dalam freeze-drying. Dalam tahap ini, suspensi
larutan didinginkan, dan kristal es dari air murni terbentuk. Karena proses freezing terus berlanjut, maka ada semakin banyak air dalam cairan yang membeku. Hal ini menyebabkan meningkatnya konsentrsi dari cairan yang tertinggal. Ketika suspensi cairan menjadi lebih terkonsentrasi, peningkatan viskositasnya menghalangi kristalisasi lebih lanjut. Cairan yang mengeras dengan konsentrasi dan viskositas yang tinggi ini berfasa amorf, kristal atau gabungan amorf-kristal. Sebagian kecil air yang tertinggal dalam cairan dan tidak membeku disebut bound water.
B. Tahap Primary Drying
Tahap primary drying melibatkan sublimasi es dari produk yang membeku. Dalam tahap ini, 1) panas berpindah dari shelf ke larutan yang membeku melalui tray dan vial, dan terjadilah sublimasi, 2) es yang tersublimasi dan uap air yang terbentuk
keluar melewati bagian yang kering dari produk menuju permukaan sampel, 3) uap air berpindah dari permukaan produk ke kondensor melalui chamber, dan 4) uap air terkondensasi di dalam kondensor. Di akhir tahap sublimasi terbentuklah bagian yang berpori-pori. Tiap-tiap pori cocok dengan ruangan yang diisi dengan kristal es.
C. Tahap Secondary Drying
Tahap secondary drying melibatkan penghilangan air yang diserap dari produk. Ini adalah air yang tidak dapat dipisahkan sebagai es pada tahap freezing, dan juga tidak dapat tersublimasi.
rangkaian plates atau coil yang temperaturnya dapat dipertahankan pada titik yang sangat rendah (di bawah -50o
Setelah nano kitosan distabilkan dengan pengeringan menggunakan freeze dryer, selanjutnya nano kitosan dikarakterisasi menggunakan spektrofotometer FTIR
dan SEM.
C). Satu atau lebih pompa vakum dalam rangkaian yang dihubungkan ke condenser chamber untuk dapat mencapai tekanan antara 4-40 Pa di dalam keseluruhan sistem selama pengoperasian.
2.8 Fourier Transform Infra Red (FTIR)
Fourier Transform Infra Red (FTIR) merupakan suatu metode spektroskopi infra red.
Spektroskopi infra red (IR) dapat mengidentifikasi kandungan gugus kompleks dalam senyawa tetapi tidak dapat menentukan molekular unsur penyusunnya. Pada spektroskopi IR, radiasi IR dilewatkan pada sampel. Sebagian dari radiasi IR diserap oleh sampel dan sebagian lainnya diteruskan. Jika frekuensi dari suatu vibrasi spesifik sama dari frekuensi radiasi IR yang langsung menuju molekul, molekul akan menyerap radiasi tersebut. Spektrum yang dihasilkan menggambarkan absorpsi dan transmisi molekular, membentuk sidik jari molekular suatu sampel. Karena bersifat sidik jari, tidak ada dua struktur molekuler unik yang menghasilkan spektrum IR yang sama (Kencana, 2009).
Sistem optik spektrofotometer FTIR dilengkapi dengan cermin yang bergerak tegak lurus dan cermin diam. Dengan demikian radiasi IR akan menimbulkan perbedaan jarak yang ditempuh menuju cermin yang bergerak dan jarak cermin yang diam. Perbedaan jarak tempuh radiasi tersebut selanjutnya disebut sebagai retardasi (δ). Hubungan antara intensitas radiasi IR yang diterima detektor terhadap retardasi disebut sebagai interferogram. Sedangkan sistem optik dari Spektrofotometer IR yang didasarkan atas bekerjanya interferometer disebut sebagai sistem optik Fourier Transform Infra Red.
Mengetahui informasi struktur suatu senyawa organik dengan membandingkan daerah sidik jarinya.
Cahaya tampak terdiri dari beberapa range frekuensi elektromagnetik yang berbeda dimana setiap frekuensi bisa dilihat sebagai warna yang berbeda. Radiasi IR juga mengandung beberapa range frekuensi tetapi tidak dapat dilihat oleh mata. Pengukuran pada spektrum IR dilakukan pada daerah cahaya IR tengah (mid-infrared) yaitu pada panjang gelombang 2,5-50 µm atau bilangan gelombang
4000-200 cm-1
Jika suatu frekuensi tertentu dari radiasi IR dilewatkan pada sampel suatu senyawa organik maka akan terjadi penyerapan frekuensi oleh senyawa tersebut. Detektor yang ditempatkan pada sisi lain dari senyawa akan mendeteksi frekuensi yang dilewatkan pada sampel yang tidak diserap oleh senyawanya. Banyaknya frekuensi yang melewati senyawa (yang tidak diserap) akan diukur sebagai persen transmitan.
. Energi yang dihasilkan oleh radiasi ini akan menyebabkan vibrasi atau getaran pada molekul. Pita absorbsi IR sangat khas dan spesifik untuk setiap tipe ikatan kimia atau gugus fungsi. Metode ini sangat berguna untuk mengidentifikasi senyawa organik dan organometalik.
Persen transmitan 100 berarti tidak ada frekuensi IR yang diserap oleh senyawa. Pada kenyataannya, hal ini tidak pernah terjadi. Selalu ada sedikit dari frekuensi ini yang diserap dan memberikan suatu transmitan sebanyak 95%. Transmitan 5% berarti bahwa hampir seluruh frekuensi yang dilewatkan diserap oleh senyawa. Serapan yang sangat tinggi ini akan memberikan informasi penting tentang ikatan dalam senyawa ini.
Ewing, GW (1985) menyatakan bahwa penyerapan radiasi IR ditentukan dari peningkatan energi vibrasi atau rotasi yang dihubungkan dengan ikatan kovalen, asalkan berupa peningkatan hasil dalam mengubah momen dipol dari molekul. Ini berarti hampir seluruh molekul yang mengandung ikatan kovalen akan menunjukkan beberapa tingkat penyerapan tertentu dalam IR.
Mikroskop merupakan alat untuk melihat benda yang berukuran kecil (mm). Salah satu jenis mikroskop adalah Scanning Electron Microscopy (SEM). SEM menggunakan elektron dan cahaya tampak sebagai sumber cahayanya. Elektron menghasilkan gelombang yang lebih pendek dibandingkan cahaya foton dengan ukuran 0,1 nm dan menghasilkan gambar dengan resolusi yang lebih baik (Lee 1993 dalam Rini 2010).
Scanning Electron Microscopy (SEM) menghasilkan gambar dari suatu
permukaan spesimen dengan kedalaman fokus 500 kali lebih besar dibandingkan mikroskop cahaya. Gambar yang dihasilkan memiliki fokus yang baik pada kedalaman spesimen, sehingga gambar yang dihasilkan berupa bentuk tiga dimensi spesimen. Hal ini disebabkan oleh ketajaman pancaran elektron yang menyinari spesimen. Mikroskop SEM memiliki perbesaran hingga 50.000 kali (Fujita et al dalam Rini 2010).
Mikroskop SEM memiliki lensa yang berbeda dengan mikroskop cahaya. Bagian electron gun berfungsi memancarkan elektron. Condensing lenses berfungsi untuk memantulkan elektron. Lensa yang berdekatan dengan sampel adalah lensa objek. Pancaran elektron yang mengenai permukaan sampel diteruskan oleh detektor, sehingga penampakan permukaan sampel dapat terlihat pada monitor (Chandler 1980 dalam Rini 2010).
BAB 3
METODA PENELITIAN
3.1 Bahan dan Alat 3.1.1 Peralatan
- Peralatan gelas Pyrex
- Timbangan elektrik Chyo Electronic Balance
- Hot plate stirer Ikamag Rec-G
- Ultrasonic bath - Jar test
- Plat kaca - Freeze dryer - FTIR
- SEM
3.1.2 Bahan-Bahan
- Kitosan dari cangkang belangkas
- CH3
- Sodium tripolifosfat
COOH glasial p.a (E.Merck)
- Tween 80 - Akuades
3.2 Prosedur Penelitian
3.2.1 Pembuatan Nano Kitosan Cangkang Belangkas
baru diaduk menggunakan magnetik stirrer pada suhu kamar dan terakhir dilakukan proses freeze-drying. Nano kitosan ini dibuat dengan mencampurkan larutan kitosan, TPP, dan tween 80 dengan volume dan konsentrasi tertentu. Awalnya, kitosan yang berasal dari cangkang belangkas dilarutkan dalam larutan asam asetat 1%, Tween 80 dan TPP masing-masing dilarutkan dalam akuades. Kemudian, dilakukan pemecahan molekul larutan kitosan melalui ultrasonikasi. Setelah itu ditambahkan tween 80 dan TPP setetes demi setetes sambil diaduk menggunakan magnetik stirrer. Selanjutnya, campuran yang diperoleh distabilkan dengan freeze-dryer.
3.2.2 Karakterisasi Nano Kitosan Cangkang Belangkas
3.3 Bagan Penelitian
Larutan kitosan 0,3%
diambil 25 mL
ditreatmen dalam ultrasonik bath selama 60 menit ditambahkan 12,5 mL Tween 80 setetes demi setetes distirer selama 30 menit
Larutan nanokitosan
ditambahkan 1 mL larutan tripolifosfat 1% distirer selama 30 menit
dimasukkan dalam freeze dryer dengan variasi waktu 1; 2; 4; 6; 8; dan 10 jam
BAB 4
HASIL DAN PEMBAHASAN
4.1 Analisa Spektrum Infra Merah 4.1.1 Analisa Kualitatif
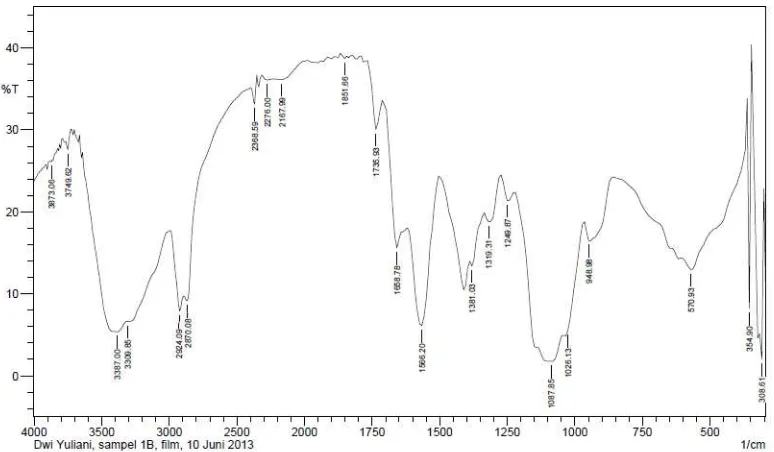
Nano kitosan yang telah diketahui spektrumnya dianalisis secara kualitatif, ditunjukkan pada Gambar 4.1.
Gambar 4.1. Spektrum infra merah kitosan nanopartikel dengan perlakuan 1 jam freeze drying.
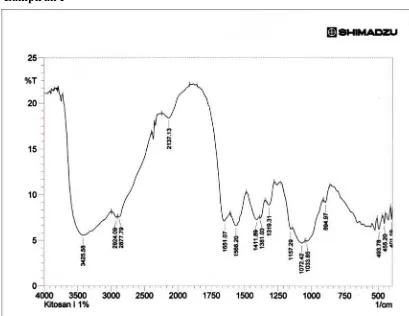
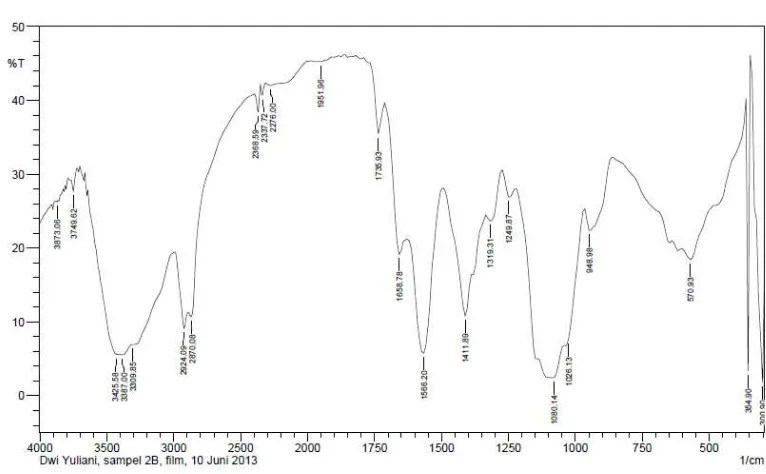
Spektra infra merah dari nano kitosan dengan perlakuan tanpa freeze drying (K0), freeze drying selama 2 jam (K2), freeze drying selama 4 jam (K4), freeze drying selama 6 jam (K6), freeze drying selama 8 jam (K8), dan freeze drying selama 10 jam (K10) dapat dilihat pada Lampiran 1-6.
Perbedaan yang dapat diamati yaitu pergeseran bilangan gelombang dan perubahan nilai transmitant yang menunjukkan kuantitas dari gugus tersebut didalam nano kitosan.
Pada masing-masing nano kitosan yang dikarakterisasi terdapat juga gugus-gugus lain seperti ulur O-H, ulur N-H, ulur C-H, ulur C-O, dan ulur C-N. Ulur O-H pada masing-masing nano kitosan terlihat membentuk spektra yang melebar kebawah sehingga ulur N-H yang juga berada pada daerah ini tidak dapat diamati. Adanya ulur N-H dapat diperjelas dengan adanya tekukan N-H pada masing-masing polimer.
Ulur C-O pada nano kitosan tersebut berasal dari gugus metanol yang melekat pada rantai polimer, sedangkan ulur C-H berasal dari rantai utama kiotosan. Adanya ulur C-H akan diperkuat dengan tekukan C-H dari metil maupun metilen pada masing-masing polimer. Ulur C-N pada polimer-polimer tersebut berasal dari gugus amida dan amina.
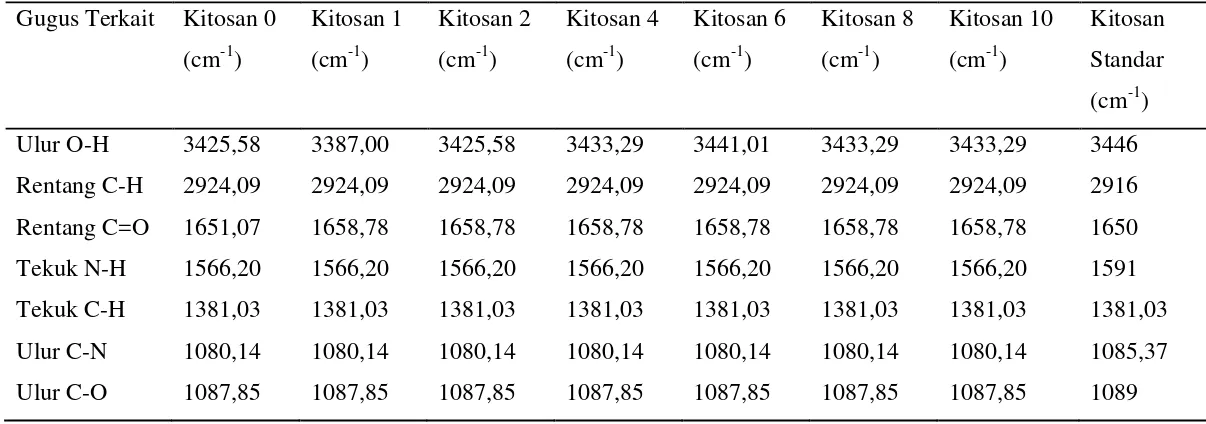
Besarnya bilangan gelombang pada gugus-gugus nano kitosan dapat dibandingkan dengan spektra FT-IR dari kitosan standar untuk melihat kualitas dari nano kitosan kitosan yang dihasilkan.
Tabel 4.1 Perbandingan spektra FT-IR nano kitosan dengan kitosan standarnya Gugus Terkait Kitosan 0
4.1.2 Analisa Kuantitatif
Analisa kuantitatif kitosan nanopartikel yang diperoleh ditentukan dengan menggunakan rumus derajat deasetilasi (% DD) sebagai berikut :
% �� = 1− ��1655 �3450 �
1
1,33� � 100%
Dengan menggunakan rumus di atas, maka diperoleh %DD untuk nano kitosan K0, K1, K2, K4, K6, K8, dan K10.
4.2 Analisa Scanning Electron Microscopy (SEM)
Kitosan nanopartikel yang dihasilkan dikarakterisasi dengan menggunakan instrumen Scanning Electron Microscopy (SEM) untuk melihat morfologinya, sehingga dapat
diketahui homogenitas ukuran partikel yang dihasilkan. Prinsip kerja mikroskop SEM adalah sifat gelombang dari elektron berupa difraksi pada sudut yang sangat kecil. Elektron dapat dihamburkan oleh sampel yang bermuatan karena memiliki sifat listrik (Samsiah 2009 dalam Wulandari 2010). Hasil karakteristik SEM nano kitosan yang dibuat berdasarkan metode gelasi ionik dengan perlakuan pengecilan ukuran menggunakan magnetik stirrer dan ultrasonik bath menunjukkan partikel yang berupa bulatan menyerupai bola dan permukaan yang tidak rata. Ukuran partikel dapat ditentukan dengan mengukur diameter bola tersebut. Perbesaran yang digunakan yaitu 2.000 kali dan 10.000 kali.
(c) (d)
(e) (f)
Gambar 4.2 Foto SEM Nano Kitosan dengan Perbesaran 10.000 Kali; (a) perlakuan freeze-drying selama 1 jam, (b) perlakuan freeze-drying selama 2 jam,
(c) perlakuan freeze-drying selama 4 jam, (d) perlakuan freeze-drying selama 6 jam, (e) perlakuan freeze-drying selama 8 jam, (f) perlakuan freeze-drying selama 10 jam.
hingga permukaan menjadi tidak rata. Pada waktu 2 jam (b), kerutan ataupun gumpalan pada permukaan semakin berkurang. Hingga pada varian waktu 4 jam (c), hampir tidak terlihat kerutan ataupun gumpalan sama sekali, dan permukaan menjadi sangat rata. Sementara, untuk varian waktu 6 jam (d), mulai tampak beberapa gumpalan atau bulatan yang bentuknya sudah teratur. Dan pada waktu 8 jam (e), bulatan yang diduga sebagai nano dan mikro partikel semakin terlihat jelas. Bila waktu freeze-drying diperpanjang hingga 10 jam (f), maka bulatan yang ada tampak semakin banyak. Hal ini diperkirakan karena setelah proses freeze-drying selama 1-4 jam, emulsi yang dihasilkan masih banyak mengandung air (belum kering). Sehingga Tween 80 yang digunakan sebagai surfaktan terdifusi ke dalam air dan mengakibatkan aglomerasi. Sementara, setelah proses freeze-drying selama 6-10 jam, emulsi yang diperoleh berangsur-angsur mulai mengering, sehingga kandungan air semakin sedikit dan menghasilkan partikel dengan rentang ukuran nano sampai mikro.
Gumpalan ataupun bulatan yang teramati memiliki ukuran besar atau diameter yang beragam, mengindikasikan ukuran partikel yang didapat berbeda-beda berkisar antara mikro hingga nano. Nanopartikel adalah butiran atau partikel padat dengan kisaran ukuran 10-1000 nm (Mohanraj dan Chen, 2006). Partikel yang dihasilkan dari penelitian ini, berdasarkan pengukuran diameter dari foto SEM menunjukkan rentang ukuran antara 100-1200 nm. Berdasarkan defenisi nanopartikel yang dikemukakan Mohanraj dan Chen, maka partikel yang dihasilkan dari penelitian ini dapat digolongkan sebagai nano partikel kitosan dengan ukuran yang tidak homogen dan masih terdapat mikropartikel di dalamnya.
gumpalan berukuran lebih besar yang tampak diindikasikan sebagai mikropartikel, hal ini disebabkan karena partikel yang menempel satu sama lain. Pada alat ultrasonik, semakin tinggi persen amplitudo serta lama waktu kontak, maka semakin kecil ukuran partikel dan seragam. Namun partikel kecil yang telah terpecah melalui perlakuan ultrasonik ini mudah tergabung kembali, dan terbentuklah bulatan-bulatan yang lebih besar. Selain itu, sifat Tween 80 sebagai surfaktan juga mudah larut dalam air, sehingga kemungkinan terjadi proses difusi Tween 80 dalam air menyebabkan penggabungan partikel dan proses penggumpalan kembali terjadi (Latifah 2008).
Perlakuan pengecilan ukuran menggunakan magnetik stirrer menyebabkan penyebaran energi cenderung merata, sehingga seluruh molekul terkena energi yang sama dan molekul larutan emulsi akan terpecah dengan ukuran yang sama serta distribusi ukuran partikelnya cenderung lebih homogen. Hal ini lah yang menyebabkan nanopartikel di dalamnya juga akan dapat terpisah satu sama lain sehingga didapatkan nanosfer dengan ukuran terkecil. Selain itu, penggunaan TPP dalam proses gelasi juga besar pengaruhnya, yaitu dapat menstabilkan missel (emulsi homogen dan sangat kecil) sehingga missel tersebut menjadi lebih stabil. Hasil yang diperoleh dari penggunaan magnetik stirrer lebih stabil dalam waktu 24 jam, sementara pada ultrasonik bisa berubah kestabilannya mencapai 25 kali lebih meningkat (BPPT 2010).
Penggunaan TPP mengingat sifatnya yang nontoksik. Menurut Mi, dkk (1999) dalam Wahyono (2010), penambahan TPP bertujuan untuk membentuk silang ionik
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
- Nano kitosan cangkang belangkas dapat dibuat berdasarkan metode gelasi ionik yang dimodifikasi dengan perlakuan ultrasonik dan freeze-drying, menghasilkan partikel berukuran 100-1200 nm yang masih merupakan gabungan dari nano dan mikropartikel.
- Analisa FTIR menunjukkan kesesuaian antara spektrum nano kitosan yang diperoleh dengan spektrum kitosan standar. Selain itu, variasi waktu freeze-drying juga tidak menunjukkan pengaruh yang berarti terhadap derajat
deasetilasi nano kitosan tersebut.
- Proses freeze-drying berpengaruh terhadap jumlah dan ukuran nano kitosan yang dihasilkan. Waktu freeze-drying yang terlalu singkat (1-4 jam) mengakibatkan nano kitosan teraglomerasi. Namun saat freeze-drying dilakukan selama 8-10 jam, nano kitosan yang dihasilkan cenderung lebih banyak dan ukurannya juga lebih kecil karena jumlah partikel yang teraglomerasi relatif berkurang.
5.2 Saran
- Peneliti selanjutnya disarankan untuk melakukan sentrifugasi terhadap emulsi yang terbentuk dengan tujuan memisahkan nano dan mikropartikel kitosan. - Disarankan menganalisa menggunakan Particle Size Analyzer (PSA) dengan
DAFTAR PUSTAKA
Abdelwahed, W., Degobert, G., Stainmesse, S., Fessi, H. 2006. Freeze-drying of Nanoparticles: Formulation, Process and Storage Considerations. Advanced Drug Delivery Reviews 58: 1688-1713.
Ariesta, A. 2008. Karakteristik Mutu dan Kelarutan Kitosan dari Ampas Silase Kepala Udang Windu (Penaeus monodon) [skripsi]. Bogor: Fakultas Perikanandan Ilmu Kelautan. Institut Pertanian Bogor.
Bhuvana. 2006. Studies on Fractional Behaviour of Chitosan-Coated Fabrics. Aux. Res. J. Vol 6(4): 123-130.
Dachriyanus. 2004. Analisis Struktur Senyawa Organik Secara Spektroskopi. Cetakan Pertama. Andalas University Press.
Ewing, G. W. 1985. Instrumental Methods of Chemical Analysis. McGraw-Hill Book Company. Page: 78-90.
Gyliene, O. Razmute, I. Tarozaite, R. Nivinskiene, O. 2003. Chemical Composition and Sorption Properties of Chitosan Produced from Fly Larva Shells. Chemija (Vilnius). T.14 Nr.3: 121-127.
Kencana, A. 2009. Perlakuan Sonikasi terhadap Kitosan: Viskositas dan Bobot Molekul Kitosan [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam. Institut Pertanian Bogor.
Keuteur, J. 1996. Nanoparticles and Microparticles for Drug and Vaccine Delivery. Eur J of Pharmaceutics and Biopharmaceutics. 189: 19-34.
Khan, T.A., Peh, K. K., Chang, H. S. 2002. Reporting Degree of Deacetylation Values of Chitosan: The Influence of Analytical Methods. J Pharmaceut Sci. 5: 205-212.
Knorr, D. 1984. Functional Properties of Chitin and Chitosans. J. Food. Sci. Vol 47 : 36-38.
Komariah, S. 2010. Kombinasi Emulsi dan Ultrasonikasi dalam Nanoenkapsulasi Ibuprofen Tersalut Polipaduan Poli (As.Laktat) dan Poli (ε-Kaprolakton) [skripsi]. Fakultas Matematika dan Ilmu Pengetahuan Alam. Institut Pertanian Bogor.
Latifah, S. 2010. Stabilitas Mikrokapsul Ketoprofen dengan Penyalut Kitosan Alginat [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam. Institut Pertanian Bogor.
Mia, L. 2007. Sintesis dan Karakterisasi Membran Berbasis Kitosan dalam Aplikasi Fuel Cell [tesis]. Program Studi Kimia. ITB. Bogor.
Mohanraj, U. J., Chen, Y. 2006. Nanoparticles – A Review. Tropical Journal of Pharmaceutical Research. 5 (1): 561-573.
Noviary, H. 2012. Penyediaan dan Karakterisasi Kitosan Belangkas (Tachypleus Gigas) dengan Modifikasi Ikat Silang Genepin [tesis]. Fakultas Matematika dan Ilmu Pengetahuan Alam. Universitas Sumatera Utara.
Rachmania, D. 2011. Karakteristik Nano Kitosan Cangkang Udang Vannamei (Litopenaeus vannamei) dengan Metode Gelasi Ionik [skripsi]. Fakultas Perikanan dan Ilmu Kelautan. Institut Pertanian Bogor.
Rhoades, Roller. 2000. Antimicrobial Actions of Degraded and Native Chitosan Against Spoilage Organisms in Laboratory Media and Foods. Appl. Environ. Microbiol. 66 (1): 80-86.
Rini, I. 2010. Recovery dan Karakterisasi Kalsium dari Limbah Demineralisasi Kulit Udang Jerbung (Penaeus merguiensis deMan). [Skripsi]. Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Shu, X. Z., Zhu, K. J. 2002. Controlled Drug Release Properties of Ionically Cross-Linked Chitosan Beads: The Influence of Anion Structure. International Journal of Pharmaceutics. 233: 217-225.
Silva, S.S. 2005. Physical Properties and Biocompatibility of Chitosan / Sury Blendet Membran. Journal of Material Science 16. 575-579.
Sugita, P., Tuti, W., dkk. 2009. Sumber Biomaterial Masa Depan. Kitosan. IPB Press. Bogor. Halaman 28-45.
Suhardi. 1993. Khitin dan Khitosan. PAU Pangan dan Gizi. Universitas Gadjah Mada Press. Yogyakarta.
Tripler, Paul A. 2001. Fisika untuk Sains dan Teknik. Jilid 2. Edisi ketiga. Soegiyono B. Penerjemah. Terjemahan dari physic for Scientist and Engineers Volume 2 Third Edition. Jakarta: Erlangga.
Wahyono, D. 2010. Ciri Nanopartikel Kitosan dan Pengaruhnya pada Ukuran Partikel dan Efisiensi Penyaluran Ketoprofen [tesis]. Bogor: Program Pascasarjana. Institut Pertanian Bogor.
Wulandari, T. 2010. Sintesis Nanopartikel Ekstrak Temulawak (Curcuma xanthorrhiza Roxb.) Berbasis Polimer Kitosan, TPP dengan Metode Gelasi Emulsi [skripsi]. Fakultas Matematika dan Ilmu Pengetahuan Alam. Institut Pertanian Bogor.
Yongmei, X. Yumin, D. 2003. Effect of Moleculer Structure of Chitosan on Protein Delivery Properties of Chitosan Nanoparticles. International Journal of Pharmaceutics. 250: 215-226.
Lampiran 1
Lampiran 2
Lampiran 3
Lampiran 4
Lampiran 5
Lampiran 6