TDENTIFIKASI ZAT WARNA SINTETIS PADA SAOS CABAI
SECARA KROMATOGRAFI KERTAS (KKT)
TUGAS AKHIR
OLEH:
SELLY RIAWENNI
NIM 122410037
PROGRAM STUDI DIPLOMA III
ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KATA PENGANTAR
Puji syukur penulissampaikan ke hadirat AllahSWT,yang Maha Pengasih
lagi Penyayang atassegala rahmat dan karunia-Nya sehingga penulis dapat
menyelesaikantugas akhir iniyang berjudul “Identifikasi Zat Warna Sintetis Pada Saos Cabai Secara Kromatografi Kertas (KKT)”. Tugas akhir ini disusun sebagai salah satusyarat untuk menyelesaikan pendidikan Program
Studi Diploma III Analis Farmasi dan Makanan Fakultas Farmasi Universitas
Sumatera Utara.
Dalam menyelesaikan tugas akhir ini, penulis banyak mendapat bantuan
dan bimbingan dari berbagai pihak, untuk itu penulis mengucapkan terimakasih
yang sebesar–besarnya kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas
Farmasi USU.
2. Ibu Prof. Dr. Julia Reveny, M.Si., Apt., selaku Wakil Dekan I Fakultas
Farmasi Universitas Sumatera Utara.
3. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt., selaku Ketua Program
Studi Diploma III Analis Farmasi dan Makanan Fakultas Farmasi
Universitas Sumatera Utara.
4. Ibu Dra. Nazliniwaty, M.Si.,Apt.,selaku Dosen Pembimbing, yang telah
banyakmemberikan bimbingan dan pengarahan dalam menyelesaikantugas
akhir ini.
5. Ibu Dra. Ernawati, Apt., selaku Koordinator Praktek Kerja Lapangan di
6. BapakdanIbu dosen beserta seluruh staf Program Studi Diploma III Analis
Farmasi dan Makanan Fakultas Farmasi Universitas Sumatera Utara.
Secara khusus, penulis mengucapkan terima kasih yang tiada terhingga
kepadaAyahanda Drs. Mutiaraja Nasution dan Ibunda Hj. Fajidah Rahmawaty,
SH.,MH tercinta serta Adik Rieska, Adik Andre, dan Adik Nazly yang telah
memberikan do’a, semangat dan motivasi sehingga penulisan tugas akhir ini
dapat terselesaikan.
Terima kasih kepada teman dan sahabat penulisWilda, Linda, Rachma,
Indik, Selvy, Fanny, Dina, Soraya yang selalu memberi dukungan kepada
penulis. Seluruh teman-teman mahasiswa Analis Farmasi dan Makanan angkatan
2012 yang tidak dapat penulis sebutkan satu per satu.
Penulis menyadari sepenuhnya bahwa dalam penyusunan tugas akhir
ini masih terdapat banyak kekurangan dan kelemahan yang dimiliki penulis baik
itu sistematika penulisan maupun penggunaan bahasa. Untuk itu penulis
mengharapkan kritik dan saran dari berbagai pihak yang bersifat membangun
demi penyempurnaan tugas akhir ini.Penulis berharap semoga tugas akhir ini
dapat memberikan manfaat kepada semua pihak yang memerlukan.
Medan, Mei2015 Penulis,
Selly Riawenni NIM 122410037
ABSTRAK
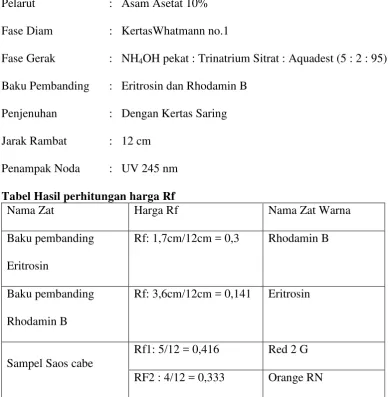
Pewarna sintetis pada umumnya terbuat dari bahan-bahan kimia. Bahan pewarna sintetis yang boleh digunakan untuk makanan pun harus dibatasi jumlahnya. Karena pada dasarnya, setiap bahan kimia yang masuk kedalam tubuh akan menimbulkan efek negatif pada tubuh . Hal ini sebanding dengan dengan zat warna sintetis yang ada di dalam saos cabai. Zat warna sintetis di dalam saos cabai mengandung zat warna sintetis yang berbahaya dalam penggunaanya. Identifikasi zat warna sintetis pada saos ini bertujuan untuk mengetahui apakah saos cabai yang akan diedarkan dipasaran mengandung zat warna sintetis atau tidak. Zat pewarna sintetis dalam makanan dapat membuat suatu makanan lebih menarik, meratakan warna makanan dan mengembalikan warna dari bahan dasar yang hilang atau berubah selama pengolahan. Identifikasi zat warna sintetis pada saos cabai dilakukan di Laboratorium Kesehatan Daerah Pemerintahan Provinsi Sumatera Utara di Medan. Identifikasinya menggunakan Kromatografi Kertas. Hasil yang diperoleh dari harga Rf baku pembanding Eritrosin adalah 0,141 dan harga Rf baku pembanding Rhodamin B adalah 0,3 sedangkan harga Rf1 pada sampel adalah 0,416 dan harga Rf2 pada sampel adalah 0,333, dari hasil ini dapat disimpulkan bahwa saos cabai positif mengandung zat warna sintetis sehingga sampel yang diuji dinyatakan tidak memenuhi persyaratan sesuai dengan Peraturan Menkes RI Nomor 239/Menkes/Per/V/85.
DAFTAR ISI
2.5 Fungsi Warna Pada Produk Pangan ... 13
2.6 Kromatografi Kertas ... 14
2.6.1 Teknik Kromatografi Kertas ... 15
BAB III METODOLOGI ... 19
3.1 Tempat Pengujian... 19
3.2 Alat ... 19
3.3 Bahan ... 19
3.4 Prosedur Pengujian ... 19
3.4.1 Larutan Uji ... 19
3.4.2 Larutan Baku ... 20
3.4.3 Identifikasi ... 20
3.5 Persyaratan ... 20
BAB IV HASIL DAN PEMBAHASAN ... 21
4.1 Hasil ... 21
4.2 Pembahasan ... 21
BAB V KESIMPULAN DAN SARAN ... 23
5.1 Kesimpulan ... 23
5.2 Saran ... 23
DAFTAR PUSTAKA ... 24
DAFTAR TABEL
Halaman
Tabel 2.1 Sifat-sifat Bahan Pewarna Alami ... 6
Tabel 2.2 Bahan Pewarna Sintetis Yang Diizinkan Di Indonesia ... 9
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Data Hasil Identifikasi Zat Warna Sintetis Pada Saos Secara
Kromatografi kertas... 25
Lampiran 2. Sampel Saos Cabai ... 26
Lampiran 3. Gambar Pengujian Sampel ... 27
ABSTRAK
Pewarna sintetis pada umumnya terbuat dari bahan-bahan kimia. Bahan pewarna sintetis yang boleh digunakan untuk makanan pun harus dibatasi jumlahnya. Karena pada dasarnya, setiap bahan kimia yang masuk kedalam tubuh akan menimbulkan efek negatif pada tubuh . Hal ini sebanding dengan dengan zat warna sintetis yang ada di dalam saos cabai. Zat warna sintetis di dalam saos cabai mengandung zat warna sintetis yang berbahaya dalam penggunaanya. Identifikasi zat warna sintetis pada saos ini bertujuan untuk mengetahui apakah saos cabai yang akan diedarkan dipasaran mengandung zat warna sintetis atau tidak. Zat pewarna sintetis dalam makanan dapat membuat suatu makanan lebih menarik, meratakan warna makanan dan mengembalikan warna dari bahan dasar yang hilang atau berubah selama pengolahan. Identifikasi zat warna sintetis pada saos cabai dilakukan di Laboratorium Kesehatan Daerah Pemerintahan Provinsi Sumatera Utara di Medan. Identifikasinya menggunakan Kromatografi Kertas. Hasil yang diperoleh dari harga Rf baku pembanding Eritrosin adalah 0,141 dan harga Rf baku pembanding Rhodamin B adalah 0,3 sedangkan harga Rf1 pada sampel adalah 0,416 dan harga Rf2 pada sampel adalah 0,333, dari hasil ini dapat disimpulkan bahwa saos cabai positif mengandung zat warna sintetis sehingga sampel yang diuji dinyatakan tidak memenuhi persyaratan sesuai dengan Peraturan Menkes RI Nomor 239/Menkes/Per/V/85.
BAB I PENDAHULUAN
1.1 Latar Belakang
Pada umumnya bahan makanan mengandung beberapa unsur seperti air,
karbohidrat, protein, lemak, vitamin, enzim, pigmen dan lain-lain. Kandungan
bahan tersebut bergantung dari sifat alamiah bahan makanan tersebut. Untuk
memperoleh produk pangan olahan yang bercita rasa lezat,berpenampilan
menarik, tahan lama serta mudah dalam pengangkutan dan pendistribusiannya
maka digunakan berbagai bahan pendukung yang disebut dengan bahan tambahan
pangan (Nugraheni, 2014).
Mutu bahan pangan pada umumnya ditentukan oleh beberapa faktor
seperti cita rasa, tekstur dan nilai gizi, tetapi sebelum faktor-faktor tersebut
mempengaruhi secara khusus faktor visual seperti warna pada makanan juga
sangat menetukan. Selain sebagai faktor yang ikut menentukan mutu, warna juga
dapat digunakan sebagai indikator kesegaran dan kematangan, baik tidaknya cara
pencampuran atau cara pengolahan dapat ditandai dengan adanya warna yang
seragam dan merata (Cahyadi, 2006).
Warna pada makanan mempunyai daya tarik tersendiri untuk seseorang
agar memakannya terlebih lagi warna tersebut terang atau cerah. Warna yang
cerah memberi kesansegar atau matang, seperti jajanan yang dijual diluar lebih
Sejak dulu, masyarakat menggunakan pewarna alami untuk mengolah
makanan. Pewarna tersebut di antaranya daun suji (warna hijau), kunyit (warna
kuning) dan karamel (warna cokelat). Namun, karena adanya beberapa faktor
mereka beralih pada pewarna sintetis. Kemajuan ilmu pengetahuan dan teknologi
juga turut mendukung ditemukannya pewarna-pewarna sintetis baru. Keberadaan
pewarna sintesis lebih dipilih karena mudah didapat, murah, lebih bervariasi dan
tentunya lebih praktis (Sulami, 2009).
Pewarna sintetis merupakan pewarna yang dibuat dengan cara sintesis
kimia. Warna dari pewarna sintetis memang lebih kuat daripada pewarna alami.
Selain itu, pewarna sintetis memberikan warna yang lebih seragam, lebih stabil
dalam penyimpanan dan lebih praktis (Sulami, 2009).
Dewasa ini keamanan penggunaan zat pewarna sintetis pada makanan
masih dipertanyakan dikalangan konsumen. Sebenarnya konsumen tidak perlu
khawatir karena semua badan pengawas obat dan makanan di dunia secara terus
menerus memantau dan mengatur zat pewarna agar tetap aman dikonsumsi. Jika
ditemukan adanya risiko terhadap kesehatan, badan pengawas obat dan makanan
akan mengevaluasi pewarna tersebut dan menyebarkan informasinya keseluruh
jaringan sosial melalui media elektronik maupun media sosial. Pewarna yang
tidak alami dan dilarang dapat mengganggu kesehatan seperti keracunan, merusak
organ tubuh dan berpotensi memicu kanker(Pahmawati, 2011).
Kromatografi adalah cara pemisahan campuran yang didasarkan atas
perbedaan distribusi dari komponen campuran tersebut diantara dua fase yaitu
atau zat cair sedangkan fase gerak dapat berupa zat cair atau gas. Meskipun dasar
kromatografi adalah suatu proses pemisahan, namun banyak diantara cara ini
dapat digunakan untuk analisis kuantitatif. Kromatografi kertas dan KLT
umumnya lebih bermanfaat untuk tujuan identifikasikarena lebih sederhana
(Yazid, 2005).
Kromatografi kertas digunakan baik untuk analisa kualitatif maupun
kuantitatif. Senyawa-senyawa yang dipisahkan kebanyakan bersifat sangat polar,
misalnya asam-asam amino ,gula-gula atau pigmen-pigmen alam (Yazid, 2005).
1.2 Tujuan
Adapun tujuan dari identifikasi zat warna sintetis pada saos cabai secara
kromatografi kertas adalah untuk mengetahui pewarna sintetis apa saja yang
digunakan pada saos cabai dan apakah pewarna sintetis yang digunakan
memenuhi persyaratan.
1.3 Manfaat
Manfaat yang diperoleh dari identifikasi zat warna pada saos secara
kromatografi kertas adalah dapat mengetahui bahwa saos cabai yang diperiksa
tidak mengandung zat warna sintetis yang berbahaya sehingga aman untuk
BAB II
TINJAUAN PUSTAKA
2.1 Saos
Saos merupakan bumbu penyedap makanan atau biasanya digunakan
untuk menambah kelezatan pada makanan. Saos berbentuk seperti bubur kental
(pasta) dan umumnya bewarna orange hingga merah. Pembuatannya saos sering
ditambahkan dengan zat pewarna makanan alami maupun buatan.Warna saos
biasanya terbuat dari buah berwarna menarik seperti warna merah atau
ditambahkan zat pewarna, selain warna saos mempunyai aroma dan rasa yang
merangsang (dengan atau tanpa rasa pedas), mempunyai daya simpan panjang
karena mengandung asam, gula, garam dan seringkali ditambahkan pengawet
(Putra dkk, 2014 dan Margono, 2000).
2.1.1 Fungsi Saos
Kebutuhan akan saos dari tahun ke tahun terus meningkat. Di Indonesia,
saos merupakan produk olahan yang sangat populer, karena berfungsi sebagai
penambah cita rasa dan selera pada makanan. Saos juga banyak digunakan pada
industri pengalengan ikan. Selain sebagai campuran bumbu, saos dipakai sebagai
pelengkap hidangan (Margono, 2000).
2.2 Cabai Merah
Cabai merah (Capsicum annum L.)merupakan salah satu jenis tanaman
memiliki kandungan gizi yang cukup lengkap juga memiliki nilai ekonomis tinggi
yang banyak digunakan baik untuk konsumsi rumah tangga maupun untuk
keperluan industri makanan. Cabai merah dapat ditanam dengan kisaran suhu
antara 21oC–27oC (Nurlenawati dkk, 2010).
Klasifikasi tanaman cabai
Kingdom : Plantae
Dividi : Spermatophyta
Subdivisi : Angiospermae
Kelas : Dicotyledoneae
Subkelas : Sympetalae
Ordo : Tubiflorae
Famili : Solanaceae
Genus : Capsicum
Species : Capsicum annum L.
(Kusandriani, 1996).
2.3 Zat Pewarna 2.3.1 Pewarna Alami
Pewarna alami merupakan pewarna (pigmen) yang berasal dari tumbuh–
tumbuhan atau hewan contohnya karotenoid, klorofil, tannin, dan kuinon.
Walaupun terdapat secara alami dalam tumbuhan dan hewan, pewarna alami juga
dapat timbul akibat proses pemanasan, penyimpanan atau proses-proses
Pewarna alami dalam penggunaanya perlu dalam jumlah lebih banyak agar
dapat menghasilkan warna yang baik sehingga pewarna alami lebih mahal, selain
itu ketersediaanya pun terbatas. Warna yang tersedia juga kurang bervariasi,
sehingga hanya terbatas pada warna–warna asli dari tumbuhan atau hewan yang
menghasilkan zat warna tersebut (Murdiati dan Amaliah, 2013).
Ciri–ciri zat warna alami pada produk pangan:
a. konsentrasi pigmen rendah (warna agak suram)
b. seringkali memberikan rasa khas yang tidak diinginkan
c. mudah larut dalam air
d. satabilitas pigmen rendah
e. keseragaman warna kurang baik
f. spektrum warna tidak seluas seperti pada pewarna sintetis
g. membutuhkan waktu lama untuk meresap kedalam produk
h. mudah mengalami degradasi atau pemudaran pada saat saat diolah dan
disimpan
i. selain itu umumnya, pigmen-pigen ini bersifat tidak cukup stabil
terhadap panas, cahaya dan pH tertentu. Walau begitu, pewarna alami
umumnya aman dan tidak menimbulkan efek samping bagi tubuh
(Nugraheni, 2014).
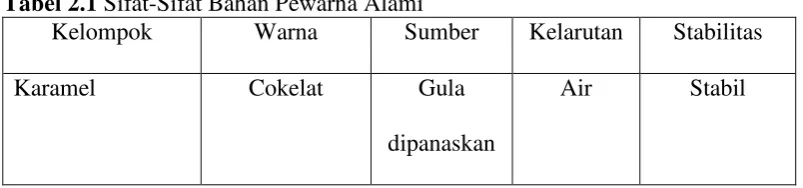
Tabel 2.1 Sifat-Sifat Bahan Pewarna Alami
Kelompok Warna Sumber Kelarutan Stabilitas
Karamel Cokelat Gula
dipanaskan
Anthosianin Jingga
Flavonoid Tanpa kuning Tanaman Air Stabil
terhadap
panas
Leucoanthosianin Tidak bewarna Tanaman Air Stabil
terhadap
panas
Tannin Tidak bewarna Tanaman Air Stabil
terhadap
panas
Batalain Kuning, merah Tanaman Air Sensitif
terhadap
panas
Quinon Kuning-hitam Tanaman
bakteria
merah hewan terhadap
panas
Klorofil Hijau,cokelat Tanaman Lipida dan
air
Sensitif
terhadap
panas
Heme Merah,cokelat Hewan Air Sensitif
terhadap
panas
(Cahyadi, 2006).
Penggunaaan pewarna makanan alami semakin lama semakin ditinggalkan
produsen makanan. Hal ini disebabkan karena kurang praktis, memberi rasa khas
yang tidak diinginkan, kurang stabil dalam penyimpanan, menghasilkan warna
yang kurang seragam yang bisa disebabkan oleh perubahan pH, proses oksidasi,
pengaruh cahaya dan pemanasan sehingga intensitas warnanya sering berkurang
selama proses pembuatan makanan. Akibatnya produsen makanan banyak yang
beralih ke pewarna sintetis (Nugraheni, 2014).
2.3.2 Pewarna Sintetis
Zat pewarna sintetis merupakan zat pewarna buatan manusia. Zat pewarna
sintetis harus melalui suatu pengujian secara intensif untuk menjamin
keamananya. Karakteristik dari zat pewarna sintetis adalah warnanya lebih cerah,
lebih homogen dan memilikiwarna yang bervariasi dibandingkan dengan zat
dihitung berdasarkan harga per unit dan efisiensi produksi akan jauh lebih murah
dibandingkan dengan zat pewarna alami (Pahmawati, 2011).
Beberapa keuntungan penggunaan zat pewarna sintetis adalah tersedia
dalam jumlah yang memadai, stabilitas bagus, kekuatan mewarnai yang tinggi
menjadikan zat pewarna sintetis menguntungkan secara ekonomi, daya larut bagus
dalam air dan alkohol, tidak berasa dan tidak berbau tersedia dalam berbagai
bentuk dan bebas bakteri (Nugraheni, 2014).
Pewarna sintetis juga mempunyai kekuranganyaitu dapat menimbulkan
berbagai macam penyakit terutama jika digunakan dengan dosis yang berlebihan
atau pemakaiannya sedikit tetapi dikonsumsi secara rutin dalam waktu yang lama
(Murdiati dan Amaliah, 2013).
Ciri–ciri pewarna sintetis antara lain:
a. warna cerah meskipun sudah mengalami proses pengolahan dan
pemanasan
b. tidak mudah larut dalam air
c. membutuhkan bahan pewarna lebih sedikit, karena dalam konsentrasi
rendah sudah mampu mewarnai dengan baik
d. cepat meresap ke dalam produk (Nugraheni, 2014).
Proses pembuatan zat warna sintetis biasanya melaui pemberian asam
sulfat atau asam nitrat yang seringkali terkontaminasi oleh arsen atau logam berat
lain yang bersifat racun. Pada pembuatan zat pewarna organik sebelum mencapai
produk akhir, harus memenuhi suatu senyawa dulu yang terkadang berbahaya dan
berbahaya. Namun sering sekali terjadi penyalahgunaan pemakaian zat pewarna
untuk bahan pangan, misalnya zat pewarna tekstil dan kulit untuk mewarnai bahan
pangan. Zat pewarna yang berbahaya terhadap kesehatan seperti Amaran,
Auramin, Methanyl Yellow dan Rhodamin B (Nugraheni, 2014).
Untuk zat pewarna yang dianggap aman, ditetapkan kandungan arsen tidak
boleh lebih dari 0,0004% dan timbal tidak boleh lebih dari 0,0001, sedangkan
logam berat lainnya tidak boleh ada (Cahyadi, 2006).
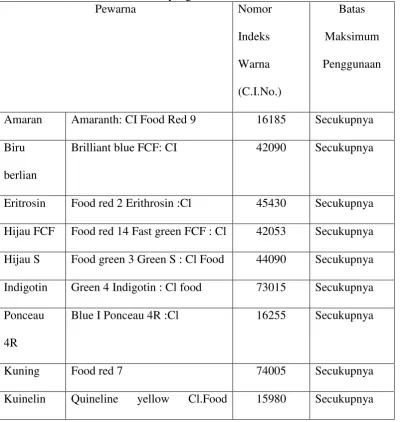
Tabel 2.2 Bahan Pewarna Sintetis yang Diizinkan di Indonesia
Pewarna Nomor
Amaran Amaranth: CI Food Red 9 16185 Secukupnya
Biru
berlian
Brilliant blue FCF: CI 42090 Secukupnya
Eritrosin Food red 2 Erithrosin :Cl 45430 Secukupnya
Hijau FCF Food red 14 Fast green FCF : Cl 42053 Secukupnya
Hijau S Food green 3 Green S : Cl Food 44090 Secukupnya
Indigotin Green 4 Indigotin : Cl food 73015 Secukupnya
Ponceau
4R
Blue I Ponceau 4R :Cl 16255 Secukupnya
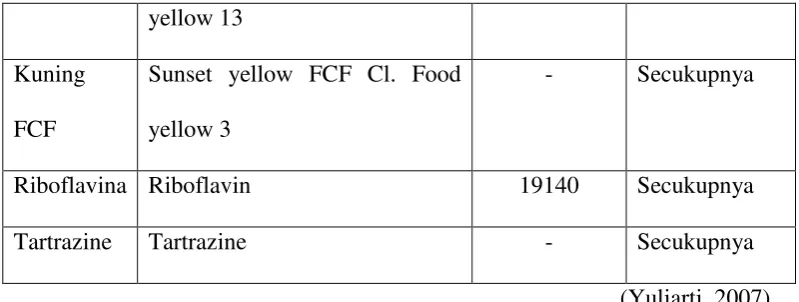
Kuning Food red 7 74005 Secukupnya
yellow 13
Kuning
FCF
Sunset yellow FCF Cl. Food
yellow 3
- Secukupnya
Riboflavina Riboflavin 19140 Secukupnya
Tartrazine Tartrazine - Secukupnya
(Yuliarti, 2007).
Tabel 2.3 Bahan Pewarna Sintetis yang Dilarang di IndonesiaBerdasarkan Peraturan Menkes RI Nomor 239/Menkes/Per/v/85
Nama Indeks Warna
Auramine (Cl basic yellow 2) 41000
Alkanet 755250
Butter Yellow (Cl solvent yellow) 11020
Chrysoidine (Cl food yellow B) 114270
Citrous 22156
Chocolate brown FB (Food Brown) -
Methanyl yellow (ext DC yellow1) 13065
Oil orange XO (Cl solvent oranges 7) 12140
Oil orange AB (Cl solvent orange 5) 11380
Orange RN (Cl food orange 1) 15970
Ponceau 3R (Cl food red 6) 16135
Ponceau SX (Cl food red 1) 14700
Rhodamin B (Cl food red 15) 45170
Scarlet GN (Cl food red 2) 14815
(Sulami, 2009).
2.3.2.1Rhodamin B
Rhodamin B dalam dunia perdagangan sering dikenal dengan nama tetra
ethyl rhodamin B, D dan Red no.19,C,I, Basic violet 10, C.I.No.45179. Zat warna
sintetis ini berbentuk serbuk kristal, tidak berbau, berwarna merah keunguan,
dalam larutan berwarna merah terang berpendar (berfluoresensi). Pewarna ini
sebenarnya adalah pewarna untuk kertas, tekstil, dan reagensia untuk pengujian
antimon, cobalt, dan bismuth (Yuliarti, 2007).
Rhodamin B tidak dapat larut dan dicerna oleh tubuh. Meskipun kadar
Rhodamin B yang dikonsumsi sangat sedikit, namun pewarna ini dapat
mengalami penumpukan dalam tubuh manusia. Keberadaan Rhodamin B pada
makanan ditandai dengan tampilan fisik makanan yang berwarna merah mencolok
dan berpendar (Sulami, 2009).
Penggunaan Rhodamin B pada makanan dalam waktu yang lama akan
dapat mengakibatkan gangguan fungsi hati maupun kanker. Namun demikian, bila
terpapar Rhodamin B dalam jumlah besar maka dalam waktu singkat akan terjadi
gejala akut keracunan Rhodamin B. Bila Rhodamin B tersebut masuk melalui
makanan maka akan mengakibatkan iritasi pada saluran pencernaan dan
mengakibatkan gejala keracunan dengan air kencing yang berwarna merah
ataupun merah muda. Jangankan lewat makanan, menghirup Rhodamin B dapat
mengakibatkan gangguan kesehatan, yakni terjadinya iritasi pada saluran
akan mengalami iritasi. Mata yang terkena Rhodamin B juga akan mengalami
iritasi yang ditandai dengan mata kemerahan dan terdapat timbunan cairan atau
udem pada mata (Yuliarti, 2007).
2.3.2.2 Eritrosin
Zat pewarna ini termasuk golongan fluorescein berupa tepung coklat
larutannya dalam alkohol 95% menghasilkan warna merah yang berfluoresensi,
sedangkan larutannya dalam air bewarna merah cherry tanpa fluoresensi. Eritrosin
arut dalam gliserol dan glikol bersifat kurang tahan terhadap cahaya dan
oksidator, tetapi tahan terhadap reduktor dan NaOH 10%. Mudah diendapkan oleh
asam, karena itu tidak dapat dipergunakan dalam produk minuman. Eritrosin juga
dapat diendapakan oleh tawas dan FeSO4. Logam Cu hanya sedikit berpengaruh
terhadap warna larutan (Nugraheni, 2014).
Eritrosin mengakibatkan reaksi alergi pada pernapasan, hiperaktif pada
anak-anak, serta menghambat perkembangan otak dan perilaku (Sulami, 2009).
2.4 Alasan Penggunaan Pewarna Tambahan
Pewarna merupakan bahan yang ditambahkan dalam makanan yang
berfungsi untuk memberikan warna yang khas dan mencari ciri khusus dari suatu
makanan. Kemajuan teknologi pangan memungkinkan zat pewarna dibuat secara
sintetis. Dalam jumlah yang sedikit suatu zat kimia bisa memberi warna yang
stabil pada produk pangan.
Beberapa alasan utama menambahkan zat pewarna pada makanan :
a. untuk menutupi perubahan warna akibat paparan cahaya, udara, atau
b. memperbaiki variasi alami warna. Produk pangan yang salah warna
akan diasosiasikan dengan kualitas rendah
c. membuat identitas produk pangan
d. menarik minat konsumen dengan pilihan warna yang menyenangkan
e. menjaga rasa dan vitamin yang mungkin yang terpengaruh sinar
matahari selama produk di simpan
f. melindungi rasa dan cahaya rentan vitamin (Nugraheni, 2014).
2.5 Fungsi Warna Pada Produk Pangan
a. sebagai indikator kematangan, terutama untuk produk pangan segar seperti
buah-buahan
b. sebagai indikator kesegaran misalnya pada produk sayuran dan daging.
c. sebagai kesempurnaan proses pengolahan pangan misalnya pada proses
penggorengan, timbulnya warna coklat sering kali sebagai indikator akhir
kematangan produk (Nugraheni, 2014).
2.6 Kromatografi Kertas
Kromatografi kertas diperkenalkan oleh Consden, Gordon, dan Martin,
yang menggunakan kertas saring sebagai penunjang fase diam. Kertas merupakan
selulosa murni yang mempunyai afinitas besar terhadap air atau pelarut polar
lainnya. Bila air diadsorpsikan pada kertas, maka akan membentuk lapisan tipis
penyangga dan air bertindak sebagai fase diam yang terserap diantara struktur pori
kertas (Yazid, 2005).
Meskipun zat yang tercovery tidak betul-betul murni, dia dimanfaatkan
juga untuk uji kualitatif dan kuantitatif. Keterbatasan metode ini adalah waktu
yang relatif lama dan resolusinya yang rendah. Susunan serat kertas membentuk
medium berpori yang bertindak sebagai tempat untuk mengalirnya fase bergerak.
Berbagai macam kertas secara komersial tersedia adalah Whatman 1, 2, 31 dan
3mm. Kertas asam asetil, kertas kieselguhr, kertas silikon dan kertas penukaran
ion yang digunakan. Tersedia juga kertas selulosa murni, kertas selulosa yang
dimodifikasi dan kertas serat kaca. Zat-zat hidrofobik dapat dipisahkan pada
kedua jenis kertas terakhir ini. Kertas asam asetil atau kertas silikon dapat
digunakan untuk zat-zat hidrofobik, sedangkan untuk reagen yang korosif, kertas
serat kaca dapat digunakan. Untuk memilih kertas, yang menjadi pertimbangan
adalah tingkat dan kesempurnaan pemisahan, difusivitas pembentukan spot, efek
tailing dan pembentukan komet serta laju pergerakan pelarut terutama untuk
teknik descending. Pembentukan komet adalah suatu fenomena dimana spot
yangdiperoleh bukannya berbentuk bundar, melainkan bulatan berbentuk panjang.
Penambahan asam dalam pelarut bisa menghindarkan pembentukan komet serta
mencegah ionisasi akibat hidrolisis ion-ion anorganik yang berbentuk komet.
Seringkali nilai Rf berbeda dari satu kertas- kertas lainnya. Pengotor yang terdapat
pada kertas saring adalah ion-ion Ca2+, Mg2+, Fe3+, Cu2+. Kertas seharusnya
Kromatografi kertas tidak memerlukan pelat pendukung dan kertas dapat
dengan mudah diperoleh dalam bentuk murni sebagai kertas saring. Lapisan
selulosa harus dicetak atau dibeli khusus. Panjang serabut pada kertas lebih
panjang daripada serabut pada lapisan selulosa lazim, menyebabkan lebih banyak
terjadi difusi ke samping dan bercak lebih besar. Akhirnya, lapisan selulosa lebih
rapat dan pelarut cenderung mengalir melaluinya lebih cepat dan menghasilkan
pemisahan tajam (Gritter, 1991)
Cairan fase bergerak yang biasanya berupa campuran dari pelarut organik
dan air, akan mengalir membawa noda cuplikan yang didepositkan pada kertas
dengan kecepatan berbeda. Pemisahan terjadi berdasarkan partisi masing-masing
komponen diantara fase diam dan fase bergeraknya. Senyawa-senyawa yang
dipisahkan kebanyakan bersifat sangat polar, misalnya asam-asam amino,
gula-gula atau pigmen-pigmen alam (Yazid, 2005).
Ditinjau dari sistem pelarut yang dipergunakan salam kromatografi partisi,
dikenal tiga kategori yaitu fase dan berair, fase diam pelarut organik hidrofilik,
dan fase diam pelarut organik hidrofobik. Fase diam berair bersifat polar ataupun
ionik. Fase diam tersebut diperoleh dengan cara mengekspos kertas pada atmosfer
air dalam ruang tertutup. Kertas tersebut tanpa direndam dalam larutan buffer dan
dapat dikeringkan sebelum digunakan. Dua metode dapat digunakan untuk
memperoleh fase diam pelarut organik hidrofilik, tergantung pada volatilitas
pelarutnya, jika pelarutnya mudah menguap digunakan teknik eksposur,
sedangkan bila pelarutnya tidak mudah menguap digunakan teknik perendaman
formida, yang terdiri atas selulosa, karbitol, gliserol dan benzoil alkohol.
Menjadikan kertas hidrofobik dapat juga dilakukan dengan impregnasi kertas
dengan pelarut hidrofobik yang terlarut dalam eluen mudah menguap serta
dibiarkan kering di udara (Khopkar, 1990).
2.6.1 Teknik Kromatografi Kertas
Proses pengeluaran asam mineral dari kertas disebut desalting. Larutan
ditempatkan pada kertas dengan menggunakan mikropipet pada jarak 2–3 cm dari
salah satu ujung kertas dalam bentuk coretan garis horizontal. Setelah kertas
dikeringkan, diletakkan di dalam ruang yang sudah dijenuhkan dengan air atau
dengan pelarut yang sesuai. Penjenuhan dapat dilakukan 24 jam sebelum analisis
(Khopkar, 1990)
Kertas dipotong memanjang sesuai ukuran bejana yang akan digunakan.
Kertas yang dipakai adalah kertas Whatman yang secara komersial tersedia dalam
berbagai macam ukuran dan lembaran. Biasanya dipakai kertas Whatman no.1
dengan kecepatan sedang. Tersedia juga kertas selulosa murni, kertas selulosa
yang dimodifikasi , kertas asam asetil dan kertas serat kaca. Untuk pemilihan
kertas yang menjadi pertimbangan adalah tingkat kesempurnaan pemisahan,
difusifitas pembentukan spot, efek tailing serta laju pergerakan pelarut. Kertas
yang akan digunakan harus disimpan dalam ruang tertutup atau di temapat yang
kering jauh dari sumber uap terutama yang mempunyai afinitas tinggi terhadap
selulosa (Yazid, 2005).
Sejumlah cuplikan kurang lebih 1 µl diteteskan menggunakan mikropipet
dengan pensil. Spot atau noda yang terbentuk dikeringkan, lalu kertas dimasukkan
dalam bejana tertutup yang sudah dijenuhkan dengan pelarut yang sesuai untuk
dikembangkan. Penjenuhan dilakukan selama 24 jam sebelum analisis (Yazid,
2005).
Terdapat tiga metode pengembangan pada kromatografi kertas ,yaitu :
a. Metode Penaikan (Ascending)
Kertas digantungkan pada penggantung berbentuk kail yang dipasang
pada penutup bejana kromatografi. Pelarut berada di dasar bejana
(Gritter, 1991).
Noda harus diusahakan tidak sampai tercelup karena dapat larut dalam
pelarut. Pelarut akan naik memalui serat-serat kertas oleh gaya kapiler
menggerakan komponen dengan jarak yang berbeda-beda (Yazid, 2005)
b. Metode Penurunan (Descending)
Bejana dilengkapi dengan sejenis wadah pelarut yang di pasang pada
penopang dan kertas kromatografi dicelupkan ke dalam pelarut di
dalam wadah itu dan diberati dengan batang kaca supaya tetap pada
tempatnya . Pelarut bergerak turun membawa komponen melaui gaya
kapiler dan gaya gravitasi (Gritter, 1991).
c. Metode Mendatar (Radial)
Metode ini sangat berbeda dari sebelumnya. Biasanya kertas dibentuk
bulat ditengahnya diberi sumbu dari benang atau gulungan kertas. Noda
sumbu sehingga membasahi kertas untuk kemudian mengembang
melingkar membawa komponen yang dipisahkan (Yazid, 2005)
Temperatur harus dikendalikan dalam variasi tidak boleh lebih dari 0,5oC.
Kertas harus didiamkan dahulu paling tidak 24 jam dengan atmosfer pelarutnya,
agar mencapai kesetimbangan sebelum pengaliran pelarutnya pada kertas.
Dilakukan beberapa pengerjaan yang parallel, Rf nya tidak boleh berbeda lebih
dari ± 0,02 (Khopkar, 1990).
Bila permukaan pelarut telah mengembang atau bergerak pada batas
tertentu, maka kertas dikeluarkan dari bejana dan batas permukaan pelarut diberi
tanda lalu kertas dikeringkan. Jika senyawa yang dipisahkan bewarna akan
nampak seperti noda- noda yang terpisah. Tetapi jika komponen zat tidak bewarna
umumnya zat organik), maka dapat dideteksi dengan cara fisika dan kimia (Yazid,
2005).
Setelah letak noda komponen diketahui dan diberi tanda batas, harga Rf
(Retardation factor) dapat dihitung
Rf =
jarak yang ditempuh komponen jarak yang ditempuh pelarutNilai Rf dapat digunakan untuk identifikasi kualitatif dari senyawa yang
tidak diketahui dengan membandingkan terhadap senyawa standar. Bila harga Rf
sama, berarti kedua senyawa tersebutidentik sedangkan untuk analisis kuantitatif,
komponen-komponen yang terpisah dapat dipotong-potong kemudian dilarutkan
secara terpisah dalam pelarut yang sesuai untuk ditetapkan kadarnya dengan
BAB III
METODOLOGI PERCOBAAN
3.1 Tempat Pengujian
Pengujian identifikasi zat warna pada saos secara kromatografi kertas
dilakukan di Laboratorium Toksikologi, Balai Laboratorium Kesehatan Daerah
Pemprovsu Medan di Jalan Williem Iskandar Pasar V Barat I No.4 Medan.
3.2 Alat
Alat yang digunakan adalah beaker glass, chamber, erlenmeyer, gelas
ukur, hot plate, kertas kromatografi, neraca analitik, pipet mikro, pipet tetes, pot
plastik.
3.3 Bahan
Bahan yang digunakan adalah aquadest, asam asetat 10%, bulu domba,
Larutan Pembanding Eritrosin , Larutan pembanding Rhodamin B, NH4OH(p),
metanol, sampel saus cabai, Tri-natrium citrat.
3.4 Prosedur 3.4.1 Larutan Uji
Saos ditimbang sebanyak 50 g, dimasukkan ke dalam labu erlenmeyer,
ditambahkan 10 ml asam asetat 10%, ditambahkan 3-4 bulu domba bebas lemak,
dalam erlenmeyer lebih kurang 25 ml NH4OH 10% kemudian didihkan selama 10
menit. Zat warna yang larut dimasukkan kedalam larutan basa, dibuang bulu
dombanya, diuapkan diatas penangas air larutan yang bewarna, residu dilarutkan
dalam sedikit metanol, ditotolkan pada kertas kromatografi, dilakukan
kromatografi, bandingkan dengan standart warna dan dihitung harga Rf nya.
3.4.2 Larutan Baku
Sejumlah ±1 mg Eritrosin dan Rhodamin B ditimbang seksama. Larutkan
dan encerkan dengan aquadest secukupya.
3.4.3 Identifikasi
Larutan A, B, dan C masing-masing ditotolkan secara terpisah dan
dilakukan kromatografi kertas sebagai berikut :
Fase diam : Kertas Whatman
Fase gerak : NH4OH pekat : Trinatrium Sitrat : Aquadest
Penjenuhan : Dengan kertas saring
Volume penotolan : Larutan A 50 µl , larutan B 50µl , larutan C 100µl
Jarak rambat : 12 cm
Penampak noda : UV 245 nm
3.5 Persyaratan
Saos cabai tidak boleh mengandung bahan pewarna sintetis yang
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil
Dari hasil identifikasi zat warna sintetis pada saos cabai secara kromatografi
kertas, diketahui bahwa saos cabai yang diuji mengandung zat warna sintetis
karena pada saos menghasilkan kromatogram.
Perhitungan Rf dan kromatogram hasil pengujian dari kromatografi kertas
(KKT) dapat dilihat pada lampiran.
4.2 Pembahasan
Dari hasil pengujian kromatografi kertas, menunjukkan bahwa sampel
mengandung zat warna sintetis yang berbahaya karena pada sampel menghasilkan
kromatogram.
Warna pada makanan merupakan daya tarik tersendiri untuk menggugah
selera. Jajanan anak lebih banyak mempunyai variasi warna, karena
anak-anak akan lebih memilih makanan yang berwarna dan berbentuk menarik tanpa
mempertimbangkan nilai gizi dari makanan tersebut. Pemberian warna pada
makanan umumnya bertujuan agar makanan terlihat lebih segar dan menarik,
sehingga menimbulkan selera orang untuk memakannya. Namun, pewarna
makanan merupakan bahan tambahan pangan yang perlu pengawasan lebih karena
penggunaannya yang terkadang tidak sesuai anjuran atau bahkan menggunakan
Baik zat pewarna sintetis maupun alami digunakan dalam industri makanan
harus memenuhi standart nasional dan internasional. Penyalahgunaan zat pewarna
melebihi ambang batas maksimum atau penggunaan secara ilegal zat pewarna
yang dilarang digunakan dapat mempengaruhi kesehatan konsumen, seperti
timbulnya keracunan akut dan bahkan kematian. Pada tahap keracunan kronis,
dapat terjadi gamgguam fisiologis tubuh seperti kerusakan syaraf, gangguan organ
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Hasil pengujian identifikasi zat warna sintetis pada saos cabai secara
kromatografi kertas menunjukkan bahwa saos cabai mengandung zat warna
sintetis Red 2G dan Orange RN sehingga dapat disimpulkan bahwa saos cabai
yang diuji tidak memenuhi persyaratan menurut dengan Peraturan Menkes RI
Nomor 239/MENKES/V/85.
5.2 Saran
Sebaiknya pengujian untuk bahan tambahan pangan tidak hanya pada pada
pengujian zat warna sintetis saja, akan tetapi pengujian-pengujian lain untuk
memenuhi persyaratan dari bahan tambahan pangan juga harus dilakukan agar
saos cabai yang akan dipasarkan benar-benar merupakan makanan yang
DAFTAR PUSTAKA
Cahyadi, W. (2006). Analisis & Aspek Kesehatan Bahan Tambahan Pangan. Jakarta: Bumi Aksara. Hal 53-55.
Effendi, S. (2012). Teknologi Pengolahan dan Pengawetan Pangan. Bandung: Alfabeta. Hal 162.
Gritter, J.R. (1991). Pengantar Kromatografi. Bandung: ITB. Hal 158.
Kusandriani. (1996). Botani Tanaman Cabai Merah. Bandung: Balai Penelitian Sayuran.
Khopkar, M.S. (1990). Konsep Dasar Kimia Analitik. Jakarta: Universitas Indonesia Press. Hal 153-156.
Margono, T. (2000). Saos Pepaya. Jakarta: PT Grasindo. Hal 2.
Murdiati, A. dan Amaliah. (2013). Panduan Penyiapan Pangan Sehat Untuk Semua. Edisi Kedua. Jakarta: Kencana. Hal 173-174.
Nugraheni, M. (2014). Pewarna Alami. Yogyakarta: Graha Ilmu. Hal 1-2, 12-13, 19, 28, dan 30.
Nurlenawati,N., Jannah,A., Nimih.(2010),Respon Pertumbuhan Dan Hasil Tanaman Cabai Merah (Capsicum AnnuumL.) Varietas Prabu TerhadapBerbagai Dosis Pupuk Fosfat DanBokashi Jerami Limbah Jamur Merang. Vol 4(1).Program Studi Agroteknologi, Fakultas Pertanian Universitas Singaperbangsa Karawang(UNSIKA). Hal 9-10.
Pahmawati, Y. (2011). Kegunaan dan Efek Samping Bahan Kimia. Jakarta: Adfale.Hal 35-37.
Putra,R.I., Asterina., Isrona,L. (2014). Gambaran Zat Pewarna Merah Pada Saus Cabai Yang Terdapat Pada Jajanan Yang Dijual di Sekolah Dasar Negeri Kecamatan Padang Utara . Vol3 (3). Jurnal Kesehatan Andalas. Hal 299.
Sulami, E. (2009). Sehatkah Bahan Tambahan Makananmu?. Klaten: PT Intan Pariwara. Hal 1,3dan 8.
Yazid, E. (2005). Kimia Fisika Untuk Paramedis. Yogyakarta: ANDI. Hal 205-208.
Yuliarti, N. (2007). Awas! Bahaya di Balik Lezatnya Makanan. Yogyakarta: ANDI. Hal 90, 92-93.
Lampiran 1. DataHasil Identifikasi Zat Warna Sintetis Pada Saos Cabai Secara Kromatografi Kertas (KKT)
Pelarut : Asam Asetat 10%
Fase Diam : KertasWhatmann no.1
Fase Gerak : NH4OH pekat : Trinatrium Sitrat : Aquadest (5 : 2 : 95)
Baku Pembanding : Eritrosin dan Rhodamin B
Penjenuhan : Dengan Kertas Saring
Jarak Rambat : 12 cm
Penampak Noda : UV 245 nm
Tabel Hasil perhitungan harga Rf
Nama Zat Harga Rf Nama Zat Warna
Baku pembanding
Eritrosin
Rf: 1,7cm/12cm = 0,3 Rhodamin B
Baku pembanding
Rhodamin B
Rf: 3,6cm/12cm = 0,141 Eritrosin
Sampel Saos cabe
Rf1: 5/12 = 0,416 Red 2 G
RF2 : 4/12 = 0,333 Orange RN
Nama Contoh : Saos Cabai
No. Lab : 0457/L II/2015
Jam : 10.00 WIB
Tanggal diterima : 04/02/2015
Pemerian
Bentuk : Pasta
Rasa : Pedas
Warna : Merah
Bau : Khas
Sampel Saos Cabai
Pemanasan bulu domba