ANALISA UNSUR NITROGEN PADA DAUN KELAPA SAWIT
DENGAN METODE DESTRUKSI BASAH
SECARA TITRIMETRI
KARYA ILMIAH
SURYADI CIBRO
072401004
ANALISA UNSUR NITROGEN PADA DAUN KELAPA SAWIT DENGAN METODE DESTRUKSI BASAH SECARA TITRIMETRI
KARYA ILMIAH
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Ahli Madya
SURYADI CIBRO 072401004
PROGRAM STUDI D3 KIMIA ANALIS DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : ANALISA UNSUR NITROGEN PADA DAUN KELAPA SAWIT DENGAN METODE DESTRUKSI BASAH \ SECARA TITRIMETRI
Kategori : KARYA ILMIAH Nama : SURYADI CIBRO NIM : 072401004
Program Studi : D3 KIMIA ANALIS Departemen : KIMIA
PERNYATAAN
ANALISA UNSUR NITROGEN PADA DAUN KELAPA SAWIT DENGAN METODE DESTRUKSI BASAH SECARA TITRIMETRI
KARYA ILMIAH
Saya mengakui bahwa karya ilmiah ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juni 2010
PENGHARGAAN
Alhamdulillahirabbil’alamin segala puji dan syukur kita panjatkan kehadirat Allah SWT yang telah mencurahkan hidayah-Nya berupa kesehatan dan keterbukaan fikiran bagi penulis, serta shalawat dan salam penulis panjatkan kepada junjungan Nabi besar Muhammad SAW sehingga penulis dapat menyelesaikan karya ilmiah ini sebagai salah satu syarat dalam menyelesaikan pendidikan di program D3 Kimia Analis Departemen Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara dengan judul ANALISA UNSUR NITROGEN PADA
DAUN KELAPA SAWIT DENGAN METODE DESTRUKSI BASAH SECARA TITRIMETRI .
Penyusunan karya ilmiah ini dilakukan berdasarkan pengamatan secara langsung yang dilaksanakan di PUSAT PENELITIAN KELAPA SAWIT (PPKS)
MEDAN.
Dalam kesempatan ini penulis ingin mengucapkan rasa hormat dan terima kasih yang setinggi – tingginya kepada kedua orang tua penulis yaitu Ayahanda Alm. Ismail Cibro dan Ibunda Kartini Boangmanalu, serta semua kakanda tercinta Rinto Cibro, Erlinawati Cibro, Sudarmi Cibro, Roma Cibro, dan Susilawati Cibro yang telah memberikan dukungan, doa serta kasih sayang kepada penulis sehingga penulis dapat menyelesaikan karya ilmiah ini.
Selain itu penulis juga ingin mengucapkan terima kasih yang sebesar-besarnya kepada :
1. Bapak Drs. Saut Nainggolan selaku dosen pembimbing tugas akhir yang telah begitu sabar dan banyak meluangkan waktu, tenaga, memberikan pemikiran serta masukan kepada penulis sehingga telah dapat menyelesaikan karya ilmiah ini.
2. Bapak Prof. Dr. Eddy Marlianto, M.Sc selaku Dekan FMIPA USU
3. Ibu Dr. Rumondang Bulan, MS selaku Kepala Departemen Kimia FMIPA USU.
4. Ibu Dr. Marpongahtun, M.Sc selaku dosen pembimbing akademik yang telah membimbing penulis selama menjalankan pendidikan di FMIPA USU.
5. Seluruh staf pengajar dan karyawan di FMIPA USU yang telah memberikan ilmu dan bantuannya kepada penulis.
6. Bapak Drs. Eka Nuryanto, M.Si selaku pembimbing praktek kerja lapangan dan manager laboratorium pelayanan di Pusat Penelitian Kelapa Sawit (PPKS) Medan.
disebutkan namanya satu-persatu, terima kasih atas semangat, bantuan, doa, kebersamaan, nasehat dan sebuah persahabatan terindah yang telah diberikan selama penulis menjalani hari-hari suka dan duka sebagai mahasiswa.
9. Seluruh anggota keluarga yang telah memberikan doa dan semangatnya kepada penulis.
Dengan kerendahan hati penulis berharap semoga karya ilmiah ini dapat memberikan sumbangsih dalam pengembangan ilmu pengetahuan. Penulis menyadari sepenuhnya bahwa tugas akhir ini belum sempurna, oleh karena itu penulis sangat mengharapkan kritik dan saran yang bersifat membangun menuju yang lebih baik. Akhir kata penulis mengharapkan semoga karya ilmiah ini dapat berguna bagi para pembaca.
Medan, Juni 2010
Penulis
ABSTRAK
NITROGEN ELEMENTS ANALYSIS IN OIL PALM LEAVES WITH METHOD WET DESTRUCTION
BY TITRIMETRY
ABSTRACT
DAFTAR ISI
1.2. Permasalahan 3
1.3. Tujuan 3
1.4. Manfaat 4
BAB 2 TINJAUAN PUSTAKA 5
2.1. Tanaman Kelapa Sawit 5
2.2. Daun Kelapa Sawit 5
2.3. Morfologi Daun Kelapa Sawit 7 2.4. Unsur-Unsur Hara Yang Dibutuhkan Kelapa Sawit 8 2.4.1. Unsur Hara Nitrogen 8 2.4.2. Peranan Unsur Hara Nitrogen 10 2.4.3. Gejala Defisiensi Unsur Hara Nitrogen 12
2.5. Analisis titrimetri 13
BAB 3 METODOLOGI PERCOBAAN 17
3.1. Alat 17
3.2. Bahan 17
3.3. Persiapan Contoh Daun Kering 19 3.3.1. Membersihkan Contoh Daun Kelapa Sawit 19 3.3.2. Mengeringkan dan Menggiling Contoh Daun Kelapa Sawit 19 3.4. Prosedur Destruksi Basah (H2SO4 + H2O2) Daun Kelapa Sawit 20
3.5. Prosedur Penetapan Nitrogen (N) Pada Daun Kelapa Sawit 21
BAB 4 HASIL DAN PEMBAHASAN 22
4.1. Hasil Dan Analisa Data 22
4.2. Perhitungan 22
BAB 5 KESIMPULAN DAN SARAN 26
5.1. Kesimpulan 26
5.2. Saran 26
DAFTAR PUSTAKA 27
DAFTAR TABEL
ABSTRAK
NITROGEN ELEMENTS ANALYSIS IN OIL PALM LEAVES WITH METHOD WET DESTRUCTION
BY TITRIMETRY
ABSTRACT
BAB 1
PENDAHULUAN
1.1. Latar belakang
Daun kelapa sawit mirip daun kelapa yaitu membentuk susunan daun majemuk,
bersisip genap, dan bertulang sejajar. Daun-daun membentuk satu pelepah yang
panjangnya mencapai lebih dari 7,5 - 9 m. Jumlah anak daun di setiap pelepah
berkisar antara 250 - 400 helai. Daun muda yang masih kuncup berwarna kuning
pucat. Pada tanah yang subur daun cepat membuka sehingga makin efektif melakukan
fungsinya sebagai tempat berlangsungnya fotosintesis dan sebagai alat respirasi.
Semakin lama proses fotosintesis berlangsung semakin banyak bahan makanan yang
dibentuk sehingga produksi akan meningkat. Produksi daun tergantung iklim
setempat. Di Sumatera Utara, misalnya produksi daun mencapai 20 – 24 helai/tahun.
Umur daun mulai terbentuk sampai tua sekitar 6 – 7 tahun. Daun kelapa sawit yang
sehat dan segar berwarna hijau tua.
Jumlah pelepah, panjang pelepah, dan jumlah anak daun tergantung pada umur
tanaman. Tanaman yang berumur tua, jumlah pelepah dan anak daun lebih banyak.
Begitu pula pelepahnya akan lebih panjang dibandingkan dengan tanaman yang masih
muda. Serta kering satu pelepah dapat mencapai 4,5 kg. pada tanaman dewasa
ditemukan sekitar 40 – 50 pelepah. Saat tanaman berumur sekitar 10 - 13 tahun dapat
akan berinteraksi dengan tingkat produktivitas tanaman. Semakin luas permukaan atau
semakin banyak jumlah daun maka produksi akan meningkat karena proses
fotosintesis akan berjalan dengan baik. Proses fotosintesis akan optimal jika luas
permukaan daun mencapai 11 m2.
Jumlah kedudukan pelepah daun pada batang kelapa sawit disebut juga
phyllotaxis yang dapat ditentukan berdasarkan perhitungan susunan duduk daun, yaitu
dengan menggunakan rumus duduk daun 1/8. Artinya, setiap satu kali berputar
melingkari batang, terdapat duduk daun (pelepah) sebanyak 8 helai. Pertumbuhan
melingkar duduk daun mengarah ke kanan atau ke kiri menyerupai spiral. Pada
tanaman yang normal dapat dipilih 2 set spiral berselang 8 daun yang mengarah ke
kanan dan berselang 13 daun mengarah ke kiri.
Arah duduk daun sangat berguna untuk menentukan letak duduk daun ke-9 dan
ke-17 saat pengambilan contoh daun. Disamping itu, duduk daun juga berguna untuk
menentukan jumlah daun yang harus tetap di bawah buah terendah yang disebut
songgoh.
Pengambilan contoh daun bertujuan terutama untuk memperoleh data tentang
kandungan unsur hara dalam daun melalui analisis laboratorium, mengingat adanya
hubungan antara kandungan hara daun dengan pertumbuhan tanaman dan produksi
Kandungan hara daun digunakan sebagai salah satu bahan pertimbangan dalam
menyusun rekomendasi pemupukan tanaman kelapa sawit pada masa berikutnya. (
Warta PPKS, 2007).
Unsur Nitrogen merupakan komponen utama dalam tubuh tanaman, terutama
dalam protoplasma sel, protein, asam amino, amida dan alkohol. Klorofil juga
mengandung Nitrogen, dan bila daun kekurangan unsur Nitrogen, daun itu akan
berwarna pucat.Oleh karena itu, penulis tertarik dalam analisa unsur hara Nitrogen
pada daun kelapa sawit secara Titrimetri (Tim Bina Karya 2009).
1.2. Permasalahan
Apakah kandungan Nitrogen total pada daun kelapa sawit sudah mencukupi
kebutuhan akan unsur Nitrogen dalam pertumbuhannya.
1.3. Tujuan
Tujuan karya ilmiah ini adalah :
1.4. Manfaat
Manfaat penulisan karya ilmiah ini adalah :
Untuk memberikan informasi tentang kandungan unsur hara Nitrogen yang
terdapat pada daun kelapa sawit yang dapat menyusun rekomendasi pemupukan
tanaman kelapa sawit pada masa berikutnya. Sehingga dapt meningkatkan jumlah
BAB 2
TINJAUAN PUSTAKA
2.1. Tanaman kelapa sawit
Kelapa sawit pertama kali diperkenalkan di Indonesia oleh pemerintah kolonial
Belanda pada tahun 1848. Ketika itu ada empat batang bibit kelapa sawit yang dibawa
dari Mauritius dan Amsterdam dan ditanam di Kebun Raya Bogor. Tanaman kelapa
sawit mulai diusahakan dan dibudidayakan secara komersial pada tahun 1911.
Perintis usaha perkebunan kelapa sawit di Indonesia adalah Adrien Hallet,
seorang Belgia yang telah belajar banyak tentang kelapa sawit di Afrika. Budidaya
yang dilakukannya diikuti oleh K.Schadt yang menandai lahirnya perkebunan kelapa
sawit di Indonesia. Sejak saat itu perkebunan kelapa sawit di Indonesia mulai
berkembang. Perkebunan kelapa sawit pertama berlokasi di pantai timur Sumatera
(Deli) dan Aceh. Luas areal perkebunannya mencapai 5.123 ha (Yan, Fauzi. 2008).
2.2. Daun Kelapa Sawit
Daun kelapa sawit mirip daun kelapa yaitu membentuk susunan daun
majermuk, bersirip genap, dan bertulang sejajar. Daun – daun membentuk satu
setiappelepah berkisar antara 250 – 400 helai. Daun muda yang masih kuncup
berwarna kuning pucat. Pada tanah yang subur, daun cepat membuka sehingga makin
efektif melakukan fungsinya sebagai tempat berlangsungnya fotosintesis dan sebagai
alat respirasi. Semakin lama proses fotosintesis berlangsung, semakin banyak bahan
makanan yang dibentuk sehingga produksi akan meningkat. Produksi daun tergantung
iklim setempat. Di Sumatera Utara, misalnya produksi daun mencapai 20 – 24
helai/tahun. Umur daun mulai terbentuk sampai tua sekitar 6 – 7 tahun. Daun kelapa
sawit yang sehat dan segar berwarna hijau tua.
Jumlah pelepah, panjang pelepah, dan jumlah anak daun tergantung pada umur
tanaman. Tanaman yang berumur tua, jumlah pelepah dan anak daun lebih banyak.
Begitu pula pelepahnya akan lebih panjang dibandingkan dengan tanaman yang
masih muda . Pada tanaman dewasa ditemukan sekitar 40-50 pelepah. Saat tanaman
berumur sekitar 10-13 tahun dapat ditemukan daun yang luas permukaannya mencapai
10-15 m2. Luas permukaan daun akan berinteraksi dengan tingkat produktivitas
tanaman. Semakin luas permukaan atau semakin banyak jumlah daun maka
produksinya akan meningkat karena proses fotosintesis akan berjalan dengan baik
(Yan, Fauzi 2008).
Sekalipun proses fotosintesis dapat berlangsung pada bagian lain dari tanaman
dengan sumbangan yang dapat berarti pada saat tertentu seperti fotosintesis dari kulit
menjelaskan proses pertumbuhan yang terjadi seperti pada pembentukan biomassa
tanaman ( Sitompul, S.M. 1995 ).
2.3. Morfologi Daun Kelapa Sawit
Pengetahuan tentang daun kelapa sawit dan perkembangannya sangat penting
bagi staf perkebunan. Pada daun itulah, terletak “pabrik” yang sebenarnya bagi
produksi MKS dan IKS.
Daun kelapa sawit terdiri dari beberapa bagian, sebagai berikut :
1. Kumpulan anak daun (leaflets) yang mempunyai helaian (lamina) dan tulang anak
daun (midrib).
2. Rachis yang mempunyai tempat anak daun melekat.
3. Tangkai daun (petiole) yang merupakan bagian antara daun dan batang.
4. Seludang daun (sheath) yang berfungsi sebagai perlindungan dari kuncup dan
memberi kekuatan pada batang.
Bentuk seludang daun yang terlihat pada daun dewasa sudah tidak lengkap dan
merupakan sisa dari perkembangan yang ada. Pada daun yang sedang berkembang,
seludang berbentuk pipa dan membungkus daun muda secara sempurna. Namun,
karena daun berkembang terus – menerus, sedangkan seludang sudah tidak
berkembang lagi, serabut – serabut seludang menjadi robek dan tercerai membentuk
barisan duri (spine) sepanjang tepi – tepi petiole yang merupakan pangkal dari serabut
2.4. Unsur – Unsur Hara Yang di Butuhkan Kelapa Sawit
Unsur – unsur hara yang dibutuhkan tanaman biasanya dibagi atas dua
kelompok, yaitu unsur – unsur makro dan mikro. Alasan pembagian ini sederhana,
yaitu : unsur makro adalah yang dibutuhkan dalam jumlah besar, dan unsur mikro
dibutuhkan dalam jumlah kecil. Unsur mikro hanya diberikan dalam bentuk pupuk
bila analisis tanah menunjukkan adanya kekahatan (defisiensi), atau bila tanaman
menunjukkan gejala – gejala defisiensi.
Unsur – unsur yang tergolong unsur makro adalah Nitrogen (N), Fosfor (P),
Kalium (K), Magnesium (Mg), Kalsium (Ca), Belerang (S), dan Natrium (Na),
sedangkan unsur mikro adalah Klor (Cl), Mangan (Mn), Besi (Fe), Seng (Zn),
Tembaga (Cu), Molibden (Mo), dan Boron (B).
2.4.1 Unsur hara Nitrogen
Nitrogen atau Zat lemas adalah sebuah unsur kimia dalam table periodic yang
memiliki lambang N dan nomor atom 7. Biasanya ditemukan sebagai gas tanpa warna,
tanpa bau, tanpa rasa dan merupakan gas diatomik bukan logam yang stabil, sangat
Nitrogen adalah 78,08% dari atmosfir bumi dan terdapat banyak dalam
jaringan hidup. Zat lemas mebentuk banyak senyawa penting seperti asam amino,
amoniak, asam nitrat, dan sianida
Nitrogen merupakan hara mineral esensil paling banyak dimanfaatkan dalam
praktek pertanian yang diberikan dalam bentuk pupuk. Nitrogen merupakan unsure
penyusun asam amino, protein, asam nukleat dan sebagainya disamping unsur hara
lainnya.
Nitrogen yang dapat di manfaatkan oleh tanaman tinggkat tingggi khususnya
tanaman budidaya dapat di bedakan atas empat kelompok utama yaitu: nitrogen nitrat
(NO3-), nitrogen ammonia (NH4+), nitrogen molekuler (N2) dan nitrogen organic.
Tidak semua bentuk – bentuk ini dapat dimanfaatkan oleh suatu jenis tnaman.
Umumnya tanaman pertanian memanfaatkan nitrat dan ammonium kecuali pada
beberapa tanaman legume mampu memanfaatkan N bebas melalui proses fiksasi N
dengan bersimbiosis dengan bakteri. N organic kadang – kadang dapat dimanfaatkan
oleh tanaman tinggi akan tetapi tidak mampu mencukupi kebutuahan N tanaman dan
umumnya dimanfaatkan lewat daun melalui pemupukan lewat daun. Bagi tanaman
pertanian terutama manfaat N dalam bentuk ion nitra, akan tetapi dalam kondisi
tertentu khususnya pada tanah – tanha masam dan kondisi an aerobic tanaman akan
memanfaatkan N dalam bentuk ion ammonium (NH4+).
Pada tanaman – tanaman yang tumbuh aktif dengan cepat nitrat yang
terabsopsi oleh akar tanaman akan terangkut dengan cepat ke daun mengikuti alur
umumnya terjadi didaun walaupun metabolism nitrogen juga terjadi pada akar
tanaman (http://worldplant.multiply.com/journal/item/13).
2.4.2. Peranan Unsur Hara Nitrogen
Nitrogen (N) telah dikenal bertanggung jawab untuk pertumbuhan vegetative
yang lebat dan warna daun yang hijau gelap setelah ditetapkannya sebagai suatu unsur
mineral yang esensial untuk tanaman berakar pada tahun 1800-an. Cukupnya Nitrogen
untuk tanaman mendorong pertumbuhan vegetatif bagian diatas tanah, meningkatkan
rasio pucuk/akar, dan essensial untuk pembentukan buah dan biji. Sebagai suatu anasir
esensial asam amino, Nitrogen dibutuhkan dalam sintesis protein, merupakan 12-19%
dan berbagai protein dengan rata-rata sekitar 16% atas dasar berat. Karena
pembentukan biji tergantung pada kadar kritik tertentu protein, produksi biji secara
nyata berhubungan dengan pasokan Nitrogen, terutama pada tanaman-tanaman
serealia. Berlimpahnya Nitrogen dalam medium pertumbuhan juga tercermin dalam
kadar protein kasar dari biji dan dalam hijauan. Di antara unsur-unsur mineral esensial
untuk pertumbuhan dan reproduksi tanaman-tanaman hijau tingkat tinggi, terdapat
lebih banyak atom Nitrogen dalam bahan organik kering daripada tiap unsur lainnya
yang berasal dari tanah. Berdasarkan massa, Nitrogen dalam bahan tanaman sering
dijumpai dalam jumlah yang lebih banyak daripada masing-masing unsur yang
Dengan mengingat berlimpahnya Nitrogen dalam tanaman, peranan sentralnya
dalam fungsi tanaman dan reaktivitasnya dalam biosfer, tidaklah mengherankan jika
unsur ini merupakan yang paling universal kahat untuk produksi tanaman yang
optimum (Engelstad, O.P. 1997).
Nitrogen merupakan unsur hara utama bagi pertumbuhan tanaman, yang pada
umumnya sangat diperlukan untuk pembentukan atau pertumbuhan bagian-bagian
vegetative tanaman, seperti daun, batang dan akar.
Fungsi Nitrogen yang selengkapnya bagi tanaman adalah:
1. Untuk meningkatkan pertumbuhan tanaman
2. Dapat menyehatkana pertumbuhan daun, daun tanaman lebar dengan
warna yang lebih hijau
3. Meningkatkan kadar protein dalam tubuh tanaman
4. Meningkatkan kualitas tanaman penghasil daun-daunan
5. Meningkatkan berkembangbiaknya mikro-organisme di dalam tanah.
Sebagaimana deiketahui hal itu penting sekali bagi kelangsungan
pelapukan bahan organis ( Sutedjo,M.M. 1999 )
Nitrogen juga merupakan komponen utama dalam tubuh tanaman, terutama
dalam protoplasma sel, protein, asam amino, amida, dan alcohol. Juga berperan pada
pertumbuhan vegetatif, warna, panjang umur tanaman, dan penggunaan karbohidrat
2.4.3. Gejala Defisiensi Unsur Hara Nitrogen
Menurut Yan Fauzi (2008) gejala defisiensi unsur hara Nitrogen pada tanaman
kelapa sawit adalah:
1. Warna daun menjadi kuning pucat
2. Pada kondisi buruk, jaringan daun menjadi kering dan mati
3. Helaian daun menjadi pendek dan keras
4. Pertumbuhan tanaman terhambat dan kerdil
Defisiensi Nitrogen biasanya diketahui pertama melalui warna hijau pucat atau
hijau-kekuningan, terutama pada rumput-rumputan, dan nekrosisi premature dari
daun-daun yang lebih tua, mulai dari pucuk dan menyebar sepanjang tulang daun
kearah leher batang dan tepi daun. Asosiasi dengan pewarnaan hijau ini
berkemungkinan disebabkan oleh kenyataan bahwa Nitrogen bersama-sama Mg,
merupakan satu dari dua anasir penyusun klorofil. Kekurangan Nitrogen
menyebabkan khlorosisi pada daun muda berwarna kuning dan partumbuhan tertekan.
2.5. Analisis Titrimetri
Analisis titrimetri mengacu pada analisis kimia kuantitatif yang dilakuka n
dengan menetapkan volume suatu larutan yang konsentrasinya diketahui dengan tepat
, yang diperlukan untuk bereaksi secara kuantitatif dengan larutan dari zat yang akan
ditetapkan. Larutan dengan kekuatan ( konsentrasi) yang diketahui tepat itu, disebut
larutan standar. Bobot zat yang hendak ditetapkan, dihitung dari volume larutan
standard yang digunakan dan hukum-hukum stoikiometri yang diketahui.
Larutan standard biasanya ditambahkan dari dalam sebuah buret. Proses
penambahan larutan standar sampai reaksi tepat lengkap, disebut titrasi, danzat yang
akan ditetapkan, dititrasi. Titik pada mana reaksi itu tepat lengkap, disebut titik
ekuivalen (setara) atau titik akhir teoritis (atau titik akhir steokiometri ). Lengkapnya
titrasi, lazimnya harus terdeteksi oleh suatu perubahan, yang tak dapat disalah lihat
oleh mata, yang dihasilkan oleh larutan standar itu sendiri. Pada titrasi yang ideal, titik
akhir yang terlihat, akan terjadi berbarengan dengan titik titik akhir stoikiometri atau
teoriti. Namun dalam prakteknya, biasanya akan terjadi perbedaan yang sangat sedikit.
Ini merupakan sesatan (error) titrasi. Indikator dan kondisi-kondisi eksperimen harus
dipilih sedemikian, sehingga perbedaan antara titik akhir terlihat dan titik ekuivalen,
adalah sekecil mungkin.
Untuk digunakan dalam analisis titrimetri, suatu reaksi harus memenuhi
kondisi-kondisi berikut:
1. Harus ada suatu reaksi yang sederhana, yang dapat dinyattakan dengan
dengan dengan reagensia dalam proporsi yang stoikiometrik atau
ekuivalen.
2. Reaksi harus praktis berlangsung dalam sekejap atau berjalan dengan
sangat cepat sekali (kebanyakan reaksi ionic memenuhi kondisi ini). Dalam
beberapa keadaan, penambahan suatu katalis akan menaikkkan kecepatan
reaksi itu.
3. Harus ada perubahan yang menyolok dalam energy bebas, yang
menimbulkan perubahan dalam sifat fisika atau kimia larutan pada titik
ekuivalen.
4. Harus tersedia suatu indicator, yang oleh perubahan sifat-sifat fisika
(warna atau pembentukan endapan), harus dengan tajam menetapkan titik
akhir titrasi.
Metode titrasi lazimnya dapat dipakai untuk ketelitian yang tinggi (1 bagian
dalam 1000) dan memiliki beberapa keuntungan, dimana ia dapat diterapkan,
melebihui metode-metode gravimetric. Metode-metode ini memerlukan peralatan
yang lebih sederhana, dan umumnya cepat dikerjakan, pemisahan yang menjemukan
dan sukar sering dapat dihindari.
Reaksi penetralan, atau asidimetri dan alkalimetri. Ini melibatkan titrasi basa
bebas, atau basa yang terbentuk karena hidrolisis garam yang berasal dari asam lemah,
Volumetri atau titrimetri merupakan suatu metode analisis kuantitatif
didasarkan pada pengukuran volume titran yang bereaksi sempurna dengan analit.
Titran merupakan zat yang digunakan untuk mentitrasi. Analit adalah zat yang akan
ditentukan konsentrasi/kadarnya.
Standar primer
Larutan titran haruslah diketahui komposisi dan konsentrasinya. Idealnya kita
harus memulai dengan larutan standar primer. Larutan standar primer dibuat dengan
melarutkan zat dengan kemurnian yang tinggi (standar primer) yang diketahui dengan
tepat beratnya dalam suatu larutan yang diketahui dengan tepat volumnya. Apabila
titran tidak cukup murni, maka perlu distandardisasi dengan standar primer. Standar
yang tidak termasuk standar primer dikelompokkan sebagai standar sekunder,
contohnya NaOH; karena NaOH tidak cukup murni (mengandung air, natrium
karbonat dan logam-logam tertentu) untuk digunakan sebagai larutan standar secara
langsung, maka perlu distandardisai dengan asam yang merupakan standar primer
misal: kalium hidrogen ftalat (KHP).
Persyaratan standar primer
1. Kemurnian tinggi
2. Stabil terhadap udara
3. Bukan kelompok hidrat
4. Tersedia dengan mudah
5. Cukup mudah larut
6. Berat molekul cukup besar
1. Cukup stabil sehingga penentuan konsentrasi cukup dilakukan sekali
2. Bereaksi cepat dengan analit sehingga waktu titrasi dapat dipersingkat
3. Bereaksi sempurna dengan analit sehingga titik akhir yang memuaskan dapat
dicapai
4. Melangsungkan reaksi selektif dengan analit
Keakuratan hasil metode titrasi amat bergantung pada keakuratan penentuan
konsentrasi larutan standar. Untuk menentukan konsentrasi suatu larutan standar dapat
digunakan 2 cara:
1. Dengan cara langsung, menimbang dengan tepat standar primer, melarutkannya
dalam pelarut hingga volume tertentu
2. Dengan standarisasi, yaitu titran yang akan ditentukan konsentrasinya digunakan
untuk mentitrasi standar primer/sekunder yang telah diketahui beratnya
Titrasi balik (back-titration)
Terkadang suatu reaksi berlangsung lambat dan tidak dapat diperoleh titik
akhir yang tegas. Untuk itu metoda titrasi balik dapat digunakan untuk mengatasinya.
Caranya dengan menambahkan titran secara berlebih, setelah reaksi dengan analit
berjalan sempurna, kelebihan titran ditentukan dengan menitrasi dengan larutan
standar lainnya. Dengan mengetahui mmol titran dan menghitung mmol yang tak
bereaksi, akan diperoleh mmol titran yang bereaksi dengan analit
BAB 3
METODOLOGI PERCOBAAN
3.2. Alat
1. Timbangan analitik Mettler Toledo
2. Mesin giling listrik daun Bra Blender
3. Penangas listrik khusus tabung reaksi Techne
4. Tabung reaksi Pyrex
5. Kjeltec 2200 Auto Destilation FOSS
6. Pipet volume Pyrex
7. Gelas beaker 250 ml Pyrex
8. Oven pengering Gallenhamp
9. Tabung destilasi Pyrex
10.Spatula
11.Desikator
12.Kertas saring whatman No. 40
13.Bola karet
14.Botol akuades
15.Botol plastik bertutup 20 ml
16.Rak botol plastik
17.Corong plastik
18.Rak tabung reaksi
3.3. Bahan
1. H2SO4 pekat p.a
2. H2O2 30 % p.a
3. Akuades
4. Larutan indikator campuran
Ditimbang 0,2 g Methyl red kemudian dilarutkan dengan Alkohol 95% dalam
labu ukur 100 mL dan 0,1 g Bromcresol green dilarutkan dalam Alkohol 95%
dalam labu ukur 100 mL. Campurkan 100 mL Bromcresol green dengan 34
mL Methyl red.
5. Larutan Asam Borat (H3BO3) 3%
Ditimbang 3 g H3BO3 dan dimasukkan kedalam labu ukur 100 mL.Tambahkan
±50 mL air destilasi, lalu dipanaskan hingga H3BO3 larut sempurna, setelah
dingin penuhkan dengan air destilat hingga tanda garis, lalu dihomogenkan.
6. Larutan Asam klorida (HCl) 0,01 N
Larutan HCl 0,1 N
Pipet 8,3 mL HCl 37% p.a kemudian diencerkan dengan air destilasi hingga 1
Ditimbang 15 g NaOH Kristal kemudian dilarutkan dengan air destilasi dalam
labu takar 100 mL.
3.4. Persiapan Contoh Daun Kering
3.4.1. Membersihkan Contoh Daun Kelapa Sawit
Contoh yang diterima di laboratorium terlebih dahulu dicatat dan diberi
nomor laboratorium secara beraturan. Contoh segera dibersihkan dengan kapas
yang telah dibasahi air destilasi. Bagian tulang yang kasar dibuang dengan
gunting. Begitu juga dengan bagian pinggir daun terutama daun yang agak
lebar digunting dan dibuang. Kemudian contoh daun dimasukkan kedalam
kain kelambu ukuran 15 x 30 cm dan disertai label nomor laboratorium.
3.4.2.Mengeringkan dan Menggiling Contoh Daun Kelapa Sawit
Contoh daun yang sudah bersih di dalam kantongan kelambu
dikeringkan dalam oven pengering pada suhu 105 oC ± 2 jam sampai contoh
daun menjadi kering dengan indikasi terasa rapuh bila diremas dengan tangan.
Contoh daun kering digiling dengan mesin giling listrik menggunakan
saringan kehalusan 35 mesh. Contoh daun yang sudah halus dimasukkan
3.5. Prosedur Destruksi Basah (H2SO4 + H2O2) Daun Kelapa Sawit
1. Ditimbang 0,1 g contoh kering mutlak 1050 C, lalu dimasukkan kedalam
tabung reaksi 20 mL.
2. Ditambahkan 1 mL H2SO4 pekat dan 0,5 mL H2O2 30%, digoyang
perlahan-lahan. Larutan contoh didestruksi menggunakan penangas listrik khusus untuk
tabung reaksi, suhu dinaikkan perlahan-lahan sampai dengan ± 1800 C. Contoh
akan menjadi hitam dan agak berbuih. Bila larutan contoh sudah tidak berbuih
lagi, tabung diangkat dan didinginkan.
3. Setelah dingin kemudian ditambah 0,5 mL H2O2 30% dan didestruksi kembali.
Penambahan H2O2 30% diulangi sampai larutan contoh menjadi bening dan
destruksi disempurnakan pada suhu 2800 C selama ± 15 menit. Tabung reaksi
diangkat dan didinginkan.
4. Larutan diencerkan dengan air destilat kedalam labu ukur 100 mL, kemudian
disaringan dengan menggunakan kertas saring whatman No. 40 kedalam botol
platik 100 mL.
5. Filtrat digunakan untuk penetapan N, P, K, Ca dan Mg.
3.6. Prosedur Penetapan Nitrogen (N) Pada Daun Kelapa Sawit
1. Pipet 20 mL filtrat hasil destruksi contoh daun dalam H2SO4 pekat dan H202
30% (destruksi basah), kemudian dimasukkan kedalam tabung destilasi dan
diletakkan pada alat destilasi. Alat destilasi secara otomatis akan
menambahkan 3 mL larutan NaOH 15% kedalam tabung destilasi.
2. Destilat ditampung kedalam Erlenmeyer 250 mL yang berisi 5 mL Asam borat
serta larutan indikator campuran.
3. Destilasi dilakukan selama ± 3 menit
4. Destilat dititrasi dengan HCl 0,01 N hingga warna larutan menjadi merah
jambu
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil dan Analisa Data
Hasil analisa Nitrogen (N) daun Kelapa Sawit terdapat pada table berikut:
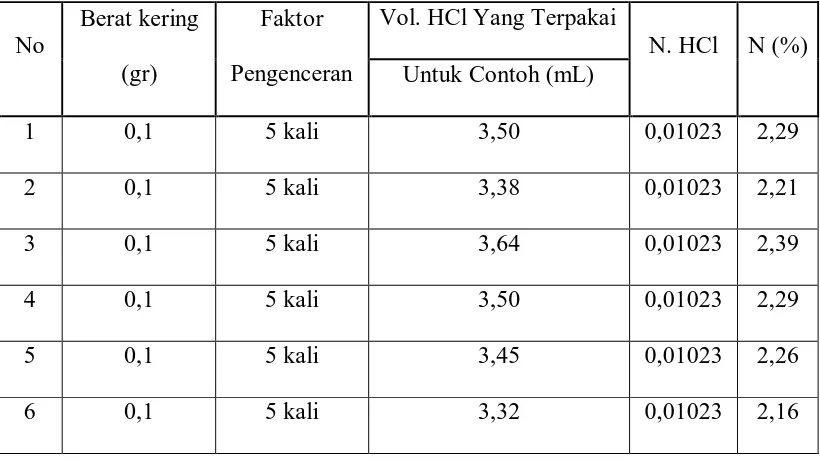
Tabel 4.1. Data Analisa Nitrogen (N)
No
Berat kering
(gr)
Faktor
Pengenceran
Vol. HCl Yang Terpakai
N. HCl N (%)
Volume HCl yang terpakai untuk blanko = 0,30 mL
4.2. Perhitungan
Standard Deviasi ( σ) = √σ2
= 8
= 0,076
4.3.Pembahasan
Dari hasil analisa daun kelapa sawit di laboratorium diperoleh kadar
Nitrogen adalah 2,267±0,076 %. Ketersediaan akan Nitrogen dalam tumbuhan kelapa
sawit semakin lama akan semakin berkurang. Hilangnya atau berkurangnya
ketersediaan hara Nitrogen didalam daun sangat di pengaruhi oleh berbagai faktor
yang berawal dari dalam tanah seperti daya serap akar, banyaknya bahan organik,
populasi jasad renik, iklim, karena proses panen, dan proses pencucian akibat hujan,
jenis tanah dan sebagainya. Adanya proses panen mengakibatkan unsur hara tersebut
berpindah secara langsung melalui pemangkasan daun dari pemanenan tandan. Pada
proses pencucian, kadar unsur hara yang hilang bervariasi bergantung pada tipe tanah
dan intensitas curah hujan. Pencucian dapat dikurangi dengan cara menanam tanaman
penutup lahan dengan baik atau mencegah aliran air yang deras. Tanah yang
Nitrat sangat mudah larut dalam tanah sehingga cepat hilang karena proses
pembusukan. Taraf ketersediaan nitrogen dalam tanah tergantung pada banyaknya
bahan organik, populasi jasad renik, tingkat pembasuhan. Dlm keadaan alami terjadi
keseimbangan antara laju pertumbuhan dan gaya-gaya yangg menentukan penyediaan
nitrogen dalam tanah. Pemanenan menyebabkan terkurasnya nitrogen karena
pengambilan bahan organik dan erosi. Hal ini menyebabkan pertanian intensif sangat
tergantung pada tambahan pupuk nitrogen
Nitrogen memegang peranan sentral dalam pertanian modern. Nitrogen
adalah suatu hara esensial dan juga merupakan hara pembatas utama pada sebagian
besar tanah pertanian yang ditanami tanaman-tanaman bukan legum. Kebutuhan
Nitrogen tanaman terlibat dalam penentuan kebutuhan pupuk Nitrogen. Karena
tanaman adalah konsumen Nitrogen utama dan mengasimilasi sejumlah 30 sampai
70% dari Nitrogen pupuk yang diberikan. Jadi penggantian unsur hara atau
pemupukan harus dilakukan sebelum tanaman menunjukkan gejala defisiensi hara.
Selain itu, perlu diperhatikan perubahan-perubahan tanah akibat pengelolaan tanaman.
Tanah perkebunan yang dipupuk terus-menerus selama berpuluh tahun akan
mengalami degradasi , bias membuat pemupukan tidak respon terhadap tanaman.
Pupuk yang biasa digunakan untuk menambahn Nitrogen adalah pupuk Sulphat of
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari hasil percobaan yang telah dilakukan diperoleh kadar N dalam daun
kelapa sawit adalah sebesar 2,267±0,076 %.
5.2. Saran
Agar dilakukan pemupukan terhadap tanaman kelapa sawit sesuai
rekomendasi yang ditelah ditentukan dari hasil analisa unsur Nitrogen. Dimana pupuk
diberikan dengan kadar yang optimum. Pemupukan harus dilakukan sebelum tanaman
menunjukkan gejala defisiensi hara sehingga tidak akan menimbulkan kerugian yang
DAFTAR PUSTAKA
Engelstad, O. P. 1997. Teknologi Dan Penggunaan pupuk. Edisi Ke – 3. UGM-
Press. Yogyakarta.
Fauzi, Y. 2008. Kelapa Sawit , Edisi revisi. Penerbit Penebar Swadaya. Jakarta.
http://blog.unila.ac.id/widiarto/files/2009/10/volumetri.pdf.
http://id. Wikipedia.org/wiki/Nitrogen.
http://worldplant.multiply.com/journal/item/13
Pahan, I. 2006. Panduan Lengkap Kelapa Sawit. Penebar Swadaya. Jakarta.
Sitompul, S. M, dan Bambang G. 1995. Analisis Pertumbuhan Tanaman.
Penerbit UGM-Press. Yogyakarta.
Sutedjo, M. M. 1987. Pupuk Dan Cara Pemupukan. Penerbit Rineka Cipta.
Jakarta.
Tim Bina Karya Tani. 2009. Pedoman Bertanam Kelapa Sawit. Penerbit Yrama
Widya. Bandung.
Vogel. 1994. Kimia Analisis Kuantitatif Anorganik. Edisi Ke-4. Penerbit Buku
Kedokteran-EGC. Jakarta.
Tabe 1. Data Hasil Analisa Nitrogen
No Berat kering (gr)
Faktor Pengenceran
Vol. HCl Yang Terpakai
N. HCl N (%) Untuk Contoh (mL)
1 0,1 5 kali 3,50 0,01023 2,29 2 0,1 5 kali 3,38 0,01023 2,21 3 0,1 5 kali 3,64 0,01023 2,39 4 0,1 5 kali 3,50 0,01023 2,29 5 0,1 5 kali 3,45 0,01023 2,26 6 0,1 5 kali 3,32 0,01023 2,16
BAGAN PROSES ANALISA NITROGEN
Penyaringan dengan kehalusan 35 mesh
Berat sampel (gr)
Dititrasi dengan HCl 0,01 N Penggilingan
Destruksi H2SO4 + H2O2
Didestilasi Pengeringan pada suhu
105 0C
PROSES PENENTUAN KADAR NITROGEN
DALAM DAUN KELAPA SAWIT
Didestruksi dengan H2SO4 + H2O2
Hasil destruksi diencerkan dengan aquadest
dalam labu ukur 100 mL
Dipipet sebanyak 20 mL dan dimasukkan keda-
lam tabung destilasi, kemudian didestilasi
selama ± 3 menit
Destilat ditampung dalam Erlenmeyer yang
berisi 5 mL asam borat dan indikator campuran
Dititrasi dengan HCl 0,01 N
0,1 g contoh daun kering