ANALISA UNSUR HARA FOSFOR (P) PADA DAUN KELAPA SAWIT DENGAN METODE DESTRUKSI BASAH
SECARA SPEKTROFOTOMETRI DI PUSAT PENELITIAN KELAPA SAWIT (PPKS) MEDAN
Diajukan Untuk Melengkapi Tugas dan Memenuhi Syarat Memperoleh Gelar Ahli Madya
MARA FAJAR AMIN LUBIS 062401008
PROGRAM STUDI D3 KIMIA ANALIS DEPARTEMEN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA MEDAN
ANALISA UNSUR HARA FOSFOR (P) PADA DAUN KELAPA SAWIT DENGAN METODE DESTRUKSI BASAH
SECARA SPEKTROFOTOMETRI DI PUSAT PENELITIAN KELAPA SAWIT (PPKS) MEDAN
KARYA ILMIAH
MARA FAJAR AMIN LUBIS 062401008
PROGRAM STUDI D 3 KIMIA ANALIS DEPARTEMEN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA MEDAN
PERSETUJUAN
Judul : ANALISA UNSUR HARA FOSFOR (P) PADA
DAUN KELAPA SAWIT DENGAN METODE DESTRUKSI BASAH SECARA SPEKTRO-FOTOMETRI DI PUSAT PENELITIAN KELAPA SAWIT (PPKS) MEDAN
Kategori : TUGAS AKHIR
Nama : MARA FAJAR AMIN LUBIS
NIM : 062401008
Program Studi : D3 KIMIA ANALIS
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di : Medan, Juli 2009
Diketahui/Disetujui Oleh :
Departemen Kimia FMIPA USU
Ketua , Dosen Pembimbing
PERNYATAAN
ANALISA UNSUR HARA FOSFOR (P) PADA DAUN KELAPA SAWIT DENGAN METODE DESTRUKSI BASAH SECARA SPEKTROFOTOMETRI
DI PUSAT PENELITIAN KELAPA SAWIT (PPKS) MEDAN
KARYA ILMIAH
Saya mengakui bahwa Karya Ilmiah ini adalah hasil kerja saya sendiri. Kecuali beberapa kutipan dari ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juli 2009
PENGHARGAAN
Puji dan syukur penulis haturkan kehadirat Allah SWT yang mencurahkan rahmat, berkah dan hidayahNya kepada penulis sehingga dapat menyelesaikan perkuliahan dan penulisan karya ilmiah ini yang merupakan salah satu syarat guna menyelesaikan Studi Program Diploma 3 pada Fakults Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara. Semoga niat dan amalan ini dapat dinilai sebagai ibadah. Shalawat dan salam penulis panjatkan kepada junjungan Nabi besar Muhammad SAW yang syafaatnya kita harapkan d kemudian hari.
Karya ilmiah ini ditulis berdasarkan pengamatan penulis selama melaksanakan Praktek Kerja Lapangan (PKL) di Pusat Penelitian Kelapa Sawit (PPKS) Medan, dengan judul “ ANALISA UNSUR HARA FOSFOR (P) PADA DAUN KELAPA SAWIT DENGAN DESTRUSKI BASAH SECARA SPEKTROFOTOMETRI”.
Selesainya Karya Ilmiah ini juga tidak lepas dari bantuan dan bimbingan dari berbagai pihak. Oleh karena itu dengan kerendahan hati penulis mengucapkan terima kasih yang sebesar-besarnya :
1. Orang tua tercinta Ibunda Hj.Masdinar dan Ayahanda H.Abd. Shomad Lubis yang telah memberikan do’a restunya yang tiada terhingga, dan telah banyak memberikan pengorbanan moril maupun materil serta kesabaran yang tulus, serta seluruh keluarga saya yang telah memberikan dukungan kepada penulis. 2. Ibu Dr.Rumondang MS, selaku Ketua Departemen Kimia FMIPA USU, dan
sekaligus sebagai dosen pembimbing yang telah banyak meluangkan waktu dalam memberikan bimbingan kepada penulis.
3. Ibu Dr,Marpongahtun,M.Sc selaku Ketua Program Studi D3 Kimia Analis 4. Bapak Drs.EkaNuryanto,MSi, yang telah meluangkan waktu dan membimbing
penulis dalam penulisan laporan PKL dan Karya Ilmiah ini.
5. Bapak Baharuddin AR,B.Sc, selaku penanggung jawab laboratorium tanah dan daun, seluruh karyawan PPKS Medan khususnya laboratorium tanah dan daun terima kasih atas dukungan dan bantuannya kepada penulis.
6. Kawan-kawan kost sei padang 72 yang telah memberikan bantuan kepada penulis.
7. Rekan-rekan mahasiswa/I Kimia Analis D-3 angkatan 2006 sekaligus sahabat-sahabat yang lain yang tidak dapat saya sebutkan satu persatu yang telah memberikan dukungan sehingga penulis dapat menyelesaikan karya ilmiah ini. Penulis menyadari bahwa karya ilmiah ini masih jauh dari kesmpurnaan dalam materi dan penyajian. Untuk itu penulis mengharapkan saran dan kritik ytang brsifat membangun dari semua pihak yang dapat menjadi bahan masukan bagi penulis. Semoga penulisan karya ilmiah ini dapat bermanfaat bagi kita semua, Amin.
Medan, Juli 2009
ABSTRAK
ANALYSIS ELEMENT OF HARA PHOSPHORUS (P) AT PALM LEAF WITH WET DESTRUCTION METHOD BY SPEKTROFOTOMETRI
IN INDONESIA OIL PALM RESEARCH INSTITUTE (PPKS) MEDAN
ABSTRACT
DAFTA ISI
PERSETUJUAN i
PERNYATAAN ii
PENGHARGAAN iii
ABSTRAK iv
ABTRACT v
DAFTAR ISI vi
DAFTAR TABEL viii
BAB 1 PENDAHULUAN 1
2.3.1. Kesatuan Contoh Daun (KCD) 7
2.3.2. Susunan Letak Daun Kelapa Sawit 9 2.4. Pengambilan Contoh Daun Tanaman Muda Kelapa Sawit 9 2.4.1. Syarat Dalam Pengambilan Contoh Daun Kelapa Sawit 10 2.5. Unsur Hara Pada Tanaman Kelapa Sawit 11
2.6. Serapan Daun 11
2.7. Fosfor 12
2.7.1. Sejarah Fosfor 12
2.7.2. Bentuk Fosfor 12
2.7.3. Sifat-sifat Fosfor 13
2.8. Manfaat Fosfor Pada Tanaman 13
2.9. Gejala Kekurangan Unsur Hara Fosfor Bagi Tanaman 14
2.10. Spektrofotometri 15
2.10.1. Teori Spektrofotometri 15
2.10.2. Prinsip Kerja Alat Spektrofotometri 19 2.10.3. Permasalahan Spektrofotometri 20
BAB 3 METODOLOGI PERCOBAAN 21
3.1. Alat 21
3.2. Bahan 22
3.3. Persiapan Contoh Daun Kering 23
3.3.1. Membersihkan Contoh Daun Tanaman Kelapa Sawit 23
3.3.2. Mengeringkan dan Menggiling 23
3.4. Prosedur Destruksi Basa (HNO3 + HClO4) Daun Kelapa Sawit 24 3.5. Prosedur Penetapan Fosfor (P) Daun Kelapa Sawit Secara
Spektrofotometri UV-Visible 24
BAB 4 HASIL DAN PEMBAHASAN 27
4.1. Hasil 27
4.2. Perhitungan 28
4.2.1. Penentuan Persamaan Garis Regresi 28
4.2.2. Mencari Konsentrasi Sampel 29
4.2.3. Menghitung Kadar Fosfor (P) Daun Kelapa Sawit 30
4.3. Pembahasan 32
BAB 5 KESIMPULAN DAN SARAN 34
4.1. Kesimpulan 34
4.2. Saran 34
DAFTAR TABEL
Tabel 4.1. Data Absorbansi Larutan P Standar 27
Tabel. 4.2. Absorbansi P-Grafik Berat Contoh 27
ABSTRAK
ANALYSIS ELEMENT OF HARA PHOSPHORUS (P) AT PALM LEAF WITH WET DESTRUCTION METHOD BY SPEKTROFOTOMETRI
IN INDONESIA OIL PALM RESEARCH INSTITUTE (PPKS) MEDAN
ABSTRACT
BAB 1 PENDAHULUAN
1.1. Latar Belakang
Kebutuhan unsur hara untuk tanaman kelapa sawit biasanya diduga melalui analisis dari bahan panen dan daun batang sebagai pedoman yang mudah untuk dapat memberikan indikasi kebutuhan unsur hara buatan tanaman kelapa sawit adalah dari hasil analisis daun.
Hal ini disebabkan karena daun merupakan bagian yang paling efektif dari tanaman. Dari hasil analisis daun akan dapat diperoleh petunjuk secara kuantitatif unsur hara yang diserap oleh tanaman baik yang berasal dari tanah, air hujan, dan pupuk yang ditambahkan.
Interpretasi hasil analisis daun secara nyata dapat menunjukkan defisiensi yang terjadi dengan membandingankan angka tarif krisis untuk daun kelapa sawit. Dari angka hasil analisis daun yang diperoleh dari laboratorium kemudian dibandingkan dengan angka tarif krisis, maka akan dapat disimpulkan gejala kekurangan unsur hara tertentu.
Berdasarkan uraian di atas maka dilakukan analisa unsur hara Fosfor pada daun kelapa sawit dengan metode destruksi basah secara spektrofotometri.
1.2. Permasalahan
Beberapa jumlah kadar unsur hara Fosfor yang dibutuhkan oleh tanaman kelapa sawit untuk menghindari tanah kekurangan Fosfor dapat ditentukan berapa banyak pupuk Fosfor yang harus diberikan pada tanaman sehingga diperoleh pertumbuhan yang cepat dan hasil buah yang maksimal.
1.3. Tujuan
Adapun tujuan penulisan karya ilmiah ini adalah :
Mengetahui tingkat kesuburan tanaman kelapa sawit berdasarkan unsur hara Fosfor pada daun kelapa sawit secara spektrofotometri yang berguna untuk meningkatkan kualtitas tanaman kelapa sawit.
1.4. Manfaat
BAB 2
TINJAUAN PUSTAKA
2.1. Kelapa Sawit
Berdasarkan bukti-bukti yang ada, kelapa sawit diperkirakan berasal dari Nigeria, Afrika Barat. Namun ada pula yang menyatakan bahwa tanaman tersebut dari Amerika yakni dari Brazilia. Zeven menyatakan bahwa tanaman kelapa sawit berasal dari daratan tersier, yang merupakan daratan penghubung yang terletak antara Afrika dan Amerika. Kedua daratan ini kemudian terpisah oleh lautan menjadi banua Afrika dan Amerika sehingga tempat asal komoditas kelapa sawit ini tidak lagi dipermasalahkan orang.
Kelapa sawit (Elaeis guineesis) saat ini telah bekembang pesat di Asia Tenggara, khususnya Indonesia dan Malaysia, dan justru bukan di Afrika barat atau Amerika yang dianggap sebagai daerah asal-usulnya. Masuknya bibit kelapa sawit ke Indonesia pada tahun 1948 hanya sebanyak 4 batang yang berasal dari Bourbon (Mauritius) dan Amsterdam. Keempat batang bibit kelapa sawit tersebut ditanam di Kebun Raya Bogor dan selanjutnya disebarkan ke Deli Sumatera Utara.
2.2. Perkebunan Kelapa Sawit
Menurut Hunger (1924) pada tahun 1869 Pemerintah Kolonia Belanda mengembangkan tanaman kelapa sawit di Muara Enim pada tahun 1970 di Musi Hulu.
Pada masa penjajahan Jepang 1942, pemerintah pendudukan meneruskan perkebunan kelapa sawit ini dan hasilnya dikirim ke Jepang sebagai bahan mentah industri perang. Kemudian semua terhenti karena terjadinya serangan sekutu pada tahun 1943.
Pada tahun 1947 Pemerintah Belanda merebut kembali dua pertiga dari perkebunan yang pernah dikuasai kelaskaran. Kemudian menjelang akhir tahun 1948 maskapai-maskapai perkebunan asing hampir memperoleh perkebunan mereka masing-masing dan menjadi milik mereka kembali.
Pada akhir tahun 1957 seluruh perusahaan milik maskapai Belanda diambil alih oleh Pemerintah Indonseia. Namun milik perusahaan Inggris, Prancis, Belgia, dan Amerika dikembalikan lagi kepada miliknya pada akhir Desember 1967.
Pada masa pemerintahan Orde Lama relatif perkebunan sawit sangat terlantar, karena tidak ada peremajaan dan rehabilitasi pabrik. Akibatnya produksi sangat menurun drastis dan kedudukan Indonesia di dipasar internasional sebagai pemasok minyak sawit nomor satu terbesar sejak tahun 1966 telah digeser oleh Malaysia hingga sekarang ini.
Pada masa Orde baru telah mulai membangun kembali perkebunan kelapa sawit secara besar-besaran dengan mengadakan peremajaan dan penanaman baru. Selanjutnya pemerintah telah bertekad pula membangun perkebunan kelapa sawit dengan mengembangkan melalui berbagai pola.
pengembangan perkebunan besar kelapa sawit dilakukan dengan pola PIR, (Risza,S.1994).
2.3. Daun Kelapa Sawit
Daun (folium) pertama yang keluar pada stadia bibit adalah berbentuk anceolate, kemudian muncul bifurcate dan menyusul bentuk pinnate. Pada bibit yang
berumur 5 bulan misalnya akan dijumpai 5 lanceolate, 4 bifurcate dan 3 pinnate. Pada 12 bulan akan ada 5 anceolate, 4 bifurcate dan 10 pinnate. Pangkal pelepah daun atau petiole adalah bagian daun yang mendukung atau tempat duduknya helaian daun .
Daun kelapa sawit memiliki rumus daun 1/8, lingkaran atau spiralnya ada yang berputar kekiri dan kekanan tetapi kebanyakan putar kekanan. Pengenalan ini penting diketahui agar kita dapat mengetahui letak daun ke-9, ke-17 dan lain-lain yang dipakai sebagai standar pengukuran pertumbuhan maupun pengambilan contoh daun dan pengamatan lainnya. Produksi pelepah daun tergantung pada umur tanaman. Produksi pelepah daun pada tanaman selama setahun dapat mencapai 20-30 kemudian akan berkurang sesuai umur menjadi 18-25 atau kurang. Panjang cabang daun diukur dari pangkalnya dapat mencapai 9 m pada tanaman dewasa sedang pada tanaman muda kurang dari pangkal tersebut. Panjang pelepah ini dapat bervariasi tergantung pada tipe varitasnya dan pengaruh kesuburan tanah. Pada tiap pelepah diisi oleh anak daun di kiri kanan rachis. Jumlah anak daun pada tiap isi dapat mencapai 125-200. anak daun yang tengah dapat mencapai panjang1,2 m. Berat satu pelepah dapat mencapai 4,5 kg berat kering, (Adlin,U,L.2008).
berbetuk bulu. Susunan daun kelapa sawit mirip dengan kelapa (nyiur), yaitu membentuk daun menyirip. Letak daun pada batang mengikuti pola tertentu yang disebut filotaksis. Daun yang berurutan dari bawah ke atas membentuk suatu spiral, dengan rumus daun 1/8. Terdapat dua pola filotaksis, yang secara sederhana dapat dikatakan yang satu berputar kekiri, dan yang lain berputar kekanan, dimana menunjukkan secara umum jumlah pohon yang jumlah filotaksisnya berputar kekiri tidak berbeda dengan yang ke kanan, dan produktivitas pohon dengan kedua pola ini pun tidak berbeda nyata. Hal ini berbeda dengan pendapat beberapa pakar mengenai mengenai kalapa nyiur (cocos nucifera), yang kecendrungannya lebih banyak pohon yang berpola filotaksis ke kiri, dan yang filotaksisnya ke kiri produktivitasnya dapat 20% lebih tinggi ketimbang yang kekanan. Sebenarnya pola filotaksis pada kelapa sawit sangat rumit dan memiliki genetis.
Daun terdiri atas tangkai daun (petiole) yang pada kedua tepinya terdapat dua baris duri (spines). Tangkai daun bersambung dengan tulang daun utama (rachis), yang jauh lebih panjang dari tangkai dan pada kiri kanannya terdapat anak-anak daun (pinna;pinnata). Tiap anak daun terdiri atas tulang anak daun (lidi) dan helai daun (lamina). Anak daun terpanjang (pada pertengahan daun) dapat mencapai 250-300 helai per tahun pada pohon-pohon yang berumur 5-6 tahun, setelah itu di produksi daun menurun menjadi 20-25 daun per tahun, (Semangun,H.2003).
Luas permukaan daun tanaman dewasa dapat mencapai 15 meter. Daun kelapa sawit berfungsi sebagai tempat berlangsungnya fotosintesis dan alat respirasi. Oleh karena itu pemangkasan pelepah daun sejauh mungkin dihindarkan, kecuali pangkas pendahuluan dan pangkas pemeliharaan.
Jika pelepah dapat dipertahankan lebih lama berarti semakin lama pula proses fotosintesis berlangsung dan semakin banyak bahan makanan yang dikirim ke buah. Hal ini berarti tandan akan meningkat lebih berat, (Risza,S.1994).
2.3.1. Kesatuan Contoh Daun (KCD)
Kesatuan contoh daun adalah satu unit areal yang dipakai sebagai tempat pengambilan contoh daun dari pokok yang ditetapkan. Unit areal ini harus dapat mewakili suatu luasan yang tertentu yang seragam dalam hal jenis tanah dan kesuburannya, umur tanaman, perlakuan yang diberikan dan memiliki variasi yang kecil dalam hal-hal lainnya. Luasnya tergantung pada keseragaman tanaman dan tanah, misalnya 20, 25, 32, ha sesuai dengan luas blok. Dari tiap KCD dipilih 30 pokok yang memenuhi syarat untuk dipakai sebagai pokok contoh. Untuk mendapat keseragaman yang lebih baik dan mengurangi faktor kebetulan maka dikenal sistim tersebar yang ditetapkan berdasarkan luas dan jumlah pokok. Sebagai contoh untuk areal yang luasnya 20,25, 30 dan 35 ha akan terdapat penyebaran pokok contoh. Pengambilan contoh daun dapat dilakukan dengan dua cara yaitu dengan sistim terpusat dan tersebar.
Disamping cara tersebar ini, terdapat sistim lainnya yaitu sistim terpusat yakni pokok contoh tersebut terkumpul pada 2 atau 3 barisan yang umumnya berada dengan areal yang dianggap mewakili. Sistim ini dipakai kalau kondisi area dan tanaman benar-benar homogen.
Pokok yang dipakai sebagai pokok contoh haruslah memenuhi beberapa ketentuan seperti berikut :
a. Pokok normal
b. Sehat dan tidak terserang penyakit.
c. Tidak dekat dari jalan, parit atau bangunan.
d. Tidak bersebelahan dengan pokok mati atau sisipan
2.3.2. Susunan Letak Daun Kelapa Sawit
Daun ke-9 maupun 17 ditentukan dengan memperhatikan susunan letak daun dapat ditentukan dengan pedoman sebagai berikut :
a. Daun pertama adalah daun termuda, dimana helai daun telah mekar seluruhnya.
b. Daun ke-3 letaknya 274 dari daun yang pertama dihitung dari daun kearah kiri pada tanaman yang mempunyai pusingan spiral ke kanan dihitung kearah kanan pada tanaman yang mempunyai pusingan ke kiri.
c. Daun ke-9 berada dibawah 1 agak kesebelah kiri pada spiral kanan agak kekanan pada pokok yang berspiral kiri.
d. Daun ke-17 letaknya dibawah daun ke-9 agak ke kiri pada pokok yang berspiral kanan dan agak ke kanan pada pokok yang berspiral kiri.
2.4. Pengambilan Contoh Daun Tanaman Muda Kelapa Sawit
Contoh daun diambil mulai jam 7.00-12.00 dan tidak waktu hujan. Dari pelepah daun ke-17 ini diambil masing-masing 3 helai anak daun sebelah kiri dan kanan. Letak anak daun yang diambil ini berada kira-kira diantara 1/2-1/3 bagian dari ujung pelepah atau pada titik ujung permukaan daun bagian atas pelepah.
Helai daun dibersihkan dengan kapas yang dibasahi dengan aquadest, lalu 1/3 dari ujung dan pangkal daun dipotong, sedangkan bagian tengahnya dipakai sebagai contoh setelah dibuang lidinya. Helai daun dari pokok-pokok satu KCD dikumpulkan menjadi satu dan dimasukkan ke dalam kantong plastik dengan label yang berisi : nama kebun, No.KCD, Afdeling, Blok, No.pelepah, tahun tanam, tanggal pengambilan , dan nama petugas pencatat, (Adlin,U.L.2008).
2.4.1. Syarat Dalam Pengambilan Contoh Daun Kelapa Sawit a. Dilakukan minimal 2 buah setelah pemupukan terakhir. b. Tidak dilakukan pada musim kemarau panjang.
c. Tidak dilakukan pada bulan dengan curah hujan lebih dari 400 mm.
d. Untuk dapat membandingkan hasil analisa daun hendaknya pengambilan contoh daun dilakukan pada bulan yang sama setiap tahunnya.
e. Untuk Tandan Buah Masak (TBM) pengambilan contoh daun dilakukan hanya jika diperlukan dan pengambilan contoh daun mulai dapat dilakukan pada 6-12 bulan sesudah penanaman.
f. Pengambilan contoh daun dapat dilakukan oleh tim yang terdapat di setiap afdeling atau divisi yang sebelumnya dilatih oleh lembaga yang terkait.
h. Pembuatan peta Pesatuan Kesatuan Daun (KCD) yang baik akan sangat membantu kelancaran pengambilan contoh daun, (Warta PPKS, 2007).
2.5. Unsur Hara Pada Tanaman Kelapa Sawit
Menurut penelitian, setiap tanaman memerlukan paling sedikit 16 unsur (ada yang menyebut zat) agar pertumbuhannya normal. Dari ke 16 unsur tersebut, tiga unsur yaitu karbon hidrogen, dan oksigen diperoleh dari udara, sedangkan dari 13 unsur lagi disediakan oleh tanah. Jadi tanah sebagai dapur bagi tanaman setidaknya harus tersedia 13 jenis menu agar pertumbuhannya normal. Ke-13 unsur tersebut adalah Nitrogen (N), Fosfor (P), Kalsium (Ca), Kalium (K), Magnesium (Mg), Sulfur atau Belerang (S), Klor (Cl), Ferum (fe), Mangan (Mn), Kuprum atau Tembaga (Cu), Seng (Zn), Boron (B), dan Molibdenum (Mo). Akan tetapi terkadang tanah pun tidak mengandung unsur-unsur tersebut secara lengkap, atau biasa pula terjadi karena sudah habis tersedot.
2.6. Serapan daun
Serapan hara daun baik hara N, P, K, dan Mg oleh bibit kelapa sawit yang ditanam pada medium sub soil tanah typic Hapludult secara umum lebih baik dibandingkan pada penggunaan medium sub soil tanah typic Hapludult. Sementara serapan hara bibit ditanam dengan medium sub soil tanah typic Hapludult memberikan hasil yang paling rendah.
juga memiliki peranan dalam ketersediaan hara dan akan meningkatkan serapan hara bibit, (Warta Vol.11.nomor.1.2003.PPKS Medan).
2.7. Fosfor
Fosfor adalah unsur kimia yang memiliki lambang P dengan nomor atom 15. Fosfor berupa nonlogam, bervalensi banyak, termasuk golongan nitrogen, banyak ditemui dalam batuan Fosfat anorganik dan dalam semua sel hidup tetapi tidak pernah ditemui dalam bentuk unsur bebasnya. Fosfor amatlah reaktif, memancarkan pendar cahaya yang lemah ketika bergabung dengan oksigen, ditemukan dalam berbagai bentuk, dan merupakan unsur penting dalam makhluk hidup. Kegunaan fosfor yang terpenting adalah dalam pembuatan pupuk, dan secara luas digunakan dalam bahan peledak, korek api, kembang api, pestisida, odol, dan deterjen.
2.7.1. Sejarah Fosfor
Unsur ini ditemukan oleh Hannig Brand pada tahun 1669 di Hamburg, Jerman. Dia menemukan unsur ini dengan cara 'menyuling' air urin melalui proses penguapan dan setelah dia menguapkan 50 ember air urin, dia baru menemukan unsur yang dia inginkan. Namanya berasal dari bahasa Latin yaitu phosphoros yang berarti 'pembawa terang karena keunikannya yaitu bercahaya dalam gelap (glow-in-the dark).
2.7.2. Bentuk Fosfor
gesekan. Fosfor hitam mempunyai struktur seperti grafit – atom-atom tersusun dalam lapisan-lapisan heksagonal yang menghantarkan listrik
2.7.3. Sifat-sifat Fosfor
Secara umum Fosfor membentuk padatan putih yang lengket yang memiliki bau yang tak enak tetapi ketika murni menjadi tak berwarna dan transparan. Nonlogam ini tidak larut dalam air, tetapi larut dalam karbon disulfida. Fosfor murni terbakar secara spontan di udara membentuk fosfor pentoksida 2.8. Manfaat Fosfor Pada Tanaman
Fosfor merupakan unsur untuk pertumbuhan di dalam tanaman, berfungsi untuk pembentukan protein, lemak, biji-bijian. Kadar hara P pada daun yang dianalisis tidak menunjukkan adanya perbedaan antara tanaman yang mengalami patah daun. Namun tanaman yang tidak mengalami patah daun juga tidak menunjukkan adanya pola yang jelas. Adapun manfaatnya sebagai berikut :
a. Memacu pertumbuhan akar dan pembentukan sistem perakaran yang baik sehingga tanaman dapat mengambil unsur hara lebih banyak dan pertumbuhan tanaman menjadi sehat serta kuat.
b. Menggiatkan pertumbuhan jaringan tanaman yang membentuk titik tumbuh tanaman.
c. Memacu pembentukan bunga dan masaknya buah/biji, sehingga mempercepat masa panen.
d. Memperbesar persentase terbentuknya bunga menjadi buah dan biji.
2.9. Gejala Kekurangan Unsur Hara Fosfor Bagi Tanaman
Kekurangan salah satu atau beberapa unsur hara akan mengakibatkan pertumbuhan tanaman tidak sebagaimana mestinya yaitu ada kelainan atau penyimpangan-penyimpangan dan banyak pula tanaman yang mati muda
Gejala kekurangan ini cepat atau lambat akan terlihat pada tanaman, tergantung pada jenis dan sifat tanaman. Ada tanaman yang cepat sekali memperlihatkan tanda-tanda kekurangan atau sebaliknya ada yang lambat. Pada umumnya pertama-tama akan terlihat pada bagian tanaman yang melakukan kegiatan fisiologis terbesar yaitu pada bagian yang ada di atas tanah terutama pada daun-daunnya.
Bila tidak ada faktor lain yang mempengaruhi, maka tanda-tanda kekurangan unsur hara terlihat sebagai berikut:
Kekurangan unsur hara Fosfor (P)
a. Terhambatnya pertumbuhan sistem perakaran, batang dan daun
b. Warna daun seluruhnya berubah menjadi hijau tua/keabu-abuan, mengkilap, sering pula terdapat pigmen merah pada daun bagian bawah, selanjutnya mati. c. Pada tepi daun, cabang dan batang terdapat warna merah ungu yang lambat
laun berubah menjadi kuning.
2.10. Spektrofotometri
Spektrofotomteri sesuai dengan namanya adalah alat yang terdiri dari spektrometer dan fotometer. Spektrofotometer manghasilkan sinar dari spektrum dengan panjang gelombang tertentu dan fotometer adalah alat pengukur intensitas cahaya yang ditransmisikan atau yang diabsorbsi. Jadi spektrofotometer digunakan untuk mengukur energi secara relatif jika energi tersebut ditransmisikan, direfleksikan atau diemisikan sebagai fungsi dari panjang gelombang.
2.10.1. Teori Spektrofotometri
Kelebihan spektrofotometer dibandingakan fotometer adalah panjang gelombang dari sinar putih dapat lebih terseleksi dan ini diperoleh dengan alat pengurai seperti prisma, gating ataupun celah optis. Pada fotometer filter, sinar dengan panjang gelombang yang diinginkan diperoleh dengan berbagai filter dari berbagai warna yang mempunyai spesifikasi melewatkan trayek panjang gekombang tertentu. Pada fotometer filter, tidak mungkin diperoleh panjang gelombang yang benar-benar monokromatis, melainkan suatu trayek panjang gelombang 30-40 nm. Sedangkan pada spektrofotometer, panjang gelombang yang benar-benar terseleksi dapat diperoleh dengan bantuan alat pengurai cahaya seperti prisma.
Jika suatu berkas sinar melewati suatu medium homogen, sebagian dari cahaya datang (P0) diabsopsi sebanyak (Pa) sebagian dapat diabaikan dipantulkan (Pr), sedangkan sisanya ditransmisikan (Pt) dengan efek intensitas murni sebesar :
P0 = Pa + Pt + Pr
Tetapi pada prakteknya, nilai Pr adalah kecil sekali (~ 4%); sehingga untuk tujuan praktis Lambert dan Beer dan juga Bouger menunjukkan hubungan berikut:
T =
b = jarak tempuh optic, c = konsentrasi
log (T) = log
a = tetapan absorpsivitas T = transmitansi
log
hukum di atas dapat ditinjau sebagai berikut:
a. Jika suatu berkas radiasi monokromatik yang sejajar jatuh pada medium pengabsorpsi pada sudut tegak lurus setiap lapisan yang sangat kecilnya akan menurunkan intensitas berkas.
b. Jika suatu cahaya monokromatis mengenai suatu medium yang transparan, laju pengurangan intensitas dengan ketebalan medium sebanding dengan intensitas cahaya.
c. Intensitas berkas sinar monokomatis berkurang secara eksponensial bila konsentrasi zat pengabsopsi bertambah.
Hal diatas adalah persamaan mendasar untuk spktroskopi absorpsi, dikenal sebagai hukum Beer’s Lambert atau hukum Beer Bougar.
A = abc, Aα c bila ab konstan
Aα b bila ac konstan Aα bc bila a konstan.
Hukum secara matematika adalah sah. Bila C- dinyatakan dalam mol/l dan b- dinyatakan dalam cm/a absorpsivitas molar, yaitu persamaan ini menyatakan absorbansi bial b = 1, c = 1 cm. Berarti absorpsivitas molar adalah absorbansi larutan yang diukur dengan ketebalan c = 1cm dan konsentrasi 1 mol/l. Absorpsivitas molar
juga dikenal sebagai koefisien ekstingsi molekular (ε).
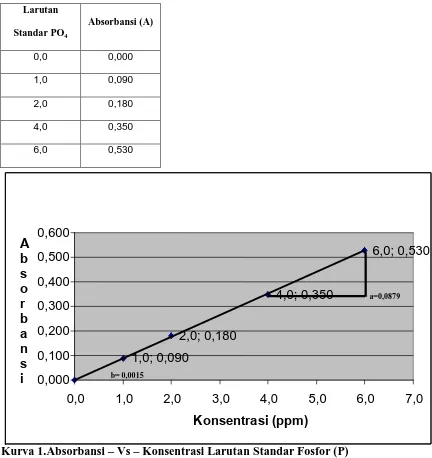
larutan encer terjadi reaksi kimia seperti polimerisasi , hidrolisis, asoiasi atau disosiasi, maka hukum Lambert Beer tidak berlaku. Jika suatu sistem mengikuti hukum Lambert Beer, grafik antara absorbansi terhadap konsentrasi akan menghasilkan garis lurus melalui (0,0).
Jika hukum Lambert Beer benar-benar diikuti maka grafik tersebut dapat disebut sebagai kurva kalibrasi. Arah dari grafik tersebut adalah ab dapat digunakan untuk menghitung absorpsivitas molar.
Suatu spektrofotometer tersusun dari sumber spektrum tampak yang kontinyu, monokromator, sel pengabsorpsi untuk larutan sampel atau blanko dan suatu alat untuk mengukur perbedaan absorpsi antara sampel dan blanko ataupun pembanding.
1. Sumber : sumber yang biasa digunakan pada spektroskopi absorpsi adalah lampu wolfram. Arus cahaya tergantung pada tegangan lampu.
3. Sel absorpsi : pada pengukuran di daerah tampak kuvet kaca atau kuvet kaca corex dapat digunakan, tetapi untuk pengukuran pada daerah UV kita harus
menggunakan sel kuarsa kaena gelas tidak tembus cahaya pada daerah ini. 4. Detektor : peranan detetor penerima adalah memberikan respon terhadap
cahaya pada berbagai panjang gelombang.
Cara kerja spektrofotometer secara singkat adalah sebagai berikut. Tempatkan larutan pembanding, misalkan blanko dalam sel pertama sedangkan larutan yang akan dianalisis pada sel kedua. Kemudian pilih fotosel yang cocok 200nm - 650nm (650nm – 110nm) agar daerah panjang gelombang yang diperlukan dapat terliputi. Dengan ruang fotosel dalam keadaan tertutup “nol” galvanometer dengan menggunakan tombol dark-current. Pilih h yang diinginkan, buka fotosel dan lewatkan berkas cahaya pada waktu blangko dan “nol” galvanometer didapat dengan memutar tombol sensitivitas. Dengan menggunakan tombol transmitansi, kemudian atur besarnya pada 100%. Lewatkan berkas cahaya pada larutan sampel yang akan dianalisis. Skala absorbansi menunjukkan absorbansi larutan sample, (Khopkar.SM.2003).
2.10.2. Prinsip Kerja Alat Spektrofotometri
2.10.3. Permasalahan Spektrofotometri
Pada metode spektrofotometri terdapat permasalahan ataupun gangguan seperti sidik jari, kotoran padat yang telah kering yang menempel pada dinding sel yang dapat mengganggu penembusan sinar, juga gelembung udara dan lemak, (Alaerts,G.1987).
Permasalahan analisis dengan metode spektrofotometri adalah kesalahan pengukuran detektor yang disebabkan antara lain oleh :
a. Adanya radiasi sesatan (stary radiation) yang ditimbulkan oleh peralatan spektrofotmeter itu sendiri dan ditimbulkan oleh faktor-faktor dari lingkungan seperti debu dan sebagainya.
BAB 3
METODOLOGI PERCOBAAN
3.1. Alat
1. Spektrofotometer UV-Visible Perkin Elmer 2. Botol reaksi 30
3. Rak tabung reaksi
4. Tabung digestion 50 mL Pyrex
5. Labu ukur 1000 mL Pyrex
6. Labu ukur 500 mL Pyrex
7. Labu uku 100 mL Pyrex
8. Labu ukur 50 mL Pyrex Pyrex
9. Pipet volum 50 mL Pyrex
10.Pipet volum 20 mL Pyrex
11.Timbangan Mettler Toledo
12.Oven pengering Gallenhamp
13.Kuvet 10 mL 14.Eksikator
15.Kertas saring Whatman No.40 16.Botol aquadest
17.Botol plastik bertutup 18.Corong plastik 19.Digestion blok
3.2. Bahan
1. HNO3 (pekat) (65 %) 2. HClO4 (pekat) (60 %)
3. Standar 0 (larutan HClO4 0,6 %)
Pipet 1 mL HClO4 (pekat) (60%) ke dalam labu ukur 100 mL yang telah berisi air bebas ion kira-kira setenganya, goyangkan dan tambahkan lagi air bebas ion hingga tepat 100 mL (pengenceran 100x).
4. Pereaksi Fosfor pekat
Larutkan 12 g (NH4)6Mo7O24.4H2O dalam air, tambahkan140 mL H2SO4 (pekat) dan 0,227g K(SbO)C4H4O6 .0,5 H2O, jadikan 1 liter dengan air bebas ion 5. Pereaksi pewarna Fosfor
Campurkan 1,06 g asam askorbat dan 100 mL pereaksi Fosfor (pekat), kemudian dijadikan 1 liter dengan air murni, pereaksi Fosfor ini harus dibuat baru.
6. Standar induk untuk PO4 1000 ppm
Pindahkan secara kuantitatif larutan standar induk PO4 di dalam ampul ke dalam labu ukur 1 liter, tambahkan dengan air bebas ion sampai dengan tanda garis, kocok.
7. Standar PO4 200 ppm
Pipet 50 mL standar induk PO4 1000 ppm ke dalam labu 250 mL, tambahkan dengan air bebas ion sampai tanda garis, kocok.
8. Standar PO4 20 ppm
9. Standar PO4 (0-1-2-4-6 ppm)
Pipet berturut-turut 0; 0,5; 1; 2; dan 3 ml standar 20 ppm PO4 ke dalam tabung reaksi. Tambahkan standar 0 sehingga volume masing-masing menjadi 10 mL. deret standar ini memiliki kepekatan : 0; 1; 2; 4; dan 6 ppm.
10.Daun kelapa sawit. 11.Air bebas ion
3.3. Persiapan Contoh Daun Kering
3.3.1.Membersihkan Contoh Daun Tanaman Kelapa Sawit
Contoh yang telah diterima dilaboratorium terlebih dahulu dicatat dan diberi nomor laboratorium secara beraturan. Contoh segera dibersihkan dengan kapas yang telah dibasahi air destilasi. Bagian tulang kasar (lidinya) dibuang dengan gunting, begitu juga bagian pinggir daun terutama daun yang agak lebar digunting dan dibuang. Kemudian contoh daun dimasukkan ke dalam kain kelambu ukuran 15 x 30 cm dan disertai label nomor contoh/nomor laboratorium.
3.3.2.Mengeringkan dan Menggiling
3.4Prosedur Destruksi Basa (HNO3 + HClO4) Daun Kelapa Sawit
1. Ditimbang 0,5 g contoh kering, lalu dimasukkan ke dalam tabung digestion 50mL.
2. Ditambahkan 5 mL HNO3 (pekat) dan 0,5 mL HClO4 (pekat) biarkan satu malam. 3. Setelah satu malam dipanaskan dalam digestion blok dengan suhu 1000 C
selama satu jam, kemudian suhu ditingkatkan menjadi 1500 C.
4. Setelah uap kuning habis suhu digestion blok ditingkatkan menjadi 2000 C, destruksi selesai setelah keluar asap putih dan siasa ekstrak kurang lebih 0,5mL.
5. Tabung diangkat dan dibiarkan dingin.
6. Larutan diencerkan dengan air bebas ion ke dalam labu ukur 50 mL, dikocok. 7. Disaring dengan menggunakan kertas whatman No. 40 ke dalam botol plastik
100 mL.
8. Filtrat dipergunakan untuk pengukuran unsur-unsur makro : P, K, Ca, Mg, Na, S, dan unsur-unsur mikro : Fe, Al, Mn, Cu, Zn, dan B.
9. Dilakukan juga destruksi blanko.
3.5. Prosedur Penetapan Fosfor (P) Daun Kelapa Sawit Secara Spektrofotometri UV-Visible
1. Dipipet 1 mL filtrat (hasil destruksi dalam HNO3 (pekat) dan HClO4 (pekat)) ke dalam tabung gelas.
2. Ditambahkan 9 mL air bebas ion dan dikocok.
3. Dipipet masing-masing 2 ml ektrak encer contoh dan deret standar P (0-1-2-4-6 ppm) ke dalam tabung gelas.
5. Dokocok sampai homogen 6. Didiamkan 30 menit.
3.6 Flowsheet
←Dipipet 1 mL
←Dimasukkan ke dalam tabung gelas
←Ditambahkan 9 mL air bebas ion
←Dikocok
←Dipipet 2 mL ekstrak encer
←Dimasukkan ke dalam tabung gelas
←Ditambahkan 10 mL pereaksi pewarna Fosfor
←Dikocok
←Didiamkan selama 30 menit
←Diukur absorbansinya dengan menggunakan alat spektrofotmeter UV-Visible pada panjang gelombang 693 nm
Ekstrak Daun Kelapa Sawit
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil dan Analisa Data
Hasil analisa Fosfor (P) Daun Kelapa Sawit terdapat pada tabel berikut ini:
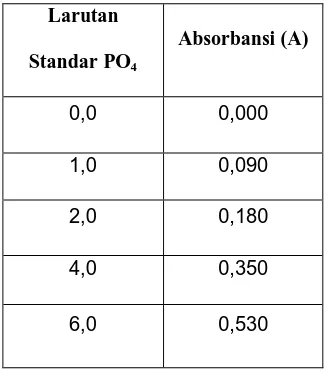
Tabel 4.1. Data Absorbansi Larutan Fosfor Standar Larutan
Standar PO4
Absorbansi (A)
0,0 0,000
1,0 0,090
2,0 0,180
4,0 0,350
6,0 0,530
Tabel 4.2. Absorbansi P-Grafik Berat Contoh
N0. Lab
Berat Kering Contoh daun
1050C
Absorbansi
Konsentrasi Sampel (ppm)
P (%)
564 0,05 0,151 1,70 0,17
565 0,05 0,204 2,30 0,230
4.2. Perhitungan
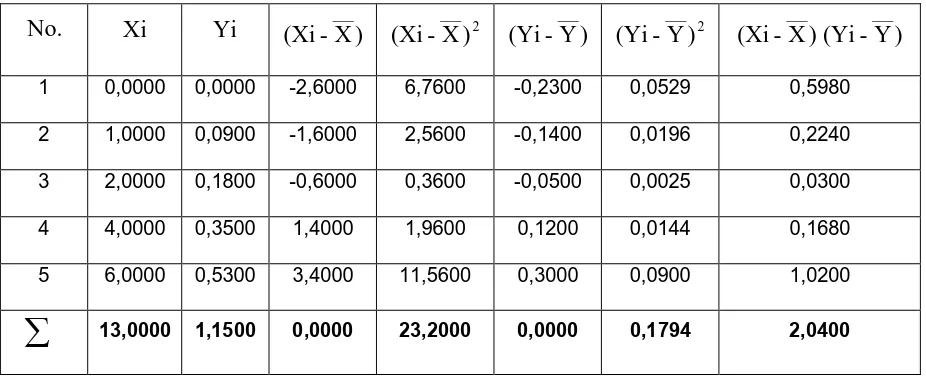
4.2.1. Penentuan Persamaan Garis Regresi Tabel 4.3. Penentuan Persamaaan Garis Regresi
No. Xi Yi (Xi-___X) ___ 2
Dimana harga X rata-rata = ___
Dimana harga Y rata-rata = ___
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan garis :
Y = ax + b, dimana a = Slope
Selanjutnya harga (a) = slope ditentukan dengan menggunakan metode Least Squere sebagai berikut :
a =
Dengan mensubsitusikan harga-harga yang tercantum pada label sebelumnya kepada persamaan ini, akan diperoleh :
a =
Maka harga b dapat diperoleh melalui : ___
Maka persamaan garis regresi yang diperoleh adalah : Y = 0,0879X + 0,0015
4.2.2. Mencari Konsentrasi Sampel Untuk No.Lab 564
Untuk No.Lab 565
Untuk No.Lab 566
4.2.3. Menghitung Kadar Fosfor (P) Daun Kelapa Sawit
Untuk Lab.No.566 P% = 1,72 X
1000 50
X
500 100
4.3. Pembahasan
Pemberian unsur hara pada tanaman kelapa sawit merupakan usaha kultur teknis yang penting untuk meningkatkan produksi persatuan luas dengan tujuan akhir keuntungan ekonomis yang maksimal. Kebutuhan unsur hara untuk tanaman kelapa sawit melalui hasil analisis dari bahan panen dan daun sebagai pedoman yang memudahkan untuk memberikan indikasi kebutuhan unsur hara buatan tanaman kelapa sawit. Hal ini disebabkan karena daun merupakan bagian yang paling efektif dari tanaman.
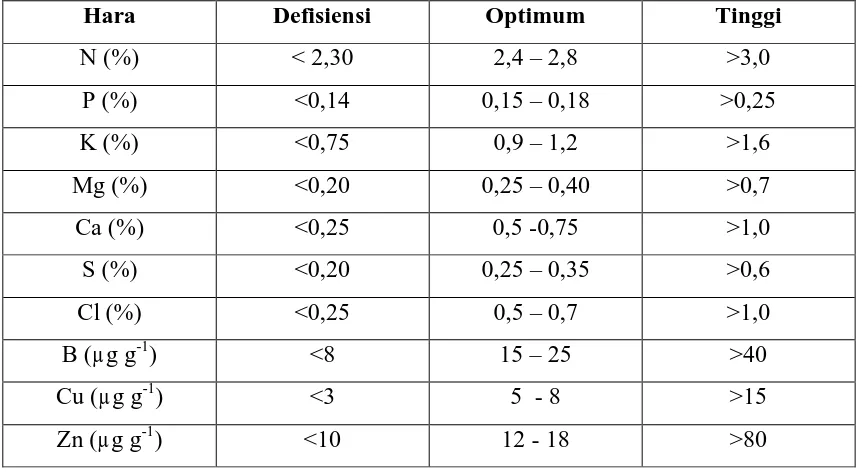
Dari hasil analisa daun kelapa sawit secara spektrofotometri di laboratorium diperoleh hasil Fosfor untuk No. laboratorium 564 adalah 0,17%, 565 adalah 0,230% dan 566 adalah 0,172%, dibanding dengan nilai tarif krisis antara 0,16 – 0,19%, maka dapat disimpulkan unsur hara dalam daun kelapa sawit untuk No.564 dan 566 menunjukkan nilai optimum, sedangkan untuk No. 565 menunjukkan nilai yang tinggi..Hasil yang diperoleh untuk memudahkan para petani untuk mengetahui beberapa kebutuhan unsur hara buatan yaitu berupa pemupukan sesuai dosis yang dibutuhkan karena pemupukan merupakan menambah ketersediaan unsur hara di dalam tanah.
Pada analisis fosfor pada daun kelapa sawit ini diperoleh fosfor yang optimum dan fosfor yang tinggi. Unsur hara di dalam tanah terbagi dalam unsur makro dan unsur mikro, mengenai peranan utama Fosfor bagi tanaman adalah :
a. Memacu pertumbuhan akar dan pembentukan sistim perakaran yang baik sehingga tanaman dapat mengambil unsur hara lebih banyak dan pertumbuhan tanaman menjadi sehat dan serta kuat.
c. Memacu pembentukan bunga dan masaknya buah/biji, sehingga mempercepat masa panen.
d. Memperbesar persentase terbentuknya bunga menjadi buah dan biji. e. Menambahkan daya tahan tanaman terhadap serangan hama dan
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari hasil analisa daun diperoleh bahwa :
Kadar Fosfor yang diperoleh dari daun kelapa sawit pada sampel No.564, 565, 566 adalah 0,17%; 0,230%; dan 0,172%, dimana tingkat kesuburan tanaman kelapa sawit berdasarkan unsur hara yang terdapat pada daun secara spektrofotometri berbeda-beda, hal ini disebabkan oleh faktor cuaca, curah hujan, lingkungan dan keadaan tanah.
5.2. Saran
1. Agar mahasiswa/i selanjutnya dapat menganalisa unsur fosfor (P) dengan menggunakan metode yang lain.
1,0; 0,090
Tabel. Data hasil pengukuran Absorbansi Larutan Standar Unsur Fosfor (P) Larutan
Kurva 1.Absorbansi – Vs – Konsentrasi Larutan Standar Fosfor (P) Y = 0,0879X + 0,0015
KADAR HARA DAUN KELAPA SAWIT YANG MENUNJUKKAN DEFISIENSI, OPTIMUM DAN TINGGI
TABEL TANAMAN SAWIT MUDA ( < 6 TAHUN ) DAUN KE 17
Hara Defisiensi Optimum Tinggi
N (%) < 2,50 2,6 – 2,9 >3,1
Hara Defisiensi Optimum Tinggi
N (%) < 2,30 2,4 – 2,8 >3,0
DAFTAR PUSTAKA
Alaerts, G. 1987. Metoda Penelitian Air. Surabaya : Penerbit Usaha Nasional. Aldin, U.L. 2008. Kelapa Sawit di Indonesia. Medan. : PPKS.
tanggal 21 maret 2009.
Khopkar, SM. 2003. Konsep Dasar Analitik. Jakarta. : Universitas Indonesia Press. Mulja, M. 1995. Analisis Instrumental. Surabaya : Airlangga University.
Risza, S. 1994. Kelapa Sawit Upaya Peningkatan Produktivitas. Yogyakarta. : Kanisius.