PERAN SALINITAS TERHADAP TOKSISITAS MERKURI
DAN PENGARUHNYA TERHADAP KONDISI FISIOLOGIS
IKAN BANDENG (
Chanos chanos
Forsskal)
RIRI EZRANETI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis dengan judul Peran Salinitas terhadap Toksisitas Merkuri dan Pengaruhnya terhadap Kondisi Fisiologis Ikan Bandeng (Chanos chanos Forsskal) adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Juli 2011
Riri Ezraneti
ABSTRACT
RIRI EZRANETI. Salinity influence to mercury toxicity and the effect to milkfish
(Chanos chanos Forsskal) physiologic conditions. Under direction of KUKUH NIRMALA and RIDWAN AFFANDI.
Mercury is a very dangerous heavy metal that can damage nerve and enzyme system in fish body. This research aimed to knows mercury toxicity to milkfish with different salinity. It consisted of two steps; they were preliminary research (range value test and acute toxicity test) and main research (the salinity influence of mercury toxicity and milkfish’s physiologic condition). Range value test was done in fresh water consisting of five treatments (0, 0.006,0.06, 0.6 and 6 mg Hg/l). Acute toxicity test also consisted of five treatments (0, 0.110, 0.195, 0.347 and 0.618 mg Hg/l). Moreover, main research consisted of one control and three treatments with three replications at the same concentrate of mercury 0.012 mg Hg/l. Those treatments were salinity 0 ppt, 10 ppt and 20 ppt. The result demonstrated that LC50 96 hour in fresh water was 0.147 mg Hg/l. The main
research showed that mercury can increased osmotic gradient, decreased oxygen consumption rate, increased blood glucose rate, decreased hematologic conditions, growth rate, feeding efficiency, and survival rate. Mercury is collected in body gland, for example in gill and liver. Treatment C (10 ppt) showed better physiologic conditions than other treatments. The effect of mercury toxicity would get minimal while maintained at optimal salinity.
RINGKASAN
RIRI EZRANETI. Peran Salinitas Terhadap Toksisitas Merkuri Dan Pengaruhnya Terhadap Kondisi Fisiologis Ikan Bandeng (Chanos chanos Forsskal). Dibimbing oleh KUKUH NIRMALA dan RIDWAN AFFANDI.
Diantara berbagai macam logam berat, merkuri digolongkan sebagai pencemar yang paling berbahaya. Kadar merkuri terus meningkat akibat penggunaannya diberbagai bidang yang cukup luas. Merkuri akan masuk ke perairan tawar, payau dan akhirnya sampai di laut serta dapat mempengaruhi organisme yang hidup di dalamnya. Perbedaan salinitas akan mempengaruhi tingkat toksisitas merkuri. Apabila ikan bandeng yang dipelihara baik di air tawar, payau dan laut terkontaminasi oleh merkuri maka kondisi fisiologis ikan akan terganggu.
Penelitian ini bertujuan untuk menentukan ambang batas dan toksisitas akut merkuri terhadap kondisi fisiologis ikan bandeng di air tawar, menganalisa pengaruh merkuri terhadap ikan bandeng yang dipaparkan pada salinitas yang berbeda dan menentukan salinitas yang baik untuk mengurangi pengaruh merkuri terhadap ikan bandeng. Penelitian ini dilakukan dalam dua tahap yaitu penelitian pendahuluan yang terdiri atas uji nilai kisaran (Range value test) dan uji toksisitas akut. Sedangkan penelitian inti yaitu pemeliharaan ikan bandeng pada media yang tercemar merkuri dengan salinitas berbeda. Ikan yang digunakan berukuran 7-8 cm dan berat 3-5 gram. Sedangkan bahan pencemar yang digunakan adalah merkuri nitrat (Hg(NO3)2). Uji nilai kisaran dengan konsentrasi menggunakan
metode logaritmik berbasis 10 yaitu A (kontrol), B (0.006), C (0.06), D (0.6), dan E (6) mg Hg/l dengan 3 ulangan tiap perlakuan. Sedangkan uji toksisitas akut terdiri atas 4 perlakuan, 1 kontrol dan 3 ulangan dengan konsentrasi A (tanpa Hg), B (0.110 mg Hg/l), C (0.195 mg Hg/l), D (0.347 mg Hg/l) dan E (0.618 mg Hg/l). Pada penelitian inti diaplikasikan dalam 4 perlakuan dan 3 ulangan dengan konsentrasi A (Salinitas 0 ppt tanpa Hg), B (Salinitas 0 ppt + 0.012 mg Hg/l), C (Salinitas 10 ppt + 0.012 mg Hg/l) dan D (Salinitas 20 ppt + 0.012 mg Hg/l).
Hasil penelitian pendahuluan menunjukkan bahwa merkuri bersifat sangat toksik terhadap ikan bandeng dengan nilai LC50 96 jam sebesar 0.147 mg Hg/l.
Selama uji terjadi perubahan tingkah laku ikan antara lain: ikan kehilangan gerak refleks, berenang tidak beraturan dan sering muncul ke permukaan dengan bukaan mulut dan operculum yang lebih lebar dan cepat. Kemudian kembali ke dasar dengan posisi tegak dan sampai ke dasar dengan posisi bagian ventral ke atas. Ikan juga mengalami kejang-kejang dan ram jet ventilation sebelum mengalami kematian di dasar akuarium.
Hasil penelitian inti menunjukkan bahwa salinitas mempengaruhi toksisitas merkuri dan mempengaruhi kondisi fisiologis ikan bandeng. Setelah ikan bandeng terpapar merkuri pada salinitas yang berbeda gradien osmotik dan kadar glukosa darah meningkat, sedangkan kondisi hematologi dan tingkat
konsumsi oksigen mengalami penurunan. Merkuri terakumulasi pada jaringan seperti insang, hati dan daging. Akibatnya jumlah konsumsi pakan, laju pertumbuhan, efisiensi pakan dan kelangsungan hidup ikan bandeng menurun pada tiap perlakuan.
Hasil analisa menunjukkan bahwa perlakuan C (Salinitas 10 ppt + 0.012 mg Hg/l) merupakan perlakuan terbaik karena memiliki gradien osmotik terendah 0.237±0.088 Osm/kg, tingkat konsumsi oksigen tertinggi 0.257±0.037 mgO2/g/jam, jumlah eritrosit tertinggi 3.61±0.39 x 106 sel/mm3, kadar
haemoglobin tertinggi 5.37±0.86 %, kadar hematokrit tertinggi 19.90±0.41 % dan jumlah leukosit tertinggi 11.33±0.43 x 105 sel/mm3 dibandingkan perlakuan lainnya. Selanjutnya kadar glukosa darah terendah 11.77±1.30 mmol/l, jumlah konsumsi pakan tertinggi 65.03±1.85 gram, nilai efisiensi pakan tertinggi 18.63±0.79 % dan kelangsungan hidup tertinggi 68.33 %. Akumulasi merkuri di daging ikan lebih sedikit dari perlakuan lainnya yaitu 0.0844 ppm. Kerusakan pada insang dan hati lebih sedikit terlihat dengan sedikitnya deposit merkuri dibandingkan perlakuan lainnya.
Hasil pengukuran fisika kimia air memperlihatkan kisaran nilai yang didapatkan masih layak untuk pemeliharaan ikan bandeng. Sehingga dapat
dikatakan bahwa parameter fisika kimia air pada penelitian ini bukan merupakan faktor pembatas yang dapat mempengaruhi ikan bandeng.
© Hak Cipta milik IPB, tahun 2011 Hak Cipta dilindungi Undang-undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
PERAN SALINITAS TERHADAP TOKSISITAS MERKURI
DAN PENGARUHNYA TERHADAP KONDISI FISIOLOGIS
IKAN BANDENG (
Chanos chanos
Forsskal)
RIRI EZRANETI
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Ilmu Akuakultur
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Peran Salinitas terhadap Toksisitas Merkuri dan Pengaruhnya Terhadap Kondisi Fisiologis Ikan Bandeng (Chanos chanos
Forsskal) Nama : Riri Ezraneti
NRP : C151090141
Disetujui
Komisi Pembimbing
Dr. Ir. Kukuh Nirmala, M.Sc Dr. Ir. Ridwan Affandi, DEA Ketua Anggota
Diketahui
Ketua Program studi Dekan Sekolah Pascasarjana
Ilmu Akuakultur
Prof. Dr. Enang Harris, MS Dr. Ir. Dahrul Syah, M.Sc. Agr
To My Beloved Family
My Father, Zulhikmi and My Mother, Emyunar My Sisters Resi Ezrari, Popi lestari and Olga Philberta
KATA PENGANTAR
Puji syukur penulis ucapkan kehadirat Allah SWT yang telah memberikan rahmat dan karunian-Nya sehingga penulisan tesis dengan judul ”Peran Salinitas terhadap Toksisitas Merkuri dan Pengaruhnya Terhadap Kondisi Fisiologis Ikan Bandeng (Chanos chanos Forsskal)” dapat diselesaikan dengan baik.
Ucapan terimakasih yang tak terhingga penulis sampaikan secara khusus kepada Bapak Dr. Ir. Kukuh Nirmala, M.Sc dan Dr. Ir. Ridwan Affandi, DEA selaku komisi pembimbing atas waktu, kebijaksanaan, tuntunan, kesabaran, serta masukan hingga tesis ini dapat diselesaikan.
Penulis juga mengucapakan terimakasih kepada:
1. Kedua orang tua penulis, Ayahanda Zulhikmi, S.Pd. M.MPd dan Ibunda Emyunar; Adik-adikku: Resi Ezrari, Devid Zel Nofra, Popi Lestari dan Olga Philberta.
2. Bapak Dr. Ir. Eddy Supriyono, M.Sc selaku penguji luar komisi atas segala masukan dan arahan.
3. Rekan-rekan Akuakultur 2009 (Muliani, Hary Krettiawan, Eulis Marlina, Muznah Toatubun, Jenny Abidin, Dewi puspaningsih, Jacqueline Sahetapy, Tanbiyaskur, Rahman, Iko Imelda Arisa, Sefty Heza Dwinanti, Zuraida, Anwar Hasan, Dian Febriani, Alfabetian Condro Haditomo, Erna Thalib, Wahyuni Fanggi Tasik, Aras Syazili, Safrizal Putra, Novi Mayasari, Reza Samsudin, Jakomina Metungun, Mariana Beruatjaan) dan Anna Oktavera. 4. Staf dan pegawai di Departemen Budidaya Perairan FPIK IPB.
Penulis menyadari bahwa tesis ini masih jauh dari sempurna, karena keterbatasan pengetahuan dan wawasan penulis. Oleh karena itu, penulis mengharapkan saran, masukan dan kritikan untuk perbaikan serta kesempurnaan penulisan selanjutnya. Semoga tesis ini dapat bermanfaat.
Bogor, Juli 2011
DAFTAR RIWAYAT HIDUP
Penulis dilahirkan di Batu Hampar Sumatera Barat pada tanggal 24 Agustus 1983, putri pertama dari lima bersaudara pasangan Bapak Zulhikmi, S.Pd. M.MPd dan Ibu Emyunar.
Tahun 2001 penulis lulus dari SMU Negeri 1 Harau. Pada tahun yang sama penulis melanjutkan pendidikan Strata Satu (S1) pada jurusan Ilmu Kelautan Fakultas Perikanan dan Ilmu Kelautan Universitas Riau Pekanbaru dan berhasil lulus pada tahun 2005.
Penulis sempat bergabung sebagai staf pengajar di program study Budidaya Perairan Fakultas Pertanian Universitas Malikussaleh Lhokseumawe Aceh, kemudian pada rahun 2009 penulis melanjutkan pendidikan kembali pada program Master (S2) di Sekolah Pascasarjana Institut Pertanian Bogor pada Mayor Ilmu Akuakultur. Penulis berhasil menyelesaikan pendidikan Master (S2) pada tahun 2011 dengan judul tesis “Peran Salinitas Terhadap Toksisitas Merkuri dan Pengaruhnya Terhadap Kondisi Fisiologis Ikan Bandeng (Chanos chanos
DAFTAR ISI
Halaman
DAFTAR TABEL ... vi
DAFTAR GAMBAR ... vi
DAFTAR LAMPIRAN ... viii
PENDAHULUAN ... 1
Latar Belakang... 2
Perumusan Masalah ... 2
Tujuan dan Manfaat ... 4
Hipotesis ... 4
TINJAUAN PUSTAKA ... 5
Ikan Bandeng ... 5
Merkuri ... 6
Pengaruh Merkuri Terhadap Organisme ... 9
Salinitas dan Osmoregulasi ... 12
METODE PENELITIAN ... 14
Persiapan Penelitian... 14
Penelitian Pendahuluan ... 14
Tahap 1 ... 14
Tahap 2 ... 16
Penelitian Inti... 18
HASIL DAN PEMBAHASAN ... 23
Hasil ... 23
Penelitian Pendahuluan ... 23
Penelitian Inti ... 28
Pembahasan ... 46
SIMPULAN DAN SARAN ... 55
DAFTAR PUSTAKA ... 57
DAFTAR TABEL
Halaman 1 Metode dan alat untuk analisis parameter fisika kimia air ... 23
2 Data mortalitas ikan bandeng pada uji nilai kisaran (Range value test) .. 25
3 Data parameter pengamatan ikan bandeng yang terpapar dan tidak
terpapar merkuri di air tawar ... 36
4 Data parameter pengamatan ikan bandeng yang terpapar merkuri pada
salinitas yang berbeda... 45
5 Data pengamatan fisika kimia air selama uji toksisitas akut merkuri
terhadap ikan bandeng ... 45
DAFTAR GAMBAR
Halaman 1 Kerangka pemikiran penelitian ... 3
2 Nilai LC50 merkuri pada ikan bandeng selama uji toksisitas akut ... 26
3 Rata-rata frekuensi pergerakan operculum ikan bandeng selama uji
toksisitas akut ... 27
4 Gradien osmotik ikan bandeng yang terpapar dan tidak terpapar
merkuri di air tawar ... 28
5 Rata-rata tingkat konsumsi oksigen ikan bandeng yang terpapar dan
tidak terpapar merkuri di air tawar ... 29
6 Kondisi hematologi ikan bandeng yang terpapar dan tidak terpapar
merkuri di air tawar ... 30
7 Histokimia ikan bandeng pada perlakuan A (kontrol) ... 31
8 Histokimia ikan bandeng pada perlakuan B (0.012 mg Hg/l)... 31
9 Rata-rata kadar glukosa darah ikan bandeng yang terpapar dan tidak
terpapar merkuri di air tawar ... 32
10 Rata-rata jumlah pakan yang dikonsumsi ikan bandeng yang terpapar
dan tidak terpapar merkuri di air tawar ... 32
11 Rata-rata laju pertumbuhan ikan bandeng yang terpapar dan tidak
terpapar merkuri di air tawar ... 31
12 Rata-rata nilai efisiensi pakan ikan bandeng yang terpapar dan tidak
terpapar merkuri di air tawar ... 34
13 Kadar merkuri pada media dan daging ikan bandeng di air tawar pada
akhir penelitian ... 34
14 Rata-rata tingkat kelangsungan hidup ikan bandeng yang terpapar dan
tidak terpapar merkuri di air tawar ... 35
15 Rata-rata gradien osmotik ikan bandeng yang terpapar merkuri pada
salinitas berbeda ... 36
16 Rata-rata tingkat konsumsi oksigen ikan bandeng yang terpapar
17 Rata-rata kondisi hematologi ikan bandeng yang terpapar merkuri
pada salinitas berbeda ... 38
18 Histokimia insang ikan bandeng yang terpapar merkuri pada salinitas
berbeda ... 39
19 Histokimia hati ikan bandeng yang terpapar merkuri pada salinitas
berbeda ... 40
20 Rata-rata kadar glukosa darah ikan bandeng yang terpapar merkuri
pada salinitas berbeda ... 41
21 Rata-rata jumlah pakan yang dikonsumsi ikan bandeng yang terpapar
merkuri pada salinitas berbeda ... 41
22 Rata-rata laju pertumbuhan ikan bandeng yang terpapar mekuri pada
salinitas berbeda ... 42
23 Rata-rata efisiensi pakan ikan bandeng yang terpapar merkuri pada
salinitas berbeda ... 43
24 Rata-rata kadar merkuri di air dan di daging ikan bandeng yang
terpapar merkuri pada salinitas berbeda... 43
25 Rata-rata tingkat kelangsungan hidup ikan bandeng yang terpapar
DAFTAR LAMPIRAN
Halaman 1 Penentuan konsentrasi pada penelitian pendahuluan dan penelitian inti 63
2 Metode pengenceran salinitas ... 64
3 Prosedur pengamatan gradien osmotik ... 65
4 Prosedur pengamatan kondisi hematologi ... 66
5 Prosedur pembuatan preparat histokimia ... 68
6 Prosedur pengukuran kadar glukosa darah ... 71
7 Prosedur pengukuran kadar merkuri dengan AAS ... 72
8 Data mortalistas ikan bandeng selama uji nilai kisaran 48 jam ... 74
9 Data mortalitas ikan bandeng selama uji toksisitas merkuri 96 jam ... 75
10 Analisa probit untuk menentukan LC50 24 jam merkuri terhadap ikan
bandeng ... 76
11 Analisa probit untuk menentukan LC50 48 jam merkuri terhadap ikan
bandeng ... 77
12 Analisa probit untuk menentukan LC50 72 jam merkuri terhadap ikan
bandeng ... 78
13 Analisa probit untuk menentukan LC50 96 jam merkuri terhadap ikan
bandeng ... 79
14 Data frekuensi buka tutup operculum ikan bandeng selama uji
toksisitas akut ... 80
15 Analisa gradien osmotik ikan bandeng yang terpapar merkuri selama
30 hari waktu pemaparan ... 81
16 Analisa tingkat konsumsi oksigen ikan bandeng yang terpapar
merkuri selama 30 hari waktu pemaparan ... 83
17 Analisa kadar haemoglobin ikan bandeng yang terpapar merkuri
18 Analisa jumlah eritrosit ikan bandeng yang terpapar merkuri selama
30 hari waktu pemaparan ... 87
19 Analisa kadar hematokrit ikan bandeng yang terpapar merkuri selama
30 hari waktu pemaparan ... 89
20 Analisa jumlah leukosit ikan bandeng yang terpapar merkuri selama
30 hari waktu pemaparan ... 91
21 Analisa kadar glukosa darah ikan bandeng yang terpapar merkuri
selama 30 hari waktu pemaparan ... 93
22 Analisa laju pertumbuhan ikan bandeng yang terpapar merkuri selama
30 hari waktu pemaparan ... 95
23 Analisa efisiensi pakan ikan bandeng yang terpapar merkuri selama
30 hari waktu pemaparan ... 97
24 Analisa kelangsungan hidup ikan bandeng yang terpapar merkuri
PENDAHULUAN
Latar Belakang
Diantara berbagai macam logam berat, merkuri digolongkan sebagai pencemar yang paling berbahaya. Merkuri adalah salah satu logam berat yang terdapat di alam walaupun hanya dalam jumlah yang kecil. Kadar merkuri di air tawar secara alami berkisar antara 10 – 100 µg/l, sedangkan di perairan laut berkisar antara <10-30 µg/l (Moore 1991 dalam Saputra 2009). Selanjutnya Connel dan Miller (1995) menyatakan bahwa konsentrasi logam akan meningkat seiring menurunnya salinitas. Namun seiring dengan perkembangan zaman, kadar merkuri di alam terus meningkat akibat penggunaannya diberbagai bidang yang cukup luas. Penggunaan merkuri antara lain pada pabrik alat-alat listrik seperti pembuatan baterai, pabrik klor alkali yang memproduksi klorin (Cl2), dibidang
pertanian sebagai pembasmi jamur, bahan campuran cat dan pertambangan seperti tambang emas yang marak dilakukan sekarang ini. Merkuri yang digunakan akan tercuci dan masuk ke perairan tawar seperti sungai, danau dan waduk, sehingga menyebabkan terjadinya penurunan kualitas air dan lingkungan sekitarnya.
Selanjutnya merkuri akan dibawa oleh aliran sungai ke muara yang airnya payau dan akhirnya merkuri akan masuk ke perairan laut.
Logam merkuri yang masuk ke perairan baik dalam bentuk organik maupun anorganik bersifat toksik dan dapat diakumulasi dalam tubuh organisme yang hidup di perairan. Toksisitas merkuri di perairan berbeda antara perairan tawar, payau dan laut karena salinitas merupakan salah satu faktor yang dapat mempengaruhi akumulasi logam berat pada makhluk hidup.
Salah satu organisme perairan yang dapat mengakumulasi merkuri adalah
ikan bandeng. Ikan bandeng memiliki sifat eurihalin yang mampu hidup pada
rentang salinitas yang lebar yaitu antara 0 ppt sampai dengan 50 ppt. Apabila
salinitas naik secara bertahap, bandeng mampu hidup hingga salinitas 70 ppt
Apabila energi yang digunakan untuk proses osmoregulasi sedikit maka akan banyak tersedia energi yang dapat digunakan untuk pertumbuhan dan ketahanan
tubuh ikan terhadap penurunan kualitas lingkungan perairan akan lebih baik, begitu juga sebaliknya.
Waduk Djuanda Jatiluhur dan waduk Cirata Jawa Barat merupakan waduk yang berpotensi sebagai tempat pemeliharaan ikan bandeng. Triyanto (2010) menyatakan bahwa ikan bandeng yang diintroduksi di waduk Djuanda Jatiluhur mampu memanfaatkan plankton yang tersedia sebagai makanannya. Waduk Djuanda Jatiluhur menerima pasokan air dari sungai Citarum melalui waduk Saguling dan waduk Cirata. Wurdiyanto (2007) menyatakan bahwa sungai Citarum merupakan salah satu sungai di Jawa Barat yang tercemar oleh merkuri. Selanjutnya Saputra (2009) mengemukakan bahwa tahun 2008 akumulasi Hg telah terdapat dalam sedimen, air dan daging ikan yang dipelihara di waduk Cirata. Kandungan Hg dalam sedimen waduk Cirata mencapai 26,83 mg/kg, sedangkan di air 0.002 mg/l dan di daging ikan patin 0.0001 mg/kg. Oleh karena itu waduk Djuanda Jatiluhur dan waduk Cirata juga berpotensi tercemar oleh merkuri.
Dengan menurunnya kualitas perairan akibat adanya senyawa merkuri tentu akan memberikan pengaruh terhadap budidaya ikan bandeng terutama yang dipelihara di perairan tawar. Apabila ikan bandeng tersebut mengakumulasi
merkuri maka akan dapat membahayakan masyarakat yang mengkonsumsi ikan tersebut. Sejauhmana pengaruh merkuri terhadap ikan bandeng yang dipelihara pada media salinitas yang berbeda belum banyak diketahui, oleh karena itu maka penelitian ini dilakukan.
Perumusan Masalah
Ikan bandeng merupakan ikan yang mempunyai nilai ekonomis yang
tubuh ikan bandeng karena tekanan osmotik cairan dalam tubuh ikan bandeng lebih tinggi dibandingkan lingkungannya.
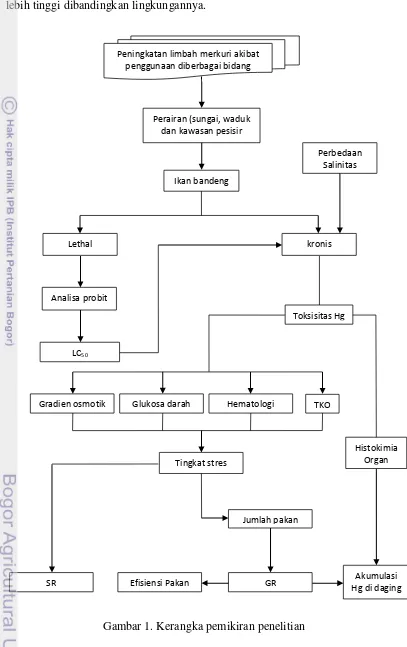
Gambar 1. Kerangka pemikiran penelitian
Peningkatan limbah merkuri akibat penggunaan diberbagai bidang
Perairan (sungai, waduk dan kawasan pesisir
Ikan bandeng
Lethal kronis
Analisa probit
Gradien osmotik LC50
TKO Glukosa darah
Jumlah pakan
GR Efisiensi Pakan
Hematologi
Akumulasi Hg di daging
Histokimia Organ
SR
Perbedaan Salinitas
Toksisitas Hg
Sebaliknya ikan bandeng yang dipelihara di air yang bersalinitas mempunyai tekanan osmotik cairan tubuh lebih rendah dari lingkungannya,
sehingga air cenderung keluar dari tubuh ikan. Untuk itu ikan banyak meminum air sehingga dapat mengganti kekurangan air dalam tubuhnya.
Apabila tempat pemeliharaan ikan bandeng tercemar merkuri, maka merkuri tersebut akan lebih mudah masuk kedalam tubuh ikan bandeng bersamaaan dengan air yang masuk dalam proses osmoregulasi pada ikan tersebut. Kondisi ini menyebabkan resiko ikan bandeng mengakumulasi merkuri dalam tubuhnya akan lebih besar. Sehubungan dengan tingginya peluang ikan-ikan yang dipelihara di air tawar tercemar merkuri, maka penelitian ini dilakukan.
Tujuan dan Manfaat
Penelitian ini dilakasanakan dengan tujuan sebagai berikut:
1. Menentukan ambang batas dan toksisitas akut merkuri pada ikan bandeng yang dipelihara di air tawar.
2. Menganalisa pengaruh merkuri terhadap kondisi fisiologis ikan bandeng yang dipaparkan pada salinitas yang berbeda.
3. Menentukan salinitas yang ideal untuk mengurangi pengaruh toksik merkuri terhadap ikan bandeng
Sedangkan manfaat dari penelitian ini adalah sebagai informasi bagi para pelaku budidaya perikanan mengenai bahaya toksisitas merkuri dalam perairan bagi organisme budidaya khususnya ikan bandeng pada salinitas yang berbeda sehingga lebih memperhatikan manajemen budidaya ikan bandeng tersebut agar tetap berkelanjutan.
Hipotesis
TINJAUAN PUSTAKA
Ikan Bandeng
Ikan bandeng (Chanos chanos) adalah ikan yang termasuk kedalam kingdom animalia, Filum Chordata, Kelas Pisces, Ordo Malacopterigii, Family Chanidae, Genus Chanos, Spesies Chanos chanos (Saanin 1984)
Ikan bandeng (Chanos chanos) mempunyai bentuk tubuh memanjang dan bersisik halus, putih seperti susu. Karena itu diluar negeri terkenal dengan nama “Milkfish” (Evy 2001). Jari-jari sirip semuanya lunak, dan jumlahnya pada sirip punggung antara 14 -16, pada sirip dubur antara 10 -11, pada sirip dada antara 16 -17, dan pada sirip perut antara 11-12. Sirip ekornya panjang dan bercagak. Jumlah sisik pada gurat sisi berkisar antara 75-80 keping (Djuhanda 1981).
Di alam, ikan ini merupakan ikan pemakan plankton dan makroalgae seperti Enteromorpha, Chaetomorpha dan Oscillatoria. Di tambak ikan ini biasanya memakan “klekap” yang terdiri atas berbagai jenis algae dasar dan berbagai hewan benthos. Ikan ini sangat responsif terhadap pakan buatan dengan kadar protein antara 20 – 30 % (Cholik 2005). Selanjutnya ikan ini memiliki sifat dapat mengimbangi keterlambatan tumbuh (compensatory growth) karena proses pembantutan (stunting). Gelondongan yang terlambat tumbuh karena kurang
makan akan segera tumbuh dengan cepat setelah mendapat suasana lingkungan yang baik dan cukup makanan.
Daerah penangkapan nener yang terkenal ialah Nusa Tenggara, Madura dan sulawesi selatan. Selanjutnya Evy (2001) menyatakan bahwa nener banyak
didapatkan di daerah pantai yang landai, berpasir, berarus tenang dan berair jernih. Ikan bandeng tidak hanya ada di Indonesia, tetapi juga di malaysia, Muangthai, Philipina, Taiwan, Jepang, India, Srilangka, Meksiko dan Hawaii (Evy 2001). Penyebaran ikan bandeng dari utara ke selatan mulai dari bagian selatan Jepang sampai di New South Wales, dan dari timur ke Barat mulai dari pantai timur Afrika sampai di kepulauan Paumotu bagian timur (Djuhanda 1981).
Merkuri
Nama kimia merkuri adalah Hydragynum yang berarti perak cair dengan lambang Hg. Pada tabel periodik unsur-unsur kimia, merkuri menempati urutan (NA) 80 dan mempunyai bobot atom (BA) 200,59 (Palar 1994). Secara umum
3. Merupakan logam yang paling mudah menguap jika dibandingkan dengan logam-logam lainnya.
4. Tahanan listrik yang dimiliki sangat rendah sehingga merkuri dijadikan sebagai penghantar listrik yang baik
5. Dapat melarutkan bermacam-macam logam untuk membentuk alloy yang disebut juga dengan amalgam
6. Merupakan unsur yang sangat beracun untuk semua makhluk hidup. Baik itu dalam bentuk unsur ataupun dalam bentuk persenyawaan.
Menurut Darmono (1995) di perairan tawar, logam berat yang terkandung
bersangkutan dengan hasil produksinya seperti pabrik baterai/aki, listrik, cat warna, tekstil, pestisida, gelas, dan keramik (Darmono 1995).
David dan Ferguson dalam Budiono (2003) mengemukakan beberapa kemungkinan bentuk merkuri yang masuk ke dalam lingkungan perairan alam yaitu:
Sebagai merkuri inorganik, melalui hujan, run-off atau aliran sungai. Unsur ini bersifat stabil terutama pada pH rendah.
Dalam bentuk merkuri organik berupa phenyl merkuri (C6 H5-Hg), methyl
merkuri (CH3-Hg), Alkoxyalkyl merkuri atau methyoxy-ethyl merkuri
(CH3O-CH2-CH2-Hg+). Merkuri organik yang terdapat di perairan alam
dapat berasal dari kegiatan pertanian (pestisida).
Terikat dalam suspended solid sebagai Hg22+ (ion merkuro), mempunyai
sifat reduksi yang baik
Sebagai metalik merkuri (Hg0), masuk ke perairan melalui kegiatan
perindustrian dan manufaktur. Unsur ini memiliki sifat reduksi yang tinggi, berbentuk cair pada temperatur ruang dan mudah menguap.
Logam merkuri yang paling toksik dan berbahaya adalah dalam bentuk organik yaitu bentuk senyawa alkil merkuri (metil dan etil merkuri). Logam-logam berat yang bersifat racun seperti Hg, Cd, dan Pb yang terdapat dalam air kebanyakan juga berbentuk ion (Darmono 1995).
Di perairan, bakteri dan fitoplankton dapat melakukan transfer merkuri karena kedua organisme tersebut biasanya ditemukan di perairan dalam jumlah yang relatif banyak. Bakteri dapat merubah merkuri menjadi metil merkuri dan membebaskan merkuri dari sedimen di dasar perairan (Goldwater dan Wood
Wang (2002) menyatakan bahwa kenaikan suhu, penurunan pH dan penurunan salinitas perairan dapat menyebabkan tingkat bioakumulasi logam berat semakin
besar. Sebaliknya Modassir (2000) mengemukakan bahwa efek toksik merkuri dipengaruhi oleh salinitas. Mortalitas remis mangrove semakin meningkat seiring meningkatnya salinitas. Selanjutnya Prakasam (1989) melakukan penelitian mengenai ikan mujair yang dipelihara di media yang terkontaminasi merkuri pada rentang salinitas 0-31 ppt. Hasil penelitiannya menyatakan bahwa mortalitas ikan tinggi terjadi pada salinitas tertinggi dan terendah.
Thongra-ar et al (2003) menyatakan bahwa ketersediaan dan daya toksisitas logam berat sangat tergantung pada bentuk kimianya. Pada lingkungan yang konsentrasi Cl- nya rendah bentuk merkuri organiknya didominasi oleh tiga bentuk kompleks yaitu HgCl2, HgOHCl dan Hg(OH)2 dengan komplek terbanyak
adalah Hg(OH)2. Sedangkan pada konsentrasi Cl- yang tinggi, yang paling
dominan adalah dalam bentuk HgCl4-2 dan HgCl3- dan memiliki daya toksisitas
yang rendah. HgCl2 lebih banyak terdapat pada lingkungan yang konsentrasi Cl
-rendah dibandingkan konsentrasi Cl- yang tinggi. Hal ini menyebabkan toksisitas merkuri akan meningkat seiring menurunnya salinitas. Selanjutnya dikemukakan bahwa menurut prinsip Asam Basa Kuat dan Lemah (HSAB), merkuri adalah asam lemah dan dapat bereaksi lebih cepat dengan basa lemah terutama ligan yang mengandung unsur N dan S tetapi jauh lebih kuat bereaksi dengan ligan
yang mengandung unsur S dari pada unsur N. Jadi dari mekanisme ini dapat diketahui bahwa Hg cenderung membentuk kompleks yang kuat dengan kelompok sulfhidril (-SH) yang ada dalam protein dibandingkan dengan Cl. Ikan mengandung banyak protein, oleh karenanya maka jumlah kelompok sulfhidril yang terkandung dalam jaringan ikan dapat menentukan jumlah Hg yang dapat terabsorpsi.
jaringan tubuh organisme air melalui proses bioakumulasi. Bioakumulasi terjadi karena kecepatan pengambilan merkuri (up take rate) oleh organisme air lebih
cepat dari pada proses eksresi organisme tersebut (Sanusi 1985). Pada kondisi stress, penyerapan logam berat akan semakin meningkat dan pengambilan logam terlarut tersebut terutama terjadi di insang (Modassir 2000). Selanjutnya dikatakan bahwa tingginya pergantian/pengambilan air karena proses osmoregulasi akan menyebabkan akumulasi merkuri lebih cepat sehingga toksisitas merkuri menjadi lebih besar.
Pengaruh Merkuri Terhadap Organisme
APHA (1979) dan Effendi (1993) mengemukakan bahwa tingkatan dari kematian yang disebabkan oleh polutan termasuk merkuri atau faktor lingkungan dibagi menjadi 5 kategori sebagai berikut:
1. Lethal Concentration (LC)
LC ditentukan pada saat mortalitas mencapai >50 % dan terjadi setelah 24 jam, 48 jam atau 96 jam hewan dimasukkan ke dalam media.
2. Effectif Concentration (EC)
EC ditentukan dengan konsentrasi yang dapat menyebabkan efek berbahaya seperti perbedaan pola tingkah laku biota dan ketikseimbangan pada 50 % populasi biota akuatik.
3. Incipient Letal Concentration (ILC)
ILC ditentukan pada saat paling tidak 50 % dari populasi yang bertahan. 4. Save Consentration (SC)
Konsentrasi tertinggi yang paling aman bagi biota akuatik. 5. Maksimum Allowable Toxicant Concentration (MATC)
Konsentrasi tertinggi yang diperbolehkan ada di perairan yang tidak akan menyebabkan bahaya apapun bagi organisme akuatik.
Selanjutnya Balazs (1970) menentukan dari nilai LC50, potensi ketoksikan
akut senyawa uji dapat digolongkan menjadi: 1. Sangat tinggi : < 1 mg/l
2. Tinggi : 1-50 mg/l
3. Sedang : 50-500 mg/l
5. Hampir tidak toksik : 5000-15000 mg/l 6. Relatif tidak berbahaya : > 15000 mg/l
Darmono (2001) menyatakan bahwa toksisitas logam berat terhadap makhluk hidup sangat bergantung pada spesies, lokasi, umur (fase siklus hidup), daya tahan (detoksifikasi), dan kemampuan individu untuk menghindarkan diri dari pengaruh polusi. Selanjutnya Modassir (2000) mengemukakan bahwa toksisitas merkuri meningkat pada organisme laut pada kondisi yang tidak baik berkaitan dengan perubahan laju penyerapan logam berat tersebut. Laju penyerapan tersebut bervariasi tergantung pada kondisi percobaan, jenis spesies yang diuji dan tahap perkembangan dari hewan uji.
Hasil penelitian Wood, Anderson dan D’Apollonia dalam Sanusi (1985) menunjukkan bahwa antara 90 – 100 % dari total Hg yang terakumulasi pada tubuh ikan merupakan metil merkuri. Selanjutnya dikatakan bahwa metil merkuri yang terdapat di perairan umumnya bersifat sangat beracun, dan dapat menimbulkan efek toksik yang bersifat akut maupun kronis terhadap kehidupan organisme air. Hal ini disebabkan karena sifat senyawa tersebut relatif stabil dan memiliki umur biologis yang relatif lama dalam tubuh organisme air.
Darmono (2001) menyatakan bahwa logam berat masuk ke dalam jaringan tubuh makhluk hidup melalui beberapa jalan yaitu melalui saluran pernafasan, saluran pencernaan dan melalui penetrasi kulit. Di dalam tubuh hewan, logam
Budiono (2003) menyatakan bahwa toksisitas logam berat yang melukai insang dan struktur jaringan luar lainnya, dapat menyebabkan kematian terhadap
ikan yang disebabkan oleh proses anoxemia, yaitu terhambatnya fungsi sirkulasi dan ekskresi dari insang. Unsur–unsur logam yang berpengaruh terhadap insang adalah timah, seng, besi, tembaga dan merkuri. Enzim yang sangat berperan dalam insang ikan ialah enzim karbonik anhidrase dan transpor ATP ase. Karbonik anhidrase adalah enzim yang mengandung Zn dan berfungsi menghidrolisis CO2 menjadi asam karbonat. Apabila ikatan Zn itu diganti dengan
logam lain, fungsi enzim karbonik anhidrase tersebut akan menurun.
Toksisitas sub akut logam berat terhadap organisme air erat hubungannya dengan sifat bioakumulasi logam dalam jaringan organisme air tersebut. Toksisitas sub akut logam berat ini diantaranya dapat menghambat aktivitas enzim. Seperti aktifitas enzim alpha-glycerophosphat dehydrogenase yang terdapat dalam jaringan ikan dihambat oleh beberapa ion logam dengan urutan intensitas sebagai berikut: Hg+2 > Cd+2 > Zn+2 > Pb+2 > Ni+2 >Co+2 (Darmono 1995). Tetapi berdasarkan toksisitasnya terhadap organisme air sendiri, urutan itu berbeda. Urutan toksisitas itu adalah sebagai berikut: Hg+2>Ag+>Cu+2>Zn+2> Ni+2>Pb+2>Cd+2>As+2>Cr+3>Sn+3>Fe+3>Mn+2>Al+3>Be+2>Li+.
Bentuk organik dan inorganik dari Hg menyebabkan pengaruh yang berbeda pada insang ikan (Olson dan Fromm Lock et al.,dalam Sorensen (1991). Sorensen (1991) menyatakan bahwa reaksi toksisitas akut dari Hg+2 dan CH3Hg+
berpengaruh pada lapisan epitel lamella sekunder pada insang. Hg+2 inorganik menyebabkan nekrosis yang hebat pada sel epitel pada rainbow trout (Salmo gairdneri). Berbeda dengan CH3Hg+, senyawa ini dapat menyebabkan hiperplasia
pada sel epitel dalam bentuk gelembung pertambahan sel epitel tersebut. Pengaruh Hg+2 pada anak ikan rainbow trout atau fingerling yaitu dapat menghasilkan sel mucosa dalam jumlah yang banyak sedangkan CH3Hg+ tidak
berpengaruh (Wobeser dalam Sorensen 1991). Hg+2 inorganik akan terjebak dalam sel mukosa sedangkan CH3Hg+ terlihat lebih mudah melewati sel mukosa
dapat menyebabkan kerusakan jaringan pada insang yaitu berupa hipertropi dan hiperplasia pada lapisan epitel insang.
Salinitas dan Osmoregulasi
Salinitas dapat didefisnisikan sebagai konsentrasi total semua ion yang terlarut dalam air (Boyd 1982). Salinitas dinyatakan dalam satuan gram/kg atau promil (%0). Salinitas berhubungan erat dengan tekanan osmotik dan tekanan
ionik air, sebagai media internal maupun eksternal (Affandi dan Tang 2002). Sifat osmotik air bergantung pada seluruh ion yang terlarut dalam air tersebut, tingkat
kepekatan osmotik larutan akan semakin tinggi dengan semakin besar jumlah ion yang terlarut, hal ini menyebabkan semakin bertambah besar tekanan osmotik medium. Ion-ion yang dominan dalam menentukan tekanan osmotik (osmolaritas) air laut adalah Na+ dan Cl-.
Ikan mempunyai tekanan osmotik yang berbeda dengan lingkunganya, oleh karena itu ikan harus mengatur tekanan osmotiknya dengan mencegah kelebihan air atau kekurangan air dalam tubuhnya agar proses fisiologi dalam tubuhnya berlangsung normal (Affandi dan Usman 2002). Selanjutnya Fujaya (2004) menyatakan bahwa osmoregulasi adalah upaya hewan air untuk mengontrol keseimbangan air dan ion antara tubuh dan lingkunganya, atau suatu proses pengaturan tekanan osmotik. Semakin jauh perbedaan tekanan osmotik antara tubuh dan lingkungan maka semakin banyak energi metabolisme yang dibutuhkan untuk melakukan proses osmoregulasi sebagai upaya adaptasi, namun tetap ada batas toleransi.
Osmoregulasi pada ikan air laut berbeda dengan ikan air tawar. Ikan air laut hidup dalam media yang memiliki konsentrasi osmotik lebih besar dari cairan tubuhnya sehingga ikan cenderung kehilangan air melalui kulit dan insang serta kemasukan garam-garam. Oleh sebab itu ikan banyak minum air laut yang
sehingga sejumlah garam yang ada dalam tubuh ikan akan hilang melalui permukaan jaringan insang dan kulit pada proses difusi, melalui feces dan juga
urin. Untuk menjaga agar garam-garam tubuh yang hilang seminimum mungkin, maka dilakukan penyerapan kembali garam-garam dalam pembuluh proksimal ginjal. Kehilangan garam-garam ini akan digantikan oleh garam-garam yang terdapat dalam pakan dan penyerapan aktif ion-ion garam yang berasal dari lingkungan perairan melalui insang (Baldisserotto 2007).
Selanjutnya ikan air laut yang dipindahkan ke media yang bersalinitas lebih rendah akan kemasukan air secara terus menerus pada kecepatan yang tidak normal dan mendapat keseimbangan kembali setelah 10 – 48 jam. Sebaliknya ikan air tawar yang dipindahkan ke media yang bersalinitas lebih tinggi akan kemasukan garam-garam (Black dalam Fitrani 2009).
Alava (1998) mengemukakan bahwa pemeliharaan juvenil ikan bandeng pada salinitas 0 ppt dapat meningkatkan laju pertumbuhan karena dilihat dari tahapan perkembangannya juvenil ikan bandeng akan beruaya dari perairan laut masuk ke lingkungan estuari atau air tawar. Selanjutnya Swanson (1998) menyatakan bahwa pemeliharaan juvenil ikan bandeng pada salinitas yang tinggi (55 ppt) dapat menurunkan kemampuan osmoregulasi dan kinerja renang ikan. Hal ini menunjukkan bahwa adaptasi salinitas pada ikan eurihalin harus mempertimbangkan interaksi efek salinitas pada proses fisiologis dan tingkah laku
METODE PENELITIAN
Penelitian ini terdiri atas 2 tahap yaitu penelitian pendahuluan dan penelitian inti. Penelitian pendahuluan terdiri atas 2 tahap yaitu uji nilai kisaran (range value test) dan uji toksisitas akut merkuri. Sedangkan penelitian inti yaitu pemeliharaan ikan bandeng pada media yang tercemar merkuri dengan salinitas berbeda.
Persiapan Penelitian
Akuarium yang digunakan sebelumnya dicuci bersih dan diberi desinfektan. Selanjutnya akuarium diisi air sesuai dengan volume pada perlakuan dan diaerasi selama 1 hari agar jenuh oksigen. Sedangkan untuk membuat larutan stok merkuri nitrat dilakukan pelarutan merkuri nitrat ke dalam akuades.
Sebelum melakukan penelitian pendahuluan, terlebih dahulu dilakukan aklimatisasi ikan uji. Aklimatisasi ini dilakukan selama seminggu yang bertujuan untuk membiasakan ikan agar dapat hidup dalam suasana laboratorium.
Penelitian Pendahuluan Tahap 1
Penelitian pendahuluan tahap 1 adalah melakukan uji nilai kisaran (range value test) merkuri yang bertujuan untuk menentukan ambang batas atas (N) dan ambang batas bawah (n) yang digunakan untuk uji toksisitas akut. Konsentrasi ambang batas atas adalah konsentrasi terendah dari bahan uji yang dapat menyebabkan semua ikan uji mati pada periode waktu pemaparan 24 jam. Sedangkan konsentrasi ambang batas bawah adalah kosentrasi tertinggi dari bahan uji yang dapat menyebabkan semua hewan uji hidup setelah pemaparan 48 jam.
Waktu dan Tempat
Alat dan Bahan Wadah Percobaan
Wadah yang digunakan adalah akuarium dengan ukuran 30 x 30 x 30 cm3 sebanyak 15 unit. Masing-masing akuarium diisi dengan air sebanyak 20 liter.
Media Percobaan
Untuk media percobaan digunakan air tawar. Sebelum digunakan air tersebut diendapkan dan diaerasi selama 24 jam agar jenuh oksigen.
Bahan Uji
Ikan yang digunakan adalah ikan bandeng dengan ukuran 7-8 cm dan bobot 3-5 gram sebanyak 150 ekor dengan padat tebar 10 ekor/akuarium. Sedangkan bahan pencemar yang digunakan adalah Merkuri Nitrat (Hg(NO3)2)
dengan penentuan konsentrasi menggunakan metode logaritmik berbasis 10 (lampiran 1) yaitu A (kontrol), B (0.006), C (0.06), D (0.6), dan E (6) mg Hg/l dengan 3 ulangan tiap perlakuan. Perhitungan konsentrasi larutan uji mengacu pada persamaan berikut:
V1 N1 = V2 N2
Keterangan:
N1 : Konsentrasi merkuri dalam larutan stok (mg/l)
V1 : Volume larutan stok yang akan diambil (ml)
N2 : Konsentrasi merkuri yang diinginkan dalam media air (mg/l)
V2 : Volume media air penelitian yang diinginkan (ml)
Parameter Pengamatan
Selama penelitian, setiap unit akuarium diberi aerasi namun tidak dilakukan pergantian air dan pemberian pakan. Parameter yang diukur adalah mortalitas ikan yang dihitung pada jam ke- 0, 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22 dan 24. Sedangkan perhitungan berikutnya dilakukan setiap 6 jam sekali sampai jam ke- 48.
Tahap 2
Penelitian pendahuluan tahap 2 adalah melakukan uji toksisitas akut untuk mengetahui toksisitas akut merkuri yang dinyatakan dengan LC50. Nilai LC50 yang
Waktu dan Tempat
Penelitian pendahuluan tahap 2 ini dilakukan di Laboratorium Lingkungan
Departemen Ilmu Akuakultur Fakultas Perikanan IPB. Penelitian ini dilakukan selama 96 jam (4 hari).
Alat dan Bahan Wadah Percobaan
Wadah yang digunakan adalah akuarium dengan ukuran 30 x 30 x 30 cm3 sebanyak 15 unit. Masing-masing akuarium diisi dengan air sebanyak 20 liter.
Media Percobaan
Untuk media percobaan digunakan air tawar. Sebelum digunakan air tersebut diendapkan dan diaerasi selama 24 jam agar jenuh oksigen.
Bahan Uji
Ikan yang digunakan adalah ikan bandeng dengan ukuran 7-8 cm dan bobot 3-5 gram sebanyak 150 ekor dengan padat tebar 10 ekor/akuarium. Sedangkan bahan pencemar yang digunakan adalah Merkuri Nitrat (Hg(NO3)2).
Dari uji nilai kisaran didapatkan bahwa nilai ambang batas atas (N) adalah 0.6 mg Hg/l dan nilai ambang batas bawah adalah 0.06 mg Hg/l. Nilai ambang batas dan ambang bawah ini dimasukkan kedalam rumus menurut Wardoyo (1977), sehingga didapatkan konsentrasi yang akan digunakan dalam uji toksisitas ini. Rumus tersebut adalah sebagai berikut:
Log N/n = k (log a – log n) a/n = b/a = c/b = d/c = N/d Keterangan:
N : Konsentrasi ambang atas n : Konsentrasi ambang bawah
k : Jumlah konsentrasi yang diuji
a,b,c,d : Konsentrasi yang diuji dengan nilai a sebagai konsentrasi terkecil
Rancangan Percobaan
A : Tanpa merkuri B : 0.110 mg Hg/l
C : 0.195 mg Hg/l D : 0.347 mg Hg/l E : 0.618 mg Hg/l
Metode dan Parameter Pengamatan
Selama penelitian tidak dilakukan pergantian air dan setiap perlakuan diberi aerasi agar kematian ikan tidak disebabkan karena kekurangan oksigen.
Parameter yang diukur adalah mortalitas ikan yang dihitung pada jam ke- 0, 6, 12, 18, 24 dan selanjutnya dilakukan perhitungan setiap 12 jam sekali sampai jam ke- 96. Indikator pengamatan tingkah laku ikan uji yaitu gejala Ram-jet ventilation
(mulut terbuka terus menerus dan tutup insang terabduksi), frekuensi pernafasan yaitu gerak membuka dan menutup insang/mulut per menit (perhitungan dimulai dari 30 menit setelah pemberian bahan uji dan selanjutnya dibandingkan dengan kontrol), pola gerak renang dan refleksi (normal, diam di dasar, ke permukaan, tidak seimbang, atau kehilangan gerak reflek). Sedangkan pengukuran fisika kimia air dilakukan setiap hari.
Analisa Data
Untuk dapat menentukan nilai konsentrasi LC50 dilakukan analisa probit
dengan SPSS 17. Analisa probit adalah suatu cara transformasi statistik dari data presentase kematian ke dalam varian yang disebut probit dan kemudian digunakan untuk menentukan fungsi regresi probit dengan log konsentrasi agar dapat mengestimasi LC50.
Penelitian Inti
Waktu dan Tempat
Penelitian inti dilakukan di Laboratorium Lingkungan Departemen Ilmu
Akuakultur Fakultas Perikanan IPB. Penelitian inti ini dilakukan selama 30 hari.
Alat dan Bahan Wadah Percobaan
Wadah yang digunakan adalah akuarium dengan ukuran 60 x 30 x 40 cm3 sebanyak 12 unit. Masing-masing akuarium diisi dengan air sebanyak 40 liter dengan tanpa resirkulasi (static renewal).
Media Percobaan
Untuk media percobaan digunakan campuran air laut dan air tawar. Sebelum digunakan campuran air tersebut diendapkan dan diaerasi selama 24 jam agar jenuh oksigen. Untuk pergantian air setiap harinya dibuat media stok dengan salinitas 20 ppt, 10 ppt dan air tawar.
Bahan Uji
Ikan yang digunakan adalah ikan bandeng dengan ukuran 7 – 8 cm dan bobot 3 - 5 gram sebanyak 240 ekor dengan padat tebar 20 ekor/akuarium. Bahan pencemar digunakan adalah merkuri dengan konsentrasi 10 % dari LC50.
Pakan
Pakan yang digunakan adalah pakan komersil berupa pellet yang akan diberikan dengan frekuensi pemberian pakan 3 kali sehari yaitu pukul 8.00, 12.00 dan 16.00 wib.
Rancangan Percobaan
Rancangan percobaan yang digunakan adalah Rancangan Acak Lengkap (RAL) dengan mengaplikasikan 4 perlakuan dan 3 ulangan. Konsentrasi merkuri yang digunakan mengacu pada hasil penelitian pendahuluan. Satuan percobaan yang digunakan adalah sebagai berikut (Lampiran 1):
Metode dan Parameter Pengamatan
Ikan yang digunakan untuk penelitian inti sebelumnya diaklimasi pada air tawar, salinitas 10 ppt dan 20 ppt selama lebih kurang 5 hari. Untuk mendapatkan
media percobaan dengan tingkat salinitas yang sesuai dengan perlakuan yang diterapkan, maka dilakukan pengenceran air laut dengan air tawar (lampiran 2). Sedangkan untuk mendapatkan salinitas yang sesuai dengan perlakuan dilakukan perubahan salinitas secara bertahap dengan perubahan 3 ppt setiap harinya sehingga ikan dapat bertahan dan menyesuaikan diri dengan salinitas yang baru. Selama durasi aklimasi ikan, media pada setiap unit perlakuan diberi aerasi dan filter.
Sebelum ikan dimasukkan ke dalam media penelitian inti, ikan ditimbang terlebih dahulu sebagai data awal. Selama penelitian inti setiap unit perlakuan diberi aerasi dan dilakukan penyiponan sisa pakan dan feses yang mengendap di dasar akuarium. Selanjutnya ditambahkan air dengan konsentrasi yang sama. Sedangkan parameter yang diukur adalah:
1. Tingkat Kerja Osmotik/ Gradien Osmotik
Tingkat kerja osmotik dihitung berdasarkan formula yang digunakan oleh Anggoro (1992).
TKO = │Osmolaritas darah benih ikan (mOsm/LH2O) – Osmolaritas media
(mOsm/LH2O)│
Pengukuran tingkat kerja osmotik ikan bandeng dilakukan sebanyak 2 kali
yaitu pada awal dan akhir penelitian (lampiran 3). 2. Tingkat Konsumsi Oksigen (TKO)
Tingkat konsumsi oksigen akan diukur dengan menghitung selisih oksigen terlarut pada awal dan akhir penelitian per satuan waktu. TKO diukur dengan menggunakan toples tertutup tidak berwarna volume 3 liter yang diisi air. Air yang digunakan adalah air yang telah diaerasi selama 1 hari sehingga jenuh oksigen. Selanjutnya 1 ekor ikan yang sebelumnya telah dipuasakan selama 1 hari ditimbang kemudian dimasukkan ke dalam toples dan diukur DO awalnya. Setelah 1 jam, dihitung lagi DO akhirnya. Maka akan didapatkan tingkat konsumsi oksigen ikan tersebut dengan menggunakan rumus berikut:
Keterangan:
TKO : Tingkat konsumsi oksigen (mg O2/gr tubuh/jam)
DO awal : Oksigen terlarut pada awal pengamatan (mg/l) DO akhir : Oksigen terlarut pada akhir pengamatan (mg/l) W : Berat ikan uji (gr)
T : Periode pengamatan (jam)
V : Volume air dalam respirometer (L)
Pengukuran konsumsi oksigen pada setiap perlakuan dilakukan sebanyak 4 kali yaitu pada hari ke-0, 10, 20, dan hari ke-30.
3. Kondisi hematologi (Gambaran darah)
Pengamatan dan pengukuran gambaran darah terdiri atas:
a. Haemoglobin: metode yang digunakan metode sahli dengan sahlinometer (Wedemeyer dan Yasutake 1977).
b. Hematokrit adalah perbandingan antara volume sel darah dengan total volume darah (Anderson and Siwichki 1993).
c. Jumlah eritrosit
Σ eritrosit = Σ sel terhitung x 104
sel/mm3 (Blaxhall dan Daisley 1973) d. Jumlah leukosit mengakumulasi merkuri dalam jaringan tubuhnya. Oleh karena itu dibuat histokimia untuk melihat deposit merkuri pada jaringan ikan. Masing-masing diambil satu ekor per unit penelitian untuk diambil sampel organ dalamnya yaitu insang dan hati pada akhir penelitian. Uji histokimia ini dilakukan menggunakan
5. Kadar glukosa darah
Pemeriksaan kadar glukosa darah ikan dilakukan sebagai indikator stres
sekunder akibat toksisitas Merkuri. Pengukuran kadar glukosa darah dilakukan sebanyak 3 kali yaitu pada hari ke-0, 15 dan hari ke- 30 (lampiran 6). Rumus yang digunakan adalah:
Data laju pertumbuhan ikan uji diperoleh dengan melakukan pengambilan ikan uji pada awal dan akhir penelitian, kemudian ditimbang beratnya. Laju
pertumbuhan harian ikan dianalisa dengan menggunakan rumus berdasarkan Effendie (1979):
Efisiensi pakan dihitung dengan menggunakan rumus sebagai berikut:
Keterangan:
EP = Efisiensi pakan (%)
Bt = Biomasa mutlak ikan pada akhir percobaan (g)
Bd = Biomasa mutlak ikan yang mati selama percobaan (g)
B0 = Biomasa mutlak ikan pada awal percobaan (g)
F = Jumlah pakan yang dikonsumsi oleh ikan selama percobaan (g) 8. Kadar merkuri dalam media dan ikan bandeng
Untuk pengukuran kadar merkuri pada ikan diukur di daging ikan bandeng (Lampiran 7).
9. Kelangsungan hidup (SR)
Ikan yang dipelihara diamati setiap hari. Apabila terdapat ikan yang mati segera dikeluarkan dari wadah uji, dicatat dan tidak dilakukan pergantian ikan yang mati tersebut. Tingkat kelulusan hidup ikan bandeng dihitung dengan rumus berikut:
Keterangan:
SR : Tingkat kelangsungan hidup (%) Nt : Jumlah ikan yang hidup pada waktu t
No : Jumlah ikan yang hidup pada awal penelitian 10. Fisika kimia air
Data kualitas air yang diukur adalah salinitas, suhu, DO, pH, alkalinitas, kesadahan dan TAN. Pengukuran kualitas air dilakukan setiap 7 hari sekali selama masa penelitian.
Tabel 1. Metode dan alat untuk analisis parameter fisika kimia air
Parameter Satuan Alat
HASIL DAN PEMBAHASAN
Hasil
Penelitian Pendahuluan Uji Nilai Kisaran
Hasil uji nilai kisaran (Range value test) merkuri pada ikan bandeng menunjukkan bahwa nilai konsentrasi ambang bawah sebesar 0.06 mg Hg/l yang merupakan konsentrasi tertinggi merkuri yang tidak mematikan ikan bandeng dalam waktu pemaparan selama 48 jam. Sedangkan nilai ambang atas sebesar 0.6 mg Hg/l yang merupakan konsentrasi terendah merkuri yang dapat mematikan
100 % ikan bandeng dalam waktu pemaparan selama 24 jam. Berikut tabel data mortalitas ikan bandeng pada uji nilai kisaran (Range value test) (lampiran 8). Tabel 2. Data mortalitas ikan bandeng pada uji nilai kisaran (Range value test)
Konsentrasi
Pada perlakuan kontrol setelah jam ke- 48 tidak ditemukan ikan yang mati, hal ini menunjukkan bahwa kualitas air sebagai media pemeliharaan selama masa pemaparan dalam kondisi baik.
Uji Toksisitas Akut
Uji toksisitas akut yang dilakukan selama 96 jam dibuat dengan konsentrasi yang lebih kecil dibandingkan uji nilai kisaran. Konsentrasi yang digunakan diperoleh dari nilai yang didapatkan dari uji nilai kisaran. Untuk konsentrasi uji toksisitas yaitu perlakuan A (tanpa merkuri), perlakuan B (0,110 mg Hg/l), perlakuan C (0,195 mg Hg/l), perlakuan D (0,346 mg Hg/l) dan perlakuan E (0.618 mg Hg/l).
0.618 mg Hg/l (E) mengalami kematian sampai 100 %. Sedangkan konsentrasi 0,346 mg Hg/l (D) pada pengamatan jam ke- 36 juga mengalami kematian sampai
100 %. Selanjutnya konsentrasi 0,195 mg Hg/l (C) sampai akhir penelitian mengalami kematian sampai 90 %. Untuk perlakuan konsentrasi 0,110 mg Hg/l (B) pada jam ke- 96 kelangsungan hidup ikan bandeng mencapai 90 %. Pada ikan kontrol tidak ditemukan ikan yang mati dan gejala klinis akibat stres sampai waktu pemaparan 96 jam, hal ini menunjukkan bahwa media pemeliharaan dan keadaan ikan selama uji toksisitas akut dalam keadaan baik. Data kelangsungan hidup ikan bandeng pada uji toksisitas akut merkuri dapat dilihat pada lampiran 9.
Data mortalitas ikan bandeng selanjutnya dianalisa dengan menggunakan analisa probit (SPSS 17) untuk menentukan nilai LC50 pada waktu pemaparan
pada jam ke- 24, 48, 72 dan 96 jam (Lampiran 10, 11, 12 dan 13). Hasil analisa menunjukkan bahwa nilai LC50 pada waktu pemaparan 24, 48, 72 dan 96 jam
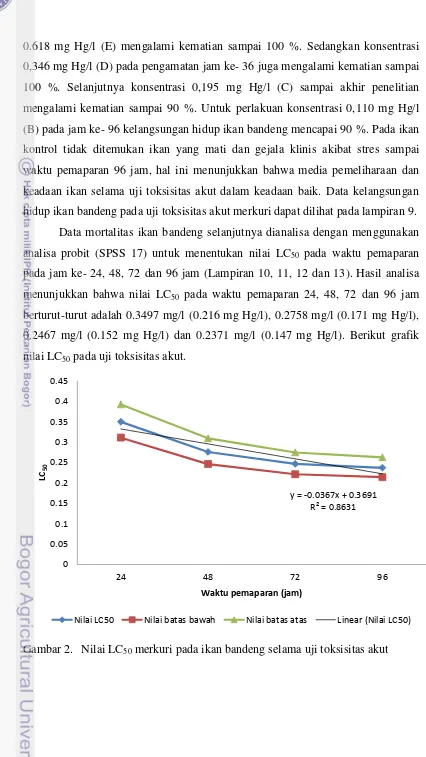
berturut-turut adalah 0.3497 mg/l (0.216 mg Hg/l), 0.2758 mg/l (0.171 mg Hg/l), 0.2467 mg/l (0.152 mg Hg/l) dan 0.2371 mg/l (0.147 mg Hg/l). Berikut grafik nilai LC50 pada uji toksisitas akut.
Gambar 2. Nilai LC50 merkuri pada ikan bandeng selama uji toksisitas akut y = -0.0367x + 0.3691
Nilai LC50 dari grafik di atas menunjukkan bahwa semakin lama waktu
pemaparan maka nilai LC50 merkuri terhadap ikan bandeng akan semakin rendah.
Dari nilai LC50 96 jam yang diperoleh dapat dikatakan bahwa merkuri bersifat
toksik sangat tinggi terhadap benih ikan bandeng.
Frekuensi buka tutup operculum ikan bandeng selama uji toksisitas akut merkuri meningkat seiring meningkatnya konsentrasi merkuri yang diberikan. Frekuensi rata-rata bukaan operculum ikan bandeng pada perlakuan A (0 ppm) adalah 68.13 kali/menit. Selanjutnya terjadi peningkatan pada setiap perlakuan yaitu perlakuan B (0.110 mg Hg/l) sebanyak 124.93 kali/menit, perlakuan C (0.195 mg Hg/l) sebanyak 130.5 kali/menit, perlakuan D (0.347 mg Hg/l) sebanyak 139.62 kali/menit dan perlakuan E (0.618 mg Hg/l) sebanyak 173.17 kali/menit (Lampiran 14). Hal ini dapat dilihat pada grafik berikut ini:
Gambar 3. Rata-rata frekuensi pergerakan operculum ikan bandeng selama uji toksisitas akut
Pemaparan ikan bandeng pada merkuri mengakibatkan rusaknya sistem pernafasan ikan bandeng tersebut, sehingga ikan akan lebih sering membuka mulut dan operculumnya untuk mendapatkan oksigen lebih banyak. Hal ini dilakukan sebagai suatu adaptasi fisiologis sehingga ikan dapat bertahan hidup atau memperlambat kematian.
Respon tingkah laku ikan bandeng setelah dipaparkan pada merkuri
menunjukkan bahwa semakin tinggi konsentrasi merkuri yang diberikan, akan mempercepat perubahan tingkah laku ikan bandeng tersebut. Perubahan tingkah
laku ikan tersebut antara lain: ikan kehilangan gerak refleks, berenang tidak beraturan dan sering muncul ke permukaan dengan bukaan mulut dan operculum
yang lebih lebar dan cepat. Kemudian kembali ke dasar dengan posisi tegak dan sampai ke dasar dengan posisi bagian ventral ke atas. Ikan juga mengalami kejang-kejang sebelum mengalami kematian di dasar akuarium. Pada perlakuan C (0.195 mg Hg/l), ikan mengalami ram-jet ventilation sebelum mengalami kematian. hal ini disebabkan karena ikan terpapar merkuri pada konsentrasi yang tinggi dan jangka waktu yang lama sehingga sistem pernafasannya mengalami kerusakan yang parah.
Penelitian Inti
Pengaruh Merkuri Pada Ikan Bandeng yang Dipelihara di Air Tawar (0 ppt) Gradien Osmotik
Dari hasil penelitian dapat diketahui bahwa gradien osmotik ikan bandeng yang terpapar merkuri (perlakuan B) lebih tinggi dibandingkan kontrol (perlakuan A) dimana perlakuan B sebesar 0.303±0.093 Osm/kg dan perlakuan A sebesar 0.284±0.025 Osm/kg (Lampiran 15). Hal ini mengakibatkan energi yang dibutuhkan oleh ikan pada perlakuan B untuk proses osmoregulasi lebih besar dibandingkan ikan kontrol. Berikut grafik gradien osmotik ikan bandeng yang terpapar dan tidak terpapar merkuri di air tawar.
Gambar 4. Gradien osmotik ikan bandeng yang terpapar merkuri dan tidak terpapar merkuri di air tawar
Tingkat Konsumsi Oksigen
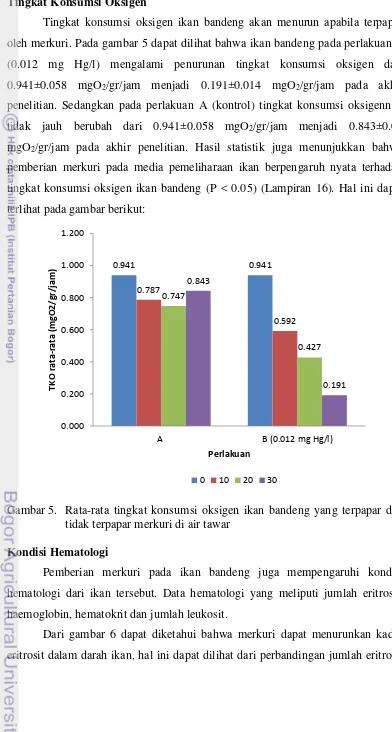
Tingkat konsumsi oksigen ikan bandeng akan menurun apabila terpapar
oleh merkuri. Pada gambar 5 dapat dilihat bahwa ikan bandeng pada perlakuan B (0.012 mg Hg/l) mengalami penurunan tingkat konsumsi oksigen dari 0.941±0.058 mgO2/gr/jam menjadi 0.191±0.014 mgO2/gr/jam pada akhir
penelitian. Sedangkan pada perlakuan A (kontrol) tingkat konsumsi oksigennya tidak jauh berubah dari 0.941±0.058 mgO2/gr/jam menjadi 0.843±0.06
mgO2/gr/jam pada akhir penelitian. Hasil statistik juga menunjukkan bahwa
pemberian merkuri pada media pemeliharaan ikan berpengaruh nyata terhadap tingkat konsumsi oksigen ikan bandeng (P < 0.05) (Lampiran 16). Hal ini dapat terlihat pada gambar berikut:
Gambar 5. Rata-rata tingkat konsumsi oksigen ikan bandeng yang terpapar dan tidak terpapar merkuri di air tawar
Kondisi Hematologi
Pemberian merkuri pada ikan bandeng juga mempengaruhi kondisi hematologi dari ikan tersebut. Data hematologi yang meliputi jumlah eritrosit, haemoglobin, hematokrit dan jumlah leukosit.
Dari gambar 6 dapat diketahui bahwa merkuri dapat menurunkan kadar eritrosit dalam darah ikan, hal ini dapat dilihat dari perbandingan jumlah eritrosit
ikan kontrol (perlakuan A) dengan jumlah eritrosit ikan perlakuan B. Jumlah eritrosit ikan perlakuan B adalah 3.39±0.62 x 106 sel/mm3 sedangkan jumlah
eritrosit ikan kontrol jauh lebih besar yaitu 5.63±0.46 x 106 sel/mm3. Kadar haemoglobin pada perlakuan B juga mengalami penurunan dibandingkan perlakuan kontrol. Kadar haemoglobin ikan perlakuan B adalah 4.47±0.46 % sedangkan perlakuan A sebesar 9.33±0.5 %. Untuk kadar hematokrit perlakuan B juga lebih rendah dibandingkan ikan kontrol yaitu sebesar 10.16±0.32 %. Jumlah leukosit ikan perlakuan B juga lebih rendah dibandingkan ikan kontrol yaitu sebesar 8.37±0.66 x 105 sel/mm3. Hal ini juga didukung dengan uji statistik yang menyatakan bahwa merkuri berpengaruh nyata (P<0.05) terhadap penurunan jumlah eritrosit, haemoglobin, hematokrit dan leukosit pada ikan bandeng yang dipelihara di air tawar (Lampiran 17, 18 19 dan 20). Berikut grafik kondisi hematologi ikan yang terpapar dan tidak terpapar merkuri di air tawar.
Gambar 6. Kondisi hematologi ikan bandeng yang terpapar dan tidak terpapar merkuri di air tawar
Histokimia
Histokimia merupakan salah satu cara yang digunakan untuk melihat deposit logam berat seperti merkuri dalam jaringan makhluk hidup. Hasil histokimia menunjukkan bahwa ada deposit merkuri dalam jaringan insang dan hati ikan bandeng yang terkontaminasi oleh merkuri di air tawar.
Gambar 7. Histokimia ikan bandeng pada perlakuan A (kontrol) a. Insang; b. Hati.
Gambar 8. Histokimia ikan bandeng pada perlakuan B (0.012 mg Hg/l) a. Insang; b. Hati
Kadar Glukosa Darah
Kadar glukosa darah merupakan salah satu pendekatan yang digunakan untuk bisa mengenali ikan dalam kondisi stres. Dari hasil penelitian dapat diketahui bahwa penambahan merkuri pada media air tawar meningkatkan kadar glukosa darah ikan bandeng selama waktu pemaparan. Hal ini mengindikasikan bahwa ikan bandeng mengalami stress akibat pemaparan merkuri pada media pemeliharaan.
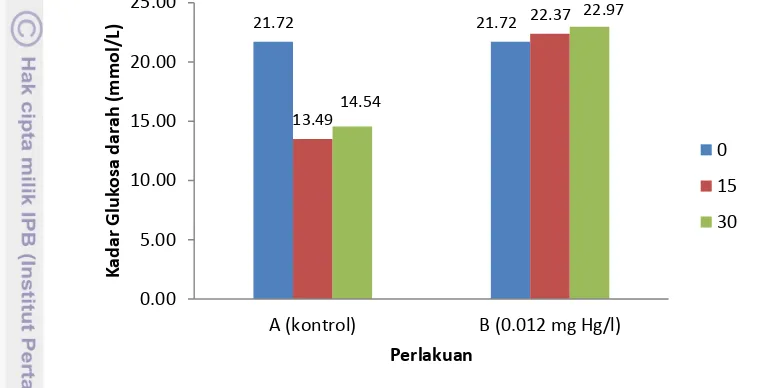
Dari gambar 9 dapat diketahui bahwa terjadi peningkatan kadar glukosa darah pada ikan bandeng perlakuan B dengan konsentrasi merkuri 0.012 mg Hg/l dari 21.72 mmol/L menjadi 22.97 mmol/L pada hari ke 30 waktu pemaparan. Sedangkan pada perlakuan A (kontrol) terjadi penurunan kadar glukosa darah dari
50 µm a 50 µm b
Hg
21.72 mmol/L menjadi 14.54 mmol/L pada hari ke 30 waktu pemaparan. Hal ini menunjukkan bahwa ikan pada perlakuan B (0.012 mg Hg/l) mengalami stress
akibat pemaparan merkuri pada media pemeliharaan. Dari uji statistik juga memperlihatkan adanya pengaruh yang nyata (P < 0.05) (Lampiran 21) pemberian merkuri terhadap peningkatan kadar glukosa darah ikan bandeng.
Gambar 9. Rata-rata kadar glukosa darah ikan bandeng yang terpapar dan tidak terpapar merkuri di air tawar
Jumlah Konsumsi Pakan
Jumlah pakan yang dikonsumsi ikan bandeng mengalami penurunan setelah terpapar merkuri. Hal ini dapat dilihat pada grafik berikut ini.
Gambar 10. Rata-rata jumlah pakan yang dikonsumsi ikan bandeng yang terpapar dan tidak terpapar merkuri di air tawar.
Ikan yang terpapar merkuri di air tawar mengalami stres sehingga menyebabkan kadar glukosa darah meningkat. Akibatnya nafsu makan ikan
menurun sehingga ikan kurang respon terhadap pakan yang diberikan.
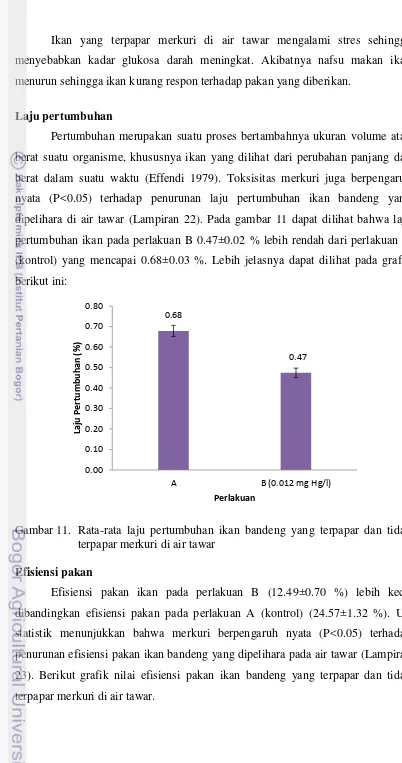
Laju pertumbuhan
Pertumbuhan merupakan suatu proses bertambahnya ukuran volume atau berat suatu organisme, khususnya ikan yang dilihat dari perubahan panjang dan berat dalam suatu waktu (Effendi 1979). Toksisitas merkuri juga berpengaruh nyata (P<0.05) terhadap penurunan laju pertumbuhan ikan bandeng yang
Gambar 12. Rata-rata nilai efisiensi pakan ikan bandeng yang terpapar dan tidak terpapar merkuri di air tawar
Kadar Merkuri di Air dan di Daging Ikan Bandeng
Kadar merkuri dalam media pemeliharaan ikan dan daging ikan dihitung pada awal dan akhir penelitian. Hasil penelitian menunjukkan bahwa terjadi penurunan kadar merkuri di air dan peningkatan kadar merkuri di tubuh ikan setelah terpapar merkuri 0.012 mg Hg/l pada perlakuan B selama 30 hari. Hal ini terjadi karna merkuri dapat diabsorbsi dan terakumulasi dalam jaringan tubuh ikan bandeng tersebut. Sedangkan pada perlakuan A (kontrol) tidak terjadi perubahan kadar merkuri baik di air maupun di daging ikan bandeng. Berikut grafik kadar merkuri dalam media dan tubuh ikan bandeng pada akhir penelitian.
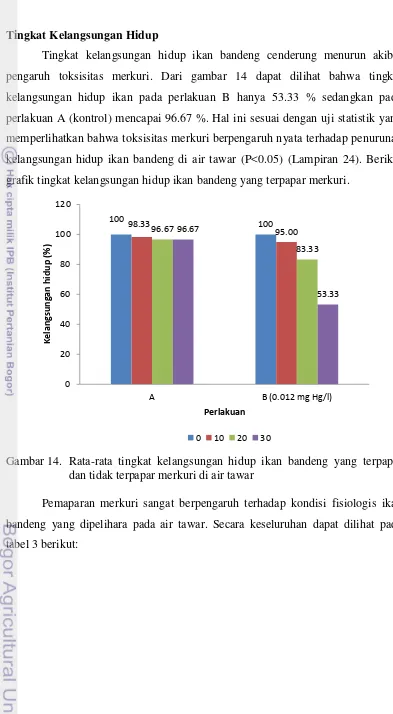
Tingkat Kelangsungan Hidup
Tingkat kelangsungan hidup ikan bandeng cenderung menurun akibat
pengaruh toksisitas merkuri. Dari gambar 14 dapat dilihat bahwa tingkat kelangsungan hidup ikan pada perlakuan B hanya 53.33 % sedangkan pada perlakuan A (kontrol) mencapai 96.67 %. Hal ini sesuai dengan uji statistik yang memperlihatkan bahwa toksisitas merkuri berpengaruh nyata terhadap penurunan kelangsungan hidup ikan bandeng di air tawar (P<0.05) (Lampiran 24). Berikut grafik tingkat kelangsungan hidup ikan bandeng yang terpapar merkuri.
Gambar 14. Rata-rata tingkat kelangsungan hidup ikan bandeng yang terpapar dan tidak terpapar merkuri di air tawar
Tabel 3. Data parameter pengamatan ikan bandeng yang terpapar dan tidak terpapar merkuri di air tawar
Parameter pengamatan Perlakuan
A (kontrol) B (0.012 mg Hg/l)
Gradien osmotik (Osm/kg) 0.284±0.025 0.303±0.093
Tingkat konsumsi oksigen (mgO2/g/jam) 0.843±0.06 0.191±0.014
∑ Eritrosit (106 sel/mm3) 5.63±0.46 3.39±0.62
Kadar Haemoglobin (%) 9.33±0.5 4.47±0.46
Kadar Hematokrit (%) 21.06±0.27 10.16±0.32
∑ Leukosit (105 sel/mm3) 30.59±1.88 8.37±0.66
Kadar Glukosa darah (mmol/L) 14.54±0.91 22.97±1.33
∑ konsumsi pakan (g) 72.17±1.19 61.81±1.47
Laju Pertumbuhan (GR) (%) 0.68±0.03 0.47±0.02
Efisiensi Pakan (EP) (%) 24.57±1.32 12.49±0.70
Kadar Hg di air (ppm) <0.0002 0.0081
Kadar Hg di daging ikan (ppm) 0.0005 0.2664
Kelangsungan Hidup (SR) (%) 96.67 53.33
Pengaruh Salinitas dan Toksisitas Merkuri Terhadap Ikan Bandeng
Pada perlakuan ini konsentrasi merkuri yang diberikan sama yaitu 0.012 mg Hg/l pada salinitas 0 ppt, 10 ppt dan 20 ppt.
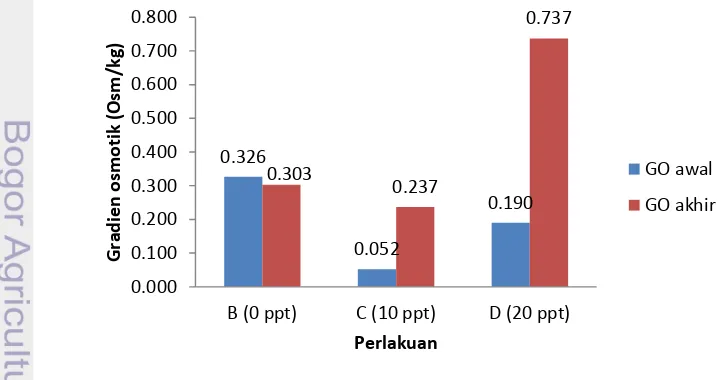
Gradien Osmotik
Selisih antara nilai osmolaritas cairan tubuh dan osmolaritas media pemeliharaan ikan dapat diartikan sebagai nilai gradien osmotik. Toksisitas merkuri pada salinitas yang berbeda sangat mempengaruhi gradien osmotik ikan Bandeng yang dipelihara. Hal ini dapat dilihat pada gambar berikut:
Dari gambar 15 dapat diketahui gradien osmotik yang terkecil pada perlakuan C (10 ppt) (Lampiran 15). Hal ini menunjukkan energi yang dibutuhkan
untuk proses osmoregulasi lebih sedikit pada perlakuan C (10 ppt) dibandingkan perlakuan B (0 ppt) dan perlakuan D (20 ppt) sehingga banyak energi yang tersimpan untuk pertumbuhan dan pertahanan tubuh.
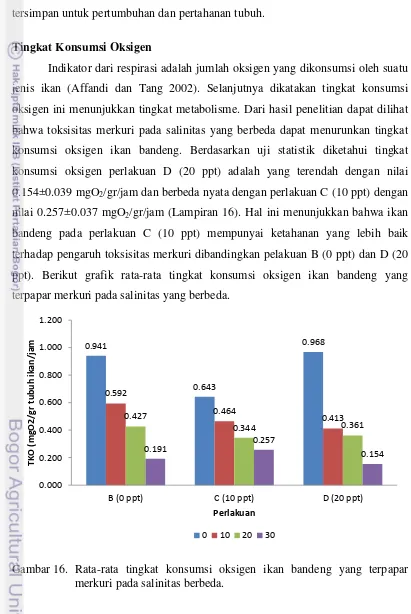
Tingkat Konsumsi Oksigen
Indikator dari respirasi adalah jumlah oksigen yang dikonsumsi oleh suatu jenis ikan (Affandi dan Tang 2002). Selanjutnya dikatakan tingkat konsumsi
oksigen ini menunjukkan tingkat metabolisme. Dari hasil penelitian dapat dilihat bahwa toksisitas merkuri pada salinitas yang berbeda dapat menurunkan tingkat konsumsi oksigen ikan bandeng. Berdasarkan uji statistik diketahui tingkat konsumsi oksigen perlakuan D (20 ppt) adalah yang terendah dengan nilai 0.154±0.039 mgO2/gr/jam dan berbeda nyata dengan perlakuan C (10 ppt) dengan
nilai 0.257±0.037 mgO2/gr/jam (Lampiran 16). Hal ini menunjukkan bahwa ikan
bandeng pada perlakuan C (10 ppt) mempunyai ketahanan yang lebih baik terhadap pengaruh toksisitas merkuri dibandingkan pelakuan B (0 ppt) dan D (20 ppt). Berikut grafik rata-rata tingkat konsumsi oksigen ikan bandeng yang terpapar merkuri pada salinitas yang berbeda.
Kondisi Hematologi
Data hematologi meliputi jumlah eritrost, haemoglobin, hematokrit dan
leukosit. Berikut gambar grafik perubahan kondisi hematologi ikan bandeng yang dipelihara pada salinitas berbeda. Dari gambar 17 dapat diketahui bahwa kondisi hematologi terbaik terdapat pada perlakuan C (10 ppt) dengan jumlah eritrosit 3.61±0.39 x 106 sel/mm3, haemoglobin 5.37±0.86 %, hematokrit 19.90±0.41 % dan jumlah leukosit 11.33±0.43 x 105 sel/mm3. Hasil analisa statistik menunjukkan bahwa toksisitas merkuri berpengaruh nyata (P<0.05) terhadap penurunan kadar haemoglobin, hematokrit dan jumlah leukosit pada setiap perlakuan (Lampiran 17, 18 19 dan 20). Grafik kondisi hematologi ikan bandeng yang terpapar merkuri pada salinitas yang berbeda disajikan pada gambar di bawah ini.
Gambar 17. Rata-rata kondisi hematologi ikan bandeng yang terpapar merkuri pada salinitas berbeda
Histokimia
Merkuri merupakan salah satu logam berat yang mudah diabsorbsi dan terakumulasi dalam jaringan tubuh ikan. Insang dan Hati merupakan jaringan yang rentan terhadap akumulasi merkuri. Akumulasi merkuri tersebut dapat berupa deposit yang dapat mengganggu kerja insang dan hati tersebut.