Lampiran 1. Bobot kering (g) sisa serasah daun C. tagal tiap ulangan pada berbagai salinitas
Salinitas Ulangan Lama masa dekomposisi
Kontrol 15 30 45 60 75 90
Lampiran 3. Perhitungan Laju Dekomposisi Metode Oslon (Oslon, 1963 dalam Subhkan, 1991) :
Dimana : Xt = Berat serasah setelah periode pengamatan ke-t
X0 = Berat serasah awal
e = Bilangan logaritma (2,72)
t = Periode pengamatan k = Laju dekomposisi
A. Salinitas 0-10 ppt Xt = 17,99 gr
X0 = 50 gr
B. Salinitas 11-20 ppt Xt = 14,98 gr
Lampiran 3. Lanjutan
C. Salinitas 21-30 ppt Xt = 22,36 gr
X0 = 50 gr
Lampiran 4. Laju rata-rata dekomposisi serasah daun C. tagal
Laju Dekomposisi Salinitas 0-10 ppt Salinitas 11-20 ppt Salinitas 21-30 ppt
Hari ke 15 0,011 0,013 0,016
Hari ke 30 0,025 0,045 0,046
Hari ke 45 0,045 0,070 0,060
Hari ke 60 0,050 0,116 0,100
Hari ke 75 0,169 0,167 0,165
Lampiran 5. Makrobentos yang terdapat dalam kantong serasah daun C. tagal
Salinitas Ulangan Hari ke- Organisme Jumlah
0-10 ppt
Siput, Cacing, Kepiting 5
U2 Cacing, siput 4
Siput, Cacing, kepiting 6
U2 Cacing, siput 3
Lampiran 5. Lanjutan
Salinitas Organisme Jumlah
0-10 ppt Kepiting, Cacing, , siput 80
11-20 ppt Cacing, kepiting, siput 86
21-30 ppt Siput, , cacing, kepiting 78
DAFTAR PUSTAKA
Allo, M. P. R., Fahruddin, Eva, J. 2014. Pengaruh Jenis Bioaktivator pada Laju Dekomposisi Sampah Daun Ki Hujan Samanea Saman dari Wilayah Kampus unhas. UNHAS Press. Makassar.
Alrasjid, H. 1986. Jalur Hijau Pengelolaan Hutan Mangrove Pamanukan, Jawa Barat. Bul. Pen. Hutan 475 : 29 - 65.
Ansori, S. 1998. Studi Sifat Fisik dan Pasang Surut Air Laut Terhadap Penyebaran Jenis Rhizophora Hutan Mangrove Pantai Tempora Jatim. Fakultas Kehutanan. Institut Pertanian Malang. Malang.
Anwar, E.K. 2007. Pengaruh inokulan cacing tanah dan pemberian bahan organik terhadap kesuburan dan produktivitas Tanah Ultisol. J. Tanah Trop. 12 (2) : 121-130
Aprianis, Y. 2011. Produksi dan Laju Dekomposisi Serasah Acacia Crassicarpa A. Cunn di PT.ARARA ABADI. Balai Penelitian Hutan Penghasil Serat. Riau.
Azis, Nurdiana. 2006. Analisis Ekonomi Alternatif Pengelolaan Ekosistem Mangrove Kecamatan Barru Kabupaten Barru. Bogor: Institut Pertanian Bogor.
Bengen, D.G. 2002. Pedoman Teknis Pengenalan dan Pengelolaan Ekosistem Mangrove. Pusat Kajian Sumberdaya Pesisir dan Lautan. Institut Pertanian Bogor, Bogor.
Dahuri, R. 2003. Keanekaragaman Hayati Laut Aset Pembangunan Berkelanjutan Indonesia. PT. Gramedia Pustaka Utama, Jakarta.
Darkuni, M. N. 2001. Mikrobiologi (Bakteriologi, Virologi, dan Mikologi). Universitas Negeri Malang.
Dedi, S. 2008. Ekosistem Mangrove. Ekologi Laut Tropis. Institut Pertanian Bogor.
Dewi, N. 2010. Laju Dekomposisi Serasah Daun Avicennia marina Pada Berbagai Tingkat Salinitas di Kawasan Hutan Mangrove Sicanang Belawan Medan. [Skripsi]. USU. Medan.
Dita, F. L. 2007. Pendugaan Laju Dekomposisi Serasah Daun Shorea balangeran
(Korth.) Burck Dan Hopea bancana (Boerl.) Van Slooten Di Hutan
Effendi, H. 2003. Telaah Kualitas Air Bagi Pengelolaan Sumberdaya dan
Lingkungan Perairan. Penerbit Kanisius. Yogyakarta.
Emma, L.S. 2009. Jenis-jenis Fungi Yang Terdapat Pada Serasah Daun Rhizophora Mucronata Yang Mengalami Dekomposisi Pada Berbagai Tingakt Salinitas [Skripsi]. USU Press. Medan.
Ghufron, M. H. Kordi K. M. 2012. Ekosistem Mangrove : Potensi, Fungsi, Dan Pengelolaan. p. 44-45. Jakarta: PT. Rineka Cipta.
Gultom, I, M. 2009. Laju Dekomposisi Serasah Daun Rhizophora mucronataPada Berbagai Tingkat Salinitas. [Skripsi]. USU. Medan.
Hogarth, P. J. 1999. The Biology of Mangrove. Oxford university Press. New York.
Hutching, P. And P. Saenger. 1987. Ecology of Mangrove. University of Queensland Press. Australia.
Indriani, Y. 2008. Produksi dan Laju Dekomposisi Mangrove Api-Api (Avicennia
marina forks. Vierh) di Desa Lontar, Kecamatan Kemiri, Kabupaten
Tangerang, Provinsi Banten. [Skripsi] Program Studi Ilmu dan Teknologi Kelautan Fakultas Perikanan dan Ilmu Kelautan, ITB. Bogor.
Mardiana, S. 2005. Perbedaan Kondisi Fisik Lingkungan Terhadap Pertumbuhan Berbagai Tanaman Mangrove. Fakultas Pertanian Universitas Medan Area. Medan. Jurnal Penelitian Bidang Ilmu Pertanian Volume 3, Nomor
1, April 2005.
Mason, C. F. 1974. Mollusca. Hlm. 555-591 dalam Biology of Plant Litter Decomposition. Vol ke-1. C.H. Dickinson dan G. J. Pugh (Peny.). Academic Press. London, New York.
Moore-Landecker, E. 1990. Fundamentals of Fungi. Fourth Edition. Prentice Hall, Englewood. New Jersey.
Mukhlis, 2007. Analisis Tanah Tanaman. USU Press. Medan.
Naibaho, R. F. 2014. Laju Dekomposisi Serasah Daun Avicennia marina dan Kontribusinya Terhadap Nutribusi di Perairan Pantai Serambi Deli Kecamatan Pantai Labu. [Skripsi]. USU. Medan.
Notohadiprawiro, T. 1998. Tanah dan Lingkungan. Direktorat Jenderal Pendidikan Tinggi Departemen Pendidikan dan Kebudayaan. Jakarta.
Odum, W.E. dan Heald, E.J. 1975. The detritus-based food web of an estuarine
mangrove community. In L.E. Cronin, ed. Estuarine Research. p. 265-286..
Diterjemahkan oleh: M. Ghufran H. Kordi K. Jakarta: PT. Rineka Cipta.
Rismunandar. 2000 . Laju Dekomposisi Serasah Daun Avicennia marina pada Berbagai Tingkat Salinitas (Studi Kasus di Kawasan Hutan Mangrove Blanakan, RPH Tegal Tangkil, BKPH Ciasem-Pamanukan, KPH Purwakarta, Perum Perhutani Unit III Jawa Barat). Skripsi. Fakultas Kehutanan. Institut Pertanian Bogor. Bogor.
Romimohtarto, K. dan Sri, J. 2001. Biologi Laut. Ilmu Pengetahuan Tentang Biota Laut. Penerbit Djambatan. Jakarta.
Setiawan, M. A. 2013. Laju Dekomposisi Serasah Daun Rhizopora mucronata Pada Berbagai Tingkat Salinitas. Jurnal Program Strata 1 Ilmu Kelautan. Universitas Padjajaran. Bandung.
Sriharti., Salim, T., 2008. Pemanfaatan Limbah Pisang Untuk Pembuatan Pupuk
Kompos Menggunakan Kompos Rotary Drum. Prosising Seminar Nasional Bidang Teknik Kimia dan Tekstil, Yogyakarta.
Soeroyo. 1993. Pertumbuhan Mangrove dan Permasalahannya. Buletin Ilmiah INSTIPER. Yogyakarta.
Subkhan. 1991. Produksi dan Penguraian Serasah Hutan Mangrove di Sungai Talidendan Besar, HPH PT Bina Lestari, Riau. Skripsi. Jurusan Konservasi Sumberdaya Hutan, Fakultas Kehutanan IPB. Bogor.
Sunarto. 2003. Peranan Dekomposisi dalam Proses Produksi pada Ekosistem Laut. Pengantar Falsafah Sains, Program Pascasarjana/S3 IPB. Bogor.
Parmelee, R. W., Beare, W. Cheng, P. F. Hendrix, S.J. Rider, D. A. Crossley Jr., and D. C. Coleman. 1990. Earthworm and Enchytraeids in conventional and notilage agroecosystems: A biocide approach to ases theirnrolenin organic matter breakdown. Biol. Fertil. Soil 10: 1-10
Vaiphasa C., A.K., Skidmore, W.F., de Boer. 2006. A Post-classifier for Mangrove Mapping Using Ecological Data.Elsevier.International Journal of Photogrammetry & Remote Sensing. 61 (1) : 1-10
METODE PENELITIAN
Lokasi dan Waktu Penelitian
Penelitian ini dilaksanakan dari bulan Juni-september 2015 di kawasan
hutan mangrove Kampumg Nipah Desa Sei Nagalawan, Kecamatan Perbaungan,
Kabupaten Serdang Bedagai, Sumatera Utara. Pengambilan sampel dilakukan di
Pulau Sembilan, Kecamatan Pangkalan Susu, Kabupaten Langkat, Sumatera
Utara. Penimbangan serasah dilakukan di Laboratorium Hama dan Penyakit
Tanaman, Fakultas Pertanian, Universitas Sumatera Utara. Analisis unsur hara
karbon (C), nitrogen (N), dan fosfor (P) di lakukan di Laboratorium Riset dan
Teknologi, Fakultas Pertanian, Universitas Sumatera Utara, Medan.
Alat dan Bahan
Bahan yang diperlukan dalam melakukan penelitian ini adalah serasah
daun Ceriops tagal yang diambil dari kawasan hutan mangrove Pulau Sembilan
Kabupaten Langkat. Peralatan yang digunakan meliputi : Hand refractometer,
oven, timbangan analitik, kantong serasah (litter bag) yang berukuran 40 x 30 cm
yang terbuat dari nilon, kantong plastik dengan ukuran ¼ kg, tali palastik, patok
bambu, amplop sampel, alat tulis dan koran.
Prosedur Penelitian Penentuan zona salinitas
Penentuan zona salinitas dilakukan dengan pengukuran tingkat salinitas
yang dilakukan dari arah laut menuju ke darat dengan menggunakan
Handrefractometer. Lokasi penelitian terdiri atas 3 zona yaitu, zona 1 dengan
berjarak 55 meter dari pantai, zona 3 dengan salinitas 21-30 ppt berjarak 262
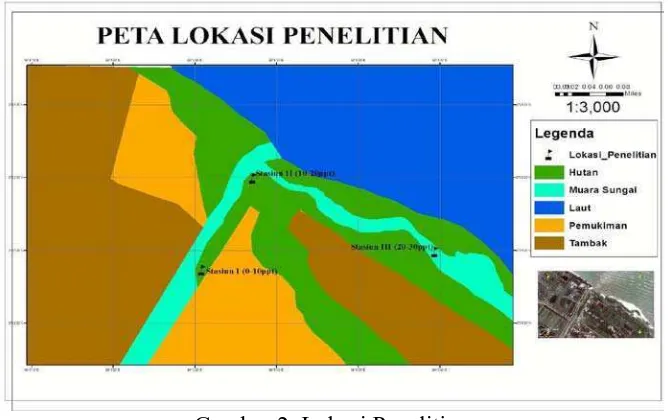
meter dari pantai dapat dilihat pada Gambar 2.
Gambar 2. Lokasi Penelitian
Pengumpulan sampel serasah daun C. tagal
Pengambilan sampel serasah daun C. tagal dilakukan di beberapa lokasi
pada hutan mangrove Pulau Sembilan, Kecamatan Pangkalan Susu, Kabupaten
Langkat, Sumatera Utara, yang banyak ditumbuhi oleh jenis C. tagal.
Pengumpulan dilakukan di Pulau Sembilan karena jumlah serasah daun C. tagal
tergolong banyak dan jumlah serasah yang dibutuhkan tersedia, berbeda dengan
lokasi penelitian yang dilakukan di Kampung Nypa Desa Sei Nagalawan yang
merupakan lokasi rehabilitas mangrove dengan jumlah serasah yang terbatas.
Pengambilan serasah dilakukan secara langsung dari lantai hutan dan
dikumpulkan ke dalam kantong plastik berukuran 20 kg dan kemudian dikering
udarakan untuk mengurangi kadar airnya dan selanjutnya dilakukan penimbangan
Penempatan Sampel Serasah Daun C. tagal
Serasah daun C. tagal yang telah ditimbang sebanyak 50 gram
dimasukkan ke dalam kantong serasah yang terbuat dari nilon. Kantong serasah
dipasang pada tiga tingkat salinitas yang telah ditentukan, masing-masing
sebanyak 18 kantong serasah. Total keseluruhan kantong serasah yang digunakan
adalah 54 kantong serasah. Selama penelitian kantong serasah diikat pada pancang
bambu sebagai antisipasi kantong serasah terbawa oleh pasang surut air laut dan
dapat dilihat pada Gambar 3.
Gambar 3. Lokasi penempatan kantong serasah. (A) 0-10 ppt, (B) 11-20 ppt, dan (C) 21-30 ppt.
Kawasan hutan mangrove lokasi penelitian terletak di Desa Sei
Nagalawan, Kecamatan Perbaungan, Kabupaten Serdang Bedagai, Provinsi
Secara geografis jarak Desa Sei Nagalawan adalah salah satu desa dari 41
desa dari desa yang ada di Perbaungan Kabupaten Serdang Bedagai. Desa Sei
Nagalawan mempunyai luas wilayah 871 Ha, yang terbagi atas tiga dusun wilayah
nya memiliki batas-batas yakni:
- Sebelah utara berbatasan dengan Selat Malaka
- Sebelah selatan berbatasan dengan desa Lubuk Bayas
- Sebelah timur berbatasan dengan Teluk Mengkudu, dan
- Sebelah barat berbatasan dengan kecamatan Pantai Cermin.
Pengambilan sampel serasah daun C. tagal
Pengambilan serasah C. tagal dilakukan dikawasan hutan Pulau Sembilan
Kabupaten Langkat yang banyak ditumbuhi C tagal. Kemudian serasah daun
C. tagal dimasukkan ke dalam kantong plastik/karung plastik dan dibawa ke
laboratorium untuk ditimbang. Selanjutnya serasah daun C. tagal yang
dimasukkan kedalam kantong serasah dengan berat 50 gram untuk setiap kantong
serasah. Kantong serasah dipasang pada setiapa zona salinitas yang telah
ditentukan dengan serasah secara acak. Semua kantong serasah tersebut akan
diikatkan pada bambu agar tidak terbawa arus pasang.
Pengambilan kantong serasah akan dilakukan 15 hari sekali, sebanyak 3
buah kantong berisi sisa serasah untuk setiap zona salinitas selama 90 hari.
Kemudian serasah C. tagal dari kantong serasah tersebut dikeluarkan dan
ditiriskan (dikering-anginkan), untuk selanjutnya dimasukkan ke dalam kantong
kertas HVS Folio. Kantong kertas yang berisi serasah daun C. tagal tersebut
dimasukkan kedalam oven pada suhu 70ºC selama 2 x 24 jam. Setelah dioven
serasah daun C. tagal di hitung dari penyusutan bobot serasah yang
terdekomposisi dalam satu satuan waktu. Sebagai kontrol digunakan serasah
yang tidak ditempatkan di lapangan dan juga digunakan untuk analisis unsur hara.
Pengolahan Data
Laju dekomposisi serasah daun Ceriops tagal
Pendugaan nilai laju dekomposisi serasah dilakukan menurut persamaan
berikut (Olson, 1963 dalam Subkhan, 1991) :
Xt/ X0= e-kt (1)
Adapun penentuan lama masa serasah terdapat (resiedence time) di lantai hutan
digunakan rumus:
1/k (2)
Keterangan : Xt = Berat serasah setelah periode pengamatan ke-t (g)
X0 = Berat serasah awal (g)
e = Bilangan logaritma natural (2,72)
t = Periode pengamatan (hari)
k = Laju dekomposisi
Analisis serasah daun Ceriops tagal
Contoh serasah daun C. tagal dari setiap zona salinitas yang telah
diketahui berat keringnya sebanyak 5 gram dibawa ke Laboratorium Riset dan
Teknologi, Fakultas Pertanian, Universitas Sumatera Utara. Medan. untuk
dianalisis unsur hara karbon, nitrogen dan fosfor dengan menggunakan metode
Kjehdahl (Unsur Nitrogen) dan metode pengabuan kering (Unsur Karbon dan
Analisis Unsur Hara Karbon (C), nitrogen (N) dan fosfor (P)
a. Karbon (C)
Penentuan kadar unsur hara C dilakukan dengan metode Walkey dan
Black (Mukhlis, 2007). Ditimbang 0,1 gram daun kering oven, dimasukkan
ke dalam Erlenmeyer 500 cc, ditambahkan 5 ml K2CrO7 1 N (menggunakan
pipet) digoncang dengan tangan. Ditambahkan 10 mL H2SO4 pekat, kemudian
digoncang 3-4 menit, selanjutnya diamkan 30 menit. Ditambahkan 100 ml air
suling dan 5 ml H3PO4 85%, NaF 4% 2,5 ml, kemudian ditambahkan 5 tetes
Diphenylamine dan digoncang hingga larutan berwarna biru tua kehijauan kotor.
Dititrasikan dengan Fe (NH4)2 (SO4) 0,5 N dari buret hingga warna berubah
menjadi hijau terang. Dilakukan kerja ini lagi (tanpa daun) untuk mendapat
volume titrasi Fe (NH4)2(SO4) 0,5 N untuk blanko.
Perhitungan :
Kadar C organik = 5 0,003
Keterangan :
T = Volume titrasiFe (NH4)2(SO4) 0,5 N dengan daun
S = Volume titrasiFe (NH4)2 0,5 N blanko (tanpa daun)
0,003 = 1 mL K2Cr2O7 1 N + H2SO4 mampu mengoksidasi 0,003 g C-organik
1/0,77 = Metode ini hanya 77% C-organik yang dapat dioksidasi
BCT = Berat Contoh Tanaman
b. Nitrogen (N)
Penentuan kadar nitrogen daun dilakukan dari ekstraksi destruksi basah.
Ditempatkan 20 ml cairan destruksi pekat kedalam tabung destilasi dan tambahan
40% ± 15 ml (langsung pada alat). Ditampung hasil destilasi berupa amoniak pada
Erlenmeyer 250cc yang berisi 25 mL H3BO3 4% dan ditetesi indikator campuran.
Titrasi berakhir bila H3BO3 telah berwarna hijau dan volumenya telah mencapai
75 ml. Amonika hasil destilasi diukur dengan mentitrasi dengan HCL 1 N sampai
warna berubah dari hijau ke warna merah (Mukhlis, 2007).
Perhitungan:
N daun (%) =
= mL HCl x N HCl x 11,2
c. Fosfor (P)
Diambil dengan pipet 5 ml cairan destruksi encer dari ekstraksi destruksi basah
atau cairan dari ekstraksi pengabuan kering tempatkan pada tabung reaksi.
Ditambahkan 10 ml reagen fosfat B biarkan ± 10 menit, kemudian diukur
transmittance (absorbence) pada spectronic dengan π 660 nm. Dilakukan pada
larutan standar 0-2-4-6-8 dan 10 ppm P, dengan cara mengambil masing-masing
5 ml dan ditambahkan 10 ml reagen fosfat B dan diukur pada spectronic
(Mukhlis, 2007).
Perhitungan:
P daun (%) =
HASIL DAN PEMBAHASAN
Laju Dekomposisi
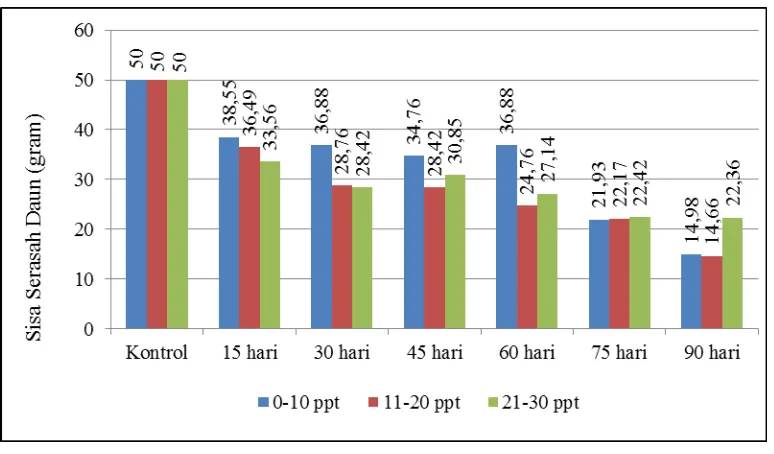
Serasah daun C. tagal yang mengalami dekomposisi mulai dari hari ke-15
sampai dengan hari ke-90 mengalami penurunan bobot kering. Perubahan bobot
kering serasah C. tagal rata-rata pada berbagai tingkat salinitas untuk setiap waktu
pengamatan dapat dilihat pada Gambar 4. Perubahan bobot kering serasah daun
C. tagal dari ketiga tingkat salinitas menunjukkan bahwa tingkat salinitas 11-20
ppt lebih cepat terdekomposisi sehingga laju dekomposisinya lebih tinggi
daripada tingkat salinitas yang lainnya dalam pengambilan data (15 hari). Tingkat
salinitas 21-30 ppt menunjukkan nilai laju dekomposisi serasah terendah dan
tingkat salinitas 11-20 ppt menunjukkan nilai laju dekomposisi tertinggi. Semakin
cepat hilangnya bobot kering serasah maka semakin tinggi nilai laju
dekomposisinya.
Hasil penelitian pada Gambar 4 memperlihatkan bahwa proses
dekomposisi tertinggi terjadi pada 15 hari pertama, hal ini terjadi pada semua
stasiun penelitian. Tingginya dekomposisi serasah pada 15 hari pertama diduga
karena kehilangan bahan-bahan organik serasah akibat kelimpahan penguraian
bakteri maupun makrobentos (dekomposer) yang terjadi di waktu awal serasah
diletakkan. Hasil penelitian ini sesuai dengan hasil penelitian oleh
(Setiawan, 2013) dari data penelitiannya menunjukan bahwa sisa bobot kering
serasah daun R. mucronata pada berbagai tingkat salinitas dari awal sampai
ke hari 15 itu mengalami proses dekomposisi paling besar.
Laju dekomposisi serasah daun C. tagal pada tingkat salinitas 0-10 ppt,
11-20 ppt dan 21-30 ppt cukup beragam dan menghasilkan laju dekomposisi dari
masing-masing tingkat salinitas sebesar 0,252, 0,297 dan 0,198 disajikan pada
pada Tabel 2.
Tabel 2. Rata-rata laju dekomposisi dan lama masa serasah terdapat di lingkungan dengan berbagai tingkat salinitas.
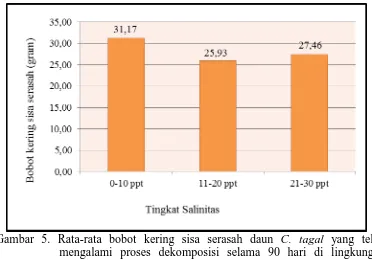
Laju dekomposisi serasah daun C. tagal pada tingkat salinitas 0-10 ppt
yaitu 0,252, tingkat salinitas 11-20 ppt yaitu 0,297, tingkat salinitas 21-30 ppt
yaitu 0,198 dapat dilihat pada Gambar 5. Tingkat salinitas 11-20 ppt menunjukkan
nilai laju dekomposisi tertinggi dan tingkat salinitas 21-30 ppt menunjukkan nilai
laju dekomposisi terendah.
Laju dekomposisi dapat dilihat dengan terjadinya perubahan bentuk dari
serasah daun C. tagal dari daun utuh menjadi cercahan-carcahan daun. Serasah
NO Tingkat Salinitas K (tahun -1) Lama masa serasah terdapat
(tahun)
1 0-10 ppt 0,252 3,96
2 11-20 ppt 0,297 3,36
daun C. tagal mengalami proses dekomposisi dengan berkurangnya bobot kering
serasah pada tingkat salinitas yang berbeda seiring berjalannya waktu pengamatan
mulai dari hari ke-15 sampai dengan hari ke-90. Hal ini menunjukkan bahwa
salinitas berpengaruh terhadap proses dekomposisi karena serasah yang
ditempatkan di dalam kantong serasah pada masing-masing tingkat salinitas
mengalami penurunan bobot kering serasah daun. Data laju dekomposisi
diperoleh karena adanya peran organisme dekomposer di dalam tanah yang
memanfaatkan serasah C. tagal sebagai bahan makananan dengan
menguraikannya menjadi bahan makanan yang dibutuhkan organisme-organisme
tersebut. Menurut Dedi (2000) dalam oleh Emma, (2009) menyebutkan bahwa
secara umum di perairan terdapat dua tipe rantai makanan yaitu rantai makanan
langsung dan rantai makanan detritus. Di ekosistem mangrove, rantai makanan
yang ada untuk biota perairan adalah rantai makanan detritus. Detritus diperoleh
dari daun mangrove yang gugur ke perairan kemudian mengalami penguraian dan
berubah menjadi partikel kecil yang dilakukan oleh mikroorganisme seperti
bakteri dan fungi.
Adapun laju dekomposisi yang terjadi paling lama terdapat pada tingkat
salinitas 21-30 ppt dengan lama masa serasah terdapat (tahun) yaitu 5,05 dengan
nilai k sebesar 0,198/tahun dengan sisa bobot kering serasah yaitu 22,35 g. Hal ini
disebabkan karena jenis organisme pada tingkat salinitas 21-30 ppt merupakan
yang paling sedikit ditemukan organisme laut yaitu sebanyak 78 organisme dan
kondisi vegetasi mangrove yang seragam pada tingkat salinitas 21-30 ppt, hal ini
didukung oleh Dita (2007) bahwa kondisi vegetasi yang seragam mendukung
mikroorganisme yang berperan dalam proses dekomposisi. Jika serasah cocok
tehadap mikroorganisme tanah apalagi jika kaya akan nutrisi dan mengandung
sedikit kayu atau kulit, dan kondisi kelembaban, drainase serta aerasi tanah cukup
baik, maka bahan organik akan terdekomposisi secara cepat dan tidak akan
terakumulasi dalam tanah.
Sisa serasah dari pengamatan hari ke-15 sampai hari ke-90 mengalami
penurunan bobot basah serasah dan penampakan fisiknya menunjukkan cercahan
daun C. tagal semakin menuju hari ke-9 berubah menjadi partikel yang lebih kecil
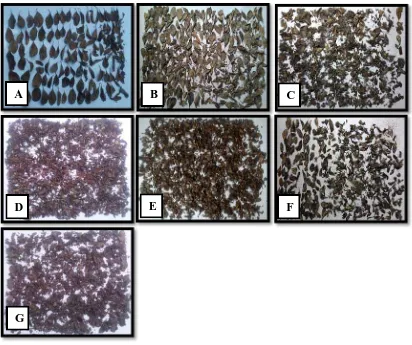
dan semakin menurun bobot keringnya. Penampakan bentuk dan rata-rata berat
bobot kering serah C. tagal disajikan pada Gambar 5 dan Gambar 6.
Gambar 6. Bentuk serasah daun C. tagal yang mengalami proses dekomposisi selama 90 hari pada tingkat salinitas 11-20 ppt. Kontrol (A), 15 hari (B), 30 hari (C), 45 hari (D), 60 hari (E), 75 hari (F) dan 90 hari (G).
Data yang diperoleh dari proses dekomposisi yang terjadi pada serasah
daun C. tagal selama 90 hari dilapangan pada berbagai tingkat salinitas cukup
bervariasi ditandai dengan adanya perubahan berat kering dan perubahan fisik
serasah dapat dilihat pada Gambar 5 dan Gambar 6. Rata-rata berat kering
berbeda-beda pada setiap tingkat salinitas. Pada hari ke-90, bobot berat kering
serasah daun C. tagal pada salinitas 0-10 ppt adalah sebesar 31,17, salinitas 11-20
ppt sebesar 25,93, dan pada salinitas 21-30 ppt sebesar 27,46. Nilai bobot kering
terendah terdapat pada salinitas 11-20 ppt sebesar 25,93 yang artinya salinitas
11-20 ppt mengalami laju dekomposisi paling cepat. Penurunan bobot kering pada
E
G
A B C
serasah daun C. tagal diduga adanya peran organisme yang membantu dalam
proses laju dekomposisi. Organisme tersebut berperan pada awal
pendekomposisian yaitu dengan mencacah dan merobek-robek serasah daun yang
kemudian dikeluarkan kembali menjadi kotoran dan diteruskan oleh bakteri dan
fungi. Menurut Dix dan Webster (1995) dalam oleh Yunasfi (2006) kecepatan
dekomposisi serasah dipengaruhi oleh kecepatan serasah tersebut terpecah-pecah
(fragmented). Pemecahan ini sebagian besar dilakukan oleh banyak hewan tanah
seperti siput, cacing, larva serangga dan lain-lain.
Dibandingkan dengan hasil penelitian Dewi (2010) yang dilakukan di
Sicanang Belawan didapatkan data bahwa laju dekomposisi serasah daun
A. marina yang paling lambat juga terjadi pada tingkat salinitas 20-30 ppt
sedangkan laju dekomposisi serasah daun A. marina yang tertinggi terjadi pada
tingkat salinitas >20 ppt. Hal ini disebabkan menurut Sunarto (2003) bahwa
kecepatan terdekomposisi mungkin berbeda dari waktu ke waktu tergantung
faktor-faktor yang mempengaruhinya.
Makrobentos merupakan salah satu organisme yang membantu proses
dekomposisi dengan cara mengurai atau mencacah daun menjadi cacahan daun
yang berukuran yang lebih kecil. Jenis makrobentos yang terdapat dalam kantong
serasah selama proses dekomposisi dapat dilihat pada Tabel 3 dan Gambar 7.
Tabel 3. Jenis-jenis makrobentos yang ditemukan di dalam kantong serasah daun
C. tagal
Kelas Ordo Genus
Gastropoda Mesogastropoda Telescopium
Turbellaria Macrostomida Microstonum
Kehidupan makrobentos membutuhkan habitat berlumpur yang telah
dihambat oleh perakaran pohon. Selain itu, makrobentos harus mampu hidup dan
membenamkan diri dalam lumpur di bawah pohon (Gultom, 2009). Hal ini sesuai
dengan lokasi penelitian pada setiap tingkat salinitas, dimana semua salinitas
memiliki substrat yang berlumpur sehingga terdapat keanekaragaman
makrobentos yang mempengaruhi proses laju dekomposisi serasah daun
dilapangan.
Gambar 7. Makrobentos yang ditemukan di dalam kantong serasah daun
C. tagal Kepiting (A), siput (B), dan cacing (C).
Makrobentos yang terdapat di dalam kantong serasah yaitu kelas
Gastropoda, Turbellaria, Insecta, dan Crustaceae (Tabel 2), banyak makrobentos
yang terdapat di dalam kantong serasah dipengaruhi oleh tingkat salinitas
(Lampiran 5). Makrobentos dapat hidup berkoloni di hutan mangrove tergantung
pada rendahnya tingkat salinitas ataupun sebaliknya dan jumlah makrobentos
yang terdapat setiap tingkat salinitas dipengaruhi konsentrasi salinitas yang
A B
terdapat dilingkungan. Ini sesuai dengan pendapat Arief (2003) dalam Gultom
(2009) yang menyatakan bahwa perkembangan salinitas berpengaruh terhadap
perkembangan jenis makrobentos dan kehidupan beberapa makrobentos
tergantung pada rendahnya salinitas, tetapi ada juga sebaliknya. Adanya
organisme tersebut menunjukkan bahwa kadar C-organik serasah dan biomassa
serasah, secara tidak langsung dapat memberikan peran dalam kehadiran dan
aktivitas organisme dalam ekosistem mangrove. Hal ini didukung oleh
Notohadiprawiro (1998) yang menyatakan bahwa laju dekomposisi bahan organik
ditentukan oleh faktor bahan organik dan lingkungan yang mempengaruhi
berbagai aktivitas organisme, organisme tersebut membantu pada proses awal
perombakan bahan organik dalam tanah.
Kandungan Unsur Hara Karbon (C), Nitrogen (N), Fosfor (P) dan Rasio C/N
Nilai kandungan unsur hara karbon, nitrogen, dan fosfor dari setiap
pengamatan unsur hara memiliki nilai yang beragam. Hal ini membuktikan bahwa
kadar salinitas yang berbeda berpengaruh dalam pelepasan unsur hara serasah
selama proses dekomposisi. Proses pelepasan unsur hara dari setiap sampel
serasah ini juga dipengaruhi mikroorganisme dekomposer yang berperan dalam
proses dekomposisi serasah daun C. tagal sesuai dengan pernyataan dari Aprianis
(2011) yang menyatakan bahwa perubahan bobot serasah persatuan waktu
disebabkan terjadinya proses dekomposisi dimana mikroorganisme tanah
memanfaatkan karbon serasah sebagai bahan makanan dan membebaskannya
sebagai CO2.
Proses dekomposisi serasah daun C. tagal terjadi mulai hari ke-15 sampai
fosfor. Berdasarkan analisis nilai kandungan unsur karbon lebih tinggi dari
kandungan unsur nitrogen dan unsur fosfor. Unsur hara karbon berperan dalam
pembentukan iklim dan pelapukan kimia batuan dan mineral. Kandungan unsur
hara karbon, nitrogen dan fosfor dapat dilihat pada Gambar 8, Gambar 9 dan
Gambar 10.
Unsur Hara Karbon (C)
Unsur hara karbon pada serasah C. tagal yang telah mengalami masa
dekomposisi pada berbagai tingkat salinitas dan waktu pengambilan serasah dapat
dilihat pada Gambar 8.
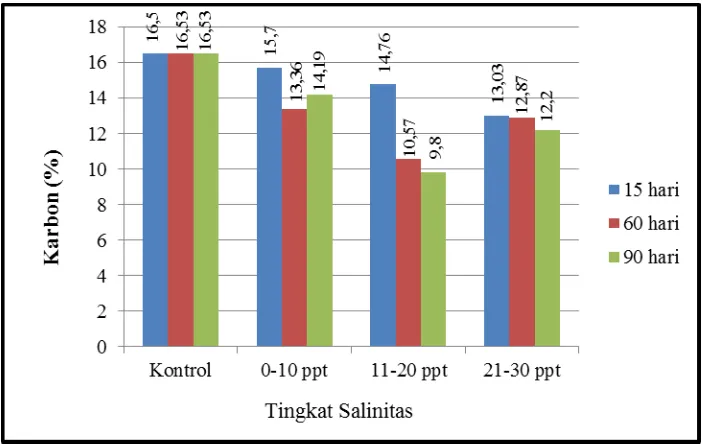
Gambar 8. Kadar unsur hara karbon pada berbagai tingkat salinitas
Berdasarkan Gambar 8, dapat diketahui bahwa kandungan unsur hara
karbon mengalami penurunan dari hari ke-15 sampai hari ke-90. Unsur hara
karbon tertinggi terdapat pada tingkat salinitas 0-10 ppt, dan unsur hara karbon
terendah terdapat pada salinitas 21-30 ppt.
Kandungan unsur hara karbon (C) yang terdapat dalam serasah daun
ke-90 pengamatan terutama pada tingkat salinitas 21-30 ppt. Unsur hara karbon
yang paling tinggi terjadi pada salinitas 0-10 ppt pada hari ke-15 yang mencapai
15,7% sedangkan yang paling kecil terjadi pada hari ke-90 salinitas 11-20 ppt
yaitu 9,8%. Menurut Effendi (2003) kadar karbondioksida di perairan dapat
mengalami pengurangan akibat proses fotosintesis dan evaporasi yang terjadi.
Karbon yang terdapat di atmosfer dan perairan diubah menjadi karbon organik
melalui proses fotosintesis.
Unsur Hara Nitrogen (N)
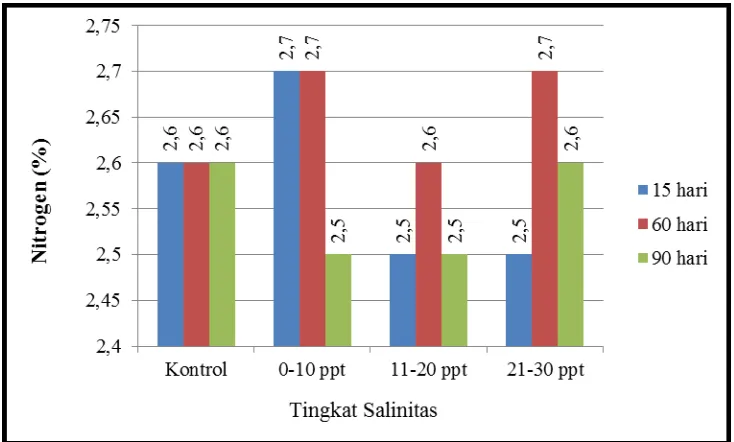
Kandungan unsur hara nitrogen mengalami peningkatan dibandingkan
dengan persen (%) nitrogen pada kontrol. Unsur hara nitrogen tertinggi terdapat
pada tingkat salinitas 0-10 ppt, dan unsur hara nitrogen terendah terdapat pada
tingkat salinitas 11-20 ppt dapat dilihat pada Gambar 9.
Gambar 9. Kadar unsur hara nitogen pada berbagai tingkat salinitas
Nitrogen merupakan unsur yang penting dalam penyusunan asam amino,
pengamatan hari ke-15 sampai hari ke-90 pada setiap tingkat salinitas 11-20 ppt
mengalami penurunan dan terjadi peningkatan pada tingkat salinitas 21-30 ppt, hal
ini dikarenakan pada tingkat salinitas 21-30 ppt organisme yang memanfaatkan
nitrogen sedikit dijumpai hal ini diduga disebabkan salinitas yang tinggi sehingga
terjadi kenaikan. Hal ini sesuai dengan pernyataan Effendi (2003) dalam Gultom
(2009) yang menyatakan bahwa dengan bertambahnya waktu, kadar nitrogen
organik berkurang karena konversi menjadi amonia. Beberapa jenis organisme
memanfaatkan nitrogen pada daun dan mengeluarkan tinja (kotoran) dari
organisme tersebut.
Kadar nitrogen yang terdapat pada daun serasah daun C. tagal pada
berbagai tingkat salinitas mengalami kenaikan dan penurunan kadar nitrogen.
Naik dan turunnya kandungan kadar nitrogen pada serasah daun C. tagal
berpengaruh terhadap aktifitas mikroorganisme atau dekomposer. Kadar nitrogen
yang terdapat pada serasah daun dibutuhkan mikroorganisme untuk
perkembangan. Menurut Sriharti (2008) kadar nitrogen dibutuhkan
mikroorganisme untuk memelihara dan pembentukan sel tubuh. Semakin banyak
kandungan nitrogen, maka akan semakin cepat bahan organik terurai, karena
mikroorganisme yang menguraikan bahan kompos memerlukan nitrogen untuk
perkembangannya.
Unsur Hara Fosfor (P)
Kandungan unsur hara mengalami penurunan dari hari ke-15 sampai hari
ke-90. Fosfor juga berperan dalam proses metabolisme tanaman. Kandungan
dan kandungan unsur hara terendah terdapat pada tingkat salinitas 11-20 ppt dapat
dilihat pada Gambar 10.
Gambar 10. Kadar unsur hara fosfor pada berbagai tingkat salinitas
Berdasarkan Gambar 10 diketahui nilai persen (%) unsur hara fosfor pada
serasah C. tagal menunjukkan sesuai lamanya pengamatan serasah dilingkungan.
Rata-rata kandungan unsur hara fosfor serasah C. tagal pada tingkat salinitas 0-10
ppt, 11-20 ppt dan 21-30 ppt adalah 0,19 %, 0,18 dan ,18 %.
Kandungan unsur hara fosfor mengalami penurunan pada tingkat salinitas
0-10 ppt dan 11-20 ppt. Kandungan unsur hara fosfor pada C. tagal dibutuhkan
tanaman dalam proses metabolisme. Menurut Effendi (2003) di perairan, bentuk
unsur fosfor berubah secara terus-menerus, akibat proses dekomposisi dan sintesis
antara bentuk organik dan bentuk anorganik yang dilakukan oleh mikroba.
Keberadaan fosfor di perairan alami biasanya relatif kecil, dengan kadar yang
sedikit daripada kadar nitrogen karena sumber fosfor lebih sedikit dibandingkan
dengan sumber nitrogen di perairan. Kadar fosfat yang tinggi diduga berasal dari
dengan pertumbuhan lumut yang berada di perairan. Menurut Effendi (2003)
bahwa keberadaan fosfor yang berlebihan dapat diakibatkan oleh pertumbuhan
alga di perairan.
Rasio C/N
Rasio C/N merupakan salah satu indikator dalam laju dekomposisi serasah
C. tagal. Hasil analisis diketahui nilai C/N tertinggi hari pada tingkat salinitas
0-10 ppt yaitu sebesar 5,34%. Nilai C/N terendah terdapat tingkat salinitas 11-20
ppt yaitu sebesar 3,92%. Hasil perbandingan Rasio C/N dapat dilihat pada
Gambar 11.
Gambar 11. Rasio C/N pada serasah daun C. tagal
Rasio C/N tertinggi yang diperoleh dari pengamatan dan perhitungan
terdapat pada tingkat salintas 21-30 ppt yaitu pada pengamatan hari ke-90 sebesar
4,69% dan nilai C/N terendah terdapat tingkat salinitas 11-20 ppt yaitu sebesar
3,92 %. Menurut Hairiah dan Rahayu (2007) dalam oleh Dewi (2010) bahwa C/N
merupakan salah satu indikator untuk melihat laju dekomposisi bahan organik,
terdekomposisi. Semakin cepat serasah terdekomposisi maka akan semakin
banyak unsur hara yang tersedia bagi tanaman, makrobentos dan mikroorganisme.
Hal ini sesuai dengan hasil laju dekomposisi serasah daun C. tagal yang
menunjukkan pada 21-30 ppt adalah salinitas yang paling lama mengalami proses
dekomposisi. Hal ini juga dipengaruhi oleh keberadaan makrobentos seperti
cacing, siput, dan kepiting yang berperan dalam penghancuran serasah daun C.
tagal dimana pada tingkat salinitas 21-30 ppt tidak terlalu banyak dijumpai
keberadaan Makrobentos. Menurut Allo., dkk (2014) Ratio C/N merupakan faktor
kimia pembentuk kecepatan dekomposisi dan mineralisasi nitrogen. Penyebab
pembusukan pada bahan organik diakibatkan adanya karbon dan nitrogen. Rasio
C/N digunakan untuk mendapatkan degradasi biologis dan bahan-bahan organik
yaitu sampah tersebut baik atau tidak untuk dijadikan kompos, serta menunjukkan
kematangan kompos.
Rasio C/N dapat dipengaruhi dari aktifitas cacing, dimana cacing
memakan daun serasah yang ada dilantai hutan. Daun serasah mengandung
nitrogen dimana pada mulanya nitrogen tidak tersedia menjadi tersedia
disebabkan cacing mengeluarkan kotoran yang mengandung nitrogen yang berasal
dari kotoran cacing. Menurut Permelee et al (1990), cacing tanah juga berperan
dalam menurunkan rasio C/N bahan organik, dan mengubah nitrogen tidak
tersedia menjadi nitrogen tersedia setelah dikeluarkan berupa kotoran. Terdapat
interaksi antara pemberian bahan organik dan cacing tanah terhadap status hara
tanah terutama N dan K, dan pemberian inokulum cacing tanah juga berpengaruh
KESIMPULAN DAN SARAN
Kesimpulan
1. Laju dekomposisi serasah daun C. tagal pada tingkat salinitas 11-20 ppt lebih
cepat terdekomposisi dengan nilai k sebesar 0,297/tahun dibandingkan laju
dekomposisi pada tingkat salinitas 0-10 ppt sebesar 0,252/tahun dan tingkat
salinitas 21-30 ppt sebesar 0,198/tahun.
2. Nilai kandungan rata-rata unsur hara Karbon tertinggi terdapat pada tingkat
salinitas 0-10 ppt sebesar 16,36 % dan terendah terdapat pada salinitas
11-20 ppt sebesar 15,2 %. Kandungan rata-rata unsur hara Nitrogen tertinggi
terdapat pada tingkat salinitas 20-30 ppt sebesar 2,6 % dan terendah terdapat
pada salinitas 0-10 ppt sebesar 2,5 %. Kandungan rata-rata unsur hara Fosfor
tertinggi terdapat pada tingkat salinitas 11-20 ppt sebesar 0,20 % dan terendah
terdapat pada salinitas 21-30 ppt sebesar 0,18 %.
Saran
Perlu dilakukan uji lanjutan mengenai mikroorganisme seperti fungi dan
jamur yang berperan dalam proses laju dekomposisi serasah daun C. tagal
danpada saat penentuan zona salinitas dilakukan dengan memilih lokasi yang
TINJAUAN PUSTAKA
Mangrove Secara Umum
Hutan mangrove merupakan tipe hutan tropika dan subtropika yang khas,
tumbuh di sepanjang pantai atau muara sungai yang dipengaruhi oleh pasang surut
air laut. Mangrove banyak di jumpai di wilayah pesisir yang terlindung dari
gempuran ombak dan daerah yang landai. Mangrove tumbuh optimal di wilayah
pesisir yang memiliki muara sungai besar dan delta yang aliran airnya banyak
mengandung lumpur. Sedangkan di wilayah pesisir yang tidak bermuara sungai,
pertumbuhan vegetasi mangrove tidak optimal. Mangrove sulit tumbuh di wilayah
pesisir yang terjal dan berombak besar dengan arus pasang surut kuat, karena
kondisi ini tidak memungkinkan terjadinya pengendapan lumpur yang diperlukan
sebagai substrat bagi pertumbuhannya (Dahuri, 2003).
Hutan mangrove meliputi pohon-pohon dan semak yang tergolong ke
dalam 8 (delapan) famili, dan terdiri atas 12 (dua belas) genera tumbuhan
berbunga yaitu Avicennia, Sonneratia, Rhyzophora, bruguiera, Ceriops,
Xylocarpus, Lumnitzera, Languncularia, Aegiceras, Aegiatilis, Snaeda, dan
Conocarpus (Bengen, 2002).
Mangrove merupakan karakteristik dari bentuk tanaman pantai, estuari
atau muara sungai, dan delta di tempat yang terlindung daerah tropis dan sub
tropis. Dengan demikian maka mangrove merupakan ekosistem yang terdapat di
antara daratan dan lautan dan pada kondisi yang sesuai mangrove akan
membentuk hutan yang ekstensif dan produktif. Karena hidupnya di dekat pantai,
mangrove sering juga dinamakan hutan pantai, hutan pasang surut, hutan payau,
bakau, dan disebut hutan payau karena hutannya tumbuh di atas tanah yang selalu
tergenang oleh air payau (Dedi, 2008).
Bentuk morfologi C. tagal dapat dilihat pada Gambar 1, sedangkan taksonomi C.
tagal adalah sebagai berikut:
Kingdom : Plantae
Divisi : Magnoliophyta
Kelas : Magnoliopsida
Ordo : Malpighiales
Famili : Rhizophoraceae
Genus : Ceriops
Spesies : Ceriops tagal
Gambar 1. Ceriops tagal
Tengar adalah nama sekelompok tumbuhan dari marga Ceriops, suku
Rhizophoraceae. Dari segi penampilan, tengar mirip dengan bakau, meski
umumnya lebih kecil. Deskripsi umum dari C. tagal yaitu pohon kecil atau semak
dengan ketinggian mencapai 25 m. Kulit kayu berwarna abu-abu, kadang-kadang
tumbuhan ini juga dikenal dengan beberapa nama lain seperti tangar, tengal,
tengah, tingi, palun, parun, bido-bido dan lain-lain (Noor et al., 1999).
Akar banir dari bentukan seperti akar tunjang, kadang membentuk akar
lutut atau akar nafas yang menonjol. Batang berkayu, warna coklat agak jingga.
Bagian bawah batang terdapat banyak akar tunjang dengan panjang ± 50 cm.
Percabangannya banyak dan tidak teratur. Hipokotil berbintil, berkulit halus, agak
menggelembung dan seringkali agak pendek. Leher kotiledon menjadi kuning jika
sudah matang/dewasa. Ukuran hipokotil silindris panjang 4-25 cm dan diameter
8-12 mm. Daun hijau mengkilap dan sering memiliki pinggiran yang melingkar ke
dalam, ukuran daunnya 1-10 x 2-3,5 cm (Noor et al, 1999).
Faktor-Faktor Lingkungan yang Mempengaruhi Pertumbuhan C. tagal Tanah
Jenis tanah yang mendominasi kawasan mangrove biasanya adalah fraksi
lempeng berdebu, akibat rapatnya bentuk perakaran-perakaran yang ada. Fraksi
lempung berpasir hanya terdapat dibagian depan (arah pantai). Nilai pH tanah
dikawasan mangrove berbeda-beda, tergantung pada tingkat kerapatan vegetasi
yang tumbuh dikawasan tersebut. Jika kerapatan rendah, tanah akan mempunyai
nilai pH yang tinggi. Nilai pH tidak banyak berbeda, yaitu antara 4,6-6,5 dibawah
tegakan jenis Rhizophora spp (Noor et al., 1999).
Hutan mangrove tanahnya selalu basah, mengandung garam, mempunyai
sedikit oksigen dan kaya akan bahan organik. Bahan organik yang terdapat di
dalam tanah, terutama berasal dari sisa tumbuhan yang diproduksi oleh mangrove
sendiri. Serasah secara lambat akan diuraikan oleh mikroorganisme, seperti
kasar, seperti potongan batu dan koral, pecahan kulit kerang dan siput. Biasanya
tanah mangrove kurang membentuk lumpur berlempung dan warnanya bervariasi
dari abu-abu muda sampai hitam (Soeroyo, 1993).
Umumnya tanah yang ditumbuhi mangrove adalah tanah-tanah yang
bertekstur halus, mempunyai tingkat kematangan rendah, mempunyai kadar
garam rendah alkalinitas tinggi, dan sering mengandung lapisan sulfat masam atau
bahan sulfidik (cat clay). Kandungan liat atau debu umumnya tinggi, kecuali
tanah-tanah atau pecahan batu karang. Lapisan gambut dengan kandungan garam
tinggi kadang-kadang ditemukan pada tanah mangrove baik di daerah batu karang
maupun di daerah endapan liat (Mardiana, 2005).
Suhu
Suhu penting dalam proses fisiologis, seperti fotosintesis dan respirasi.
Pada Rhizophora spp., Ceriops spp., Exocoecaria spp., dan Lumnitzera spp., laju
tertinggi produksi daun baru adalah pada suhu 26-28 ºC, untuk Bruguiera spp
adalah 27ºC dan Avicennia marina memproduksi daun baru pada suhu 18-20 ºC
(Hutchings and Saenger, 1987).
Pasang Surut
Pasang surut menentukan zonasi komunitas flora dan fauna mangrove.
Durasi pasang surut berpengaruh besar terhadap perubahan salinitas pada areal
mangrove. Salinitas air menjadi sangat tinggi pada saat pasang naik dan menurun
selama pasang surut. Perubahan tingkat salinitas pada saat pasang merupakan
salah satu faktor yang membatasi distribusi jenis mangrove. Pada areal yang
Bruguiera spp dan Xylocarpus spp jarang mendominasi daerah yang sering
tergenang. Pasang surut juga berpengaruh terhadap perpindahan massa antara air
tawar dengan air laut, dan oleh karenanya mempengaruhi organisme mangrove
(Ansori, 1998).
Salinitas
Kebanyakan tumbuhan memiliki toleransi sangat rendah terhadap salinitas,
sehingga tidak mampu tumbuh di dalam atau di dekat air laut. Hal ini terjadi
karena kebanyakan jaringan makhluk hidup lebih cair daripada air laut, akibatnya
air dari dalam jaringan tumbuhan dapat keluar akibat proses osmosis, sehingga
tumbuhan kekeringan, menjadi layu, dan mati. Lingkungan yang keras ini
menyebabkan diversitas hutan mangrove cenderung lebih rendah daripada
umumnya hutan hujan tropis (Noor et al., 1999).
Secara umum di perairan terdapat dua tipe rantai makanan yaitu rantai
makanan langsung dan rantai makanan detritus. Di ekosistem mangrove, rantai
makanan yang ada untuk biota perairan adalah rantai makanan detritus. Detritus
diperoleh dari daun mangrove yang gugur ke perairan kemudian mengalami
penguraian dan berubah menjadi partikel kecil yang dilakukan oleh
mikroorganisme seperti bakteri dan fungi (Dedi, 2000 dalam oleh Emma, 2009).
Fungsi Ekologis Hutan Mangrove
Fungsi ekologis mangrove menurut Dahuri et al. (1996) dalam
a. Dalam ekosistem hutan mangrove terjadi mekanisme hubungan antara
ekosistem mangrove dengan jenis-jenis ekosistem lainnya seperti padang
lamun dan terumbu karang.
b. Dengan sistem perakaran yang kokoh ekosistem hutan mangrove memiliki
kemampuan meredam gelombang, menahan lumpur dan melindungi pantai
dari abrasi, gelombang pasang dan topan.
c. Sebagai pengendalian banjir, hutan mangrove yang banyak tumbuh di daerah
estuaria juga dapat berfungsi untuk mengurangi bencana banjir.
d. Hutan mangrove dapat berfungsi sebagai penyerap bahan pencemar
(environmental service), khususnya bahan-bahan organik.
e. Sebagai penghasil bahan organik yang merupakan mata rantai utama dalam
jaring-jaring makanan di ekosistem pesisir, serasah mangrove yang jatuh dan
gugur ke dalam air akan menjadi substrat yang baik bagi bakteri dan sekaligus
berfungsi membantu proses daun-daun tersebut menjadi detritus. Selanjutnya
detritus menjadi bahan makanan bagi hewan pemakan, seperti cacing,
udang-udang kecil dan akhirnya hewan-hewan ini akan menjadi makanan larva
ikan,udang, kepiting dan hewan lainnya.
f. Merupakan daerah asuhan (nursery ground) hewan-hewan muda (juvenile
stage) yang akan bertumbuh kembang menjadi hewan-hewan dewasa dan juga
merupakan daerah pemijahan (spawning ground) beberapa perairan seperti
udang,ikan dan kerang-kerangan.
Salinitas Mangrove
Di Indonesia, areal yang selalu digenangi walaupun pada saat pasang
yang digenangi oleh pasang sedang didominasi oleh jenis-jenis Rhizophora.
Adapun areal yang digenangi hanya pada saat pasang tinggi, yang mana areal ini
lebih ke daratan, umumnya didominasi oleh jenis-jenis Bruguiera dan Xylocarpus
granatum, sedangkan areal yang digenangi hanya pada saat pasang tertinggi
(hanya beberapa hari dalam sebulan) umumnya didominasi oleh Bruguiera
sexangula dan Lumnitzera littorea.
Pengaruh Salinitas Terhadap Fisiologi
Dalam kaitannya dengan adaptasi terhadap kandungan garam, mangrove
dikelompokkan menjadi dua kelompok yakni (1) salt-excreting mangrove, seperti
jenis Avicennia, Aegiceras, dan Aegialitis, dan (2) non-secretor mangrove, seperti
jenis Rhizophora, Bruguiera, Sonneratia, dan lain-lain. Sehubungan dengan ini
Hutching dan Saenger (1987) mengemukakan tiga cara mangrove beradaptasi
terhadap garam sebagai berikut:
1. Sekresi garam (salt extrusion/salt secretion)
Flora mangrove menyerap air dengan salinitas tinggi kemudian
mengekskresikan garam dengan kelenjar garam yang terdapat pada daun.
Mekanisme ini dilakukan oleh Avicennia, Sonneratia, Aegiceras, Aegialitis,
Acanthus, Laguncularia dan Rhizophora (melalui unsur-unsur gabus pada
daun).
2. Mencegah masuknya garam (salt exclusion)
Flora mangrove menyerap air tetapi mencegah masuknya garam, melalui
saringan yang terdapat pada akar. Mekanisme ini dilakukan oleh Rhizophora,
Ceriops, Sonneratia, Avicennia, Osbornia, Bruguiera, Excoecaria, Aegiceras,
3. Akumulasi garam (salt accumulation)
Flora mangrove seringkali menyimpan Na dan Cl pada bagian kulit
kayu, akar dan daun yang lebih tua. Daun penyimpan garam umumnya
sukulen dan pengguguran daun sukulen ini diperkirakan merupakan
mekanisme mengeluarkan kelebihan garam yang dapat menghambat
pertumbuhan dan pembentukan buah.
Laju Dekomposisi Serasah
Mason (1974) membagi proses-proses dekomposisi menjadi tiga yaitu
pelindihan (leaching), penghawaan (weathering) dan aktivitas biologi. Ketiga
proses tersebut berlangsung secara simultan. Leaching adalah mekanisme
hilangnya bahan-bahan yang dapat larut dari serasah atau detritus organik oleh
hujan atau aliran air. Weathering adalah mekanisme pelapukan oleh faktor-faktor
fisik, seperti pengikisan dan penguapan air dari serasah oleh angin, es dan
pergerakan gelombang. Aktivitas biologi adalah proses yang menghasilkan
pecahan-pecahan detritus bahan organik secara bertahap oleh mahkluk hidup.
Makhluk hidup yang melakukan dekomposisi dikenal sebagai dekomposer,
pengurai atau saproba. Serasah atau organik yang berasal dari bahan tumbuhan
yang telah mati setelah mengalami beberapa tahapan dekomposisi dapat
menghasilkan energi potensial bagi kehidupan konsumer. Sebutan serasah
biasanya digunakan untuk bahan dalam ekosistem daratan khususnya bahan yang
berasal dari tumbuhan tingkat tinggi, sedang detritus digunakan untuk bahan
dalam ekosistem perairan.
Proses dekomposisi dimulai dari proses penghancuran yang dilakukan oleh
ukuran yang lebih kecil. Kemudian dilanjutkan dengan proses biologi yang
dilakukan oleh bakteri dan fungi untuk menguraikan partikel-partikel organik.
Proses dekomposisi oleh bakteri dan fungi sebagai dekomposer mengeluarkan
enzim yang dapat menguraikan bahan organik menjadi protein. Kecepatan
terdekomposisi mungkin berbeda dari waktu ke waktu tergantung faktor-faktor
yang mempengaruhinya (Sunarto, 2003).
Laju dekomposisi bahan organik ditentukan oleh faktor bahan organik dan
lingkungan yang mempengaruhi berbagai aktivitas organisme, organisme tersebut
membantu pada proses awal perombakan bahan organik dalam tanah
(Notohadiprawiro, 1998).
Proses dekomposisi serasah daun A. marina terjadi selama 105 hari. Hasil
penelitian memperlihatkan adanya perubahan berat kering dan perubahan fisik
serasah daun A. marina yang bervariasi. Rata-rata berat kering berbeda-beda pada
setiap stasiun. Pada hari ke-105, bobot berat kering serasah daun A. marina pada
stasiun I adalah sebesar 1,83, stasiun II sebesar 5,0, dan pada stasiun III sebesar
3,73. Nilai bobot kering terendah terdapat pada stasiun I sebesar 1,83 yang artinya
stasiun I mengalami laju dekomposisi paling cepat. Hal ini sesuai dengan literatur
(Indriani, 2008), Perubahan bobot kering serasah daun A. marina mengalami
penurunan dengan lamanya penguraian per 15 hari. Penurunan berat kering daun
terbesar yaitu pada daerah dekat dengan aliran air laut yang berfungsi untuk
memberikan asupan air laut bagi tambak-tambak di sekitarnya (Naibaho, 2014).
Kecepatan dekomposisi serasah dapat diketahui dengan menempatkan
serasah daun mangrove yang massanya diketahui di dalam kantong serasah yang
Gastropoda dan kepiting. Kantong-kantong berisi serasah daun ini selanjutnya
ditempatkan di areal mangrove dan pengamatan dilakukan dengan selang waktu
tertentu. Tiap kali pengamatan sisa serasah yang terdapat dalam kantong tersebut
ditimbang (Hogarth, 1999).
Hasil Penelitian Odum dan Heald (1975) dilaporkan bahwa sekitar 83%
dari total produksi daun daun mangrove (880 gram berat kering/m²/tahun)
didekomposisi. Lebih lanjut dilaporkan bahwa laju dekomposisi serasah daun
tersebut sangat bervariasi, tergantung kondisi substrat dimana serasah daun
tersebut jatuh. Serasah daun yang jatuh di tempat atau substrat dasar yang kering,
proses dekomposisinya cenderung lebih lambat dibandingkan bila jatuh di
perairan. Adapun kecepatan dekomposisinya juga berbeda, tergantung pada kadar
garam perairan dimana serasah daun itu jatuh, air laut cenderung lebih cepat
mendekomposisi serasah daun mangrove dibandingkan dengan air payau dan
terlambat adalah air tawar.
Perubahan bobot serasah per satuan waktu disebabkan terjadinya proses
dekomposisi dimana mikroorganisme tanah memanfaatkan karbon serasah sebagai
bahan makanan dan membebaskannya sebagai CO2. Perubahan bobot molekul
juga terjadi pada proses dimana senyawa kompleks yang berbobot molekul tinggi
akan diubah menjadi senyawa yang lebih sederhana dengan bobot molekul yang
lebih rendah (Aprianis, 2011).
Laju dekomposisi serasah dipengaruhi oleh jenis serasah, jenis pohon, dan
penggenangan lantai hutan mangrove oleh air laut (Day, 1982 dalam oleh
Alrasjid, 1986). Selama 10 sampai 14 hari, hampir semua kehilangan bobot
Organic Carbon) tercuci. Diketahui bahwa sekitar 30 sampai 50 persen
bahan-bahan organik serasah daun hilang dengan cara seperti ini dan sisanya yaitu
karbohidrat seperti selulosa yang tidak larut. Bahan-bahan ini selanjutnya
diuraikan dengan bantuan enzim ekstraseluler yang dihasilkan oleh bakteri atau
fungi. Satu di antara berbagai macam substrat yang banyak terurai di awal proses
dekomposisi adalah tannin. Keberadaan tannin pada serasah daun dapat
menghambat pertumbuhan bakteri pada serasah daun yang mengalami
dekomposisi, terjadi setelah kandungan taninnya berkurang
(Gonzales dan Mee, 1988 dalam Yunasfi, 2006).
Faktor fisik kimia lingkungan, termasuk salinitas mempengaruhi
keberadaan mikroorganisme dimana suatu mikroorganisme memiliki kemampuan
beradaptasi yang tinggi terhadap lingkungannya dalam melangsungkan aktivitas
kehidupan meliputi pertumbuhan, menghasilkan energi dan bereproduksi
(Darkuni, 2001).
Dekomposisi menjadi sempurna ketika campuran bahan organik
dikembalikan kelingkungan dalam bentuk anorganik atau bentuk mineral, yaitu
karbon dalam bentuk karbondioksida, nitrogen dalam bentuk ammonia dan fosfor
dalam bentuk fosfat (Moore-Landecker, 1990).
Dari hasil penelitian Dewi (2010) tentang laju dekomposisi serasah daun
Avicennia marina di hutan mangrove Sicanang Belawan, Medan. Didapatkan laju
dekomposisi daun Avicennia marina pada tingkat salinitas 0-10 ppt, 10-20 ppt,
Tabel 1. Laju dekomposisi serasah daun Avicennia marina pada berbagai tingkat salinitas di Secanang Belawan
Salinitas Laju Dekomposisi (gram)
Kontrol Hari ke-15 Hari ke-30 Hari ke-45 Hari ke-60
Ratio C/N merupakan faktor kimia pembentuk kecepatan dekomposisi dan
mineralisasi nitrogen. Penyebab pembusukan pada bahan organik diakibatkan
adanya karbon dan nitrogen. Rasio C/N digunakan untuk mendapatkan degradasi
biologis dan bahan-bahan organik yaitu sampah tersebut baik atau tidak untuk
dijadikan kompos, serta menunjukkan kematangan kompos (Allo., dkk 2014).
Penguraian bahan-bahan organik yang terkandung dalam sampah organik
daun adalah hasil kegiatan penguraian oleh mikroorganisme dan selanjutnya
diperlukan oleh mikroorganisme itu sendiri sebagai sumber energi. Adanya
perbedaan hasil pengiraian bahan organik dapat disebabkan oleh perbedaan
bioaktivator yang diberikan dan kandungan mikroorganisme yang ada dalam
activator (Marady, 2009 dalam Allo., dkk 2014).
Dengan bertambahnya waktu, kadarnitrogen organik berkurang karena
konversi menjadi amonia. Beberapa jenis organisme memanfaatkan nitrogen pada
daun dan mengeluarkan tinja (kotoran) dari organisme tersebut. Kotoran itu
mengandung amonia yang menempel pada serasah daun tanaman. Berdasarkan
jumlah makrobentos memiliki empat tingkat salinitas kandungan nitrogen yang
(Effendi, 2003 dalam Gultom, 2009).
Nilai N yang mengalami peningkatan dan penurunan selama proses
keseluruhan kadar nitrogen pada kompos matang masing-masing komposter
mengalami peningkatan. Kadar nitrogen dibutuhkan mikroorganisme untuk
memelihara dan pembentukan sel tubuh. Semakin banyak kandungan nitrogen,
maka akan semakin cepat bahan organik terurai, karena mikroorganisme yang
menguraikan bahan kompos memerlukan nitrogen untuk perkembangannya
(Sriharti, 2008).
Perkembangan salinitas berpengaruh terhadap perkembangan jenis
makrobentos. Adanya masukan air sungai atau hujan akan menurunkan kadar
salinitas, yang mengakibatkankematian beberapa makrobentos tersebut.
Kehidupan beberapa makrobentos tergantung pada rendahnyasalinitas, tetapi ada
juga sebaliknya. Aktivitas makroorganisme yang tahan terhadap salinitas yang
tinggi dan mikoorganisme membantu dalam proses pendekomposisian bahan
organik dalam tanah (Arief, 2003 dalam Gultom, 2009).
Menurut Effendi (2003) kadar karbondioksida di perairan dapat
mengalami pengurangan akibat proses fotosintesis dan evaporasi yang terjadi.
Karbon yang terdapat di atmosfer dan perairan diubah menjadi karbon organik
melalui proses fotosintesis. Di perairan, bentuk unsur fosfor berubah secara
terus-menerus, akibat proses dekomposisi dan sintesis antara bentuk organik dan bentuk
anorganik yang dilakukan oleh mikroba. Keberadaan fosfor yang berlebihan dapat
Latar Belakang
Di Indonesia diperkirakan luas hutan mangrove sangat beragam. Luas
mangrove di Indonesia 4,25 juta hektar. Umumnya mangrove dapat ditemukan di
seluruh kepulauan Indonesia. Mangrove tersebar luas, di Irian Jaya sekitar
2,94 juta hektar (38%), Kalimantan 978 hektar (28%) dan Sumatera 673.300
hektar (Noor et al., 1999). Saat ini, kondisi mangrove benar-benar dalam proses
kemunduran. Tingginya tekanan populasi, konversi mangrove ke pertanian dan
produksi garam, industri tambang, industrialisasi pesisir dan urbanisasi, serta
konversi pesisir ke pertambakan menjadi penyebab utama degradasi ekosistem
mangrove (Vaiphasa dkk., 2006).
Kawasan hutan mangrove dari tahun ke tahun semakin berkurang, menurut
BAKOSURTANAL (Badan Koordinasi Survei dan Pemetaan Nasional, 2009)
dalam Ghufran (2012) tercatat untuk wilayah Sumatera Utara tahun 2009 luas
wilayah kawasan mangrove hanya mencapai 50.369,793 ha dimana jumlah ini
jauh berkurang berdasarkan data dari Direktorat Jenderal Inventarisasi dan Tata
Guna Hutan tahun 1996 yang mencapai 136.900 ha.
Aliran energi di ekosistem mangrove bermula dari daun. Daun memegang
peran penting dan merupakan sumber nutrisi sebagai awal rantai makanan. Pada
ekosistem mangrove, rantai makanan yang terjadi adalah rantai makanan detritus.
Sumber utama detritus berasal dari daun-daun dan ranting-ranting yang telah
membusuk. Daun-daun yang gugur akan dimakan oleh jenis-jenis bakteri dan
fungi. Bakteri dan fungi ini akan dimakan oleh sebagian Protozoa dan Avertebrata
karnivor sedang, kemudian karnivor sedang ini dimakan oleh karnivor
yang lebih tinggi (Romimohtarto dan Sri, 2001).
Kondisi salinitas sangat mempengaruhi komposisi mangrove. Berbagai
jenis mangrove mengatasi kadar salinitas dengan cara yang berbeda-beda.
Beberapa diantaranya secara selektif mampu menghindari penyerapan garam dari
media tumbuhnya, sementara beberapa jenis yang lainnya mampu mengeluarkan
garam dari kelenjar khusus pada daunnya (Noor et al., 1999).
Serasah yang jatuh di lantai hutan mangrove mengalami proses
dekomposisi baik secara fisik maupun biologis, yang dapat menyuburkan kawasan
pesisir. Serasah yang sudah terdekomposisi tersebut berguna untuk menjaga
kesuburan tanah mangrove dan merupakan sumber pakan untuk berbagai jenis
ikan dan Avertebrata melalui rantai makanan fitoplankton dan zooplankton
sehingga keberlangsungan populasi ikan, kerang, udang dan lainnya dapat tetap
terjaga. Serasah mangrove yang terdekomposisi akan menghasilkan unsur hara
yang diserap oleh tanaman dan digunakan oleh jasad renik di lantai hutan dan
sebagian lagi akan terlarut dan terbawa air surut ke perairan sekitarnya
(Suwarno, 1985 dalam Rismunandar, 2000). Sesuai dengan pernyataan di atas
maka dilakukan penelitian mengenai Laju dekomposisi serasah daun
Ceriops tagal pada berbagai tingkat salinitas dan kandungan unsur hara karbon,
nitrogen, fosfor di Kampung Nipah Desa Sei Naga Lawan Kecamatan
Perbaungan.
Tujuan Penelitian
1. Menentukan laju dekomposisi serasah daun Ceriops tagal pada berbagai
2. Menentukan kandungan unsur hara karbon (C), nitrogen (N) dan fosfor (P)
pada serasah daun C. tagal yang mengalami dekomposisi pada berbagai tingkat
salinitas.
Hipotesis Penelitian
1. Laju dekomposisi serasah daun C. tagal lebih lambat pada tingkat salinitas
21-30 ppt
2. Pelepasan unsur hara C, N dan P pada proses dekomposisi serasah daun
C. tagal lebih cepat pada tingkat salinitas 21-30 ppt
Manfaat Penelitian
1. Dapat digunakan sebagai satu acuan dalam pengelolaan ekosistem mangrove
untuk menentukan zonasi pemanfaatan kawasan mangrove.
2. Dapat digunakan sebagai satu acuan untuk penentu lokasi yang sesuai untuk
AHMAD RUDIANSAH. Decomposition rate of C. tagal litter leaf at the various levels of salinity in the village of Sei Nagalawan Nipah sub-district of Perbaungan. Under academic supervisior by YUNASFI and DENI ELFIATI
Litter is beneficial to the process of decomposition of marine organisms as a source of food for the preservation of mangrove ecosystems. In the process of litter decomposition also releases nutrients that are needed by the mangrove plants were affected by the salinity level of seawater. For that research in the mangrove forest areas Kampung Nipa in the village of Sei Nagalawan Nipah sub-district of Perbaungan in June-September, 2015. This study aims to determine the effect of salinity on the rate of leaf litter decomposition C. tagal and determine the availability of nutrients carbon (C), nitrogen (N) and phosphorus (P) contained in the leaf litter C. tagal. The results of the study of leaf litter C. tagal at 10-20 ppt salinity level more quickly decomposes. The average weight of the rest of the leaf litter C. tagal which decompose at a rate of 0-10 ppt salinity, 10-20 ppt and 20-30 ppt was 31,17 grams, 25,93 grams, dan 27,46 grams. The rate of leaf litter decomposition C. tagal at a rate of 0-10 ppt salinity, 10-20 ppt and 20-30 ppt was 0,252, 0,297, and 0,198. Carbon levels of nutrients in the leaf litter C. tagal ppt salinity level 0-10, 10-20 ppt and 20-30 ppt was 13,36%, 9,8%, dan 12,2%. Levels of nutrients nitrogen in leaf litter C. tagal ppt salinity level 0-10 ppt, 10-20 ppt and 20-30 ppt was 2,5%, 2,5%, and 2,6%. . Levels of the nutrient phosphorus leaf litter C. tagal on ppt salinity level 0-10 ppt, 10-20 ppt and 20-30 ppt was 0,19%, 0,20%, and 0,18%. respectively. C/N ratio litter C. tagal on ppt salinity level 0-10 ppt, 10-20 ppt and 20-30 ppt was 5,34 %, 3,92% and 4,69%.respectively.
AHMAD RUDIANSAH. Laju Dekomposisi Serasah Daun C. tagal pada berbagai Tingkat Salinitas Di Kampung Nipah Desa Sei Nagalawan Kecamatan Perbaungan. Dibawah bimbingan YUNASFI dan DENI ELFIATI.
Serasah yang mengalami proses dekomposisi bermanfaat bagi organisme laut sebagai sumber makanan bagi kelestarian ekosistem mangrove. Dalam proses dekomposisi serasah juga melepaskan unsur hara yang sangat dibutuhkan oleh tanaman mangrove yang dipengaruhi oleh tingkat salinitas air laut. Untuk itu dilakukan penelitian di kawasan hutan mangrove Kampung Nipah Desa Sei Nagalawan Kecamatan Perbaungan pada bulan Juni – September 2015. Penelitian ini bertujuan untuk menentukan pengaruh tingkat salinitas terhadap laju dekomposisi serasah daun C. tagal dan menentukan ketersediaan unsur hara
karbon (C), Nitrogen (N) dan fosfor (P) yang terdapat pada serasah daun
C. tagal. Hasil penelitian serasah daun C. tagal pada tingkat salinitas 10-20 ppt
lebih cepat terdekomposisi. Rata-rata bobot sisa serasah daun C. tagal yang mengalami dekomposisi pada tingkat salinitas 0-10 ppt, 10-20 ppt dan 20-30 ppt yaitu 31,17 gram, 25,93 gram, dan 27,46 gram. Laju dekomposisi serasah daun
C. tagal pada tingkat salinitas 0-10 ppt, 10-20 ppt dan 20-30 ppt yaitu 0,252,
0,297, dan 0,198. Kadar unsur hara C serasah daun C. tagal pada tingkat salinitas 0-10 ppt, 10-20 ppt dan 20-30 ppt yaitu 13,36%, 9,8%, dan 12,2%. Kadar unsur hara N serasah daun C. tagal pada tingkat salinitas 0-10 ppt, 10-20 ppt dan 20-30 ppt yaitu 2,5%, 2,5%, dan 2,6%. Kadar unsur hara P serasah daun C. tagal pada tingkat salinitas 0-10 ppt, 10-20 ppt dan 20-30 ppt yaitu 0,19%, 0,20%, dan 0,18%. Rasio C/N serasah daun C. tagal pada tingkat salinitas 0-10 ppt, 10-20 ppt dan 20-30 ppt yaitu 5,34 %, 3,92% dan 4,69%.
NIPAH DESA SEI NAGALAWAN KECAMATAN
PERBAUNGAN
SKRIPSI
Oleh:
Ahmad Rudiansah 121201022 Budidaya Hutan
PROGRAM STUDI KEHUTANAN
FAKULTAS KEHUTANAN
UNIVERSITAS SUMATERA UTARA
Judul Penelitian : Laju Dekomposisi Serasah Daun Ceriops tagal Perr pada Berbagai Tingkat Salinitas di Kampung Nipah Desa Sei Naga Lawan Kecamatan Perbaungan.
Nama : Ahmad Rudiansah
NIM : 121201022
Program Studi : Kehutanan
Minat : Budidaya Hutan
Disetujui oleh Komisi Pembimbing
Dr. Ir. Yunasfi, M.Si. Dr. Deni Elfiati, SP., MP
Ketua Anggota
Mengetahui,
AHMAD RUDIANSAH. Decomposition rate of C. tagal litter leaf at the various levels of salinity in the village of Sei Nagalawan Nipah sub-district of Perbaungan. Under academic supervisior by YUNASFI and DENI ELFIATI
Litter is beneficial to the process of decomposition of marine organisms as a source of food for the preservation of mangrove ecosystems. In the process of litter decomposition also releases nutrients that are needed by the mangrove plants were affected by the salinity level of seawater. For that research in the mangrove forest areas Kampung Nipa in the village of Sei Nagalawan Nipah sub-district of Perbaungan in June-September, 2015. This study aims to determine the effect of salinity on the rate of leaf litter decomposition C. tagal and determine the availability of nutrients carbon (C), nitrogen (N) and phosphorus (P) contained in the leaf litter C. tagal. The results of the study of leaf litter C. tagal at 10-20 ppt salinity level more quickly decomposes. The average weight of the rest of the leaf litter C. tagal which decompose at a rate of 0-10 ppt salinity, 10-20 ppt and 20-30 ppt was 31,17 grams, 25,93 grams, dan 27,46 grams. The rate of leaf litter decomposition C. tagal at a rate of 0-10 ppt salinity, 10-20 ppt and 20-30 ppt was 0,252, 0,297, and 0,198. Carbon levels of nutrients in the leaf litter C. tagal ppt salinity level 0-10, 10-20 ppt and 20-30 ppt was 13,36%, 9,8%, dan 12,2%. Levels of nutrients nitrogen in leaf litter C. tagal ppt salinity level 0-10 ppt, 10-20 ppt and 20-30 ppt was 2,5%, 2,5%, and 2,6%. . Levels of the nutrient phosphorus leaf litter C. tagal on ppt salinity level 0-10 ppt, 10-20 ppt and 20-30 ppt was 0,19%, 0,20%, and 0,18%. respectively. C/N ratio litter C. tagal on ppt salinity level 0-10 ppt, 10-20 ppt and 20-30 ppt was 5,34 %, 3,92% and 4,69%.respectively.
AHMAD RUDIANSAH. Laju Dekomposisi Serasah Daun C. tagal pada berbagai Tingkat Salinitas Di Kampung Nipah Desa Sei Nagalawan Kecamatan Perbaungan. Dibawah bimbingan YUNASFI dan DENI ELFIATI.
Serasah yang mengalami proses dekomposisi bermanfaat bagi organisme laut sebagai sumber makanan bagi kelestarian ekosistem mangrove. Dalam proses dekomposisi serasah juga melepaskan unsur hara yang sangat dibutuhkan oleh tanaman mangrove yang dipengaruhi oleh tingkat salinitas air laut. Untuk itu dilakukan penelitian di kawasan hutan mangrove Kampung Nipah Desa Sei Nagalawan Kecamatan Perbaungan pada bulan Juni – September 2015. Penelitian ini bertujuan untuk menentukan pengaruh tingkat salinitas terhadap laju dekomposisi serasah daun C. tagal dan menentukan ketersediaan unsur hara
karbon (C), Nitrogen (N) dan fosfor (P) yang terdapat pada serasah daun
C. tagal. Hasil penelitian serasah daun C. tagal pada tingkat salinitas 10-20 ppt
lebih cepat terdekomposisi. Rata-rata bobot sisa serasah daun C. tagal yang mengalami dekomposisi pada tingkat salinitas 0-10 ppt, 10-20 ppt dan 20-30 ppt yaitu 31,17 gram, 25,93 gram, dan 27,46 gram. Laju dekomposisi serasah daun
C. tagal pada tingkat salinitas 0-10 ppt, 10-20 ppt dan 20-30 ppt yaitu 0,252,
0,297, dan 0,198. Kadar unsur hara C serasah daun C. tagal pada tingkat salinitas 0-10 ppt, 10-20 ppt dan 20-30 ppt yaitu 13,36%, 9,8%, dan 12,2%. Kadar unsur hara N serasah daun C. tagal pada tingkat salinitas 0-10 ppt, 10-20 ppt dan 20-30 ppt yaitu 2,5%, 2,5%, dan 2,6%. Kadar unsur hara P serasah daun C. tagal pada tingkat salinitas 0-10 ppt, 10-20 ppt dan 20-30 ppt yaitu 0,19%, 0,20%, dan 0,18%. Rasio C/N serasah daun C. tagal pada tingkat salinitas 0-10 ppt, 10-20 ppt dan 20-30 ppt yaitu 5,34 %, 3,92% dan 4,69%.
Penulis lahir di Desa Kampung Pajak tanggal 28 Oktober 1994 dari
pasangan Bapak Baharuddin Sinaga dan Ibu Ummi Kalsum Pohan. Penulis
merupakan anak pertama dari dua bersaudara.
Tahun 2012 penulis lulus dari MAN Aek Natas. Penulis selanjutnya tahun
yang sama penulis melanjutkan studi kuliah di Fakultas Kehutanan Program Studi
Budidaya Hutan Universitas Sumatera Utara melalui Seleksi Nasional Masuk
Perguruan Tinggi Negeri (SNMPTN).
Selama mengikuti Kuliah, penulis mengikuti kegiatan praktik Pengenalan
dan Pengelolaan Ekosistem Hutan (P2EH) di Pulau Sembilan Kecamatan
Pangkalan Susu, selama 10 hari. Tahun 2015, penulis menjadi asisten praktik
Pengenalan dan Pengelolaan Ekosistem hutan (P2EH) di kawasan Balai Penelitian
Konservasi Aek Nauli. Pada tahun 2013-2014 penulis menjadi Asisten Praktikum
Dendrologi Hutan. Pada tahun 2016 penulis mengikuti Praktik Kerja Lapangan di
Taman Nasional Manupeu Tanah Daru (TNMT), Nusa Tenggara Timur (NTT)
selama satu bulan. Tahun 2016, Penulis juga melakukan penelitian di kawasan
Hutan Mangrove Kampung Nipah Desa Sei Nagalawan Kecamatan Perbaungan
selama 90 hari.
Penulis mengikuti organisasi kemahasiswaan Kesatuan Aksi Mahasiswa
Muslim Indonesia (KAMMI) di Bidang Kaderisasi, Unit Kegiatan Mahasiswa
Muslim (UKMI) Baytul Asyjaar Fakultas Kehutanan Sebagai Ketua Umum