1 I. PENDAHULUAN
A. LATAR BELAKANG
Gambir asalan adalah produk tanaman gambir (Uncaria gambir (Hunt.) Roxb) yang berasal dari getah daun gambir dengan mengalami tahapan pengolahan tertentu. Gambir asalan merupakan produk ekspor andalan Indonesia yang memiliki negara tujuan ekspor seperti India, Pakistan, Nepal, Banglades, Filipina, Singapura, dan Australia. Sebesar 84% total gambir asalan Indonesia diekspor menuju India (BPS, 2008).
Mutu gambir Indonesia mengalami kondisi yang fluktuatif sehingga menyebabkan ketidakstabilan nilai ekspor yang ditunjukkan dengan pertumbuhan ekspor yang kurang baik setiap tahunnya. Mutu gambir yang rendah menyebabkan harga di pasaran dunia menjadi rendah dan memberikan pengaruh pada penurunan permintaan pasar ekspor. Berdasarkan data ekspor gambir Indonesia pada tahun 2008, jumlah negara tujuan ekspor gambir Indonesia berkurang seperti Korea Selatan, Taiwan, Thailand, Yaman, Sudan, dan Italia (BPS, 2008).
Penurunan pasar ekspor gambir Indonesia memerlukan adanya upaya peningkatan mutu produk gambir. Peningkatan mutu gambir dapat dilakukan dengan perbaikan proses pada pembuatan produk gambir dan diversifikasi gambir menjadi beberapa produk turunan yang memiliki nilai tambah yang tinggi. Diversifikasi gambir menjadi produk olahan atau produk turunan gambir diharapkan dapat meningkatkan nilai jual gambir, meningkatkan nilai ekspor gambir mentah maupun gambir olahan (produk turunan), menyejahterakan kehidupan petani gambir dan membuka lapangan pekerjaan.
2 Menurut Gumbira-Sa’id, et al. (2009a), katekin dan tanin merupakan dua produk utama hasil pemurnian komponen yang terkandung dalam produk gambir asalan. Rasio nilai tambah dari pengolahan gambir menjadi tanin untuk tiga kilogram gambir adalah 83,81 % dan katekin adalah 91,67 %. Berdasarkan hal tersebut, pengembangan produksi gambir olahan menjadi tanin memiliki potensi besar untuk dilakukan dan tidak kalah penting dengan katekin.
Penelitian yang dilakukan oleh Nazir dan Norman (2001) menunjukkan bahwa proses pemurnian gambir menjadi katekin murni dapat menghasilkan tanin yang berasal dari sisa pencucian pemurnian katekin. Berdasarkan hal tersebut, tidak hanya katekin, tetapi tanin juga dapat dihasilkan dari gambir. Berbagai penelitian yang dilakukan dalam proses pemurnian gambir pada umumnya berkaitan dengan cara pemurnian untuk menghasilkan katekin murni. Penelitian tentang pemurnian gambir yang menghasilkan tanin (ekstraksi tanin) perlu dilakukan lebih lanjut untuk menghasilkan produk tanin yang lebih baik.
Tanin merupakan senyawa polifenol yang memiliki manfaat cukup banyak. Tanin dapat digunakan dalam industri kulit, industri tekstil, industri farmasi, industri kosmetik dan dalam laboratorium. Tanin dalam indstri tekstil digunakan sebagai pewarna. Tanin dikenal sebagai senyawa antioksidan dan dapat digunakan sebagai senyawa peluruh karat (rust converter) dan senyawa anti karat (rust inhibitor) (Gumbira-Sa’id, et al. 2009a). Menurut Carter et al. (1978), tanin dapat mengikat logam berat, serta adanya zat yang bersifat anti rayap dan jamur. Tanin adalah zat yang berfungsi membersihkan dan menyegarkan mulut, sehingga dapat mencegah kerusakan gigi dan penyakit gusi.
3 dilakukan proses pembuatan tanin bubuk dari gambir asalan yang diharapkan dapat menghasilkan tanin yang memiliki kadar tanin tinggi dengan tahapan proses yang optimum.
B. TUJUAN
Tujuan yang ingin dicapai dari penelitian ini adalah untuk mendapatkan tanin dari gambir asalan dengan proses ekstraksi dan mendapatkan perlakuan terbaik dalam produksi tanin bubuk dari gambir asalan.
C. RUANG LINGKUP
Ruang lingkup pada penelitian ini adalah sebagai berikut:
1. Melakukan ekstraksi tanin dari gambir asalan dan menentukan perlakuan terbaik dengan faktor perlakuan suhu air (400C, 600C dan 800C ) dan perlakuan perbandingan jumlah pelarut (air) dan gambir asalan (8:1, 10:1 dan 12:1 v/b)
2. Melakukan pengeringan larutan ekstrak tanin dengan menggunakan alat pengering semprot (spray dryer)
4 II. TINJAUAN PUSTAKA
A. TANAMAN GAMBIR
Tanaman gambir (Uncaria gambir (Hunt.) Roxb) merupakan spesies tanaman berbunga genus Uncaria dalam family Rubiaceae. Berdasarkan karakteristik morfologinya, tanaman gambir termasuk jenis tanaman perdu setengah merambat yang memiliki batang berkayu (Fiani dan Denian, 1994 dalam Nazir, 2000). Secara botanis, tanaman gambir diklasifikasikan sebagai berikut (Nazir, 2000):
Spesies : Uncaria gambir Roxb.
Daun gambir tumbuh tunggal pada tangkai batang dan saling berhadapan, berwarna hijau dan memiliki panjang 8-13 cm dan lebar 4-7 cm. Bentuk daun oval, bagian ujung meruncing, bagian tepi bergerigi, dan permukaan tidak berbulu. Tanaman gambir memiliki bunga mejemuk berbentuk lonceng dan berwarna merah muda atau hijau yang tumbuh di ketiak daun. Bunga gambir memiliki panjang sekitar 5 cm dengan lima helai mahkota bunga. Buah gambir berbentuk bulat telur, berwarna hitam memiliki panjang sekitar 1.5 cm dan dua ruang buah (Brown, 2009 dalam Gumbira-Sa’id , et al. 2009a).
5 Gambar 1. Contoh Penampakan Tanaman Gambir (Gumbira-Sa’id , et al., 2009b)
Menurut Sastrapradja et al., (1980) dalam Nazir (2000), tanaman gambir ditemukan liar di hutan-hutan di Sumatra, Kalimantan, dan di Semenanjung Malaya. Di samping itu, tanaman gambir juga dibudidayakan di Jawa, Bali, dan Maluku. Tanaman ini umumnya tumbuh dengan baik pada ketinggian 0-800 m di atas permukaan laut.
B. GAMBIR
6 Tabel 1. Komponen-Komponen dalam Gambir
No. Nama Komponen Jumlah (%)
1 Catechin 7 – 33
2 Asam catechutannat 20 – 55
3 Pyrocathecol 20 -30
4 Gambir flouresensi 1 – 3
5 Red Catechu 3 – 5
6 Quersetin 2 – 4
7 Fixed oil 1 – 2
8 Lilin 1 – 2
9 Alkaloid Sedikit
Sumber : Thorpe dan Whiteley (1921) dalam Gumbira Sa’id, et al. (2009a) Berikut ini merupakan karakteristik umum komponen-komponen yang terkandung dalam gambir (Thorpe dan Whiteley, 1921; Nazir, 2000 dalam Gumbira-Sa’id, et al. 2009a):
1. Katekin
Katekin (C15H14O6) tergolong dalam jenis pseudotanin dan termasuk
polifenol antioksidan yang bersifat dapat larut dalam alkohol dingin, air panas, serta asam asetat glasial dan aseton. Katekin sukar larut dalam air dingin dan eter, selain itu tidak larut dalam CHCl3, metil eter dan benzene.
Katekin membentuk endapan jika bereaksi dengan Pb(CH3COO)2.
Katekin menghasilkan larutan yang berwarna biru jika bereaksi dengan FeCl3. Jika katekin bereaksi dengan pine wood dan HCl akan terbentuk
phloro glucinol.
Menurut Muchtar (2000), senyawa katekin memberikan rasa manis dan enak, tidak mudah larut dalam air dingin dan larut baik dalam air panas, jika dalam bentuk kering berbentuk kristal berwarna kuning. Struktur kimia katekin dapat dilihat pada Gambar 2.
7 2. Asam catechutannat
Asam catechutannat larut dalam alkohol dan air dingin, tidak larut dalam eter. Asam catechutannat membentuk endapan jika bereaksi dengan Pb (CH3COO)2 dan membentuk endapan berwarna hijau jika bereaksi dengan
CHCl3. Asam catechutannat bereaksi dengan pine wood dan HCl
membentuk reaksi phloro glucinol. Asam catechutannat disebut anhydride dan dapat dihasilkan apabila larutan dipanaskan pada suhu 110oC dengan larutan alkali karbonat. Struktur kimia asam catechutannat dapat dilihat pada Gambar 3.
Gambar 3. Struktur Kimia Asam Catechutannat (Nazir, 2000) 3. Pyrocathecol
Pyrocathecol larut dalam air, alkohol, eter, benzene, klorofom dan larut baik pada piridin dengan larutan bersifat basa, jika dipanaskan akan membentuk catechol. Pyrocathecol membentuk warna hijau dengan FeCl3
dan membentuk endapan dengan brom. Larutannya dalam air cepat berwarna coklat. Pyrocathecol dapat mereduksi perak amoniakal dan larutan Fehling.
4. Gambir flouresensi
Gambir flouresensi dapat dilihat apabila larutan gambir dikocok dengan petroleum eter dalam suasana sedikit basa. Gambir flouresensi pada lapisan petroleum eter akan terlihat perpendaran berwarna hijau.
5. Red catechu
Red catechu merupakan gambir yang memberikan warna merah. 6. Fixed oil
8 7. Quersetin
Quersetin (C15H10O7) merupakan senyawa turunan flavonoid tanaman
yang larut dalam air dan alkohol. Warna quersetin berubah menjadi warna gelap dengan pemanasan. Quersetin memiliki manfaat sebagai anti-inflammatory dan antioksidan serta berbagai potensi kesehatan yang menguntungkan lainnya. Struktur kimia quercetin dapat dilihat pada Gambar 4.
Gambar 4. Struktur Kimia Quersetin (Gumbira-Sa’id, et al. 2009a) 8. Lilin
Lilin terdapat pada permukaan daun gambir. Lilin merupakan monoester dari suatu asam lemak dan alkohol.
9. Alkaloid
Alkaloid terdapat tujuh jenis alkaloid pada tanaman gambir yaitu dihidrogambir taninna, gambirdina, gambirina, isogambirina, auroparina, oksogambir-tanina. Tanin yang terdapat dalam gambir merupakan tanin yang tidak dapat dihidrolisa (tanin kondensasi). Tanin tersebut merupakan turunan dari flavanol yang tidak dapat dihidrolisis dengan asam ataupun basa.
9 Gambir dapat dimanfaatkan dalam industri kulit, tekstil, dan kosmetika. Getah gambir dapat digunakan sebagai zat penyamak kulit dalam industri kulit. Dalam industri tekstil, gambir dapat digunakan sebagai zat warna. Gambir digunakan sebagai pembantu untuk mendapatkan warna coklat dan kemerah-merahan pada pembuatan kain batik. Dalam industri kosmetika, gambir dapat digunakan untuk astringent yang berfungsi untuk melembutkan kulit dan menambah kelenturan serta daya regang kulit (Nazir, 2000).
Berdasarkan perbedaan bentuknya, gambir asalan yang diproduksi di Indonesia terdiri dari empat jenis yaitu gambir bootch, lumpang, coin, wafer block, dan stick. Gambar beberapa jenis gambir dapat dilihat pada Gambar 5.
Gambar 5. Berbagai Jenis Gambir Indonesia (Gumbira-Sa’id, et al. 2009a) a. Gambir stick; b. Gambir coin; c. Gambir bootch;
10
Daun
Perebusan
Pengepresan
Pengendapan
Penirisan
Pencetakan
Pengeringan
Gambir
Gambar 6. Diagram Alir Pengolahan Gambir Rakyat (Gumbira-Sa’id, et al.
2009a)
Berdasarkan laporan Gumbira-Sa’id, et al. (2009b), secara rinci urutan proses pengolahan gambir yang dilakukan di Kabupaten Lima Puluh Kota adalah sebagai berikut:
1. Perebusan daun
dibolak-11 balik sambil ditusuk-tusuk dengan kayu untuk memberi jalan air panas agar perebusan merata.
2. Pengempaan
Setelah daun gambir selesai direbus dan diangkat, daun kemudian dililit kembali oleh rajut agar daun tetap berada dalam gulungan. Air bekas rebusan disiramkan kembali ke daun yang akan dikempa karena masih banyak asam samak yang terlarut dalam proses perebusan. Alat kempa yang digunakan dapat berupa kempa yang terbuat dari dua bilah kayu besar berbentuk huruf V dengan panjang kayu sekitar tiga meter. Proses pengempaan membutuhkan waktu sekitar 60 menit.
3. Pengendapan
Getah gambir yang diperoleh dari proses pengepresan dimasukkan ke dalam sebuah tempat pengendapan terdiri dari kayu mirip perahu yang disebut peraku. Pengendapan memerlukan waktu sekitar 8-12 jam. Endapan yang diperoleh berbentuk kristal-kristal seperti pasta tetapi lebih encer.
4. Penirisan
Alat penirisan terbuat dari kain blacu, tali, dan alat pemberat seperti kayu dan lain-lain. Getah dalam bentuk pasta encer dimasukkan ke dalam kain blacu, diikat dan dipres lagi dengan alat pemberat agar pasta yang terjadi lebih pekat dan dapat segera dicetak. Penirisan biasanya memerlukan waktu 10-20 jam, tergantung pada banyaknya bahan yang ditiriskan.
5. Pencetakan
Bentuk cetakan gambir terdiri dari tiga macam. Untuk konsumsi dalam negeri (makan sirih), gambir dicetak berbentuk silinder cekung. Untuk tujuan ekspor atau industri batik, penyamak dan lain-lain, gambir dicetak berbentuk koin dan silinder. Setiap kilogram bahan baku gambir mampu dicetak dalam waktu sekitar 25-30 menit per orang.
12 Pengeringan merupakan proses terakhir dalam pengolahan gambir. Gambir hasil cetakan kemudian diletakkan di atas tempat seperti baki, kemudian dijemur di panas matahari. Bila cuaca mendung, gambir dikeringkan di atas tungku perebusan daun. Pengeringan memerlukan waktu dua hingga tiga hari tergantung pada cuaca.
C. TANIN
Tanin dapat dijumpai pada hampir semua jenis tumbuhan hijau di seluruh dunia, baik tumbuhan tingkat tinggi maupun tingkat rendah dengan kadar dan kualitas yang berbeda-beda. Di Indonesia sumber tanin antara lain diperoleh dari jenis bakau-bakauan atau jenis-jenis dari hutan tanaman industri seperti akasia (Acacia sp), eukaliptus (Eucalyptus sp), pinus (Pinus sp) dan sebagainya. Tanin adalah polifenol alami yang selama ini banyak digunakan sebagai bahan perekat tipe eksterior, yang terutama terdapat pada bagian kulit kayu. Tanin memiliki sifat dapat larut dalam air atau alkohol karena tanin banyak mengandung fenol yang memiliki gugus OH, dapat mengikat logam berat, serta adanya zat yang bersifat anti rayap dan jamur (Carter et al., 1978).
Menurut Muchtar (2000), senyawa tanin memberikan bau dan rasa yang khas dan memberikan warna merah kecoklatan, mudah larut dalam air dingin dan alkohol, tetapi tidak larut dalam ester dan bila airnya diuapkan akan membentuk kristal yang berwarna coklat kemerahan. Berdasarkan Hathway (1962), tanin adalah senyawa organik yang terdiri dari campuran senyawaan polifenol kompleks, dibangun dari elemen C, H dan O serta sering membentuk molekul besar dengan bobot molekul lebih besar dari 2000.
Menurut Sjostrom (1981), tanin adalah suatu senyawa polifenol yang dari struktur kimianya dapat digolongkan menjadi dua macam, yaitu tanin terhidrolisis (hidrolizable tannin) dan tanin terkondensasi (condensed tannin). Ekstrak dari tanin tidak dapat murni 100%, karena selain terdiri dari tanin terdapat juga zat non tanin seperti glukosa dan hidrokoloid yang memiliki bobot molekul tinggi (Pizzi, 1983).
13 warna merah yang disebut flobafen atau tanin merah. Tanin yang terdapat dalam gambir merupakan tanin yang tidak dapat dihidrolisis (tanin terkondensasi). Tanin terhidrolisis adalah tanin yang mudah terhidrolisis dengan asam, basa, dan enzim yang membentuk asam galat dan beberapa asam lainnya (Tyler dalam Yeni et al., 2004). Contoh struktur molekul tanin terhidrolisis dapat dilihat pada Gambar 7 dan tanin terkondensasi pada Gambar 8.
Gambar 7. Contoh Struktur Molekul Tanin Terhidrolisis (Gross, 1992).
14 Menurut Browning (1966), sifat utama tanin tumbuh-tumbuhan tergantung pada gugusan fenolik-OH yang terkandung dalam tanin, dan sifat tersebut secara garis besar dapat diuraikan adalah sebagai berikut:
1. Sifat kimia tanin
a. Tanin memiliki sifat umum, yaitu memiliki gugus fenol dan
bersifat koloid. Oleh karena itu, di dalam air bersifat koloid dan asam lemah
b. Semua jenis tanin dapat larut dalam air. Kelarutannya besar, dan akan bertambah besar apabila dilarutkan dalam air panas. Begitu juga tanin akan larut dalam pelarut organik seperti metanol, etanol, aseton dan pelarut organik lainnya
c. Dengan garam besi memberikan reaksi warna. Reaksi tersebut digunakan untuk menguji klasifikasi tanin, karena tanin dengan garam besi memberikan warna hijau dan biru kehitaman. Tetapi uji ini kurang baik, karena selain tanin yang dapat memberikan reaksi warna, zat-zat lain juga dapat memberikan warna yang sama
d. Tanin akan terurai menjadi pyrogallol, pyrocatechol, dan phloroglucinol bila dipanaskan sampai suhu 98,890C-101,670C e. Tanin dapat dihidrolisis oleh asam, basa, dan enzim
f. Ikatan kimia yang terjadi antara tanin-protein atau polimer- polimer lainnya terdiri dari ikatan hidrogen, ikatan ionik dan ikatan kovalen
2. Sifat fisik tanin
a. Umumnya tanin mempunyai bobot molekul tinggi dan cenderung mudah dioksidasi menjadi suatu polimer, sebagian besar tanin tidak berbentuk (amorf) dan tidak mempunyai titik leleh
b. Tanin berwarna putih kekuning-kuningan sampai coklat terang, tergantung dari sumber tanin tersebut
c. Tanin berbentuk serbuk atau berlapis-lapis seperti kulit kerang, berbau khas dan mempunyai rasa sepat (astringent)
15 e. Tanin mempunyai sifat atau daya bakteriostatik, fungistatik dan
merupakan racun
Tanin dapat digunakan dalam industri kulit, industri tekstil, industri farmasi, industri kosmetik dan dalam laboratorium. Tanin dalam indstri tekstil digunakan sebagai pewarna. Tanin dapat digunakan untuk mewarnai sutera, wool, dan kain batik. Dalam industri farmasi, tanin dapat digunakan sebagai obat anti diare, obat kumur, dan obat sakit kulit (Nazir, 2000 dalam Yeni, et al.,2004). Tanin dikenal sebagai senyawa antioksidan dan dapat digunakan sebagai senyawa peluruh karat (rust converter) dan senyawa anti karat (rust inhibitor) (Gumbira-Sa’id, et al. 2009a).
Tanin dapat berfungsi sebagai zat yang dapat membersihkan dan menyegarkan mulut sehingga dapat mencegah kerusakan gigi dan penyakit gusi. Tanin juga memiliki fungsi sebagai zat antibakteri. Secara garis besar, mekanisme tanin sebagai zat antibakteri adalah sebagai berikut: toksisitas tanin dapat merusak membran sel bakteri, senyawa astringent tanin dapat menginduksi pembentukan kompleks senyawa ikatan terhadap enzim atau subtrat mikroba dan pembentukan suatu kompleks ikatan tanin terhadap ion logam yang dapat menambah daya toksisitas tanin sendiri (Akiyama, et al. 2001). Menurut Masduki (1996), tanin juga mempunyai daya antibakteri dengan cara mempresipitasi protein. Efek antibakteri tanin antara lain melalui reaksi dengan membran sel, inaktivasi enzim, dan destruksi atau inaktivasi fungsi materi genetik
D. EKSTRAKSI TANIN
16
1962). Fengel (1993) menambahkan dalam proses ekstraksi, tanin yang dihasilkan bukan merupakan tanin murni tetapi masih mengandung unsur-unsur lainnya. Tanin yang banyak terdapat dalam tumbuhan berpembuluh dapat diperoleh dengan melakukan ekstraksi pada bagian kayu dan kulit kayu dengan menggunakan air atau pelarut organik seperti aseton atau etanol.
Proses ekstraksi tanin yang berasal dari gambir asalan merupakan serangkaian proses pemurnian gambir yang dapat menghasilkan produk tanin dan katekin. Proses pemurnian gambir yang dapat menghasilkan tanin dapat dilihat pada Gambar 9.
17 Menurut Syafii (2000), tanin yang terdapat pada kulit Acacia decurrens dapat diperoleh dengan cara mengekstraksi kulit pada suhu dan waktu tertentu serta jenis pengekstrak tertentu, tergantung pada asal bahan baku. Suhu dan lama ekstraksi merupakan faktor yang perlu untuk diperhatikan karena dapat mempengaruhi efisiensi dalam proses ekstraksi. Pada pemanasan dengan suhu yang terlalu tinggi akan diperoleh tanin dalam jumlah yang besar tetapi kualitas tanin yang dihasilkan kurang baik karena komponen non tanin yang terlarut semakin besar.
Kelarutan suatu senyawa dalam pelarut akan meningkat dengan meningkatnya suhu karena peningkatan suhu akan mempermudah penetrasi pelarut dalam sel bahan. Namun, penggunaan suhu yang tinggi akan menyebabkan kehilangan senyawa tertentu yang tidak stabil pada kondisi tersebut (Houghton dan Raman, 1998).
Menurut Bernardini (1983), beberapa faktor yang mempengaruhi jumlah rendemen hasil ekstraksi adalah perlakuan pendahuluan terhadap bahan yang meliputi pengecilan ukuran bahan dan pengeringan bahan, pemilihan jenis pelarut, perbandingan jumlah pelarut dan bahan serta pengaturan kondisi ekstraksi seperti lama ekstraksi dan suhu ekstraksi.
E. PENGERING SEMPROT (SPRAY DRYER)
Proses pengeringan semprot adalah proses yang mengubah bahan fluida menjadi produk kering dalam satu operasi (Filkova dan Mujumdar, 1995). Alat pengering semprot digunakan untuk mengeringkan larutan, campuran atau produk cair lain menjadi tepung dengan kadar air yang mendekati kesetimbangan dengan kondisi udara pada tempat produk keluar (Wirakartakusumah et al., 1989).
18 diserap oleh udara dan dikeluarkan dari alat pengering semprot. Serbuk kering kemudian jatuh ke bawah dan ditampung dalam wadah tertentu (Speer, 1998).
Keunggulan pengering semprot antara lain adalah sifat dan mutu produk dapat terkontrol secara efektif, dapat digunakan pada makanan yang peka terhadap panas, produk biologi dan farmasi dapat dikeringkan pada suhu atmosfer dan suhu rendah, menghasilkan produk yang relatif seragam, partikel-partikelnya berbentuk bulat mendekati proporsi yang sama (Widodo, 2006). Waktu kontak antara droplet bahan dengan udara panas dalam ruangan pengering berlangsung hanya beberapa detik sehingga kecil kemungkinan nutrisi terdegradasi akibat panas (Master, 1979).
Menurut Singh dan Heldman (2001), keuntungan dari penggunaan alat pengering semprot adalah siklus pengeringannya yang cepat, retensi dalam ruang pengeringan (residence time) singkat dan produk akhir siap dikemas ketika selesai proses dengan kadar air produk sekitar 5%. Residence time pada alat pengering semprot antara 5-100 detik dan partikel yang dihasilkan mempunyai ukuran 10-500 µ m (Canovas dan Mercado, 1996).
19 Tahap 4
Pemisahan Produk Dari Udara Kering Tahap 1
Atomisasi
Tahap 3 Evaporasi
Ruang Pengering Tahap 2
Kontak partikel uadara
Siklon
Produk
Scrubber
Bahan Udara
20 III. METODE PENELITIAN
A. ALAT DAN BAHAN
Alat-alat yang digunakan dalam ekstraksi tanin adalah pemanas, wadah pelarutan, termometer, palu, gelas ukur, botol, kain saring, corong, timbangan, dan spray dryer. Alat-alat yang digunakan untuk pengujian antara lain adalah spektrofotometer HACH, erlenmeyer, gelas piala, oven, desikator, gelas ukur, pipet, cawan alumunium, cawan porselen, colorimeter Colortech PCM, labu takar, dan tanur. Bahan yang digunakan dalam penelitian meliputi gambir asalan dari daerah Kampar (Riau), kertas saring, NaOH, CuSO4, HCl, H2SO4,
air panas, reagen Folin Ciocalteu, larutan jenuh Na2CO3, tannic acid, dan
akuades.
B. WAKTU DAN TEMPAT PENELITIAN
Penelitian ini dilakukan dari bulan April sampai Juli 2010, bertempat di Bengkel Kerja Departemen Teknologi Industri Pertanian, Laboratorium Dasar Ilmu Terapan, Laboratorium Pengawasan Mutu, dan Laboratorium Instrumen, Departemen Teknologi Industri Pertanian, Fakultas Pertanian, Institut Pertanian Bogor.
C. TATA LAKSANA PENELITIAN
Pada penelitian utama dilakukan ekstraksi tanin dari gambir asalan dengan faktor suhu dan jumlah pelarut yang berbeda. Variasi suhu yang digunakan untuk melarutkan adalah 400C, 600C dan 800C. Jumlah air dengan gambir asalan memiliki variasi perbandingan antara 8:1 , 10:1, dan 12:1 (v/b). Jumlah gambir asalan yang digunakan pada tiap perlakuan adalah sebanyak 150 gram.
21 dengan melakukan pemanasan hingga suhu 400C, 600C dan 800C. Tahap selanjutnya, larutan gambir disaring untuk menyaring kotoran dalam gambir yang tidak larut dalam air. Tahapan setelah penyaringan adalah pengendapan yang dilakukan selama 12 jam untuk memisahkan senyawa tanin dan katekin. Setelah proses pengendapan, untuk mengambil fraksi yang mengendap (katekin) dan tidak mengendap (tanin) dilakukan dengan menggunakan proses penyaringan. Fraksi tidak mengendap kemudian diperas dan disaring kembali sehingga diperoleh filtrat tanin.
Larutan tanin yang diperoleh kemudian dikeringkan menggunakan spray dryer dengan suhu inlet 1300C -1400C dan suhu outlet 750C-780C sehingga terbentuk tanin bubuk. Alat pengering semprot (spray dryer) yang digunakan dalam penelitian dapat dilihat pada Gambar 11 dan Lampiran 1. Diagram alir pembuatan tanin bubuk dari gambir asalan dapat dilihat pada Gambar 12.
22
Pelarutan
Air panas
(suhu air: 400C, 600C, 800C) (jumlah air:bahan = 8:1 v/b,10:1 v/b,12:1 v/b)
Pengendapan
Gambar 12. Diagram Alir Pembuatan Tanin Bubuk dari Gambir Asalan pada Penelitian Ini
D. PROSEDUR ANALISIS
Analisis yang dilakukan dalam penelitian ini dilakukan terhadap bahan baku yaitu gambir asalan dan produk tanin bubuk. Beberapa pengujian yang dilakukan dalam penelitian ini antara lain adalah analisis proksimat, kadar tanin, kadar bahan tidak larut air, dan uji warna. Prosedur analisis dapat dilihat pada Lampiran 2.
E. RANCANGAN PERCOBAAN
23 digunakan adalah suhu air (400C, 600C, dan 800C) dan perbandingan jumlah air dengan gambir asalan (8:1, 10:1, dan 12:1 v/b). Dengan demikian terdapat 9 unit perlakuan dengan dua kali ulangan. Model yang digunakan untuk desain penelitian ini adalah sebagai berikut (Walpole, 1997):
Yijk = µ + Ai +Bj + ABij+ єk(ij)
Keterangan:
Ai : pengaruh perbandingan jumlah air dengan gambir asalan pada
taraf ke-i
Bj : pengaruh suhu pelarut (air) taraf ke-j
ABij : pengaruh interaksi antara faktor A taraf ke-i dan faktor B
taraf ke-j
єk(ij) : pengaruh acak antara faktor A taraf ke-i dan faktor B taraf
24 IV. HASIL DAN PEMBAHASAN
A. KARAKTERISTIK GAMBIR ASALAN
Produk tanaman gambir yang sering dikenal sebagai gambir asalan merupakan ekstrak getah dari daun dan ranting tanaman gambir yang telah mengalami pengeringan. Getah tanaman gambir yang telah dikeringkan tersebut memiliki beberapa kandungan senyawa kimia dengan jumlah tertentu. Gambir asalan yang digunakan dalam penelitian adalah gambir asalan yang berasal dari daerah Kampar, Riau. Untuk mengetahui karakteristik gambir asalan yang digunakan dalam penelitian ini dilakukan analisis proksimat. Hasil pengujian analisis proksimat dapat dilihat pada Tabel 2.
Tabel 2. Hasil Analisis Proksimat Gambir Asalan No. Karakteristik Hasil Pengujian (%)
1 Air 12,36
Kadar air gambir asalan yang digunakan dalam penelitian bernilai 12,36%. Nilai kadar air tersebut dipengaruhi oleh proses pengeringan dan penyimpanan gambir asalan. Proses pengeringan gambir asalan yang bersifat tradisional dengan menggunakan sinar matahari memungkinkan gambir asalan masih memiliki kandungan air yang tinggi. Nilai kadar air yang masih tinggi setelah pengeringan dapat menyebabkan tumbuhnya kapang pada saat penyimpanan.
25 pembuatan gambir asalan memiliki kandungan mineral dan sebagian mineral tersebut dapat larut dalam air serta terbawa selama proses pengolahan gambir. Hasil pengujian kandungan kadar lemak pada gambir asalan adalah 1,61%. Gambir asalan diolah dengan menggunakan air panas sebagai pelarut untuk mengekstraksi getah pada daun dan ranting tanaman gambir. Air merupakan senyawa polar sehingga tidak dapat melarutkan lemak yang bersifat non polar. Oleh karena hal tersebut, nilai kadar lemak pada gambir asalan bernilai sangat kecil. Namun demikian, proses pengolahan yang kurang baik dapat menyebabkan adanya kontaminasi sehingga nilai kandungan lemak meningkat.
Nilai hasil pengujian kadar serat kasar gambir asalan yang digunakan dalam penelitian adalah 6,16%. Berdasarkan Sudarmadji et al. (1989), serat kasar mengandung senyawa selulosa, lignin, dan zat lain yang belum dapat diidenstifikasi dengan pasti. Serat kasar digunakan sebagai penilaian kualitas suatu bahan dan mengevaluasi efisiensi dalam proses pengolahan. Selama proses pengolahan gambir asalan, sebagian serat kasar yang terdapat dalam daun dan ranting tanaman gambir dapat ikut terbawa dalam getah gambir. Banyaknya nilai serat yang ikut terekstrak dipengaruhi oleh proses pengolahan yang terjadi dan nilai kandungan serat kasar dalam daun dan ranting gambir asalan.
26 katekin, dan senyawa lainnya. Senyawa tanin dapat berikatan dengan karbohidrat membentuk senyawa kompleks sehingga senyawa tersebut dapat dimasukan dalam kadar bahan lain-lain pada gambir asalan. Menurut Caolate (1990) dalam Yeni, et al. (2004) komponen dasar dalam tanin adalah asam galat dan flavonoid yang dapat membentuk glikosida bila polifenol berikatan dengan karbohidrat.
Karakteristik gambir asalan sebagai bahan baku berpengaruh pada tanin bubuk yang dihasilkan dari proses ekstraksi. Beberapa karakteristik kandungan kimia gambir asalan yang berpengaruh terhadap produk tanin bubuk antara lain nilai kadar abu dan nilai kadar tanin gambir asalan. Nilai kadar abu berpengaruh terhadap jumlah mineral yang ikut terekstrak selama proses pengolahan sedangkan nilai kadar tanin berpengaruh terhadap tingkat kemurnian produk tanin yang dihasilkan. Gambir yang memiliki kadar tanin tinggi menjadi bahan baku pembuatan tanin bubuk yang potensial untuk digunakan. Dengan nilai kandungan tanin dalam bahan baku yang tinggi, jumlah ekstrak tanin yang diperoleh diharapkan juga semakin tinggi.
B. EKSTRAKSI TANIN
Senyawa utama yang terkandung di dalam gambir asalan adalah katekin dan asam catechutannat. Katekin merupakan senyawa polifenol yang memiliki bentuk sederhana cathecol. Asam catechutannat merupakan anhidrat katekin yang sering disebut tanin dalam gambir. Tanin yang terdapat dalam gambir dapat diekstrak untuk diperoleh produk tanin yang memiliki tingkat kemurnian tinggi. Proses pengambilan tanin dalam gambir asalan melibatkan proses pemisahan antara senyawa katekin dan tanin yang keduanya merupakan jenis senyawa polifenol. Menurut Fessenden (1982), polifenol merupakan senyawa yang memiliki struktur dasar berupa fenol dan fenol merupakan struktur yang terbentuk dari benzene yang tersubstitusi dengan gugus OH.
27 jenis pelarut yang sesuai sangat mempengaruhi proses ekstraksi. Menurut Gemse (2002), faktor penting dalam ekstraksi adalah pemilihan pelarut. Pelarut yang digunakan dalam ekstaksi harus dapat menarik komponen aktif dalam campuran. Hal-hal penting yang harus diperhatikan dalam pemilihan pelarut adalah selektivitas, sifat pelarut, kemampuan untuk mengekstraksi, tidak bersifat racun, kemudahan untuk diuapkan, dan harga yang relatif murah.
Penggunaan air sebagai pelarut dalam penelitian ini didasarkan pada beberapa pertimbangan. Beberapa pertimbangan tersebut antara lain karena air tidak berbahaya dalam penggunaannya, tidak bersifat racun, tidak bersifat korosif terhadap peralatan ekstraksi, mudah diperoleh, dan, harganya murah. Selain itu, dengan menggunakan pelarut air, katekin dan tanin dapat dipisahkan dengan metode pemisahan yang sederhana yaitu pengendapan.
Tanin dapat larut dalam air dan kelarutannya semakin besar jika dilarutkan pada suhu tinggi (Browning, 1966). Untuk mengetahui pengaruh peningkatan suhu pelarut pada proses ekstraksi, dalam penelitian ini digunakan tiga taraf suhu yaitu 400C, 600C,dan 800C. Selain suhu, faktor lainnya yang digunakan adalah perbandingan jumlah pelarut dan gambir asalan. Perbandingan jumlah air dan gambir asalan yang digunakan sebanyak tiga taraf yaitu 8:1, 10:1, dan 12:1 (v/b).
28
a b
Gambar 13. Gambir Asalan sebagai Bahan Baku
a. Gambir Asalan Utuh; b. Gambir Asalan yang Telah Mengalami Pengecilan ukuran
Pemanasan dilakukan untuk melarutkan gambir asalan dan memudahkan pelarut agar dapat mengekstrak senyawa-senyawa yang terdapat dalam gambir asalan. Pemanasan dapat merusak jaringan pada bahan yang akan diekstraksi sehingga senyawa-senyawa akan dapat mudah diikat oleh pelarut. Pemanasan dilakukan hingga semua gambir asalan terlarut dengan lama pemanasan setelah mencapai suhu yang ditentukan kurang lebih 10 menit.
Larutan gambir yang telah dipanaskan disaring untuk memisahkan kotoran yang tidak larut dalam air panas. Kotoran tersebut dapat berupa pasir, tanah, logam tempat pemasakan, dan daun gambir yang terikut dalam proses pengolahan hingga menjadi gambir asalan. Hasil penyaringan berupa kotoran dalam gambir dapat dilihat pada Gambar 14. Larutan gambir kemudian didiamkan selama 12 jam untuk mengendapkan katekin yang ikut terekstrak oleh pelarut air. Proses pengendapan dapat dilihat pada Gambar 15.
29 Gambar 15. Proses Pengendapan dalam Ekstraksi Tanin
Katekin memiliki sifat dapat larut dalam air panas, alkohol, asetat glasial, aseton dan sukar larut dalam air dingin. Tanin memiliki sifat dapat larut dalam alkohol dan air dingin. Dengan proses pengendapan, katekin yang sukar larut dalam air dingin akan mengendap dan dapat dipisahkan dengan tanin yang masih terlarut dalam air. Pemisahan antara katekin yang mengendap dengan tanin yang masih terlarut dalam air dilakukan dengan proses penyaringan. Fraksi yang mengendap (katekin) dapat dilihat pada Gambar 16. Fraksi yang tidak mengendap (tanin) dapat dilihat pada Gambar 17.
a b
Gambar 16. Fraksi Katekin
30 Gambar 17. Larutan Tanin
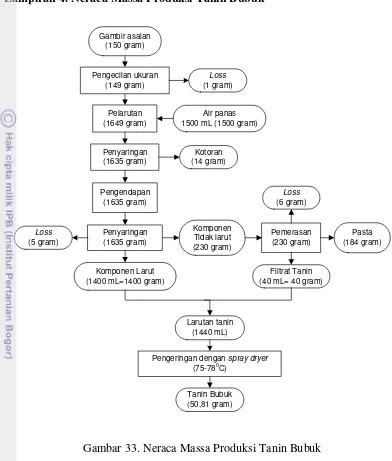
Senyawa hasil pengendapan yang berupa fraksi tidak larut air dingin kemungkinan masih mengandung komponen tanin. Oleh karena hal tersebut, endapan kemudian diperas dan disaring kembali untuk mendapatkan larutan tanin. Hasil penyaringan yang berupa cairan kemudian dikeringkan dengan menggunakan alat pengering semprot untuk memperoleh hasil serbuk yang seragam. Neraca massa pembuatan tanin bubuk dapat dilihat pada Lampiran 4. Proses pengeringan larutan tanin dilakukan dengan metode spray drying. Pada metode spray drying, bahan disemprotkan dan diatomisasi membentuk droplet ke dalam suatu media pengering yang panas kemudian air dalam bentuk droplet akan menguap meninggalkan bahan kering (Dubey et al., 2009). Fungsi atomisasi pada metode spray drying adalah untuk menghasilkan droplet yang berukuran kecil sehingga luas permukaan menjadi lebih besar dan mengakibatkan proses penguapan lebih cepat.
Penggunaan alat pengering semprot memiliki beberapa keunggulan dari beberapa teknik pengeringan lainnya seperti oven yang biasa digunakan untuk mengeringkan produk gambir pada skala laboratorium. Penggunaan oven memerlukan waktu cukup lama karena menggunakan suhu rendah dan hasil yang terbentuk masih memerlukan perlakuan lanjutan untuk menyeragamkan ukuran butiran produk.
31 lebih baik (lebih cerah) dibandingkan metode pengeringan lainya seperti dengan evaporator, vacuum drying, dan freeze drying (Gumbira-Sa’id, et al. 2009b). Contoh tanin hasil pengeringan menggunakan spray dryer dapat dilihat pada Gambar 18.
Gambar 18. Tanin Bubuk Hasil Pengeringan dengan Spray Dryer Proses pengeringan larutan tanin dengan spray dryer menggunakan suhu inlet 1300C - 1400C dan suhu outlet 750C - 780C. Suhu inlet dan outlet yang digunakan mengacu pada penelitian sebelumnya yang telah dilakukan oleh Gumbira-Sa’id, et al. (2009). Penggunaan suhu yang terlalu tinggi pada suhu outlet dapat menyebabkan warna tanin menjadi lebih gelap yang berpengaruh pada penampakan dan dikhawatirkan dapat merusak komponen penyusun tanin. Penggunaan suhu outlet yang terlalu rendah menyebabkan produk yang dihasilkan masih memiliki nilai kadar air yang tinggi.
Penelitian yang mendukung dan berkaitan dengan penggunaan suhu inlet 1300C-1400C adalah pada penelitian penggunaan pengering semprot dalam mengeringkan ekstrak kulit buah manggis dan anggur. Pada penelitian Sagara (2010), komponen fenolik yang terdapat pada kulit buah manggis baik bila dikeringkan pada suhu inlet 1600C dengan konsentrasi bahan pengisi maltrodekstrin. Penelitian dari Larrauri, et al. (1997) menyatakan bahwa komponen fenolik pada ekstrak kulit buah anggur akan mengalami kerusakan pada kondisi pengeringan 1400C. Dengan acuan tersebut, penggunaan suhu inlet spray dryer pada pengeringan larutan tanin berkisar antara 1300C-1400C.
32 pengeringan. Suhu outlet yang digunakan berpengaruh pada kekeringan produk yang dihasilkan. Pengaturan bahan yang masuk ke dalam pengering semprot mempengaruhi outlet pada proses pengeringan. Laju bahan masuk yang terlalu kecil akan menyebabkan kenaikan pada suhu outlet. Kenaikan suhu outlet dapat menyebabkan pengeringan dengan panas yang berlebihan sehingga berpengaruh pada warna produk yang dihasilkan.
Setelah produk mengalami pengeringan dengan spray dryer, bubuk tanin dikemas dengan kemasan plastik. Pengemasan dan penyimpanan bubuk tanin sangat perlu diperhatikan. Kemasan tanin harus dapat melindungi tanin dari udara luar dan kondisi lingkungan sekitar yang dapat merusak tanin bubuk. Tanin bubuk yang tidak disimpan dengan baik dapat mengalami perubahan warna menjadi lebih gelap. Sesuai dengan sifat tanin yang dinyatakan Browning (1966) bahwa warna tanin akan menjadi gelap apabila terkena cahaya langsung atau dibiarkan di udara terbuka. Contoh perubahan warna tanin dapat dilihat pada Gambar 19. Tanin bubuk yang sudah dikemas dapat dilihat pada Gambar 20.
Gambar 19. Tanin yang Telah Mengalami Perubahan Warna
33 C. ANALISIS PRODUK
1. Rendemen
Nilai rendemen tanin bubuk menunjukkan jumlah ekstrak tanin dari gambir asalan yang dapat diperoleh dari serangkaian proses hingga mengalami pengeringan manjadi bubuk. Rendemen tanin bubuk yang dihasilkan dari ekstraksi gambir asalan bervariasi dengan kisaran antara 16% hingga 42% dry basis (Lampiran 5a). Nilai rendemen tanin bubuk antar sampel memiliki rentang yang cukup jauh dan bervariasi. Nilai rendemen tanin bubuk yang diperoleh dari ekstraksi tanin masih cukup kecil akibat kehilangan yang terjadi pada proses ekstraksi. Kehilangan bahan selama proses ekstraksi dapat terjadi pada tahap penyaringan dan pengeringan dengan spray dryer.
Pada proses ekstraksi tanin dari gambir asalan, bahan bukan tanin yang larut dalam air seperti katekin, quersetin, pyrocatechol, mineral, vitamin, dan karbohidrat dapat ikut terekstrak. Menurut Linggawati, et al. (1992), ekstrak tanin terdiri dari campuran senyawa polifenol yang sangat kompleks dan biasanya tergabung dengan karbohidrat rendah. Oleh karena itu, nilai rendemen ekstrak belum dapat secara pasti menunjukkan nilai kandungan senyawa tanin dalam produk. Grafik hubungan rendemen tanin (dry basis) dan perbandingan jumlah air dengan gambir asalan dapat dilihat pada Gambar 21.
34 Berdasarkan Gambar 21, nilai rendemen tanin memiliki kecenderungan adanya peningkatan seiring dengan kenaikan jumlah pelarut yang digunakan. Secara umum, semakin tinggi perbandingan air dan gambir asalan yang digunakan, semakin tinggi jumlah rendemen ekstrak tanin. Pada perlakuan jumlah perbandingan air dengan gambir asalan, rendemen terbesar dimiliki oleh perbandingan 12:1 (v/b) untuk setiap taraf suhu air yang digunakan. Menurut Yusro (2004), semakin banyak jumlah pelarut yang digunakan, kesetimbangan penjenuhan yang terbentuk semakin besar sehingga jumlah senyawa yang terekstrak semakin banyak. Menurut Suryandari (1981), rendemen hail ekstraksi akan terus meningkat hingga larutan menjadi jenuh. Setelah mencapai titik jenuh, tidak akan terjadi peningkatan rendemen dengan penambahan pelarut.
Jika ditelaah berdasarkan perlakuan suhu, nilai rendemen tanin bubuk mengalami peningkatan dari suhu 400C ke 600C lalu mengalami penurunan pada suhu 800C. Secara umum, nilai rendemen ekstrak tanin akan mengalami kenaikan seiring dengan kenaikan suhu pelarut yang digunakan sesuai dengan sifat tanin bahwa tanin larut dalam air dan akan bertambah besar apabila dilarutkan dalam air panas (Browning, 1966). Namun, pada proses ekstraksi tanin, senyawa fenol lainnya dalam gambir seperti katekin, quercetin dan pyrocathecol dapat ikut terekstrak. Hal tersebut dapat mempengaruhi nilai rendemen karena perbedaan sifat kelarutan dari senyawa-senyawa fenol tersebut. Pada suhu sekitar 600C terdapat kemungkianan bahwa senyawa fenol lainnya dalam gambir telah mengalami kondisi jenuh untuk dapat diekstrak.
Menurut Earle (1983), peningkatan suhu secara umum dalam proses ekstraksi akan mempercepat proses difusi pelarut ke dalam sel jaringan, sehingga pertemuan permukaan pelarut dengan padatan jumlahnya meningkat. Oleh karena hal tersebut, rendemen yang dihasilkan bertambah banyak.
35 laju ekstraksi senyawa fenolik jauh lebih tinggi dibandingkan dengan laju degradasi fenolik. Hal tersebut dapat menunjukkan bahwa senyawa fenolik selain tanin yang terdapat dalam gambir asalan kemungkian telah mengalami kondisi optimum ekstraksi pada suhu 600C sehingga pada suhu 800C mengalami penurunan nilai rendemen. Nilai rendemen tanin bubuk tertinggi adalah 42,72% dimiliki produk S6P12 yaitu produk yang diekstraksi dengan suhu 600C dan perbandingan jumlah air dengan gambir asalan 12:1 (v/b).
Berdasarkan hasil perhitungan analisis ragam pada α = 0,0,5 (Lampiran 6), faktor perlakuan perbandingan jumlah air dan gambir asalan memberikan pengaruh yang nyata terhadap nilai rendemen produk tanin bubuk. Faktor perlakuan suhu memberikan pengaruh tidak nyata terhadap nilai rendemen. Namun, interaksi antara faktor perbandingan jumlah air dengan gambir asalan dan faktor suhu air memberikan pengaruh yang berbeda nyata terhadap hasil rendemen. Penggunaan jumlah pelarut yang semakin banyak dan suhu pelarut yang semakin tinggi menyebabkan senyawa yang terekstrak semakin banyak sehingga rendemen meningkat. Hasil uji lanjut Duncan (Lampiran 7) menunjukkan bahwa penggunaan suhu 600C dan jumlah pelarut 1800 ml tiap 150 gram gambir merupakan perlakuan terbaik dalam penelitian yang menghasilkan rendemen tanin bubuk tertinggi yaitu 42,72%.
2. Kadar Tanin
Kadar tanin merupakan banyaknya tanin yang terdapat dalam suatu bahan. Menurut Hathway (1962), tanin adalah senyawa organik yang terdiri dari campuran senyawaan polifenol kompleks, dibangun dari elemen C, H dan O serta sering membentuk molekul besar dengan bobot molekul lebih besar dari 2000.
36 Dengan membandingkan kadar tanin bahan awal, proses ekstraksi tanin dari gambir asalan pada penelitian ini dapat meningkatkan kadar tanin produk hingga mencapai 89% - 95% dry basis (Lampiran 5b). Grafik hubungan kadar tanin (dry basis) dengan jumlah air dan gambir asalan dapat dilihat pada Gambar 22.
Gambar 22. Grafik Hubungan Kadar Tanin dengan Jumlah Air dan Gambir Asalan
37 Setelah mencapai titik jenuh, tidak akan terjadi peningkatan rendemen dengan penambahan pelarut.
Jika ditelaah berdasarkan faktor suhu, hasil penelitian menunjukkan bahwa nilai kadar tanin produk cenderung naik dengan meningkatnya suhu air yang digunakan. Semakin tinggi suhu air yang digunakan, semakin tinggi nilai kadar tanin produk. Hal tersebut menjelaskan tentang sifat tanin bahwa tanin larut dalam air dan akan bertambah besar apabila dilarutkan dalam air panas. Penggunaan suhu yang lebih tinggi dalam mengekstraksi akan menyebabkan reaksi yang terjadi lebih kuat karena energi yang dihasilkan lebih tinggi sehingga zat yang pada awalnya tidak terlarut menjadi larut dalam air (Browning, 1966).
Berdasarkan hasil perhitungan analisis ragam dengan α = 0,05 (Lampiran 8), faktor perlakuan perbandingan jumlah air dengan gambir asalan memiliki pengaruh yang tidak berbeda nyata terhadap nilai kadar tanin. Begitu pula perlakuan faktor suhu yang digunakan tidak berpengaruh nyata terhadap nilai kadar tanin. Interaksi antara faktor perlakuan perbandingan jumlah air dengan gambir asalan dan faktor suhu juga tidak berpengaruh nyata terhadap nilai kadar tanin.
Namun secara ideal, peningkatan suhu air yang digunakan memberikan pengaruh peningkatan nilai kadar tanin pada produk yang diperoleh. Apabila dilihat berdasarkan Gambar 22, secara umum nilai kadar tanin meningkat dengan adanya kenaikan suhu air dan perbandingan jumlah air dengan gambir asalan yang digunakan. Nilai kadar tanin tertinggi mencapai 95,37% dan dimiliki oleh produk yang diekstrak menggunakan suhu air 800C dan perbandingan air dengan gambir asalan 12:1 (v/b).
3. Kadar Air
38 waktu yang cukup lama. Bahan yang memiliki nilai kadar air yang tinggi apabila disimpan dalam keadaan kelembaban tinggi akan menyebabkan penurunan kualitas produk. Untuk produk tanin bubuk, penyimpanan yang tidak tepat dapat menyebabkan warna bubuk tanin menjadi gelap.
Tanin bubuk yang dihasilkan pada penelitian melalui tahap pengeringan menggunakan spray dryer. Nilai kadar air dalam dry basis untuk tanin bubuk berkisar antara 4 % - 6,06 % (Lampiran 5c). Kadar air dengan rentang nilai tersebut masih termasuk dalam rentang bahan yang memiliki kestabilan optimum dalam proses penyimpanan jangka waktu yang lama. Menurut Winarno (1997), apabila kadar air bahan berkisar antara 3% hingga 7% maka kestabilan optimum bahan akan tercapai dan pertumbuhan mikroorganisme dapat dikurangi. Grafik hubungan kadar air tanin bubuk (dry basis) dengan jumlah pelarut dapat dilihat pada Gambar 23.
Gambar 23. Grafik Hubungan Kadar Air Tanin Bubuk (Dry Basis) dengan Perbandingan Jumlah Air dan Gambir Asalan
39 jumlah air dan gambir asalan. Pada perbandingan jumlah air dan gambir asalan 10:1 (v/b), nilai kadar air mengalami penurunan. Jika dilihat dari faktor suhu air yang digunakan, secara umum kadar air meningkat secara berturut-turut pada tanin bubuk yang diekstrak menggunakan suhu air 400C, 800C, dan 600C. Namun peningkatan tersebut tidak terjadi pada perlakuan perbandingan air dan gambir asalan 12:1 (v/b).
Hasil analisis ragam pada α = 0,05 (Lampiran 9) menunjukkan bahwa faktor perlakuan suhu air dan faktor perlakuan jumlah air dengan gambir asalan serta interaksi antara keduanya tidak berpengaruh nyata terhadap nilai kadar air. Hal tersebut menjelaskan bahwa nilai kadar air pada tanin bubuk tidak tergantung pada faktor perlakuan selama proses ekstraksi, tetapi tergantung pada proses pengeringan larutan tanin dengan menggunakan spray dryer.
Penggunaan suhu inlet dan outline spray dryer yang sesuai dan stabil berpengaruh pada nilai kadar air produk tanin bubuk yang dihasilkan. Apabila suhu yang yang digunakan terlalu rendah, pengeringan tidak berlangsung sempurna sehingga nilai kadar air pada tanin bubuk menjadi tinggi. Sebaliknya, penggunaan suhu yang terlalu tinggi dapat mempengaruhi warna tanin bubuk yang dihasilkan. Dalam proses pengeringan, ketidakstabilan suhu outlet yang digunakan dapat disebabkan oleh laju pemasukan bahan atau proses atomisasi yang mengalami gangguan. Apabila laju bahan rendah, suhu outlet akan mengalami peningkatan.
4. Kadar Abu
40 pengolahan. Grafik hubungan kadar abu (dry basis) dengan jumlah pelarut dan bahan dapat dilihat pada Gambar 24.
Gambar 24. Grafik Hubungan Kadar Abu Tanin Bubuk dengan Perbandingan Jumlah Air dan Gambir Asalan
Nilai kadar abu tanin bubuk (dry basis) berkisar antara 3,85% - 5,17% (Lampiran 5d). Mineral yang terdapat dalam tanin bubuk berasal dari mineral gambir yang ikut terlarut dalam air. Kadar abu gambir asalan adalah 12,21%. Penurunan kadar abu hingga mencapai 7,41%-8,61% (wet basis) memperlihatkan bahwa proses ekstraksi tanin bubuk yang telah dilakukan cukup baik karena mineral atau bahan pengotor yang terdapat dalam gambir asalan tidak banyak yang terekstrak. Nilai kadar abu yang semakin rendah menunjukkan tanin yang terekstrak lebih murni karena tidak banyak mengandung mineral yang merupakan bahan bukan tanin.
41 temperatur. Beberapa parameter yang mempengaruhi kelarutan mineral adalah tempertaur, pH, dan nilai redox potential (Eh).
Pada dasarnya, kadar abu merupakan pengujian untuk mengetahui jumlah mineral anorganik yang terdapat dalam produk tanin bubuk setelah mengalami proses pembakaran. Menurut Sudarmadji et. al. (1989), komponen mineral dalam suatu bahan sangat bervariasi dan beberapa contoh mineral antara lain fosfor (P), besi (Fe), Na, K, Mg, S, Co, dan Zn. Menurut Betts (1999), sejumlah kecil mineral dapat larut dalam air. Sebagian besar mineral membutuhkan waktu beberapa jam untuk dapat larut dalam air dan sedikit mineral yang dapat larut dengan cepat dalam air. Hasil penelitian menunjukkan bahwa nilai kadar abu terkecil yaitu 3,85% dimiliki oleh produk yang diekstrak dengan air suhu 600C dengan perbandingan jumlah air dan gambir asalan 12:1 (v/b).
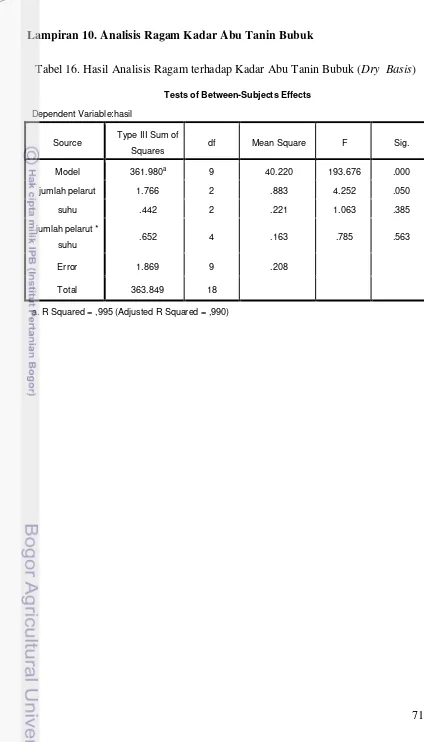
Berdasarkan hasil penghitungan analisis ragam pada α = 0,05 (Lampiran 10), faktor perlakuan suhu dan perlakuan jumlah air dengan gambir asalan serta interaksi antara keduanya tidak berpengaruh nyata terhadap nilai kadar abu. Hal tersebut menjelaskan bahwa perlakuan yang terjadi selama proses ekstraksi tidak mempengaruhi nilai kadar abu produk karena hasil yang diperoleh tidak menunjukkan hasil yang signifikan. Nilai kadar abu dapat dipengaruhi oleh kandungan kadar abu dari gambir asalan yang digunakan dan proses ekstraksi yang dilakukan. Pemilihan bahan baku yang memiliki nilai kadar abu rendah perlu diperhatikan untuk dapat menekan nilai kadar abu pada produk tanin bubuk yang dihasilkan.
5. Warna
42 (1990), sistem notasi Hunter mempunyai tiga parameter untuk mendeskripsikan warna yaitu L, a, dan b.
Parameter L mempunyai nilai yang berkisar dari 0 (hitam) sampai 100 (putih). Nilai L menyatakan cahaya pantul yang menghasilkan warna akromatik putih, abu-abu, dan hitam. Notasi a menyatakan warna kromatik campuran merah-hijau dengan kisaran nilai +a berkisar mulai 0 sampai +100 untuk warna merah dan nilai –a mulai dari 0 sampai -80 untuk warna hijau. Notasi b mnyatakan warna kromatik campuran biru kuning, dengan nilai +b mulai dari 0 sampai +70 untuk warna biru dan nilai –b mulai dari 0 sampai -70 untuk warna kuning (Soekarto, 1990).
Tanin gambir pada umumnya berwarna kuning kecoklatan. Nilai a dan b hasil pembacaan colorimeter untuk tanin bubuk adalah positif yang masing-masing menunjukkan warna merah dan kuning. Rentang nilai a pengujian warna pada tanin bubuk adalah 21,09-24,56 sedangkan rentang nilai b adalah 11,19-12,12. Hasil pengukuran warna untuk nilai L bervariasi antara 48,91 dan 54,30. Hasil pengukuran warna dapat dilihat pada Tabel 3.
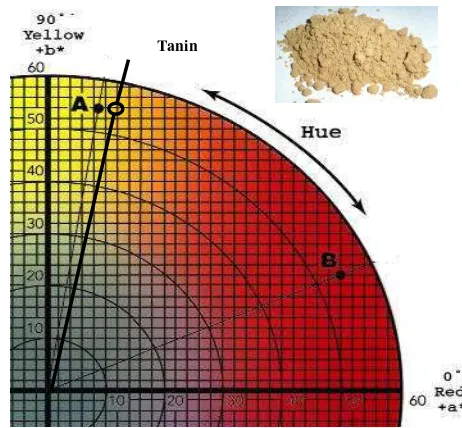
43 invers tangen perbandingan nilai b dan a. Nilai 0H kemudian dibandingkan dengan diagram warna 0H sehingga dapat diketahui warna bahan secara visual. Rata-rata nilai 0H produk tanin bubuk adalah 79,82 yang menunjukkan spektrum warna kuning. Nilai 0H dari produk tanin bubuk dapat dilihat pada diagram warna Gambar 25. Warna yang diperlihatkan pada diagram warna hue menunjukkan warna tanin produk yang dihasilkan.
Gambar 25. Diagram Warna Hue Tanin Bubuk
Selain 0H, data L, a, dan b hasil pengukuran dengan colorimeter dapat dikonversi menjadi nilai derajat putih atau whiteness produk tanin bubuk yang distandarisasi dengan warna putih BaSO4. Nilai whiteness produk bubuk berkisar antara 64,99% dan 74,26% (Lampiran 5e). Nilai whiteness yang semakin tinggi menunjukkan bahwa tanin bubuk semakin mendekati warna putih yang berarti semakin cerah. Grafik hubungan antara nilai whiteness dan perbandingan jumlah air dengan gambir asalan dapat dilihat pada Gambar 26.
44 Gambar 26. Grafik Hubungan Whiteness Tanin Bubuk dengan Jumlah Air
dan Gambir Asalan
Berdasarkan Gambar 26, nilai whiteness produk gambir tidak menunjukkan suatu kecenderungan tertentu terhadap faktor-fakor yang digunakan dalam penelitian. Nilai whiteness produk tanin bubuk tertinggi adalah 74,26% yang dimiliki produk S6P10 yaitu produk yang diekstrak dengan suhu 600C dan perbandingan air dengan gambir asalan 10:1 (v/b). Nilai whiteness yang tinggi menunjukkan kualitas tanin yang lebih baik. Menurut Browning (1966), tanin berwarna putih kekuning-kuningan sampai coklat terang, tergantung dari sumber tanin. Warna tanin akan berubah menjadi lebih gelap apabila terkena cahaya langsung atau dibiarkan di udara terbuka. Semakin gelap warna bubuk tanin, kualitas tanin bubuk semakin rendah. Penampakan contoh produk tanin bubuk dapat dilihat pada Gambar 27.
45 Hasil analisis ragam pada α = 0,05 (Lampiran 11) menunjukkan bahwa faktor perbandingan jumlah air dan gambir asalan serta interaksi antara faktor suhu dan jumlah perbandingan air dengan bahan menunjukkan pengaruh yang berbeda nyata terhadap nilai whiteness. Namun, faktor suhu air yang digunakan dalam ekstraksi tidak memberikan pengaruh yang berbeda nyata terhadap nilai whiteness. Hasil uji lanjut Duncan (Lampiran 12) menunjukkan bahwa perlakuan terbaik yang menghasilkan nilai whiteness tertinggi sebesar 74,26% adalah perlakuan dengan suhu air panas 600C dan jumlah air dengan gambir asalan 10:1 (v/b).
Meskipun hasil analisis ragam menunjukkan bahwa terdapat pengaruh jumlah pelarut yang digunakan dan pengaruh interaksi antara suhu dan jumlah pelarut yang ditambahkan, terdapat kemungkinan bahwa proses pengeringan juga berpengaruh pada warna tanin bubuk yang dihasilkan. Proses pengeringan menggunakan spray dryer dengan suhu yang tidak stabil antar perlakuan berpengaruh pada warna masing-masing tanin bubuk. Penggunaan suhu yang terlalu tinggi menyebabkan warna tanin menjadi lebih gelap dan nilai whiteness menjadi rendah.
6. Kadar Bahan Tidak Larut Air
46 Gambar 28. Grafik Hubungan Kadar Bahan Tidak Larut Air Tanin Bubuk
dengan Jumlah Pelarut dan Bahan
Berdasarkan Gambar 28, secara umum nilai kadar bahan tidak larut air cenderung mengalami penurunan dengan semakin tinggi suhu air yang digunakan dalam ekstraksi. Hal tersebut menunjukkan bahwa pada suhu yang tinggi, jumlah tanin yang terlarut semakin banyak sehingga ketika dilarutkan dalam air kembali, jumlah bahan yang tidak larut dalam air bernilai kecil. Nilai kadar bahan tidak larut air terendah adalah 2,99% dimiliki oleh produk yang diekstrak dengan suhu 800C dan perbandingan jumlah air dengan gambir asalan 10:1 (v/b). Semakin rendah nilai kadar bahan tidak larut air menunjukkan semakin tinggi kualitas produk tanin bubuk.
47 Hasil penghitungan analisis ragam pada α = 0,05 (Lampiran 13) menunjukkan bahwa faktor perlakuan suhu dan faktor perlakuan perbandingan jumlah air dengan gambir asalan serta interaksi antara keduanya memiliki pengaruh yang tidak berbeda nyata terhadap nilai kadar bahan tidak larut air. Hal tersebut menjelaskan bahwa variasi perlakuan yang terjadi selama proses ekstraksi tidak mempengaruhi nilai kadar bahan tidak larut air karena tidak menunjukkan hasil yang signifikan.
Besarnya nilai kadar bahan tidak larut air dipengaruhi oleh proses ekstraksi. Kadar bahan tidak larut air dapat berupa kotoran yang ikut terbawa pada proses ekstraksi. Kotoran atau bahan tidak larut air yang terbawa saat ekstraksi dapat berasal dari gambir asalan. Selama proses pengolahan gambir asalan, terdapat kemungkinan para petani menambahkan zat pengisi seperti pasir sehingga kandungan bahan tidak larut air menjadi tinggi. Proses ekstraksi yang dapat meningkatkan nilai kadar bahan tidak larut air adalan proses penyaringan. Proses penyaringan bertujuan untuk memisahkan bahan yang tidak larut (kotoran dan pasta) dengan larutan tanin yang akan dikeringkan dengan menggunakan spray dryer.
D. PERLAKUAN TERBAIK
48 Tabel 4. Standar Tanin Industrial Grade GB 5308-85
Grade I II III
Tannic acid content (%) ≥ 81,0 ≥ 78,0 ≥ 75,0
Loss in drying (%) ≤ 9,0 ≤ 9,0 ≤ 9,0
Water insoluble (%) ≤ 0,6 ≤ 0,8 ≤ 1,0
Total colour (lovibond) ≤ 2,0 ≤ 3,0 ≤ 4,0 Sumber: CIFOR Occasional Paper No.6 NWFPs in China (1995)
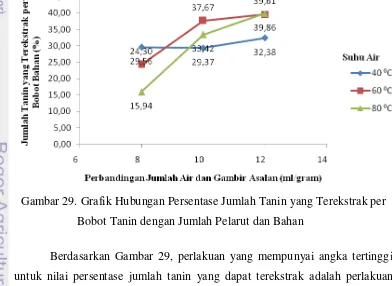
Pemilihan perlakuan terbaik dapat ditinjau dari segi efisiensi proses dan kualitas produk tanin bubuk yang dihasilkan. Untuk segi efisiensi proses berkaitan dengan banyaknya tanin murni yang dapat diekstrak dengan perlakuan tertentu. Data untuk efisiensi proses melibatkan data rendemen dry basis yang dikonversi bersama nilai kadar tanin dry basis menjadi jumlah tanin yang dapat terkestrak tiap bobot bahan yang digunakan. Hasil konversi tersebut dapat dilihat pada Gambar 29 yang menunjukkan persentase bobot tanin yang dapat diekstrak per bobot bahan yang digunakan.
Gambar 29. Grafik Hubungan Persentase Jumlah Tanin yang Terekstrak per Bobot Tanin dengan Jumlah Pelarut dan Bahan
49 sebesar 39,86%. Nilai persentase tersebut menunjukkan bahwa dengan perlakuan percobaan menggunakan suhu 800C dan perbandingan jumlah air dan gambir asalan 12:1 (v/b) dapat menghasilkan ekstrak murni tanin (dry basis) sebanyak 39,86 gram per 100 gram bahan gambir asalan.
Data nilai efisiensi proses yang menunjukkan banyaknya tanin murni yang dapat diekstrak kemudian dibandingkan dengan hasil pengujian produk tanin bubuk. Berdasarkan hasil pengujian kadar tanin dan hasil analisis ragam, semua perlakuan dalam penelitian tidak memberikan pengaruh signifikan untuk nilai kadar tanin. Hal tersebut menunjukkan bahwa semua perlakuan dapat terpilih sebagai perlakuan terbaik. Nilai kadar tanin (dry basis) tertinggi pada penelitian adalah 95,67% dimiliki oleh produk S8P12 yaitu produk yang diekstraksi dengan suhu 800C dan perbandingan jumlah air dan gambir asalan 12:1 (v/b).
Jika dikaitkan dengan standar GB 5308-85, selain kadar tanin, parameter lainnya yang menjadi acuan untuk menilai kualitas produk tanin adalah kadar air, pengujian warna, dan kadar bahan tidak larut dalam air. Berdasarkan hasil pengujian kadar air, perlakuan yang mempunyai nilai kadar air terendah sebesar 4,04% adalah perlakuan yang menggunakan suhu 400C dan perbandingan jumlah air dan gambir asalan 10:1 (v/b). Namun, hasil analisis ragam menyebutkan bahwa pengggunaan variasi perlakuan pada penelitian tidak berpengaruh nyata pada nilai kadar air produk. Hal tersebut menunjukkan bahwa semua perlakuan pada pembuatan produk tanin bubuk memiliki kesempatan yang sama untuk menjadi perlakuan terbaik. Kadar air produk lebih dipengaruhi oleh proses pengeringan yang memerlukan kestabilan dan ketepatan suhu pengeringan.
50 Berdasarkan hasil pengujian kadar bahan tidak larut air, nilai terendah dihasilkan oleh perlakuan suhu 600C dan perbandingan jumlah air dan gambir asalan 10:1 (v/b) yaitu sebesar 2,99%. Namun, hasil analisis ragam menunjukkan bahwa nilai kadar bahan tidak larut dalam air tidak dipengaruhi secara nyata oleh variasi perlakuan pada percobaan. Sama halnya dengan kadar air, hasil analisis ragam kadar bahan tidak larut air menunjukkan bahwa semua perlakuan pada pembuatan produk tanin bubuk memiliki kesempatan yang sama untuk menjadi perlakuan terbaik.
Dengan demikian, berdasarkan data nilai efisiensi proses dalam mengekstraksi tanin dan nilai kadar tanin diperoleh perlakuan terbaik adalah suhu 800C dengan perbandingan jumlah air dan gambir asalan 12:1 (v/b). Berdasarkan hasil pengujian nilai kadar air dan kadar bahan tidak larut air, semua perlakuan dapat dijadikan perlakuan terbaik. Oleh karena hal tersebut, dapat dipilih perlakuan terbaik dalam penelitian ini adalah perlakuan dengan suhu 800C dan perbandingan jumlah air dan gambir asalan 12:1 (v/b). Namun, berdasarkan nilai whiteness, perlakuan terbaik adalah suhu 600C dengan perbandingan jumlah air dan gambir asalan 10:1 (v/b). Nilai whiteness untuk produk S8P12 adalah 71,73% yang memiliki selisih tidak berbeda jauh dengan nilai whiteness pada produk S6P10 (74,26%) yaitu sebesar 2,43%.
Perlakuan ekstraksi pada penelitian dengan suhu air 800C dan perbandingan jumlah air dengan gambir asalan 12:1 (v/b) menghasilkan produk yang memiliki nilai kadar tanin 95,67% (dry basis), rendemen 41,79 % (dry basis), kadar air 4,85% (dry basis), kadar abu 4,04 % (dry basis), whiteness 71,73%, dan kadar bahan tidak larut air 3,72% (dry basis).
51 V. KESIMPULAN DAN SARAN
A. KESIMPULAN
Tanin pada gambir dapat diekstrak untuk diperoleh produk tanin yang memiliki tingkat kemurnian yang tinggi. Proses ekstraksi tanin dari gambir asalan dapat dilakukan dengan menggunakan air sebagai pelarut. Proses pengambilan tanin dalam gambir asalan melibatkan proses pemisahan antara senyawa katekin dan tanin yang terkandung dalam gambir dan keduanya termasuk jenis senyawa polifenol. Proses pemisahan antara kedua senyawa tersebut didasarkan pada perbedaan sifat kelarutan keduanya pada pelarut yang digunakan. Dengan proses pengendapan, katekin yang sukar larut dalam air dingin akan mengendap dan dapat dipisahkan dengan tanin yang masih terlarut dalam air.
Pada proses ekstraksi tanin dari gambir asalan, secara umum penggunaan suhu pelarut yang semakin tinggi meningkatkan nilai kadar tanin produk. Penggunaan perbandingan jumlah pelarut dengan gambir asalan yang semakin banyak dapat meningkatkan rendemen tanin bubuk dan kadar tanin pada produk. Proses pengeringan dengan spray dryer menghasilkan tanin bubuk dengan ukuran butiran yang seragam. Kestabilan suhu pada proses pengeringan memberikan pengaruh terhadap proses pembuatan tanin bubuk seperti pada nilai kadar air dan whiteness.
52 B. Saran
Beberapa saran yang dapat diberikan setelah melakukan penelitian ini adalah sebagai berikut:
1. Perlakuan ekstraksi lainnya seperti penggunaan pelarut yang berbeda, penggunaan suhu ekstraksi dan perbandingan jumlah pelarut dengan gambir asalan yang lebih tinggi dapat dilakukan untuk mengetahui pengaruh yang terjadi pada produk tanin yang dihasilkan
1 KAJIAN PRODUKSI TANIN BUBUK DARI GAMBIR ASALAN
DENGAN PENGERING SEMPROT (SPRAY DRYER)
Oleh
OKTAVIA LESTARI F34061939
2010
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
53 DAFTAR PUSTAKA
Akiyama, H., K. Fujii, O. Yamasaki, T. Oono, dan T. Iwatsuki. 2001. Antibacterial Action of Several Tannins Agains Staphylococcus aureus. Journal of Antimicrobial Chemotherapy. Vol. 48 : 487-91.
AOAC. 2005. Official Method of The Association of Official Chemist. AOAC. Inc. Virginia.
Bernardini, E.1983. Oilseeds, Oils, and Fats, Volume I, Raw Material and Extraction Techniques. Publishing House. Rome.
Betts, J. 1999. Mineral Properties and Identification Procedures. http://www.minerals.net/resource/property/taste.htm [diakses 25 Juli 2010]
BPS Kabupaten 50 Kota. 2008. Kabupaten Lima Puluh Kota dalam Angka 2007. BPS Kabupaten Lima Puluh Kota. Sumatra Barat.
Brown, G.G.. 1950. Unit Operation. Webster School and Office Supplier. Manila. Browning, B.L. 1966. Methods of Wood Chemistry. Interscience Publishers. New
York.
Canovas, V.B. dan H.V. Mercado. 1996. Dehydration of Foods. Chapman and Hall. New York.
Carter, F. L., A. M. Carlo, dan J. B. Stanley. 1978. Termiticidal Components of Wood Extracts : 7- Methyljuglone from Diospyros virginia. Journal Agriculture Food Chemistry. 26(4): 869-873.
Copriady, Jimmi, Miharty, dan Herdini. 2002. Gallokatekin : Senyawa Flavonoid Lainnya dari Kulit Batang Rengas (Gluta Renghas Linn.). Jurnal Natur Indonesia, 4 (1): 4
Covey, S. 2010. The Solubility of Minerals.
http://www.galleries.com/minerals/property/parting.htm [diakses 25 Juli 2010]
Dubey, R., T.C. Tsami, dan B.Rao. 2009. Microencapsulation Technology and Preparation. Journal Devence Science 59 (1): 82-95.
54 Earle, R. L. 1983. Unit Operation in Food Processing Second Edition. Pergamon
Press. Inggris.
Fessenden, R. J. dan J. S. Fessenden. 1982. Kimia Organik. Erlangga. Jakarta. Fengel D.,G. Wegener, dan H. Sostrohamidjojo. 1993. Kayu, Kimia,
Ultrastruktur, Reaksi- Reaksi. Gadjah Mada University Press. Yogyakarta.
Filkova, I. dan A.S. Mujumdar. 1995. Industrial Spray Drying Systems. Mujumdar, A.S. (ed) Handbook of Industrial Drying. Marcel Decker, Inc. New York.
Gemse, T. 2002. Liquid-Liquid Extraction and Solid Liquid Extraction. Graz University of Technology. Styria.
Gumbira-Sa’id, E., K. Syamsu, E. Mardliyati, A. Herryandie, N.A. Evalia, D.L.Rahayu, A.A.A. Ratih P., Aang A., dan A. hadiwijoyo. 2009a. Agroindustri Bisnis dan Gambir Indonesia. IPB Press. Bogor.
Gumbira-Sa’id, E. K. Syamsu, E. Mardliyati, A.H. Brontoadie, dan N.A. Evalia. 2009b. Perbaikan Rekayasa Proses, Pengembangan Produk dan Peningkatan Mutu Gambir Ekspor Indonesia: Pendalaman Studi Kasus di Kabupaten Lima Puluh Kota, Propinsi Sumatera Barat. Laporan Penelitian Hibah Unggulan Strategis Nasional. Institut Pertanian Bogor. Bogor.
Gross, G.G. 1992. Enzimes in The Biosynthesis of Hydrolyzable Tannins. Hemingway, R.W. and P.E. Laks (ed.). Plant Polyphenols: Synthesis, Properties,and Significance. New York: Plenum Press.
Hagerman, A.E. 2002. Tannin Chemistry. Department of Chemistry and Biochemistry, Miamy University. USA.
Harborne, J.B. 1987. Metode Fitokimia, Penuntun Cara Modern Menganalisis Tumbuhan. Penerbit ITB. Bandung.
Hathway, D. E. 1962. The Condensed Tannins. In Wood Extractives (Hillis W. E). Academic Press. New York.
Houghton, P.J. dan A.Raman. 1998. Laboratory Handbook for Fractionation of Natural Extracts. Chapman and Hall. London.
Larrauri, J. A., P. Ruperez and F. Saura-Calixto. 1997. Effect of drying temperature on the stability of polyphenols and antioxidant activity of red grape pomace peels. Journal Agric. Food Chem. 44: 1390-1393.