GITA ALVERNITA. The Histopathology of MiceLiver Treated by Kepel (Stelechocarpus burahol) Suspension Intragastrically for 14 Days. Under direction of EVA HARLINA and SITI SA’DIAH.
The aim of this study was to examine the effect of kepel (Stelechocarpus burahol) to the mice hepatocytes. Thirty male mice of 4 week aged were divided into three groups; control group was treated by aquadest, dose 1x group was treated by 2.6 mg/g BW/day kepel powder (0,5 ml kepel suspension/day) and dose 5x group was treated by 13 mg/g BW/day kepel powder (1.0 ml kepel suspension/day). The treatment was intragastrically for 14 days. The mice were euthanized and then followed by the liver collection for histopathology processed. The histopathlogical examination of liver showed hydropic degeneration, apoptosis and extramedullary hematopoietic observed on mice hepatocytes.The ANOVA analysis showed that kepel caused increase significantly (p<0,05) of hydropic degeneration and decrease significantly (p<0,05) of apoptosis of mice hepatocytes.
(Stelecho
DEPAR
ocarpus bu
RTEMEN
FAKU
INS
urahol) SE
1
GITA
KLINIK
ULTAS KE
STITUT P
ECARA IN
14 HARI
ALVERN
REPROD
EDOKTE
ERTANIA
BOGOR
2011
NTRAGAS
NITA
DUKSI DA
RAN HEW
AN BOGO
STRIK SE
AN PATO
WAN
OR
ELAMA
Dengan ini saya menyatakan bahwa skripsi Gambaran Histopatologi Hati Mencit Setelah Pemberian Suspensi Daging Buah Kepel (Stelechocarpus burahol) Secara Intragastrik Selama 14 Hari adalah karya saya dengan arahan dosen pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Bogor, November 2011
Gita Alvernita
© Hak Cipta milik IPB, tahun 2011
Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya illmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB.
GITA ALVERNITA. The Histopathology of MiceLiver Treated by Kepel (Stelechocarpus burahol) Suspension Intragastrically for 14 Days. Under direction of EVA HARLINA and SITI SA’DIAH.
The aim of this study was to examine the effect of kepel (Stelechocarpus burahol) to the mice hepatocytes. Thirty male mice of 4 week aged were divided into three groups; control group was treated by aquadest, dose 1x group was treated by 2.6 mg/g BW/day kepel powder (0,5 ml kepel suspension/day) and dose 5x group was treated by 13 mg/g BW/day kepel powder (1.0 ml kepel suspension/day). The treatment was intragastrically for 14 days. The mice were euthanized and then followed by the liver collection for histopathology processed. The histopathlogical examination of liver showed hydropic degeneration, apoptosis and extramedullary hematopoietic observed on mice hepatocytes.The ANOVA analysis showed that kepel caused increase significantly (p<0,05) of hydropic degeneration and decrease significantly (p<0,05) of apoptosis of mice hepatocytes.
(Stelechocarpus burahol) SECARA INTRAGASTRIK SELAMA
14 HARI
GITA ALVERNITA
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Kedokteran Hewan pada
Fakultas Kedokteran Hewan Institut Pertanian Bogor
DEPARTEMEN KLINIK REPRODUKSI DAN PATOLOGI
FAKULTAS KEDOKTERAN HEWAN
INSTITUT PERTANIAN BOGOR
BOGOR
Nama : Gita Alvernita
NIM : B04070175
Disetujui,
Dr. drh. Eva Harlina, M.Si, APVet. Siti Sa’diah, S.Si,Apt,M.Si
Pembimbing I Pembimbing II
Diketahui,
Dr. Nastiti Kusumorini
Wakil Dekan Fakultas Kedokteran Hewan Institut Pertanian Bogor
melimpahakan rahmat dan karunianya sehingga penulis dapat menyelesaikan skripsi yang berjudul Gambaran Histopatologi Mencit Setelah Pemberian Suspensi Daging Buah Kepel (Stelechocarpus burahol) Secara Intragastrik Selama 14 Hari. Skripsi ini disusun sebagai salah satu syarat untuk memperoleh gelar sarjana pada Fakultas Kedokteran Hewan, Institut Pertanian Bogor.
Terima kasih penulis sampaikan kepada Dr. drh. Eva Harlina, M.Si, APVet. dan Siti Sa’diah, S.Si, Apt, M.Si selaku pembimbing skripsi yang begitu sabar memberikan pengarahan dan bimbingan bagi penulis. Ucapan terimakasih juga penulis sampaikan kepada drh. Huda Darusman, M.Si atas saran dan masukannya selama penelitian, drh. Isdoni, M.Biomed selaku dosen pembimbing akademik, seluruh staf dan pegawai Bagian Toksikologi dan Farmakologi (Pak Edi dan Mbak Anti), seluruh staf dan pegawai Bagian Patologi (Pak Kasnadi, Pak Endang dan Pak Sholeh) serta staf dari Pusat Studi Biofarmaka LPPM IPB (Mbak Dina dan Pak Taufik) atas bantuannya selama penelitian.
Ucapan terima kasih dan penghargaan yang tak terhingga penulis tujukan untuk Ayah dan Ibu tercinta, Andre R. Rustam dan Farida Daulay, Reynaldo Belmundo Andre (Kakak), Dian Ayu Wardhani (Kakak ipar), serta segenap keluarga yang telah berdoa dengan tulus dan memberikan dukungan selama ini. Ucapan terima kasih dan penghargaan yang sangat dalam penulis tujukan kepada Arie Mardjan Tampubolon, Adilla Adha dan Andrini Aditya Wardhani atas kebersamaan dan kesabarannya dalam berjuang sebagai rekan penelitian (Thank you Bang!). Terima kasih penulis ucapkan kepada orang terdekat (Mbung, Astri Priyanti Parameswari, Puti Lenggogeni, Meta Levi, Patricia Noreva, Trismawati Wahid, Azrul Zulmy, dan Dardjat Darul Falah) atas dukungan, saran dan kritikannya, serta rekan-rekan Gianuzzi 44 dan Himpro SATLI. Semoga karya ini bermanfaat bagi pengembangan ilmu pengetahuan.
Bogor, November 2011
Andre R. Rustam dan Farida Daulay. Penulis merupakan anak kedua dari dua bersaudara.
Penulis memulai pendidikan formal pada tahun 1995 di SD Islam Al-Azhar 6 Jakapermai, Bekasi dan lulus pada tahun 2001. Pada tahun yang sama penulis melanjutkan pendidikan ke SMP Islam Al-Azhar 8 Kemang Pratama, Bekasi dan lulus pada tahun 2004. Penulis kemudian masuk ke SMA Islam Al-Azhar 4 Kemang Pratama, Bekasi dan lulus pada tahun 2007. Tahun 2007 penulis diterima di Institut Pertanian Bogor melalui jalur Seleksi Penerimaan Mahasiswa Baru (SPMB) di Fakultas Kedokteran Hewan.
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
PENDAHULUAN Latar Belakang ... 1
Tujuan... ... 2
Manfaat... ... 2
Hipotesis. ... 3
TINJAUAN PUSTAKA Tanaman Herbal... ... 4
Kepel (Stelechocarpus burahol) ... 6
Hati... ... 9
Mencit.... ... 11
METODE PENELITIAN Waktu dan Tempat ... 12
Bahan dan Alat ... 12
Hewan Coba ... 12
Pembuatan Sediaan Kepel ... 13
Desain Penelitian ... 13
Pembuatan Preparat Histopatologi Hati ... 13
Pengamatan Sediaan Histopatologi Mencit ... 14
Analisis Statistik ... 14
Diagram Alir Penelitian ... 14
HASIL DAN PEMBAHASAN Pengaruh Pemberian Suspensi Daging Buah Kepel (Stelechocarpus burahol) Terhadap Gambaran Histopatologi Hati ... 16
SIMPULAN DAN SARAN Simpulan ... 24
Saran ... 24
DAFTAR PUSTAKA ... 25
1. Fitokimia tanaman kepel ... 9 2. Persentase perubahan hepatosit mencit pada pemberian suspensi
Halaman 1. Bentuk pohon, daun dan buah kepel ... 8 2. Diagram alir penelitian ... 14 3. Grafik persentase perubahan hepatosit mencit pada pemberian
suspensi daging buah Kepel (Stelechocarpus burahol) selama 14 hari . 16 4. Hepatosit yang mengalami degenerasi hidropis pada kelompok dosis 5x 17 5. Hepatosit yang mengalami apoptosis pada kelompok kontrol ... 20 6. Extramedullary hematopoiesis (EMH) pada hati kelompok dosis 5x .... 23
Halaman
1. Penghitungan dosis pemberian kepel ... 31
2. Penghitungan volume pemberian kepel ... 32
3. Pembuatan sediaan histopatologi dan pewarnaan HE ... 33
4. Analisis perubahan degenerasi hidropis pada sel hati ... 35
5. Analisis perubahan apoptosis pada sel hati ... 36
PENDAHULUAN
Latar Belakang
Penggunaan obat-obatan herbal menjadi sebuah alternatif yang saat ini
digandrungi oleh masyarakat. Mayoritas masyarakat lebih memilih pengobatan
herbal karena bahan alami dianggap bersifat lebih aman, selain itu juga relatif
lebih murah dibandingkan obat modern. Faktor pendorong berpindahnya
masyarakat memakai obat herbal adalah usia harapan hidup yang lebih panjang
setelah mengonsumsi obat herbal saat prevalensi penyakit kronik meningkat dan
adanya kegagalan penggunaan obat modern untuk penyakit tertentu seperti
kanker. Herbal kembali dilirik kajian ilmiahnya oleh peneliti setelah melihat
kemampuan alami hewan di alam liar mengonsumsi tanaman untuk self-treatment dalam mengurangi rasa sakit pada saat-saat tertentu.
Indonesia memiliki lebih dari 30.000 jenis spesies tumbuhan yang 960
spesies diantaranya telah tercatat sebagai tumbuhan berkhasiat, dan 283 jenis
diantaranya merupakan tumbuhan yang penting bagi industri obat tradisional
(Kusuma dan Zaky 2005). Diantara tanaman berkhasiat tersebut adalah daun
jambu biji (Psidium guava) yang mengandung psiditanin yang berguna sebagai obat diare, atau Echinacea purpurea yang mengandung echinasida yang berfungsi sebagai immunomodulator. Beberapa tanaman yang telah menjadi obat herbal terstandar diantaranya Kiranti®, yang mengandung kunyit (Curcuma domestic) berguna untuk meredakan nyeri pada saat haid, dan Stimuno®, contoh
immunomodulator dari herbal alami yang membantu meningkatkan daya tahan tubuh. Stimuno® terdaftar sebagai sediaan fitofarmaka yang berasal dari ekstrak
tanaman meniran (Phyllantus niruri) yang terstandarisasi, karena telah melalui berbagai uji preklinik dan klinik (Anonim 1 2009). Berdasarkan temuan-temuan
di atas memicu para peneliti untuk menelaah lebih jauh potensi tumbuhan khas
Indonesia dalam mewujudkan kesehatan masyarakat, hewan dan lingkungan.
Salah satu tanaman asli Indonesia yang biasa digunakan sebagai jamu adalah
tanaman khas asal Yogyakarta yang sering disebut dengan kepel.
bagi masyarakat Keraton, Yogyakarta. Putri keraton dahulu menggemari buah ini
sebagai penghilang bau badan, memberi efek wangi pada produk ekskresi manusia
seperti keringat, urin dan feses. Selain itu daun kepel mengandung banyak zat
sitotoksik bagi sel kanker (Wiart 2007), dan mengandung banyak senyawa
flavonoid yang bersifat sebagai antioksidan (Sunarni et al. 2007). Bunga dari tumbuhan kepel diketahui memiliki efek antiimplantasi sehingga dapat digunakan
sebagai kontrasepsi (Warningsih 1995). Bagian kulit batangnya juga diketahui
sebagai antiagregasi platelet (Sunardi et al. 2007). Banyaknya potensi obat yang dimiliki tanaman kepel berbanding terbalik dengan langkanya tanaman ini.
Kelangkaan disebabkan oleh kurangnya nilai ekonomis dari tanaman ini, dan
kepel termasuk tanaman yang berbuah setahun sekali. Karena faktor inilah
mengapa masyarakat urung membudidayakan dan memanfaatkan kepel. Adanya
publikasi ilmiah mengenai potensinya diharapkan menjadi ujung tombak
memasyarakatkan kepel sebagai tanaman yang memiliki nilai ekonomi tinggi.
Penelitian ini bertujuan untuk mempelajari gambaran histopatologi organ
hati terhadap pemberian suspensi daging kepel, karena hati merupakan organ
interna pertama yang terkena efek toksik dari suatu substansi yang masuk ke
dalam tubuh. Hati juga memiliki peranan yang sangat penting karena merupakan
pusat metabolisme zat makanan sebelum diedarkan ke seluruh tubuh (Banks
1986). Berdasarkan data empiris dari masyarakat Keraton, kepel dikonsumsi
sebanyak 2 buah dalam 1 hari. Bersumber dari data empiris tersebut maka
dilakukan penelitian untuk mempelajari adakah perubahan pada gambaran
histopatologi hati mencit setelah pemberian kepel selama 14 hari. Dari hasil
penelitian ini diharapkan semakin banyak masyarakat yang mengetahui potensi
kepel sehingga tertarik membudidayakan dan memanfaatkannya.
Tujuan
Penelitian ini bertujuan untuk mempelajari pengaruh pemberian suspensi
Manfaat
Manfaat penelitian adalah untuk mengetahui potensi kepel sehingga
masyarakat tertarik untuk membudidayakan dan memanfaatkannya, dan juga
meningkatkan pamor dan nilai ekonomis kepel sehingga dapat merubah gaya
hidup untuk semakin mencintai buah nasional.
Hipothesis
Hipotesis penelitian ini adalah sebagai berikut:
H0: Suspensi daging buah kepel tidak berpengaruh terhadap gambaran
histopatologi organ hati mencit.
H1: Suspensi daging buah kepel berpengaruh terhadap gambaran histopatologi
TINJAUAN PUSTAKA
Tanaman Herbal
Tanaman herbal memiliki keistimewaan yang tidak dimiliki oleh
farmakologi konvensional. Farmakologi konvensional saat ini bersifat single compound yang spesifik khasiatnya terhadap suatu penyakit. Hal ini berbeda dengan tanaman herbal yang memiliki multi compound yang mengandung berbagai macam substansi dengan khasiat yang berbeda sehingga dapat
menyeimbangkan efek samping. Farmakologi konvensional umumnya tetap
dianggap sebagai pilihan pengobatan karena khasiatnya bersifat spesifik sehingga
respon penyembuhannya lebih cepat. Tanaman herbal dianggap sebagai pilihan
yang tepat dalam pengobatan penyakit kronis karena memiliki bahan alami yang
dapat memperbaiki metabolisme sehingga dianggap lebih aman dalam
penggunaan jangka panjang.
Pengobatan herbal mewakili berbagai macam disiplin ilmu seperti botani,
sejarah, etnomedisinal dan farmakologi (Wynn dan Fougere 2007). Pengobatan
herbal pada hewan diawali dengan adanya perilaku hewan yang mampu
melakukan self-treatment saat terserang penyakit. Perilaku alami hewan ini menjadikan salah satu alasan para ahli herbal meneliti tanaman obat dan
interaksinya dalam tubuh. Sebagai contoh, kera besar di Tanzania memakan
daun-daun berambut yang berasal dari 34 spesies tanaman obat berbeda, tanpa
mengunyah namun langsung menelannya. Beberapa daun yang dipilih diketahui
mengandung fitokimia aktif dan sebagian tidak, namun semua daun yang dipilih
memiliki tekstur permukaan kasar dengan mikrostruktur mirip dengan kait yang
biasa disebut dengan trichomes. Dedaunan tersebut biasanya dikonsumsi hewan pada saat musim hujan dimana infestasi cacing meningkat sehingga menyebabkan
diare, malaise dan sakit perut (Huffman et al. 1997). Hasil penelitian menunjukkan bahwa tekstur kasar pada permukaan daun berperan sebagai
pembersih mekanis cacing yang menginfestasi saluran pencernaan. Dedaunan
kasar juga meningkatkan motilitas usus dan merangsang diare, sehingga
Interaksi dedaunan di dalam tubuh menghasilkan efek yang cepat dalam
menanggulangi gejala penyakit yang diderita kera tersebut seperti malaise pada
saluran pencernaan (Huffman et al. 1997). Perilaku alami mengonsumsi dedaunan berambut juga telah membantu simpanse di Taman Nasional Kibale,
Uganda untuk menyingkirkan infestasi cacing pita (Bertiella studeri) dalam saluran pencernaan (Wrangham 1994).
Perilaku alami juga ditemukan pada simpanse dengan gejala diare, malaise
dan infeksi nematode dengan mengonsumsi daun pahit Vernonia amygdalina. Dalam waktu 24 jam, simpanse yang mengonsumsi daun ini sembuh. Waktu
persembuhannya serupa dengan masyarakat lokal yang mengonsumsi daun ini
untuk mengatasi gejala penyakit saluran pencernaan. Vernonia amygdalina berasal dari Gunung Mahale, Tanzania, yang mengandung tujuh glukosida steroid
serta empat sesquiterpene lakton yang mampu membunuh parasit yang
menyebabkan schistosomiasis, malaria dan leishmaniasis. Sesquiterpene lakton
bukanlah antihelmintik namun antiamoeba, antitumor dan antimikroba. Lapis luar
dari daun yang dikunyah oleh simpanse merupakan lapisan yang mengandung
vernoniosida B1 yang tinggi dan dapat bersifat sangat toksik terhadap simpanse.
Simpanse tidak hanya dapat mencari pakan yang dapat menangani gejala penyakit
yang menyerangnya, namun juga mampu menemukan bagian tumbuhan yang
memiliki khasiat tanpa bersifat merugikan dirinya (Ohigashi et al. 1994).
Tanaman herbal membutuhkan waktu tertentu untuk pembentukan
senyawa aktif yang terkandung di dalamnya. Oleh karena itu, usia kematangan
dari bagian tanaman herbal sangat mempengaruhi jumlah dan jenis senyawa yang
dikandungnya. Selain itu faktor ekstrinsik seperti suhu, kelembaban udara, iklim
dan demografi tanah juga memiliki peranan vital dalam pembentukan senyawa
aktif dalam tanaman herbal. Senyawa aktif ini bekerja sama dalam menghasilkan
khasiat sehingga apabila salah satu senyawa aktif berhasil diisolasi belum tentu
dapat menghasilkan khasiat yang sama.
Badan POM mengelompokkan obat tradisional menjadi tiga, yaitu sediaan
jamu, sediaan herbal terstandar dan sediaan fitofarmaka. Sediaan jamu
merupakan sediaan obat tradisional yang pemakaiannya secara empiris
sediaan obat tradisional yang bahan bakunya harus distandarisasi dan sudah diuji
farmakologi secara eksperimental yaitu uji pra klinik, efikasi dan toksisitas.
Sediaan fitofarmaka adalah sediaan obat tradisional yang bahan bakunya harus
distandarisasi dan harus melalui uji klinik. Pengembangan obat tradisional seperti
halnya pengembangan obat modern yaitu melalui uji praklinik dan uji klinik. Uji
praklinik meliputi uji farmakodinamik, uji toksikologi dan uji farmasetik,
sedangkan uji klinik meliputi uji klinik fase I (dilakukan terhadap 50-150
sukarelawan sehat), uji klinik fase II (dilakukan terhadap 100-200 pasien), uji
klinik fase III (dilakukan terhadap 50-5000 pasien) dan post marketing surveillance sebagai uji klinik fase IV. Dalam melakukan pengembangan obat tersebut, bagian tanaman obat yang digunakan dapat berasal dari batang, akar,
daun, buah, kulit, biji atau bahkan semua bagiannya. Tanaman obat yang diuji
dapat berupa simplisia (bahan alami yang dikeringkan), ekstrak kental, ekstrak
kering dan ekstrak cair.
Kepel (Stelechocarpus burahol)
Stelechocarpus burahol merupakan tanaman yang termasuk ke dalam Kingdom: Plantae, Subkingdom: Tracheobinta, Divisio: Magnoliophyta, Klas:
Magnoliopsida, Ordo: Magnoliales, Famili: Annonaceae, Genus: Stelechocarpus,
Spesies: Stelechocarpus burahol.
Di Indonesia terdapat tiga spesies dari tanaman ini yaitu Stelechocarpus burahol, Stelechocarpus cauliflorus dan Stelechocarpus schefferii. Ketiga spesies ini dapat ditemukan di lembaga observasi herbarium seperti di taman nasional
sebagai tanaman koleksi dan tanaman untuk diuji kembangkan propagasinya.
Propagasi kepel dilakukan dengan menggunakan biji yang diambil dari buah yang
matang. Telah dicoba propagasi dengan cara lain namun gagal (Sunarto 1987,
Sunarto1992). Hal inilah yang menyebabkan dilakukannya program penanaman
kembali kepel sebagai tanaman langka.
Kepel menjadi salah satu tanaman langka yang masuk ke dalam Daftar
Tanaman yang Terancam Punah (Sastrapradja dalam Mogea 2001). Namun kepel
dapat ditemukan di berbagai taman nasional seperti Kebun Raya Bogor, Taman
Jember, Taman Buah Mekarsari dan hutan lindung Leuweng Sancang, Cikalong
(Anonim 2 2003). Spesies Stelechocarpus burahol ditanam sebagai pohon ornamen di perkebunan masyarakat Yogyakarta, namun terbatas di daerah selain
Yogyakarta. Kepel dapat ditemui di daerah Jawa Barat, Jawa Tengah dan Jawa
Timur. Masyarakat di daerah Garut Selatan, Tasikmalaya selatan dan Banyumas
memanfaatkan kepel sebagai buah segar. Selebihnya kepel dapat ditemukan di
perkebunan masyarakat seperti di daerah Karang Anyar, Kebumen dan Solo.
Kepel merupakan tanaman berkayu dengan batang berbentuk silinder.
Daunnya tipis, berwarna hijau kehitaman, mengkilat dan berbentuk lonjong.
Buahnya berbentuk bulat, berwarna kecokelatan dengan diameter 5-6.3 cm
(Umiyah 2005). Daging buahnya memiliki kandungan air yang tinggi sebesar
87-90% sehingga kadar rendemen atau bahan kering yang dimiliki hanya sekitar
10-13% (Darusman 2010). Kepel memiliki biji yang cukup besar dibandingkan
ukuran buah keseluruhannya yaitu 27%, sehingga daging buah yang dapat
dikonsumsi sangat sedikit, hanya 49% (Verhejj dan Coronell 1997). Pohon kepel
mencapai masa berbuah pada usia 6-8 tahun dan hidup di daerah kaki pegunungan
dengan ketinggian 150-300 m diatas permukaan laut. Tanaman ini memiliki tajuk
berbentuk kubah meruncing dan buah yang menyerupai buah buni (berrylike ripe carpels) yang bertangkai pada batang utama pohon. Kepel berbunga pada bulan September hingga Oktober (Sunarto 1992), Maret hingga Oktober (Backer &
Bakhuizen dalam Umiyah 2005) bahkan dapat berbunga pada bulan Juni di
Taman Nasional Meru Betiri, Jember (Umiyah 2005). Gambar pohon, buah dan
daun kepel disajikan pada Gambar 1.
Masyarakat keraton percaya dengan mengonsumsi buah kepel, bau
keringat, bau nafas dan bau air seni menjadi wangi (Fachrurozi 1980; Heyne
1987; Sunarto 1987; Verheij dan Coronell 1997). Zaman dahulu, para Sultan dari
Yogyakarta dan Solo menggunakan buah kepel sebagai deodoran tradisional. Hal
ini dilakukan sebagai bentuk pengabdian terhadap pasangan. Oleh karena itu,
dahulu buah kepel hanya diperbolehkan dikonsumsi oleh putri dan bangsawan
Keraton dan dilarang untuk dikonsumsi oleh masyarakat biasa, sehingga kepel
tanaman kepel dalam aspek hortikultura, seleksi dan analisis sifat aromatiknya
masih belum banyak dilakukan.
Ekstrak daun kepel memiliki sifat sitotoksik yang tinggi terhadap zat
kanker carcinoma colorectal (Shiddiqi et al. 2008). Daun kepel juga dapat menurunkan asam urat (Purwatiningsih et al. 2009). Daging buah kepel memiliki kandungan bahan aktif antioksidan yang tinggi (Tisnadjaja et al. 2006). Kajian khasiat kepel yang ditarik secara filogenis dari tanaman famili Annonaceae lainnya seperti sirsak (Annona muricata), tanaman asli Trinidad yang mirip dengan apel yaitu cashima (Rollinia exsucca) dan Rollinia pittieri menunjukkan potensi kandungan zat sitotoksik (Osorio et al. 2007).
Gambar 1 Bentuk pohon, daun dan buah kepel. Sumber: Wong (2010).
Studi lain yang menunjukkan khasiat dari tanaman ini adalah
menghambat enzim DNA isomerase dan tyrosine kinase (Piersen 2003). Kandungan fitokimia kepel menurut Darusman (2010) disajikan pada Tabel 1.
Tabel 1 Kandungan Fitokimia Tanaman Kepel (Darusman 2010).
No Sampel Flavo noid Ta nin Steroid Triterp enoid Sap onin Alkaloid Drage ndorf Me yer Wagner
1. Daun + + + - - - - -
2. Daging buah + + - - - - 3. Kulit Buah + - - - + - - -
4. Biji + + - + - - - -
Hati
Hati merupakan organ terbesar dalam tubuh dengan unit histologi dasar
yaitu lobulus. Lobulus hati dikelilingi oleh ruang portal yang berisi
cabang-cabang dari buluh empedu, arteri hepatika dan vena porta, yang disebut juga
sebagai segitiga Kiernan. Hepatosit merupakan sel parenkim hati yang mengisi lobulus hati dan dipisahkan oleh sinusoid. Di dalam lumen sinusoid terdapat
sel-sel Kupffer yang berperan sebagai makrofag residen yang melapisi sinusoid dan
memfagositosis bakteri dan benda asing dalam darah sinus hepatikus (Guyton dan
Hall 2007). Sel-sel Kupffer mengandung sitokines seperti faktor tumor nekrosis,
interleukin dan interferon. Lapisan endotel sinusoid mempunyai pori-pori yang
sangat besar. Di bawah lapisan ini terdapat ruang yang sangat sempit yang
terletak di antara sel endotel dan hepatosit yaitu ruang Disse atau ruang
perisinusoidal.
Hepatosit memiliki retikulum endoplasma yang kasar dan halus, kompleks
Golgi, mitokondria, lisosom, peroksisom, glikogen dan lemak. Sel sinusoid
memiliki tiga tipe yaitu sel endothelial yang membatasi sinusoid secara tidak
teratur, sel-sel Kupffer yang berada di antara sel endotel atau pada lapisan
sinusoid dan yang terakhir adalah sel-sel Stellate yang sering disebut dengan sel
Ito yang berfungsi menyimpan vitamin A dan kolagen ekstraseluler (Kmiec 2001).
Hati merupakan organ interna yang memiliki banyak fungsi dalam sistem
pencernaan diantaranya sekresi empedu, metabolisme lemak, protein dan
fungsi metabolisme hormon, obat dan racun. Oleh karena itu hati memiliki
peranan yang signifikan dalam melepaskan hasil metabolisme zat makanan
sebelum diedarkan ke seluruh tubuh. Hati juga berfungsi dalam mengubah
produk metabolisme protein menjadi urea untuk diekskresikan oleh ginjal. Selain
itu hati memiliki peran dalam mekanisme penggumpalan darah sebagai
pertahanan diri. Semua fungsi hati ini didukung dengan kemampuan hati dalam
beregenerasi sehingga hati dapat melakukan banyak fungsinya (Maher 1997).
Distribusi peredaran darah dalam organ hati dimulai dari cabang-cabang
portal arteri hepatika dan vena porta menuju vena sentralis. Melalui vena sentralis
darah dialirkan ke vena hepatika. Unit fungsional hati adalah asinar dengan
pusatnya pada saluran portal yang berbeda dengan unit histologinya. Hepatosit
berdasarkan sistem asinar dibagi menjadi tiga zona. Zona satu di sekitar saluran
portal yang merupakan zona paling teroksigenasi, mengandung konsentrasi nutrisi
dan hormon tertinggi. Zona tiga berada di tepi area asinar mengandung sedikit
oksigen, dan zona dua sebagai zona intermediet.
Tiap sel hati memiliki dua lapisan sinusoid yang dibatasi oleh mikrovili.
Kanalikuli empedu yang dibentuk oleh sel-sel hati juga dibatasi oleh mikrovili.
Segitiga Kiernan atau area porta berada di antara tiga atau lebih lobulus dan
masing-masing berisi satu atau lebih cabang arteri hepatika, vena porta hepatika
dan pembuluh darah limfatik beserta buluh empedu (Aughey dan Frey 2001).
Aliran empedu bertolak belakang dengan arah aliran darah.
Sel-sel hati merupakan sel-sel yang mudah melakukan regenerasi sehingga
hati masih dapat berfungsi walaupun sel-sel hatinya telah mengalami kerusakan
hingga 70% (Guyton dan Hall 2007). Regenerasi sel hati berlangsung sangat
cepat dan membutuhkan waktu hanya 5 sampai 7 hari pada tikus. Selama
regenerasi, hepatosit diperkirakan mengalami replikasi sebanyak satu atau dua
kali, dan setelah mencapai ukuran dan volume hati sebelumnya, hepatosit kembali
kepada keadaan semula. Regenerasi hati dipengaruhi oleh Hepatocyte Growth Factor (HGF) yang diproduksi oleh sel mesenkimal di dalam hati dan jaringan lain, namun bukan hepatosit. Selain itu regenerasi hati dapat terjadi karena
Mencit
Hewan percobaan adalah hewan yang sengaja dipelihara dan diternakkan
untuk dipakai sebagai hewan model guna mempelajari dan mengembangkan
berbagai macam ilmu dalam skala penelitian atau pengamatan laboratorik (Malole
dan Pramono 1989). Mencit termasuk kedalam salah satu jenis hewan percobaan
yang sering digunakan karena cepat berkembang biak, mudah dipelihara dalam
jumlah banyak, variasi genetiknya cukup besar serta sifat anatomis dan
fisiologisnya tercirikan dengan baik. Mencit jantan dewasa memiliki berat badan
berkisar antara 20-40 g, sedangkan mencit betina dewasa memiliki berat badan
berkisar antara 25-40 g. Berdasarkan Spiridonova et al. (2003), mencit termasuk kedalam Kingdom: Animalia, Filum: Chordata, Sub Filum: Vertebrata, Kelas:
Mamalia, Ordo: Rodentia, Sub Ordo: Myomorpha, Familia: Muridae, Genus: Mus
BAHAN DAN METODE
Waktu dan Tempat
Penelitian ini dilaksanakan pada bulan April 2010 hingga Juli 2011, yang
bertempat di Pusat Studi Biofarmaka LPPM IPB, Bagian Farmakologi dan
Toksikologi, Departemen Anatomi, Fisiologi, dan Farmakologi dan Bagian
Patologi, Departemen Klinik, Reproduksi, dan Patologi FKH IPB.
Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah buah kepel
(Stelechocarpus burahol), pelet pakan mencit, air minum, dan bahan-bahan pembuat preparat histopatologi hati yaitu larutan buffer neutral formalin 10%,
alkohol 70%, 80%, 90% dan 95%, alkohol absolut, xylol, parafin cair, pewarna
Mayer’s Hematoxylin, lithium karbonat, akuades, dan pewarna Eosin.
Alat-alat yang digunakan dalam penelitian ini adalah labu ukur, blender,
sonde lambung, spoit, tissue cassette, blok parafin, kaca objek, kaca penutup, dan alat-alat nekropsi yaitu gunting, scalpel, pinset, kapas, timbangan, mikrotom,
refrigerator serta inkubator.
Hewan Coba
Hewan coba yang digunakan dalam penelitian ini adalah mencit jantan
(Mus musculus) berumur 4 minggu dengan berat 20 g. Hewan coba ditempatkan di dalam boks plastik yang dimodifikasi sebagai kandang. Pakan yang diberikan
berupa pelet ikan sebanyak 0.6 g/ekor/hari, dan air minum diberikan secara ad-libitum. Sekam digunakan sebagai alas kandang yang diganti setiap dua hari sekali. Sebelum perlakuan dimulai, hewan diadaptasikan dan dilakukan
pretreatment selama 5 hari. Pretreatment berupa pemberian antibiotik Clavamox® (asam klavulanat dan amoksisilin) dengan dosis 0.001 mg/g BB
(Hrapkiewicz dan Medina 2007) selama 3 hari, dan anti cacing Pyrantel Pamoat
dengan dosis 0.015 mg/g BB. Perlakuan mulai dilaksanakan pada hari keenam
Metode
Penelitian ini dilaksanakan dalam tiga tahap yaitu tahap pembuatan serbuk
buah kepel, tahap pencekokan mencit dan tahap pembuatan dan pengamatan
preparat histopatologi organ hati.
Pembuatan Sediaan Kepel
Buah kepel dicuci, kemudian dipisahkan daging buah dari kulit dan
bijinya. Daging buah dipotong kecil-kecil, kemudian dikeringkan di dalam oven
selama 3-4 hari dengan suhu 40oC. Setelah kering, potongan buah kepel
digrinding agar menjadi serbuk dengan ukuran 100 mesh. Selanjutnya serbuk halus dilarutkan dalam akuades sehingga terbentuk suspensi dan siap digunakan.
Desain Penelitian
Sebanyak 30 ekor mencit dibagi menjadi tiga kelompok, yaitu kelompok
kontrol, kelompok dosis 1x dan kelompok dosis 5x. Kelompok kontrol hanya
dicekok akuades, kelompok dosis 1x dan kelompok dosis 5x masing-masing
dicekok sediaan kepel dengan dosis 2.6 mg/g BB dan 13 mg/g BB. Penentuan
dosis pada mencit berdasarkan hasil konversi dosis empiris pada manusia, dengan
faktor konversi sebesar 0.0026 (Laurence dan Bacharach 1964). Perhitungan
dosis dan volume cekok suspensi daging buah kepel disajikan pada Lampiran 1.
Volume pencekokan pada kelompok kontrol sebesar 0.5 ml/hari, dosis 1x sebesar
0.5 ml/hari, dan dosis 5x sebesar 1 ml/ hari. Pada kelompok dosis 5x pencekokan
dibagi dua, yang dilakukan pada siang dan malam hari. Untuk kelompok lainnya
pencekokan dilakukan pada siang hari selama 14 hari. Pada akhir penelitian,
mencit dieuthanasi dan diambil hatinya untuk dibuat sediaan histopatologi.
Pembuatan Preparat Histopatologi Hati
Hati difiksasi dalam larutan buffer neutral formalin 10% selama 3 hari.
HE. Metode pembuatan dan pewarnaan sediaan histopatologi hati selengkapnya
disajikan pada Lampiran 2.
Pengamatan Sediaan Histopatologi Hati Mencit
Pengamatan dilakukan dengan menggunakan mikroskop cahaya dengan
perbesaran 10x, 20x dan 40x. Pada setiap preparat hati dilakukan pemotretan
pada 20 lapang pandang menggunakan lensa okuler Webcam® dan lensa objektif
40x. Evaluasi organ hati dilakukan pada hasil foto dengan menghitung jumlah
hepatosit yang mengalami degenerasi hidropis dan apoptosis dengan
menggunakan software ImageJ (Ferreira dan Rasband 2011).
Analisis Statistik
Persentase hasil penghitungan degenerasi hidropis dan apoptosis hepatosit
dari tiap 20 lapang pandang dianalisis menggunakan analisis sidik ragam
(ANOVA). Jika perlakuan berbeda nyata maka dilakukan uji lanjutan Post-Hoc yaitu uji Duncan (α = 0.05).
HASIL DAN PEMBAHASAN
Pengaruh Pemberian Suspensi Daging Buah Kepel (Stelechocarpus burahol) terhadap Gambaran Histopatologi Hati
Pengamatan histopatologi hati dilakukan hanya pada tiga ekor mencit pada
setiap kelompok perlakuan. Hal ini disebabkan tujuh ekor mencit dari kelompok
dosis 5x mati dalam perjalanan penelitian. Tujuan penelitian ini ingin mengetahui
pengaruh pemberian suspensi daging buah kepel pada dosis normal (dosis 1x)
dalam jangka panjang terhadap fungsi hati, sedangkan pemberian dosis 5x
bertujuan untuk mengetahui adakah pengaruh peningkatan dosis terhadap
perubahan hepatosit.
Hasil pengamatan seluruh sediaan histopatologi hati mencit pada
umumnya ditemukan perubahan pada hepatosit berupa degenerasi hidropis dan
apoptosis. Selain itu ditemukan pula fokus-fokus sel radang yang terdiri atas
sel-sel myeloblast dan eritroblast di sinusoid, di daerah segitiga Kiernan maupun
ditepi-tepi vena sentralis. Kumpulan sel-sel radang tersebut merupakan
extramedullary hematopoiesis (Marchiori et al. 2007). Hasil analisis statistik persentase hepatosit mencit yang mengalami degenerasi hidropis dan apoptosis
disajikan pada Tabel 2 dan Gambar 3.
Tabel 2 Persentase perubahan hepatosit mencit pada pemberian suspensi daging buah kepel (Stelechocarpus burahol) selama 14 hari.
Persentase (%) Hepatosit
Kelompok Hepatosit Normal Degenerasi Hidropis Apoptosis
Kontrol 38.79 ± 15.00a 36.05 ± 12.50a 25.16 ± 13.57a
Dosis 1x 36.89 ± 12.67a 41.45 ± 13.07b 21.66 ± 7.757b
Dosis 5x 30.17 ± 11.73b 57.70 ± 12.57c 12.13 ± 6.47c
0 20 40 60 80 100
Kontrol Dosis 1x Dosis 5x
Apoptosis Degenerasi Hidropis Hepatosit Normal
Kelompok
Gambar 3 Persentase perubahan hepatosit mencit pada pemberian suspensi daging buah kepel (Stelechocarpus burahol) selama 14 hari.
Hasil analisis statistik persentase hepatosit yang mengalami degenerasi
hidropis pada kelompok dosis 1x lebih tinggi dan berbeda nyata (p<0,05)
dibandingkan dengan kelompok kontrol. Namun jika ditelaah, kenaikannya tidak
terlalu besar dibandingkan tingginya kejadian degenerasi hidropis pada kelompok
dosis 5x. Persentase degenerasi hidropis pada kelompok dosis 5x lebih tinggi dan
berbeda nyata (p<0,05) dibandingkan kelompok dosis 1x dan kelompok kontrol.
Peningkatan persentase degenerasi hidropis sejalan dengan meningkatnya dosis
pemberian kepel. Dengan demikian degenerasi hidropis pada hepatosit
disebabkan oleh pemberian suspensi daging buah kepel.
Degenerasi hidropis merupakan kerusakan sel yang dimulai dengan
terjadinya hipoksia yang akan menyebabkan kerusakan membran sel dan
penurunan fosforilasi oksidatif, sehingga mengakibatkan terjadinya penurunan
ATP. Turunnya ATP menyebabkan penurunan kerja pompa Na. Adanya
kerusakan membran sel, ion K+ keluar dari sel sedangkan air, ion Na+ dan ion
Ca2+ masuk ke dalam sel secara berlebihan sehingga terjadi pembengkakan sel.
Penurunan ATP juga mengakibatkan peningkatan glikolisis sehingga pH sel akan
mengalami penurunan. Penurunan pH mengakibatkan benang khromatin pada inti
menyebabkan hilangnya benang khromatin dan protein yang terkandung sehingga
apabila berlanjut akan berujung pada nekrosis sel (Hanna 2011).
Degenerasi hidropis merupakan repson awal hepatosit terhadap
bahan-bahan yang bersifat toksik yang masuk ke hati melalui aliran darah. Dengan
demikian degenerasi hidropis biasanya dimulai pada hepatosit-hepatosit yang
berada pada tepi lobuler yang kemudian akan menyebar ke sentra lobuler
(Talukder 2001). Selain itu, degenerasi hidropis juga dapat terjadi pada hewan
yang mengalami hipoksia. Pemberian oksigen yang cukup serta penghentian
paparan bahan toksik dapat memulihkan sel yang mengalami degenerasi hidropis.
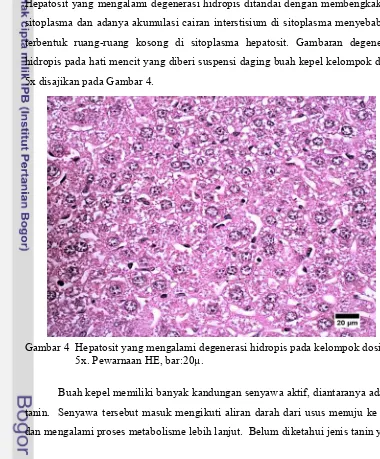
Hepatosit yang mengalami degenerasi hidropis ditandai dengan membengkaknya
sitoplasma dan adanya akumulasi cairan interstisium di sitoplasma menyebabkan
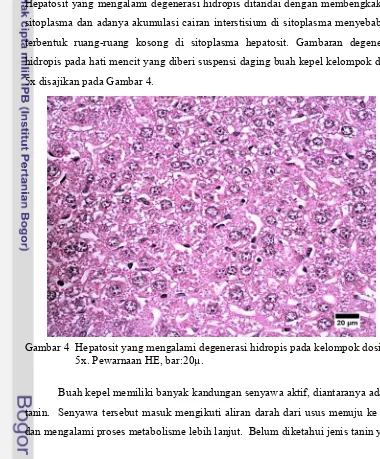
terbentuk ruang-ruang kosong di sitoplasma hepatosit. Gambaran degenerasi
hidropis pada hati mencit yang diberi suspensi daging buah kepel kelompok dosis
[image:30.612.108.488.259.718.2]5x disajikan pada Gambar 4.
Gambar 4 Hepatosit yang mengalami degenerasi hidropis pada kelompok dosis 5x. Pewarnaan HE, bar:20µ.
Buah kepel memiliki banyak kandungan senyawa aktif, diantaranya adalah
tanin. Senyawa tersebut masuk mengikuti aliran darah dari usus menuju ke hati
dikandung kepel, namun tanin merupakan senyawa yang bersifat toksik sehingga
hati merespon bahan tersebut dengan terbentuknya lesio degenerasi hidropis.
Jika ditarik secara filogenis buah kepel memiliki kesamaan famili dengan
sirsak (Annona muricata) yaitu Annonaceae. Tanaman dengan famili ini memiliki senyawa aktif yang khas yaitu acetogennin atau Annonaceous acetogennin (ACGs). ACGs memiliki bioaktivitas yang luas, diantaranya adalah antimalaria,
insektisida, antibakteria dan fungisida (Gonzalez-Coloma et al. 2002). ACGs bekerja dengan cara menghambat pembentukan ATP pada kompleks I
mitokondria (Wiart 2007). Oleh sebab itu, ACGs diduga memiliki peranan dalam
menyebabkan terjadinya degenerasi hidropis hepatosit. Penurunan produksi ATP
mengakibatkan sel hipoksia sehingga terjadi kerusakan membran sel. Hal ini
yang menyebabkan cairan interstisium masuk dan mengisi ruang-ruang
sitoplasma. Namun perlu dilakukan uji lebih lanjut untuk mengetahui kadar
kandungan ACGs di dalam buah kepel.
Hasil analisis statistik persentase hepatosit yang mengalami apoptosis
berbanding terbalik dengan yang mengalami degenerasi hidropis. Persentase
apoptosis pada kelompok dosis 1x lebih rendah dan berbeda nyata (p<0,05)
dibandingkan kelompok kontrol. Demikian pula persentase apoptosis kelompok
dosis 5x lebih rendah dan berbeda nyata (p<0,05) dibandingkan kelompok dosis
1x dan kelompok kontrol.
Apoptosis merupakan suatu bentuk kematian sel terprogram yang bersifat
aktif yang ditandai dengan adanya kondensasi kromatin dan fragmentasi
kromosom (D’Amico dan McKenna 1994). Apoptosis berbeda dengan nekrosis
dimana sel berperan aktif dalam proses terminasi diri, sedangkan pada nekrosis sel
berperan pasif. Menurut Underwood (1996), proses nekrosa melibatkan banyak
sel yang diiringi oleh terjadinya peradangan dan fagositasi oleh makrofag. Sel-sel
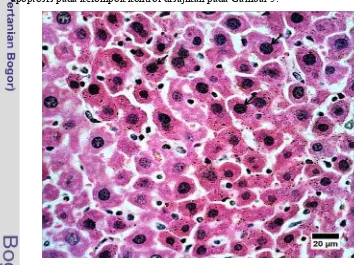
yang mengalami apoptosis akan menyerap lebih banyak pewarna eosin, sehingga
sitoplasma sel hati yang mengalami apoptosis berwarna lebih merah dengan inti
yang berwarna lebih ungu.
Apoptosis biasanya dicirikan oleh sel yang mengalami terminasi diri yang
tidak diikuti oleh peradangan. Menurut Dash (2011), apoptosis dapat terjadi
virus, ekspresi gen proapoptosis melalui aktivasi enzim caspase, tekanan pada sel seperti deplesi faktor pertumbuhan, tekanan pada sitoplasma, dan radikal bebas.
Apoptosis secara normal muncul selama proses perkembangan dan
penuaan sebagai mekanisme homeostasis untuk menjaga populasi sel dalam
jaringan (Kresno 2001). Sekitar 10 miliar sel hati dibuat setiap harinya untuk
menyeimbangkan sel-sel hati yang mengalami apoptosis (Renehan et al. 2001). Kejadian ini disebut juga dengan istilah regenerasi sel. Menurut Kuntz dan Kuntz
(2008), regenerasi fisiologis hati mengikuti fisiologi penuaan sel sehingga sel
apoptosis merupakan kematian sel yang terprogram. Regenerasi hepatosit akan
mengisi ruang jaringan hati yang hilang. Regenerasi sempurna menghasilkan
bentuk sel dan perbaikan fungsi spesifik sel, sedangkan regenerasi tidak sempurna
akan menyebabkan area nekrosis diisi oleh jaringan pengganti. Apoptosis juga
muncul sebagai respon terhadap keadaan stres oksidatif akibat adanya radikal
bebas (Norbury dan Hickson 2001).
Daging buah kepel mengandung flavonoid tertinggi dibandingkan bagian
buah lainnya yaitu sebesar 29,12 ppm sedangkan standar flavonoid pada vitamin
C hanya sebesar 5.35 ppm. Flavonoid diproduksi oleh tanaman sebagai respon
alami saat tanaman mengalami luka (Tisnadjaja et al. 2006). Flavonoid merupakan senyawa pigmen paling umum di dunia tanaman, kadang bersifat
fluorescent setelah dilakukan radiasi UV dan merupakan derivat dari asam
shikimik melalui jalur propanoid. Komponen terkait yang dihasilkan melalui
reaksi kompleks jaringan adalah isoflavon, auron, flavananon dan flavononol yang
dihasilkan dari kalkon. Leukoantosianidin, flavanon dan flavanol dihasilkan dari
flavanonol, sedangkan antosianidin dihasilkan dari leukoantosianidin (Kintzios
dan Barberaki 2004).
Flavonoid merupakan senyawa antioksidan yang berfungsi sebagai
penangkap radikal bebas hasil metabolisme aerob. Proses metabolisme aerob
menghasilkan oksigen reaktif atau Reactive Oxygen Species (ROS) (Fleury et al. 2002). Oksigen reaktif ini disebut dengan istilah radikal bebas yang dihasilkan di
mitokondria. ROS atau sering juga disebut dengan pro-oxidant bersifat tidak stabil dan reaktif terhadap jaringan. Stres oksidatif terbentuk apabila terjadi
dengan anti-oxidant dalam jaringan. Stres oksidatif juga dianggap berperan dalam proses penuaan (Yan et al. 1997).
ROS berbahaya apabila mengoksidasi senyawa tertentu seperti asam
lemak tak jenuh, yang prosesnya disebut dengan lipid peroxidation (Kuntz dan Kuntz 2008). Peroksidasi lipiddapat menyebabkan kerusakan membran sel yang
memicu terjadinya apoptosis. Selama apoptosis, permeabilitas mitokondria
mengalami peningkatan, terjadi pengaktivan enzim-enzim proapoptosis seperti
caspase activator dan procaspase. Enzim-enzim ini dapat memicu kerusakan membran mitokondria sehingga merangsang sel melakukan apoptosis (Fleury et al. 2002).
Adanya apoptosis pada kelompok kontrol diduga merupakan respon
fisiologis sel hati menanggapi stres oksidatif. Persentase apoptosis yang lebih
rendah pada kelompok perlakuan dosis 5x dan 1x dibandingkan kontrol
kemungkinan disebabkan oleh senyawa flavonoid yang dikandung buah kepel.
Senyawa flavonoid berfungsi sebagai antioksidan yang memperpanjang masa
hidup sel-sel hati, sehingga semakin besar dosis pemberian kepel maka jumlah sel
hati yang mengalami apoptosis semakin rendah. Hepatosit yang mengalami
[image:33.612.122.481.419.684.2]apoptosis pada kelompok kontrol disajikan pada Gambar 5.
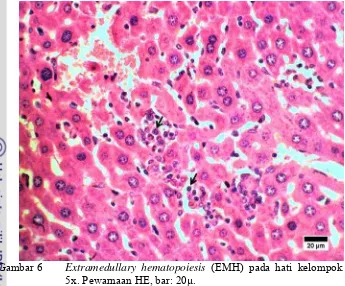
Di tepi-tepi vena sentralis, vena porta dan sinusoid ditemukan kumpulan
atau fokus-fokus sel-sel myeloblast dan eritroblast. Kumpulan sel ini merupakan
extramedullary hematopoiesis (EMH), yang terbentuk terutama bila hewan mengalami anemia dan myelofibrosis. Selain itu EMH juga ditemukan pada
kasus tumor jinak kelenjar mammae pada anjing (Grandi et al. 2010). EMH biasanya ditemukan di organ hati, limpa dan limfonodus yang terdiri atas sel-sel
mieloblast dan eritroblast (NIEHS 2010).
Anemia didefinisikan sebagai suatu keadaaan yang ditandai dengan
rendahnya konsentrasi hemoglobin dalam darah yang dapat disebabkan oleh
beberapa faktor. Salah satu faktor tersebut adalah nutrisi, yang memiliki peranan
penting pada kejadian anemia. Beberapa vitamin seperti vitamin B12, asam folat
dan riboflavin mempengaruhi pembentukan hemoglobin, akan tetapi faktor nutrisi
yang paling berperan dalam kejadian anemia adalah defisiensi zat besi.
Defisiensi zat besi awalnya ditandai dengan deplesi penyimpanan zat besi,
eritropoiesis akibat kurangnya zat besi dan anemia defisiensi zat besi. Salah satu
indikator terpenting dalam menentukan status zat besi dalam darah adalah
pengukuran feritin. Pada awal terjadinya defisiensi zat besi, konsentrasi feritin
sudah mulai menurun sehingga membuat feritin sebagai parameter yang sangat
sensitif dalam menentukan terjadinya anemia. Feritin yang rendah selalu
mengindikasikan terjadinya deplesi penyimpanan zat besi (Biesalski dan Erhardt
2007). Feritin merupakan protein penyimpan zat besi dalam darah. Zat besi
dalam darah yang dapat disimpan tiap molekul feritin dapat mencapai 4500 atom
(Lynch 2007). Feritin berada di sekitar sel makrofag pada organ hati, limpa, dan
otot rangka. Zat besi di dalam darah memiliki peranan vital dalam transpor dan
penyimpanan oksigen, metabolisme oksidatif dan proses fisiologis lainnya.
Selain flavonoid, menurut Darusman (2010) daging buah kepel juga
mengandung senyawa tanin. Tanin merupakan senyawa kelas fenol yang
dibentuk melalui jalur fenilpropanoid. Terdapat dua jenis tanin yang
mempengaruhi nutrisi hewan yaitu tanin yang dapat dihidrolisis (hydrolyzable tannins/Hts) dan tanin padat yang disebut dengan proantosianidin. Proantosinidin merupakan polimer dari flavonoid yang dihubungkan oleh ikatan karbon, dan
tumbuhan jauh lebih banyak dibandingkan jumlah tanin terhidrolisis. Tanin memiliki aktivitas mengendapkan protein dan bentuk senyawa kompleks seperti
alkaloid dan glikosida.
Kapasitas tanin dalam mengikat protein bersifat spesifik dan bergantung
pada struktur dari tanin, protein maupun kondisi reaksinya. Protein yang diikat
tanin merupakan protein dengan ukuran molekul yang besar, memiliki struktur
yang fleksibel dan terbuka serta kaya akan prolin, sedangkan tanin yang mengikat
protein memiliki berat molekul yang tinggi dan mobilitas konformasi yang tinggi.
Faktor yang mendukung terjadinya interaksi protein dengan tanin adalah pH,
suhu, komposisi protein terlarut dan waktu (Hagerman 1992). Tanin memiliki
sifat astringensia yang bekerja dengan cara melapisi mukosa usus sehingga
menurunkan daya serap nutrisi oleh usus.
Tanin dapat menginduksi terjadinya anemia karena dapat mengikat protein
darah yaitu feritin sehingga tubuh mengalami defisiensi zat besi. Walaupun kadar
tanin dalam daging buah kepel belum diketahui hingga saat ini, namun adanya
senyawa tanin cukup memberikan landasan dugaan pengaruhnya terhadap hati
mencit. Protein yang diikat oleh tanin dapat mengakibatkan mencit mengalami
hipoproteinemia, yang pada akhirnya akan berujung pada anemia. Anemia yang
terjadi pada mencit dapat dilihat dari terbentuknya fokus-fokus extramedullary hematopoiesis (EMH) pada jaringan hati. Agregat sel-sel EMH ini ditemukan pada seluruh kelompok mencit, dan fokus EMH jauh lebih banyak ditemukan
pada kelompok kepel dengan dosis 5x. Hal ini disebabkan lebih banyak suspensi
daging buah kepel yang dikonsumsi sehingga lebih banyak pula senyawa tanin
yang dicerna. Akibatnya, semakin sedikit nutrisi pakan yang dapat diserap oleh
mencit kelompok dosis 5x dibandingkan kelompok dosis 1x dan kontrol.
SIMPULAN DAN SARAN
Simpulan
Pemberian suspensi daging buah kepel (Stelechocarpus burahol) pada dosis 2.6 mg/g BB dan dosis 13 mg/g BB selama 14 hari menginduksi terjadinya
degenerasi hidropis dan extramedullary hematopoiesis (EMH), serta menurunkan terjadinya apoptosis pada hepatosit mencit. Dengan demikian konsumsi buah
kepel harus dengan dosis rendah dan jangan terlalu lama.
Saran
1. Perlu dilakukan uji toksisitas subkronis untuk mengetahui pengaruh
pemberian buah kepel dengan dosis 2.6 mg/g BB dan dalam jangka waktu
yang lebih panjang terhadap sel hati mencit.
2. Perlu dilakukan uji toksisitas LD50 terhadap daging buah kepel
(Stelechocarpus burahol).untuk mengetahui dosis aman hingga dosis lethal. 3. Perlu dilakukan pretreatment pada hewan coba sebelum perlakuan dimulai,
seperti pemberian antibiotik, obat cacing dan obat antiprotozoa agar hewan
DAFTAR PUSTAKA
[[Anonim 1]. 2009. Stimuno.
http://www.dexa-medica.com/ourproducts/otc/detail.php?id=35. [7 Juli 2011].
[Anonim 2]. 7 Agustus 2003. Memanfaatkan potensi buah burahol. Pikiran Rakyat. www.pikiran-rakyat.com. [16 Agustus 2011].
Aughey E, Frey FL. 2001. Comparative Veterinary Histology with Clinical Correlates. London: Manson Publishing. 124-127p.
[BPOM]. Badan Pengawas Obat dan Makanan. 2004. Ketentuan Pengawasan Obat dan Makanan. Jakarta.
Banks WJ. 1986. Applied Veterinary Histology. Baton Rouge, Louisiana: Williams & Wilkins.
Biesalski HK, Erhardt JG. 2007. Diagnosis of nutritional anemia-laboratory assessment of iron status. Didalam: Kraemer K dan Zimmermann MB, editor. Nutritional Anemia.Germany: Sight and Life. hlm 37-44.
D’amico AV, McKenna WG. 1994. Apoptosis and re-investigation of the biologic basis of cancer therapy, radiotherapy and oncology. Radiother Oncol 33:3-10.
Dash P. 2011. Apoptosis. Basic Medical Sciences, St. George’s University of London. [terhubung berkala]. www.sgul.ac.uk/dept/immunology/~dash. [2 Oktober 2011].
Darusman HS. 2010. Aktivitas Farmakologis Tanaman Kepel (Stelechocarpus burahol (Blume) Hook & Thompson) Sebagai Deodoran Topikal dan Oral. [Thesis]. Bogor: Fakultas Kedokteran Hewan Institut Pertanian Bogor.
Elmore S. 2007. Apoptosis: a review of programmed cell death. Toxicol Pathol. 35 (4): 495-516.
Fachrurozi Z. 1980. Burahol (Stelechocarpus burahol (Blume) Hook & Thomson) deodoran tempo dulu dan masalah pelestariannya. Buletin Kebun Raya 4 (4): 127-130.
Ferreira T, Rasband W. 2011. ImageJ User Guide: IJ 1.45m. [terhubung berkala]. http://rsb.info.nih.gov/ij/docs/index.html. [6 November 2011].
http://www.sciencedirect.com/science/article/pii/S030090840201369X . [2 Oktober 2011].
Gonzalez-Coloma A, Guadano A, De Ines C, Martinez-Diaz R, Cortes D. 2002. Selective actions of acetogennin mitochondrial complex I inhibitors. Z. Naturforsch 57:1028-1034.
Grandi F, Colodel MM, Monteiro LN, Leao JR, Rocha NS. 2010. Extramedullary hematopoiesis in a case of benign mixed mammary tumor in a female dog: cytological and histopathological assessment. BMC Vet Res (6) 45.
Guyton AC, Hall JE. 2007. Buku Ajar Fisiologi Kedokteran Edisi 11. Jakarta: EGC. 902-908p.
Hagerman AE. 1992. Tannin-Protein Interaction. Phenolics Compounds in Food and How They Affect on Health I 506: 236-247 [terhubung berkala]. http://pubs.acs.org/doi/abs/10.1021/bk-1992-0506.ch019 [10 Oktober 2011].
Hanna P. 2011. Cellular pathology. [terhubung berkala]. http://people.upei.ca/hanna/. [2 Oktober 2011]
Heyne K. 1987. Tumbuhan Berguna di Indonesia Jilid II. Jakarta: Badan Litbang Kehutanan.
Huffman MA, Gotoh S, Turner LA, Hamai M, Yoshida K.1997. Seasonal trends in intestinal nematode infection and medicinal plant use among chimpanzees in the Mahale Mountains, Tanzania. Primates 38:111-125.
Kintzios SE, Barberaki MG. 2004. Plants That Fight Cancer. Boca Raton: CRC Press. 22-23p.
Kmiec Z. 2001. Cooperation of liver cells in health and diseases. Adv Anat Embriol Cell Biol. 161 (III-XIII): 1-151.
Kresno SB. 2001. Ilmu Onkologi Dasar. Bagian Patologi Klinik FK UI: Indonesia. hlm 13-15.
Kuntz E, Kuntz HD. 2008. Hepatology: Textbook and Atlas. Germany: Springer. hlm 407.
Kusuma FR, Zaky MB. 2005. Tumbuhan Liar Berkhasiat Obat. Jakarta : Agromedia Pustaka.
Laurence J, Bacharach M. 1964. Analytical Toxicology. Philadelphia: CRC Press.
Maher JJ. 1997. Exploring alcohol’s effects on liver function. Alchl Health and Res Wor. 21:5-12.
Malole MBM, Pramono CSU. 1989. Bahan Pengajaran Penggunaan Hewan-hewan Percobaan di Laboratorium. Bogor: Departemen Pendidikan dan Kebudayaan, Direktorat Jenderal Pusat Antar Universitas Bioteknologi, Institut Pertanian Bogor. 94-103p.
Marcheix JJ, Fleuriel A, Billiot J. 1990. Fruit Phenolics. Boca Raton: CRC Press.\
Marchiori E, Escuisato DL, Irion KL, Zanetti G, Rodrigues RS, Meirelles GS, Hochhegger B. 2007. Extramedullary hematopoiesis: findings on computed tomography scans of the chest in 6 patients. Jor. Bras. Pneum.
[terhubung berkala].
http://www.scielo.br/scielo.php?script=sci_arttext&pid=S1806-37132008001000009&lng=en&nrm=iso&tlng=en . [12 Oktober 2011]
[NIEHS]. National Institute of Environmental Health Sciences. 2011. The Digitized Atlas of Mouse Liver Lesions: Extramedullary Hematopoiesis.
[terhubung berkala].
http://www.niehs.nih.gov/research/atniehs/labs/lep/path-support/core-support/lverpath/miscellaneous.cfm [6 Oktober 2011].
Norbury CJ, Hickson ID. 2001. Cellular responses to DNA damage. Annu Rev Pharmacol Toxicol 41:367–401.
Ohigashi H, Huffman MA, Izutsu D, et al. 1994. Toward the chemical ecology of medicinal plant use in chimpanzee: the case of Vernonia amygdalina Del. A plant used by will chimpanzees possible for parasite-related diseases. J Chem Ecol 20:246-252.
Osorio E, Arango GJ, Jimenez N, Alzate F, Ruiz G, Guiterrez D, Paco MA, Gimenez A, Robledo S. 2007. Antiprotozoal and Cytotoxic Activities In Vitro of Colombian Annonaceae. J Ethnopharmacol.111(3):630-5.
Spiridonova LN, Chelomina GN, Moriwaki K, Yonekawa H, Bognado AH. 2003. Genetic and taxonomic diversity of the house mouse Mus musculus from the Asian part of the former Soviet Union. Russ J of Gen 40 (10): 1134-1143.
Piersen CE. 2003. Phytoestrogen in Botanical Dietary Supplements: Implication for Cancer. Integr Cancer Ther Jun 2 (2): 120-138.
Renehan AG, Booth C, Potten CS. 2001. What is apoptosis, and why is it important?. BMJ 322:1536–8.
Shiddiqi T, Rindiastuti Y, Sri NA. 2008. Potensi In Vitro Zat Sitotoksik AntiKkanker Daun Tanaman Kepel (Stelechocarpus burahol) terhadap carcinoma colorectal. Surakarta: Fakultas Kedokteran, Universitas Sebelas Maret.
Sinclair J. 1955. A Revised of the Malayan Annonaceae. The Gardens' Bulletin Singapore. 14 (15): 149-515
Sunardi CSA, Padmawinata K, Kardono LBS, Gana A. 2007. Isolasi dan Identifikasi Kulit Batang Burahol (Stelechocarpus burahol) Terhadap sel Leukimia [disertasi]. Bandung : Institut Teknologi Bandung, Sekolah Farmasi.
Sunarni T, Pramono S, Asmah R. 2007. Flavonoid antioksidan penangkap radikal dari daun kepel (Stelechocarpus burahol). Majalah Farmasi Indonesia ; 18(3).
Sunarto AT. 1992. Burahol kosmetika alam bagi kerabat keraton. Trubus 18 (207): 103-104.
Talukder SI. 2001. Lecture notes on pathology of hepatobiliary system.
[terhubung berkala]. http://www.talukderbd.com/lectures/hepatobiliary_system_note.pdf [6
September 2011].
Tisnadjaja D, Saliman E, Silvia, Simanjuntak P. 2006. Pengkajian Burahol (Stelechocarpus burahol (Blume) Hook & Thompson) sebagai buah yang memiliki kandungan senyawa antioksidan. Biodiv 7 (2): 199-202.
Umiyah. 2005. Existence of Stelechocarpus burahol (Blume) Hook & Thompson. in wilderness zone, Bande Alit Resort, Meru Betiri National Park. Berk. Penel.Hayati: 10 (85-88).
Underwood JCE. 1996. General and Systematic Pathology: 2nd Ed. Churchill Livingstone: NewYork-London-Madrid. hlm 117-119.
Verhejj EWM, Coronell RE. 1997. Sumber Daya Nabati Asia Tenggara 2. Buah-buahan yang Dapat Dimakan. Bogor: Prosea.
Warningsih. 1995. Uji fitokimia dan efek antiimplantasi ekstrak etanol bunga hibiscus rosa-sinensis, buah Piper nigrum, dan buah Stelechocarpus burahol [abstrak]
Wong KF. 2010. Kepel dan Matoa. http://wongkamfung.boogoor.com/kepel-dan-matoa112.html. [15 Agustus 2011]
Wrangham RW. 1994. Feeding behavior of chimpanzee in Gombe National Park, Tanzania, In: Clutton-Brock TH, ed. Primate Ecology. New York: Academic Press : 504-538.
Wynn SG, Fougere BJ. 2007. Veterinary Herbal Medicine. Missouri: Mosby, Inc. hlm 12-20.
Lampiran 1. Penghitungan Dosis Pemberian Kepel.
• Berat keseluruhan daging buah kepel yang masih basah:440 g, dan setelah dikeringkan diperoleh 60 g serbuk simplisia kering. Jadi rendemen kepel:60 g/440 g x 100% = 13.63%
• Dosis empiris konsumsi kepel pada manusia adalah 2 buah kepel dalam 2 hari. Jika diasumsikan berat kepel adalah 70 g/buah dan BB manusia 70 kg, maka konsumsi kepel pada manusia dalam dua hari adalah 140 g/70 kg. Konsumsi buah kepel dalam bentuk serbuk kering pada manusia adalah: 13.63/100 x 140 g= 19.08 g atau rata-rata 20 g serbuk kering.
• Faktor konversi dosis manusia ke mencit: 0.0026 (Laurence & Bacharach 1964), sehingga dosis konsumsi kepel normal (sama dengan dosis pada manusia) adalah:
= 20 g x 0.0026 = 0.052 g/20g mencit = 52 mg/20 g mencit
= 2.6 mg/g BB mencit (Dosis 1x)
Lampiran 2. Penghitungan Volume Pemberian Kepel.
• Dosis 1x = 2.6 mg/g BB
Volume pemberian = (Dosis x BB)/Konsentrasi = (2.6 mg/g BB x 20 g)/10% = (2.6 mg/g x 20 g)/(10 g/100 ml)
= (52 mg)/100 mg/ml
= 0.5 ml
• Dosis 5x = 13 mg/g BB
Volume pemberian = (Dosis x BB)/konsentrasi 0.5 ml= (13 mg/g x 20 g BB)/konsentrasi Konsentrasi = 260 mg/0.5 ml
= 520 mg/ml
Konsentrasi = 5.2 g/10mlÆ5.2 g serbuk buah dilarutkan ke dalam 10 ml akuades.
Lampiran 3. Pembuatan Sediaan Histopatologi dan Pewarnaan HE.
Hati difiksasi dalam larutan Buffer Neutral Formalin 10% selama 3 hari.
Hati yang sudah difiksasi dipotong-potong atau ditrimming dan dimasukkan kedalam tissue cassette.
Selanjutnya jaringan didehidrasi dengan cara dimasukkan secara
berturut-turut ke dalam larutan alkohol 70%, 80%, 90% dan alkohol 95% selama 2 jam.
Kemudian dehidrasi dilanjutkan ke dalam alkohol absolut I selama 2 jam, alkohol
absolut II selama 2 jam, xylol I, xylol II dan xylol III masing-masing selama 40
menit, parafin I, parafin II, parafin III dan parafin IV masing-masing selama 30
menit dalam suhu 60o C.
Proses selanjutnya adalah embedding dimana jaringan dimasukkan ke dalam blok pencetak berisi parafin cair kemudian parafin cair ditambahkan lagi ke
dalam blok pencetak hingga penuh dan ditunggu sampai seluruh parafin
mengeras. Setelah paraffin mengeras blok paraffin dimasukkan ke dalam
refrigerator dengan suhu sekitar 4-6°C.
Proses pembuatan sediaan histopatologi dilanjutkan dengan pengirisan
blok parafin menggunakan mikrotom dengan ketebalan 3-5 mµ. Kemudian
potongan jaringan tersebut diletakkan di atas permukaan air hangat dengan suhu
45°C untuk menghilangkan lipatan-lipatan. Setelah itu potongan jaringan diangkat
(mounting) dengan kaca objek yang sudah diulas dengan larutan albumin.
Sediaan dikeringkan selama minimal 2 jam dalam inkubator bersuhu 58°C.
Selanjutnya dilakukan pewarnaan HE, dengan mencelupkan sediaan ke dalam
larutan-larutan dengan urutan sebagai berikut: larutan xylol I dan xylol II
masing-masing selama dua menit, alkohol absolut selama 2 menit, alkohol 95% dan 80%
masing-masing selama 1 menit, kemudian dicuci dalam air keran atau akuades
selama 1 menit, dilanjutkan dengan memasukkan sediaan ke dalam larutan
pewarna Mayer’s Hematoksilin selama 8 menit, kemudian dicuci kembali dengan
air keran selama 30 detik. Setelah itu sediaan dimasukkan ke dalam larutan
lithium karbonat selama 15-30 detik dan kembali dicuci dengan air keran atau
akuades selama 2-3 menit. Selanjutnya sediaan diwarnai dengan pewarna eosin
Langkah selanjutnya adalah mencelup sediaan ke dalam larutan alkohol
95% sebanyak sepuluh kali, alkohol absolut I sebanyak sepuluh kali, alkohol
absolut II selama dua menit, xylol I selama satu menit, dan xylol II selama dua
menit. Setelah itu sediaan dikeringkan dan diberi perekat permount, lalu ditutup
dengan kaca penutup dan disimpan selama beberapa menit sampai zat perekat
Lampiran 4 Analisis Perubahan Degenerasi Hidropis Pada Sel Hati.
dh * perlakuan
Dh
perlakuan Mean N Std. Deviation
kontrol 36.0500 60 12.49736
dosis 1x 41.4500 60 13.07012
dosis 5x 57.7000 60 12.57291
Total 45.0667 180 15.65323
Dh
Duncan
perlakuan N
Subset
1 2 3
kontrol 60 36.0500
dosis 1x 60 41.4500
dosis 5x 60 57.7000
Sig. 1.000 1.000 1.000
Means for groups in homogeneous subsets are displayed.
Based on observed means.
Lampiran 5 Analisis Perubahan Apoptosis Pada Sel Hati.
apoptosis * perlakuan
apoptosis
perlakuan Mean N Std. Deviation
kontrol 25.1667 60 13.56862
dosis 1x 21.6667 60 7.74743
dosis 5x 12.1333 60 6.46887
Total 19.6556 180 11.16975
apoptosis
Duncan
perlakuan N
Subset
1 2 3
dosis 5x 60 12.1333
dosis 1x 60 21.6667
kontrol 60 25.1667
Sig. 1.000 1.000 1.000
Means for groups in homogeneous subsets are displayed.
Based on observed means.
Lampiran 6 Analisis Sel Hati Normal.
normal * perlakuan
normal
perlakuan Mean N Std. Deviation
kontrol 38.7833 60 15.00406
dosis 1x 36.8833 60 12.67467
dosis 5x 30.1667 60 11.71724
Total 35.2778 180 13.64353
normal
Duncan
perlakuan N
Subset
1 2
dosis 5x 60 30.1667
dosis 1x 60 36.8833
kontrol 60 38.7833
Sig. 1.000 .443
Means for groups in homogeneous subsets are
displayed.
Based on observed means.
The error term is Mean Square(Error) =
183.017.
PENDAHULUAN
Latar Belakang
Penggunaan obat-obatan herbal menjadi sebuah alternatif yang saat ini
digandrungi oleh masyarakat. Mayoritas masyarakat lebih memilih pengobatan
herbal karena bahan alami dianggap bersifat lebih aman, selain itu juga relatif
lebih murah dibandingkan obat modern. Faktor pendorong berpindahnya
masyarakat memakai obat herbal adalah usia harapan hidup yang lebih panjang
setelah mengonsumsi obat herbal saat prevalensi penyakit kronik meningkat dan
adanya kegagalan penggunaan obat modern untuk penyakit tertentu seperti
kanker. Herbal kembali dilirik kajian ilmiahnya oleh peneliti setelah melihat
kemampuan alami hewan di alam liar mengonsumsi tanaman untuk self-treatment dalam mengurangi rasa sakit pada saat-saat tertentu.
Indonesia memiliki lebih dari 30.000 jenis spesies tumbuhan yang 960
spesies diantaranya telah tercatat sebagai tumbuhan berkhasiat, dan 283 jenis
diantaranya merupakan tumbuhan yang penting bagi industri obat tradisional
(Kusuma dan Zaky 2005). Diantara tanaman berkhasiat tersebut adalah daun
jambu biji (Psidium guava) yang mengandung psiditanin yang berguna sebagai obat diare, atau Echinacea purpurea yang mengandung echinasida yang berfungsi sebagai immunomodulator. Beberapa tanaman yang telah menjadi obat herbal terstandar diantaranya Kiranti®, yang mengandung kunyit (Curcuma domestic) berguna untuk meredakan nyeri pada saat haid, dan Stimuno®, contoh
immunomodulator dari herbal alami yang membantu meningkatkan daya tahan tubuh. Stimuno® terdaftar sebagai sediaan fitofarmaka yang berasal dari ekstrak
tanaman meniran (Phyllantus niruri) yang terstandarisasi, karena telah melalui berbagai uji preklinik dan klinik (Anonim 1 2009). Berdasarkan temuan-temuan
di atas memicu para peneliti untuk menelaah lebih jauh potensi tumbuhan khas
Indonesia dalam mewujudkan kesehatan masyarakat, hewan dan lingkungan.
Salah satu tanaman asli Indonesia yang biasa digunakan sebagai jamu adalah
tanaman khas asal Yogyakarta yang sering disebut dengan kepel.
bagi masyarakat Keraton, Yogyakarta. Putri keraton dahulu menggemari buah ini
sebagai penghilang bau badan, memberi efek wangi pada produk ekskresi manusia
seperti keringat, urin dan feses. Selain itu daun kepel mengandung banyak zat
sitotoksik bagi sel kanker (Wiart 2007), dan mengandung banyak senyawa
flavonoid yang bersifat sebagai antioksidan (Sunarni et al. 2007). Bunga dari tumbuhan kepel diketahui memiliki efek antiimplantasi sehingga dapat digunakan
sebagai kontrasepsi (Warningsih 1995). Bagian kulit batangnya juga diketahui
sebagai antiagregasi platelet (Sunardi et al. 2007). Banyaknya potensi obat yang dimiliki tanaman kepel berbanding terbalik dengan langkanya tanaman ini.
Kelangkaan disebabkan oleh kurangnya nilai ekonomis dari tanaman ini, dan
kepel termasuk tanaman yang berbuah setahun sekali. Karena faktor inilah
mengapa masyarakat urung membudidayakan dan memanfaatkan kepel. Adanya
publikasi ilmiah mengenai potensinya diharapkan menjadi ujung tombak
memasyarakatkan kepel sebagai tanaman yang memiliki nilai ekonomi tinggi.
Penelitian ini bertujuan untuk mempelajari gambaran histopatologi organ
hati terhadap pemberian suspensi daging kepel, karena hati merupakan organ
interna pertama yang terkena efek toksik dari suatu substansi yang masuk ke
dalam tubuh. Hati juga memiliki peranan yang sangat penting karena merupakan
pusat metabolisme zat makanan sebelum diedarkan ke seluruh tubuh (Banks
1986). Berdasarkan data empiris dari masyarakat Keraton, kepel dikonsumsi
sebanyak 2 buah dalam 1 hari. Bersumber dari data empiris tersebut maka
dilakukan penelitian untuk mempelajari adakah perubahan pada gambaran
histopatologi hati mencit setelah pemberian kepel selama 14 hari. Dari hasil
penelitian ini diharapkan semakin banyak masyarakat yang mengetahui potensi
kepel sehingga tertarik membudidayakan dan memanfaatkannya.
Tujuan
Penelitian ini bertujuan untuk mempelajari pengaruh pemberian suspensi
Manfaat
Manfaat penelitian adalah untuk mengetahui potensi kepel sehingga
masyarakat tertarik untuk membudidayakan dan memanfaatkannya, dan juga
meningkatkan pamor dan nilai ekonomis kepel sehingga dapat merubah gaya
hidup untuk semakin mencintai buah nasional.
Hipothesis
Hipotesis penelitian ini adalah sebagai berikut:
H0: Suspensi daging buah kepel tidak berpengaruh terhadap gambaran
histopatologi organ hati mencit.
H1: Suspensi daging buah kepel berpengaruh terhadap gambaran histopatologi
TINJAUAN PUSTAKA
Tanaman Herbal
Tanaman herbal memiliki keistimewaan yang tidak dimiliki oleh
farmakologi konvensional. Farmakologi konvensional saat ini bersifat single compound yang spesifik khasiatnya terhadap suatu penyakit. Hal ini berbeda dengan tanaman herbal yang memiliki multi compound yang mengandung berbagai macam substansi dengan khasiat yang berbeda sehingga dapat
menyeimbangkan efek samping. Farmakologi konvensional umumnya tetap
dianggap sebagai pilihan pengobatan karena khasiatnya bersifat spesifik sehingga
respon penyembuhannya lebih cepat. Tanaman herbal dianggap sebagai pilihan
yang tepat dalam pengobatan penyakit kronis karena memiliki bahan alami yang
dapat memperbaiki metabolisme sehingga dianggap lebih aman dalam
penggunaan jangka panjang.
Pengobatan herbal mewakili berbagai macam disiplin ilmu seperti botani,
sejarah, etnomedisinal dan farmakologi (Wynn dan Fougere 2007). Pengobatan
herbal pada hewan diawali dengan adanya perilaku hewan yang mampu
melakukan self-treatment saat terserang penyakit. Perilaku alami hewan ini menjadikan salah satu alasan para ahli herbal meneliti tanaman obat dan
interaksinya dalam tubuh. Sebagai contoh, kera besar di Tanzania memakan
daun-daun berambut yang berasal dari 34 spesies tanaman obat berbeda, tanpa
mengunyah namun langsung menelannya. Beberapa daun yang dipilih diketahui
mengandung fitokimia aktif dan sebagian tidak, namun semua daun yang dipilih
memiliki tekstur permukaan kasar dengan mikrostruktur mirip dengan kait yang
biasa disebut dengan trichomes. Dedaunan tersebut biasanya dikonsumsi hewan pada saat musim hujan dimana infestasi cacing meningkat sehingga menyebabkan
diare, malaise dan sakit perut (Huffman et al. 1997). Hasil penelitian menunjukkan bahwa tekstur kasar pada permukaan daun berperan sebagai
pembersih mekanis cacing yang menginfestasi saluran pencernaan. Dedaunan
kasar juga meningkatkan motilitas usus dan merangsang diare, sehingga
Interaksi dedaunan di dalam tubuh menghasilkan efek yang cepat dalam
menanggulangi gejala penyakit yang diderita kera tersebut seperti malaise pada
saluran pencernaan (Huffman et al. 1997). Perilaku alami mengonsumsi dedaunan berambut juga telah membantu simpanse di Taman Nasional Kibale,
Uganda untuk menyingkirkan infestasi cacing pita