UIN SYARIF HIDAYATULLAH JAKARTA
STUDI HUBUNGAN KUANTITATIF STRUKTUR
AKTIVITAS DARI AMIDASI SENYAWA ETIL-
P
-METOKSISINAMAT SEBAGAI ANTIINFLAMASI
DENGAN PENDEKATAN HANSCH DAN
KOMPUTASI
SKRIPSI
EKO WAHYUDI
1111102000028
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
JAKARTA
ii
UIN SYARIF HIDAYATULLAH JAKARTA
STUDI HUBUNGAN KUANTITATIF STRUKTUR
AKTIVITAS DARI AMIDASI SENYAWA ETIL-
P
-METOKSISINAMAT SEBAGAI ANTIINFLAMASI
DENGAN PENDEKATAN HANSCH DAN
KOMPUTASI
SKRIPSI
Diajukan sebagai salah satu syarat memperoleh gelar Sarjana Farmasi
EKO WAHYUDI
1111102000028
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
JAKARTA
iii
HALAMAN PERNYATAAN ORISINALITAS
Skripsi ini adalah hasil karya saya sendiri,
dan semua sumber baik yang dikutip maupun dirujuk
telah saya nyatakan dengan benar.
Nama : EKO WAHYUDI
NIM : 1111102000028
Tanda Tangan :
iv
HALAMAN PERSETUJUAN PEMBIMBING
Nama : Eko Wahyudi
NIM : 1111102000028
Program Studi : Farmasi
Judul : STUDI HUBUNGAN KUANTITATIF STRUKTUR
AKTIVITAS DARI AMIDASI SENYAWA ETIL-P -METOKSISINAMAT SEBAGAI ANTIINFLAMASI
DENGAN PENDEKATAN HANSCH DAN
KOMPUTASI
Disetujui oleh :
Pembimbing I
Supandi, M.Si, Apt
Pembimbing II
Andrianopsyah Mas Jaya Putra, M.Sc
v
HALAMAN PENGESAHAN SKRIPSI
Skripsi ini diajukan oleh :
Nama : Eko Wahyudi
NIM : 1111102000028
Program Studi : Farmasi
Judul : STUDI HUBUNGAN KUANTITATIF STRUKTUR
AKTIVITAS DARI AMIDASI SENYAWA ETIL-P -METOKSISINAMAT SEBAGAI ANTIINFLAMASI
DENGAN PENDEKATAN HANSCH DAN
KOMPUTASI
Telah berhasil dipertahankan di hadapan Dewan Penguji dan diterima sebagai bagian persyartan yang diperlukan untuk memperoleh gelar Sarjana Farmasi pada Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta.
DEWAN PENGUJI
Pembimbing I : Supandi, M.Si, Apt (………..)
Pembimbing II : Andrianopsyah Mas Jaya Putra, M.Sc. (….……….)
Penguji I : Ismiarni Komala, Ph.D., Apt. (………..)
Penguji II : Drs. Umar Mansyur, M.Sc., Apt (….……….)
Ditetapkan di : Ciputat
vi
HALAMAN PENYATAAN PERSETUJUAN PUBLIKASI TUGAS AKHIR UNTUK KEPENTINGAN AKADEMIK
Sebagai sivitas akademik Universitas Islam Negeri (UIN) Syarif
Hidayatullah Jakarta, saya yang bertanda tanfan dibawah ini :
Nama : Eko Wahyudi
NIM : 1111102000028
Program Studi : Farmasi
Fakultas : Kedokteran dan Ilmu Kesehatan Jenis Karya : Skripsi
Demi perkermbangan ilmu pengetahuan, saya menyetujui skripsi/karya ilmiah saya, dengan judul :
STUDI HUBUNGAN KUANTITATIF STRUKTUR AKTIVITAS DARI AMIDASI SENYAWA ETIL-P-METOKSISINAMAT SEBAGAI
ANTIINFLAMASI DENGAN PENDEKATAN HANSCH DAN KOMPUTASI
Untuk dipublikasi atau disampaikan di internet atau media lain yaitu Digital Library
Perpustakaan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta untuk kepentingan akademik sesuai Undang-Undang Hak Cipta.
Demikian pernyataan persetujuan publikasi karya ilmiah ini saya buat dengan sebenarnya
Dibuat di : Jakarta Pada tanggal : 20 Juni 2015
Yang Menyatakan,
vii ABSTRAK
Nama : Eko Wahyudi
Program Studi : Farmasi
Judul : STUDI HUBUNGAN KUANTITATIF STRUKTUR
AKTIVITAS DARI AMIDASI SENYAWA ETIL-P -METOKSISINAMAT SEBAGAI ANTIINFLAMASI
DENGAN PENDEKATAN HANSCH DAN
KOMPUTASI
Telah dilakukan studi hubungan kuantitatif struktur aktivitas (HKSA) antiinflamasi dari 10 senyawa turunan asam sinamat dengan pendekatan Hansch berdasarkan analisis multiregresi linier dan penambatan molekul terhadap enzim COX-2. Deskriptor digunakan untuk mewakili parameter hidrofobisitas (log P), sterik (indeks Harary, indeks Randic, dan molar refraksi), dan elektronik (polarisabilitas, EHUMO, ELOMO, dan selisih EHUMO-LOMO). Hasil HKSA berdasarkan
analisis multiregresi linier (MLR) adalah:
Log 1/IC50 = -6.559 + 0.017 [Log P] – 0.025 [Indeks Harary] + 0.039 [MR] + 0.016
[Polarisabilitas] - 0.396 [ELUMO] + 0.427 [∆EHOMO-LUMO]
Dari persamaan, didapatkan prediksi potensi tertinggi sebagai antiinflamasi dari senyawa amidasi etil p-metoksisinamat, yaitu senyawa dengan log 1/IC50 sebesar
-0.677. Proses inflamasi terjadi dengan adanya enzim siklooksigenasie. Enzim siklooksigenase merupakan enzim yang mengkatalisis pembentukan prostaglandin, suatu mediator inflamasi, dan produk metabolisme asam arakidonat. COX-2 merupakan enzim yang terinduksi pada sel yang mengalami inflamasi oleh sitokin, endotoksin, dan faktor pertumbuhan (growth factors). Interaksi dari senyawa
amidasi EPMS dengan COX-2 dapat dilakukan dengan cara penambatan molekul. Penambatan molekul antara senyawa uji dari amidasi EPMS dengan molekul COX-2 (PDB:1CXCOX-2), diperoleh senyawa dengan energi ikatan sebesar -7.5 kkal/mol dengan membandingkan energy ikatan ibuprofen (-7.5 kkal/mol).
viii ABSTRACT
Nama : Eko Wahyudi
Major : Pharmacy
Title : STUDY QUANTITATIVE STRUCTURE ACTIVITY
RELATIONSHIP OF COMPOUNDS AMIDATION
ETHYL p-METHOXYCINNAMATE AS
ANTIINFLAMMATORY HANSCH APPROACH AND COMPUTATION
Study quantitative structure activity relationship (QSAR) of 10 derivatives cinnamic acid compound as anti-inflammatory has been carried out by Hansch approach based multiple linier regression (MLR) and molecular docking to COX-2 enzym. Descriptor used to represent parameter hydrophobicity (Log P), steric (index Harary, index Randic and Molar refractivity (MR), and electronic (EHUMO,
ELOMO, ΔEHUMO-LUMO, and Polarizability). Best QSAR equationby applying analysis MLR as follows :
Log 1/IC50 = -6.559 + 0.017 [Log P] – 0.025 [Index Harary] + 0.039 [MR] + 0.016
[Polarizability] - 0.396 [ELUMO] + 0.427 [∆EHOMO-LUMO]
Following equation, obtained high prediction activity as anti-inflammatory from amidation ethyl p-methoxycinnamate (EPMS) compound is compound 1B with
substituent aniline is -0.677. Inflammation occurred process by cyclooxygenase enzyme. Cyclooxygenase enzyme is enzyme to catalyst prostaglandin formation, inflammatory mediator, and metabolic product arachidonate acid. COX-2 is and enzyme to induced inflammatory cells by cytokines, endotoxin, and growth factors. Interaction of amidation EPMS compound with COX-2 molecule can be carried out by molecular docking. Docking amidation compound with COX-2 molecule obtained binding energy of -7.5 kcal/mol with compared energy binding ibuprofen (-7.5 kcal/mol).
ix
KATA PENGANTAR
Puji syukur kehadirat Allah SWT., karena atas berkat dan rahmat-Nya proses penelitian hingga penulisan skripsi ini dapat berjalan. Penulisan skripsi ini dilakukan dalam rangka memenuhi salah satu syarat untuk mencapai gelar Sarjana Farmasi pada Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta.
Saya menyadari bahwa, tanpa bantuan dan bimbingan dari berbagai pihak, dari masa perkuliahan sampai pada penyusunan skripsi ini, sangatlah sulit bagi saya untuk menyelesaikan skripsi ini. Oleh karena itu, saya mengucapkan terima kasih kepada :
1. Kepada kedua orang tua tercinta, Ibu Sriyati dan Bapak Tukimin, yang selalu mengingatkan untuk fokus belajar, jangan pulang larut malam, jaga kondisi tubuh, dan lulus kulias. Tak lupa ucapan terima kasih yang sedalam-dalam atas kontribusi yang selama ini diberikan berupa dukungan moril, finansial, dan doa yang selalu diberikan kepada penulis dan adik tercinta Dwi Puji Astuti yang selalu memberikan dukungan kepada penulis
2. Bapak Supandi, M.Si, Apt., selaku pembimbing pertama dan Bapak Andrianopsyah Mas Jaya Putra, M.Sc., selaku pembimbing kedua, yang tak lelah memberikan kontribusi nyata berupa masukan, bimbing, dan kritik terhadap penulis dalam menyelesaikan skripsi. Penulis hanya bisa berdoa, semoga mendapatkan berkah, kesehatan jasmani dan rohani dari Allah S.W.T. 3. Bapak Drs. Arief Sumantri, S.KM., M.KM selaku Dekan Fakultas Kedokteran
dan Ilmu Kesehatan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta.
x
5. Seluruh dosen – dosen di Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta.yang telah banyak membantu penulis dalam menyelesaikan studi hingga saat ini.
6. Bapak Drs. Umar Mansyur, M.Sc., Apt., selaku dosen terfavorit penulis di Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta yang selalu memberikan nasihat dan bimbingan agar mahasiswa/I dapat lulus tepat waktu dan menjadi teman curhat penulis ketika sedang kesulitan.
7. Kak Fikri, yang saat ini sedang melanjutkan program apoteker, yang telah menjadi mentor dalam skripsi penulis dan tim docking sehingga dapat mengerjakan skripsi ini dengan lancar dan Docking Team berisi Arsyad (cacad), Wahidin (dindin), Mazaya, Fitri, Haidar, Wahyu, yang menjadi teman sharing skripsi dan tempat
bertukar ilmu dan sekaligus menjadi teman curhat.
8. Rekan-rekan di Program Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta angkatan 2011 yang telah menjadi teman sekaligus menjadi keluarga besar penulis selama ini. Kemudian teman-teman pengurus BEM FKIK periode 2013 – 2014, serta teman-teman di HMI KOMFAKDIK.
Penulis menyadari bahwa dalam penulisan dan penyusunan skripsi ini masih jauh dari kata sempurna, karena itu penulis mengharapkan kritik dan saran dari pembaca yang bersifat membangun dan dapat memacu penulis untuk berkarya lebih baik di masa yang akan datang.
Akhir kata, saya berharap Allah SWT berkenan membalas segala kebaikan semua pihak yang telah membantu. Semoga skripsi ini dapat bermanfaat bagi penulis khususnya, dan dapat memberikan kontribusi ilmu pengetahuan bagi semua pihak.
Ciputat, Juni 2015
xi DAFTAR ISI
HALAMAN SAMPUL………..ii
HALAMAN PERNYATAAN ORISINALITAS ... iii
HALAMAN PERSETUJUAN PEMBIMBING ...iv
HALAMAN PENGESAHAN SKRIPSI ... v
HALAMAN PENYATAAN PERSETUJUAN PUBLIKASI ...vi
ABSTRAK ... vii
BAB II TINJAUAN PUSTAKA... 4
2.1. Hubungan Kuantitatif Struktur – Aktivitas (HKSA) ... 4
2.2. Analisis Statistik HKSA model Hansch ... 11
2.3. Asam Sinamat ... 13
2.4. Etil p-metoksisinamat ... 16
2.5. Ester ... 17
2.6. Amida ... 18
2.7. Inflamasi ... 20
2.8. Enzim Siklooksigenase 2 (COX-2) ... 22
2.9. Protein dan Asam Amino ... 22
2.10. Interaksi Protein dengan Ligan ... 25
2.11. Molecular docking (Penambatan Molekul) ... 27
2.12. Protein Data Bank (PDB) ... 30
xii
3.1. Tempat dan Waktu Penelitian ... 32
3.2. Alat ... 32
3.3.3. Struktur Tiga Dimensi (3D) Ligan Amidasi EMPS ... 33
3.4. Cara Kerja... 33
3.4.1. Penyiapan Model HKSA ... 33
3.4.2. Penambatan Molekul ... 34
BAB IV HASIL DAN PEMBAHASAN ... 36
4.1. Hubungan Kuantitatif Struktur-Aktivitas (HKSA) ... 36
4.1.1. Pemilihan Data Set ... 36
4.1.2. Pemilihan Deskriptor Training set dan Test set ... 39
4.1.3. Analisa Korelasi Deskriptor dengan Aktivitas Biologis ... 46
4.1.4. Pemodelan Persamaan HKSA dengan metode MLR ... 47
4.1.5. Validasi Persamaan HKSA ... 49
4.2. Penambatan Molekul (Molecular Docking) ... 53
4.2.1. Penyiapan Molekul ... 53
4.2.2. Penyiapan Ligan ... 54
4.2.3. Penambatan Molekul ... 55
4.2.4. Analisa dan Visualisasi Penambatan Molekul ... 56
BAB V KESIMPULAN DAN SARAN ... 67
5.1. Kesimpulan... 67
5.2. Saran ... 67
DAFTAR PUSTAKA ... 68
xiii
DAFTAR GAMBAR
Gambar 2.1. Hubungan antara aktivitas biologis dengan log P……… 7
Gambar 2.2. Struktur umum senyawa etil p-metoksisinamat ... 17
Gambar 2.3. Struktur umum senyawa ester ... 17
Gambar 2.4. Contoh penamaan amida... 18
Gambar 2.5. Reaksi pembuatan amida ... 18
Gambar 2.6. Reaksi pembuatan amina primer ... 19
Gambar 2.7. Reaksi pembuatan amina sekunder ... 19
Gambar 2.8. Mekanisme inflamasi melalui jalur asam arakidonat ... 21
Gambar 2.9. Asam amino alifatik bersifat hidrofobik ... 26
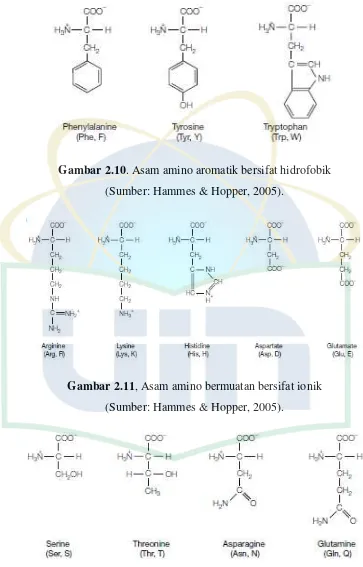
Gambar 2.10. Asam amino aromatik bersifat hidrofobik ... 24
Gambar 2.11. Asam amino aromatik bersifat ionic ... 24
Gambar 2.12. Asam amino aromatik bersifat polar... 24
Gambar 4.1. Struktur Caffeic acid oktil ester yang telah dioptimasi ... 37
xiv
DAFTAR TABEL
Tabel 2.1. Turunan Asam sinamat dengan sifat antiinflamasi ... 14
Tabel 4.1. Data set dari 15 senyawa turunan asam sinamat ... 37
Tabel 4.2. Training set ... 40
Tabel 4.3. Test Set ... 40
Tabel 4.4. Data deskriptor hidrofobik dan sterik dari 15 senyawa turunan asam sinamat ... 41
Tabel 4.5. Data deskriptor elektronik dari 15 senyawa turunan asam sinamat .... 46
Tabel 4.6. Nilai Korelasi antara deskriptor dengan nilai aktivitas ... 48
Tabel 4.7. Model Persamaan HKSA dengan metode MLR ... 49
Tabel 4.8. Perbandingan aktivitas eksperimen dan prediksi training set ... 51
Tabel 4.9. Nilai RMSD test set ... 51
Tabel 4.10. Hasil prediksi aktivitas antiinflamasi dengan HKSA ... 53
Tabel 4.11. Hasil visualisai penambatan molekul (3D dan 2D) dengan ligan uji dan kontrol positif (Ibuprofen) ... 58
Tabel 4.12. Interaksi molekul ligan dengan asam amino terikat ... 63
Tabel 4.13. Jenis asam amino yang terikat pada ligan ... 66
xv
DAFTAR LAMPIRAN
Lampiran 1. Alur penelitian HKSA dan penambatan molekul ... 65
Lampiran 2. Tabel rekapitulasi perhitungan deskriptor hidrofobik, sterik, dan elektronik 15 senyawa turunan asam sinamat ... 67
Lampiran 3. Hasil analisi korelasi antara deskriptor dengan aktivitas biologis ... 68
Lampiran 4. Hasil analisis MLR dengan Training Set ... 69
Lampiran 5. Struktur3D protein COX-2 ... 71
Lampiran 6. Prosedur kerja penambatan molekul (molecular docking) ... 72
1 BAB I PENDAHULUAN
1.1. Latar Belakang
Inflamasi secara sederhana dapat diartikan sebagai respon jaringan terhadap sel yang rusak. Inflamasi masuk dalam keadaan patologis yang sering menyebabkan kelainan sel rusak atau nekrosis, itu berarti inflamasi (peradangan) biasa dianggap sebagai penyakit, kisarannya mulai dari gigitan serangga hingga menimbulkan banyak komplikasi dan keadaan serius seperti kanker. Inflamasi kronik berhubungan dengan berbagai penyakit seperti penyakit infeksi, kanker atau kelainan autoimun yang menghasilkan immunosupressan oleh terhambatnya sel natural killer dan sel
T, sehingga menyebabkan penyakit (Umar et al, 2012). Enzim yang
berperan dalam terjadinya inflamasi adalah enzim siklooksigenase 2 (COX-2). COX-2 merupakan enzim yang terinduksi pada sel yang mengalami inflamasi oleh sitokin, endotoksin, dan faktor pertumbuhan (growth
factors). COX-2 juga berperan dalam proliferase sel kanker. Ekspresi
berlebihan ditemukan pada kebanyakan tumor (Zullies et al, 2006).
Penelitian yang dilakukan untuk menemukan senyawa yang mempunyai antiinflamasi, salah satunya adalah adalah etil p-metoksisinamat (EPMS).
Etil p-metoksisinamat (EPMS) merupakan salah satu senyawa yang
diperoleh dari rimpang kencur (Kaemferia galanga L.), dan telah banyak
digunakan sebagai pengobatan nyeri dan peradangan, senyawa ini juga menunjukan aktivitas penghambat proliferasi sel tumor pada jaringan epidermis tikus dan papiloma (Ekowati et al, 2012). Umar et al (2012)
melaporkan bahwa senyawa EPMS dapat menghambat karagenan penginduksi edema dengan MIC 100 mg/kg. EPMS non selektif menghambat aktifitas siklooksigenasi 1 dan 2, dengan nilai IC50 1.12 μm dan 0.83 μm. Sirisangtragul et al (2011) melaporkan bahwa efek ekstrak
diklorometan K. galanga L dan komponen utama etil p-metoksisinamat
(EPMS) menunjukan aktivitas mikrosomal hepatic pada enzim sitokrom
silico (komputasi), yakni : Hubungan Kuantitatif Struktur Aktivitas
(HKSA) dan Penambatan Molekul (Molecular Docking).
Hubungan Kuantitatif Aktivitas Struktur Aktivitas adalah pendekatan yang menghubungkan struktur dan akvitas biologi didalam tubuh yang dinyatakan secara matematis. Metode HKSA yang banyak diketahui adalah Metode Free-Wilson dan Hansch. Namun, metode yang banyak digunakan adalah metode Hansch, dimana metode lebih sederhana; konsepnya secara langsung berhubungan dengan prinsip-prinsip kimia fisika organik yang sudah ada; data parameter sifat fisika kimia substituen sudah banyak tersedia; penggunaan pendekatan model Hansch telah banyak menjelaskan hubungan struktur – aktivitas suatu turunan obat (Siswandono, 2000). Interaksi dari suatu ligan terhadap molekul dapat dilakukan dengan metode penambatan molekul.
Penambatan molekul merupakan metode yang memprediksi satu atau dua molekul ketika mengikat satu sama lain membentuk komplek stabil yang digunakan untuk memprediksi kekuatan ikatan atau afinitas bidding
antara dua molekul digunakan untuk penentuan nilai sampel (Bachwani Mukesh et al, 2011). Pada penelitian ini menggunakan senyawa etil p
-metoksisinamat yang dimodifikasi dengan amidasi, kemudian dilakukan analisa hubungan kuantitatif struktur aktivitas dengan pendekatan Hansch dilanjutkan dengan penambatan molekul. Metode penambatan molekul ini dipilih karena secara cepat meramalkan atau memprediksi aktifitas ligan yang ditambatkan melalui hasil scoring dari tiap-tiap ligan sehingga hasil
yang didapat lebih memudahkan membandingkannya. Penelitian ini diharapkan mampu memberikan gambaran dan membandingkan interaksi antara senyawa amidasi etil p-metoksisinamat (EPMS) dengan COX-2.
1.2. Rumusan Masalah
a. Apakah metode pendekatan Hansch dapat menunjukan hubungan kuantitatif struktur aktivitas antiinflmasi dari struktur senyawa amidasi etil p-metoksisinamat ?
b. Apakah senyawa dari proses amidasi etil p-metoksisinamat memiliki
c. Bagaimanakah perbandingan aktivitas dari masing-masing molekul ligan senyawa amidasi etil p-metoksisinamat terhadap enzim
siklooksigenase-2 (COX-2) ?
1.3. Hipotesis
Parameter Hidrofobik (Log P), Elektronik (EHOMO, ELUMO,
ΔEHOMO-LOMO, Polarisabilitas), dan Sterik (Indeks Harary, Indeks Randic, Molar
refraksi) mempunyai pengaruh terhadap aktivitas antiinflamasi.
1.4. Tujuan Penelitian
a. Memperoleh model persamaan HKSA Hansch dan prediksi aktivitas senyawa amidasi etil p-metoksisinamat.
b. Menganalisis interaksi penambatan molekul ligan senyawa amidasi etil
p-metoksisinamat terhadap enzim COX-2.
1.5. Manfaat Penelitian
4 BAB II
TINJAUAN PUSTAKA
2.1. Hubungan Kuantitatif Struktur – Aktivitas (HKSA)
Aktivitas biologis suatu obat diperoleh setelah terjadi interaksi senyawa dengan molekul spesifik dalam objek biologis. Interaksi tersebut ditunjangn dengan spesifitas sifat kimia fisika senyawa yang tinggi. Aktivitas obat berhubungan dengan sifat kimia obat, dan merupakan fungsi dari struktur molekul obat. Hubungan struktur kimia dan aktivitas biologis yang tidak baik dapat disebabkan oleh kurang baiknya metode penelitian yang digunakan. Konsep bahwa aktivitas biologis suatu senyawa berhubungan dengan struktur kimia, pertama kali dikemukakan oleh Crum, Brown dan Fraser pada tahun 1869.
Hubungan kuantitatif struktur kimia dan aktivitas biologis obat merupakan bagian terpenting rancangan obat, dalam usaha mendapatkan suatu oobat baru dengan aktivitas yang lebih besar, keselektifan yang lebih tinggi, toksisitas atau efek samping sekecil mungkin dan kenyamanan yang lebih besar. Selain itu dengan menggunakan model HKSA, akan lebih menghemat biaya atau lebih ekonomis, karena untuk mendapatkan obat baru dengan aktivitas yang dikehendaki (Siswandono, 2000).
Kajian hubungan kuantitatif struktur aktivitas (HKSA) menjabarkan suatu model persamaan yang menghubungkan ketergantungan harga aktivitas suatu senyawa secara eksperimen dengan struktur molekul. Menurut Kubinyi, struktur suatu senyawa tersebut dapat direpresentasikan sebagai parameter fisik dan kimiawi (analisis Hansch), variable indikator (analisis Free-Wilson) atau dengan peninjauan sifat molekul secara tiga dimensi (HKSA – 3D) (Tahir et al, 2003).
A. Model Pendekatan Free-Wilson
Free dan Wilson (1964), mengembangkan suatu konsep hubungan struktur dan aktivitas biologis obat, yang dinamakan model
de novo atau model matematika Free-Wilson. Mereka
aktivitas dari gugus-gugus substituent terhadap aktivitas biologis senyawa induk, yang dinyatakan melalui persamaan :
Metode Free-Wilson digunakan jika cara kerja obat tidak diketahui, uji biologis lambat daripada sintesis senyawa turunannya, dan atau sifat-sifat fisika kimia substituen tidak diketahui. Model ini didasarkan pada perkiraan bahwa masing-masing substituen pada struktur senyawa induk memberikan sumbangan tetap pada aktivitas bilogis. Perkiraan dasar pada model Free-Wilson adalah semua obat yang diuji harus mempunyai struktur induk sama dan substituen harus memberikan aktivitas biologis secara aditif dalam kedudukan yang sama dengan jumlah tetapan yang bebas dari ada atau tidaknya substituen (Leach, 1996).
Model de novo ini kurang berkembang karena tidak dapat
digunakan bila efek substituent bersifat tidak linier atau bila ada interaksi antar substituent. Selain itu model ini memerlukan banyak senyawa dengan kombinasi substituen yang bervariasi untuk dapat menarik kesimpulan yang benar. Meskipun demikian model ini juga mempunyai keuntungan karena dpat menghubungan secara kuantitatif struktur kimia dan aktivitas biologus dari turunan senywa dengan bermacam-macam gugus substituent pada berbagai zona (Siswandono, 2000).
B. Model Pendekatan HKSA Hansch
Hansch (1963) mengemukakan suatu konsep bahwa hubungan struktur kimia dengan aktivitas biologi (log 1/C) suatu turunan senyawa dapat dinyatakan secara kuantitatif melalui parameter-parameter sifat kimia fisika dari substituent yaitu
parameter hidrofobik (π), eletronik (σ), dan sterik (Es). Model pendekatan ini disebut model hubungan energy bebas linier (linier
free energy relationship = LFER) atau pendekatan ekstra
Log 1/C = a Σ π + b Σ σ + c Σ Es –d
C : Kadar untuk respon biologis baku
Σ π, Σ σ dan Σ Es : Sumbangan sifat-sifat lipofilik, eletronik dan sterik dari gugus-gugus terhadap sifat-sifat senyawa induk yang berhubungan dengan aktivitas biologis.
a, b, c dan d : Bilangan (tetapan) yang didapat dari perhitungan analisis regresi linier.
Dalam hubungan struktur-aktivitas, model Hansch lebih berkembang dan lebih banyak digunakan dibanding model de novo
Free-Wilson oleh karena: a) Lebih sederhana
b) Konsepnya secara langsung berhubungan dengan prinsip-prinsip kima fisika organic yang sudah ada
c) Data parameter sifat kimia fisika substituent sudah banyak tersedia dalam tabel-tabel.
d) Penggunaan pendekatan model Hansh telah banyak menjelaskan hubungan struktur dan aktivitas suatu turunan obat.
Parameter sifat kimia fisika yang digunakan dalam pemodelan HKSA Hansch adalah parameter hidrofobik (π), elektronik (σ) dan sterik (Es).
a. Parameter hidrofobik
Karakter hidrofobik suatu obat dapat dinilai secara eksperimen dengan menguji sebaran distribusi obat didalam campuran n-oktanol/air. Molekul hidrofobik akan lebih
terlarut dalam lapisan n-oktanol dalam sistem dua fase, dimana
molekul hidropilik akan lebih ke lapisan air. Distribusi relatif diketahui sebagai koefisien pastisi (P) dan diperoleh dari suatu persamaan:
Senyawa hidrofobik dengan nilai P tinggi, dan dimana senyawa hidrofilik mempunyai nilai P rendah. Variasi substituen pada senyawa penuntun akan memproduksi seri analog yang mempunyai perbedaan hidrofobisitas dan perbedaan nilai P. Dengan memplot atau membandingkan nilai P dengan aktivitas biologis obat, maka mungkin untuk melihat jika adanya hubungan antara kedua sifat tersebut. Normalnya aktivitas obat ditunjukan sebagai 1/C, dimana C adalah konsentrasi obat yang diperlukan untuk mencapai tingkat aktivitas biologis. Hubungan timbal-balik konsentrasi (1/C) digunakan, sejak obat yang lebih aktif akan mencapai aktivitas biologis pada konsentrasi yang rendah (Patrick, 2009).
Pada grafik (gambar 2.1) plot log (1/C) dengan log P,
dimana rentang nilai log P adalah terbatas pada rentang yang kecil (log P = 1 – 4), garis lurus pada grafik yang diperoleh
menunjukan bahwa hubungan antara hidrofobisitas dan aktivitas biologis.
Gambar 2.1. Hubungan antara aktivitas biologis dengan log P
Parameter hidrofobik (lipofilik) yang sering digunakan dalam HKSA antara lain adalah logaritma koefisien partisi
(log P), tetapan π Hansch, tetapan fragmentasi f Rekker -Mannhold dan tetapan kromatografi Rm.
b. Parameter elektronik
elektronik memungkinkan mempunyai efek bagaiman obat dengan mdah melewati membran sel atau seberapa kuat efek tersebut dapat berinteraksi dengan lokasi ikat. Untuk itu efek tersebut berguna untuk menilai efek elektronik pada substituen. Deskriptor elektronik telah banyak digunakan untuk membuat persamaan HKSA maupun HKSS (Hubungan Kuantitatif Sifat-Struktur). Deskriptor tersebut dibedakan dari nilai tunggal konstanta elektronik substituen yang diberikan senyawa.
Jumlah deskriptor elektronik dapat dibedakan berdasarkan dari efek atau kekuatan interaksi intermolekular. Secara luas dikenal dari kekuatan interaksi intermolekulat mengikuti: ion-ion, ion-dipol, dipol-dipol, dipol-induksi dipol, dispersi, dan ikatan hidrogen.
Interaksi ion telah dikodekan didalam studi potensi obat melalu penggunan konstanta ionisasi. Sebagai deskriptor, konstanta ionisasi menyajikan informasi tentang tingkat ionisasi, yang diketahui termasuk absorbsi dan distribusi dari obat. Menurut Lien et al yang meriview penggunaan deskriptor pada HKSA bahwa momen dipole menyandikan kekuatan interaksi kepolaran.
Molekular polarisabilitas dan refraksi molar mempunyai kedekatan hubungan sifat pengukuran pada kerentanan molekul menjadi polar. Deskriptor tersebut sering digunakan pada kondisi dimana dipol-induksi dipole dan dispersi memainkan peranan penting dalam interaksi. Indeks reaktifitas biasanya dikategorikan sebagai elektrofilik atau nukleofilik tergantung dari kereaktifan dari tarikan yang melibatkan serangan elektrofilik atau nukleofilik.
trmodinamik dan momen dwikutub tetapi hanya metode kimia kuantum yang dapat memperkirakan muatan-muatan atom, energi orbital molekul, dan beberapa deskriptor elektronik lainnya dalam studi HKSA. Metode kimia kuantum dapat diaplikasikan dalam HKSA dengan menurunkan deskriptor elektronik secara langsung dari fungsi gelombang molekular (Katritzky et al, 1996).
Energi HOMO (Highest Occupied Molecul Orbital) dan
LUMO (Lowest Occupied Molecul Orbital), merupakan
deskriptor yang sangat populer dalam kimia kuantum. Orbital-orbital ini memainkan peran yang sangat penting dalam menentukan berbagai reaksi kimia dan dalam penentuan celah pita elektronik. Energi HOMO berhubungan langsung dengan potensial ionisasi dan sifat kerentanan molekul dalam penyerangan terhadap elektrofil. Sedangkan LUMO berhubungan dengan afinitas elektron. Selisih antara energi HOMO dan LUMO (celah HOMO-LUMO) penting dalam penentuan ukuran stabilitas molekul. Molekul dengan celah HOMO-LUMO yang besar berarti molekul tersebut memiliki stabilitas yang tinggi, sehingga memiliki reaktivitas yang rendah dalam reaksi-reaksi kimia. Celah ini juga digunakan pada perkiraan energi eksitasi terendah molekul (Katritzky et al, 1996).
Ada tiga jenis sifat elektronik yang digunakan dalam HKSA model LFER Hansch, yaitu :
1. Pengaruh berbagai substituent terhadap reaktivitas bagian molekul yang tidak mengalami perubahan.
2. Sifat elektronik yang berikatan dengan tetapan ionisasi (pKa) dan berhubungan dengan bentuk terionkan dan tak terionkan dari suatu senyawa pada pH yang tertentu. 3. Sifat oksidasi-reduksi atau reaktivitas senyawa.
Bulk, ukuran dan bentuk suatu obat akan mempengaruhi bagaimana obat mudah berikatan dan berinteraksi dengan situs aktif. Substituen bulk dapat bertindak sebagai pelindung yang cocok berinteraksi antara obat dan situs aktifnya. Sebagai alternatif, substituen bulk dapat membantu obat berorientasi dengan maksimum pada situs aktif dan meningkatkan aktivitas. Sifat sterik sangat sulit untuk dihitung dibanding sifat hidrofobik dan elektronik. Perhitungan sifat sterik bisa
dilakukan dengan metode molar refraksi, faktor sterik Taft’s,
parameter sterik Verloop dan indeks topologi (Patrick, 2009). Deskriptor yang digunakan pada penelitian ini adalah indeks topologi dan refraksi molar (MR). Indeks topologi banyak digunakan sebagai deskriptor struktur pada model hubungan kuantitatif struktur-aktifitas (HKSA) dan hubungan kuantitatif sifat-struktur (HKSS). Indeks topologi menawarkan cara yang mudah dalam pengukuran cabang molekul, bentuk, ukuran, siklisitas, simetri, sentrisitas, dan kompleksitas (Devillers, 1997). Indeks topologi menjelaskan bahwa suatu struktur kimia, disebut sebagai grafik kimia, yaitu suatu model kimia yang digunakan untuk menjelaskan sifat interaksi antara obyek-obyek kimia (atom, ikatan, gugusan atom, molekul, pasangan molekul, dan sebagainya). Pada penelitian ini digunakan, yakni: Indeks Randic dan Indeks Harary dan Molar Refraksi (MR).
a. Indeks Harary
Indeks Harary yang dinyatakan dengan H
dengan lainnya daripada situs-situs yang letaknya berdekatan.
b. Indeks Randic
Indeks Randic atau indeks konektivitas molekular Randic sangat mirip dengan indeks Zagreb, namun lebih dapat diterima dan digunakan secara luas. Sesuai dengan definisi yang diberikan, maka semakin rapat grafik, maka
akan semakin rendah harga χ (Ivanciuc dan Balaban,
1998).
c. Molar refraksi (MR)
Selain itu, pengukuran sterik yang diketahui dengan refraksi molar. MR mengukur volume yang diisi oleh suatu atom atau gugus atom. MR diperoleh dari persamaan:
Dimana n adalah indeks refraksi, MW adalah berat
molekul, dan d adalah berat jenis. MW/d didefinisakn
sebagai volume, dan (n2 – 1)/(n2 + 2) merupakan faktor
koreksi yang didefinisikan bagaimana suatu substituen dapat dengan mudah berpolar. Faktor koreksi menunjukan
signifikan jika substituen memiliki π elektron atau
pasangan elekron bebas (Patrick, 2000). Tetapan sterik substituent dapat diukur berdasarkan sifat meruah gugus-gugus dan efek gugus-gugus pada kontak obat dengan sisi reseptor yang berlekatan.
2.2. Analisis Statistik HKSA model Hansch
SPSS, MICROSAT, ABSTAT, QSAR, STATGRAPICH, SIGMASTAT, atau program statistik lain (Siswandono. 1995).
Penggunaan analisa statistik pada HKSA bertujuan untuk melihat hubungan atau pengaruh deskriptor terhadap aktivitas dan hubungan antara deskriptor dengan aktivitas adalah linier. Analisa regresi merupakan suatu model matematis yang dapat digunakan untuk mengetahui bentuk hubungan anatara dua atau lebih variabel. Tujuan analisa regresi adalah untuk membuat perkiraan (prediksi) nilai suatu variabel bebas dengan variabel terikat (Sutanto. 2011). Regresi linier merupakan persamaan yang melibatkan dua variabel bebas dan terikat. Metode analisa regresi dibagi menjadi dua yaitu analisa regresi linier sederhana dan analisa regresi berganda/multilinier atau analisa multi regression linier.
Analisa statistik Multiple Linier Regression (MLR) merupakan
suatu analisa statistik yang melibatkan dua atau lebih variabel bebas (independen) terhadap satu variabel terikat (dependent). Analisa suatu
persamaan regresi ditentukan oleh beberapa kriteria statistik untuk memperoleh keabsahan atau validitas persamaan yang diperoleh, yakni: 1. Nilai r (koefisien korelasi) menunjukan tingkat hubungan antara data
aktivitas biologis pengamatan percobaan dengan data hasil perhitungan berdasarkan persamaan yang diperoleh dari analisis regresi. Koefisien korelasi adalah angka yang bervariasi mulai dari -1 sampai 1. Semakin tinggi nilainya semakin baik hubungannya. Untuk mendapatkan nilai korelasi yang dapat diterima tergantung jumlah data penelitian. Semakin banyak jumlah data semakin rendah koefisien korelasi atau nilai r yang dapat diterima.
2. Nilai r2menunjukan berapa % aktivitas biologis yang dapat dijelaskan
hubungannya dengan parameter sifat kimia fisika yang digunakan. Contoh : suatu hubungan yang mempunyai koefisien korelasi (r) = 0.990 berarti dapat menjelaskan (0.990)2 x 100% = 98 % dari antar data.
3. Nilai F menunjukan kemaknaan hubungan bila dibandingkan dengan
yang dinyatakan oleh persamaan yang didapat, adalah benar atau merupakan kejadian kebetulan.
4. Nilai t menunjukan perbedaan koefisien regresi a, b, c dan d dari
persamaan regresi bila dibandingkan dengan tabel t.
5. Nilai SE (simpang baku) menunjukan nilai variasi kesalahan dalam
percobaan.
6. PRESS (Prediction Residual Sum of Square) menggambarkan suatu persamaan dapat memprediksi aktivitas. Semakin kecil suatu nilai PRESS pada suatu persamaan atau model maka dipilih sebagai persamaan terbaik untuk memprediksi nilai aktivitas.
2.3. Asam Sinamat
Dalam kimia biologi, asam sinamat merupakan kunci kunci intermediet pada jalur sikimat dan phenylpropanoid. Asam sikimat merupakan precursor dari banyak turunanan alkaloid, asam amino aromatic, dan indol. Asam sikimat ditemukan dalam bentuk bebas, dan terutama dalam bentuk ester (etil, cinamil, benzyl), dalam jenis minyak esensial, resin dan balsam, minyak cinnamon, balsam Peru dan balsam Tolu, dll. Asam sinamat memainkan peran vital dalam sintesis senyawa penting. Sebagai contoh, turunan asam sinamat dapat diubah menjadi senyawa yang penting termasuk stiren dan stilbn melalui reaksi dekarboksilasi. Turunan asam sinamat dikategorikan berdasarkan profil farmakologinya, yakni : Anti TB, antidiabetis, antioksidan, antimikroba, hepatoprotektif, despresan CNS, Antikolesterolemik, antijamur dan fungitoksik, antihiperglikemik, antimalaria, antiviral, anxiolitik, sitotoksik, antiinflamasi (Sharma, 2011).
Beberapa turunan asam sinamat mempunyai aktivitas antiinflamasi yang telah banyak diketahui, yakni: Etil p-metoksisinamat, turunan caffeic
acid, turunan ferulic acid, turunan hidroksisinamat, dll. Berikut turunan asam sinamat yang memiliki aktivitas antiinflamasi yang diperoleh dari penelitian yang dilakukan Nguyen et al [1] (2015), Liu et al [2] (2014), dan
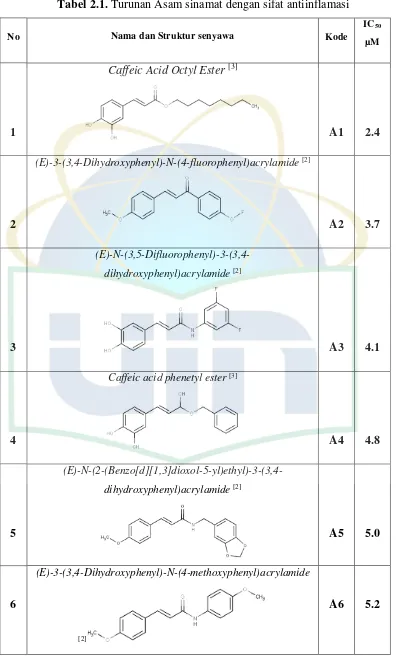
Tabel 2.1. Turunan Asam sinamat dengan sifat antiinflamasi
No Nama dan Struktur senyawa Kode IC50
µM
1
Caffeic Acid Octyl Ester [3]
A1 2.4
2
(E)-3-(3,4-Dihydroxyphenyl)-N-(4-fluorophenyl)acrylamide [2]
A2 3.7
3
(E)-N-(3,5-Difluorophenyl)-3-(3,4-dihydroxyphenyl)acrylamide [2]
A3 4.1
4
Caffeic acid phenetyl ester [3]
A4 4.8
5
(E)-N-(2-(Benzo[d][1,3]dioxol-5-yl)ethyl)-3-(3,4-dihydroxyphenyl)acrylamide [2]
A5 5.0
6
(E)-3-(3,4-Dihydroxyphenyl)-N-(4-methoxyphenyl)acrylamide
[2]
7
(E)-N,N-Dibutyl-3-(3,4-dihydroxyphenyl)acrylamide [2]
A7 6.1
8
(E)-N-(2-(1H-Indol-3-yl)ethyl)-3-(3,4-dihydroxyphenyl)acrylamide [2]
A8 6.7
9
(E)-3-(3,4-Dihydroxyphenyl)-N-(3-(trifluoromethyl)phenyl)acrylamide [2]
A9 7.9
10
Caffeic acid butil ester [3]
A10 8.4
11
Caffeic acid benzyl ester [3]
A11 10.7
12
Caffeic acid ethyl ester [3]
13
1-O-caffeoylglycerol [1]
A13 18.5
14
Caffeic acid methyl ester [1]
A14 21.4
15
Caffeoylglycolic acid methyl ester [1]
A15 29
2.4. Etil p-metoksisinamat
Etil p-metoksisinamat (EPMS) merupakan salah satu senyawa yang
diperoleh dari rimpang kencur (Kaemferia galanga L.), dan telah banyak
digunakan sebagai pengobatan nyeri dan peradangan, senyawa ini juga menunjukan aktivitas penghambat proliferasi sel tumor pada jaringan epidermis tikus dan papiloma (Ekowati et al, 2012). EPMS termasuk
kedalam senyawa ester yang mengandung cincin benzene dan gugus metoksi yang bersifat nonpolar dan juga gugus karbonil yang mengikat etil yang bersifat sedikit polar (Rosbina, 2009). EPMS telah dilaporkan mempunyai anti-tuberkolosis, nematisidal, penolak nyamuk, larvasidal, antineoplastic dan potensi anti microbial (Umar et al, 2014).
2.5. Ester
Ester adalah suatu senyawa organik yang terbentuk melalui pergantian satu (atau lebih) atom hidrogen pada gugus karboksil dengan suatu gugus organik. Kebanyakan ester tersebar luas pada semua senyawa alam. Sebagai contoh, metil butanoat ditemukan pada minyak nanas dan isopentil asetat merupakan senyawa pokok minyak pisang (Mc Murry, 2008). Penamaan ester terdiri dari dua kata, kata pertama adalah nama gugus alkil yang terikat pada oksigen ester sedangkan kata kedua berasal dari nama asam karboksilatnya, dengan membuang kata asam (Inggris: -ic acid
menjadi –ate) (Siswandono, 2000). Pada dasarnya ester merupakan asam
karboksilat dengan menghilangkan gugus hidrogen dan digantikan oleh gugus R dan ester merupakan senyawa yang mempunyai aroma yang enak dan aroma yang tercium dari buah-buahan, misalnya : propil pentanoat (nanas), etil butanoat (Winter, A., 2005).
Gambar 2.3, Struktur umum senyawa ester
Esterifikasi adalah reaksi pembentukan ester. Reaksi ini dapat dilakukan dengan berbagai cara:
1. Reaksi antara asam karboksilat dengan alcohol
RCOOH + R’OH → RCOOR’ + H2O 2. Reaksi antara halide asam dengan alcohol
RCOCl + R’OH → RCOO’R + HCl
3. Reaksi antara anhidrida dan alcohol (RCO)2O + R’OH → RCOOR’ + RCOOH
4. Reaksi antara suatu karboksilat dan alkil halid relatif
RCOOH + R’X → RCOOR’ + HX
2.6. Amida
Suatu amida ialah suatu senyawa yang mempunyai nitrogen trivalent yang terikat pada suatu gugus karbonil. Suatu amida diberi nama dari asam
karboksilat induknya, dengan mengubah imbuhan asam …-oat (atau –at)
menjadi –amida.
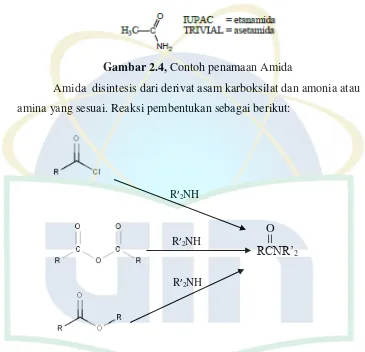
Gambar 2.4, Contoh penamaan Amida
Amida disintesis dari derivat asam karboksilat dan amonia atau amina yang sesuai. Reaksi pembentukan sebagai berikut:
Gambar 2.5. Reaksi pembuatan amida (Sumber: Fessenden & Fessenden, 1999)
Reaksi pembentukan amida dapat dilakukan secara industry maupun secara laboratorium. Amida asam lemak pada industri oleokimia dapat dibuat dengan mereaksikan asam lemak atau metil ester dengan suatu amina (Maag, 1984). Amida asam lemak dibuat secara sintesis pada industri oleokimia dalam proses batch, dimana ammonia dan asam lemak bebas
bereaksi pada suhu 200oC dan tekanan 345 – 690 kpa selama 10 – 12 jam.
Dengan proses tersebutlah dibuat amida primer seperti lauramida, stearamida, dll.
R’2NH R’2NH R’2NH
RCNR’2
Amida primer juga dibuat dengan mereaksikan ammonia dengan metil ester asam lemak. Reaksi ini mengikuti konsep HSAB dimana H+dari
ammonia merupakan hard acid yang mudah bereaksi dengan hard base
CH3O- untuk membentuk metanol. Sebaliknya NH2- lebih soft-base
dibandingkan dengan CH3O- akan terikan dengan R-CO- yang lebih soft
acid dibandingkan H+ membentuk amida.
Gambar 2.6. Reaksi pembuatan amina primer
Pembuatan amida sekunder dilakukan dengan mereaksikan asam lemak dengan amina.
Gambar 2.7. Reaksi pembuatan amina sekunder
Senyawa amina yang digunakan untuk reaksi tersebut antara lain etanolamin, urea, anilin, dietanolamin, asetamid, dll yang jika direaksikan dengan asam lemak ada suhu tinggi, 150o C – 200oC akan membentuk suatu
amida dan melepaskan air.
Senyawa amida mempunyai banyak kegunaan dalam bidang-bidang tertentu, salah satu contoh yang paling nyata adalah senywa sulfonamida. Sulfonamida adalah suatu senyawa kemoterapeutik yang digunakan didalam pengobatan untuk mengobati bermacam-macam penyakit infeksi, antara lain disentri baksiler yang akut, radang usus dan untuk mengobati infeksi yang telah resisten terhadap antibiotikan (Nuraini, W., 1998) dan juga N-Steroyl Glutamida yang berguna sebagai surfaktan dan antimikroba (Miranda, 2003).
2.7. Inflamasi
Inflamasi merupakan respon imun yang terjadi secara imunologi saat sel diaktifkan untuk merespon organisme asing asing atau melepaskan antigen yang menghasilkan respon inflamasi akut atau kronik (Kaztung, 2006). Mekanisme pertahanan merupakan bagian dari host yang diketahui membawa reaksi inflamasi seperti pelepasan histamin, bradykinin dan prostaglandin (Siju et al., 2012). Proses inflamasi merupakan suatu
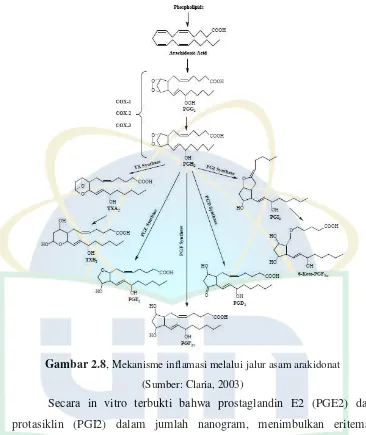
Gambar 2.8, Mekanisme inflamasi melalui jalur asam arakidonat (Sumber: Claria, 2003)
Secara in vitro terbukti bahwa prostaglandin E2 (PGE2) dan protasiklin (PGI2) dalam jumlah nanogram, menimbulkan eritema, vasodilatasi dan peningkatam aliran darah lokal. Histamin dan bradikinin dapat meningkatkan permeabilitas vascular, tetapi efek vasodilatasinya tidak besar. Dengan penambahan sedikit PG, efek eksudasi histamine plasma dan bradikinin menjadi lebih jelas. Migrasi leukosit ke jaringan radang merupakan aspek penting dalam proses inflamasi. (Ganiswarna, 1995).
2.8. Enzim Siklooksigenase 2 (COX-2)
Enzim adalah suatu kelompok protein yang menjalankan dan mengatur perubahan-perubahan kimia dalam sistem biologi, zat ini dihasilkan oleh organ-organ hewan dan tanaman, yang secara katalitik menjalankan berbagai reaksi, seperti pemecahan hidrolisis, oksidasi, reduksi, isomerasi, adisi, transfer radikal dan kadang-kadang pemutusan rantai karbon (Hammes & Hopper, 2005).
Enzim siklooksigenase merupakan enzim yang mengkatalisis pembentukan prostaglandin, suatu mediator inflamasi, dan produk metabolisme asam arakidonat. Enzim COX terdiri dari 2 iso-enzim yaitu COX-1 dan COX-2. Enzim COX-1 ber-sifat konstitutif untuk memelihara fisiologi normal dan homeostasis, sedangkan COX-2 merupakan enzim yang terinduksi pada sel yang mengalami inflamasi oleh sitokin, endotoksin, dan faktor per-tumbuhan (growth factors). COX-2 juga berperan dalam
proliferasi sel kanker. Ekspresi berlebihan COX-2 ditemukan pada kebanyakan tumor.
Penemuan isoform COX-2 membuka lem-baran baru penelitian yang didasarkan pada asum-si bahwa patologis prostaglandin (PG) diproduksi oleh induktif yang isoform, sedangkan fisiologis prostaglandin diproduksi oleh konstitutif COX-1 (Zukhurullah, 2012).
2.9. Protein dan Asam Amino
Asam amino merupakan suatu susunan protein. Protein dari semua spesies, dari bakteri sampai manusia, terdiri dari kumpulan dari 20 asam
amino standar yang sama. Sembilan belas di antaranya adalah asam α-amino dengan gugus amino primer (-NH3+) dan asam karboksilat (karboksil; - COOH) yang terikat pada atom karbon pusat, yang disebut atom α-karbon
(Cα) karena berdekatan dengan gugus karboksil dan juga terikat pada atom Cα yaitu atom hidrogen dan variabel rantai samping atau gugus 'R'. Nama -nama asam amino sering disingkat menjadi tiga huruf atau satu huruf. Contoh: prolin disingkat Pro atau P (Hammes & Hopper, 2005).
tiga gugus tersebut, terdapat juga gugus R yang merupakan rantai samping yang akan membedakan tiap asam amino dalam hal struktur, ukuran, dan muatan listrik. Terdapat 20 jenis asam amino umum yang menyusun protein (Gambar 2.6). Asam amino yang pertama kali ditemukan adalah asparagin pada tahun 1806, sedangkan asam amino yang terakhir kali ditemukan adalah treonin, yang belum teridentifikasi hingga 1938 (Nelson & Cox, 2008).
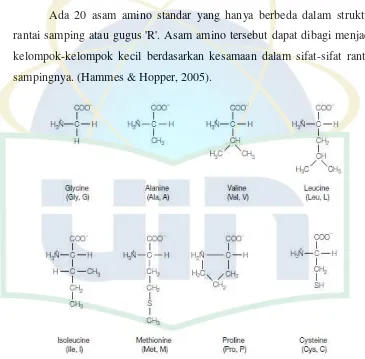
Ada 20 asam amino standar yang hanya berbeda dalam struktur rantai samping atau gugus 'R'. Asam amino tersebut dapat dibagi menjadi kelompok-kelompok kecil berdasarkan kesamaan dalam sifat-sifat rantai sampingnya. (Hammes & Hopper, 2005).
Gambar 2.9. Asam amino alifatik bersifat hidrofobik
Gambar 2.10. Asam amino aromatik bersifat hidrofobik
(Sumber: Hammes & Hopper, 2005).
Gambar 2.11, Asam amino bermuatan bersifat ionik
(Sumber: Hammes & Hopper, 2005).
Gambar 2.12, Asam amino tak bermuatan bersifat polar
(Sumber: Hammes & Hopper, 2005).
sistein juga termasuk dalam struktur primer. Gabungan antara dua struktur primer membentuk struktur protein sekunder. Struktur sekunder protein ini mengacu pada lipatan teratur daerah dari rantai polipeptida. Dua jenis struktur sekunder adalah α-helix dan β-pleated sheet. α-helix berbentuk
silinder, rangkaian heliks asam amino seperti batang dalam rantai polipeptida yang ditahan oleh ikatan hidrogen yang sejajar dengan sumbu helix. Dalam β-pleated sheet, ikatan hidrogen terbentuk antara bagian yang
berdekatan dari polipeptida yang baik berjalan di arah yang sama (β-pleated
sheet paralel) atau dalam arah yang berlawanan (β-pleated sheet
antiparalel). β-membalikkan arah rantai polipeptida dan seringkali ditemukan terhubung dengan ujung β-pleated sheet antiparallel (Hammes &
Hopper, 2005).
Protein dapat diklasifikasikan berdasarkan kelarutan, bentuk, fungsi biologis, atau struktur tiga dimensinya. Berdasarkan fungsi biologis tersebut, protein dapat diklasifikasikan sebagai enzim (dehidrogenase, kinase), protein penyimpanan (feritin, mioglobin), protein pengatur (protein pengikat DNA, hormon polipeptida), protein struktural (kolagen, proteoglikan), protein pelindung (faktor pembekuan darah, imunoglobulin), protein pengangkut (hemoglobin, lipoprotein plasma), dan protein kontraktil/ motil (aktin, tubulin) (Murray et al, 2003).
2.10. Interaksi Protein dengan Ligan A. Ikatan Hidrogen
Ikatan hidrogen adalah interaksi antara atom hidrogen bermuatan positif parsial dalam dipol molekuler dengan elektron tidak berpasangan dari atom lain, baik pada molekul yang sama maupun molekul yang lain. Secara normal, atom hidrogen membentuk ikatan hidrogen hanya dengan satu atom lainnya, namun atom hidrogen yang terikat secara kovalen dengan atom donor elektronegatif dapat berinteraksi membentuk ikatan hidrogen dengan atom akseptor.
pasangannya adalah atom akseptor. Jika salah satu atau kedua atom pada ikatan hidogen bermuatan penuh, maka interaksi keduanya akan lebih kuat. Jika keduanya bermuatan penuh, energi ikatan diantaranya sangat tinggi dan pasangan ion ikatan hidrogen tersebut dinamakan jembatan garam (Petsko & Ringe, 2003).
Secara umum, ikatan hidrogen didasari dengan donor X-H dan akseptor A, yakni X–H---A. Jika ikatan hidrogen diperpanjang di sisi akseptor sebagai X–H---A–Y, sudut akseptor H---A–Y juga dapat didefinisikan (Desiraju & Steiner, 1999).
B. Ikatan Ionik
Ikatan ion terbentuk antara gugus – gugus yang memiliki muatan yang berlawanan dan sangat penting untuk beberapa interaksi ikatan obat-target. Beberapa pengantar pesan kimia alami tubuh berinteraksi melalui ikatan ion (Patrick, 2001).
C. Ikatan van der Waals
Interaksi van der waals adalah interaksi lemah yang muncul diantara gugus – gugus hidrofobik seperti cincin aromatik dan gugus alkil. Interaksi ini muncul disebabkan adanya fluktuasi acak dalam densitas elektron sehingga membentuk daerah sementara yang kaya elektron atau sedikit elektron. Daerah kaya elektron pada satu molekul akan menarik daerah yang elektronnya sedikit pada molekul lain. Interaksi ini lebih lemah dari ikatan ion dan ikatan hidrogen dan melibatkan molekul hidrogen netral (Patrick, 2001).
Energi ikatan van der Waals terbilang kecil, yaitu sekitar 2-4 kJ/mol per-pasang atom (Berg, Tymoczko, & Stryer, 2007). Interaksi van der Waals berkurang ketika jarak antar atom menjauh, maka hanya
atom yang saling berdekatan (hanya terpisah 5 Ǻ atau kurang) yang
memungkinkan terjadinya interaksi ini Interakasi var der Waals yang ada pun biasanya lemah, namun jumlahnya yang banyak pada protein memberikan peran yang cukup besar (Petsko & Ringe, 2003).
Hidrokarbon adalah molekul yang terdiri atas karbon dan hidrogen dan tidak larut dalam air. Ikatan kovalen antara dua atom karbon dan antara atom karbon dan atom hidrogen adalah ikatan nonpolar yang paling umum dalam sistem biologis. Molekul nonpolar tidak mengandung gugus bermuatan, momen dipol, atau terhidrasi, sehingga tidak larut atau hampir tidak larut dalam air. Karenanya, mereka disebut hidrofobik (Lodish, et al., 2008).
Interaksi hidrofobik merujuk pada kecenderungan senyawa nonpolar untuk bergabung satu sama lain dalam lingkungan encer (Murray, Granner, Mayes, & Rodwell, 2003). Molekul nonpolar juga dapat bergabung melalui interaksi van der Waals walaupun lemah. Gabungan antara interaksi hidrofobik dan van der Waals membuat molekul hidrofobik cenderung berinteraksi dengan satu sama lainnya, bukan dengan air. Sederhananya, sesuai kaidah like dissolves like, molekul polar terlarut dalam pelarut polar seperti air, sementara molekul nonpolar terlarut dalam pelarut nonpolar seperti heksan (Lodish, et al., 2008).
2.11. Molecular docking (Penambatan Molekul)
Penambatan molekul atau molecular docking adalah prosedur
komputasional yang digunakan untuk memprediksikan ikatan non-kovalen makromolekul, lebih sering, sebuah molekul besar (reseptor) dan sebuah molekul kecil (ligan) secara efisien, dimulai dari struktur-struktur yang tidak saling berikatan struktur yang ditemukan dari simulasi dinamika molekul, homology modeling, dan lain-lain (Arry Yanuar, 2012). Molecular
docking adalah metode yang memprediksi orientasi sebuah molekul ketika
berikatan satu sama lain membentuk kompleks yang stabil. Orientasi dapat digunakan untuk memprediksi kekuatan asosiasi atau afinitas bidding antara
dua molekul yang digunakan sebagai contoh scoring function. (Bachwani
Mukesh et al, 2011).
penerapannya pada bidang kedokteran. Ligan adalah molekul kecil yang berinteraksi dengan lokasi ikatan protein. Lokasi ikatan adalah daerah protein yang diketahui aktif dalam pembentukkan senyawa. Ada beberapa konformasi mutual yang memungkinkan di mana ikatan dapat terjadi. Hal tersebut dinamakan model ikatan.
Hubungan antara molekul biologis yang relevan seperti protein, asam nukleat, karbohidrat, dan lipid memainkan peran sentral dalam transduksi sinyal. Selanjutnya, orientasi relatif dari dua pasangan yang berinteraksi dapat mempengaruhi jenis sinyal yang dihasilkan. Oleh karena itu docking berguna untuk memprediksi baik kekuatan dan jenis sinyal yang
dihasilkan. Docking sering digunakan untuk memprediksi orientasi ikatan
kandidat obat bermolekul kecil terhadap target proteinnya untuk memprediksi afinitas dan aktivitas molekul kecil. Maka docking memainkan
peran penting dalam desain obat secara rasional (Bachwani Rakesh, 2011). Fokus Penambatan molekul untuk mensimulasikan secara komputasi proses pengenalan molekul. Tujuan dari Penambatan molekul adalah untuk mencapai konformasi yang optimal untuk kedua protein dan ligan serta orientasi relatif antara protein dan ligan sehingga energi bebas dari sistem secara keseluruhan diminimalkan. Proses komputasi mencari ligan yang cocok baik secara geometris dan energi ke situs pengikatan protein ini disebut penambatan molekul. Penambatan molekul membantu dalam mempelajari obat / ligan atau interaksi reseptor / protein dengan mengidentifikasi situs aktif yang cocok pada protein, mendapatkan geometri terbaik dari ligan - kompleks reseptor, dan menghitung energi interaksi dari ligan yang berbeda untuk merancang ligan yang lebih efektif (Bachwani Mukesh, 2011).
docking tergantung pada dua komponen: pencarian algoritma dan fungsi scoring (Bachwani Mukesh, 2011).
Beberapa algoritma penambatan yang umum digunakan antara lain dinamika molekuler, metode Monte Carlo, algoritma genetika,
Fragment-based methods, point complementary methods, distance geometry methods, tabu searches, dan systematic searches. Dua pendekatan yang paling
populer adalah metode Monte Carlo dan algoritma genetika (Kitchen, Decornez, Furr, & Bajorath, 2004).
Setelah melalui beberapa metode algoritma penambatan seperti yang dijelaskan di atas, proses penambatan molekuler dilanjutkan dengan fungsi penilaian untuk memperkirakan energi bebas dari ligan dalam model ikatannya. Fungsi penilaian dikelompokkan menjadi beberapa bagian yaitu berdasarkan empiris, berdasarkan force field, dan berdasarkan pengetahuan (knowledge-based) (Tiikkainen, 2010). Proses penambatan molekuler
menyangkut prediksi konformasi ligan dan orientasi (penentuan posisi) dengan sisi penambatan yang ditargetkan. Aspek teoritis mengenai penambatan molekuler dilakukan dengan memprediksikan posisi suatu ligan [I] pada suatu makromolekul protein [E] dibawah kondisi ekuilibrum (conformational search).
Fungsi scoring dapat memprediksi afinitas ikatan antara makromolekul dengan ligan. Identifikasi ini didasarkan pada beberapa teori seperti teori energi bebas Gibbs. Nilai energi bebas Gibbs yang kecil menunjukkan bahwa konformasi yang terbentuk adalah stabil, sedangkan nilai energi bebas Gibbs yang besar menunjukkan tidak stabilnya kompleks yang terbentuk. Sedangkan penggunaan algoritma berperan dalam penentuan konformasi (docking pose) yang paling stabil dari pembentukan
kompleks (Funkhouser, 2007).
Berdasarkan interaksi yang terjadi, terdapat beberapa jenis
molecular docking, yaitu:
- Docking protein / ligan kecil
- Docking protein / peptida
- Docking protein / nukleotida (Bachwani Mukesh, 2011)
2.12. Protein Data Bank (PDB)
Protein Data Bank (PDB; http://www.rcsb.org/pdb/) adalah sebuah dokumen atau kumpulan data eksperimental struktur tiga dimensi dari makromolekul biologis, yang sekarang berjumlah lebih dari 32.500 (Berman, et al., 2000), termasuk protein dan asam nukleat. Molekul – molekul tersebut adalah molekul yang ditemukan di semua organisme termasuk bakteri, ragi, tanaman, lalat, hewan lain, dan manusia. Informasi ini dapat digunakan untuk membantu menyimpulkan peran struktur dalam kesehatan manusia dan penyakit, dan dalam pengembangan obat. Struktur yang terdapat dalam arsip ini mulai dari protein kecil dan potongan-potongan DNA sampai molekul kompleks seperti ribosom (RCSB, 2014).
2.13. PubChem
PubChem (http://PubChem.ncbi.nlm.nih.gov) adalah gudang informasi molekuler untuk umum, sebuah karya ilmiah dari Institut Kesehatan Nasional Amerika (US National Institutes of Health / NIH). Basis
data PubChem memiliki lebih dari 27 juta catatan struktur kimia khusus dari senyawa yang berasal dari hampir 70 juta senyawa endapan, dan berisi lebih dari 449.000 catatan bioassay dengan lebih dari ribuan biokimia in vitro dan
skrining berbasis sel, dengan menargetkan lebih dari 7000 protein dan gen yang terhubung dengan lebih dari 1,8 juta senyawa (Xie, 2010). Pada situs PubChem ini dapat diunduh struktur kimia dari suatu senyawa secara gratis yang dibutuhkan dalam studi penambatan molekul.
2.14. Autodock
2.15. Autodock Vina
AutoDock Vina adalah salah satu perangkat lunak yang tepat dan dapat diandalkan yang tersedia untuk penemuan obat, penambatan molekul dan skrining virtual yang dirancang dan diterapkan oleh Dr. Oleg Trott. Vina menawarkan fungsi yang beragam, tingkat kinerja tinggi dan meningkatkan akurasi untuk mempermudah penggunaan. Perangkat lunak ini dapat dioperasikan dengan bantuan AutoDockTools (ADT) atau instruksi command line (Sandeep, Nagasree, Hanisha, Murali, & Kumar, 2011).
2.16. Pymol
PyMOL merupakan salah satu program visualisasi yang digunakan untuk memahami suatu struktur biologi dan dapat menampilkan gambar tiga dimensi yang berkualitas dan mampu menyajikan tampilan struktur dalam beberapa warna dari suatu molekul kecil maupun makromolekul seperti protein. Visualisasi sangatlah penting untuk lebih memahami dan mendalami struktur suatu molekul. Perangkat lunak ini dikomersilkan oleh DeLano Scientific LLC (Delano & Bromberg, 2004).
2.17. Marvin Skecth
32 BAB III
METODE PENELITIAN
3.1. Tempat dan Waktu Penelitian
Penelitian dilaksanakan bertempat di Fakultas Kedokteran dan Ilmu Kesehatan (FKIK) Universita Islam Negeri Syarif Hidayatullah Jakarta dan di Lembaga Ilmu Pengetahuan Indonesia (LIPI) Serpong selama bulan Februari hingga Mei 2015.
3.2. Alat
3.2.1. Perangkat Keras
Notebook Acer (4750z Aspire series) dengan spesifikasi Intel®
pentium® CPU (B940 @ 2.00GHz (2 CPUS), ~2.00 GHz), RAM (Random
Access Memory) 2.00 gigabyte, dan Graphic Card (Intel® HD Graphics
Family) 798 megabyte. Notebook terhubung dengan AC/DC adapter dan
terkoneksi internet.
3.2.2. Perangkat Lunak
Sistem operasi menggunakan Windows 7 Ultimate 32 bit, Autodock Tools, Python 2.5.2 dan MGLTools 1.5.6 (Scripps Research Institute),
Discovery Studio 3.5 Visualizer (Accelrys Enterprise Platform),
Hyperchem 8.0, Open Babel 2.3.2, Autodock Vina, Pymol (De Lano
Scitientific LLC), SPSS 16.0.0, LigPlot+ 1.4.5, Marvin Sketch 5.5.1.0
(http://www.chemaxon.com), ACD/Labs 2012 (www.acdlabs.com), Protein
Data Bank (http://www.rcsb.org/pdb).
3.3. Bahan
3.3.1. Training Set dan Test Set
Training set dan test set didapatkan dari literatur dari pengujian
secara in vitro. Data training set dan test yang digunakan harus seragam dari
segi jenis pengujian, aktivitas dan kemiripan struktur.
3.3.2. Molekul Tiga Dimensi (3D)
3.3.3. Struktur Tiga Dimensi (3D) Ligan Amidasi EMPS
Ligan yang digunakan adalah ligan dari amidasi etil p-metoksisinamat (EPMS) yang dibuat dengan Marvin Sketch dengan format
.mol.
3.4. Cara Kerja
3.4.1. Penyiapan Model HKSA
a. Pemodelan Training Set dan Test Set
Training set dan test set yang didapatkan dari literatur dan dibuat ke dalam bentuk 2 dimensi menggunakan Marvin Skecth, kemudian optimasi ke dalam bentuk 3 dimensi pada menu structure→ clean 3d
dan disimpan kedalam format .mol. Training set yang digunakan untuk
membangun persamaan sebanyak 11 struktur yang dipilih secara acak dan sisanya digunakan untuk Test set untuk mevalidasi persamaan.
b. Pemilihan Deskriptor
Pemilihan deskriptor berdasarkan parameter hidrofobitas, parameter elektronik, dan parameter sterik. Parameter hidrofobik menggunakan deskriptor Log P, parameter elektronik menggunakan descriptor EHOMO, ELUMO, Selisih EHOMO-LUMO dan Polarisabilitas,
parameter sterik menggunakan deskriptor indeks topologi menggunakan indeks Randic dan Harary serta molar refraksi (MR). Kemudian, masing-masing training set dan test dihitung nilai deskriptor menggunakan software Marvin Skecth untuk menghitung deskriptor log
P dan indeks topologi, ACD Labs untuk menghitung MR dan
Polarisabilitas dan Hyperchem 8.0 untuk menghitung EHOMO dan ELUMO.
c. Analisa Korelasi Statistik
Nilai dari tiap-tiap deskriptor dari training set yang sudah
dihitung (variabel bebas), kemudian dianalisa korelasi atau hubungannya dengan nilai aktivitas biologis (variabel tergantung) pada tingkat kepercayaan 95% (0.05) dengan menggunakan software SPSS 16.0.0. Analyze → correlate → bivariate
d. Analisa Multiple Linies Regression (MLR)
Rekapitulasi nilai dari tiap-tiap deskriptor training set dan nilai
di program SPSS 16.0.0. Masukan varibel dependent adalah aktivitas
biologis dan variabel independent adalah deskriptor Setelah itu dilakukan analisa multiregresi untuk mendapatkan prediksi model dengan metode backward. Pemilihan akhir model ditentukan dengan
nilai R dan R2> 0.8, Fhit > Ftab. Analyze→ regression →linier.
e. Validasi Persamaan HKSA
Validasi persamaan HKSA dengan menggunakan test set untuk
menghitung nilai dari RMSD (Root Mean Square Deviation) < 1 dan
PRESS (Prediction Residual Sum of Square) < 1.
3.4.2. Penambatan Molekul
A. Penyiapan Struktur Molekul COX-2
Pengunduhan makromolekul COX-2 dari Bank Data Protein melalui situs http://www.rcsb.org/pdb/. Identitas molekul yaitu 1CX2. Data makromolekul diunduh dalam format text (gz).
1. Pemisahan Makromolekul Air dan Ligan
Makromolekul protein yang telah diunggah, dipisahkan dari ligan dan pelarut dan molekul air. Pemisahan menggunakan Discovery
Studio 3.5 Visualizer. Setelah dipisahankan, kemudian simpan dalam
format .pdb.
2. Optimasi Molekul
Optimasi makromolekul dilakukan dengan menggunakan Autodock Tool dan buka makromolekul yang disimpan dalam format
.pdb (file → read molecule→ .pdb).
3. Menentukan Lokasi Penambatan Molekul – Ligan
Penentuan lokasi penambatan molekul dilakukan berdasarkan jurnal atau buku referensi dengan menggunakan Autodock Tools. Pengaturan dilakukan dengan grid box (grid→ grid box) yang meliputi
ukuran (size x, y, z), kordinat (center x, y, z) dan, besarnya ukuran
(amstrong) dan simpan (file → close saving current).
B. Penyiapan Struktur Tiga Dimensi (3D) Ligan
Ligan yang digunakan adalah Ibuprofen diunggah melalui PubChem
amidasi yang dibuat dengan menggunakan Marvin Sketch yang disimpan
dengan format .pdb.
Struktur ligan yang telah dibuat, kemudian dioptimasi dengan menggunakan Autodock Tools. Kemudian, buka ligan yang telah dibuat
(ligand → input → open), setelah itu simpan dalam bentuk .pdbqt (ligand
→ output → save as pdbqt →save).
C. Penambatan Molekul dengan Autodock Vina
Ligan dan Protein yang telah tersimpan dalam format .pdbqt dikopi atau dipindah kedalam folder Vina. Kemudian buat konfigurasi file vina
yang diketik pada notepad yang disimpan dengan nama conf.txt. Jalankan
Vina melalui Command prompt.
D. Analisa dan Visualisasi Penambatan Molekul
Hasil kalkulasi penambatan dilihat pada output dalam format
out.pdbqt atau bentuk notepad. Hasil docking dilakukan dengan memilih
ligan yang memiliki energi ikatan yang paling rendah, nilai ikatan dapat
dilihat di ‘log.txt’.
Posisi ligan-ligan pada makromolekul, serta asam amino yang terikat pada ligan divisualisasikan dengan perangkat lunak PyMol untuk
melihat kecocokan bentuk dan volume antara ligan dan situs tambatanya.
E. Analisa Interaksi Ligan dan Molekul
Makromolekul dan output dalam bentuk .pdbqt dibuka dengan
menggunakan Wordpad. Kopi isi dalam output.pdbqt dan tambahkan
kedalam makromolekul dan simpan dalam format .pdb.
Visualisi interaksi makromolekul dan ligan dengan menggunakan
Ligplot untuk melihat kekuatan interaksi dan ikatan pada asam amino dalam
36 BAB IV
HASIL DAN PEMBAHASAN
4.1. Hubungan Kuantitatif Struktur-Aktivitas (HKSA) 4.1.1. Pemilihan Data Set
Data set yang digunakan harus memenuhi beberapa parameter agar data yang digunakan seragam, parameter tersebut adalah keseragaman pengujian (bahan dan cara pengujian), keseragaman aktivitas, dan senyawa yang diuji (turunan asam sinamat). Data turunan asam sinamat yang digunakan adalah berasal dari hasil penelitian secara in vitro yang dilakukan
oleh Nguyen et al [1] (2015), Liu et al [2] (2014), Da Cunha et al [3] (2004)
terhadap penghambatan aktifitas inflamasi atau konsentrasi hambat 50% (IC50). Kemudian data senyawa dari 15 asam sinamat dibagi menjadi 2
bagian yakni 10 training set dan 9 test set.
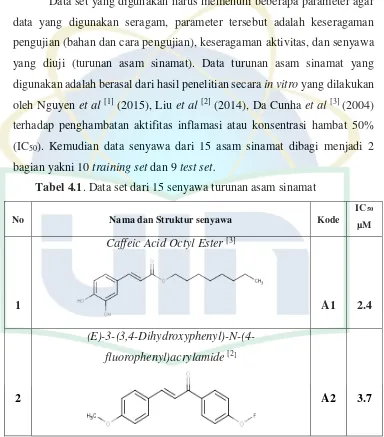
Tabel 4.1. Data set dari 15 senyawa turunan asam sinamat
No Nama dan Struktur senyawa Kode IC50
µM
1
Caffeic Acid Octyl Ester [3]
A1 2.4
2
( E)-3-(3,4-Dihydroxyphenyl)-N-(4-fluorophenyl)acrylamide [2]