PENENTUAN KADAR NATRIUM SIKLAMAT
DALAM MINUMAN RINGAN SECARA
SPEKTROFOTOMETRI UV-VIS
KARYA ILMIAH
DARLINA BR TARIGAN
062401031
PROGRAM STUDI D-III KIMIA ANALIS
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN
ALAM
KARYA ILMIAH
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Ahli Madya pada Fakultas Matematika Dan Ilmu Pengetahuan Alam
DARLINA BR TARIGAN
062401031
PROGRAM STUDI D-III KIMIA ANALIS
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : PENENTUAN KADAR NATRIUM SIKLAMAT
DALAM MINUMAN RINGAN SECARA
SPEKTROFOTOMETRI UV-VIS
Kategori : KARYA ILMIAH
Nama : DARLINA BR TARIGAN
Nomor Induk Mahasiswa : 062401031
Program Studi : DIPLOMA (D3) KIMIA ANALIS
Departemen : KIMIA
Fakulta : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di Medan, Juli 2009
Diketahui/Disetujui oleh Disetujui oleh
Departemen Kimia FMIPA USU Pembimbing
Ketua,
Dr. Rumondang Bulan, MS
NIP : 131 459 466 NIP : 130 422 438
PERNYATAAN
PENENTUAN KADAR NATRIUM SIKLAMAT DALAM MINUMAN RINGAN SECARA SPEKTROFOTOMETRI UV-VIS
KARYA ILMIAH
Saya mengakui bahwa Karya Ilmiah ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juli 2009
062401031
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Kuasa, karena atas Rahmat dan Berkat-Nya penulis dapat menyelesaikan Karya Ilmiah ini dengan baik. Karya Ilmiah ini merupakan salah satu persyaratan dalam memenuhi tugas akhir yang nantinya berguna dalam memperoleh gelar di Perguruan Tinggi Program Diploma III Kimia Analis Fakultas Matematika dan Ilmu Pengetahuan Alam di Universitas Sumatera Utara.
Karya ilmia hyang penulis sajikan berjudul Penentuan kadar Natrium
siklamat dalam Minuman Ringan Secara Spektrofotometri UV-VIS. Dengan
selesainya karya ilmiah ini penulis mengucapkan terima kasih yang sebesar-besarnya kepada seluruh pihak yang telah banyak membantu, terutama kepada :
1. Kedua orang tua saya yang telah mendidik, serta memberikan dukungan yang baik moril maupun materil sehingga penulis dapat menyelesaikan karya ilmiah ini.
2. Bapak Drs. Saut Nainggolan, selaku Dosen Pembimbing yang telah banyak meluangkan waktu dan kesempatan untuk memberikan bimbingan dan arahan kepada penulis.
3. Ibu DR.Rumondang Bulan Nst, MS, selaku Ketua Departemen Kimia Fakultas Matematika dan Pengetahuan Alam Universitas Sumatera Utara.
4. Ibu Dr. Marpongahtun, MSc, selaku Ketua Program Studi Diploma III Kimia Analis Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara.
5. Bapak Prof.DR. Eddy Marlianto MSc, selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara. 6. Seluruh staff dan karyawan Balai besar Pengawas Obat dan Makanan
yang telah banyak meluangkan waktu dan kesempatan untuk memberikan bimbingan dan arahan dalam pelaksanaan PKL.
7. Rekan-rekan mahasiswa Kimia Analis angkatan 2006 yang telah banyak membantu penulis dalam menyelesaikan karya ilmiah ini. Demikianlah karya ilmiah ini penulis perbuat dan penulis menyadari bahwa karya ilmiah ini masih jauh dari kesempurnaan baik dari segi isi maupun susunanya dikarenakan keterbatasan, kemampuan serta pengetahuan penulis. Oleh sebab itu penulis mengharapkan kritik dan saran yang membangun dari pembaca demi kesempurnaan penulisan ini.
Akhir kata penulis berharap semoga tulisan ini bermanfaat dan berguna bagi pihak-pihak yang menggunakanya.
Medan, Juni 2009
ABSTRAK
Natrium Siklamat (NHSO3Na) merupakan bahan pemanis yang sering digunakan dalam makanan dan minuman. Pada Karya Ilmiah ini telah dilakukan penentuan kadar natrium siklamat dalam minuman ringan secara spektrofotometri UV-VIS dengan panjang gelombang 314 nm.
Dari hasil analisis diperoleh kadar natrium siklamat dalam minuman ringan merek kuades rasa anggur adalah 0,17 % dan ion tubuh sweat adalah 0,04 %.
DETERMINATION OF SODIUM CYCLAMATE IN SOFT DRINK BY USING SPECTROPHOTOMETRY UV-VIS METHOD
ABSTRACT
Sodium cyclamate (NHSO3Na ) is a sweetener that usually used in food and drink. Determination of sodium cyclamate in soft drink by using spectrophotometry UV-VIS on this paper had been analyzed with wave length 314 nm.
From the analysis was got that the concentration of sodium cyclamate in soft drink kuades rasa anggur is 0,17 % and ion tubuh sweat is 0,04 %.
DAFTAR ISI
BAB 4 HASIL DAN PEMBAHASAN
4.1. Data Percobaan 24 4.2. Pembahasan 24
BAB 5 KESIMPULAN DAN SARAN
5.1. Kesimpulan 25 5.2. Saran 25
DAFTAR TABEL
DAFTAR GAMBAR
ABSTRAK
Natrium Siklamat (NHSO3Na) merupakan bahan pemanis yang sering digunakan dalam makanan dan minuman. Pada Karya Ilmiah ini telah dilakukan penentuan kadar natrium siklamat dalam minuman ringan secara spektrofotometri UV-VIS dengan panjang gelombang 314 nm.
Dari hasil analisis diperoleh kadar natrium siklamat dalam minuman ringan merek kuades rasa anggur adalah 0,17 % dan ion tubuh sweat adalah 0,04 %.
DETERMINATION OF SODIUM CYCLAMATE IN SOFT DRINK BY USING SPECTROPHOTOMETRY UV-VIS METHOD
ABSTRACT
Sodium cyclamate (NHSO3Na ) is a sweetener that usually used in food and drink. Determination of sodium cyclamate in soft drink by using spectrophotometry UV-VIS on this paper had been analyzed with wave length 314 nm.
From the analysis was got that the concentration of sodium cyclamate in soft drink kuades rasa anggur is 0,17 % and ion tubuh sweat is 0,04 %.
BAB 1
PENDAHULUAN
1.1.Latar Belakang
Bahan pemanis sintesis dalam bentuk senyawa kimia yang sering ditambahkan dan digunakan untuk produk pangan dan minuman. Pemanis berfungsi untuk meningkatkan cita rasa dan aroma, memperbaiki sifat-sifat fisik, sebagai pengawet, memeperbaiki sifat-sifat kimia sekaligus merupakan sumber kalori bagi tubuh, mengembangkan jenis minuman dan makanan dengan jumlah kalori terkontrol, mengontrol program pemeliharaan dan penurunan berat badan,mengurangi kerusakan gigi, sebagai bahan subsitusi pemanis. Perkembangan industri pangan dan minuman akan kebutuhan pemanis dari tahun ke tahun semakin meningkat. Industri pangan dan minuman lebih menyukai menggunakan pemanis sintesis karena selain harganya relatif murah, tingkat kemanisan pemanis sintesis jauh lebih tinggi dari pemanis alami. Hal ini mengakibatkan terus meningkatnya penggunaan pemanis sintesis terutama sakarin dan siklamat.
merupakan zat pemanis sintesis yang diduga bersifat karsinogenik, ekskresinya melalui urine dapat merangsang pertumbuhan tumor. Penelitian yang lebih baru menunjukkan bahwa siklamat dapat menyebabkan atropi, yaitu terjadinya pengecilan testikular dan kerusakan kromosom.
Menurut SNI 01-6993-2004 dan Permenkes 722/ Menkes/ Per/ IX/ 88 kadar siklamat yang diperbolehkan dalam minuman ringan adalah maksimum 3 g/kg. Dalam karya ilmiah ini cara analisis kadar siklamat dalam minuman ringan dilakukan dengan metode spektrofotometri.
1.2. Metodologi
- Sampel diambil secara acak dalam memilih minuman yang bermerek kuades
rasa anggur dan ion tubuh sweat.
- Penentuan asam siklamat dengan menggunakan metode spektrofotometri
1.3. Permasalahan
Berapakah kadar siklamat dalam minuman ringan merek kuades rasa anggur dan ion tubuh sweat.
1.4. Tujuan
Untuk menentukan kadar siklamat yang terdapat dalam minuman ringan merek kuades rasa anggur dan ion tubuh sweat dengan metode spektrofotometri.
1.5. Manfaat
BAB 2
TINJAUAN PUSTAKA
2.1.Zat Pemanis Sintetik
2.1.1.Pengertian Zat Pemanis Sintesik
Zat pemanis sintetik merupakan zat yang dapat menimbulkan rasa manis atau dapat membantu mempertajam penerimaan terhadap rasa manis tersebut, sedangkan kalori yang dihasilkanya jauh lebih rendah dari pada gula. Umumnya zat pemanis sintetik mempunyai struktur kimia yang berbeda dengan struktur polihidrat gula alam. Meskipun telah banyak ditemukan zat pemanis sintetik, tetapi hanya beberapa saja yang boleh dipakai dalam bahan makanan. Mula-mula garam Na- dan Ca-siklamat yang kemanisanya tiga puluh kali kemanisan sukrosa digunakan sebagai pemanis. Di Indonesia penggunaan siklamat masih diizinkan, tetapi sebenarnya hasil metabolisme siklamat yaitu sikloheksamina merupakan senyawa karsinogenik,pembuangan sikloheksamina malalui urin dapat merangsang tumbuhnya tumor kandung kemih pada tikus.
Zat pemanis sintetik yang kini banyak digunakan dalam makanan dan minuman adalah garam Ca- atau Na-sakarin. Penggunaan sakarin tergantung dari intensitas kemanisan yang dikehendaki. Pada konsentrasi tinggi, sakarin akan menimbulkan rasa pahit-getir. Kemanisan sakarin empat ratus kali lebih besar dari kemanisan larutan sukrosa 10 % (Winarno,1997 ).
dipeptide). Pada awalnya,dipeptide ini mungkin dapat menyebabkan tumor otak pada tikus dan hewan-hewan laboratorium lain, tetapi tidak didukung oleh pengamatan lain. FDA memperkirakan bahwa pemanis ini tidak banyak meningkatkan keterbelakangan mental terlihat dengan fwenilketonurik yang tidak terdiagnosis walaupun konsumsi meningkat sampai 3 mg fenilalanin/kg/hari. Sebagai dipeptida yang terdiri dari asam amino secara normal konsumsinya dalam jumblah besar (dalam bentuk protein) tidak diharapkan karena pemanis tersebut terbukti berbahaya bagi manusia dan hewan. Sebagai substitusi untuk sakarin, aspartame mempunyai satu kekeurangan karena kehilangan rasa manisnya (karena terhidrolisis) kalau lama diekspos dengan air atau panas, oleh karena itu tidak dapat digunakan secara baik dalam persiapan produk suatu bahan makanan(Linder, 1992).
2.1.2. Jenis Bahan Pemanis Sintetik 1.Sakarin
harganya relatif murah, selain itu sakarin banyak digunakan untuk mengganti sukrosa bagi penderita diabetes mellitus atau bahan pangan berkalori rendah.
Penggunaan sakarin biasanya dicampur dengan bahan pemanis lain seperti siklamat atau aspartam. Hal itu dimaksudkan untuk menutupi rasa tidak enak dari sakarin dan memperkuat rasa manis. Sebagai contoh kombinasi sakarin dan siklamat dengan perbandingan 1:3 merupakan campuran paling baik sebagai pemanis yang menyerupai gula dalam minuman.
Produk pangan dan minuman yang menggunakan sakarin diantaranya adalah minuman ringan (soft drinks), permen, selai, bumbu salad, gelatin rendah kalori, dan hasil olahan lain tanpa gula. Selain itu sakarin digunakan sebagai bahan tambahan pada produk kesehatan mulut seperti pasta gigi dan obat pencuci (penyegar) mulut (Cahyadi, 2006).
2.Siklamat
Sejak tahun 1950 siklamat ditambahkan kedalam pangan dan minuman.Siklamat biasanya tersedia dalam bentuk garam natrium dari asam siklamat dengan rumus molekul C6H11NHSO3Na.Nama lain dari siklamat adalah natrium sikloheksisulfamat atau natrium siklamat.
NHSO3Na
Tidak seperti sakarin, siklamat berasa manis tanpa rasa ikutan yang kurang disenangi. Bersifat mudah larut dalam air dan intensitas kemanisanya ± 30 kali kemanisan sukrosa. Dalam industri pangan natrium siklamat dipakai sebagai bahan pemanis yang tidak mempunyai nilai gizi untuk pengganti sukrosa. Siklamat bersifat tahan panas, sehingga sering digunakan dalam pangan yang diproses dalam suhu tinggi misalnya pangan dalam kaleng. Meskipun memiliki tingkat kemanisan yang tinggi dan rasanya enak (tanpa rasa pahit) tetapi siklamat dapat membahayakan kesehatan. Hasil penelitian bahwa tikus yang diberikan siklamat dan sakarin dapat menimbulkan kanker kantong kemih. Hasil metabolisme siklamat, yaitu sikloheksiamin bersifat karsinogenik. Oleh karena itu ekskresinya melalui urine dapat merangsang pertumbuhan tumor. Penelitian yang lebih baru menunjukkan bahwa siklamat dapat menyebabkan atropi, yaitu terjadinya pengecilan testikular dan kerusakan kromosom ( Cahyadi, 2006 ).
3.Aspartam
Aspartam tersusun oleh asam amino sehingga didalam tubuh akan mengalami metabolisme seperti halnya asam amino pada umumnya. Bagi penderita keturunan yang berhubungan dengan kelemahan mental (phenil keton urea / PKU) dilarang mengkonsumsi aspartam karena adanya fenilalanian yang tidak dapat dimetabolisme oleh penyakit tersebut. Kelebihan fenilalanin dalam tubuh penderita PKU diduga dapat menyebabkan kerusakan pada otak dan pada akhirnya akan mengakibatkan cacat mental. Mengacu pada asam amino pembentuk aspartam maka aspartam bukanlah termasuk suatu bahan pemanis nonkalori karena seperti protein, aspartam dimetabolisme menjadi asam amino penyusunya dan memiliki energi 4 kkal/g. Tetapi karena dalam penggunaanya 100 g sukrosa dapat diganti dengan 1 g aspartam maka dapat dikatakan bahwa aspartam merupakan bahan pemanis nonkalori.
2.1.3. Hubungan Sifat Kimia Dan Rasa Manis
Konsep adanya empat rasa pokok (manis, asin, pahit, dan asam) sebenarnya hanya penyederhanaan supaya praktis. Rangsangan yang diterima oleh otak karena rangsangan elektrik yang diteruskan dari sel perasa sebetulnya sangat kompleks. Rasa asin terutama disebabkan oleh rangsangan ion-ion negatif (anion) bahan kimia pada reseptor rasa. Tetapi tidak ada kelompok bahan kimia tertentu yang menyebabkan rasa manis meskipun telah diketahui bahwa struktur molekul sederhana kelompok senyawa-senyawa gula yang terbentuk tertutup sangat merangsang rasa manis. Sakarin yang struktur kimianya sangat berlainan dengan gula ternyata tidak dapat dibedakan rasa manisnya. Sampai saat ini mekanisme respons rasa manis belum diketahui dengan baik. Perubahan struktur molekul sedikit saja dapat menghasilkan senyawa baru dengan rasa yang berbeda.
Faktor-faktor yang perlu diperhatikan untuk mengetahui hubungan struktur kimia bahan pemanis dengan rasa manis adalah .
1.Mutu rasa manis
terkait dengan struktur molekulnya, karena dengan pemurnian yang bagaimanapun tidak dapat menghilangkan rasa pahit.
2.Intensitas rasa manis.
Intensitas rasa manis menunjukkan kekuatan atau tingkat kadar kemanisan suatu bahan pemanis. Intensitas rasa manis berkaitan dengan nilai relatif rasa manis dalam yang sama maupun yang berbeda antara masing-masing bahan pemanis. masing-masing pemanis berbeda kemampuannya untuk merangsang indra perasa. Kekuatan rasa manis yang ditimbulkan oleh bahan pemanis dipengaruhi oleh beberapa faktor diantara adalah suhu dan sifat dan mediumnya (cair atau padat). Harga Intensitas rasa manis biasanya diukur dengan membandingkannya dengan kemanisan sukrosa 10 %.
3.Kenikmatan rasa manis
Bahan pemanis ditambahkan dengan tujuan untuk memperbaiki rasa dan bau bahan pangan sehingga rasa manis yang tinbul dan menimbulkan kelezatan. Dari beberapa pemanis tidak sempurna dapat menimbulkan rasa nikmat yang dikehendaki. Pada pemanis sintesis seperti sakarin malah tidak dapat menimbulkan rasa nikmat malah memberikan rasa yang tidak menyenangkan. Tetapi penggunaan campuran sakarin dan siklamat pada bahan pangan dapat menimbulkan rasa manis tanpa menimbulka rasa pahit.
2.1.4 Tujuan penggunaan pemanis sintesis
1. Sebagai pangan bagi penderita diabetes mellitus karena tidak menimbulkan gula darah. Pada penderita diabetes mellitus disarankan mengunakan pemanis sintesis untuk menghindari bahaya gula. Dari tahun 1955 sampai 1966 digunakan campuran siklamat dan sakarin pada pangan dan minuman bagi penderita diabetes.
2. Memenuhi kebutuhan kalori rendah untuk penderita kegemukan
Kegemukan merupakan salah satu faktor penyakit jantung yang merupakan penyebab utama kematian. Untuk orang yang kurang aktif secara fisik disarankan untuk mengurangi masukan kalori per harinya. Pemanis sintesis merupakan salah satu bahan pengan untuk mengurangi masukan kalori.
3. Sebagai penyalut obat.
Beberapa obat mempunyai rasa yan tidak menyenangkan, oleh karena itu untuk menutupi rasa yang tidak enak dari obat tersebut biasanay dibuat tablet yang bersalut. Pemanis lebih sering digunakan untuk menyalut obat karena umumnya bersifat higroskopis dan tidak menggumpal.
4. Menghindari kerusakan gigi.
Pada pangan seperti permen lebih sering ditambahkan pemanis sintesis karena bahan permen ini mempunyai rasa manis yang lebih tingi dari gula, pemakaian dalam jumlah sedikit saja menimbulkan rasa manis yang diperlukan sehingga tidak merusak gigi.
juga harganya relatif murah dibandingkan dengan gula yang diproduksi di alam ( Cahyadi, 2006 ).
2.2.Metode Spektrofotometri
Sebuah spektrofotometer adalah suatu instrumen untuk mengukur trnsminstans atau absorbans suatu sampel sebagai fungsi panjang gelombang ,pengukuran terhadap sederetan sampel pada suatu panjang gelombang tunggal dapat pula dilakukan. Instrumen semacam itu dapat dikelompokkan secara manual atau merekam atau sebagai berkas tunggal atau berkas rangkap. Dalam praktik instrumen berkas tunggal biasanya dijalankan secara manual, dan instrumen berkas rangkap umumnya mencirikan perekaman automatik terhadap spektra absorpsi, namun dimungkinkan untuk merekam suatu spektrum dengan instrumen berkas tunggal.
Prinsip Metoda Spektrofotometri
2.2.1.Komponen-komponen Spektrofotometer 1.Sumber Radiasi
Sumber energi radiasi yang biasa untuk daerah tampak dari spektrum itu maupun daerah ultrviolet dekat dengan inframerah dekat adalah sebuah lampu pijar dengan kawat rambut terbuat dari wolfram ( Underwood, 2002 ).
2.Monokromator
Ini adalah piranti optis untuk mengisolasi suatu berkas radiasi dari suatu sumber berkesinambungan, berkas mana mempunyai kemurnian spektral yang tinggi dengan panjang gelombang apa saja yang diinginkan. Komponen yang esensial dari sebuah monokromator adalah suatu sistem celah masuk, kemudian disejajarkan oleh lensa atau cermin sehingga suatu berkas sejajar jatuh keunsur pendispersi, yang berupa prisma atau suatu kisi difraksi. Dengan memutar prisma atau kisi itu secara mekanis, aneka porsi spektrum yang dihasilkan oleh unsur dispersi dipusatkan pada celah keluar, dari situ, lewat jalan optis lebih jauh, porsi-porsi itu menjumpai sampel (Underwood, 2002 ).
3.Sel
sangat pendek, kurang daripada 1 milimeter sampai 10 cm atau bahkan lebih ( Underwood, 2002 ).
4.Detektor
Dalam sebuah detektor untuk suatu spektrofotometer, kita menginkan kepekaan yang tinggi dalam daerah spektral yang diminati, respons yang linear terhadap daya radiasi, waktu respons yang cepat, dapat digandakan, dan kesetabilan yang tinggi atau tingkat noise yang rendah, meskipun dalam praktiknya perlu untuk mengkompromikan faktor-faktor ini (Underwood, 2002 ).
2.2.2.Hal-hal yang harus diperhatikan dalam analisis spektrofotometri UV-VIS
Ada beberapa hal yang harus diperhatikan dalam analisis dengan spektrofotometri UV-VIS terutama untuk senyawa yang semula tidak berwarna yang akan dianalisis dngan spektrofotometri UV karena senyawa tersebut harus diubah terlebih dahulu menjadi senyawa berwarna dengan spektrofotometri visibel.
a. Pembentukan molekul yang dapat menyerap sinar UV-VIS
Hal ini perlu dilakukan jika senyawa yang dianalisis tidak menyerap pada daerah tersebut. Cara yang digunakan adalah dengan merubah menjadi senyawa lain atau direaksikan dengan pereaksi tertentu. Pereaksi yang digunakan harus memenuhi beberapa persyaratan yaitu :
- Reaksinya selektif dan sensitif
Keselektifan dapat dinakkan dengan mengatur pH, pemakaian masking agent, atau penggunaan teknik ekstraksi ( Rohman, 2007 ).
b. Waktu operasional
Cara ini biasa digunakan untuk pengukuran hasil reaksi atau pembentukan warna. Tujuannya adalah untuk mengetahui waktu pengukuran yang stabil. Waktu operasional ditentukan dengan mengukur hubungan antara waktu pengukuran dengan absorbansi larutan.
Pada saat awal terjadi reaksi, absorbansi senyawa yang berwarna ini meningkat sampai waktu tertentu hingga diperoleh absorbansi yang stabil. Semakin lama waktu pengukuran, maka ada kemungkinan senyawa yang berwarna tersebut menjadi rusak atau terurai sehingga intensitas warnanya turun akibatnya absorbansinya juga turun. Karena alasan inilah, maka untuk pengukuran senyawa berwarna (hasil suatu reaksi kimia) harus dilakukan pada saat waktu operasional (Rohman, 2007 ).
c. Pemilihan panjang gelombang
Panjang gelombang yang digunakan untuk analisis kuantitatif adalah panjang gelombang yang mempunyai absorbansi yang maksimal. Untuk memilih panjang gelombang maksimal, dilakukan dengan membuat kurva hubungan antara absorbansi dengan panjang gelombang dari suatu larutan baku pada konsentrasi tertentu.
- Pada panjang gelombang maksimal, kepekaanya juga maksimal karena pada panjang gelombang maksimal tersebut, perubahan absorbansi untuk setiap satuan konsentrasi adalah yang paling besar.
- Disekitar panjang gelombang maksimal, bentuk kurva absorbansi datar dan pada kondisis tersebut hukum Lambert-Beer akan terpenuhi.
- Jika dilakukan pengukuran ulang maka kesalahan yang disebabkan oleh pemasangan ulang panjang gelombang akan kecil sekali, ketika digunakan panjang gelombang maksimal.
Kadang-kadang dijumpai keadaan yang mana pemakaian panjang gelombang yang maksimal kurang baik. Hal ini kareana misalnya, selain zat yang akan dianalisis, juga terdapat zat lain yang mempunyai absorbansi pada panjang gelombang tersebut. Ada beberapa variabel yang mempengaruhi absorbansi yaitu : jenis pelarut, pH larutan, konsentrasi tinggi dan zat-zat penggangu ( Rohman, 2007 ).
d. Pembuatan kurva baku
Dibuat seri larutan baku dari zat yang akan dianalisis dengan berbagai konsentrasi. Masing-masing absorbansi larutan dengan berbagai konsentrasi diukur, kemudian dibuat kurva yang merupakan hubungan antara absorbansi (y) dengan konsentrasi (x). Bila hukum Lambert-Beer terpenuhi, maka kurva baku berupa garis lurus ( Rohman, 2007 ).
e. Pembacaan absorbansi sampel atau cuplikan
berdasarkan anggapan bahwa kesalan dalam pembacaan T adalah 0,005 atau 0,5 % (kesalahan fotometrik) ( Rohman, 2007 ).
2.2.3. Aspek Kualitatif dan Kuantitatif Spektrofotometri UV-VIS
Spektra UV-VIS dapat digunakan untuk informasi kualitatif dan sekaligus dapat digunakan untuk analisis kuantitatif.
1.Aspek Kualitatif
Data spektra UV-VIS secara tersendiri tidak dapat digunakan untuk identifikasi kualitatif obat dan metabolitnya. Akan tetapi jika digabung dengan cara lain seperti spektroskopi infra merah, resonansi magnet inti, dan spektroskopi massa, maka dapat digunakan untuk maksud identifikasi/analisis kualitatif suatu senyawa tersebut. Data yang diperoleh dari spekstroskopi UV dan VIS adalah panjang gelombang maksimal, intensitas, efek pH, dan pelarut yang kesemuanya itu dapat diperbandingkan dengan data yang sudah dipublikasikan (publissed data) ( Rohman, 2007 ).
2. Analisis Kuantitatif
Analisis kuantitatif dengan metode spektrofotometri UV-VIS dapat digolongkan tiga macam pelaksanaan pekerjaan yaitu :
- Analisis kuantitatif zat tunggal (analisis satu komponen )
- Analisis kuantitatif campuran dua macam zat (analisis dua komponen)
a. Analisis kuantitatif zat tunggal dilakukan pengukuran harga A pada panjang gelombang maksimum atau dilakukan pengukuran % T pada panjang gelombang minimum. Alasan ini dilakukan pengukuran pada panjang gelombang tersebut adalah:
prubahan absorban untuk setiap satuan konsentrasi adalah paling besar pada panjang gelombang maksimal, sehingga akan diperoleh kepekaan analisis yang maksimal datar dan pengukuran ulang dengan kesalahan yang kecil dengan demikian akan memenuhi hukum Lambert-Beer
b. Analisis kuantitatif campuran dua komponen merupakan teknik pengembangan analisis kuantitatif komponen tunggal. Prinsip pelaksanaanya adalah mencari absorban atau beda absorban tiap-tiap komponen yang memberikan korelasi yang linear terhadap konsentrasi, sehingga akan dapat dihitung masing-masing kadar campuran zat tersebut secara serentak atau salah satu komponen dalam campuranya dengan komponen yang lainya. Beberapa cara yang telah dipakai para ilmuwan untuk analisis kuantitatif campuran dua komponen dengan metode spektrofotometri UV-Vis antara lain dengan cara :
- serapan individual - grafik
- simultan
- perbandingan serapan dari Pernarowski - panjang gelombang ganda
- differensial beda pelarut
Diantara cara-cara analisis tersebut diatas yang umum sering dipakai adalah cara derivatif dan dengan cara pengamatan tiga panjang gelombang atau lebih. Pada prinsipnya semua spektrum yang dihasilkan oleh semua spektrofotometer UV-Vis jenis apapun dapat diturunkan spektra derivatifnya secara manual maupun otomatis.
Pada spektrofotometer UV-Vis yang modern dapat membuat spektrum derivatif sampai tingkat sembilan secara otomatis. Kegunaan spektrofotometer UV-Vis cara derivatif adalah :
- Apabila menghadapi campuran dua komponen yang spektrumnya saling tumpang tindih, maka analisis kuantitatif cara derivatif akan menjadi metode yang terpilih
- Analisis kuantitatif campuran 2 komponen yang keruh
- Analisis kuantitatif campuran 2 komponen yang merupakan isomeri (kecuali isomer optis aktif atau resemik)
- Spektra derivatif dapat dipakai un tuk maksud kualitatif atau sebagai dat pendukung
Analisis kuantitatif dengan metode spektrofotometri UV-Vis dengan cara pengamatan tiga panjang gelombang, prinsip kegunaanya hampir sama dengan cara derivatif yaitu - Untuk analisis kuantitatif campuran dua komponen yang spektrumnya saling tumpang tindih
- Untuk analisis kuantitatif campuran komponen dalam sampel yang keruh
dua macam larutan standar yaitu larutan standar murni (pure standard) dan larutan standar campuran (mixed standard).
Larutan standar campuran teknik pembuatan dan dampak kesalahanya sudah jelas lebih rumit.Selanjutnya cara-cara perhitungan kadar tiap-tiap komponen juga dikenal dua macam cara yaitu konvensional dan cara modern yang tergantung pada instrumen yang dipakai.. Pada spektrofotometer UV-Vis yang konvensional perhitungan dilakukan pada setiap puncak (panjang gelombang maksimum) tiap komponen. Untuk campuran pembacaan absorban adalah hasil jumblah absorban tiap komponen. (Mulja,1995 ).
2.3.Kesalahan-kesalahan dalam spektrofotometri
Kesalahan dalam pengukuran secara spektrometri dapat ditimbul dari banyak sebab. Sebab-sebab yang bisa menyebabkan kesalahan antara lain adalah :
- kuvet yang kotor atau telah tergores
- sidik jari yang dapat menyerap radiasi ultra violet - penempatan kuvet yang tidak tepat posisinya - ukuran kuvet yang tidak seragam
- adanya gelembung udara/gas dalam lintasan radiasi panjang gelombang yang dihasilkan sudah tidak cocok dengan yang tertera pada instrumen
BAB 3
METODOLOGI PERCOBAAN
3.1. Alat-alat dan Bahan
3.1.1. Alat-alat yang digunakan
- Spektrofotometer UV-Visible Hitachi
- Gelas Beaker Pyrex
- Corong pisah Pyrex
- Gelas ukur Pyrex
- Pipet tetes
- Corong Pyrex
- Kertas saring Pyrex
- Labu ukur Pyrex
3.1.2. Bahan-bahan yang digunakan
- NaOH 0,5 N p.a
- NaOH 10 N p.a
- H2SO4 30 % p.a
- Hipoklorit 1 % p.a
- Sikloheksan p.a
- Etil asetat p.a
3.2. Prosedur
3.2.1. Pembuatan Pereaksi - NaOH 0,5 N
Timbang 20 g NaOH, larutkan dalam aquadest bebas CO2 sampai 1000 ml dalam labu ukur
- NaOH 10 N
Timbang 400 g NaOH, larutkan dalam aquadest bebas CO2 sampai 1000 ml dalam labu ukur
- H2SO4 30 %
Encerkan 30 ml H2SO4 (p) dengan aquadest sampai 100 ml dalam labu ukur
3.2.2.Larutan Uji
- Sejumlah 1 gr sampel diencerkan dengan 100 ml aquadest dimasukkan kedalam corong pisah 250 ml
- Tambahkan 5 ml H2SO4 30 %
- Setelah dingin, tambah 100 ml etil asetat - Kocok selama 2 menit
- Lapisan etil asetat dimasukkan kedalam corong pisah kedua - Dikocok 3 kali, setiap kali dengan 30 ml aquadest
- Kumpulan lapisan air dimasukkan kedalam corong pisah ketiga - Tambah 2 ml NaOH 10 N dan 10 ml sikloheksana
- Kocok selama 1 menit
- Lapisan air dipisah dan dimasukkan kedalam corong pisah keempat
- Tambah 5 ml H2SO4 30 % dan 10 ml sikloheksana dengan pipet volume dan 10 ml Na-hipoklorit 1 %
- Kocok selama 2 menit
tambah lagi 10 ml Na-hipoklorit 1 %
- Lapisan air dibuang, lapisan sikloheksana dicuci dengan 50 ml NaOH 0,5 N - Kocok selama 1 menit, lapisan bawah dibuang
- Lapisan sikloheksana dikocok dengan 50 ml air,lapisan air dibuang
- Lapisan sikloheksana disaring melalui kapas, masukkan dalam labu ukur 10 ml ( A )
3.2.3. Larutan Baku
- Timbang teliti 50 mg Na-siklamat sebagai baku pembanding
- Masukkan kedalam labu ukur 100 ml dan encerkan dengan aquadest sampai garis tanda
- Pipet 1,0 ml; 2,0 ml ; 4,0 ml ; 6,0 ml; dan 8,0 ml dan masing-masing masukkan kedalam labu ukur 100 ml
- Tambah aquadest sampai garis tanda dan diperlakukan sama seperti larutan uji.
3.2.4. Cara Penetapan
- Masing-masing larutan A dan B diukur pada panjang gelombang
maksimum ± 314 nm, menggunakan air yang diperlakukan sama seperti larutan uji sebagai blanko
- Kadar Na siklamat dalam minuman
Fp sampel = faktor pengenceran sampel Fp baku = faktor pengenceran baku Kb = kemurnian baku (%)
3.2.5. Prosedur Analisa Spektrofotometri
- Hubungkan alat dengan sumber arus listrik
- Hidupkan dengan menekan tombol power pada posisi ON pada seluruh alat tunggu sampai proses initialisasi selesai
- Hidupkan CPU, monitor, printer
- Pada menu windows, double klik icon UV-probe - Klik icon spektrum
- Tekan tombol F4 ( Pc control pada alat ) spektrofotometer UV 1700 probe - Untuk menghubungkan alat spektrofotometer dengan CPU klik ditaskbar connect
- Pengisian parameter klik icon metode :
a. Pada tabulasi pengukuran pada panjang gelombang 314 nm, amati pada 314 nm
b. Pada tabulasi preparasi sampel, isi berat volume pengenceran
c. Pada tabulasi instrumen parameter isi cara pengukuran, slith, klik OK - Masukkan blanko pada kuvet reference dan kuvet sampel, klik pada Taksbar garis dasar tunggu sampai pembacaan selesai
BAB 4
HASIL DAN PEMBAHASAN
4.1 Data Percobaan
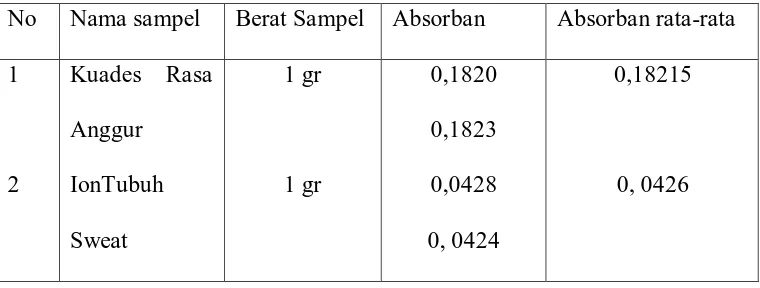
No Nama Sampel Kadar Na Siklamat 1 Kuades Rasa Anggur 0,17 % 2 Ion Tubuh Sweat 0.04 %
4.2. Pembahasan
Natrium siklamat (C6H11NHSO3Na) merupakan bahan pemanis sintesis yang luas penggunaanya terutama dalam industri pangan dan minuman. Natrium siklamat merupakan bahan pemanis yang tidak mempunyai nilai gizi, bersifat mudah larut dalam air dan tahan terhadap panas.
Penentuan kadar natrium siklamat dapat dilakukan dengan metode spektrofotometri pada panjang gelombang 314 nm. Dari data diperoleh kadar natrium siklamat dalam minuman ringan merek kuades rasa anggur adalah 0,17 % dan ion tubuh sweat adalah 0,04 %, ternyata kadar natrium siklamat dalam minuman ringan merek kuades rasa anggur lebih tinggi dari pada ion tubuh sweat. Karena komposisi dari kedua minuman ini berbeda, dimana kuades rasa anggur mengandung pewarna makanan yang menyebabkan larutannya berwarna sehingga pengukuranya berada pada daerah spektrofotometri visible sedangkan untuk ion
BAB 5
KESIMPULAN DAN SARAN
5.1.Kesimpulan
Kadar natrium siklamat yang terdapat dalam minuman merek kuades rasa anggur adalah 0,17 % dan ion tubuh sweat adalah 0,04 % dan kadar natrium siklamat dalam kuades rasa anggur lebih tinggi dibandingkan dengan ion tubuh sweat.
5.2. Saran
Sebaiknya pemakaian siklamat dalam minuman ringan jangan sampai
DAFTAR PUSTAKA
Alaerts, G.1987. Metode Penelitian Air. Surabaya : Penerbit Usaha Nasional.
Cahyadi, W.2006. Bahan Tambahan Pangan.Jakarta : PT Bumi Aksara Linder, M.C. 1992. Biokimia Nutrisi Dan Metabolisme. Cetakan 1. Jakarta : UI-Press
Mulja, M. 1995. Analisis Instrumental. Surabaya : Airlangga University Press Rohman, A. 2007. Kimia Farmasi Analisis. Cetakan 1. Yogyakarta : Penerbit Pustaka Pelajar
Sudarmaji, S. 1989. Analisis Bahan Makanan Dan Pertanian. Yogyakarta : Penerbit Liberty
Underwood, A.L. 2002. Analisis Kimia Kuantitatif. Jakarta : Erlangga
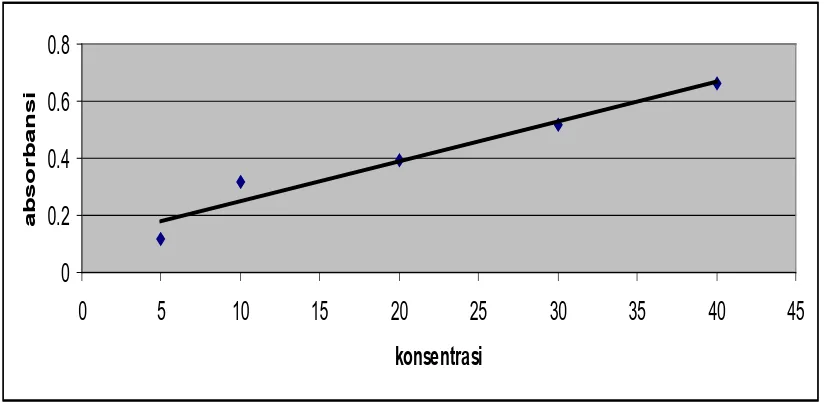
Tabel 4.1.1. Baku Seri Siklamat
No Konsentrasi Vol.larutan Absorban Absorban rata-rata
1 5 ppm 1 ml 0, 1150
Konsentrasi Absorbansi rata-rata
5 0.1148
10 0.31665
20 0.3958
30 0.5191
40 0.6628
Grafik: Baku Seri Siklamat Absorbansi VS Konsentrasi
0
0.2
0.4
0.6
0.8
0
5
10
15
20
25
30
35
40
45
konsentrasi
a
b
s
o
r
b
a
n
s