PEMBUATAN KAPLET ASAM MEFENAMAT SECARA GRANULASI BASAH DENGAN PATI KENTANG MERAH (Solanum tuberosum L.)
SEBAGAI DISINTEGRAN
SKRIPSI
OLEH
CYANITA FRANSISKA BAWONI NIM 060804001
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
PEMBUATAN KAPLET ASAM MEFENAMAT SECARA GRANULASI BASAH DENGAN PATI KENTANG MERAH (Solanum tuberosum L.)
SEBAGAI DISINTEGRAN
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk mencapai gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH
CYANITA FRANSISKA BAWONI NIM 060804001
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
LEMBAR PENGESAHAN
PEMBUATAN KAPLET ASAM MEFENAMAT SECARA GRANULASI BASAH DENGAN PATI KENTANG MERAH (Solanum tuberosum L.)
SEBAGAI DISINTEGRAN OLEH
CYANITA FRANSISKA BAWONI NIM 060804001
Dipertahankan dihadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : Maret 2011
Pembimbing I Panitia Penguji
Drs. Agusmal Dalimunthe, MS., Apt. Dra. Juanita Tanuwijaya, Apt. NIP 195406081983031005 NIP 130672239
Pembimbing II Drs. Agusmal Dalimunthe, MS., Apt. NIP 195406081983031005
Dra. Fat Aminah, M.Sc., Apt. Dra. Djendakita Purba, M.Si., Apt. NIP 195011171980022001 NIP 195011171980022001
Drs. Suryanto, M.Si., Apt. NIP. 195112231980032002
Disahkan Oleh : Dekan
Prof. Dr. Sumadio Hadisahputra, Apt.
NIP. 195311281983031002
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa, karena limpahan rahmat
kasih dan karunianya, sehingga penulis dapat menyelesaikan skripsi ini yang berjudul
”Pembuatan Kaplet Asam Mefenamat secara Granulasi Basah dengan Pati Kentang
Merah (Solanum tuberosum L.) sebagai Disintegran”. Skripsi ini diajukan sebagai
salah satu syarat untuk memperoleh gelar sarjana farmasi pada Fakultas Farmasi
Universitas Sumatera Utara.
Terima kasih dan penghargaan yang tulus kepada almarhum daddy Ir.Ronny
RJ Bawoni, ME, M.Kes dan mommy tercinta, Corry Kalidjasuma, S.Pd yang tiada
pernah ada hentinya berkorban dengan tulus ikhlas dan selalu setia memberi doa,
dorongan dan semangat.
Pada kesempatan ini penulis juga mengucapkan terima kasih yang tulus dan
ikhlas kepada :
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi
USU Medan yang telah memberikan fasilitas sehingga penulis dapat
menyelesaikan pendidikan.
2. Bapak Drs. Agusmal Dalimunthe, M.S, Apt. dan Dra. Fat Aminah, M.Sc, Apt.
selaku pembimbing yang telah memberikan waktu, bimbingan, dan nasehat selama
penelitian hingga selesainya penyusunan skripsi ini.
3. Ibu Dra. Juanita Tanuwijaya, Apt., Ibu Dra. Djendakita Purba, M.Si, Apt. dan
Bapak Drs. Suryanto, M.Si, Apt. selaku dosen penguji yang telah memberikan
4. Bapak dan Ibu staf pengajar Fakultas Farmasi USU Medan yang telah mendidik
selama perkuliahan dan Bapak Drs. Chairul Azhar Dalimunthe, Apt selaku
penasehat akademis yang telah memberikan bimbingan kepada penulis selama ini.
5. Ibu kepala Laboratorium Teknologi Formulasi Sediaan Tablet dan Ibu kepala
Laboratorium Kimia Farmasi Kuantitatif yang telah memberikan bantuan dan
fasilitas selama penulis melakukan penelitian.
6. Sahabat-sahabatku Siti, Mimi, Fika, Zack dan Icha yang selalu memberi bantuan,
dukungan, dan motivasi. Para superheroes Rico, Gokman, Roni, Rian, Jon dan Ari.
Rekan-rekan farmasi stambuk 2006, kakak/abang senior (terkhusus Kak Vini,
Bang Lambok dan Bang Parna) dan junior mahasiswa fakultas farmasi, para
asisten laboratorium serta kawan-kawan yang tidak dapat disebutkan satu persatu.
Penulis menyadari bahwa penulisan skripsi ini masih belum sempurna. Oleh
karena itu, penulis mengharapkan kritik dan saran yang membangun untuk
penyempurnaannya. Harapan saya semoga skripsi ini dapat bermanfaat bagi ilmu
pengetahuan kefarmasian.
Medan, 25 Maret 2011
Penulis
Pembuatan Kaplet Asam Mefenamat secara Granulasi Basah dengan Pati Kentang Merah (Solanum tuberosum L.) sebagai Disintegran
ABSTRAK
Asam mefenamat merupakan salah satu bahan obat anti inflamasi non-steroid (AINS) yang bekerja sebagai analgesik untuk mengurangi/menghilangkan rasa sakit ringan sampai sedang. Karakteristik asam mefenamat yaitu kelarutannya yang praktis tidak larut dalam air. Efek samping tersering adalah gangguan saluran cerna, seperti diare dan peradangan abdomen.
Untuk mengatasi masalah tidak larutnya asam mefenamat ini, maka dilakukan formulasi kaplet asam mefenamat dengan menggunakan penambahan disintegran. Disintegran merupakan bahan tambahan (eksipien) dalam yang ditambahkan ke dalam formulasi kaplet untuk mendorong pecahnya kaplet ketika terjadi kontak dengan cairan. Disintegran yang digunakan disini adalah amilum solani yang diisolasi dari kentang merah. Konsentrasi amilum solani yang digunakan adalah 2%, 4%, 6% dan 8%, dan dibuat dengan metode granulasi basah. Kaplet yang dihasilkan dievaluasi dengan menggunakan parameter antara lain: kekerasan, friabilitas, waktu hancur, penetapan kadar, keseragaman sediaan, dan disolusi.
Hasil penelitian menunjukka n bahwa kaplet asam mefenamat yang dibuat dengan metode granulasi basah menggunakan amilum solani sebagai disintegran memenuhi persyaratan penetapan kadar, keragaman bobot, kekerasan, friabilitas. Walaupun tidak memenuhi persyaratan waktu hancur dan uji disolusi namun kaplet asam mefenamat memberikan hasil disolusi yang lebih baik dari kaplet pembanding dan tidak jauh berbeda dengan hasil disolusi kaplet yang telah ada di pasaran. Dengan kata lain amilum solani dapat digunakan sebagai disintegran pada pembuatan kaplet asam mefenamat.
Caplet Preparation of Mefenamic Acid with Wet Granulation Method Using Red Potato (Solanum tuberosum L.) Starch as Disintegration Agent
ABSTRACT
Mefenamic acid is one of non-steroidal anti-inflammatory drugs which works as analgesic for reducing slight to moderate pain. Mefenamic acid cannot dissolve in water. Common side effects are gastrointestinal disturbances, such as diarrhoea and abdominal discomfort.
To overcome this solubility problem, mefenamic acid caplet formulation is carried out by using the addition of disintegrant. Disintegrant is an additional materials (excipients) were added to the caplet formulation to encourage the breakup of the caplet when it comes in contact with liquid. Disintegrant used here is red potato starch. Its concentrations used were 2%, 4%, 6% and 8%, and made with the wet granulation method. The resulting caplets were evaluated using parameters such as: hardness, friability, disintegration time, determination, weight uniformity, and dissolution.
The result shows that mefenamic acid caplets which are prepared with wet granulation method using red potato starch as disintegrant fulfilled the requirements of content determining, weight uniformity, hardness, and friability analysis. Even the caplets not fulfilled of the requirements of disintegration and dissolution test but it gives a better result than the comparing caplets. It showed that potato starch can be used as disintegration agent in mefenamic acid caplet.
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xiii
DAFTAR GAMBAR ... xiv
DAFTAR LAMPIRAN ... xvi
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 2
1.3 Hipotesis ... 2
1.4 Tujuan Penelitian ... 2
1.5 Manfaat Penelitian ... 2
BAB II TINJAUAN PUSTAKA ... 3
2.1 Asam Mefenamat ... 3
2.1.1 Tinjauan Umum ... 3
2.1.2 Farmakologi ... 3
2.1.3 Efek Samping, Indikasi dan Sediaan ... 4
2.2.1 Sistematika Tumbuhan ... 4
2.2.2 Kandungan Kimia ... 4
2.3 Pati dan Sifat – Sifat Pati... 5
2.4 Sediaan Tablet ... 6
2.4.1 Uraian Tablet ... 6
2.4.2 Metode Pembuatan Tablet ... 6
2.4.3 Komposisi Tablet ... 7
2.4.4 Uji Preformulasi ... 9
2.4.5 Evaluasi Tablet ... 9
2.5 Spektrofotometri Ultraviolet... 12
BAB III METODOLOGI PENELITIAN ... 13
3.1 Alat ... 13
3.2 Bahan ... 13
3.3 Prosedur Kerja ... 13
3.3.1 Isolasi Pati Kentang Merah ... 13
3.3.2 Evaluasi Terhadap Pati Hasil Isolasi... 14
3.3.2.1 Penetapan Kadar Abu Total ... 14
3.3.2.2 Penetapan Susut Pengeringan ... 14
3.3.3 Pembuatan Kaplet Asam Mefenamat ... 14
3.3.4 Pembuatan Granul Asam Mefenamat... 15
3.3.5 Uji Preformulasi ... 16
3.3.5.1 Sudut Diam Massa Granul ... 16
3.3.5.3 Indeks Tap Granul ... 17
3.3.6 Pembuatan Pereaksi 3.3.6.1. Air Suling Bebas Karbondioksida ... 17
3.3.6.2 Pembuatan Dapar Fosfat pH 7,4 ... 17
3.3.6.3 Larutan NaOH 0,1 N ... 18
3.3.7 Penentuan Kurva Serapan dan Linieritas Kurva Kalibrasi Asam Mefenamat ... 18
3.3.7.1 Pembuatan Larutan Induk Baku ... 18
3.3.7.2 Penentuan Kurva Serapan Asam Mefenamat ... 18
3.3.7.3 Penentuan Linieritas Kurva Kalibrasi Asam Mefenamat ... 18
3.4 Evaluasi Kaplet ... 19
3.4.1 Penetapan Kadar Asam Mefenamat dalam Kaplet ... 19
3.4.2 Uji Kekerasan Kaplet ... 19
3.4.3 Uji Friabilitas... 20
3.4.4 Uji Waktu Hancur ... 20
3.4.5 Uji Disolusi Kaplet ... 21
3.4.6 Analisis Data secara Statistik... 22
BAB IV HASIL DAN PEMBAHASAN ... 23
4.1 Isolasi Pati Kentang Merah ... 23
4.2 Hasil Uji Preformulasi Massa Granul ... 23
4.2.1 Uji Sudut Diam ... 24
4.2.2 Uji Waktu Alir ... 25
4.3 Hasil Evaluasi Kaplet ... 27
4.3.1 Hasil Pembuatan Kurva Serapan Maksimum dan Kurva Kalibrasi Asam Mefenamat BPFI dalam NaOH 0,1 N serta Penetapan Kadar Asam Mefenamat dalam Kaplet ... 27
4.3.2 Keragaman Bobot ... 29
4.3.3 Kekerasan Kaplet... 30
4.3.4 Waktu Hancur ... 31
4.3.5 Friabilitas ... 32
4.3.6 Uji Disolusi Kaplet ... 33
4.3.6.1 Hasil Pembuatan Kurva Serapan Maksimum dan Kurva Kalibrasi Asam Mefenamat BPFI dalam Dapar Fosfat pH 7,4 ... 33
4.3.6.2 Hasil Uji Disolusi Asam Mefenamat dalam Kaplet.. 34
BAB V KESIMPULAN DAN SARAN ... 36
5.1 Kesimpulan ... 36
5.2 Saran ... 36
DAFTAR PUSTAKA ... 37
DAFTAR TABEL
Halaman
Tabel 1. Formula Kaplet Asam Mefenamat ... 15
Tabel 2. Kriteria Penerimaan zat aktif yang Larut dengan Disolusi ... 22
Tabel 3. Data Uji Preformulasi Massa Granul ... 24
Tabel 4. Hasil Penetapan Kadar Kaplet Asam Mefenamat ... 28
Tabel 5. Data Hasil Evaluasi Kaplet ... 30
DAFTAR GAMBAR
Halaman Gambar 1. Pati Kentang Merah...23 Gambar 2. Sudut Diam Massa Granul dengan Jenis dan Persentase Bahan
Pengembang yang Berbeda ... 25
Gambar 3. Waktu Alir Massa Granul dengan Jenis dan Persentase Bahan
Pengembang yang Berbeda ... 26
Gambar 4. Indeks Tap Massa Granul dengan Jenis dan Persentase Bahan
Pengembang yang Berbeda ... 26
Gambar 5. Kurva Serapan Asam Mefenamat BPFI dalam NaOH 0,1 N
pada c = 10 mcg/ml ... 27
Gambar 6. Data Panjang Gelombang Maksimum dan Absorbansi Asam
Mefenamat BPFI dalam NaOH 0,1 N pada c = 10 mcg/ml .... 27
Gambar 7. Kurva Kalibrasi Asam Mefenamat BPFI dalam NaOH 0,1 N
secara Spektro Ultraviolet pada λ = 285 nm ... 28
Gambar 8. Kekerasan Kaplet dengan Jenis dan Persentase Bahan
Pengembang yang Berbeda ... 31
Gambar 9. Waktu Hancur Kaplet dengan Jenis dan Persentase Bahan
Pengembang yang Berbeda ... 32
Gambar 10. Friabilitas Kaplet dengan Jenis dan Persentase Bahan
Pengembang yang Berbeda ... 32
Gambar 11. Kurva Serapan Asam Mefenamat BPFI dalam Dapar Fosfat
pH 7,4 pada c = 10 mcg/ml... 33
Gambar 12. Data Panjang Gelombang Maksimum dan Absorbansi Asam
Mefenamat BPFI dalam Dapar Fosfat pH 7,4 pada
c = 10 mcg/ml... 33
Gambar 13. Kurva Kalibrasi Asam Mefenamat BPFI dalam Dapar Fosfat
pH 7,4 secara Spektro Ultraviolet pada λ = 286 nm... 34
Bahan Pengembang yang Berbeda dalam Dapar Fosfat pH 7,4... 35
DAFTAR LAMPIRAN Halaman Lampiran 1. Gambar Alat Pencetak Kaplet ... 38
Lampiran 2. Perhitungan Karakteristik Pati Kentang Merah ... 39
Lampiran 3. Perhitungan Pembuatan Kaplet Asam Mefenamat ... 40
Lampiran 4. Perhitungan Friabilitas Kaplet Asam Mefenamat ... 42
Lampiran 5. Data Hasil Uji Kekerasan, Uji Friabilitas dan Uji Waktu Hancur ... 43
Lampiran 6. Hasil Penentuan Persamaan Regresi dari Kurva Kalibrasi Asam Mefenamat BPFI pada Panjang Gelombang = 285 nm dalam NaOH 0,1 N ... 44
Lampiran 7. Hasil Penentuan Persamaan Regresi dari Kurva Kalibrasi Asam Mefenamat BPFI pada Panjang Gelombang = 286 nm dalam Dapar Fosfat pH 7,4 ... 46
Lampiran 8. Perhitungan Kadar Kaplet Asam Mefenamat ... 38
Lampiran 9. Perhitungan Keragaman Bobot ... 51
Lampiran 10. Perhitungan Hasil Uji Disolusi. ... 54
Lampiran 11. Hasil Penetapan Kadar Kaplet Asam Mefenamat pada Berbagai Perbandingan Konsentrasi Amilum Solani dan Formula Kaplet Pembanding ... 56
Lampiran 12. Gambar Kaplet Asam Mefenamat ... 57
Lampiran 13. Sertifikat Asam Mefenamat Baku Pembanding ... 58
Lampiran 14. Sertifikat Bahan Baku Asam Mefenamat. ... 59
Pembuatan Kaplet Asam Mefenamat secara Granulasi Basah dengan Pati Kentang Merah (Solanum tuberosum L.) sebagai Disintegran
ABSTRAK
Asam mefenamat merupakan salah satu bahan obat anti inflamasi non-steroid (AINS) yang bekerja sebagai analgesik untuk mengurangi/menghilangkan rasa sakit ringan sampai sedang. Karakteristik asam mefenamat yaitu kelarutannya yang praktis tidak larut dalam air. Efek samping tersering adalah gangguan saluran cerna, seperti diare dan peradangan abdomen.
Untuk mengatasi masalah tidak larutnya asam mefenamat ini, maka dilakukan formulasi kaplet asam mefenamat dengan menggunakan penambahan disintegran. Disintegran merupakan bahan tambahan (eksipien) dalam yang ditambahkan ke dalam formulasi kaplet untuk mendorong pecahnya kaplet ketika terjadi kontak dengan cairan. Disintegran yang digunakan disini adalah amilum solani yang diisolasi dari kentang merah. Konsentrasi amilum solani yang digunakan adalah 2%, 4%, 6% dan 8%, dan dibuat dengan metode granulasi basah. Kaplet yang dihasilkan dievaluasi dengan menggunakan parameter antara lain: kekerasan, friabilitas, waktu hancur, penetapan kadar, keseragaman sediaan, dan disolusi.
Hasil penelitian menunjukka n bahwa kaplet asam mefenamat yang dibuat dengan metode granulasi basah menggunakan amilum solani sebagai disintegran memenuhi persyaratan penetapan kadar, keragaman bobot, kekerasan, friabilitas. Walaupun tidak memenuhi persyaratan waktu hancur dan uji disolusi namun kaplet asam mefenamat memberikan hasil disolusi yang lebih baik dari kaplet pembanding dan tidak jauh berbeda dengan hasil disolusi kaplet yang telah ada di pasaran. Dengan kata lain amilum solani dapat digunakan sebagai disintegran pada pembuatan kaplet asam mefenamat.
Caplet Preparation of Mefenamic Acid with Wet Granulation Method Using Red Potato (Solanum tuberosum L.) Starch as Disintegration Agent
ABSTRACT
Mefenamic acid is one of non-steroidal anti-inflammatory drugs which works as analgesic for reducing slight to moderate pain. Mefenamic acid cannot dissolve in water. Common side effects are gastrointestinal disturbances, such as diarrhoea and abdominal discomfort.
To overcome this solubility problem, mefenamic acid caplet formulation is carried out by using the addition of disintegrant. Disintegrant is an additional materials (excipients) were added to the caplet formulation to encourage the breakup of the caplet when it comes in contact with liquid. Disintegrant used here is red potato starch. Its concentrations used were 2%, 4%, 6% and 8%, and made with the wet granulation method. The resulting caplets were evaluated using parameters such as: hardness, friability, disintegration time, determination, weight uniformity, and dissolution.
The result shows that mefenamic acid caplets which are prepared with wet granulation method using red potato starch as disintegrant fulfilled the requirements of content determining, weight uniformity, hardness, and friability analysis. Even the caplets not fulfilled of the requirements of disintegration and dissolution test but it gives a better result than the comparing caplets. It showed that potato starch can be used as disintegration agent in mefenamic acid caplet.
BAB I PENDAHULUAN 1.1 Latar Belakang
Sediaan tablet merupakan sediaan yang paling banyak diproduksi dan juga
banyak mengalami perkembangan dalam formulasinya. Beberapa keuntungan sediaan
tablet adalah sediaan lebih kompak, dosisnya tepat, mudah pengemasannya dan
penggunaannya lebih praktis dibanding sediaan yang lain (Lachman dkk., 1994).
Tablet merupakan sediaan padat kompak, dibuat secara kempa cetak, dalam
bentuk tabung pipih atau sirkuler, kedua permukaannya rata atau cembung,
mengandung satu jenis obat atau lebih dengan atau tanpa zat tambahan (Ditjen POM,
1979).
Pada pembuatan tablet, pati biasanya digunakan sebagai bahan tambahan yang
berfungsi sebagai bahan pengisi, pengikat dan pengembang. Pati bersifat hidrofilisasi
yaitu meninggikan porositas dan pembasahan tablet sehingga memudahkan penetrasi
air melalui pori – pori ke bagian dalam tablet yang menyebabkan percepatan
penghancuran tablet (Voigt, 1995). Efek porositas disebabkan oleh sifat pati yang
tidak termampatkan dan kohesifitasnya yang rendah. Hal ini menyebabkan
terbentuknya kapiler – kapiler di antara partikel – partikel tablet, yang menyebabkan
air dapat masuk ke dalam tablet sehingga dapat memecahkan tablet.
Bahan penghancur ditambahkan untuk memudahkan pecahnya atau hancurnya
tablet ketika kontak dengan cairan saluran pencernaan. Bahan penghancur berfungsi
bagian bagian. Fragmen tablet itu mungkin sangat menentukan kelarutan selanjutnya
dari obat dapat tercapainya bioavailabilitas yang diharapkan (Voigt, 1995).
Granulasi basah merupakan salah satu cara pembuatan tablet metode cetak tidak
langsung, yang lebih banyak digunakan dibandingkan dengan cara lain. Granul yang
dihasilkan lebih spheris sehingga tablet yang dihasilkan biasanya lebih kompak
(Soekemi, dkk., 1987).
1.2 Perumusan Masalah
Apakah pati kentang merah (Solanum tuberosum L.) dapat digunakan sebagai
disintegran pada pembuatan kaplet asam mefenamat secara granulasi basah?
1.3 Hipotesis
Pati kentang merah dapat digunakan sebagai disintegran untuk pembuatan kaplet
asam mefenamat secara granulasi basah.
1.4 Tujuan Penelitian
Tujuan dari penelitian ini untuk memformulasi kaplet asam mefenamat secara
granulasi basah dengan pati kentang merah sebagai disintegran.
1.5 Manfaat Penelitian
Manfaat penelitian ini adalah sebagai informasi kegunaan pati kentang merah
sebagai disintegran dalam pembuatan kaplet asam mefenamat yang bersifat praktis
BAB II
TINJAUAN PUSTAKA
2.1 Asam Mefenamat 2.1.1 Tinjauan Umum
Rumus bangun :
Rumus molekul : C
Nama kimia : Asam N-2,3-xililantranilat [61-68-7]
Berat molekul : 241,29
Pemerian : Serbuk hablur, putih atau hampir putih; melebur pada suhu
lebih kurang 230o disertai peruraian.
Kelarutan : Larut dalam larutan alkali hidroksida; agak sukar larut dalam
kloroform; sukar larut dalam etanol dan dalam metanol; praktis
tidak larut dalam air.
(Ditjen POM, 1995)
2.1.2 Farmakologi
Obat ini merupakan salah satu AINS yang mempunyai efek
analgetik-antipiretik. Efek analgetik zat ini dapat dimanfaatkan pada nyeri akut atau kronik
trauma. Waktu paruh dalam plasma 2 sampai 4 jam. Absorpsi berlangsung di usus;
terikat 99% pada protein plasma ( Clarke’s, 2004 ).
2.1.3 Efek Samping, Indikasi dan Sediaan
Indikasi zat ini ialah berbagai penyakit reumatik. Asam mefenamat dapat
menyebabkan iritasi lambung, kolik usus, dan diare. Gejala yang mungkin
berdasarkan kepekaan ialah eksantema makulopapulosa dan leukopenia. Zat ini tidak
boleh digunakan jika ada tukak lambung atau tukak usus, diare, kehamilan maupun
asma. Asam mefenamat tersedia dalam bentuk kapsul 250 mg dan kaplet 500 mg
(Zubaidi dkk., 1981 ).
2.2 Uraian Tumbuhan 2.2.1 Sistematika Tumbuhan
Sistematika dari kentang adalah sebagai berikut :
Kingdom : Plantae
Subkingdom : Tracheobionta
Divisi : Magnoliophyta
Kelas : Magnoliopsida
Sub Kelas : Asteridae
Ordo : Solanales
Famili : Solanaceae
Genus : Solanum
Kandungan kimia dari kentang ( Solanum tuberosum L.) antara lain :
karbohidrat 19 g, pati 15 g, serat pangan 2,2 g, lemak 0,1 g, protein 2 g, air 75 g.
2.3 Pati dan Sifat – Sifat Pati
Pati adalah sumber karbohidrat yang dihasilkan tumbuh – tumbuhan untuk
persediaan makanan yang dijumpai didalam biji (beras), umbi (kentang, ubi jalar),
dan batang (sagu). Pati merupakan butir atau granul yang berwarna putih mengkilat,
tidak berbau dan tidak berasa. Butiran pati yang mempunyai bentuk dan ukuran yang
beraneka ragam, tetapi pada umumnya berbentuk bola atau elips. Pati kentang
mengandung kadar pati sekitar 79,60% , kadar air 19,22% material Nitrogen 0,69%
dan 0,33% ( Bailliere, Tindal and Cox, 1952 ).
Pati biasanya berbentuk massa angular tidak beraturan atau bubuk putih. Tidak
larut dalam air dingin maupun membentuk larutan koloid jika dipanaskan dengan air
sejumlah sekitar 15 kali bobotnya. Larutan ini akan membentuk semacam jeli
transparan jika didinginkan. Musilago pati berwarna biru gelap pada perlakuan
dengan iodin, warna akan hilang pada pemanasan hingga 93oC tetapi muncul kembali
setelah dingin. Jika pati dipanaskan dengan air pertama – tama butirannya akan
mengembang dan kemudian membentuk gelatin ( Bailliere, Tindal and Cox, 1952 ).
Pada dasarnya pati merupakan polimer glukosa dengan ikatan ( 1,4 ) glukosa.
Pati terdiri dari dua fraksi yang dapat dipisahkan dengan air panas. Fraksi yang tidak
larut dalam air disebut amilopektin dan fraksi yang dapat larut dalam air disebut
amilosa (Leach, 1965).
Butiran pati terdiri dari bagian amorf dan bagian kristal. Bagian kristal terjadi
yang lainnya berikatan dengan ikatan hidrogen. Bagian kristal ini yang
mengakibatkan pati tidak larut dalam air (Colison, 1968).
2.4 Sediaan Tablet 2.4.1 Uraian Tablet
Tablet adalah sediaan padat mengandung bahan obat dengan atau tanpa bahan
pengisi. Sebagian besar tablet dibuat dengan cara pengempaan dan merupakan bentuk
sediaan yang paling banyak digunakan. Tablet kempa dibuat dengan memberikan
tekanan tinggi pada serbuk atau granul menggunakan cetakan baja (Ditjen POM,
1995).
Tablet dicetak dari serbuk kering, kristal atau granulat, umumnya dengan
penambahan bahan pembantu, pada mesin yang sesuai, dengan menggunakan tekanan
tinggi. Tablet dapat memiliki bentuk silinder, kubus, batang, atau cakram, serta
bentuk seperti telur atau peluru. Garis tengah tablet pada umumnya 5-17 mm,
sedangkan bobot tablet 0,1-1 g (Voigt, 1995).
2.4.2 Metode Pembuatan Tablet
Tablet dibuat dengan 3 cara umum, yaitu granulasi basah, granulasi kering
(mesin rol atau mesin slag) dan kempa langsung. Tujuan granulasi basah dan kering
adalah untuk meningkatkan aliran campuran dan atau kemampuan kempa (Ditjen
POM, 1995).
Butiran granulat yang diperoleh, partikel-partikelnya mempunyai daya lekat.
Daya alirnya menjadi lebih baik sehingga pengisian ruang cetak dapat berlangsung
secara kontiniu dan homogen. Keseragaman bentuk granulat menyebabkan
a. Granulasi basah
Zat berkhasiat, pengisi dan penghancur dicampur homogen, lalu dibasahi
dengan larutan pengikat, bila perlu ditambahkan pewarna. Diayak menjadi granul dan
dikeringkan dalam lemari pengering pada suhu 40-50°C. Setelah kering diayak lagi
untuk memperoleh granul dengan ukuran yang diperlukan dan ditambahkan bahan
pelicin dan dicetak dengan mesin tablet (Anief, 1994).
b. Granulasi kering
Metode ini digunakan pada keadaan dosis efektif terlalu tinggi untuk
pencetakan langsung, obatnya peka terhadap pemanasan, kelembaban, atau keduanya
(Lachman, dkk, 1994).
Setelah penimbangan dan pencampuran bahan, serbuk di slugged atau
dikompresi menjadi tablet yang lebar dan datar dengan garis tengah sekitar 1 inci.
Kempaan harus cukup keras agar ketika dipecahkan tidak menimbulkan serbuk yang
berceceran. Tablet kempaan ini dipecahkan dengan tangan atau alat dan diayak
dengan lubang yang diinginkan, pelicin ditambahkan dan tablet dikempa (Ansel,
1989).
c. Kompresi Langsung
Beberapa bahan obat seperti kalium klorida, kalium iodida, amonium klorida,
dan metenamin bersifat mudah mengalir, sifat kohesifnya juga memungkinkan untuk
langsung dikompresi tanpa memerlukan granulasi (Ansel, 1989).
Tablet oral umumnya di samping zat aktif mengandung, pengisi, pengikat,
penghancur, dan pelincir. Tablet tertentu mungkin memerlukan pemacu aliran, zat
warna, zat perasa, dan pemanis (Lachman, dkk, 1994).
Komposisi umum dari tablet adalah zat berkhasiat, bahan pengisi, bahan
pengikat atau perekat, bahan pengembang dan bahan pelicin. Kadang-kadang dapat
ditambahkan bahan pewangi (flavoring agent), bahan pewarna (coloring agent) dan
bahan-bahan lainnya (Ansel, 1989).
a. Pengisi
Digunakan agar tablet memiliki ukuran dan massa yang dibutuhkan. Sifatnya
harus netral secara kimia dan fisiologis, selain itu juga dapat dicernakan dengan baik
(Voigt, 1995). Bahan-bahan pengisi yaitu : laktosa, sukrosa, manitol, sorbitol,
amilum, bolus alba, kalsium sulfat, natrium sulfat, natrium klorida, magnesium
karbonat (Soekemi, dkk, 1987).
b. Pengikat
Untuk memberikan kekompakan dan daya tahan tablet, juga untuk menjamin
penyatuan beberapa partikel serbuk dalam butir granulat (Voigt, 1995). Pengikat yang
umum digunakan yaitu: amilum, gelatin, glukosa, gom arab, natrium alginat, cmc,
polivinilpirolidon, dan veegum (Soekemi, dkk, 1987).
c. Penghancur
Untuk memudahkan pecahnya tablet ketika berkontak dengan cairan saluran
pencernaan dan mempermudah absorpsi (Lachman, dkk, 1994). Bahan yang
digunakan sebagai pengembang yaitu: amilum, gom, derivat selulosa, alginat, dan
d. Pelicin
Ditambahkan untuk meningkatkan daya alir granul-granul pada corong
pengisi, mencegah melekatnya massa pada punch dan die, mengurangi pergesekan
antara butir-butir granul, dan mempermudah pengeluaran tablet dari die. Bahan
pelicin yaitu : metalik stearat, talk, asam stearat, senyawa lilin dengan titik lebur
tinggi, amilum maydis (Soekemi, dkk, 1987).
2.4.4 Uji Preformulasi
Sebelum dicetak menjadi tablet, massa granul perlu diperiksa apakah
memenuhi syarat untuk dapat dicetak. Preformulasi ini menggambarkan sifat massa
sewaktu pencetakan tablet, meliputi waktu alir, sudut diam dan indeks tap.
Pengujian waktu alir dilakukan dengan mengalirkan massa granul melalui
corong. Waktu yang diperlukan tidak lebih dari 10 detik, jika tidak maka akan
dijumpai kesulitan dalam hal keseragaman bobot tablet. Hal ini dapat diatasi dengan
penambahan bahan pelicin (Cartensen, 1977) .
Pengukuran sudut diam digunakan metode corong tegak, granul dibiarkan
mengalir bebas dari corong ke atas dasar. Serbuk akan membentuk kerucut, kemudian
sudut kemiringannya diukur. Semakin datar kerucut yang dihasilkan, semakin kecil
sudut diam, semakin baik aliran granul tersebut (Voigt, 1995).
Indeks tap adalah uji yang mengamati penurunan volume sejumlah serbuk
atau granul akibat adanya gaya hentakan. Indeks tap dilakukan dengan alat
volumenometer yang terdiri dari gelas ukur yang dapat bergerak secara teratur keatas
dan kebawah. Serbuk atau granul yang baik mempunyai indeks tap kurang dari 20%
2.4.5 Evaluasi Tablet
a. Kekerasan tablet
Ketahanan tablet terhadap goncangan saat pengangkutan, pengemasan dan
peredaran bergantung pada kekerasan tablet. Kekerasan yang lebih tinggi
menghasilkan tablet yang bagus, tidak rapuh tetapi ini mengakibatkan berkurangnya
porositas dari tablet sehingga sukar dimasuki cairan yang mengakibatkan lamanya
waktu hancur. Kekerasan dinyatakan dalam kg tenaga yang dibutuhkan untuk
memecahkan tablet. Kekerasan untuk tablet secara umum yaitu 4-8 kg, tablet hisap
10-20 kg, tablet kunyah 3 kg (Soekemi, dkk, 1987). Kekerasan tablet dipengaruhi
oleh perbedaan massa granul yang mengisi die pada saat pencetakan tablet dan
tekanan kompressi. Selain itu, berbedanya nilai kekerasan juga dapat diakibatkan oleh
variasi jenis dan jumlah bahan tambahan yang digunakan pada formulasi. Bahan
pengikat adalah contoh bahan tambahan yang bisa menyebabkan meningkatnya
kekerasan tablet bila digunakan terlalu pekat (Lachman, dkk, 1994).
b. Friabilitas
Tablet mengalami capping atau hancur akibat adanya goncangan dan gesekan,
selain itu juga dapat menimbulkan variasi pada berat dan keseragaman isi tablet.
Pengujian dilakukan pada kecepatan 25 rpm, menjatuhkan tablet sejauh 6 inci pada
setiap putaran, dijalankan sebanyak 100 putaran. Kehilangan berat yang dibenarkan
yaitu lebih kecil dari 0,5 sampai 1% (Lachman, dkk, 1994). Kerenyahan tablet dapat
dipengaruhi oleh kandungan air dari granul dan produk akhir. Granul yang sangat
menghasilkan tablet yang renyah daripada granul yang kadar kelembapannya 2
sampai 4% (Lachman, dkk, 1994).
c. Waktu hancur
Waktu hancur yaitu waktu yang dibutuhkan tablet pecah menjadi
partikel-partikel kecil atau granul sebelum larut dan diabsorpsi. Menyatakan waktu yang
diperlukan tablet untuk hancur di bawah kondisi yang ditetapkan dan lewatnya
seluruh partikel melalui saringan mesh-10 (Lachman, dkk, 1994). Hancurnya tablet
tidak berarti sempurna larutnya bahan obat dalam tablet. Tablet memenuhi syarat jika
waktu hancur tablet tidak lebih dari 15 menit (Soekemi, dkk, 1987). Kebanyakan
bahan pelicin bersifat hidrofob, bahan pelicin yang berlebihan akan memperlambat
waktu hancur. Tablet dengan rongga-rongga yang besar akan mudah dimasuki air
sehingga hancur lebih cepat daripada tablet yang keras dengan rongga-rongga yang
kecil (Soekemi, dkk, 1987).
d. Kadar zat berkhasiat
Untuk mengevaluasi kemanjuran suatu tablet, jumlah obat dalam tablet harus
dipantau pada setiap tablet atau batch, begitu juga kemampuan tablet untuk
melepaskan zat atau obat yang dibutuhkan harus diketahui (Lachman, dkk, 1994).
Persyaratan kadar berbeda-beda, dan tertera pada masing monografi
masing-masing bahan obat.
e. Keseragaman sediaan
Dapat ditentukan dengan salah satu dari dua metode :
- Keseragaman bobot dilakukan terhadap tablet yang 50% bahan aktifnya lebih
- Keseragaman kandungan dilakukan terhadap tablet yang 50% bahan aktifnya
kurang dari 50 mg (Ditjen POM,1995).
f. Disolusi
Yaitu larutnya obat dalam cairan pencernaan yang berhubungan langsung
dengan efikasi (kemanjuran) dari tablet dan perbedaan bioavailabilitas dari
berbagai formula (Lachman, dkk, 1994). Disolusi adalah suatu proses larutnya zat
aktif dari suatu sediaan dalam medium. Hal ini berlaku untuk obat-obat yang
diberikan secara oral dalam bentuk padat seperti tablet, kapsul, atau suspensi. Agar
suatu obat dapat diabsorbsi, mula-mula obat tersebut harus larut dalam cairan pada
tempat absorbsi. Suatu obat yang diberikan secara oral dalam bentuk tablet atau
kapsul tidak dapat diabsorbsi sampai partikel-partikel obat tersebut larut dalam
cairan pada suatu tempat dalam saluran lambung-usus (Ansel, 1989). Cara
pengujian disolusi tablet dan kapsul, juga persyaratan yang harus dipenuhi
dinyatakan dalam masing-masing monografi obat. Yang diukur adalah jumlah zat
berkhasiat yang larut dalam satu satuan waktu dengan alat dissolution tester
(Soekemi, dkk, 1987).
2.5 Spektrofotometri Ultraviolet
Spektrofotometri ultraviolet digunakan untuk analisa kualitatif ataupun
kuantitatif suatu senyawa. Absorpsi cahaya ultraviolet maupun cahaya tampak
mengakibatkan traansisi elektron, yaitu perubahan elektron-elektron dari orbital dasar
berenergi rendah ke orbital keadaan tereksitasi berenergi lebih tinggi. Penyerapan
radiasi ultraviolet atau sinar tampak tergantung pada mudahnya transisi elektron.
menyerap pada panjang gelombang yang lebih pendek. Molekul-molekul yang
memerlukan energi lebih sedikit akan menyerap panjang gelombang lebih panjang
(Fessenden dan Fessenden, 1992).
Sinar ultraviolet dan sinar tampak memberikan energi yang cukup untuk
terjadinya transisi elektronik. Dengan demikian spektra ultraviolet dan spektra
tampak dapat dikatakan sebagai spectra elektronik. Keadaan energi yang paling
rendah disebut keadaan dasar (ground state). Transisi-transisi elektronik akan
meningkatkan energi molekular dari keadaan dasar ke satu atau lebih dari tingkat
BAB III
METODOLOGI PENELITIAN
Metodologi penelitian ini adalah eksperimental. Penelitian meliputi isolasi
pati, pembuatan formulasi sediaan dan evaluasi dari sediaan.
3.1 Alat
Alat - alat yang digunakan dalam penelitian ini adalah Disintegration Tester
(Erweka), Dissolution Tester (Erweka DT), Strong Cobb Hardness Tester
(Erweka), Roche Friabilator (Erweka), Tapped Density Tester (Erweka),
Spektrofotometer UV (UV Mini 1240 Shimadzu), Stopwatch, Neraca listrik, alat -
alat gelas dan alat laboratorium lainnya.
3.2 Bahan
Bahan – bahan yang digunakan dalam penelitian ini adalah asam mefenamat
(MUTIFA), pati kentang merah, air suling, asam klorida p.a (E.Merck), asam
mefenamat BPFI (Badan POM), magnesium stearat (Brataco), talkum (Brataco),
laktosa, amilum manihot, primojel.
3.3 Prosedur Kerja
3.3.1 Isolasi Pati Kentang Merah
Kentang merah direndam dengan air secukupnya selama 24 jam, dikupas
kulitnya dan dicuci bersih, kemudian diblender, hasilnya dikumpulkan kemudian
disaring dengan kain belacu yang bersih. Pemerasan dilakukan berulang-ulang hingga
perasannya menjadi jernih. Hasil saringan diendapkan selama 24 jam. Patinya akan
patinya dilakukan beberapa kali sampai cairan di atas menjadi jernih. Endapan pati
dikeluarkan dari wadah, dikeringkan di dalam lemari pengering.
3.3.2 Evaluasi Terhadap Pati Hasil Isolasi 3.3.2.1 Penetapan Kadar Abu Total
Caranya: sebanyak 2 g serbuk yang telah digerus dan ditimbang seksama
dimasukkan dalam krus porselin yang telah dipijar dan ditara, kemudian diratakan.
Krus porselin dipijar perlahan-lahan sampai arang habis, pemijaran dilakukan pada
suhu 600oC selama 3 jam kemudian didinginkan dan ditimbang sampai diperoleh
bobot tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan di udara
(Ditjen POM, 1989).
3.3.2.2 Penetapan Susut Pengeringan
Caranya: sebanyak 5 g serbuk yang telah ditimbang seksama dimasukkan ke
dalam botol timbang bermulut lebar yang sudah konstan, keringkan pada suhu 105oC
dan didinginkan dalam eksikator kemudian ditimbang. Hal ini dilakukan sampai
didapat berat yang konstan. Kadar air dihitung dalam persen (WHO,1992).
3.3.3 Pembuatan Kaplet Asam Mefenamat
Metode pembuatan kaplet asam mefenamat secara granulasi basah dengan
bobot kaplet 600 mg dan penampang 18,6 x 4,8 mm. Amilum solani digunakan
sebagai bahan disintegran dengan konsentrasi 2%, 4%, 6%, dan 8% (formula 1-4).
Sedangkan sebagai pembanding digunakan Primojel dengan konsentrasi 4% (formula
5) dan amilum manihot dengan konsentrasi 10% (formula 6).
R/ Asam Mefenamat 500 mg
Tabel 1. Formula Kaplet Asam Mefenamat
(Formula untuk 100 kaplet) Keterangan :
F1 = Formula kaplet asam mefenamat dengan konsentrasi amilum solani 2% F2 = Formula kaplet asam mefenamat dengan konsentrasi amilum solani 4% F3 = Formula kaplet asam mefenamat dengan konsentrasi amilum solani 6% F4 = Formula kaplet asam mefenamat dengan konsentrasi amilum solani 8% F5 = Formula kaplet asam mefenamat dengan konsentrasi Primojel 4%
F6 = Formula kaplet asam mefenamat dengan konsentrasi amilum manihot 10%
3.3.4 Pembuatan Granul Asam Mefenamat
Ke dalam lumpang dimasukkan asam mefenamat, amilum solani (pengembang
dalam) dan laktosa, gerus hingga homogen. Kemudian tambahkan musilago amili
10% sedikit demi sedikit sambil digerus sampai diperoleh massa yang baik. Massa
digranulasi dengan ayakan mesh 12. Granulat basah dikeringkan dalam lemari
pengering pada suhu 40 – 60oC. Setelah kering granulat diayak kembali dengan
ayakan mesh 14 dan ditimbang, kemudian tambahkan magnesium stearat, talkum,
dan pati kentang merah (pengembang luar) dalam jumlah tertentu, diaduk hingga
homogen, lalu dicetak menjadi kaplet dengan bobot 600 mg dan penampang
berbentuk elips berdiameter 18,6 x 4,8 mm.
3.3.5 Uji Preformulasi
Uji preformulasi ini dilakukan terhadap massa granul yang telah dicampur
dengan pelicin dan pengembang luar.
3.3.5.1 Sudut Diam Massa Granul
Sebanyak 100 gram granul dimasukkan kedalam corong yang telah dirangkai,
permukannya diratakan. Lalu penutup bawah corong dibuka, biarkan granul mengalir
sampai habis. Selanjutnya tinggi kerucut yang terbentuk diukur.
Sudut diam dihitung dengan rumus :
Tangen θ = 2h/d Keterangan : θ = sudut diam
d = diameter
h = tinggi kerucut
Granul yang bersifat free flowing akan mempunyai sudut diam < 35o (Cartensen,
1977).
Sebanyak 100 gram granul dimasukkan kedalam corong yang telah dirangkai,
permukaannya diratakan. Penutup bawah corong dibuka dan secara serentak
stopwatch dihidupkan. Stopwatch dihentikan saat granul telah habis melewati corong
dan dicatat waktu alirnya.
Menurut Cartensen (1977), waktu alir yang diperlukan oleh sejumlah serbuk untuk
mengalir harus lebih singkat dari 10 detik.
3.3.5.3 Indeks Tap Granul
Dimasukkan granul kedalam gelas ukur 50 ml dan dinyatakan sebagai volume
awalnya (V1), kemudian gelas ukur dihentakkan sebanyak 20 kali dengan alat yang
dimodifikasi. Setelah hentakan, volumenya dinyatakan sebagai volume akhir (V2).
Indeks tap dapat dihitung dengan rumus :
%
V1 = Volume awal sebelum hentakan V2 = Volume akhir sesudah hentakan Syarat: I ≤ 20% (Cartensen, 1977)
3.3.6 Pembuatan Pereaksi
3.3.6.1 Air Suling Bebas Karbondioksida
Air suling yang telah dididihkan selama 5 menit atau lebih dan didiamkan
sampai dingin dan tidak boleh menyerap karbondioksida dari udara (Ditjen POM,
1995).
3.3.6.2 Pembuatan Dapar Fosfat pH 7,4
Dilarutkan kalium dihidrogen fosfat anhidrat sebanyak 47,6 gram dalam
ditambahkan 40 ml larutan natrium hidroksida 6 N kemudian diaduk homogen. Ke
dalam wadah kemudian ditambahkan air suling sampai 7 L. pH larutan diatur dengan
menambahkan larutan natrium hidroksida 6 N sampai pH 7,4 ± 0,05.
3.3.6.3 Larutan NaOH 0,1 N
Ditimbang sebanyak 4 gram pelet natrium hidroksida dan dilarutkan dengan
air suling sampai 1 L.
3.3.7 Penentuan Kurva Serapan dan Linieritas Kurva Kalibrasi Asam Mefenamat
3.3.7.1 Pembuatan Larutan Induk Baku
Ditimbang seksama 50 mg asam mefenamat BPFI, dimasukkan ke dalam labu
tentukur 100 ml. Dilarutkan dengan NaOH 0,1 N sampai garis tanda, lalu dikocok
homogen (konsentrasi 500 mcg/ml).
Dipipet sebanyak 10 mL larutan tersebut (500 mcg/ml), dimasukkan kedalam
labu tentukur 50 mL, dicukupkan dengan NaOH 0,1 N sampai garis tanda maka
diperoleh larutan induk baku dengan konsentrasi 100 mcg/ml.
3.3.7.2 Penentuan Kurva Serapan Asam Mefenamat
Dari LIB dipipet sebanyak 5 ml dan dimasukkan ke dalam labu tentukur 50
ml, diencerkan dengan NaOH 0,1 N sampai garis tanda. Dikocok homogen maka
akan diperoleh konsentrasi 10 mcg/ml. Diukur serapannya pada panjang gelombang
200 – 400 nm dan sebagai blanko digunakan larutan NaOH 0,1 N.
3.3.7.3 Penentuan Linieritas Kurva Kalibrasi Asam Mefenamat
Dari LIB dipipet masing – masing ; 2, 4, 5, 6, dan 7 ml, dimasukkan ke
tanda, sehingga diperoleh konsentrasi 4 mcg/ml, 8 mcg/ml, 10 mcg/ml, 12 mcg/ml,
dan 14 mcg/ml. Diukur serapannya pada panjang gelombang maksimum.
3.4 Evaluasi Kaplet
3.4.1 Penetapan Kadar Asam Mefenamat dalam Kaplet
Ditimbang seksama 20 kaplet, dicatat beratnya, kemudian digerus sampai
homogen. Ditimbang sejumlah serbuk setara dengan 50 mg asam mefenamat
sebanyak 6 kali, masing – masing dimasukkan ke dalam labu tentukur 100 ml
kemudian dicukupkan dengan NaOH 0,1 N sampai garis tanda. Dikocok homogen
maka diperoleh larutan dengan konsentrasi 500 mcg/ml. Disaring dan lebih kurang 25
ml filtrat pertama dibuang dan filtrat selanjutnya ditampung. Dari larutan tersebut
dipipet sebanyak 10 ml dan dimasukkan ke dalam labu tentukur 50 ml, diencerkan
dengan NaOH 0,1 N kemudian dicukupkan sampai garis tanda, maka diperoleh
larutan dengan konsentrasi 100 mcg/ml. Dipipet 5 ml dari larutan tersebut dan
dimasukkan dalam labu tentukur 50 ml, diencerkan dengan NaOH 0,1 N sampai garis
tanda maka diperoleh larutan dengan konsentrasi 10 mcg/ml. Kemudian diukur
serapannya pada panjang gelombang 285 nm dengan menggunakan NaOH 0,1 N
sebagai blanko.
3.4.2 Uji Kekerasan Kaplet
Alat : Strong Cobb Hardness Tester ( Erweka )
Cara :
Sebuah kaplet diletakkan tegak horizontal atau vertikal di antara anvil gan
menyala, knop ditekan dan dicatat angka yang ditunjukkan jarum penunjuk skala
pada saat kaplet pecah. Percobaan ini dilakukan untuk 5 kaplet.
Ketentuan umum : Kekerasan kaplet 4 – 8 kg ( Parrot, 1970 ).
3.4.3 Uji Friabilitas
Alat : Roche Friabilator ( Erweka )
Cara :
Ditimbang 20 kaplet yang telah dibersihkan dari debu, dicatat beratnya (a
gram). Kaplet dimasukkan ke dalam alat friabilator, lalu alat dijalankan selama 4
menit (100 kali putaran). Setelah batas waktu yang ditentukan kaplet dikeluarkan dan
dibersihkan dari debu, lalu ditimbang beratnya (b gram).
Friabilitas ( F ) = ( a – b ) / a x 100 %
Ketentuan umum : Kehilangan berat ≤ 1 % (Lachman dkk, 1994).
3.4.4 Uji Waktu Hancur
Alat : Disintegration Tester (Erweka)
Cara :
Pengujian dilakukan terhadap 6 kaplet. Dimasukkan 1 kaplet pada masing –
masing tabung dari keranjang, dimasukkan satu cakram pada tiap tabung, kemudian
alat dijalankan. Digunakan air dengan suhu 37˚ ± 2˚ C sebagai media. Pada akhir batas waktu seperti yang tertera pada monografi, angkat keranjang dan amati keenam
kaplet. Semua kaplet harus hancur sempurna. Bila 1 atau 2 kaplet tidak hancur
sempurna ulangi pengujian dengan 12 kaplet lainnya, tidak kurang dari 16 kaplet dari
Persyaratan : Waktu yang diperlukan untuk menghancurkan kaplet tidak lebih dari
15 menit untuk kaplet tidak bersalut ( Ditjen POM, 1979 ).
3.4.5 Uji Disolusi Kaplet
Untuk menguji laju disolusi kaplet dilakukan dengan menggunakan alat
Dissolution Tester.
Medium : 900 ml dapar fosfat pH 7,4
Alat : tipe 2 ( metode dayung )
Kecepatan putaran : 100 rpm
Waktu : 60 menit
Cara :
Satu kaplet dimasukkan ke dalam wadah disolusi yang telah berisi 900 ml
medium disolusi yang bersuhu 37˚ ± 0,5˚ C. Kemudian dayung diputar dengan kecepatan 100 rpm. Sampel alikuot diambil sebanyak 5 ml pada menit ke 5, 10, 15,
30, 45, dan 60 menit. Kemudian serapan diukur pada panjang gelombang 286 nm dan
sebagai blanko digunakan dapar fosfat pH 7,4. Volume medium diusahakan tetap
dengan menambahkan medium dapar fosfat pH 7,4 sebanyak 5 ml setelah pemipetan.
Pengujian dilakukan terhadap 6 kaplet.
Persyaratan : Dalam waktu 45 menit harus larut tidak kurang dari 75% ( Q )
C15H15NO2 dari jumlah yang tertera pada etiket ( USP XXVI, 2003 ).
Interpretasi : Persyaratan dipenuhi bila jumlah zat aktif yang terlarut dari sediaan
yang diuji sesuai dengan tabel penerimaan. Apabila tidak memenuhi persyaratan
maka pengujian dilanjutkan sampai tiga tahap, kecuali bila hasil pengujian memenuhi
dalam masing – masing monografi, dinyatakan dalam persentase kadar pada etiket,
angka 5% dan 15% dalam tabel adalah persentase kadar pada etiket, dengan demikian
mempunyai arti yang sama dengan Q.
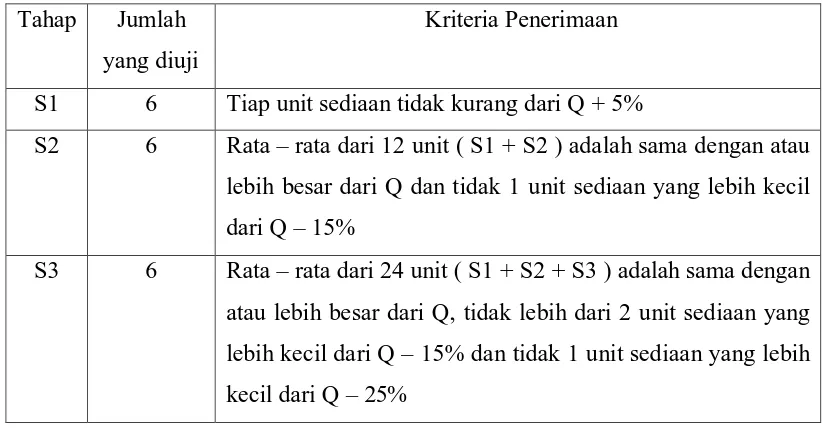
Tabel 2. Kriteria Penerimaan Zat Aktif yang Larut dengan Disolusi
Tahap Jumlah yang diuji
Kriteria Penerimaan
S1 6 Tiap unit sediaan tidak kurang dari Q + 5%
S2 6 Rata – rata dari 12 unit ( S1 + S2 ) adalah sama dengan atau lebih besar dari Q dan tidak 1 unit sediaan yang lebih kecil dari Q – 15%
S3 6 Rata – rata dari 24 unit ( S1 + S2 + S3 ) adalah sama dengan atau lebih besar dari Q, tidak lebih dari 2 unit sediaan yang lebih kecil dari Q – 15% dan tidak 1 unit sediaan yang lebih kecil dari Q – 25%
(Ditjen POM, 1995)
3.4.6 Analisis Data Secara Statistik
Kadar zat aktif sebenarnya yang terkandung dalam sampel dapat diketahui
menggunakan uji distribusi t. Data diterima atau ditolak dihitung dengan
menggunakan metode standar deviasi dengan rumus :
n = jumlah perlakuan
(
)
n SDx x
thitung = −
Dimana:
x= pKa sampel; −x= pKa rata-rata sampel; SD = Standar deviasi; n = jumlah perlakuan
Dengan dasar penolakan data adalah : t hitung > t tabel atau t hitung < -t tabel dan dasar
BAB IV
HASIL DAN PEMBAHASAN 4.1 Isolasi Pati Kentang Merah ( Solanum tuberosum L. )
Dari 10.000 gram kentang merah diperoleh pati sebanyak 550 gram, sehingga
rendemen pati kentang merah 5,5% (lampiran 2, hal. 29). Pati kentang merah yang
diperoleh berwarna putih sampai putih kecoklatan, tidak berbau, tidak berasa. Butir
pati kentang merah berbentuk bulat lonjong mempunyai lamella dan hilus yang
berada di ujungnya. Kadar abu pada pati kentang merah sebesar 0,6798% dan kadar
air sebesar 3,2744% (lampiran 2, hal.29) dimana keduanya masih memenuhi
persyaratan Materia Medika yaitu kadar abu tidak lebih dari 0,6% untuk tiap 1 gram
sampel dan kadar air tidak lebih dari 20%.
1
2
Gambar 1. Pati kentang merah (perbesaran 10 x 40).
Keterangan: 1. Hilus 2. Lamella
4.2 Hasil Uji Preformulasi Massa Granul
Sebelum massa granul dicetak menjadi kaplet dilakukan uji preformulasi yang
massa granul agar dapat diketahui apakah granul tersebut memenuhi syarat untuk
dicetak menjadi kaplet.
Tabel 3. Data Uji Preformulasi Massa Granul
Formula
F1 = Formula kaplet asam mefenamat dengan konsentrasi amilum solani 2% F2 = Formula kaplet asam mefenamat dengan konsentrasi amilum solani 4% F3 = Formula kaplet asam mefenamat dengan konsentrasi amilum solani 6% F4 = Formula kaplet asam mefenamat dengan konsentrasi amilum solani 8% F5 = Formula kaplet asam mefenamat dengan konsentrasi Primojel 4%
F6 = Formula kaplet asam mefenamat dengan konsentrasi amilum manihot 10%
4.2.1 Uji Sudut Diam
Dari tabel 3. dapat dilihat bahwa sudut diam dari variasi konsentrasi amilum
solani semakin menurun dari F1-F4. yaitu dari 29,0068 – 27,6773. Hal ini
menunjukkan bahwa semakin meningkat konsentrasi amilum solani yang digunakan
sebagai bahan pengembang maka aliran granul semakin baik (bersifat free flowing)
sehingga sudut diamnya kecil. Hal ini terjadi karena semakin banyak konsentrasi
amilum solani yang ditambahkan akan mengakibatkan granul yang terbentuk semakin
sedikit sehingga meningkatkan kelincirannya dan mengakibatkan sudut diamnya
menjadi kecil. Sudut diam yang lebih tinggi mengakibatkan granul susah mengalir
ketidakseragaman bobot kaplet. Menurut Voigt (1984), sudut diam antara 25° dan
45° memiliki aliran yang baik pada waktu pencetakan kaplet.
Sudut Diam
Gambar 2. Sudut Diam Massa Granul dengan Jenis dan Persentase Bahan
Pengembang yang Berbeda
4.2.2 Uji Waktu Alir
Berdasarkan tabel 1. dapat dilihat bahwa waktu alir semakin cepat dengan
bertambahnya konsentrasi amilum solani yang digunakan sebagai bahan
pengembang. yaitu F1>F2>F3>F4. Hal ini disebabkan karena adanya penambahan
konsentrasi amilum solani yang digunakan dapat meningkatkan kelincirannya,
sehingga waktu yang dibutuhkan granul untuk mengalir dari corong akan semakin
kecil. Menurut Cartensen (1977), partikel yang lebih besar memiliki waktu alir yang
lebih kecil, dan akan menghasilkan kaplet yang baik dalam hal keseragaman bentuk
Waktu Alir
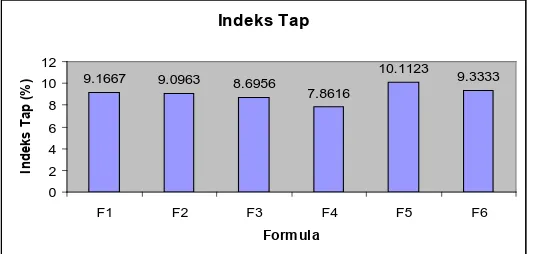
4.2.3 Uji Indeks Tap
Indeks tap dipengaruhi oleh bentuk, ukuran dan kekerasan granul. Dari tabel 1
di bawah. diperoleh data indeks tap dari F1 hingga F4 adalah sebesar 9.1667% ,
9.0963% , 8.6956% , dan 7.8616%. Hal ini berarti semakin besar konsentrasi bahan
pengembang yang digunakan maka indeks tap akan semakin kecil pula. Indeks tap
berperan penting dalam menentukan granul tersebut layak dicetak menjadi kaplet atau
tidak, di mana indeks tap menunjukkan daya tahan granul terhadap daya kompresi
dari alat pencetak kaplet. Menurut Guyot (1978), granul yang memiliki sifat alir yang
baik mempunyai indeks tap ≤ 20%. Hal ini menunjukkan bahwa uji indeks tap pada semua formula memenuhi standar yang telah ditentukan.
Pengembang yang Berbeda
4.3 Hasil Evaluasi Kaplet
4.3.1 Hasil Pembuatan Kurva Serapan Maksimum dan Kurva Kalibrasi
Asam Mefenamat BPFI dalam NaOH 0,1 N serta Penetapan Kadar Asam Mefenamat dalam Kaplet
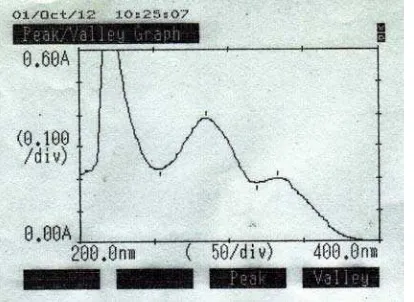
Menurut Moffat et al(2005), asam mefenamat memberikan serapan maksimum
pada panjang gelombang 285 nm di dalam larutan NaOH 0,1 N. Hal ini sesuai dengan
hasil pengukuran secara spektrofotometri ultraviolet larutan asam mefenamat BPFI
dalam NaOH 0,1 N yang dilakukan. di mana diperoleh serapan maksimum pada
panjang gelombang 285 nm (gambar 5) dengan serapan 0,3893 (gambar 6).
Gambar 5. Kurva Serapan Asam Mefenamat BPFI dalam NaOH 0,1 N pada
Gambar 6. Data Panjang Gelombang Maksimum dan Absorbansi
Asam Mefenamat BPFI dalam NaOH 0,1 N pada c = 10 mcg/ml
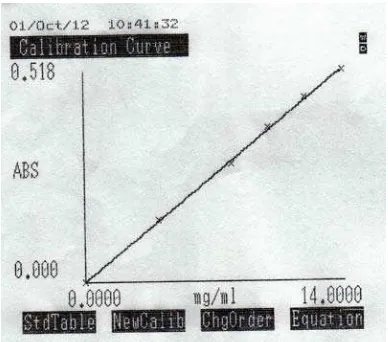
Dari hasil penentuan linieritas kurva kalibrasi asam mefenamat BPFI dalam
rentang konsentrasi 4,0 mcg/ml hingga 14,0 mcg/ml pada λmaks = 285 nm (gambar 7)
diperoleh persamaan regresi : Y = 0,037206X + 0,001152 dengan nilai r = 0,9996.
Dengan nilai r yang mendekati 1, dapat dikatakan terdapat kolerasi yang dekat antara
konsentrasi dengan pengukuran.
Gambar 7. Kurva Kalibrasi Asam Mefenamat BPFI dalam NaOH 0,1 N secara
Spektro Ultraviolet pada λ = 285 nm
Tabel 4. Hasil Penetapan Kadar Kaplet Asam Mefenamat
No Formula Kadar ( % )
1 F1 100.5750 ± 5.8636
2 F2 103.4083 ± 5.8897
3 F3 102.6267 ± 5.5484
4 F4 106.2883 ± 2.2209
5 F5 102.1767 ± 3.5558
6 F6 100.2617 ± 1.7848
Keterangan :
F1 = Formula kaplet asam mefenamat dengan konsentrasi amilum solani 2% F2 = Formula kaplet asam mefenamat dengan konsentrasi amilum solani 4% F3 = Formula kaplet asam mefenamat dengan konsentrasi amilum solani 6% F4 = Formula kaplet asam mefenamat dengan konsentrasi amilum solani 8% F5 = Formula kaplet asam mefenamat dengan konsentrasi Primojel 4%
F6 = Formula kaplet asam mefenamat dengan konsentrasi amilum manihot 10%
Menurut USP XXVI (2003) kaplet asam mefenamat mengandung asam
mefenamat tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang
tertera pada etiket. Dari hasil penetapan kadar kaplet asam mefenamat, dimana kadar
kaplet F1 (amilum solani 2%) sebesar 100.58%, F2 (amilum solani 4%) sebesar
103.41%, F3 (amilum solani 6%) sebesar 102.63%, F4 (amilum solani 8%) sebesar
106.29%, F5 (Primojel 4%) sebesar 102.18%, dan F6 (amilum manihot 10%) sebesar
100.26% terlihat bahwa kadar tablet yang diperoleh bervariasi, tetapi kadar tersebut
masih memenuhi persyaratan yang ditetapkan dalam USP XXVI (2003). Kadar asam
mefenamat dalam kaplet berkisar antara 100.26% sampai 106.29%.
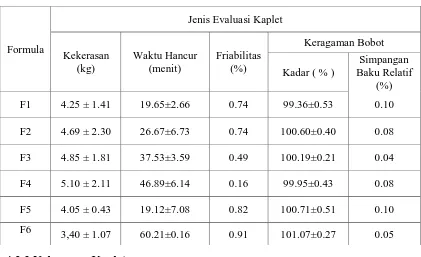
4.3.2 Keragaman Bobot
Dari tabel 5 di bawah ini dapat dilihat bahwa keragaman bobot kaplet asam
mefenamat berkisar antara 99.36% hingga 101.07% dengan simpangan baku relatif
antara 0.04% - 0.10%. Berdasarkan hal tersebut, maka keragaman bobot dari kaplet
asam mefenamat memenuhi persyaratan yang ditetapkan oleh Farmakope Indonesia
edisi IV (1995) yaitu jika jumlah zat aktif dalam masing-masing dari 10 satuan
sediaan terletak antara 85.0% hingga 115.0% dari yang tertera pada etiket, atau jika
simpangan baku relatif kurang dari atau sama dengan 6.0%. Dilihat berdasarkan hasil
simpangan baku relatifnya, maka dapat disimpulkan bahwa kaplet yang tercetak
faktor yang mempengaruhi keseragaman isi kaplet, yaitu tidak seragamnya distribusi
bahan obat pada pencampuran bubuk atau granulasi. pemisahan dari campuran bubuk
atau granulasi selama proses pembuatan dan penyimpangan berat kaplet.
Tabel 5. Data Hasil Evaluasi Kaplet
4.3.3 Kekerasan Kaplet
Hasil uji kekerasan seperti yang terlihat pada tabel 5. menunjukkan bahwa
kekerasan semakin meningkat dengan meningkatnya konsentrasi amilum solani yang
ditambahkan pada kaplet hingga pada konsentrasi 8%. yaitu F1>F2>F3>F4. Hal ini
disebabkan karena kuatnya ikatan granul membentuk kaplet sehingga kaplet menjadi
lebih keras. Namun pada uji kekerasan yang dilakukan pada F6, hasil yang diperoleh
adalah 3.40 sehingga pada pengujian ini kaplet pada F6 tidak memenuhi syarat,
karena menurut Parrot (1971), kekerasan kaplet akan memenuhi syarat pada rentang
4-8 kg. Hal ini terjadi karena kandungan pati dari amilum manihot dan amilum solani
tidaklah sama. Hasil yang menunjukkan nilai yang hampir sama dengan bahan
pembanding Primojel adalah konsentrasi amilum solani sebanyak 2% yaitu F2.
Kekerasan Tablet
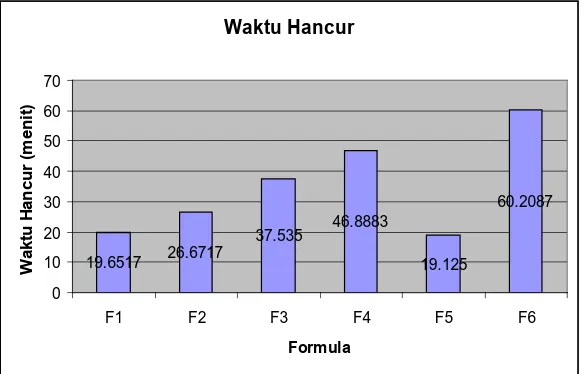
Berdasarkan data dari tabel 5, maka hasil pengujian waktu hancur terhadap
kaplet dapat diketahui di mana semakin meningkat konsentrasi amilum solani yang
digunakan maka semakin lambat waktu hancur kaplet. Pada grafik terlihat bahwa
waktu hancur dari F1 dan F5 memiliki nilai yang hampir sama, F1 memiliki
kekerasan 4.25 dan F5 memiliki kekerasan 4.05 dimana keduanya memiliki
kekerasan yang hampir sama, namun berbeda jauh dengan waktu hancur kaplet
dengan bahan pembanding amilum manihot. Hal ini terjadi karena kandungan dari
amilum solani dan amilum manihot tidaklah sama. Kaplet dengan bahan pengembang
amilum solani 2% akan terkikis sedikit demi sedikit pada waktu pengujian,
partikel kasar hingga kemudian larut dalam pelarutnya. Menurut Parrot (1971), waktu
hancur kaplet dipengaruhi oleh sifat fisik dan kimia dari bahan tambahan yang
digunakan, kekerasan dan porositas dari kaplet.
Waktu Hancur
Gambar 9. Waktu Hancur Kaplet dengan Jenis dan Persentase
Bahan Pengembang yang Berbeda
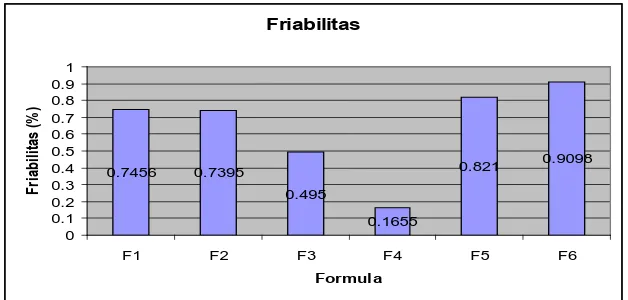
4.3.5 Friabilitas
Dari tabel 5 di atas juga dapat diketahui bahwa semakin meningkat konsentrasi
amilum solani maka friabilitas kaplet semakin menurun hingga pada F4. Dari tabel
tersebut dapat diketahui bahwa friabilitas berbanding terbalik dengan kekerasan
kaplet. Dengan kata lain, semakin meningkat kekerasan kaplet maka friabilitas kaplet
akan semakin kecil. Menurut Lachman dkk.. (1994) kehilangan berat lebih kecil dari
0.5% sampai 1% masih dapat dibenarkan. Sehingga pada pengujian ini seluruh
Friabilitas
Gambar 10. Friabilitas Kaplet dengan Jenis dan Persentase Bahan
Pengembang yang Berbeda
4.3.6 Uji Disolusi Kaplet
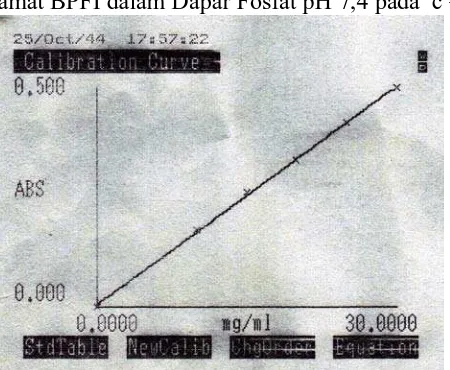
4.3.6.1 Hasil Pembuatan Kurva Serapan Maksimum dan Kurva Kalibrasi Asam Mefenamat BPFI dalam Dapar Fosfat pH 7,4
Hasil pengukuran secara spektrofotometri ultraviolet dengan menggunakan
dapar fosfat pH 7,4 diperoleh serapan maksimum asam mefenamat BPFI pada
panjang gelombang 286 nm dengan serapan 0,3656 (gambar 12).
Gambar 11. Kurva Serapan Asam Mefenamat BPFI dalam Fosfat pH 7,4 pada
Gambar 12. Data Panjang Gelombang Maksimum dan Absorbansi Asam
Mefenamat BPFI dalam Dapar Fosfat pH 7,4 pada c = 10 mcg/ml
Gambar 13. Kurva Kalibrasi Asam Mefenamat BPFI dalam Dapar Fosfat pH 7,4
secara Spektro Ultraviolet pada λ = 286 nm
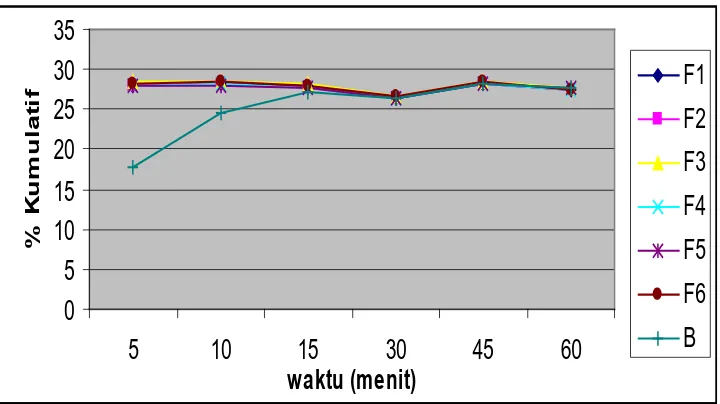
4.3.6.2 Hasil Uji Disolusi Asam Mefenamat dalam Sediaan Kaplet
Dari hasil uji disolusi kaplet yang dapat dilihat pada tabel 6 diketahui bahwa
persen kumulatif asam mefenamat yang terlarut pada menit ke-45 dari formula F1
sebesar 28.22% formula F2 sebesar 28.23% formula F3 sebesar 28.46% formula F4
sebesar 28.32% formula F5 sebesar 28.15% dan formula F6 sebesar 28.49% dan
menunjukkan bahwa formula amilum solani tidak memenuhi persyaratan USP XXVI
etiket yang terdisolusi dalam waktu 45 menit. Oleh karena itu, dilakukan juga uji
disolusi dari kaplet asam mefenamat yang ada di pasaran Bernostan® (Bernofarm).
Namun kaplet Bernostan® juga memberikan hasil disolusi yang tidak berbeda jauh
yaitu sebesar 28,26% pada menit ke-45. Hal ini menjelaskan mengapa asam
mefenamat harus diberikan dalam dosis tinggi untuk memberikan efek terapi (Tan,
2005).
Tabel 6. Hasil Uji Disolusi Kaplet Asam Mefenamat
Waktu (menit)
Persentase Kumulatif Asam Mefenamat yang Terlepas ( % )
F1 F2 F3 F4 F5 F6 B
5 28.07±0.28 28.08±0.37 28.34±0.20 27.85±0.15 27.85±0.15 28.13±0.38 17.78
10 28.30±0.16 28.27±0.35 28.56±0.69 28.16±0.38 28.05±0.48 28.60±0.00 24.66
15 27.96±0.19 27.78±0.35 28.11±0.39 27.57±0.13 27.57±0.13 27.85±0.27 27.21
30 26.49±0.20 26.49±0.20 26.77±0.15 26.30±0.00 26.33±0.10 26.51±0.17 26.51
45 28.22±0.15 28.23±0.29 28.46±0.31 28.32±0.51 28.15±0.60 28.49±0.36 28.26
Keterangan :
F1 = Formula kaplet asam mefenamat dengan konsentrasi amilum solani 2% F2 = Formula kaplet asam mefenamat dengan konsentrasi amilum solani 4% F3 = Formula kaplet asam mefenamat dengan konsentrasi amilum solani 6% F4 = Formula kaplet asam mefenamat dengan konsentrasi amilum solani 8% F5 = Formula kaplet asam mefenamat dengan konsentrasi Primojel 4%
BAB V
KESIMPULAN DAN SARAN 5.1 Kesimpulan
Dari data dapat ditarik kesimpulan bahwa amilum solani dapat digunakan sebagai
bahan pengembang pada pembuatan kaplet asam mefenamat yang merupakan bahan
aktif obat yang bersifat praktis tidak larut dalam air, terbukti dari hasil uji disolusi
kaplet asam mefenamat yang dibuat sendiri memberikan pelepasan bahan obat yang
lebih cepat daripada kaplet asam mefenamat yang ada di pasaran Bernostan®
(Bernofarm).
5.2 Saran
Disarankan pada peneliti selanjutnya untuk menggunakan bahan aktif lain yang
DAFTAR PUSTAKA
Ansel, H.C. (1989). Pengantar Bentuk Sediaan Farmasi. Edisi IV. Jakarta: UI Press. Halaman 96
Bailliere, Tindal and Cox. (1952). A Text Book of Pharmacognosy. Sixth Edition. London. Pages 732-739
Cartensen, J.T. (1977). Pharmaceutics of Solids and Solid Dosage Forms. New York: John Wiley and Sons. A Wiley Interscience Publication. Pages
133-135, 209-214, 216-218 and 342
Collison, G.K. (1968). Sweeling and Gelation of Starch, Starch and It’s Derivates. London: Chapman and Hall Ltd. Page 171
Ditjen POM. (1979). Farmakope Indonesia. Edisi III. Jakarta: Departemen Kesehatan RI. Halaman 8, 748 dan 755
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan RI. Halaman 5-6, 43, 999, 1085 dan 1143
Gandjar, I.B., Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar. Halaman 17
Lachman, L., Lieberman, H.A., Kanig, J.L. (1994). Teori dan Praktek Farmasi
Industri. Edisi III. Jakarta: UI Press. Halaman 651-654, 657-660 dan 697
Moffat, A.C., Osselton, M.D., Widdop, B. (2004). Clarke’s Analysis of Drug and
Poisons. Third Edition. London: Pharmaceutical Press. Page 89
Parrot, E.L. (1971). Pharmaceutical Technology Fundamental Pharmaceutics. Minneapolis: Burgess Publishing Company. Pages 82-83
Soekemi, R.A., Yuanita, T., Fat Aminah, Salim Usman. (1987). Tablet. Medan: PT Mayang Kencana. Halaman 5 dan 54
Tan, H.T., Rahardja, K. (2008). Obat-Obat Penting. Edisi VI. Cetakan Kedua. Jakarta: PT Elex Media Komputindo. Halaman 318 dan 331
Voigt, R., (1995). Buku Pelajaran Teknologi Farmasi. Edisi Kelima. Yogyakarta: Gadjah Mada University Press. Halaman 200, 221 and 222
Zubaidi, J. (1981). Farmakologi dan Terapi. Editor Sulistiawati. Jakarta: UI Press. Halaman 172
Lampiran 2. Perhitungan Karakteristik Pati Kentang Merah
Berat kentang merah segar = 10000 gram
Berat pati kentang merah = 550 gram
Rendemen pati kentang merah = berat pati kentang merah
berat kentang merah segar x 100%
Berat pati kentang merah = 3,6925 gram
Berat abu = 0,0251 gram
Berat awal pati kentang merah = 4,8650 gram
Berat akhir pati kentang merah = 4,7057 gram
Lampiran 3. Contoh Perhitungan Pembuatan Kaplet Asam Mefenamat
Sebagai contoh diambil kaplet asam mefenamat dengan konsentrasi 4% (Formula 2).
Dibuat formula untuk 100 kaplet, dengan berat kaplet 600 mg dan penampang elips
18,6 x 4,8 mm.
Berat 100 kaplet = 100 x 0,600 g = 60 g
Berat asam mefenamat dalam kaplet = 100 x 500 mg = 50000 mg = 50 g
Dengan menggunakan bahan pengembang amilum solani 4%:
a. Pengembang dalam = 2% x 60 g = 1,200 g
b. Pengembang luar = 2% x 60 g = 1,200 g
c. Mg stearat = 1% x 60 g = 0,6 g
d. Talkum = 1% x 60 g = 0,6 g
e. Pengikat :
i. Bahan pengikat yang digunakan dalam formula adalah musilago amili 10% yang
dibuat sebanyak 30% = 30% x 60 g = 18 g
ii. Amilum manihot yang ditimbang = 10% x 18 g = 1,80 g
f. Laktosa = 60 g – ( 50 + 1,2 + 1,2 + 0,6 + 0,6 + 1,8 )g
= 4,6 g
Cara Kerja : metode granulasi basah
1. Asam mefenamat + laktosa + amilum solani (pengembang dalam), digerus
2. Ditambahkan musilago amili sedikit demi sedikit sampai diperoleh massa
yang kompak. Musilago amili 10% yang terpakai adalah 14,80 g yang
mengandung amilum manihot 1,480 g.
3. Digranulasi dengan ayakan mesh 12.
4. Dikeringkan pada temperatur 40°C - 60°C.
5. Setelah kering, diayak lagi dengan ayakan mesh 14.
a. Berat massa secara teoritis :
= (bahan obat + pengembang dalam + pengikat + pengisi)
= (50 + 1,20 + 1,48 + 4,60)g = 57,28 g
6. Ditambahkan amilum solani (pengembang luar), talkum, Mg stearat lalu
diaduk hingga homogen.
Lampiran 4. Contoh Perhitungan Friabilitas Kaplet Asam Mefenamat
A = Bobot kaplet sebelum diputar dalam alat friabilator
B = Bobot kaplet setelah diputar dalam alat friabilator
Syarat Friabilator kaplet :
Kehilangan bobot tidak boleh lebih dari 1% (F ≤ 1%)
Sebagai contoh diambil kaplet asam mefenamat dengan konsentrasi amilum
solani 8% (F4)
Bobot 20 kaplet sebelum diputar = 12,08 g
Bobot 20 kaplet setelah diputar = 12,06 g
Lampiran 5. Data Hasil Uji Kekerasan, Uji Friabilitas, dan Uji Waktu Hancur
a. Uji Kekerasan Kaplet
No. Kekerasan Kaplet (Kg)
F1 F2 F3 F4 F5 F6
1. 4,25 3,75 4,25 4 3,75 2,75
2. 5 4,2 3,75 5,5 4 3
3. 3,25 6,5 6 4 4,25 3,75
4. 4,75 5 5,25 6 4 4
5. 4 4 5 6 4,25 3,5
Rata-rata 4,25±1,41 4,69±2,30 4,85±1,81 5,10±2,11 4,05±0,43 3,40±1,07
b. Uji Friabilitas
No. Formula Bobot 20 kaplet (gram) Friabilitas
(%) Sebelum (a) Sesudah (b)
1. F1 12,07 11,98 0,75
2. F2 12,17 12,08 0,74
3. F3 12,12 12,06 0,50
4. F4 12,08 12,06 0,17
5. F5 12,18 12,08 0,82
6. F6 12,09 11,98 0,91
c. Uji Waktu Hancur
No. Waktu Hancur (menit)
F1 F2 F3 F4 F5 F6
1. 16,9500 21,5800 34,3700 41,6700 14,8800 60,1247
3. 19,4200 26,3200 37,8800 45,0100 16,9500 60,1700
4. 20,1300 29,5800 39,0800 49,2800 18,0800 60,1730
5. 20,6700 29,8300 39,2200 49,9500 22,1700 60,2875
6. 21,6700 30,7700 39,3800 51,0500 26,3200 60,3661
Rata-rata 19,65±2,66 26,67±6,73 37,54±3,54 46,89±6,14 19,13±7,08 60,21±0,16
Lampiran 6. Hasil Penentuan Persamaan Regresi dari Kurva Kalibrasi
Asam Mefenamat BPFI pada Panjang Gelombang = 285 nm dalam NaOH 0,1 N
Tabel Data Kurva Kalibrasi
= 0,2988 – (0,037206).(8)
= 0,001152
Persamaan regresi diperoleh dengan mensubstitusikan nilai a dan b, sehingga
persamaan regresi adalah:
Y = 0,037206X + 0,001152
Dengan nilai r sebagai berikut:
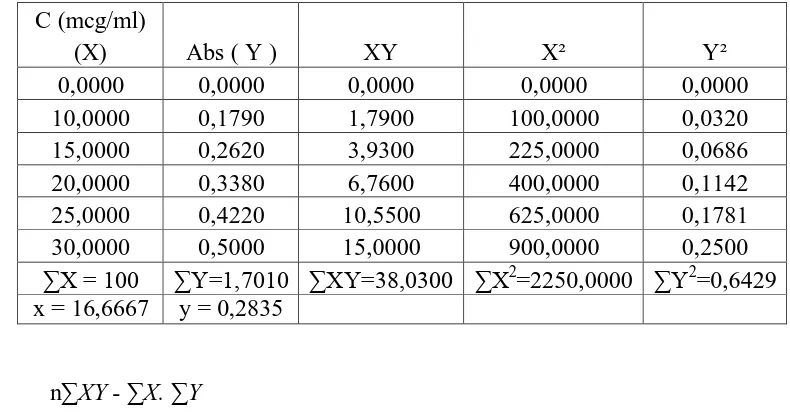
Lampiran 7. Hasil Penentuan Persamaan Regresi Dari Kurva Kalibrasi
Asam Mefenamat BPFI pada Panjang Gelombang = 286 nm dalam Dapar Fosfat pH 7,4
Tabel Data Kurva Kalibrasi
b = Y – a X
= 0,2835 – (0,016594).(16,6667)
= 0,006933
Persamaan regresi diperoleh dengan mensubstitusikan nilai a dan b, sehingga
persamaan regresi adalah:
Y = 0,016594X – 0,006933
Dengan nilai r sebagai berikut: