PERBANDINGAN BILANGAN PEROKSIDA
PADA MINYAK JAGUNG DAN MINYAK CURAH
DENGAN METODE IODOMETRI
TUGAS AKHIR
OLEH :
Marshinta Romarta Uly Hutabalian
NIM 122410081
PROGRAM STUDI DIPLOMA III
ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PERBANDINGAN BILANGAN PEROKSIDA
PADA MINYAK JAGUNG DAN MINYAK CURAH
DENGAN METODE IODOMETRI
TUGAS AKHIR
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Ahli Madya Pada Program Studi Diploma III Analis Farmasi dan Makanan
Fakultas FarmasiUniversitas Sumatera Utara
OLEH :
MARSHINTA ROMARTA ULY HUTABALIAN
NIM 122410081
PROGRAM STUDI DIPLOMA III
ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KATA PENGANTAR
Puji dan syukur penulis sampaikan kepada Tuhan Yang Maha Esa karena
hanya oleh kasih karunia dan penyertaan-Nya lah penulis mampu menyelesaikan
penulisan Tugas Akhir ini.
Penulisan Tugas Akhir ini dilaksanakan dengan tujuan untuk memenuhi
persyaratan dalam menyelesaikan pendidikan pada Program Studi Diploma III
Analis Farmasi dan Makanan Fakultas Farmasi Universitas Sumatera Utara,
Medan. Adapun judul dari Tugas Akhir ini adalah: Perbandingan Bilangan Peroksida Pada Minyak Jagung dan Minyak Curah dengan Metode Iodometri. Penulisan Tugas Akhir ini didasarkan pada hasil Praktek Kerja Lapangan yang diperoleh pada 02 – 13 Februari 2015 di Laboratorium Minyak
Nabati dan Rempah-Rempah, UPT. Balai Pengujian dan Sertifikasi Mutu Barang
Medan.
Dalam penulisan Tugas Akhir ini, penulis banyak menghadapi kendala dan
masalah. Akan tetapi atas bantuan dan dorongan dari banyak pihak, akhirnya
Tugas Akhir ini dapat diselesaikan. Oleh karena itu, pada kesempatan ini dengan
kerendahan dan ketulusan hati penulis menyampaikan ucapan terimakasih kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas
Farmasi Universitas Sumatera Utara.
2. Ibu Prof. Dr. Julia Reveny, M.Si., Apt., selaku Wakil Dekan I Fakultas
3. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt., selaku Ketua Program
studi Diploma III Analis Farmasi dan Makanan Fakultas Farmasi
Universitas Sumatera Utara
4. IbuDra. Suwarti Aris, M.Si., Apt. selaku dosen pembimbing yang telah
memberikan arahan dan membimbing penulis dalam penulisan Tugas Akhir.
5. Ibu Dra. Nazlinywati, M.Si., Apt., selaku dosen penasehat akademik penulis.
6. IbuIr. Novira Dwi Shanty Artsiwi selaku pembimbing lapangan selama
penulis melaksanakan PKL di UPT. Balai Pengujian dan Sertifikasi Mutu
Barang Medan.
7. Ibu Darwati, selaku Penyelia Laboratorium Minyak Nabati dan
Rempah-Rempah beserta pegawai di UPT. Balai Pengujian dan Sertifikasi Mutu
Barang Medan yang telah banyak mengarahkan dan membimbing penulis
selama PKL.
Terlebih kepada orangtua penulis, Amri Hutabalian/ Rosmida br. Siboro,
saudara kandung penulis dan keluarga besar yang telah memberikan dukungan
doa, dorongan semangat dan materil dalam penulisan Tugas Akhir ini.
Akhir kata, penulis mengucapkan terima kasih kepada semua pihak yang
telah membantu dan memberi semangat namun tidak dapat penulis sebutkan satu
per satu. Semoga Tugas Akhir ini bermanfaat bagi kita semua.
Medan, April2015 Penulis,
PERBANDINGAN BILANGAN PEROKSIDA PADA MINYAK JAGUNG DAN MINYAK CURAH
DENGAN METODE IODOMETRI ABSTRAK
Minyak selalu dibutuhkan oleh manusia misalnya: untuk memasak. Oleh sebab itu mutu minyak harus diperhatikan.Mutu minyak ditentukan oleh rasa, aroma dan ketengikan.Nilai ketengikan dinyatakan dengan bilangan peroksida. Penentuan bilangan peroksida dilakukan dengan cara titrasi iodometri yang mempergunakan larutan natrium tiosulfat 0,01 N sebagai pentiter. Prinsip dari bilangan peroksida adalah senyawa dalam lemak akan dioksidasi oleh KI dan lod yang dilepaskan dititrasi dengan natrium tiosulfat. Semakin tinggi bilangan peroksida semakin tinggi pula tingkat ketengikan suatu minyak.
Tujuan dalam penulisan ini adalah untuk mengetahui apakah bilangan peroksida dari minyak jagung dan minyak curah memenuhi persyaratan bilangan peroksida yang ditetapkan dalam Standar Nasional Indonesia (SNI) dan untuk membandingkan kualitas minyak jagung dan minyak curah dari nilai bilangan peroksida sebelum proses penggorengan.
Hasil analisis menuniukkan bahwa minyak jagung 2,6327 mek O2/kgdan
minyak curah 4,9724 mek O2/kg. Minyak atau lemak apabila mengalami oksidasi
maka senyawa peroksida yang dihasilkan akan meningkat dan semakin banyak jumlah ml NaS2O3 yang digunakan,maka semakin besar pula nilai bilangan
peroksida yang didapatkan. Hasil penentuan bilangan peroksida minyak jagung dan minyak curah memenuhi syarat Standar Nasional Indonesia (SNI) yaitu tidak lebih dari 10 mek O2/kg dan dengan membandingkan nilai bilangan peroksida
kedua minyak maka minyak jagung mempunyai kualitas lebih baik daripada minyak kelapa sawit (minyak curah).
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
DAFTAR ISI ... vii
DAFTAR LAMPIRAN ... x
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Tujuan ... 3
1.3 Manfaat ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Jagung ... 4
2.1.1 Sejarah Tanaman Jagung ... 4
2.1.2 Sistematika Tanaman Jagung ... 5
2.1.3 Morfologi Tanaman Jagung ... 5
2.1.4 Komposisi Kimia Biji Jagung ... 6
2.2 Kelapa Sawit ... 7
2.2.2 Sistematika Tanaman Kelapa Sawit ... 8
2.2.3 Morfologi Tanaman Kelapa Sawit ... 8
2.3 Minyak ... 10
2.4 Minyak Goreng ... 11
2.5 Minyak Jagung ... 13
2.5.1 Komposisi Minyak Jagung ... 15
2.5.2 Sifat Fisiko-Kimia ... 15
2.5.3 Daya Guna dan Nilai Gizi ... 16
2.6 Minyak Kelapa Sawit ... 16
2.6.1 Komposisi Kimia Minyak Kelapa Sawit ... 17
2.6.2 Sifat Fisiko-Kimia ... 18
2.6.3 Standar Mutu ... 19
2.7 Bilangan Peroksida ... 19
2.8 Metode Iodometri ... 21
BAB III METODE PENGUJIAN ... 23
3.1 Tempat dan Waktu Pengujian ... 23
3.2 Alat ... 23
3.3 Bahan ... 23
3.4 Pembuatan Pereaksi ... 23
3.5 Prosedur Pengujian ... 25
BAB IV HASIL DAN PEMBAHASAN ... 27
4.1 Hasil ... 27
BAB V KESIMPULAN DAN SARAN ... 30
5.1 Kesimpulan ... 30
5.2 Saran ... 30
DAFTAR PUSTAKA ... 31
DAFTAR LAMPIRAN
Lampiran Halaman
1. Perhitungan Standarisasi Natrium Tiosulfat (Na2S2O3) 0,01 N ... 33
2. Perhitungan Penentuan Bilangan Peroksida ... 34
3. Pengujian Minyak Jagung ... 36
DAFTAR TABEL
Tabel Halaman
2.1 Komposisi Biji Jagung Kering ... 7
2.2 Parameter Syarat Mutu Minyak Jagung ... 14
2.3 Komposisi Minyak Jagung ... 15
2.4 Komposisi Asam Lemak Minyak Sawit dan Inti Kelapa Sawit ... 17
2.5 Nilai Sifat Fisiko-Kimia Minyak Sawit dan Inti Sawit ... 18
4.1 Data Penentuan Bilangan Peroksida Pada Minyak Jagung ... 27
DAFTAR GAMBAR
Gambar Halaman
1.Minyak Jagung ... 36
2. Indikator Amilum ... 36
3. Erlenmeyer Berisi Hasil Standarisasi Na2S2O3 0,01 N ... 37
4. Erlenmeyer Berisi Blanko ... 37
5. Erlenmeyer Berisi Minyak Jagung Dan Pelarut ... 38
6. Erlenmeyer Berisi Minyak Jagung Hasil Titrasi ... 38
7. Minyak Kelapa Sawit ... 39
8. Erlenmeyer Berisi Minyak Curah Dan Pelarut ... 39
PERBANDINGAN BILANGAN PEROKSIDA PADA MINYAK JAGUNG DAN MINYAK CURAH
DENGAN METODE IODOMETRI ABSTRAK
Minyak selalu dibutuhkan oleh manusia misalnya: untuk memasak. Oleh sebab itu mutu minyak harus diperhatikan.Mutu minyak ditentukan oleh rasa, aroma dan ketengikan.Nilai ketengikan dinyatakan dengan bilangan peroksida. Penentuan bilangan peroksida dilakukan dengan cara titrasi iodometri yang mempergunakan larutan natrium tiosulfat 0,01 N sebagai pentiter. Prinsip dari bilangan peroksida adalah senyawa dalam lemak akan dioksidasi oleh KI dan lod yang dilepaskan dititrasi dengan natrium tiosulfat. Semakin tinggi bilangan peroksida semakin tinggi pula tingkat ketengikan suatu minyak.
Tujuan dalam penulisan ini adalah untuk mengetahui apakah bilangan peroksida dari minyak jagung dan minyak curah memenuhi persyaratan bilangan peroksida yang ditetapkan dalam Standar Nasional Indonesia (SNI) dan untuk membandingkan kualitas minyak jagung dan minyak curah dari nilai bilangan peroksida sebelum proses penggorengan.
Hasil analisis menuniukkan bahwa minyak jagung 2,6327 mek O2/kgdan
minyak curah 4,9724 mek O2/kg. Minyak atau lemak apabila mengalami oksidasi
maka senyawa peroksida yang dihasilkan akan meningkat dan semakin banyak jumlah ml NaS2O3 yang digunakan,maka semakin besar pula nilai bilangan
peroksida yang didapatkan. Hasil penentuan bilangan peroksida minyak jagung dan minyak curah memenuhi syarat Standar Nasional Indonesia (SNI) yaitu tidak lebih dari 10 mek O2/kg dan dengan membandingkan nilai bilangan peroksida
kedua minyak maka minyak jagung mempunyai kualitas lebih baik daripada minyak kelapa sawit (minyak curah).
BAB I PENDAHULUAN
1.1 Latar Belakang
Minyak dapat digunakan sebagai medium penggoreng bahan pangan,
misalnya keripik kentang, kacang dan sebagainnya yang banyak dikonsumsi di
restoran dan hotel.Kurang lebih 290 juta lemak dan minyak dikonsumsi tiap tahun
untuk kripik kentang saja. Banyak jumlah permintaan akan bahan pangan
digoreng, merupakan suatu bukti yang nyata mengenai betapa besarnya jumlah
bahan pangan digoreng yang dikonsumsi oleh lapisan masyarakat dari segala
tingkat umur (Ketaren, 1986).
Dalam penggorengan, minyak goreng berfungsi sebagai medium penghantar
panas, menambah rasa gurih, menambah nilai gizi dan kalori dalam bahan
pangan.Lemak yang baik digunakan adalah lemak babi, oleo stearin atau lemak
nabati dihidrogenasi dengan titik cair 35 – 40 OC, minyak kelapa, kacang tanah,
kelapa sawit (Ketaren, 1986).
Kerusakan minyak selama proses penggorengan akan mempengaruhi mutu
dan nilai dari minyak dan bahan yang digoreng. Pada minyak yang rusak terjadi
proses oksidasi, polimerisasi dan hidrolisis. Proses tersebut menghasilkan
peroksida yang bersifat toksik dan asam lemak bebas yang sukar dicerna oleh
tubuh (Ketaren, 1986).
Senyawa polimer yang dihasilkan akibat pemanasan yang berulang- ulang
pembengkaan organ tubuh, diare, kanker dan depresi pertumbuhan. Selain itu
akan timbul rasa tengik akibat oksidasi yang pengaruhnya tidak diharapkan pada
bahan pangan yang digoreng. Pengaruh tersebut antara lain mengakibatkan
kerusakan gizi, tekstur dan cita rasa (Gunawan, 2003).
Indikator kerusakan minyak antara lain adalah angka peroksida dan asam
lemak bebas. Angka peroksida menunjukkan banyaknya kandungan peroksida di
dalam minyak akibat proses oksidasi dan polimerisasi. Asam lemak bebas
menunjukkan sejumlah asam lemak bebas yang dikandung oleh minyak yang
rusak, terutama karena peristiwa oksidasi dan hidrolisis (Gunawan, 2003).
Minyak jagung kaya akan kalori yaitu sekitar 250 kalori per ons. Minyak
jagung merupakan minyak goreng yang stabil (tahan terhadap ketengikan) karena
adanya tokoferol yang larut dalam minyak (Ketaren, 1986).
Kelapa sawit adalah lemak semi padat yang mempunyai komposisi yang
tetap. Kandungan karoten dapat mencapai 1000 ppm atau lebih, tetapi dalam
minyak dari jenis tenera kurang lebih 500 – 700 ppm, kandungan tokoferol
bervariasi dan dipengaruhi oleh penanganan selama produksi (Ketaren, 1986).
Perlunya pengawasan mutu adalah untuk menjamin bahwa minyak jagung
dan minyak kelapa sawit hasil produksi memenuhi persyaratan yang ditetapkan.
Berangkat dari permasalahan akan pentingnyapengawasan terhadap mutu minyak
1.2 Tujuan
Adapun tujuan tugas akhir ini adalah untuk mengetahui apakah bilangan
peroksida dari minyak jagung dan minyak curah memenuhi persyaratan bilangan
peroksida yang ditetapkan dalam Standar Nasional Indonesia (SNI) dan untuk
membandingkan kualitas minyak jagung dan minyak curah dari nilai bilangan
peroksida sebelum proses penggorengan.
1.3 Manfaat
Manfaat yang diperoleh dari penentuan bilangan peroksida pada minyak
jagung dan minyak curah adalah agar dapat mengetahui bahwa produk minyak
goreng tersebut yang beredar di pasaran memenuhi persyaratan bilangan
peroksidamenurut Standar Nasional Indonesia (SNI) sehingga produk tersebut
layak untuk dipasarkan dan dikonsumsi serta untuk memberikan perbandingan
kualitas minyak jagung dan minyak curah dari nilai bilangan peroksida sebelum
BAB II
TINJAUAN PUSTAKA
2.1 Jagung
2.1.1 Sejarah Tanaman Jagung
Jagung adalah tanaman yang berasal dari Amerika Tengah, tetapi karena
penemuan baru di dunia, tanaman ini telah menyebar ke berbagai daerah tropis
dan sub-tropis lainnya.Di Amerika Serikat hampir seperempat dari areal tanaman
dikhususkan untuk budidaya jagung, terutama untuk biji-bijian.Tanaman jagung
pada umumnya digunakan untuk pakan ternak (Vaughan, 1970).
Tanaman jagung (Zea maysL) di Indonesia merupakan tanaman pangan
yang penting setelah padi dan terdapat hampir di seluruh kepulauan
Indonesia.Umumnya jagung sebagian besar masih digunakan sebagai bahan
pangan penduduk serta sebagai sumber minyak. Penyebaran daerah tanaman
jagung di Indonesia tidak merata karena adanya pengaruh iklim, keadaan tanah,
keadaan hama serta fluktuasi harga jagung (Ketaren, 1986).
Di Indonesia, jagung merupakan bahan pangan sumber karbohidrat kedua
setelah beras. Disamping sebagai bahan pangan, komoditi ini juga sebagai bahan
pakan ternak dan bahan baku industri. Menurut data yang dihimpun oleh Biro
Pusat Statistik, penggunaan jagung untuk bahan pangan menurun dari 78% pada
tahun 1975 menjadi 49% pada tahun 1985. Sebaliknya, penggunaan untuk pakan
ternak dan industri meningkat dari 15% pada tahun 1975 menjadi 38% pada tahun
Di Amerika dan negara-negara lain yang lebih maju, jagung kebanyakan
digunakan sebagai makanan ternak serta bahan baku pembuatan minyak jagung,
sirup dan hanya sebagian digunakan sebagai makanan pokok (Ketaren, 1986).
2.1.2 Sistematika Tanaman Jagung
Tanaman jagung memiliki klasifikasi berdasarkan tingkatan taksonomi
secara botani sebagai berikut :
Kingdom : Plantae
Divisi : Spermatophyta
Sub Divisi : Angiospermae
Kelas : Monocotyledone
Ordo : Graminae
Famili : Graminaceae
Genus : Zea
Spesies : Zea mays L. (Subekti, 2015).
2.1.3 Morfologi Tanaman Jagung
a. Batang
Batangnya berbentuk bulat atau agak pipih, beruas-ruas dan umumnya tidak
bercabang (Najiyati, 1999).
b. Akar
Sistem perakaran jagung terdiri atas akar primer, akar lateral, akar
c. Daun
Daun jagung tumbuh disetiap ruas batang. Daun ini berbentuk pipa,
mempunyai lebar 4 - 15 cm dan panjang 30 - 150 cm, serta didukung oleh pelepah
daun yang menyelubungi batang (Najiyati, 1999).
d. Bunga
Bunga jantan tumbuh di ujung batang.Bunga betina tersusun dalam
tongkol.Bunga ini muncul dari ketiak daun yang terletak pada pertengahan batang
(Najiyati, 1999).
e. Tongkol dan Biji
Tanaman jagung mempunyai satu atau dua tongkol, tergantung
varietas.Tongkol jagung yang terletak pada bagian atas umumnya lebih dahulu
terbentuk dan lebih besar dibanding yang terletak pada bagian bawah.Setiap
tongkol terdiri atas 10-16 baris biji yang jumlahnya selalu genap (Subekti, 2015).
2.1.4 Komposisi Kimia Biji Jagung
Jagung sebagai bahan makanan, mengandung nilai gizi yang cukup tinggi
jika dibanding dengan bahan pangan lainnya, terutama jagung kuning yang
banyak mengandung vitamin A (Ketaren, 1986).
Biji jagung terdiri dari empat bagian utama yaitu bagian kulit ari,
endosperm, lembaga dan gluten.Kulit ari terdiri dari serat kasar yang
membungkus bagian endosperm dan embrio, beratnya 5 - 6 persen dari berat
butiran biji jagung.Endosperm mempunyai lapisan aleuron yang mengandung zat
Lemak terdapat pada bagian bawah dari butiran biji jagung beratnya sekitar
9 - 12 persen dari berat butiran. Karbohidrat terdapat pada endosperm sekitar 73 -
79 persen, kadar protein dalam endosperm sekitar 10 - 19 persen dan 22,4 persen
pada kulit ari (Ketaren, 1986).
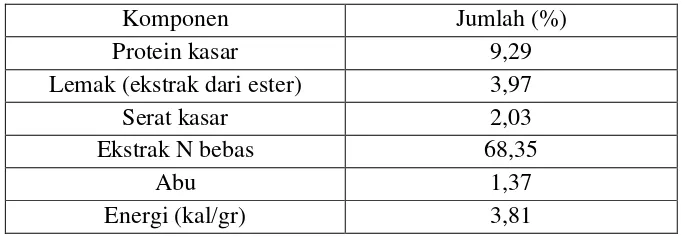
Komposisi biji jagung kering dapat dilihat pada tabel 2.1.
Tabel 2.1 Komposisi Biji Jagung Kering
Komponen Jumlah (%) Protein kasar 9,29 Lemak (ekstrak dari ester) 3,97 Serat kasar 2,03 Ekstrak N bebas 68,35
Abu 1,37
Energi (kal/gr) 3,81
2.2 Kelapa Sawit
2.2.1 Sejarah Tanaman Kelapa Sawit
Tanaman kelapa sawit (Elaeis guineensis Jacq) berasal dari Nigeria, Afrika
Barat.Meskipun demikian, ada yang menyatakan bahwa kelapa sawit berasal dari
Amerika Selatan, yakni Brazil karena lebih banyak ditemukan spesies kelapa
sawit di Hutan Brazil dibandingkan dengan Afrika.Kelapa sawit pertama kali
diperkenalkan di Indonesia oleh Pemerintah Kolonial Belanda pada tahun
1848.Ketika itu hanya ada empat batang bibit kelapa sawit yang dibawa dari
Réunion atau Mauritius dan Hortus Botanicus Amsterdam yang ditanam di Kebun
Raya Bogor (Fauzi, 2002).
Tanaman kelapa sawit mulai dibudidayakan secara komersial dan menjadi
dirintis oleh Adrien Hallet, seorang berkebangsaan Belgia.Ia membangun
perkebunan kelapa sawit pertama dalam skala besar di daerah Sungai Liput
(Pantai Timur Aceh) dan daerah Pulu Raja (Asahan). Luas areal perkebunan
kelapa sawit pertama sudah mencapai 3.250 ha (Fauzi, 2002).
2.2.2 Sistematika Tanamana Kelapa Sawit
Tanaman kelapa sawit memiliki klasifikasi berdasarkan tingkatan taksonomi
secara botani sebagai berikut (Mangoensoekarjo, 2000).
Kingdom : Plantae
Divisi : Tracheophyta
Kelas : Angiospermae
Ordo : Arecales
Famili : Palmae (Arecaceae)
Genus : Elaeis
Spesies : Elaeis guineensis Jacq.
2.2.3 Morfologi Tanaman Kelapa Sawit
Kelapa sawit termasuk tanaman monokotil.Tanaman ini merupakan
tanaman berumah satu (monoecious) dimana bunga jantan dan bunga betina
terdapat dalam satu pohon.Bagian tanaman kelapa sawit dapat dibedakan atas dua
bagian, yaitu bagian generatif dan vegetatif.Bagian generatif sebagai alat
perkembangbiakan meliputi bunga dan buah, sedangkan bagian vegetatif meliputi
a. Akar
Tanaman kelapa sawit mempunyai akar serabut. Akar kelapa sawit akan
tumbuh ke bawah dan ke samping membentuk akar primer, sekunder, tertier, dan
akar kuarterner (Mangoensoekarjo, 2000).
b. Batang
Kelapa sawit termasuk tanaman monokotil maka batangnya tidak
mempunyai kambium dan pada umumnya tidak bercabang.Pembengkakan
pangkal batang (bole) terjadi karena internodia (ruas batang) dalam masa
petumbuhan awal tidak memanjang, sehingga pangkal-pangkal pelepah daun yang
tebal berdesakan.Tinggi maksimum tanaman kelapa sawit yang ditanam di
perkebunan antara 15-18 m,sedangkan di alam mencapai 30 m (Mangoensoekarjo,
2000).
c. Daun
Susunan daun tanaman kelapa sawit mirip dengan tanaman kelapa yaitu
membentuk susunan daun majemuk. Daun-daun tersebut akan membentuk suatu
pelepah daun yang panjangnya dapat mencapai kurang lebih 7,5-9 m. Jumlah anak
daun pada tiap pelepah berkisar antara 250-400 helai. Daun muda yang masih
kuncup berwarna kuning pucat (Mangoensoekarjo, 2000).
d. Buah
Buah kelapa sawit termasuk jenis buah keras (drupe), menempel dan
bergerombol pada tandan buah.Jumlah per tandan dapat mencapai 1.600,
berbentuk lonjong sampai bulat.Panjang buah 2-5 cm, beratnya sampai 30
Warna buah kelapa sawit tergantung pada varietas dan umurnya.Buah yang
masih muda berwarna hijau pucat kemudian berubah menjadi hijau
hitam.Semakin tua warna buah menjadi kuning muda dan pada waktu sudah
masak berwarna merah kuning (jingga)(Mangoensoekarjo, 2000).
e. Bunga
Tanaman kelapa sawit sudah mulai berbunga pada umur 12-14
bulan.Tanaman ini merupakan bunga tanaman berumah satu, artinya pada satu
tanaman terdapat bunga jantan dan betina yang masing-masing terangkai dalam
satu tandan(Mangoensoekarjo, 2000).
f. Biji
Waktu proses perkecambahan berlangsung, embrio mengembang
(volumenya bertambah), bakal batang dan bakal akar tumbuh keluar dari
cangkang melalui lubang pada cangkang tersebut (germ pore) dan berkembang
selanjutnya menjadi batang, daun dan akar (Mangoensoekarjo, 2000).
2.3 Minyak
Minyak dan lemak merupakan bagian dari lipid yang berbeda satu dengan
yang lainnya dalam apakah berada dalam bentuk cairan (minyak) atau padatan
(lemak) dalam suhu kamar.Sifat fisika ini terutama tergantung pada asam lemak
yang terkandung di dalamnya. Kebanyakan lemak hewani adalah padat, sementara
minyak nabati adalah cair, meskipun demikian ada minyak nabati yang bersifat
Satu sifat yang khas dan mencirikan golongan lipida (termasuk minyak dan
lemak) adalah daya larutnya dalam pelarut organik (misalnya eter, benzene,
kloroform) atau sebaliknya ketidak-larutannya dalam pelarut air.Lemak dan
minyak atau secara kimiawi adalah trigliserida (lebih dari 80 – 85% lipid)
merupakan senyawa hasil kondensasi satu molekul gliserol dengan tiga molekul
asam lemak (Sudarmadji, 1989).
Zat warna dalam minyak terdiri dari dua golongan yaitu zat warna alamiah
dan warna dari hasil degradasi zat warna alamiah. Zat warna yang tergolong zat
warna alamiah yaitu zat warna yang secara alamiah di dalam bahan yang
mengandung minyak dan ikut terekstrak bersama minyak pada proses ekstraksi.
Zat warna tersebut antara lain terdiri dari α dan β karoten, xantofil, klorofil, dan
antosianin, zat warna ini menyebabkan minyak berwarna kuning, kuning
kecokelatan,kehijau-hijauan dan kemerahan-merahan (Ketaren, 1986).
Pigmen berwarna merah jingga atau kuning disebabkan oleh karotenoid
yang bersifat larut dalam minyak.Karotenoid merupakan persenyawaan
hidrokarbon tidak jenuh.Jika minyak dihidrogenasi, karoten tersebut juga ikut
terhidrogenasi, sehingga intensitas warna kuning berkurang.Karotenoid bersifat
tidak stabil pada suhu tinggi.Karotenoid tersebut tidak dapat dihilangkan dengan
proses oksidasi (Ketaren, 1986).
2.4 Minyak Goreng
Menggoreng adalah suatu proses untuk memasak bahan pangan
minyak goreng kedalam ketel penggorengan, kemudian dipanaskan, selanjutnya
dimasukkan bahan yang akan digoreng. Dari ketel akan diperoleh hasil gorengan,
uap yang dihasilkan dari lemak, serta hasil samping lemak akibat pemanasan dan
penggorengan serta kerak. Berbagai faktor mempengaruhi kondisi penggorengan
dalam ketel, yaitu pemanasan dengan adanya udara, minyak yang kelewat panas
(local over heating of fat), aerasi pada lemak, kontak lemak dengan logam dari
ketel, kontak bahan pangan dengan minyak, adanya kerak dan partikel yang
gosong. Dari faktor-faktor tersebut, maka pemanasan dengan adanya udara
merupakan faktor yang sangat berpengaruh (Ketaren, 1986).
Minyak goreng berfungsi sebagai penghantar panas, penambah rasa gurih,
dan penambah nilai kalori bahan pangan. Minyak goreng ketika digunakan untuk
menggoreng akan mengalami proses hidrolisis gliserol. Di mana gliserol oleh
panas akan dihidrolisis menjadi akrolein dan air. Dalam beberapa hal hidrolisis ini
akan mengalami oksidasi menjadi asam lemak teroksidasi yang dapat
membahayakan kesehatan manusia (Budiyanto, 2009).
Mutu minyak goreng ditentukan oleh titik asapnya, yaitu suhu pemanasan
minyak sampai terbentuk akrolein yang tidak diinginkan dan dapat menimbulkan
rasa gatal pada tenggorokan. Hidrasi gliserol akan membentuk aldehida tidak
jenuh atau akrolein tersebut. Makin tinggi titik asap, makin baik mutu minyak
goreng itu. Titik asap suatu minyak goreng tergantung dari kadar gliserol bebas.
Lemak yang telah digunakan untuk menggoreng titik asapnya akan turun, karena
telah terjadi hidrolisis molekul lemak. Karena itu untuk menekan terjadinya
tidak terlalu tinggi.Pada umumnya suhu penggorengan adalah 177 – 221oC
(Winarno, 1997).
Lemak dan minyak yang baik digunakan untuk minyak goreng adalah oleo
stearin, oleo oil, lemak babi (lard), atau lemak nabati yang dihidrogenasi dengan
titik cair 35 - 40 oC. Oleo stearin dan oleo oil diperoleh dari lemak sapi yang
diproses dengan cararendering pada suhu rendah (Winarno, 1997).
Indikator kerusakan minyak antara lain adalah angka peroksida dan asam
lemak bebas. Angka peroksida menunjukkan banyaknya kandungan peroksida di
dalam minyak akibat proses oksidasi dan polimerisasi. Asam lemak bebas
menunjukkan sejumlah asam lemak bebas yang dikandung oleh minyak yang
rusak, terutama karena peristiwa oksidasi dan hidrolisis (Gunawan, 2003).
2.5 Minyak Jagung
Minyak jagung sebagai minyak makanan adalah minyak yang diperoleh dari
lembaga biji jagung (Zea mays L) dan telah mengalami proses pemurnian dengan
atau tanpa penambahan yang diizinkan (SNI, 1998).
Minyak jagung diperoleh dengan jalan mengekstrak bagian lembaga.Sistem
ekstraksi yang digunakan biasanya sistem pres (pressing) atau kombinasi sistem
press dan pelarut menguap (pressing and solvent extraction) (Ketaren, 1986).
Meskipun jagung merupakan salah satu tanaman utama di Amerika Serikat,
hanya sebagian kecil dari itu digunakan untuk mendapatkan minyak
jagung.Sebagian besar minyak jagung yang dihasilkan adalah produk sampingan
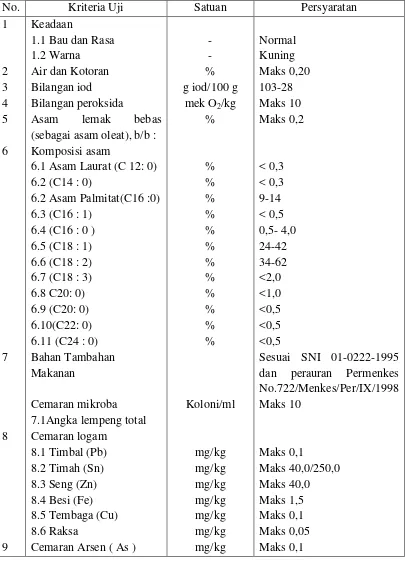
Tabel 2.2 Parameter Syarat Mutu Minyak Jagung (SNI 01-3394-1998) No. Kriteria Uji Satuan Persyaratan 1 (sebagai asam oleat), b/b : Komposisi asam
6.1 Asam Laurat (C 12: 0) 6.2 (C14 : 0)
2.5.1 Komposisi Kimia Minyak Jagung
Minyak jagung merupakan trigliserida yang disusun oleh gliserol dan
asam-asam lemak. Persentase trigliserida sekitar 98,6 %, sedangkan sisanya merupakan
bahan non minyak, seperti abu, zat warna atau lilin. Asam lemak yang menyusun
minyak jagung terdiri dari asam lemak jenuh dan asam lemak tidak
jenuh.Komposisi minyak jagung dapat dilihat pada table 2.3 (Ketaren, 1986).
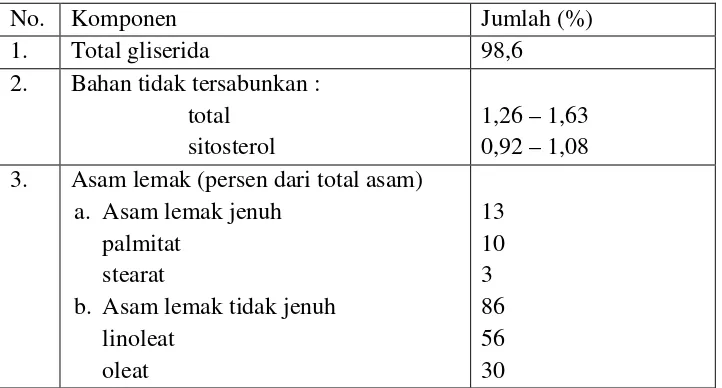
Tabel 2.3 Komposisi Minyak Jagung
No. Komponen Jumlah (%) 3. Asam lemak (persen dari total asam)
a. Asam lemak jenuh palmitat
stearat
b. Asam lemak tidak jenuh linoleat
2.5.2 Sifat Fisiko – Kimia
Minyak jagung berwarna merah gelap dan setelah dimurnikan akan
berwarna kuning keemasan. Bobot jenis minyak jagung sekitar 0,918-0,925,
sedangkan nilai indeks biasanya pada suhu 25 OC berkisar antara 1,4657-1,4659.
Kekentalan minyak jagung hampir sama dengan minyak-minyak nabati lainnya
yaitu 58 sentipois pada suhu 25 OC. Minyak Jagung larut di dalam etanol,
isopropil alkohol dan furfural, sedangkan nilai transmisinya sekitar 280 - 290
2.5.3 Daya Guna dan Nilai Gizi
Biji jagung mempunyai kegunaan yang sangat luas.Jagung memenuhi
persyaratan sebagai bahan pangan karena bernilai gizi tinggi.Selain mudah diolah
juga harganya pun cukup murah, sehingga merupakan bahan makanan tambahan
bagi sebagian penduduk Indonesia (Ketaren, 1986).
Minyak jagung kaya akan kalori yaitu sekitar 250 kalori per ons. Minyak
jagung merupakan minyak goreng yang stabil (tahan terhadap ketengikan) karena
adanya tokoferol yang larut dalam minyak (Ketaren, 1986).
Dengan proses winterisasi, minyak jagung dapat diolah menjadi minyak
salad dan sebagai hasil sampingannya adalah mentega putih (shortening). Minyak
salad yang ditambah garam dan rempah-rempah akan menghasilkan mayonnaise
(Ketaren, 1986).
Dalam minyak jagung terdapat sitosterol yang fungsinya sama dengan
kolesterol pada lemak hewan, yaitu dapat membentuk endapan pada dinding
pembuluh darah karena adanya ion Ca++. Adanya asam-asam lemak esensial itu
dapat mengurangi pembentukan kompleks Ca dengan sitosterol, sehingga minyak
jagung jauh lebih baik bila dibandingkan dengan sumber minyak yang lain,
apalagi bila dibandingkan dengan lemak yang berasal dari hewan (Ketaren, 1986).
2.6 Minyak Kelapa Sawit
Minyak kelapa sawit dapat dihasilkan dari inti kelapa sawit yang dinamakan
minyak inti kelapa sawit (palm kernel oil) dan sebagai hasil samping ialah bungkil
inti kelapa sawit yang telah mengalami proses ekstraksi dan pengeringan
(Ketaren, 1986).
Faktor-faktor yang mempengaruhi mutu adalah air dan kotoran, asam lemak
bebas, bilangan peroksida dan daya pemucatan. Faktor-faktor lain adalah titik cair,
kandungan gliserida padat, sifat transparan, kandungan logam berat dan bilangan
penyabunan. Semua faktor ini perlu dianalisis untuk mengetahui mutu minyak
kelapa sawit dan minyak inti kelapa sawit (Ketaren, 1986).
2.6.1 Komposisi Kimia Minyak Kelapa Sawit
Kelapa sawit mengandung kurang lebih 80% perikarp dan 20% buah yang
dilapisi kulit yang tipis.Kadar minyak dalam perikarp sekitar 34 – 40 %.Minyak
kelapa sawit adalah lemak semi padat yang mempunyai komposisi yang
tetap.Rata-rata komposisi asam lemak minyak kelapa sawit dapat dilihat pada
tabel 2.4 (Ketaren, 1986).
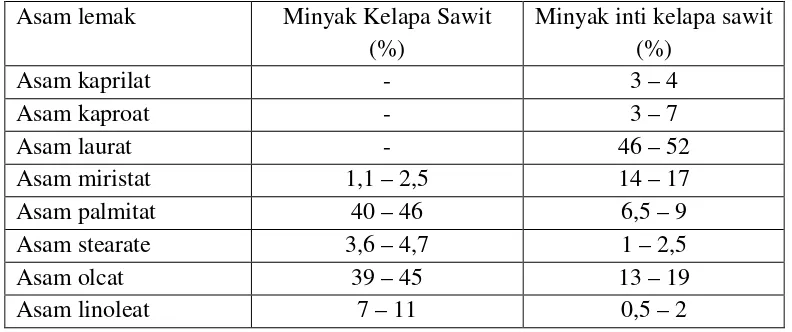
Tabel 2.4 Komposisi Asam Lemak Minyak Kelapa Sawit dan Inti Kelapa Sawit Asam lemak Minyak Kelapa Sawit
(%)
Minyak inti kelapa sawit (%)
Bahan yang tidak dapat disabunkan jumlahnya sekitar 0,3%. Kandungan
kurang lebih 500 – 700 ppm, kandungan tokoferol bervariasi dan dipengaruhi oleh
penanganan selama produksi (Ketaren, 1986).
2.6.2 Sifat Fisiko-Kimia
Sifat fisiko kimia minyak kelapa sawit meliputi warna, bau dan flavor,
kelarutan, titik cair, titik didih (boiling point), titik pelunakan, bobot jenis, indeks
bias, titik kekeruhan (turbidity point), titik asap, titik nyala dan titik api. Nilai sifat
fisiko-kimia minyak sawit dan minyak inti sawit dapat dilihat pada tabel 2.5
(Ketaren, 1986).
Tabel 2.5 Nilai Sifat Fisiko-Kimia Minyak Sawit Dan Minyak Inti Sawit Sifat Minyak Sawit Minyak Inti Sawit Bobot jenis pada suhu
kamar
0,900 0,900 – 0,913
Indeks bias D 40oC 1,4565 – 1,4585 1,495 – 1,415 Bilangan Iod 48 – 56 14 – 20 Bilangan penyabunan 196 – 205 244 – 245
Warna minyak ditentukan oleh adanya pigmen yang masih tersisa setelah
proses pemucatan, karena asam-asam lemak dan gliserida tidak berwarna. Warna
orange atau kuning disebabkan adanya pigmen karoten yang larut dalam minyak
(Ketaren, 1986).
Bau dan flavor dalam minyak terdapat secara alami, juga terjadi akibat
adanya asam-asam lemak berantai pendek akibat kerusakan minyak. Sedangkan
bau khas minyak kelapa sawit ditimbulkan oleh persenyawaan beta
Titik cair minyak kelapa sawit berada dalam nilai kisaran suhu, karena
minyak kelapa sawit mengandung beberapa macam asam lemak yang mempunyai
titik cair yang berbeda-beda (Ketaren, 1986).
2.6.3 Standar Mutu
Mutu minyak kelapa sawit yang baik mempunyai kadar air kurang dari 0,1
persen dan kadar kotoran lebih kecil dari 0,01 persen, kandungan asam lemak
bebas serendah mungkin (kurang lebih 2 persen atau kurang), bilangan peroksida
di bawah 2, bebas dari warna merah dan kuning (harus berwarna pucat) tidak
berwarna hijau, jernih dan kandungan logam berat serendah mungkin atau bebas
dari ion logam (Ketaren, 1986).
2.7 Bilangan Peroksida
Bilangan peroksida adalah nilai terpenting untuk menentukan derajat
kerusakan pada minyak atau lemak.Asam lemak tidak jenuh dapat mengikat
oksigen pada ikatan rangkapnya sehingga membentuk peroksida.Peroksida ini
dapat ditentukan dengan metode iodometri (Ketaren, 1986).
Cara yang sering digunakan untuk menentukan bilangan peroksida,
berdasarkan pada reaksi antara alkali iodide dalam larutan asam dengan ikatan
peroksida.Iod yang dibebaskan pada reaksi ini kemudian dititrasi dengan natrium
tiosulfat. Penentuan peroksida ini kurang baikdengan cara iodometri biasa
meskipun peroksida bereaksi sempurna dengan alkali iod. Hal ini disebabkan
terjadi kesalahan yang disebabkan oleh reaksi antara alkali iodide dengan oksigen
dari udara (Ketaren, 1986).
Bilangan peroksida ditentukan berdasarkan jumlah iodin yang dibebaskan
setelah lemak atau minyak ditambahkan KI. Lemak direaksikan dengan KI dalam
pelarut asam asetat dan kloroform ( 2 : 1 ) kemudian iodin yang terbentuk
ditentukan dengan titrasi memakai natrium tiosulfat (Winarno, 1997).
Sebagai ukuran oksidasi lemak untuk pemanas, bilangan peroksida berguna
untuk menentukan kualitas lemak setelah pengolahan. Dengan lemak atau minyak
diproses dengan benar dan cepat dari minyak berkualitas baik, nilai peroksida
segar akan praktis nihil. Peroksida akan mengembangkan sampai batas tertentu
dengan kuantitas tergantung pada waktu, suhu, paparan cahaya dan udara. Selama
oksidasi, nilai peroksida meningkat perlahan-lahan selama periode induksi,
kemudian dengan cepat, mencapai puncaknya.Nilai peroksida yang tinggi
menunjukkan oksidasi maju, tetapi nilai peroksida yang rendah mungkin tidak
berarti bebas dari oksidasi (Lawson, 1985).
Pada suhu penggorengan, peroksida berkembang, tetapi juga menguap dan
meninggalkan sistem penggorengan pada suhu tinggi.Bilangan peroksida adalah
sedikit atau tidak ada nilai dalam menilai kondisi bekas menggoreng lemak atau
frylife (Lawson, 1985).
Bilangan peroksida akan memecah ikatan karbonil dan aldehid pada saat
menggoreng dikarenakan suhu yang tinggi, udara dan cahaya. Reaksi ini terjadi
sebagai hasil reaksi antara trigliserida tidak jenuh dan oksigen dari udara.Molekul
2.8 Metode Iodometri
Iodometri merupakan titrasi tidak langsung dan digunakan untuk
menetapkan senyawa-senyawa yang mempunyai potensial oksidasi yang lebih
besar dari pada sistem iodium-iodida atau senyawa-senyawa yang bersifat
oksidator seperti CuSO45H2O. Pada iodometri, sampel yang bersifat oksidator
direduksi dengan kalium iodide berlebihan dan akan menghasilkan iodium yang
selanjutnya dititrasi dengan larutan baku natrium tiosulfat. Banyaknya volume
natrium tiosulfat yang digunakan sebagai titran setara dengan iodium yang
dihasilkan dan setara dengan banyaknya sampel (Rohman, 2007)
Peroksida dapat ditentukan dengan titrasi iodometri.Metode iodometri
termasuk salah satu metode yang paling akurat dalam analisis titrimetri karena
dalam kondisi yang sesuai, keberadaan satu bpj dapat dideteksi dengan
menggunakan larutan indikator kanji (Putisar, 2015).
Kegunaan banyak dari iodometri didasarkan pada kerja oksidasi iod dan
sebaliknya kerja reduksi iodide. Jika suatu senyawa dioksidasi oleh iod, maka iod
sendiri tereduksi menjadi iodida :
I2 + 2e 2I
-Dalam larutan asam iodida bekerja mereduksi oksidator kuat dan iodidanya
sendiri dioksidasi menjadi iod :
2I I2 + 2e
Oleh karena itu reaksi iodometri adalah suatu proses redoks, yang dapat
dinyatakan dengan menyatukan kedua persamaan :
Arah dari reaksi redoks ini tergantung dari potensial redoks pasangan
reaksinya dan harga pH larutan titrasi (Putisar, 2015).
Cara yang sering digunakan pada penentuan bilangan peroksida
berdasarkan pada reaksi anatara alkali iodida dalam larutan asam dengan ikatan
oksigen sebagai peroksida. Reaksi yang terjadi adalah :
ROOH + 2 I- + 2 H+ I2 + ROH + H2O
2 Na2S2O3 + I2 2 NaI + Na2S4O6
BAB III
METODE PENGUJIAN
3.1 Tempat dan Waktu Pengujian
Pengujian ini dilakukan di Laboratorium Minyak Nabati dan
Rempah-Rempah UPT.Balai Pengujian dan Sertifikasi Mutu Barang (BPSMB) Jl. STM
No. 17 Kampung Baru, Medan 20146 pada tanggal 2 sampai 13 Februari 2015.
3.2 Alat
Alat-alat yang digunakan dalam pengujian yaitu neraca analitik (mettle
toledo), Erlenmeyer 250 ml – 300 ml (pyrex), pipet gondok 20 ml (pyrex), labu
ukur 100 ml (pyrex), gelas ukur (pyrex), batang pengaduk, spatula, pipet tetes,
buret mikro (pyrex)dan botol semprot.
3.3 Bahan
Bahan yang digunakan adalah minyak jagung, minyak curah, kloroform pro
analisis, asam asetat glasial pro analisis, kalium iodide pra kristal, natrium
tiosulfat 0,1 N, air suling bebas CO2 dan indikator larutan kanji 0,5%.
3.4 Pembuatan Pereaksi
Pembuatan pereaksi yang digunakan pada pengujian minyak jagung dan
minyak kelapa sawit adalah
Dibuat campuran asam asetat glasial dan kloroform dengan perbandingan
3 : 2 (v/v)
b. Larutan kalium iodida jenuh
Larutkan kalium iodida dalam air suling hingga kondisi jenuh (adanya
kristal KI yang tidak larut).
c. Larutan natrium tiosulfat 0,1 N
Timbang 24,9 g Na2S2O3.5H2O, larutkan ke dalam labu ukur satu liter
dengan air suling bebas CO2 kemudian tera.
Pembuatan larutan standar natrium tiosulfat 0,01 N
Larutkan 10 ml larutan natrium tiosulfat 0,1 N (dengan pipet) dalam labu
ukur 100 ml lalu isi dan tera labu ukur sampai tanda garis dengan air suling bebas
CO2.
d. Standarisasi natrium tiosulfat 0,01 N
− Keringkan kalium dikromat (K2Cr2O7) dalam oven pada suhu 103oC ± 2
o
C selama 2 jam, dinginkan dalam desikator
− Timbang 0,014 g ke dalam erlenmeyer
− Larutkan dengan 25 ml air suling, tambahkan 5 ml asam klorida (HCl)
pekat dan 10 ml larutan kalium iodida 10%. Kocok dan simpan dalam
tempat gelap selama 5 menit
− Tambahkan 50 ml air suling, titrasi dengan larutan natrium tiosulfat 0,01
N sampai warna kuning muda
− Tambahkan 1 sampai 2 tetes larutan indicator kanji, lanjutkan titrasi
e. Indikator larutan kanji 1%
Timbang 1 g serbuk kanji didihkan dengan 100 ml air suling selama 3 menit
3.5 Prosedur Pengujian
Prinsip : Larutan contoh dalam asam asetat glasial dan kloroform
direaksikan dengan larutan KI. Iodium yang dibebaskan dititrasi dengan larutan
standard natrium tiosulfat.
Prosedur pengujian penentuan bilangan peroksida pada minyak jagung dan
minyak curah sebagai berikut :
a. Timbang dengan teliti 5 ± 0,05 g (W) contoh
b. Tambahkan 50 ml larutan asam asetat glasial-kloroform, tutup Erlenmeyer
dan aduk hingga larutan homogen
c. Tambahkan 0,5 ml larutan kalium iodida jenuh dengan menggunakan pipet
ukur, kemudian kocok selama 1 menit
d. Tambahkan 30 ml air suling kemudian tutup Erlenmeyer dengan segera.
Kocok dan titrasi dengan larutan natrium tiosulfat 0,1 N hingga warna
kuning hampir hilang, kemudian tambahkan indikator kanji 0,5 ml dan
lanjutkan titrasi, kocok kuat untuk melepaskan semua iod dari lapisan
pelarut hingga warna biru hilang
e. Lakukan penetapan duplo
f. Lakukan penetapan blanko
Perhitungan :
Bilangan peroksida dinyatakan sebagai miliekivalen O2 per kg lemak yang
dihitumg menggunakan rumus :
Bilangan peroksida (mek O2/kg) =
( �1−�� ) ��
� � 1000
Keterangan :
V1 = volume larutan natrium tiosulfat 0,01 N yang diperlukan untuk titrasi
contoh minyak (ml)
Vo = volume larutan natrium tiosulfat 0,01 N yang diperlukan untuk titrasi
blanko (ml)
N = normalitas natrium tiosulfat yang digunakan untuk titrasi (N)
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil
a. Pengujian Minyak Jagung
Hasil pengujian penentuan bilangan peroksida pada minyak jagung dapat
dilihat pada tabel 4.1.
Tabel 4.1 Data Penentuan Bilangan Peroksida Pada Minyak Jagung
Berat Sampel Volume Blanko Volume Titrasi Bilangan Peroksida
5,0482 g
0,4 ml 1,8 ml 2,7733 mek O2/kg 5,0159 g 1,65 ml 2,4921 mek O2/kg
Rata-rata bilangan peroksida 2,6327 mek O2/kg
b. Pengujian Minyak Kelapa Sawit
Hasil pengujian penentuan bilangan peroksida pada minyak kelapa sawit
dapat dilihat pada tabel 4.2.
Tabel 4.2 Data Penentuan Bilangan Peroksida Minyak Kelapa Sawit
Berat Sampel Volume Blanko Volume Titrasi Bilangan Peroksida
5,0428 g
0,4 ml 2,8 ml 4,7593 mek O2/kg 5,0140 g 3 ml 5,1855 mek O2/kg
4.2 Pembahasan
Indikator kerusakan minyak antara lain adalah angka peroksida dan asam
lemak bebas. Angka peroksida menunjukkan banyaknya kandungan peroksida di
dalam minyak akibat proses oksidasi dan polimerisasi. Asam lemak bebas
menunjukkan sejumlah asam lemak bebas yang dikandung oleh minyak yang
rusak, terutama karena peristiwa oksidasi dan hidrolisis (Sudarmadji, 1982).
Minyak goreng berfungsi sebagai penghantar panas, penambah rasa gurih,
dan penambah nilai kalori bahan pangan.minyak goreng ketika digunakan untuk
menggoreng akan mengalami proses hidrolisis gliserol. Di mana gliserol oleh
panas akan dihidrolisis menjadi akrolein dan air. Dalam beberapa hal hidrolisis ini
akan mengalami oksidasi menjadi asam lemak teroksidasi yang dapat
membahayakan kesehatan manusia. Lemak dan minyak yang baik untuk
digunakan sebagai minyak goreng adalah a) oleostearin dan oil yang bersumber
pada lemak sapi yang diproses dengan cararendering pada suhu rendah. Lemak
yang dihasilkan dipertahankan pada suhu 32oC sehingga terbentuk Kristal dan b)
lemak nabati yang dihidrogenasi dengan titik cair 3540oC (Budiyanto, 2009).
Pada percobaan pengujian bilangan peroksida perlakuan pertama yaitu
menimbang 5 g sampel ke dalam erlenmeyer sampel tersebut direaksikan dengan
larutan asam asetat dan kloroform tujuannya untuk melarutkan minyak dalam
larutan kemudian ditambahkan dengan larutan 0,5 ml KI jenuh tujuannya untuk
mengetahui jumlah bilangan peroksida yang ada dalam minyak. Selanjutnya
didiamkan selama 1 menit kemudian ditambahkan dengan akuades sehingga akan
dititrasi dengan larutan Na2S2O3 sampai warna kuningnya hampir hilang
tujuannya adalah untuk penentuan bilangan peroksida.
Selanjutnya setelah dititrasi semua larutan ditambahkan dengan larutan
indikator amilum tujuannya adalah untuk menyerap iodin yang dibebaskan yang
ditandai dengan perubahan warna menjadi biru.Hal ini disebabkan karena didalam
minyak tidak terdapat amilum atau pati.
Bilangan peroksida digunakan untuk menganalisis sifat fisika dan kimia dari
minyak. Nilai peroksida yang diperoleh dari masing-masing sampel yaitu minyak
jagung 1,8 ml dan 1,65 ml sedangkan untuk minyak kelapa sawit 2,8 ml dan 3 ml.
Bilangan peroksida minyak jagung 2,7733 mek O2/kg dan 2,4921 mek O2/kg
dengan rata-rata 2,6327 mek O2/kg. Bilangan peroksida minyak kelapa sawit
4,7593 mek O2/kg dan 5,1855 mek O2/kg dengan rata-rata 4,9724 mek O2/kg Dari
data yang diperoleh dapat disimpulkan bahwa semakin banyak jumlah ml
Na2S2O3 yang digunakan maka semakin besar pula nilai bilangan peroksida yang
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
a. Nilai bilangan peroksida dari minyak jagung dan minyak curah memenuhi
persyaratan bilangan peroksida yang ditetapkan dalam Standar Nasional
Indonesia (SNI).
b. Minyak atau lemak apabila mengalami oksidasi maka senyawa peroksida
yang dihasilkan akan meningkat dan semakin banyak jumlah ml NaS2O3
yang digunakan,maka semakin besar pula nilai bilangan peroksida yang
didapatkan. Nilai bilangan peroksida untuk minyak jagung 2,6327 mek
O2/kg sedangkan minyak kelapa sawit 4,9724 mek O2/kg, dengan
membandingkan nilai bilangan peroksida kedua minyak maka minyak
jagung mempunyai kualitas lebih baik daripada minyak kelapa sawit
(minyak curah).
5.2 Saran
Saran yang dapat penulis sampaikan kepada peneliti selanjutnya hendaknya
dilakukan pengujian terhadap parameter standar mutu yang lain seperti penetapan
bilangan penyabunan, kadar asam lemak bebas, bilangan iodine, ataupun
kekentalan (viskositas) untuk lebih menjamin mutu hasil produksi dalam pasar
DAFTAR PUSTAKA
Budiyanto, A. K. (2009). Dasar-Dasar Ilmu Gizi.Malang: UMM Press. Halaman: 44.
Fauzi, Y. (2002). Kelapa Sawit: Budidaya, Pemanfaatan Hasil dan Limbah, Analisis Usaha dan Pemasaran. Jakarta: Penebar Swadaya.Halaman : 22-35.
Gaman dan Sherrington.(1994). Ilmu Pangan, Pengantar Ilmu Pangan, Nutrisi dan Mikrobiologi. Edisi Kedua. Yogyakarta : Gadjah Mada University Press.Halaman : 75.
Gunawan, dkk. (2003). Analisis Pangan: Penentuan Angka Peroksida dan Asam Lemak Bebas Pada Minyak Kedelai Dengan Variasi Menggoreng. Vol.VI (3). Semarang. FMIPA UNDIP. Halaman : 2.
Ketaren, S. (1986).Minyak dan Lemak Pangan.Jakarta : UI Press. Halaman : 17, 130 - 131, 238, 241, 250 – 257.
Lawson, Harry W. (1985). Standards For Fats And Oils. Westport : The Avi Publishing company, INC. Halaman : 31, 47.
Mangoensoekarjo, S. (2000).Manajemen Agrobisnis Kelapa Sawit. Jakarta: Gadjah Mada University Press.Halaman : 30-52.
Najiyati, Sri dan Danarti. (1999). Palawija Budidaya dan Analisis Usahatani.Jakarta : Penebar Swadaya. Halaman : 60 – 62.
Putisar, E. (2015). Bilangan Peroksida Pada Minyak. http://www.jbptitbpp-gdl-ekaputisar-26922-1-2007ta-1.pdf. Diakses pada tanggal 22 Maret 2015.
Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta : Pustaka Pelajar. Halaman : 154.
Rohman, A. (2013). Analisis Komponen Makanan. Yogyakarta : Graha Ilmu. Halaman: 104.
Standar Nasional Indonesia.SNI 01-3394-1998 Minyak Jagung. Jakarta: Badan Standardisasi Nasional. Halaman: 4.
Standar Nasional Indonesia. SNI 3741 : 2013 Minyak Goreng. Jakarta: Badan Standardisasi Nasional. Halaman: 7 – 9.
Subekti, dkk.(2015). Tanaman Jagung go.id/ind/images/stories/empat.pdf. Diakses pada tanggal 20 Maret 2015.
Sudarmadji, S., Haryono, B., dan Suhardi.(1989). Analisa Bahan Makanan dan Pertanian. Yogyakarta: Liberty. Halaman : 57 - 60, 63 – 68.
Vaughan, J. G. (1970). The Structure and Utilization of Oil Seeds. Great Britain : The Chaucer Press. Halaman : 91 – 93.
Lampiran 1Perhitungan Standarisasi Natrium Tiosulfat (Na2S2O3) 0,01 N
Berat K2Cr2O7 : 0,014 g
BE K2Cr2O7 : 49
Volume titrasi : 26,5 ml
N = ��
�� �
1000 �
= 0,014 �
49 � 1000 26,5 ��
Lampiran 2 Perhitungan Penentuan Bilangan Peroksida
a. Blanko
Volume titrasi : 0,4 ml
b. Minyak Jagung
Pengujian -1
Berat minyak : 5,0482 g
Volume titrasi : 1,8 ml
Bilangan peroksida (mek O2/kg) =
( �1−�� )��
� � 1000
= ( 1,8 −0,4 )��
5,0482 � � 1000
= 2,7733mek O2/kg
Pengujian - 2
Berat minyak : 5,0159 g
Volume titrasi : 1,65 ml
Bilangan peroksida (mek O2/kg) =
( �1−�� )��
� � 1000
= ( 1,65 −0,4 )��
5,0159 � � 1000
c. Minyak Kelapa Sawit
Pengujian -1
Berat minyak : 5,0428 g
Volume titrasi : 2,8 ml
Bilangan peroksida (mek O2/kg) =
( �1−�� )��
� � 1000
= ( 2,8 −0,4 )��
5,0428 � � 1000
= 4,7593mek O2/kg
Pengujian -2
Berat minyak : 5,0140 g
Volume titrasi : 3 ml
Bilangan peroksida (mek O2/kg) =
( �1−�� )��
� � 1000
= ( 3 − 0,4 )��
5,0140 � � 1000
Lampiran 3 Pengujian Minyak Jagung
Gambar 1 Minyak Jagung
Gambar 3 Erlenmeyer berisi hasil standarisasi Na2S2O3 0,01 N
Gambar 6 Erlenmeyer berisi minyak jagung hasil titrasi
Lampiran 4 Pengujian Minyak Kelapa Sawit
Gambar 7 Minyak Kelapa Sawit
Gambar 8 Erlenmeyer berisi