SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2014
KERAGAMAN GENETIK GEN PROLAKTIN DAN GEN STAT5A
PADA SAPI BALI
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa tesis berjudul Keragaman Genetik Gen Prolaktin dan Gen STAT5A pada Sapi Bali adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Agustus 2014
Komang Alit Paramitasari
RINGKASAN
KOMANG ALIT PARAMITASARI. Keragaman Genetik Gen Prolaktin dan Gen STAT5A pada Sapi Bali. Dibimbing oleh JAKARIA dan CECE SUMANTRI.
Sapi bali merupakan sumberdaya genetik ternak asli Indonesia yang memiliki beberapa keunggulan, salah satunya adalah daya reproduksi yang tinggi. Gen prolaktin (PRL) dan gen signal transducer and activator of transcription 5A (STAT5A) merupakan anggota dari POU1F1 signaling pathway yang berhubungan dengan sifat reproduksi. Penelitian ini bertujuan untuk mengidentifikasi ada tidaknya polimorfisme gen PRL dan STAT5A pada sapi bali di pusat pembibitan sapi bali yaitu Balai Pembibitan Ternak Unggul (BPTU) sapi bali Pulukan, Balai Inseminasi Buatan Daerah (BIBD) Baturiti, Balai Besar Inseminasi Buatan (BBIB) Singosari, Balai Pembibitan Ternak-Hijauan Makanan Ternak (BPT-HMT) Serading, dan Village Breeding Centre (VBC) Kabupaten Barru dengan menggunakan metode PCR-RFLP.
Sampel sapi bali sebanyak 262 sampel dideteksi keragaman genetiknya menggunakan enzim restriksi RsaI (gen PRL) dan AvaI (gen STAT5A). Analisis data menggunakan frekuensi alel, frekuensi genotipe, heterozigositas, dan keseimbangan Hardy-Weinberg. Amplifikasi gen PRL ekson 3, gen PRL ekson 4, dan gen STAT5A ekson 7 menghasilkan fragmen dengan panjang masing-masing 156 bp, 294 bp, dan 215 bp. Penentuan genotipe gen PRL ekson 3 dan ekson 4 menghasilkan tiga genotipe pada populasi BBIB Singosari dan dua genotipe pada populasi BIBD Baturiti, BPTU sapi bali Pulukan, BPT-HMT Serading, dan VBC Kabupaten Barru. Frekuensi alel A (ekson 3) dan alel G (ekson 4) lebih tinggi dibandingkan dengan alel B (ekson 3) dan alel A (ekson 4) untuk gen PRL. Hasil analisis menunjukkan bahwa lokus STAT5A|AvaI memiliki alel monomorfik C.
Nilai heterozigositas ditemukan rendah untuk gen PRL ekson 3 dan ekson 4 pada seluruh populasi. Frekuensi genotipe gen PRL ekson 3 dan ekson 4 menyimpang dari keseimbangan Hardy-Weinberg pada populasi sapi bali di BBIB Singosari. Hasil sekuens fragmen gen PRL baik pada ekson 3 maupun ekson 4 menunjukkan adanya mutasi antara basa adenin (A) dengan guanin (G), sedangkan hasil analisis sekuens pada gen STAT5A menunjukkan bahwa tidak terjadi mutasi pada situs restriksi enzim AvaI (C|CCGAG).
SUMMARY
KOMANG ALIT PARAMITASARI. The Genetic Variability of Prolactin Gene and STAT5A Gene in Bali Cattle. Supervised by JAKARIA and CECE SUMANTRI.
Bali cattle as one of Indonesia animal genetic resources has advantages, one of which is its high reproductive ability. Prolactin (PRL) gene and signal transducer and activator of transcription 5A (STAT5A) gene were members of POU1F1 signaling pathway related to reproductive traits. The aim of this study was to identify the genetic variabilty of PRL and STAT5A gene in bali cattle from Breeding Centre of bali cattle (BPTU) Pulukan, Baturiti District Artificial Insemination Centre (BIBD Baturiti), Singosari Artificial Insemination Centre (BBIB Singosari), BPT-HMT Serading, and Village Breeding Centre (VBC) Barru District using PCR-RFLP method.
A total of 262 bali cattle were identified using RsaI(PRL gene) and AvaI (STAT5A gene) restriction enzyme. PRL gene exon 3, PRL gene exon 4, and STAT5A gene exon 7 amplification resulting in a fragment with the length of 156 bp, 294 bp, 215 bp, respectively. Data analysis were conducted using allele frequency, genotype frequency, heterozigosity, and Hardy-Weinberg equilibrium. Genotyping of PRL gene both at exon 3 and 4 produced three genotypes in BBIB Singosari population and two genotypes in the rest populations. For the PRL gene, frequencies of A allele (exon 3) and G allele (exon 4) were dominant to the B allele (exon 3) and A allele (exon 4) across all populations. The results showed that STAT5A|AvaI loci had monomorphic C allele.
Heterozygosity values were found low at both exon 3 and 4 of PRL gene in all populations. Genotype frequencies for PRL gene at exon 3 and exon 4 were in Hardy-Weinberg disequilibrium in BBIB Singosari population. Sequence analysis results of PRL gene both for exon 3 and 4 showed that there was a mutation between adenine (A) and guanine (G) bases in the RsaI recognized site, whereas in STAT5A gene there was no mutation occured in AvaI restriction site (C|CCGAG).
© Hak Cipta Milik IPB, Tahun 2014
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Ilmu Produksi dan Teknologi Peternakan
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2014
KERAGAMAN GENETIK GEN PROLAKTIN DAN GEN STAT5A
PADA SAPI BALI
Judul Tesis : Keragaman Genetik Gen Prolaktin dan Gen STAT5A pada Sapi Bali
Nama : Komang Alit Paramitasari NIM : D151130376
Disetujui oleh Komisi Pembimbing
Dr Jakaria, SPt MSi Ketua
Prof Dr Ir Cece Sumantri, MAgrSc Anggota
Diketahui oleh
Ketua Program Studi Ilmu Produksi dan Teknologi Peternakan
Dr Ir Salundik, MSi
Dekan Sekolah Pascasarjana
Dr Ir Dahrul Syah, MScAgr
Tanggal Ujian: 11 Agustus 2014
PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Agustus 2013 sampai Februari 2014 ini adalah gen-gen reproduksi pada sapi bali dengan judul “Keragaman Genetik Gen Prolaktin dan Gen STAT5A pada Sapi Bali”. Tesis ini disusun sebagai salah satu syarat untuk memperoleh gelar magister pada program studi Ilmu Produksi dan Teknologi Peternakan, Sekolah Pascasarjana, Institut Pertanian Bogor.
Penulis menyadari bahwa proses penelitian dan penyusunan karya ilmiah ini tidak dapat berjalan lancar tanpa bantuan dan dukungan dari banyak pihak. Terima kasih penulis ucapkan kepada yang terhormat Dr Jakaria, SPt MSi dan Prof Dr Ir Cece Sumantri, MAgrSc selaku komisi pembimbing atas curahan waktu, bimbingan, dan dorongan semangat mulai dari penyusunan proposal, pelaksanaan penelitian, dan penulisan karya ilmiah sejak penulis menempuh program sarjana hingga jenjang pascasarjana. Penulis menyampaikan ucapan terimakasih kepada yang terhormat Dr Ir Dedy Duryadi Solihin, DEA selaku penguji luar komisi dan Dr Ir Niken Ulupi, MS selaku Sekretaris Program Studi ITP pada ujian tesis penulis atas saran dan masukan yang diberikan guna memperkaya dan menambah manfaat pada tesis penulis. Semoga Tuhan YME memberikan balasan yang terbaik atas segala ilmu, amal ibadah, dan curahan waktu yang telah diberikan kepada penulis.
Kepada Dr Ir Salundik, MSi selaku Ketua Program Studi ITP serta jajarannya (Ibu Ade dan Mbak Okta) di sekretariat Pasca ITP, penulis menghaturkan terimakasih atas pelayanan administrasi yang diberikan selama penulis menempuh studi. Terimakasih kepada DIPA IPB dan Direktorat Jendral Perguruan Tinggi atas Penelitian Fundamental dan beasiswa Fresh Graduate
sehingga penulis dapat melaksanakan penelitian dan menyelesaikan studi dengan lancar. Kepada teman-teman di Program Studi ITP angkatan 2012 dan angkatan 2013 terimakasih atas kebersamaannya.
Penulis sampaikan terima kasih kepada Kak Eryk, Kak Shelvi, Kak Ferdy, Kak Isyana, Kak Furqon, Kak Icha, Kak Pandu, dan teman-teman ABGSCi atas segala dukungan dan kebersamaannya di Laboratorium Genetika Molekuler Ternak. Kepada Olin, Rany, Opak, Eja, Adhit serta Hoshi, penulis sampaikan terimakasih atas kebersamaan, canda tawa, dan motivasi yang diberikan.
Ungkapan terima kasih terdalam penulis sampaikan kepada kedua orang tua, Dr Ir I Nyoman Arnaya, MSc dan Putu Agustini Eliyati, kedua kakak, Putu Indira Pradnyawati dan Kadek Noni Lokasari, serta seluruh keluarga atas doa, kasih sayang, dukungan serta motivasi yang selalu diberikan pada penulis. Semoga penulis dapat menjadi sumber kebahagiaan bagi kedua orang tua dan keluarga. Kepada I Putu Arimbawa Pande, penulis ucapkan terimakasih atas segala doa dan kasih sayangnya. Kepada semua pihak yang telah membantu, yang tidak dapat disebutkan satu persatu penulis juga mengucapkan terima kasih.
Semoga karya ilmiah ini bermanfaat.
Bogor, Agustus 2014
DAFTAR ISI
DAFTAR TABEL vi
DAFTAR GAMBAR vii
DAFTAR LAMPIRAN viii
1 PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 2
Tujuan Penelitian 2
Manfaat Penelitian 2
Ruang Lingkup Penelitian 3
2 TINJAUAN PUSTAKA 3
Sapi Bali 3
Gen Signal Transducer and Activator of Transcription 5A (STAT5A) 4
Gen Prolaktin (PRL) 5
Analisis Keragaman DNA 6
3 METODE 6
Lokasi dan Waktu 6
Materi 7
Prosedur 7
Analisis Data 10
4 HASIL DAN PEMBAHASAN 12
Amplifikasi Gen PRL dan STAT5A 12
Identifikasi Genotipe Fragmen Gen PRL dan STAT5A 13 Frekuensi Genotipe dan Frekuensi Alel Fragmen Gen PRL|RsaI 15 Frekuensi Genotipe dan Frekuensi Alel Fragmen Gen STAT5A|AvaI 18
Heterozigositas 20
Keseimbangan Hardy-Weinberg 21
Homologi dan Deteksi Mutasi Gen Prolaktin (PRL) 22
Homologi dan Deteksi Mutasi Gen STAT5A 24
Strategi Pengembangan Sumberdaya Genetik Sapi Bali 25
5 SIMPULAN DAN SARAN 28
Simpulan 28
Saran 29
DAFTAR PUSTAKA 29
LAMPIRAN 34
DAFTAR TABEL
1 Primer gen STAT5A ekson 7, PRL ekson 3, dan PRL ekson 4 7 2 Frekuensi genotipe dan alel fragmen gen PRL|RsaI ekson 3
berdasarkan pusat pembibitan sapi bali 15
3 Frekuensi alel fragmen gen PRL|RsaI ekson 3 pada sapi bali hasil
penelitian dan beberapa bangsa sapi 16
4 Frekuensi genotipe dan alel fragmen gen PRL|RsaI ekson 4
berdasarkan pusat pembibitan sapi bali 17
5 Frekuensi alel fragmen gen PRL|RsaI ekson 4 pada sapi bali hasil
penelitian dan beberapa bangsa sapi 18
6 Frekuensi genotipe dan alel fragmen gen STAT5A|AvaI ekson 7
berdasarkan pusat pembibitan sapi bali 19
7 Frekuensi genotipe dan alel fragmen gen STAT5A|AvaI ekson 7 pada sapi bali hasil penelitian dan beberapa bangsa sapi 20 8 Nilai heterozigositas pengamatan (Ho), nilai heterozigositas harapan
(He), dan hasil uji keseimbangan Hardy-Weinberg berdasarkan pusat
pembibitan sapi bali 21
9 Asosiasi genotipe fragmen gen PRL|RsaI ekson 3 dengan sifat
kuantitatif pada beberapa bangsa sapi 27
10 Asosiasi genotipe fragmen gen PRL|RsaI ekson 4 dengan sifat
kuantitatif pada beberapa bangsa sapi 28
11 Asosiasi genotipe fragmen gen STAT5A|AvaI ekson 7 dengan sifat
kuantitatif pada bangsa sapi di dunia 28
DAFTAR GAMBAR
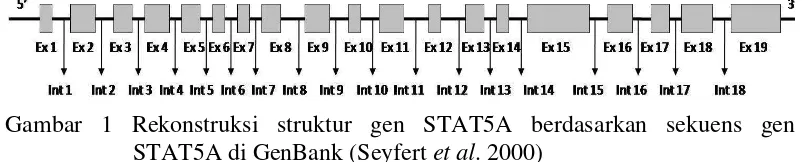
1 Rekonstruksi struktur gen STAT5A berdasarkan sekuens gen
STAT5A di GenBank (Seyfert et al. 2000) 5
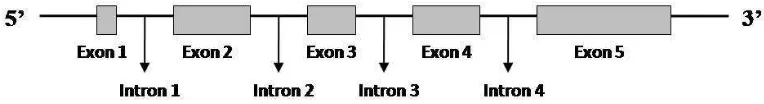
2 Rekonstruksi struktur gen PRL berdasarkan sekuens gen PRL di
GenBank (Cao et al. 2002) 6
3 Posisi penempelan primer pada fragmen gen PRL ekson 3 dan situs
pemotongan enzim RsaI 9
4 Posisi penempelan primer pada fragmen gen PRL ekson 4 dan situs
pemotongan enzim RsaI 9
5 Posisi penempelan primer pada fragmen gen STAT5A ekson 7 dan
situs pemotongan enzim AvaI 10
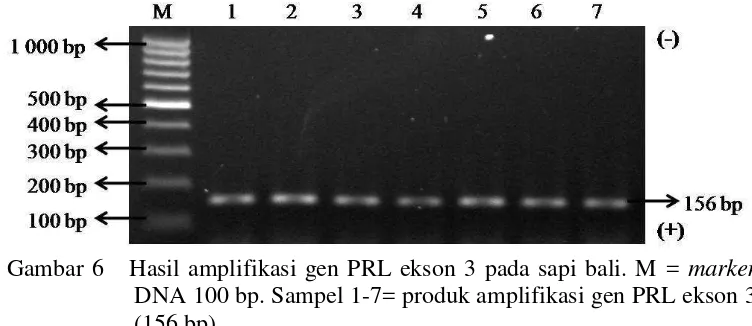
6 Hasil amplifikasi gen PRL ekson 3 pada sapi bali. M = marker DNA 100 bp. Sampel 1-7= produk amplifikasi gen PRL ekson 3 (156 bp). 12 7 Hasil amplifikasi gen PRL ekson 4 pada sapi bali. M = marker DNA
100 bp. Sampel 1-15= produk amplifikasi gen PRL ekson 4 (294 bp). 13 8 Hasil amplifikasi gen STAT5A ekson 7 pada sapi bali. M= marker
DNA 100 bp. Sampel 1-10= produk amplifikasi gen STAT5A ekson 7
9 Hasil PCR-RFLP fragmen gen PRL ekson 3 dengan enzim restriksi
RsaI pada gel agarosa 3.5%. M= marker DNA 20 bp. Sampel 1-13=
sampel sapi bali 13
10 Hasil PCR-RFLP fragmen gen PRL ekson 4 dengan enzim restriksi
RsaI pada gel agarosa 2%. M= marker DNA 100 bp. Sampel 1-16=
sampel sapi bali 14
11 Hasil PCR-RFLP fragmen gen STAT5A ekson 7 dengan enzim restriksi AvaI pada gel agarosa 2%. M= marker DNA 100 bp.
Sampel 1-7= sampel sapi bali 14
12 Hasil perunutan nukleotida sekuens gen PRL|RsaI ekson 3 pada sapi bali dengan GenBank Bos taurus (kode akses AY339391.1 dan
AF426315.1) 23
13 Hasil perunutan nukleotida sekuens gen PRL|RsaI ekson 4 pada sapi bali dengan GenBank Bos taurus (kode akses AY339391.1 dan
AF426315.1) 24
14 Hasil perunutan nukleotida sekuens gen STAT5A|AvaI ekson 7 pada sapi bali dengan GenBank Bos taurus (kode akses AJ237937.1). 25
DAFTAR LAMPIRAN
1 Sekuens gen prolaktin (PRL) berdasarkan GenBank kode akses
AF426315 34
2 Sekuens gen STAT5A ekson 7 berdasarkan GenBank kode akses
1
PENDAHULUAN
Latar Belakang
Sapi bali (Bos javanicus) sebagai ternak asli Indonesia hasil domestikasi banteng (Bibos banteng) (Payne & Rollison 1974) merupakan sumberdaya genetik ternak yang tidak ternilai harganya dan telah diakui oleh FAO sebagai salah satu bangsa sapi di dunia (DGLS 2003). Sapi bali memiliki beberapa keunggulan yaitu mampu beradaptasi terhadap lingkungan marjinal dan memiliki daya reproduksi yang tinggi terutama pada kondisi pakan yang buruk (Talib 2002). Angka kelahiran sapi bali di Provinsi Bali, NTT, NTB, dan Sulawesi Selatan masing-masing 66.3%, 66.6%, 51.7%, dan 60.4% dengan jarak melahirkan antara 14-16 bulan (Talib et al. 2002). Performa reproduksi sapi bali pada sistem pemeliharaan ekstensif (Sulawesi Selatan dan NTT) relatif sama baiknya dengan sistem pemeliharaan intensif (Pulau Bali) untuk sifat-sifat birahi dan lama bunting (Talib 2002). Oleh karena itu, sapi bali merupakan bangsa sapi yang potensial untuk dikembangkan dan dimanfaatkan untuk memenuhi kebutuhan daging secara nasional.
Distribusi sapi bali di Indonesia selain di Pulau Bali juga tersebar di beberapa daerah utama populasi sapi bali, yaitu Sulawesi Selatan, Nusa Tenggara Timur, dan Nusa Tenggara Barat (Purwantara et al. 2012). Berdasarkan Pendataan Sapi Potong, Sapi Perah, dan Kerbau (PSPK) 2011 diketahui bahwa populasi sapi bali di Indonesia adalah 4 658 781 ekor atau sekitar 31% dari total populasi sapi lokal di Indonesia. Empat provinsi dengan jumlah sapi bali tertinggi antara lain: Bali sebanyak 637 463 ekor, NTB sebanyak 672 472 ekor, NTT sebanyak 683 928 ekor, dan Sulawesi Selatan sebanyak 954 901 ekor yang sekaligus sebagai daerah dengan jumlah sapi bali terbanyak di Indonesia (BPS 2011). Strategi pemuliaan dan pelestarian sapi bali dalam rangka mendukung Program Perbanyakan Pejantan Unggul dan Program Pemurnian Sapi bali dapat dilakukan melalui daerah sumber bibit di Indonesia untuk menghasilkan bibit unggul sapi bali.
Upaya peningkatan mutu genetik ternak sapi bali dapat dilakukan melalui seleksi untuk memperoleh karakteristik genetik yang terdapat pada sapi bali seperti kemampuan sifat reproduksi tinggi. Pendekatan analisis gen kandidat sifat reproduksi yang dilakukan oleh Khatib et al. (2009)berhasil mengidentifikasi alur gen-gen yang berpengaruh terhadap sifat reproduksi seperti fertilitas dan daya tahan hidup embrio pada sapi. Gen bovine prolaktin (bPRL) terletak di kromosom 23 (Barendse et al. 1997), terdiri atas lima ekson yang dipisahkan oleh empat intron (Camper et al. 1984). Polimorfisme gen prolaktin disebabkan oleh mutasi transisi antara basa adenin dengan basa guanin (A/G) yang bersifat synonimous mutation pada asam amino 103 di ekson 3. Subtitusi antara kedua basa tersebut dilaporkan menghasilkan situs polimorfik enzim RsaI dan menghasilkan dua alel, yaitu alel A dan alel B (Lewin et al. 1992). Single Nucleotide Polymorphism
2
2009). Gen PRL|RsaI telah banyak digunakan sebagai penanda genetik untuk karakterisasi genetik populasi sapi (Brym et al. 2005).
Gen signal transducer and activator of transcription 5A (STAT5A) dilaporkan berhubungan nyata dengan daya tahan hidup embrio (Khatib et al. 2009). STAT5A dikenal sebagai mamary gland factor (MGF) yang berperan sebagai faktor transkripsi penginduksi prolaktin (Wakao et al. 1994). Gen STAT5A merupakan kandidat marka genetik untuk sifat kuantitatif pada sapi, berada di kromosom 19 yang terdiri atas 19 ekson dan 18 intron (Seyfert et al. 2000). Keragaman gen STAT5A terjadi karena adanya subtitusi dari basa sitosin (C) menjadi basa timin (T) pada posisi 6853 di ekson 7 yang menyebabkan adanya polimorfik situs AvaI (Flisikowski et al. 2003).
Informasi genetik mengenai keragaman gen-gen pengontrol sifat reproduksi pada sapi bali di Indonesia masih sangat terbatas dan belum pernah dilakukan. Oleh karena itu, keragaman gen PRL dan gen STAT5A pada populasi sapi bali, khususnya di pusat pembibitan sapi bali di Indonesia perlu diidentifikasi dengan menggunakan teknik Polymerase Chain Reaction-Restriction Fragment Length Polymorphism (PCR-RFLP). Karakterisasi terhadap penciri gen tersebut pada sapi bali diharapkan dapat melengkapi informasi dasar yang dapat dimanfaatkan untuk program pemuliaan dan pelestarian sapi bali, terutama di daerah pusat pembibitan sapi bali.
Perumusan Masalah
Sapi bali sebagai salah satu sumber daya genetik ternak asli Indonesia memiliki beberapa keunggulan, salah satunya adalah daya reproduksi tinggi. Informasi mengenai sapi bali terutama dari kajian molekuler DNA khususnya pada gen-gen pengontrol sifat reproduksi seperti gen signal transducer and activator of transcription 5A (STAT5A) dan gen prolaktin (PRL) masih sangat terbatas dan belum pernah dilakukan. Oleh karena itu, upaya memperoleh karakteristik keragaman genetik terhadap gen-gen tersebut menjadi sangat penting dilakukan pada bangsa sapi bali di pusat-pusat pembibitan sapi bali.
Tujuan Penelitian
Penelitian ini bertujuan untuk mengidentifikasi ada tidaknya polimorfisme dan distribusi alel pada gen PRL ekson 3 dan ekson 4 serta gen STAT5A ekson 7 pada sapi bali di pusat pembibitan sapi bali yaitu BPTU sapi bali Pulukan, BIBD Baturiti, BBIB Singosari, BPT-HMT Serading, dan Village Breeding Centre
(VBC) Kabupaten Barru di Sulawesi Selatan dengan menggunakan metode PCR-RFLP. Selain itu, tujuan penelitian ini adalah mendeteksi ada tidaknya mutasi pada situs enzim restriksi RsaI pada gen PRL ekson 3 dan ekson 4 serta situs enzim restriksi AvaI pada gen STAT5A ekson 7 pada sapi bali.
Manfaat Penelitian
3 Ruang Lingkup Penelitian
Penelitian ini meliputi identifikasi keragaman dan keberadaan mutasi gen prolaktin (PRL) ekson 3 dan ekson 4 dan gen signal transducer and activator of transcription 5A (STAT5A)ekson 7 pada 262 ekor sapi bali yang terdapat di lima pusat pembibitan sapi bali yaitu: BPTU sapi bali Pulukan (100 ekor), BIBD Baturiti (22 ekor), BBIB Singosari (28 ekor), BPT-HMT Serading (48 ekor), dan VBC Kabupaten Barru (64 ekor). Keragaman gen PRL dan STAT5A dianalisis menggunakan teknik Polymerase Chain Reaction-Restriction Fragment Length Polymorphism (PCR-RFLP). Ada tidaknya mutasi di fragmen gen PRL dan STAT5A dianalisis melalui teknik sequencing. Analisis data dilakukan melalui pendekatan frekuensi alel, frekuensi genotipe, heterozigositas, dan keseimbangan Hardy-Weinberg. Analisis hasil sekuensing dilakukan melalui pensejajaran sekuens nukleotida (alignment) dan Basic Local Alignment Search Tools
(BLAST) nukleotida.
2
TINJAUAN PUSTAKA
Sapi Bali
Sapi bali (Bos javanicus) merupakan salah satu bangsa sapi potong yang penting bagi perkembangan industri peternakan di Indonesia. Selain di Pulau Bali, sapi bali berada di sebagian besar daerah Indonesia bagian timur. Populasi sapi bali banyak terdapat di tiga daerah utama yaitu Sulawesi Selatan, NTT, dan NTB (Purwantara et al. 2012). Daya adaptasi dan reproduksi sapi bali di iklim tropis sangat baik, terutama dibawah cekaman lingkungan yang keras. Performa reproduksi sapi bali di sistem pemeliharaan ekstensif (Sulawesi Selatan dan NTT) relatif sama baiknya dengan sistem pemeliharaan intensif (Pulau Bali) untuk sifat-sifat birahi dan lama bunting. Ukuran tubuh dan bobot lahir yang kecil pada sapi bali kemungkinan besar merupakan upaya mempertahankan keberlangsungan hidup pada lingkungan marginal (Talib 2002). Lama bunting sapi bali berkisar antara 280 hingga 290 hari dengan rataan bobot lahir sekitar 17 kg, namun pada kondisi induk dengan kondisi nutrisi buruk maka bobot lahir pedet hanya kurang dari 9 kg (Purwantara et al. 2012).
Rata-rata panjang siklus estrus sapi bali adalah 21 hari dengan beberapa bukti yang menyatakan bahwa siklus estrus tersebut menjadi pendek dalam kondisi nutrisi yang buruk (Toelihere 2002). Estrus sebagian besar merupakan kejadian nokturnal dengan rataan durasi 18-19 jam dan belum terbukti adanya pengaruh fotoperiode terhadap siklus estrus (Fordyce et al. 2002). Sapi bali yang dipelihara secara intensif di Pusat Pembibitan Sapi Bali Pulukan dengan perbaikan manajemen pemeliharaan menunjukkan bahwa umur berahi pertama adalah 718.57±12,65 hari, umur pertama melahirkan 1 104.51±23,82 hari, calving
4
Gen Signal Transducer and Activator of Transcription 5A (STAT5A)
STAT merupakan tujuh anggota famili faktor intraselular yang menengahi aksi beberapa hormon peptida dan cytokines dalam sel target (Schindler dan Darnell 1995). Kapasitas DNA-binding STATs diinduksi oleh fosforilasi residu tirosin pada terminal-C protein sehingga menyebabkan dimerisasi dan transportasi ke nukleus. STAT5 dikenal sebagai mamary gland factor (MGF) yang berperan sebagai faktor transkripsi penginduksi PRL (Wakao et al. 1994). STAT5 diketahui berperan sebagai mediator utama aksi hormon pertumbuhan pada gen target (Argetsinger dan Carter-Su 1996).
STAT5 memegang peran utama sebagai mediator pemberian isyarat prolaktin dan dapat mengaktivasi transkripsi gen protein susu sebagai respon terhadap prolaktin (Wakao et al. 1994). Faktor transkripsi STAT5 berfungsi untuk menengahi aksi growth promoting oleh hormon pertumbuhan pituitari pada sel target. Oleh karena itu, STAT5A dan STAT5B merupakan kandidat penanda genetik untuk sifat kuantitatif pada sapi. Gen penyandi STAT5A dan STAT5B homolog karena memiliki 90% sekuens penyandi yang identik. Kedua isoform STAT5A dan STAT5B dibedakan oleh beberapa asam amino pada ujung karbosilik molekul protein yang berhubungan dengan domain aktivasi transkripsi (Moriggl et al. 1996).
Gen STAT5A pada sapi berada pada kromosom 19 dan terdiri atas 19 ekson yang menyandikan 794 rantai asam amino (Seyfert et al. 2000). Struktur gen STAT5A berdasarkan sekuens gen STAT5A di GenBank (kode akses AJ242522 dan AJ237937) dapat dilihat pada Gambar 1. Fliskowski dan Zwierzchowski (2002) melaporkan polimorfisme sekuens nukleotida pada ekson 7 gen STAT5A. Ekson 7 menyandikan 250-840 molekul STAT5A pada domain DNA-binding
yang bertanggung jawab untuk pengikatan faktor transkripsi ke promotor gen target (Pellegrini dan Dusanter-Fourt 1997). Polimorfisme sekuens nukleotida yang diteliti oleh Flisikowski et al. (2003) berhasil menemukan adanya subtitusi basa sitosin dengan basa timin (CT) pada posisi 6853 pada ekson 7 yang berasosiasi dengan sifat produksi daging. Mutasi tersebut menciptakan situs restriksi AvaI yang dapat dideteksi oleh PCR-RFLP. Analisis menunjukkan bahwa tidak terjadi perubahan sekuens asam amino pada protein yang disandikan oleh gen STAT5A ekson 7 yaitu baik kodon CCC maupun CCT sama-sama menyandikan asam amino prolin.
Gen STAT5A berasosiasi signifikan dengan laju fertilitas dan perkembangan embrio (Khatib et al. 2009). Selain itu, hasil asosiasi analisis RFLP STAT5A|AvaI ekson 7 dengan sifat performa pertumbuhan pada sapi pejantan Podolica menunjukkan bahwa genotipe CC memiliki laju pertumbuhan awal yang lebih cepat dan bobot badan yang lebih tinggi. Sebaliknya, sapi bergenotipe heterozigot CT menunjukkan performa laju pertumbuhan tahap akhir yang lebih cepat (Dario et al. 2009b). Hasil penelitian Flisikowski et al. (2003) melaporkan bahwa bangsa sapi pedaging (Charolaise, Limousine, Red Angus, dan Hereford) bergenotipe CC mengonsumsi pakan yang lebih sedikit untuk
5
Gen Prolaktin (PRL)
Gen prolaktin (PRL) berpengaruh terhadap beberapa proses biologis seperti keseimbangan elektrolit, pertumbuhan, perkembangan, endokrinologi, metabolisme, regulasi bermacam-macam fungsi dalam otak, pengaturan tingkah laku maternal, reproduksi, dan imunoregulasi (Bole-Feysot et al. 1998). Gen prolaktin termasuk ke dalam POU1F1 (Pit-1) signaling pathway dan interaksi dua arah antara kedua gen tersebut berpengaruh signifikan terhadap daya tahan hidup embrio sapi pada tahap awal (Khatib et al. 2009).
Gen bovine PRL (bPRL) terletak di kromosom 23 (Barendse et al. 1997), berukuran 10 kb, terdiri atas lima ekson yang dipisahkan oleh empat intron (Camper et al. 1984). Bagian ekson pada gen prolaktin menyandikan 229 asam amino prekursor prolaktin dan 199 asam amino (Cao et al. 2002). Struktur gen prolaktin berdasarkan sekuens gen PRL di GenBank (kode akses AF426315) dapat dilihat pada Gambar 2.
Polimorfisme gen prolaktin telah banyak dilaporkan pada beberapa penelitian. Mutasi transisi antara basa adenin dan guanin (A/G) yang bersifat
synonimous mutation pada asam amino 103 di ekson 3 dilaporkan memiliki situs polimorfik RsaI (Lewin et al. 1992). Hasil penelitian mengenai keragaman gen prolaktin ekson 3 pada 23 bangsa sapi lokal India (Bos indicus) dengan metode PCR-RFLP menghasilkan tiga genotipe (AA, AB, dan BB) dengan frekuensi alel A dan alel B masing-masing 0.52 dan 0.48 (Sodhi et al. 2011). Hasil asosiasi antara gen prolaktin ekson 3 dengan sifat produksi susu menunjukkan bahwa genotipe BB berhubungan dengan produksi susu dan produksi lemak susu yang lebih tinggi dibandingkan dengan genotipe AA dan AB (Alipanah et al. 2007).
Penelitian yang dilakukan oleh Brym et al. (2005) dengan menggunakan PCR-SSCP yang dilanjutkan dengan sekuensing pada gen bPRL ekson 4 berhasil menemukan enam SNPs (single nucleotide polymorphisms). Salah satu SNP yang terdapat pada posisi 8398 R memiliki situs polimorfik RsaI dan berasosiasi dengan sifat produksi sapi perah. Genotipe AG berhubungan dengan produksi susu yang tinggi sedangkan genotipe GG berhubungan dengan komposisi lemak susu tertinggi pada sapi Black-and White.
Keragaman gen PRL ekson 4 pada sapi Chinese Holstein telah diidentifikasi oleh Dong et al. (2013) dan ditemukan SNP (7545 GA) yang dapat dikenali oleh sekuens enzim restriksi RsaI. Hasil asosiasi pada penelitian tersebut menunjukkan bahwa sapi bergenotipe AA memiliki produksi susu yang lebih tinggi. Hal tersebut sesuai dengan hasil penelitian Mehmannavaz et al. (2009) yang menyatakan bahwa alel A berasosiasi dengan produksi susu dan protein susu yang lebih baik.
6
Situs polimorfik PRL-RsaI telah banyak digunakan sebagai penanda genetik untuk karakterisasi genetik populasi sapi. Frekuensi alel pada situs polimorfik PRL-RsaI dan pengaruh dari alel-alel tersebut terhadap sifat performa susu belum konsisten karena luasnya keberagaman pada bangsa sapi perah dan sapi pedaging (Brym et al. 2005).
Analisis Keragaman DNA
Analisis keragaman DNA dapat dilakukan dengan berbagai cara, antara lain RFLP, SSCP, DGGE, dan sequencing. Polymerase Chain Reaction (PCR) adalah suatu reaksi in vitro untuk menggandakan molekul DNA pada target yang telah ditentukan dengan cara mensintesa molekul DNA baru yang berkomplemen dengan molekul DNA tersebut dengan enzim polimerase dan oligonukleotida pendek. Analisis RFLP sering digunakan untuk mendeteksi lokasi genetik dalam kromosom yang menyandikan penyakit yang diturunkan (Orita et al. 1989). Proses yang terjadi dalam PCR meliputi tiga tahap yang penting yaitu denaturasi (pemisahan untai ganda DNA), annealing (penempelan primer), dan ekstensi (pemanjangan primer) (Muladno 2002).
Polymerase Chain Reaction-Restriction Fragment Length Polymorphism
(PCR-RFLP) adalah suatu metode analisis lanjutan dari produk PCR. Metode PCR memanfaatkan perbedaan pola pemotongan enzim restriksi atau enzim pemotong yang berbeda-beda pada setiap mikroorganisme (Orita et al. 1989). Menurut Nei dan Kumar (2000) berdasarkan terpotong atau tidaknya fragmen DNA dengan enzim pemotong, hasil fragmen potongan DNA tersebut dapat divisualisasikan melalui teknik elektroforesis yang hasilnya menunjukan ada tidaknya polimorfisme pada suatu individu atau populasi. Analisis RFLP biasa digunakan untuk mendeteksi adanya keragaman pada gen yang berhubungan dengan sifat ekonomis, seperti produksi dan kualitas susu (Sumantri et al. 2007).
3
METODE
Lokasi dan Waktu
Penelitian ini dilaksanakan di Laboratorium Genetika Molekuler Ternak, Bagian Pemuliaan dan Genetika, Fakultas Peternakan, Institut Pertanian Bogor. Penelitian ini berlangsung dari bulan Agustus 2013 hingga Februari 2014.
7 dan Balai Besar Inseminasi Buatan (BBIB) Singosari sebanyak 28 ekor.
Primer
Primer yang digunakan untuk mengamplifikasi gen STAT5A ekson 7, PRL ekson 3, dan PRL ekson 4 dapat dilihat pada Tabel 1.
Prosedur Ekstraksi DNA
Ekstraksi DNA dilakukan berdasarkan metode Sambrook et al. (1989) yang dimodifikasi. Tahap pertama merupakan preparasi sampel yaitu sampel darah dan semen diambil sebanyak 200 µl dan ditambahkan dengan 1 000 µl NaCl 0.2%, kemudian dihomogenkan menggunakan vortex dan didiamkan selama lima menit. Sampel disentrifugasi pada kecepatan 8 000 rpm selama lima menit dan bagian supernatan dibuang. Tahap kedua adalah degradasi protein yaitu endapan sampel ditambahkan dengan 10 µl Proteinase-K (5mg/ml), 350 µl 1 x STE dan 40 µl SDS 10%, kemudian diinkubasi pada suhu 55 oC selama dua jam. Tahap ketiga bertujuan untuk mendegradasi bahan organik dengan cara larutan yang telah diinkubasi ditambahkan 40 µl NaCl 5 M, 400 µl phenol dan 400 µl CIAA kemudian dikocok perlahan pada suhu ruang selama satu jam. Tahap keempat adalah presipitasi DNA yaitu larutan disentrifugasi dengan kecepatan 12 000 rpm selama lima menit sehingga terbentuk fase DNA. Fase DNA yang terbentuk diambil sebanyak 40 µl dan dipindahkan ke tabung 1.5 ml baru, ditambahkan dengan 40 µl NaCl 5 M dan 800 µl EtOH 96%, dihomogenkan, kemudian diistirahatkan overnight pada suhu -20 oC. Sampel DNA disentrifugasi pada kecepatan 12 000 rpm selama lima menit dan supernatan yang terbentuk dibuang, kemudian endapan ditiriskan sampai kering dan dilarutkan dalam 100 µl buffer TE 80% untuk digunakan pada tahap amplifikasi DNA.
Tabel 1 Primer gen STAT5A ekson 7, PRL ekson 3, dan PRL ekson 4
Gen Sekuens Primer Referensi
STAT5A
8
Amplifikasi DNA
Kondisi amplifikasi DNA terdiri atas tiga tahap, yaitu denaturasi, annealing, dan ekstensi sesuai dengan kondisi PCR (Polymerase Chain Reaction) yang sesuai bagi masing-masing fragmen gen target. Sampel DNA hasil ekstraksi diambil sebanyak 1 µl kemudian dipindahkan ke tabung 0.2 ml. Pereaksi amplifikasi DNA yang terdiri dari 10.75 µl DW, 0.2 µl primer forward, 0.2 µl primer reverse, 0.05 µl Taq polymerase, 1.5 µl buffer, 0.3 µl dNTPs dan 1 µl MgCl2 dimasukkan ke dalam tabung 1.5 µl kemudian dihomogenkan. Campuran pereaksi PCR tersebut didistribusikan ke masing-masing tabung yang berisi sampel DNA kemudian dimasukkan ke dalam mesin PCR. Amplifikasi DNA berlangsung di dalam mesin PCR Applied Biosystems dengan kondisi suhu
predenaturasi 95 oC selama lima menit, 35 siklus untuk tahapan denaturasi pada suhu 95 oC selama 10 detik, annealing pada suhu 60 oC selama 20 detik, dan ekstensi pada suhu 72 oC selama 30 detik, kemudian dilanjutkan dengan tahap ekstensiakhir pada suhu 72 oC selama lima menit dalam satu siklus. Produk PCR dielektroforesis menggunakan gel agarosa 1.5%.
Analisis Penciri PCR-RFLP
Produk amplifikasi dari gen-gen yang dianalisis (STAT5A ekson 7, PRL ekon 3, dan PRL ekson 4) dipotong dengan menggunakan enzim restriksi. Enzim restriksi yang digunakan pada gen STAT5A ekson 7 adalah AvaI (C|YCGRG), sedangkan gen PRL ekson 3 dan PRL ekson 4 dipotong dengan enzim RsaI (GT|AC). Produk PCR diambil sebanyak 5 μl dan dipindahkan ke tabung 0.5 ml. Campuran pereaksi enzim restriksi yang terdiri dari 1 μl DW, 0.3 μl enzim restriksi, dan 0.7 μl buffer tango dihomogenkan dan diambil masing-masing sebanyak 2 μl untuk setiap sampel. Campuran sampel tersebut diinkubasi di agarosa dilarutkan dalam larutan 0.5 x TBE sebanyak 30 ml kemudian dipanaskan dalam microwave selama lima menit, dikocok dengan magnetic stirrer, ditambahkan 2.5 μl EtBr, dan dicetak sehingga terbentuk sumur-sumur di dalam gel. Konsentrasi gel agarosa yang digunakan untuk elektroforesis gen PRL ekson 3 adalah 3.5% dengan komposisi bahan yang sama kecuali serbuk agarosa yang digunakan adalah 1.05 g. Produk PCR-RFLP sebanyak 5 μl dicampurkan dengan 1 μl loading dye kemudian dimasukkan ke dalam sumur-sumur gel. Marker
DNA 100 bp (gen STAT5A ekson 7 dan PRL ekson 4) dan marker 20 bp sebanyak 2 μl ditaruh ke dalam sumur paling kiri sebagai penanda. Gel dialiri listrik 100 volt selama 30-45 menit. Setelah elektroforesis selesai, gel agarosa divisualisasikan dengan menggunakan sinar ultraviolet di dalam mesin UV Transiluminator.
Penentuan Genotipe Gen PRL ekson 3, PRL ekson 4, dan STAT5A ekson 7 Pita-pita DNA yang muncul dari hasil elektroforesis dibandingkan dengan
9 DNA yang terbentuk diidentifikasi sebagai alel untuk penentuan genotipe setiap sampel.
Genotyping Gen PRL ekson 3. Penentuan genotipe gen PRL ekson 3 adalah alel
A tidak memiliki situs potong yang ditunjukkan oleh satu fragmen yang panjangnya sama dengan produk PCR yaitu 156 bp. Alel B memiliki situs potong enzim RsaI (GT|AC) dan ditunjukkan oleh dua fragmen yang masing-masing memiliki panjang 82 bp dan 74 bp (Gambar 3).
Genotyping Gen PRL ekson 4. Penentuan genotipe gen PRL ekson 4 adalah alel
G tidak memiliki situs potong yang ditunjukkan oleh satu fragmen yang panjangnya sama dengan produk PCR yaitu 294 bp. Alel A memiliki situs potong enzim RsaI (GT|AC) dan ditunjukkan oleh dua fragmen yang masing-masing memiliki panjang 162 bp dan 132 bp (Gambar 4).
Genotyping Gen STAT5A ekson 7. Penentuan genotipe gen STAT5A ekson 7
adalah alel C tidak memiliki situs potong yang ditunjukkan oleh satu fragmen yang panjangnya sama dengan produk PCR yaitu 215 pb. Alel C memiliki situs potong enzim AvaI (C|YCGRG) dan ditunjukkan oleh dua fragmen yang masing-masing memiliki panjang 181 pb dan 34 pb (Gambar 5).
Gambar 4 Posisi penempelan primer pada fragmen gen PRL ekson 4 dan situs pemotongan enzim RsaI
10
Sekuensing Fragmen Gen PRL ekson 3, PRL ekson 4, dan STAT5A ekson 7 Sekuensing dilakukan pada individu sapi bali yang mewakili genotipe berbeda dengan jumlah masing-masing dua sampel untuk setiap genotipe dari tiga gen yang dianalisis. Sekuensing dilakukan dengan menggunakan mesin sekuenser (ABI Prims 3100-Avant Genetic Analyzer) pada fragmen primer forward dan
reverse melalui jasa perusahaan sekuensing 1st Base di Selangor, Malaysia. Analisis Data
Frekuensi Alel dan Genotipe
Keragaman genotipe pada masing-masing sampel dari setiap pusat pembibitan sapi bali dapat ditentukan dari pita-pita yang ditemukan. Frekuensi genotipe adalah rasio dari jumlah suatu genotipe terhadap suatu populasi dengan menghitung perbandingan antara jumlah genotipe tertentu pada setiap populasi. Rumus menghitung frekuensi genotipe menurut Nei dan Kumar (2000) sebagai berikut :
ii nii Keterangan :
= frekuensi genotipe ke-ii
nii = jumlah individu bergenotipe ii
N = jumlah individu sampel
Frekuensi alel adalah rasio suatu alel terhadap keseluruhan alel pada suatu lokus dalam populasi. Frekuensi alel ( i dihitung berdasarkan rumus Nei dan Kumar (2000):
i 2nii2 nij Keterangan :
i = frekuensi alel ke-i
nii = jumlah individu bergenotipe ii
nij = jumlah individu bergenotipe ij
N = jumlah individu sampel
11 Heterozigositas
Keragaman genetik dapat diketahui melalui estimasi frekuensi heterozigositas pengamatan (Ho) yang diperoleh dari masing-masing populasi daerah sumber bibit sapi bali dengan menggunakan rumus Weir (1996):
H0 ∑nij i j
Keterangan :
Ho = heterozigositas pengamatan (populasi) nij = jumlah individu heterozigot
N = jumlah individu yang diamati
Heterozigositas harapan (He) berdasarkan frekuensi alel dihitung dengan menggunakan rumus Nei dan Kumar (2000) :
He 1 ∑ i2 q
i 1 Keterangan :
He = nilai heterozigositas harapan i = frekuensi alel
q = jumlah alel
Keseimbangan Hardy-Weinberg
Keseimbangan Hardy-Weinberg diuji dengan Chi-square (Hartl dan Clark 1997):
2 ∑ obs e p 2 e p
Keterangan:
2 = uji Chi-square
Obs = jumlah pengamatan genotipe ke-i Exp = jumlah harapan genotipe ke-i
Derajat bebas (db) untuk uji keseimbangan Hardy-Weinberg berdasarkan Allendorf et al. (2013) sebagai berikut:
db = (jumlah genotipe - jumlah alel)
12
4
HASIL DAN PEMBAHASAN
Amplifikasi Gen PRL dan STAT5A
Amplifikasi fragmen gen PRL ekson 3, PRL ekson 4, dan STAT5A ekson 7 pada sapi bali menghasilkan panjang produk PCR masing-masing sebesar 156 bp (Gambar 6), 294 bp (Gambar 7), dan 215 bp (Gambar 8). Amplifikasi ketiga fragmen gen tersebut dilakukan pada suhu annealing 60 oC selama 20 detik dengan menggunakan mesin thermocycler Applied Biosystems. Suhu annealing
adalah suhu optimal untuk berlangsungnya penempelan primer sesuai dengan sekuens DNA komplementer yang akan diperbanyak selama proses amplifikasi DNA berlangsung. Suhu optimal penempelan primer pada penelitian ini berbeda dengan suhu annealing yang telah dilakukan untuk primer fragmen gen PRL ekson 3, PRL ekson 4, dan STAT5A ekson 7 yaitu masing-masing pada suhu 59 o
C selama 40 detik (Sodhi et al. 2011), suhu 58.5 oC selama 30 detik (Brym et al. 2005), dan suhu 64 oC selama 1 menit (Dario et al. 2009).
Perbedaan suhu annealing tersebut antara lain disebabkan oleh perbedaan kondisi mesin PCR dan campuran komponen pereaksi PCR. Viljoen et al. (2005) menyatakan bahwa suhu annealing berkisar antara 55-72 oC, selain itu suhu optimal annealing salah satunya bergantung pada konsentrasi MgCl2. Pelt-Verkuil et al. (2008) menyatakan bahwa waktu annealing yang dibutuhkan supaya primer dapat berkomplemen dan menempel dengan targetnya bergantung pada kapasitas pemanasan mesin thermocycler yang digunakan, volume campuran PCR serta konsentrasi primer dan gen target.
13
Identifikasi Genotipe Fragmen Gen PRL dan STAT5A
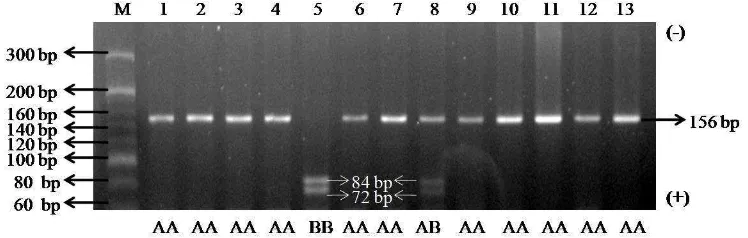
Hasil analisis penciri RFLP dengan menggunakan enzim restriksi RsaI terhadap fragmen gen PRL ekson 3 diperoleh tiga macam fragmen, yaitu fragmen yang tidak dapat dipotong (156 bp) yang dikenal dengan genotipe AA, fragmen yang dapat dipotong (84 bp dan 72 bp) yang dikenal dengan genotipe BB, dan fragmen gabungan (156 bp, 84 bp, dan 72 bp) atau heterozigot yang dikenal dengan genotipe AB (Gambar 9).
Gambar 9 Hasil PCR-RFLP fragmen gen PRL ekson 3 dengan enzim restriksi
RsaI pada gel agarosa 3.5%. M= marker DNA 20 bp. Sampel 1-13= sampel sapi bali
Gambar 8 Hasil amplifikasi gen STAT5A ekson 7 pada sapi bali. M= marker
DNA 100 bp. Sampel 1-10= produk amplifikasi gen STAT5A ekson 7 (215 bp).
Gambar 7 Hasil amplifikasi gen PRL ekson 4 pada sapi bali. M = marker
14
Hasil pemotongan fragmen gen PRL ekson 4 dengan enzim restriksi RsaI diperoleh tiga macam pola restriksi (Gambar 10). Pola pertama adalah fragmen gen yang terpotong oleh enzim RsaI, ditunjukkan oleh dua fragmen pada posisi 162 bp dan 132 bp disebut sebagai genotipe AA. Pola kedua tidak memiliki situs restriksi RsaI sehingga menghasilkan satu pita pada posisi 294 bp (genotipe GG). Pola ketiga adalah gabungan dari ketiga fragmen pada posisi 294, 162, 132 bp (genotipe heterozigot AG).
Berdasarkan hasil identifikasi genotipe ditemukan dua alel (alel A dan alel B) pada gen PRL ekson 3 serta alel A dan alel G pada gen PRL ekson 4. Fragmen gen dari individu-individu sapi bali yang memiliki sekuens situs pemotong enzim
RsaI yaitu GT|AC berarti dapat dipotong fragmen gen PRL ekson 3 maupun fragmen gen ekson 4-nya, sedangkan individu sapi bali yang hanya menunjukkan satu pita berarti terjadi mutasi sekuens enzim RsaIpada fragmen gen PRL ekson 3 dan PRL ekson 4 sehingga tidak dapat dikenali oleh enzim pemotong RsaI.
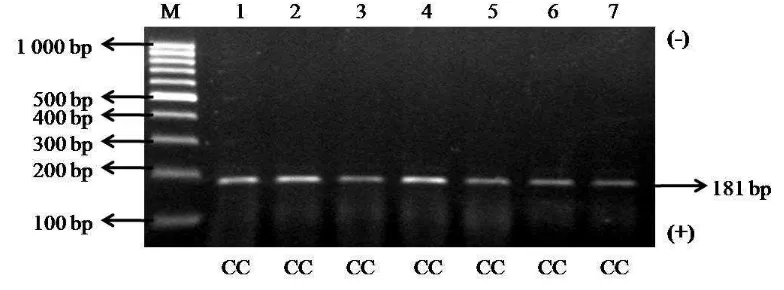
Hasil pemotongan gen STAT5A ekson 7 sapi bali dengan menggunakan enzim restriksi AvaI diperoleh hanya satu macam genotipe (CC) ditunjukkan oleh fragmen yang dapat dipotong pada posisi 181 bp dan 34 bp (Gambar 11). Seluruh individu sapi bali pada penelitian ini memiliki sekuens situs enzim pemotong AvaI yaitu C|YCGRG.
Gambar 11 Hasil PCR-RFLP fragmen gen STAT5A ekson 7 dengan enzim restriksi AvaI pada gel agarosa 2%. M= marker DNA 100 bp. Sampel 1-7= sampel sapi bali
Gambar 10 Hasil PCR-RFLP fragmen gen PRL ekson 4 dengan enzim restriksi
15
Frekuensi Genotipe dan Frekuensi Alel Fragmen Gen PRL|RsaI
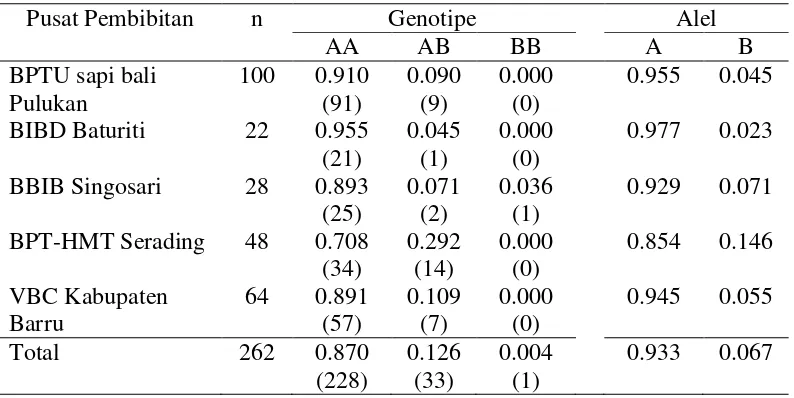
Hasil analisis frekuensi genotipe dan frekuensi alel fragmen gen PRL ekson 3 pada sapi bali yang dikelompokkan berdasarkan populasi pusat pembibitan disajikan pada Tabel 2. Proporsi genotipe fragmen gen PRL ekson 3 pada setiap populasi pembibitan sapi bali yang diteliti menunjukkan bahwa frekuensi genotipe AA paling tinggi, sebaliknya frekuensi genotipe AB rendah dan bahkan hanya ditemukan satu ekor sapi bali yang memiliki genotipe BB yaitu pada populasi BBIB Singosari. Hal tersebut menyebabkan tingginya frekuensi alel A pada seluruh populasi pusat pembibitan sapi bali. Frekuensi genotipe AA pada populasi sapi bali di BIBD Baturiti ditemukan lebih tinggi dibandingkan dengan pusat-pusat pembibitan sapi bali lainnya disebabkan hanya satu ekor sapi bali yang memiliki genotipe berbeda yaitu heterozigot AB. Frekuensi genotipe AB pada populasi sapi bali di BPT-HMT Serading lebih tinggi dibandingkan dengan populasi lainnya. Individu sapi bali yang memiliki genotipe BB ditemukan dengan frekuensi yang sangat rendah pada populasi BBIB Singosari (0.036), sedangkan genotipe BB tidak ditemukan pada populasi pembibitan sapi bali lainnya.
Distribusi alel dari lokus PRL|RsaI ekson 3 ditunjukkan oleh frekuensi alel A yang lebih tinggi dibandingkan dengan frekuensi alel B pada setiap populasi, baik pada sapi bali yang terdapat di Bali (BPTU sapi bali Pulukan dan BIBD Baturiti) maupun di BBIB Singosari, BPT-HMT Serading dan VBC Kabupaten Barru (Tabel 2). Frekuensi alel A fragmen gen PRL ekson 3 pada populasi yang terdapat di BIBD Baturiti (0.977) memiliki kecenderungan yang sama dengan populasi di BPTU sapi bali Pulukan (0.955) dan VBC Kabupaten Barru (0.945), sedangkan frekuensi alel A untuk sapi bali di BPT-HMT Serading lebih rendah (0.854) karena jumlah individu sapi bali bergenotipe AB lebih banyak pada populasi tersebut. Secara keseluruhan, frekuensi alel A gen PRL ekson 3 pada sapi bali yang diidentifikasi di penelitian lebih tinggi dibandingkan beberapa bangsa Tabel 2 Frekuensi genotipe dan alel fragmen gen PRL|RsaI ekson 3
berdasarkan pusat pembibitan sapi bali
Pusat Pembibitan n Genotipe Alel
16
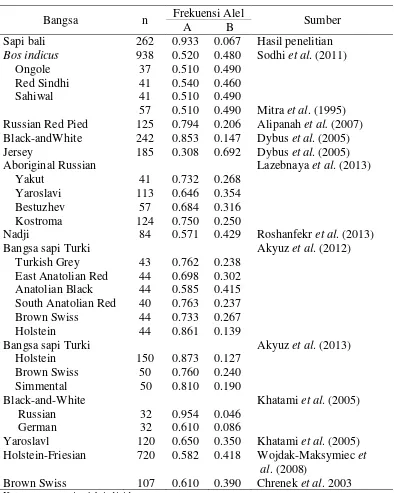
sapi di dunia seperti yang dapat dilihat pada Tabel 3. Hasil identifikasi keragaman genetik gen PRL ekson 3 memberikan informasi adanya dominasi alel A pada pusat-pusat pembibitan sapi bali di Indonesia pada penelitian ini.
Hasil asosiasi fragmen gen PRL ekson 3 dengan sifat kualitas susu yang telah dilaporkan oleh Lazebnaya et al. (2013) menunjukkan bahwa genotipe AA dan AB berhubungan dengan kandungan lemak susu yang lebih tinggi
Aboriginal Russian Lazebnaya et al. (2013)
Yakut 41 0.732 0.268
Black-and-White Khatami et al. (2005)
Russian 32 0.954 0.046
German 32 0.610 0.086
Yaroslavl 120 0.650 0.350 Khatami et al. (2005) Holstein-Friesian 720 0.582 0.418 Wojdak-Maksymiec et
al. (2008)
17 menyatakan bahwa sapi Russian Red Pied yang memiliki genotipe BB menunjukkan produksi susu, lemak susu, dan protein susu yang lebih tinggi.
Frekuensi genotipe dan alel fragmen gen PRL ekson 4 pada sapi bali berdasarkan pusat pembibitan tersaji pada Tabel 4 dan menunjukkan bahwa frekuensi genotipe GG lebih tinggi dibandingkan dengan genotipe AA dan AG. Frekuensi genotipe GG pada populasi sapi bali yang terdapat di BIBD Baturiti tertinggi dibandingkan dengan populasi pusat pembibitan sapi bali lainnya. Frekuensi genotipe AG pada populasi sapi bali di BPT-HMT Serading lebih tinggi dibandingkan dengan pusat pembibitan sapi bali lainnya. Frekuensi genotipe AA pada BBIB Singosari menunjukkan keragaman yang sangat rendah (0.036) sedangkan tidak ditemukan genotipe AA, baik pada populasi sapi bali di BPTU sapi bali Pulukan, BIBD Baturiti, BPT-HMT Serading maupun di VBC Kabupaten Barru. Hasil tersebut dapat menjadi indikator terbatasnya jumlah sapi bali bergenotipe AA di pusat pembibitan sapi bali.
Distribusi frekuensi alel G pada populasi sapi bali di BPTU sapi bali Pulukan, BIBD Baturiti, VBC Kabupaten Barru, dan BBIB Singosari berturut-turut ditemukan lebih tinggi dibandingkan frekuensi alel G pada populasi di BPT-HMT Serading. Hal tersebut disebabkan oleh tingginya jumlah sapi bali bergenotipe heterozigot AG di BPT-HMT Serading. Frekuensi alel G gen PRL ekson 4 pada sapi bali yang diidentifikasi pada penelitian ini ditemukan lebih tinggi dibandingkan dengan beberapa bangsa sapi lain yang tersaji pada Tabel 5.
Tabel 4 Frekuensi genotipe dan alel fragmen gen PRL|RsaI ekson 4 berdasarkan pusat pembibitan sapi bali
Pusat Pembibitan n Genotipe Alel
18
Brym et al. (2005) pada hasil penelitiannya mengenai asosiasi antara polimorfisme gen PRL ekson 4 dengan sifat kualitas susu pada sapi Black-and-White menunjukkan bahwa sapi Black-and-Black-and-White dengan genotipe AG menghasilkan produksi susu tertinggi, sedangkan sapi bergenotipe GG menunjukkan kandungan lemak susu tertinggi. Dong et al. (2013) melaporkan hasil yang kontras yaitu bahwa alel G merupakan alel yang dianggap kurang berpengaruh baik terhadap produksi susu dan protein susu.
Keragaman genetik atau polimorfisme genetik adalah terdapatnya lebih dari satu bentuk atau macam genotipe di dalam populasi. Sumber keragaman genetik disebabkan oleh adanya pengulangan urutan sekuen, insersi, delesi dan rekombinasi di dalam runutan DNA antar individu, kelompok atau suatu populasi (Nei dan Kumar 2000). Hasil penelitian ini menunjukkan bahwa fragmen gen PRL|RsaI ekson 3 dan ekson 4 pada sapi bali bersifat polimorfik rendah karena terdapat tiga tipe genotipe yang ditemukan pada masing-masing fragmen gen tersebut dan frekuensi alel yang diperoleh berada di kisaran 0.930.
Frekuensi Genotipe dan Frekuensi Alel Fragmen Gen STAT5A|AvaI Frekuensi genotipe gen STAT5A pada sapi bali di seluruh populasi pusat pembibitan sapi bali yang diteliti menunjukkan bahwa hanya ditemukan satu macam genotipe yaitu genotipe CC (100%) sehingga frekuensi alel C sebesar 1.00. Hasil yang tersaji pada Tabel 6 menunjukkan bahwa tidak terdapat keragaman genetik fragmen gen STAT5A ekson 7 dan tidak ditemukan alel T pada seluruh populasi sapi bali yang diteliti. Frekuensi alel C yang tinggi pada lokus STAT5A|AvaI mengarah kepada terjadinya fiksasi untuk genotipe CC karena setiap populasi sapi bali memiliki frekuensi alel C yang sama (1.00) atau dikenal sebagai alel monomorfik.
Tabel 5 Frekuensi alel fragmen gen PRL|RsaI ekson 4 pada sapi bali hasil penelitian dan beberapa bangsa sapi
Bangsa n Frekuensi Alel Sumber
A G
Sapi bali 262 0.065 0.935 Hasil penelitian Black-and-White 186 0.113 0.887 Brym et al. (2005) Jersey 138 0.706 0.294 Brym et al. (2005) Chinese Holstein 586 0.125 0.875 Dong et al. (2013)
Iranian Holstein 268 0.069 0.931 Mehmannavaz et al. (2009) Colombia Holstein 1 462 0.167 0.833 Rincon et al. (2011)
19
Dario et al. (2009b) menyatakan bahwa gen STAT5A merupakan gen kandidat untuk sifat kuantitatif hewan ternak dan hasil penelitiannya membuktikan bahwa sapi pejantan Podolica yang memiliki genotipe CC dan CT menunjukkan bobot hidup yang lebih tinggi dan pertumbuhan yang lebih cepat dibandingkan dengan genotipe TT. Gen STAT5A merupakan salah satu gen kandidat yang merupakan anggota dari interferon-τ (IFN-τ dan placental lactogen (PL) signal transduction pathways yang berperan penting dalam mengatur sifat reproduksi dan produksi susu (Khatib et al. 2008).
Polimorfisme fragmen gen STAT5A ekson 7 pada beberapa bangsa sapi di dunia dapat dilihat pada Tabel 7. Penelitian ini menunjukkan hasil bahwa lokus STAT5A|AvaI ekson 7 bersifat monomorfik karena hanya ditemukan satu tipe alel yaitu alel C pada setiap pusat pembibitan sapi bali yang diteliti. Kejadian monomorfisme ini mengindikasikan bahwa alel C merupakan alel spesifik pada sapi bali sehingga menyebabkan keterbatasan dalam penggunaan gen STAT5A ekson 7 sebagai penciri sifat reproduksi. Kejadian monomorfisme pada sapi bali telah dilaporkan oleh beberapa peneliti antara lain pada lokus GHR|AluI (Zulkharnaim et al. 2010), lokus GH|AluI (Jakaria dan Noor 2011), lokus FSH Beta-subunit|PstI (Ishak et al. 2011 , dan lokus κ-casein|HindIII Mu’in dan
Supriyantono 2012).
Penyebab kejadian monomorfisme pada sapi bali antara lain terjadinya proses seleksi alam dan program pemuliaan yang belum terarah dan berkelanjutan. Sapi bali yang berukuran besar dan memiliki performa terbaik dijual dan dipotong sehingga terjadi seleksi negatif dan berdampak pada terkurasnya keragaman genetik sapi bali. Sapi bali yang tersisa dari proses seleksi negatif tersebut menyebabkan proporsi genotipe berubah dan yang tersisa hanya sapi bali yang memiliki genotipe tertentu untuk diwariskan kepada keturunan-keturunan selanjutnya.
Oleh sebab itu, pemerintah melakukan program nasional pemurnian dan peningkatan mutu genetik ternak pada sapi bali sejak tahun 1976 di Pulau Bali berdasarkan Surat Keputusan (SK) Menteri Pertanian nomor 776/Kpts/Um/12/1976. Kegiatan yang dilakukan oleh Proyek Pengembangan dan Pembibitan sapi bali (P3Bali) adalah pemuliaan sapi bali dengan melakukan seleksi dalam bangsa sehingga diperoleh bibit sapi bali yang bermutu baik (Soehadji 1990). Pemusatan dan pemurnian genetik sapi bali di daerah tertentu dalam jangka waktu yang cukup panjang menyebabkan terjadinya silang dalam. Tabel 6 Frekuensi genotipe dan alel fragmen gen STAT5A|AvaI ekson 7
20
Noor (2008) menyatakan bahwa silang dalam adalah salah satu bentuk isolasi secara genetik karena pada suatu populasi yang terisolasi akan menyebabkan keterbatasan pilihan dalam proses perkawinan. Program pengembangan di pusat-pusat pembibitan sapi bali berkaitan dengan pewarisan sifat dari tetua yang menyumbangkan alel homozigot kepada keturunannya sehingga keragaman genotipe pada populasi bersifat monomorfik.
Heterozigositas
Marson et al. (2005) menyatakan bahwa keragaman genetik suatu populasi dapat diukur menggunakan nilai heterozigositas yang bertujuan untuk membantu program seleksi. Nilai heterozigositas (Tabel 8) menunjukkan bahwa lokus PRL|RsaI di ekson 3 dan ekson 4 pada populasi sapi bali yang terdapat di
BPT-Tabel 7 Frekuensi genotipe dan alel fragmen gen STAT5A|AvaI ekson 7 pada sapi bali hasil penelitian dan beberapa bangsa sapi
Bangsa n Frekuensi Alel Sumber
Santa Gertrudes Nelore 17 1.000 0.000 Suguisawa (2005)
Sapi Italia Dario et al. (2009a)
Sapi Pedaging Flisikowski et al. (2003)
21 HMT Serading menghasilkan nilai heterozigositas tertinggi. Nilai heterozigositas yang lebih rendah ditemukan berturut-berturut pada populasi di VBC Kabupaten Barru, BPTU sapi bali Pulukan, BBIB Singosari, sedangkan populasi sapi bali di BIBD Baturiti memiliki nilai heterozigositas yang terendah. Berdasarkan Tambasco et al. (2003), jika perbedaan antara nilai Ho dan He tidak besar, maka dapat menjadi indikator adanya keseimbangan genotipe dalam populasi yang dianalisis. Hasil analisis nilai heterozigositas harapan (He) dan heterozigositas pengamatan (Ho), baik untuk ekson 3 dan ekson 4 pada gen PRL menunjukkan bahwa frekuensi genotipe dari setiap populasi sapi bali yang diteliti berada dalam keseimbangan, kecuali pada populasi sapi bali di BBIB Singosari.
Nilai heterozigositas paling rendah ditemukan pada lokus STAT5A|AvaI ekson 7 (0.000) pada setiap populasi sapi bali yang dianalisis karena adanya alel monomorfik C. Hasil analisis heterozigositas pada penelitian ini termasuk rendah sesuai dengan pernyataan Javanmard et al. (2005) bahwa jika nilai heterozigositas dibawah 0.50 maka keragaman suatu gen pada populasi tergolong rendah.
Keseimbangan Hardy-Weinberg
Hasil uji chi-square ( menunjukkan bahwa frekuensi genotipe fragmen gen PRL|RsaI ekson 3 dan ekson 4 tidak berada dalam keseimbangan Hardy-Weinberg pada populasi sapi bali di BBIB Singosari. Keseimbangan genotipe hanya dapat dianalisis pada populasi sapi bali di BBIB Singosari karena populasi tersebut memiliki tiga macam genotipe, sedangkan pada populasi sapi bali lainnya hanya memiliki dua macam genotipe sehingga tidak dapat dilakukan analisis Tabel 8 Nilai heterozigositas pengamatan (Ho), nilai heterozigositas harapan
(He), dan hasil uji keseimbangan Hardy-Weinberg berdasarkan pusat pembibitan sapi bali
22
keseimbangan Hardy-Weinberg karena derajat bebas yang diperoleh sama dengan nol (0). Keseimbangan frekuensi genotipe pada fragmen gen STAT5A|AvaI ekson 7 tidak dapat dianalisis karena hanya ditemukan satu tipe alel yaitu alel C dengan frekuensi alel yang bersifat monomorfik yaitu 1.00.
Allendorf et al. (2013) menyatakan bahwa suatu populasi dinyatakan berada dalam keseimbangan jika frekuensi genotipe dan frekuensi alelnya konstan dari generasi ke generasi yang diakibatkan oleh penggabungan gamet yang terjadi secara acak dalam populasi yang besar. Keseimbangan gen dalam populasi terjadi jika tidak adanya mutasi, seleksi, migrasi, dan genetic drift.
Ketidakseimbangan gen dalam populasi sapi bali di BBIB Singosari terjadi karena adanya populasi yang terbagi sebagai fungsi dari BBIB Singosari sebagai penghasil semen beku. Seleksi sebagai salah satu faktor yang dapat mengubah keseimbangan dalam populasi secara cepat terjadi pada populasi sapi bali di BBIB Singosari karena populasi tersebut terdiri dari pejantan-pejantan unggul sapi bali hasil seleksi berdasarkan sifat reproduksi yang terpilih sebagai penghasil semen beku, namun hal tersebut juga dipengaruhi jumlah sampel yang terbatas (28 ekor).
Homologi dan Deteksi Mutasi Gen Prolaktin (PRL)
Hasil perunutan dan penyejajaran sekuens nukleotida gen PRL ekson 3 dengan GenBank (kode akses AY339391 dan AF426315) menggunakan pasangan primer forward dan reverse menunjukkan bahwa pada genotipe AA terjadi mutasi basa adenin (A) menjadi basa guanin (G) di posisi basa ke-75 dari produk PCR sebesar 156 bp (Gambar 12). Mutasi tersebut menyebabkan enzim restriksi RsaI tidak dapat mengenali situs pemotongnya (GT|AC) sehingga hanya dihasilkan satu fragmen pada posisi 156 bp. Mutasi di bagian ekson 3 gen PRL telah dilaporkan oleh Lewin et al. (1992), bahwa ditemukan mutasi transisi synonimous
23
Mutasi transisi antara basa adenin menjadi basa guanin (AG) juga terjadi pada bagian ekson 4 gen PRL. Genotipe GG merupakan representasi dari terjadinya mutasi basa adenin (A) menjadi basa guanin (G) sehingga terjadi perubahan situs enzim restriksi RsaI GT|AC menjadi GT|GC yang ditunjukkan oleh satu fragmen tidak terpotong pada posisi 294 bp (Gambar 13). Hal tersebut sesuai dengan hasil penelitian yang dilakukan oleh Brym et al. (2005) yang menemukan single nucleotide polymorphism (SNP) pada posisi 8938R di fragmen gen PRL ekson 4. Mehmannavaz et al. (2009) menyatakan bahwa mutasi AG pada situs restriksi PRL|RsaI untuk kedua basa tersebut merupakan silent mutation dimana tidak terjadi perubahan asam amino yaitu tetap dihasilkan asam amino valin (Val/Val). Sekuens gen PRL ekson 4 untuk genotipe GG memiliki kesamaan runutan nukleotida sebesar 99% dengan sekuens GenBank fragmen gen PRL ekson 4 Bos taurus (kode akses AY339391 dan AF426315), sedangkan genotipe AA memiliki homologi sebesar 98%.
Mutasi antara basa adenin (A) dan guanin (G) yang terjadi pada sekuens situs retriksi enzim RsaI baik pada gen PRL ekson 3 maupun ekson 4 adalah mutasi transisi. Mutasi transisi adalah mutasi titik yang disebabkan oleh perubahan basa purin menjadi purin (AG, GA) dan basa pirimidin menjadi basa pirimidin (CT, TC) (Brown 2002). Mutasi disebabkan oleh kesalahan (mispairing) basa-basa nukleotida selama replikasi DNA sehingga menghasilkan sekuens baru (Li dan Graur 1991).
24
Homologi dan Deteksi Mutasi Gen STAT5A
Hasil alignment nukleotida sekuens gen STAT5A ekson 7 sapi bali yang dibandingkan dengan GenBank (kode akses AJ237937) berhasil mengidentifikasi situs restriksi enzim AvaI (C|YCGRG). Gambar 14 menunjukkan bahwa enzim
AvaI mengenali situs pemotongnya (C|CCGAG) sehingga menghasilkan dua fragmen terpotong yang disebut sebagai genotipe CC atau alel C. Hasil BLAST nukleotida sekuens fragmen gen STAT5A|AvaI menunjukkan bahwa sapi bali memiliki kesamaan yang tinggi terhadap sekuens gen STAT5A Bos taurus yang terdapat di GenBank (kode akses AJ237937) dengan tingkat kesamaan (homologi) yang tinggi yaitu sebesar 99%.
IUPAC single-letter codes dari program MEGA5 digunakan untuk mendefinisikan sekuens nukleotida dimana simbol Y untuk basa pirimidin (C atau T/U) dan simbol G untuk purin (A atau G). Hasil analisis sekuens mengonfirmasi bahwa lokus STAT5A|AvaI untuk seluruh populasi sapi bali yang diteliti bersifat monomorfik karena tidak terjadi mutasi pada sekuens situs restriksi enzim AvaI. Gambar 13 Hasil perunutan nukleotida sekuens gen PRL|RsaI ekson 4 pada
25 Flisikowski et al. (2003) menyatakan bahwa SNP pada exon 7 gen bovine
STAT5A merupakan substitusi antara basa sitosin (C) dengan basa timin (T) pada posisi 6853. Mutasi tersebut merupakan mutasi synonimous karena kedua kodon (CCC dan CCT) menyandikan asam amino yang sama yaitu prolin.
Li dan Graur (1991) menyatakan bahwa mutasi synonimous tidak mengubah sekuens asam amino dari sebuah protein, oleh karena itu mutasi tersebut tidak dapat dideteksi pada tingkat asam amino. Namun, mutasi synonimous tidak selalu bersifat silent mutation, sebagai contoh mutasi tersebut dapat menciptakan situs
splicing baru atau menghapuskan situs splicing yang sudah ada sehingga suatu sekuens ekson berubah menjadi intron dan menyebabkan diproduksinya polipeptida yang berbeda.
Strategi Pengembangan Sumberdaya Genetik Sapi Bali
Sapi bali sebagai salah satu ternak asli Indonesia yang populasinya tersebar di beberapa daerah di Indonesia seperti Bali, Nusa Tenggara Barat, Nusa Tenggara Timur, dan Sulawesi memiliki potensi genetik dan keunggulan jika dibandingkan dengan bangsa sapi lokal lain yang berada di Indonesia. Sapi bali telah banyak dilaporkan memiliki daya adaptasi yang baik terhadap lingkungan marginal namun tetap menunjukkan kemampuan reproduksi yang luar biasa. Hal tersebut merupakan keunikan dan keunggulan sapi bali karena pada umumnya bangsa sapi lain akan mengorbankan daya reproduksinya dalam kondisi lingkungan dan pakan yang kurang mendukung.
26
Pengelolaan sumberdaya genetik ternak untuk memperoleh karakteristik genetik sapi bali sangat penting untuk dilaksanakan melalui langkah-langkah yang tepat. Karakterisasi sumberdaya genetik terdiri dari empat langkah yaitu dokumentasi, evaluasi, pengembangan program pemuliaan, dan konservasi (Turner 1981). Dokumentasi sebagai langkah pertama merupakan suatu upaya untuk mengetahui informasi mengenai keberadaan dan performa sapi bali pada berbagai kondisi lingkungan yang berbeda. Beberapa laporan mengenai performa produksi dan reproduksi sapi bali menunjukkan bahwa sapi bali tetap menunjukkan kemampuan reproduksi yang sangat baik pada berbagai kondisi di daerah Indonesia. Perbaikan pakan dan manajemen pada sapi bali diketahui dapat meningkatkan kualitas sapi bali baik secara produksi maupun reproduksi. Identifikasi gen-gen kandidat pada sapi bali merupakan suatu upaya untuk mengetahui keragaman genetik sapi bali untuk kemudian dibandingkan dengan bangsa-bangsa sapi lain sebagai langkah evaluasi dan penelusuran strategi pengembangan sumber daya genetik yang tepat.
Langkah ketiga adalah pengembangan program pemuliaan sapi bali. Jika dilihat dari dua sudut pandang maka strategi pemuliaan sapi bali dapat ditempuh melalui pelestarian dan pengembangan sapi bali. Strategi pelestarian sapi bali yang dilihat dari sudut pandang konservasi adalah menjaga supaya kemurnian dan keunikan sapi bali tetap terjaga terutama pada pusat-pusat pembibitan sapi bali sehingga diharapkan kombinasi gen-gen yang bersifat positif dapat dipertahankan. Strategi pengembangan melalui sistem tertutup atau close breeding program
merupakan salah satu sistem yang dapat diaplikasikan pada program pemuliaan sapi bali agar peningkatan mutu genetik dapat dicapai dengan tetap menjaga kemurnian sapi bali. Strategi lainnya adalah dengan cara mengeksplorasi lebih dalam dan secara menyeluruh mengenai keragaman gen-gen kandidat yang berpengaruh terhadap sifat reproduksi pada sapi bali. Pencatatansilsilah, data-data fenotipik serta sifat produksi dan reproduksi pada pusat-pusat pembibitan dapat mendukung pelaksanaan asosiasi antara sifat yang diinginkan dengan polimorfisme genetik sehingga informasi yang diperoleh menjadi sangat berharga dan bermanfaat seperti yang dapat dilihat pada Tabel 9, Tabel 10, dan Tabel 11. Hasil asosiasi tersebut berfungsi sebagai data pendukung secara ilmiah supaya pengambilan keputusan program pemuliaan dan pelestarian sapi bali dapat dilakukan secara tepat dan berkelanjutan.
Berdasarkan hasil penelitian ini diperoleh bahwa gen-gen pengatur sifat reproduksi pada sapi bali bersifat monomorfik (gen STAT5A ekson 7) dan memiliki keragaman yang sangat rendah (gen PRL ekson 3 dan ekson 4). Hal tersebut menunjukkan bahwa sapi bali sebagai hasil domestikasi langsung dari banteng (Bibos banteng) yang telah beradaptasi terhadap proses seleksi alam terbukti mampu menunjukkan penampilan reproduksi yang superior. Oleh karena itu, diduga keragaman genetik yang sangat rendah pada sapi bali merupakan profil yang memungkinkan bagi sapi bali untuk mengekspresikan fenotipiknya sebagai bangsa sapi yang sangat subur.
27 tersebut berpengaruh positif terhadap peningkatan performa sapi bali maka hal tersebut merupakan peluang untuk meningkatkan dan memperbaiki keragaman genetik pada pusat-pusat pembibitan dengan cara menyusun pola perkawinan. Pejantan tersebut dapat dimanfaatkan untuk diproduksi semennya dan digunakan untuk dikawinkan dengan ternak-ternak betina sapi bali. Namun, penggunaan semen beku pejantan tersebut harus diawasi dan dipertimbangkan supaya angka
inbreeding pada sapi bali tidak meningkat dan menyebabkan keragaman genetik semakin rendah. Selain itu, perlu adanya kebijakan pemerintah mengenai pewilayahan untuk tujuan persilangan sapi bali yang terarah dan diikuti dengan seleksi untuk menyingkirkan kemungkinan gen-gen yang bersifat letal atau membawa sifat negatif. Pewilayahan untuk persilangan sapi bali diatur supaya tidak dilakukan pada daerah-daerah konservasi maupun pusat pembibitan sapi bali.
Tabel 9 Asosiasi genotipe fragmen gen PRL|RsaI ekson 3 dengan sifat kuantitatif pada beberapa bangsa sapi
Bangsa Genotipe Sifat Sumber
Russian Red Pied
BB Produksi susu, lemak susu, dan protein susu lebih tinggi
Alipanah et al. (2007)
Yaroslavl AA Kandungan lemak susu lebih tinggi pada laktasi ketiga
Lazebnaya et al. (2013) BB Kandungan lemak susu lebih rendah Khatami et al.
(2005) Jersey AA Kandungan lemak susu lebih rendah
pada laktasi pertama
Dybus et al. (2005) AB Kandungan lemak dan protein susu
yang lebih tinggi pada laktasi ketiga
Hostein-Friesian
AA Somatic Cell Count (SCC) pada susu lebih rendah