UJI MUTU BAHAN BAKU RIBOFLAVIN SEBAGAI
BAHAN BAKU VITAMIN B KOMPLEKS YANG DIPRODUKSI
OLEH PT. KIMIA FARMA (PERSERO) TBK. PLANT MEDAN
TUGAS AKHIR
OLEH:
YULITA ARMIYA
NIM 122410079
PROGRAM STUDI DIPLOMA III
ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
ii
KATA PENGANTAR Bismillahirrahmanirrahim,
Puji dan syukur penulis panjatkan atas kehadirat Allah SWT yang telah
memberikan rahmat dan karunia-Nya, sehingga penulis dapat menyusun dan
menyelesaikan Tugas Akhir berjudul ”UJI MUTU BAHAN BAKU
RIBOFLAVIN SEBAGAI BAHAN BAKU VITAMIN B KOMPLEKS YANG
DIPRODUKSI OLEH PT. KIMIA FARMA (PERSERO) TBK. PLANT
MEDAN”. Tugas Akhir ini disusun sebagai salah satu syarat untuk dapat
menyelesaikan pendidikan Program Studi Diploma III Analis Farmasi dan
Makanan di Fakultas Farmasi Universitas Sumatera Utara, Medan.
Penulis menyadari sepenuhnya bahwa tanpa bantuan dari berbagai pihak,
penulis tidak akan dapat menyelesaikan tugas akhir ini sebagaimana mestinya.
Untuk itu penulis mengucapkan terima kasih yang sebesar-besarnya kepada
berbagai pihak antara lain:
1. Ibu Prof. Dr. Julia Reveny, M.Si., Apt., selaku Wakil Dekan I Fakultas
Farmasi Universitas Sumatera Utara.
2. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt., Ketua Program Studi
Diploma III Analis Farmasi dan Makanan.
3. Bapak Drs. Agusmal Dalimunthe M.S., Apt., selaku Dosen Pembimbing
Tugas Akhir yang telah banyak memberikan bimbingan dan pengarahan
dengan penuh perhatian hingga Tugas Akhir ini selesai.
4. Bapak Yogi Sugianto S.Farm., Apt., selaku Pembimbing Praktek Kerja
iii
membimbing dan memberikan banyak ilmu dan arahan pada saat Praktek
Kerja Lapangan.
5. Bapak Dr., Muchlisyam, M.Si., Apt., sebagai Dosen Penasehat Akademis
yang telah memberikan nasehat dan pengarahan kepada penulis dalam hal
Akademis setiap semester.
6. Dosen dan Pegawai Fakultas Farmasi Program Studi Diploma III Analis
Farmasi dan Makanan yang berupaya mendukung kemajuan mahasiswa.
7. Seluruh Staf dan Pegawai PT. Kimia Farma (Persero) Tbk. Plant Medan yang
telah meluangkan waktu, tenaga dan pikiran kepada penulis dalam
melaksanakan Praktek Kerja Lapangan.
8. Teman-teman PKL yang saling mendukung dan bahu membahu selama PKL
hingga Tugas Akhir ini selesai dan teman-teman mahasiswa Analis Farmasi
dan Makanan stambuk 2012 semuanya tanpa terkecuali, adik-adik stambuk
2013 dan 2014 yang tidak disebutkan namanya satu persatu, terima kasih atas
kebersamaan dan semangatnya selama ini, serta masukan dalam penyusunan
Tugas Akhir ini.
9. Serta pihak-pihak yang telah ikut membantu penulis namun tidak tercantum
namanya.
Teristimewa kedua orang tua penulis yaitu Alm. Ayahanda Suhaili Ismail
dan Ibunda Ulfa haini serta saudara-saudara penulis yaitu Kakak Qamarul Laily,
Emalyn Senorita dan Mona Maya Mita yang selalu memberikan doa serta
semangat, perhatian, dorongan dan pengorbanan baik moril maupun materil dalam
iv
Penulis menyadari sepenuhnya bahwa dalam penulisan maupun penyajian
tugas akhir ini terdapat kekurangan dan kelemahan serta masih jauh dari
kesempurnaan, oleh karena itu dengan segala kerendahan hati penulis
mengharapkan saran dan kritik yang sifatnya membangun demi kesempurnaan
tugas akhir ini. Akhir kata, semoga Allah SWT melimpahkan rahmat dan
karunia-Nya kepada kita semua dan harapan penulis semoga tugas akhir ini dapat
memberikan manfaat bagi kita semua. Aamiin yaa Rabbal Alamin.
Medan, April 2015 Penulis,
v
UJI MUTU BAHAN BAKU RIBOFLAVIN SEBAGAI
BAHAN BAKU VITAMIN B KOMPLEKS YANG DIPRODUKSI OLEH PT. KIMIA FARMA (PERSERO) TBK. PLANT MEDAN
Abstrak
Latar Belakang: Mutu adalah keseluruhan ciri dan karakteristik suatu produk atau layanan yang mendukung kemampuan produk atau layanan itu untuk memuaskan kebutuhan yang dinyatakan atau kebutuhan yang tersirat, sehingga mutu merupakan ketentuan konsumen, bukan produsen atau pemasok. Pengawasan terhadap mutu bahan baku riboflavin perlu dilakukan karena jika tidak memenuhi syarat dapat merugikan konsumen. Oleh karena itu, pemeriksaan terhadap mutu bahan baku riboflavin harus dilakukan sebelum diproses menjadi sediaan.
Tujuan: Pengujian ini bertujuan untuk mengetahui mutu dari bahan baku riboflavin yang akan digunakan menjadi bahan berkhasiat dalam formulasi pembuatan sediaan tablet vitamin B kompleks memenuhi syarat seperti yang tertera pada Farmakope Indonesia Edisi IV.
Hasil: Hasil pengukuran didapatkan bahwa riboflavin memenuhi spesifikasi pemerian serbuk hablur kuning atau orange kuning, kelarutan sangat sukar larut dalam air praktis tidak larut dalam etanol 96%, susut pengeringan maks 1,5%, suhu lebur ± 280ºC dan kadar yang diperoleh adalah 98,03%, 99,07%, 100,07%, 98,98%.
Kesimpulan: Hasil pemeriksaan bahan baku riboflavin yang telah ditetapkan pemerian, kelarutan, susut pengeringan, suhu lebur, dan kadarnya tersebut telah memenuhi persyaratan Farmakope Indonesia Edisi III dan IV.
vi
QUALITY TEST SUBSTANCE RIBOFLAVIN AS
BASIC SUBSTANCE VITAMIN B COMPLEX THAT PRODUCTION BY PT. KIMIA FARMA (PERSERO) TBK. PLANT MEDAN
Abstract
Background: Quality is all of characteristics a product or service that support ability a product or the service forward to satisfied need that evident or the real need, so that quality is certained the consument, neither producer nor supplier. Supervision quality basic substance riboflavin it needs to do it because if there are not fullfill condition can lose out the consument. However, inspection quality basic substance riboflavin have to do before in process can be ready.
Objective: The test have to objective to know quality from basic substance riboflavin it can be used special quality in formulation vitamin B complex tablet dosage is form fullfill condition like officially stamped of Indonesia Farmakope edition IV.
Result: The result of measure it getting that riboflavin fullfill specification form dust the yellow crystal or orange yellow, dissolved is very difficult dissolve in practis water is not dissolve in etanol 96%, decrease warming max 1,5%, melted temperature ± 280ºC and the degree getting are 98,03%, 99,07%, 100,07%, 98,98%.
Conclution: The result of inspection basic substance riboflavin decided form, dissolved, decrease of warming, melted temperature, and the degree have fullfilled condition of Indonesia Farmakope Edition III and IV.
viii
2.7.2. Instrumentasi Spektrofotometer UV-Vis ... 16
ix
3.4.3. Susut Pengeringan ... 20
3.4.4. Suhu Lebur ... 21
3.4.5. Pembuatan Larutan Baku ... 22
3.4.6. Pembuatan Larutan Uji ... 22
3.4.7. Penetapan Kadar Secara Spektrofotometer UV-Vis ... 22
3.4.8. Perhitungan ... 23
BAB IV HASIL DAN PEMBAHASAN ... 25
4.1. Hasil ... 25
4.2. Pembahasan ... 26
BAB V KESIMPULAN DAN SARAN ... 27
5.1. Kesimpulan ... 27
5.2. Saran ... 27
x
DAFTAR TABEL
Halaman
xi
DAFTAR GAMBAR
Halaman
xii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Perhitungan Penetapan Kadar Bahan Baku ... 30
Lampiran 2. Hasil Pemeriksaan Bahan Baku ... 32
Lampiran 3. Hasil Absorban Larutan Uji ... 33
Lampiran 4. Hasil Absorban Larutan Standart ... 34
Lampiran 5. Gambar Alat Digital Semi Micro Balance ... 35
Lampiran 6. Gambar Alat Melting Point Analyzer ... 35
Lampiran 7. Gambar Alat Moisture Analyzer ... 36
v
UJI MUTU BAHAN BAKU RIBOFLAVIN SEBAGAI
BAHAN BAKU VITAMIN B KOMPLEKS YANG DIPRODUKSI OLEH PT. KIMIA FARMA (PERSERO) TBK. PLANT MEDAN
Abstrak
Latar Belakang: Mutu adalah keseluruhan ciri dan karakteristik suatu produk atau layanan yang mendukung kemampuan produk atau layanan itu untuk memuaskan kebutuhan yang dinyatakan atau kebutuhan yang tersirat, sehingga mutu merupakan ketentuan konsumen, bukan produsen atau pemasok. Pengawasan terhadap mutu bahan baku riboflavin perlu dilakukan karena jika tidak memenuhi syarat dapat merugikan konsumen. Oleh karena itu, pemeriksaan terhadap mutu bahan baku riboflavin harus dilakukan sebelum diproses menjadi sediaan.
Tujuan: Pengujian ini bertujuan untuk mengetahui mutu dari bahan baku riboflavin yang akan digunakan menjadi bahan berkhasiat dalam formulasi pembuatan sediaan tablet vitamin B kompleks memenuhi syarat seperti yang tertera pada Farmakope Indonesia Edisi IV.
Hasil: Hasil pengukuran didapatkan bahwa riboflavin memenuhi spesifikasi pemerian serbuk hablur kuning atau orange kuning, kelarutan sangat sukar larut dalam air praktis tidak larut dalam etanol 96%, susut pengeringan maks 1,5%, suhu lebur ± 280ºC dan kadar yang diperoleh adalah 98,03%, 99,07%, 100,07%, 98,98%.
Kesimpulan: Hasil pemeriksaan bahan baku riboflavin yang telah ditetapkan pemerian, kelarutan, susut pengeringan, suhu lebur, dan kadarnya tersebut telah memenuhi persyaratan Farmakope Indonesia Edisi III dan IV.
vi
QUALITY TEST SUBSTANCE RIBOFLAVIN AS
BASIC SUBSTANCE VITAMIN B COMPLEX THAT PRODUCTION BY PT. KIMIA FARMA (PERSERO) TBK. PLANT MEDAN
Abstract
Background: Quality is all of characteristics a product or service that support ability a product or the service forward to satisfied need that evident or the real need, so that quality is certained the consument, neither producer nor supplier. Supervision quality basic substance riboflavin it needs to do it because if there are not fullfill condition can lose out the consument. However, inspection quality basic substance riboflavin have to do before in process can be ready.
Objective: The test have to objective to know quality from basic substance riboflavin it can be used special quality in formulation vitamin B complex tablet dosage is form fullfill condition like officially stamped of Indonesia Farmakope edition IV.
Result: The result of measure it getting that riboflavin fullfill specification form dust the yellow crystal or orange yellow, dissolved is very difficult dissolve in practis water is not dissolve in etanol 96%, decrease warming max 1,5%, melted temperature ± 280ºC and the degree getting are 98,03%, 99,07%, 100,07%, 98,98%.
Conclution: The result of inspection basic substance riboflavin decided form, dissolved, decrease of warming, melted temperature, and the degree have fullfilled condition of Indonesia Farmakope Edition III and IV.
1 BAB I PENDAHULUAN 1.1 Latar Belakang
Mutu adalah keseluruhan ciri dan karakteristik suatu produk atau layanan
yang mendukung kemampuan produk atau layanan itu untuk memuaskan
kebutuhan yang dinyatakan atau kebutuhan yang tersirat (Siregar, 2010).
Mutu harus dijaga mulai dari perencanaan terhadap produk, termasuk
perencanaan terhadap bangunan, ruang-ruang, ventilasi, kebersihan, dan sanitasi
lingkungan yang akan mendukung proses produksi nantinya (Lachman, dkk.,
1994).
Vitamin merupakan suatu molekul organik yang sangat diperlukan oleh
tubuh untuk proses metabolisme dan pertumbuhan yang normal. Vitamin-vitamin
tidak dapat dibuat oleh tubuh manusia dalam jumlah yang sangat cukup, oleh
karena itu, harus diperoleh dari bahan pangan yang dikonsumsi (Budiyanto,
2009).
Riboflavin dalam bentuk murni diperoleh dari isolasi ragi, hati, putih telur
dan susu. Vitamin ini dinamakan riboflavin karena terjadi dari persenyawaan
ribosa (satu gula lima karbon) dengan suatu zat berwarna kuning orange yang
memberikan fluoresensi kuning kehijauan pada larutan. Sumber riboflavin
terutama berasal dari hasil ternak. Hati, ginjal, dan jantung mengandung riboflavin
dalam jumlah yang sangat tinggi (Budiyanto, 2009).
Bahan baku adalah semua bahan, baik yang berkhasiat (zat aktif) maupun
2
yang digunakan dalam pengolahan obat walaupun tidak semua bahan tersebut
masih terdapat didalam produk ruahan (Siregar, 2010).
Komponen bahan baku adalah bahan aktif, bahan tambahan dan bahan
pengemas. Pada bentuk sediaan tablet bahan bakunya adalah bahan aktif (active
pharmacetical ingredient), bahan pengisi, bahan pengikat, bahan pengembang,
dan bahan pelicin. Dalam hal tertentu bisa juga ditambahkan bahan lain, bahan
pewarna, penambah rasa, antioksidan. Di industri PT. Kimia Farma Plant. Medan
salah satu tablet yang diproduksi adalah vitamin B kompleks. Salah satu Bahan
aktifnya adalah riboflavin harus memenuhi spesifikasi Farmakope Edisi III
meliputi pemerian, kelarutan, susut pengeringan, suhu lebur, dan kadar. Guna
pemeriksaan bahan baku untuk menyesuaikan persyaratan spesifikasi, serta
menghindari pemalsuan.
Pada industri PT. Kimia Farma Plant. Medan pemeriksaan bahan baku
dilakukan oleh laboratorium Quality Control. Berdasarkan hal diatas maka penulis
ingin berpartisipasi ikut melakukan pemeriksaan bahan baku pada industri
tersebut. Sehingga penulis tertarik untuk mengambil judul tugas akhir sebagai
berikut ”Uji Mutu Bahan Baku Riboflavin Sebagai Bahan Baku Vitamin B
Kompleks”. Dalam tugas akhir ini data yang ditampilkan adalah hasil
pemeriksaan bahan baku riboflavin pada siklus pertama tahun 2015 produksi
3 1.2 Tujuan dan Manfaat
1.2.1 Tujuan
Untuk mengetahui apakah mutu bahan baku riboflavin yang akan
digunakan menjadi bahan berkhasiat dalam formulasi pembuatan sediaan tablet
Vitamin B Kompleks memenuhi syarat atau tidak seperti yang tertera pada
Farmakope Indonesia edisi IV.
1.2.2 Manfaat
Untuk mengetahui mutu bahan baku riboflavin, serta menambah
pengetahuan dan keterampilan, khususnya tentang uji mutu bahan baku riboflavin
4 BAB II
TINJAUAN PUSTAKA 2.1 Pengertian Obat
Obat adalah unsur aktif secara fisiologi dipakai dalam diagnosis,
pencegahan, pengobatan, atau penyembuhan suatu penyakit pada manusia atau
hewan. Obat dapat berasal dari alam diperoleh dari sumber mineral,
tumbuh-tumbuhan atau hewan atau dapat dihasilkan dari sintesis kimia organik atau
biosintesis (Ansel, 1989).
Menurut undang-undang, yang dimaksud dengan obat adalah suatu bahan
atau campuran bahan yang dimaksudkan untuk digunakan dalam menentukan
diagnosis, mencegah, mengurangi, menghilangkan, menyembuhkan penyakit atau
gejala penyakit, luka atau kelainan badaniah atau rohaniah pada manusia atau
hewan, termasuk memperelok tubuh atau bagian tubuh manusia (Syamsuni,
2007).
Meskipun obat dapat menyembuhkan penyakit, tapi banyak kejadian yang
mengakibatkan seseorang menderita akibat keracunan obat. Oleh karena itu, dapat
dikatakan bahwa obat dapat bersifat sebagai obat dan dapat juga bersifat sebagai
racun. Obat itu akan bersifat sebagai obat apabila tepat digunakan dalam
pengobatan suatu penyakit dengan dosis dan waktu yang tepat. Jadi, apabila obat
salah digunakan dalam pengobatan atau dengan dosis yang berlebih maka akan
menimbulkan keracunan. Dan bila dosisnya kecil maka kita tidak akan
5 2.2 Bahan baku
Menurut Dirjen POM (2012), bahan aktif obat adalah tiap bahan yang
digunakan dalam pembuatan sediaan farmasi dan apabila digunakan dalam
pembuatan obat akan menjadi zat aktif obat tersebut. Bahan tersebut bertujuan
untuk menghasilkan khasiat farmakologi atau memberikan efek langsung lain
dalam diagnosis, penyembuhan, peredaan, pengobatan atau pencegahan penyakit,
atau untuk memengaruhi struktur dan fungsi tubuh.
Semua bahan baku yang digunakan harus memenuhi persyaratan resmi
farmakope atau persyaratan lain yang disetujui oleh regulator atau oleh industri
farmasi yang bersangkutan. Selain itu, bahan–bahan yang dibeli harus sesuai
dengan spesifikasi hasil uji praformulasi agar diperoleh mutu obat yang konsisten
dan memenuhi persyaratan keamanan, khasiat, stabilitas, dan ketersediaan hayati
(Siregar, 2010).
Formulasi pembuatan tablet vitamin B kompleks yang diproduksi oleh PT.
Kimia Farma Plant. Medan
6 2.3 Uji Mutu Bahan Baku
2.3.1 Pemerian
Pemerian memuat paparan mengenai sifat zat yang diuraikan secara umum
terutama meliputi wujud, rupa, warna, rasa, bau dan untuk beberapa hal
dilengkapi dengan sifat kimia atau sifat fisiknya, dimaksudkan untuk dijadikan
petunjuk dalam pembuatan, peracikan dan penggunaan, di samping juga berguna
untuk membantu pemeriksaan pendahuluan dalam pengujian. Karena itu,
pernyataan yang terdapat di dalamnya tidak cukup kuat dijadikan syarat baku
(Ditjen POM, 1984).
2.3.2 Kelarutan
Untuk menyatakan kelarutan zat kimia, istilah kelarutan dalam pengertian
umum kadang-kadang perlu digunakan, tanpa mengindahkan perubahan kimia
yang mungkin terjadi pada pelarutan tersebut. Pernyataan kelarutan zat dalam
bagian tertentu pelarut adalah kelarutan pada suhu 20º dan kecuali dinyatakan lain
menunjukkan bahwa, 1 bagian bobot zat padat atau 1 bagian volume zat cair larut
dalam bagian volume tertentu pelarut. Pernyataan kelarutan yang tidak disertai
angka adalah kelarutan pada suhu kamar. Kecuali dinyatakan lain, zat jika
dilarutkan boleh menunjukkan sedikit kotoran mekanik seperti bagian kertas
saring, serat dan butiran debu. Pernyataan bagian dalam kelarutan berarti bahwa
1g zat padat atau 1 ml zat cair dalam sejumlah ml pelarut. Jika kelarutan suatu zat
tidak diketahui dengan pasti, kelarutannya dapat ditunjukkan dengan kelarutan
yang tertera pada kelarutan dalam etanol merupakan syarat baku obat yang
7 2.3.3 Susut Pengeringan
Susut pengeringan adalah banyaknya bagian zat yang mudah menguap,
termasuk air, ditetapkan dengan cara pengeringan, kecuali dinyatakan lain,
dilakukan pada suhu 105º hingga bobot tetap (Ditjen POM, 1984).
Prosedur ini digunakan untuk penetapan jumlah semua jenis bahan yang
mudah menguap dan hilang pada kondisi tertentu. Untuk zat yang diperkirakan
mengandung air sebagai satu-satunya bahan mudah menguap, cara yang terdapat
pada penetapan kadar air sudah memadai dan dicantumkan dalam masing-masing
monografi (Ditjen POM, 1995).
2.3.4 Suhu Lebur
Suhu lebur zat adalah suhu pada saat zat tepat melebur seluruhnya yang
ditunjukkan pada saat fase padat tepat hilang (Ditjen POM, 1984).
Dalam farmakope, jarak lebur atau suhu lebur zat padat didefinisikan
sebagai rentang suhu atau suhu pada saat zat padat menyatu dan melebur
sempurna (Ditjen POM, 1995).
2.3.5 Penetapan Kadar Secara Spektrofotometer UV-Vis
Spektrofotometri serap adalah pengukuran serapan radiasi elektromagnet
panjang gelombang tertentu yang sempit, mendekati monokromatik, yang diserap
zat. Pengukuran serapan dapat dilakukan pada daerah ultraviolet (panjang
gelombang 190 nm – 380 nm) atau pada daerah cahaya tampak (panjang
gelombang 380 nm – 780 nm) (Ditjen POM, 1984).
Identifikasi zat secara spektrofotometri pada daerah ultraviolet pada
8
pelarut, dan dengan kadar seperti yang tertera pada monografi, untuk menetapkan
letak serapan maksimum atau minimum (Ditjen POM, 1984).
Penetapan secara kuantitatif dilakukan dengan mengukur serapan larutan
zat dalam pelarut serta pada panjang gelombang tertentu. Pengukuran serapan
biasanya dilakukan pada panjang gelombang serapan maksimum dan yang
umumnya telah dicantumkan pada monografi (Ditjen POM, 1984).
2.4 Vitamin
Vitamin adalah zat-zat organik kompleks yang dibutuhkan dalam jumlah
sangat kecil dan pada umumnya tidak dapat dibentuk oleh tubuh. Oleh karena itu,
harus didatangkan dari makanan. Vitamin termasuk kelompok zat pengatur
pertumbuhan dan pemeliharaan kehidupan. Tiap vitamin mempunyai tugas
spesifik di dalam tubuh. Karena vitamin adalah zat organik maka vitamin dapat
rusak karena penyimpanan dan pengolahan (Almatsier, 2009).
Vitamin dikenal sebagai mikronutrien karena vitamin dibutuhkan pada
makanan manusia hanya dalam jumlah miligram atau mirogram per hari. Vitamin
masuk ke dalam tubuh bersama makanan. Kebutuhan tubuh akan berbagai vitamin
tidak sama setiap hari sebab masing-masing vitamin mempunyai fungsi yang
berbeda. Jumlah kebutuhan vitamin per hari ada yang dapat ditentukan dengan
pasti dan ada yang tidak (Sumardjo, 2009).
Kebutuhan tubuh akan vitamin ada batasnya. Kelebihan suatu vitamin
tidak selalu dibuang, tetapi ada juga yang disimpan. Contohnya vitamin A,
disimpan dalam jumlah besar di hati, sedangkan penyimpanan vitamin K dalam
9
diperlukan tambahan setiap hari dan hal ini diperoleh dari makanan (Sumardjo,
2009).
Vitamin dibagi menjadi dua golongan yaitu (1) vitamin larut lemak:
vitamin A, D, E, dan K; dan (2) vitamin larut air: vitamin B kompleks dan vitamin
C. Vitamin larut air disimpan dalam tubuh hanya dalam jumlah terbatas dan
sisanya dibuang, sehingga untuk mempertahankan saturasi jaringan vitamin larut
air perlu sering dikonsumsi. Meskipun demikian, pemberian vitamin larut air
dalam jumlah berlebihan selain merupakan pemborosan, juga mungkin
menimbulkan efek yang tidak diinginkan. Sebaliknya vitamin larut lemak dapat
disimpan dalam jumlah banyak, sehingga untuk timbulnya gejala defisiensi
dibutuhkan waktu lebih lama dan kemungkinan terjadinya toksisitas jauh lebih
besar dari pada vitamin larut air (Setiabudy, 2007).
2.4.1 Fungsi Vitamin
Vitamin berperan dalam beberapa tahap reaksi metabolisme energi,
pertumbuhan, dan pemeliharaan tubuh, pada umumnya sebagai koenzim atau
sebagai bagian dari enzim. Sebagian besar koenzim terdapat dalam bentuk
apoenzim, yaitu vitamin yang terikat dengan protein (Almatsier, 2009).
2.4.2 Vitamin Larut Lemak
Vitamin larut lemak (vitamin A, D, E, dan K) diabsorpsi dengan cara yang
kompleks dan sejalan dengan absorpsi lemak. Vitamin-vitamin ini disimpan
terutama di hati dan diekskresi melalui feses. Karena metabolismenya sangat
10
Vitamin larut dalam lemak, pada umumnya stabil terhadap pemasakan,
namun kandungannya dalam bahan makanan akan berkurang bila bahan makanan
tersebut menjadi tengik, kering, atau layu. Penyerapan vitamin golongan ini dalam
usus membutuhkan lemak dalam makanan dan aktivitas asam-asam empedu.
Kelebihan vitamin akan disimpan dalam tubuh, terutama di hati (Sumardjo, 2009).
2.4.3 Vitamin Larut Air
Vitamin larut air terdiri dari vitamin B kompleks dan vitamin C. Vitamin
B kompleks mencakup sejumlah vitamin dengan rumus kimia dan efek biologik
yang sangat berbeda yang digolongkan bersama karena dapat diperoleh dari
sumber yang sama, antara lain hati dan ragi. Yang termasuk dalam golongan
vitamin ini adalah: tiamin (vitamin B1), riboflavin (vitamin B2), asam nikotinat
(niasin), piridoksin (vitamin B6), asam pantotenat, biotin, kolin, inositol, asam
para-amino benzoat, asam folat dan sianokobalamin (vitamin B12) (Setiabudy,
2007).
Sebagian besar vitamin larut air merupakan komponen sistem enzim yang
banyak terlibat dalam membantu metabolisme energi. Vitamin larut air biasanya
tidak disimpan di dalam tubuh dan dikeluarkan melalui urin dalam jumlah kecil.
Oleh sebab itu vitamin larut air perlu dikonsumsi tiap hari untuk mencegah
kekurangan yang dapat mengganggu fungsi tubuh normal (Almatsier, 2009).
2.5 Vitamin B2 (Riboflavin)
Vitamin B2 (riboflavin) sangat penting dalam berbagai proses yang terjadi
11
Sumber makanan yang banyak mengandung vitamin B2 adalah produk-produk
olahan susu, daging, ikan dan unggas (Kristanti, 2010).
Riboflavin terutama berfungsi sebagai komponen koenzim Flavin Adenin
Dinukleotida (FAD) dan Flavin Adenin Mononukleotida (FMN). Kedua enzim
flavoprotein terlibat dalam reaksi oksidasi-reduksi berbagai jalur metabolisme
energi dan mempengaruhi respirasi sel (Almatsier, 2009).
Riboflavin yang berwarna kuning jingga sangat sukar larut dalam air,
dalam pelarut organik praktis tidak larut. Sebaliknya senyawa ini larut baik dalam
asam klorida pekat ataupun dalam larutan alkali hidroksida encer dengan
pembentukan garam secara mudah. Larutan dalam basa terurai dengan cepat.
Penentuan kadar dilakukan dengan penentuan ekstinksi larutan riboflavin pada
444 nm. Kadarnya selanjutnya dihitung dengan bantuan ekstinksi jenis (Schunack,
dkk., 1990).
Riboflavin dalam bentuk murni diperoleh dari isolasi ragi, hati, putih telur,
dan susu. Vitamin ini dinamakan riboflavin karena terjadi dari persenyawaan
ribosa (suatu gula lima karbon) dengan suatu zat berwarna kuning oranye yang
memberikan fluoresensi kuning kehijauan pada larutan. Sifat riboflavin larut
dalam air dan tahan panas di dalam larutan netral atau asam, namun dapat rusak
bila dipanaskan dalam larutan basa atau bila kena sinar matahari (Kusharto, 1992).
Penyebab kekurangan vitamin B2 jarang terjadi, kecuali di daerah-daerah
dimana makanan terutama berupa padi giling. Kekurangan vitamin ini juga bisa
terjadi pada:
12 • Penderita penyakit hati
• Penderita diare menahun
Gejala yang paling sering terjadi adalah luka terbuka di sudut mulut, yang
diikuti dengan bibir pecah-pecah, yang bisa meninggalkan jaringan parut. Jika
didaerah mulut terjadi thrush (suatu infeksi jamur), akan tampak bercak-bercak
putih keabuan. Warna lidah berubah menjadi magenta dan pada daerah diantara
hidung dan bibir muncul bercak-bercak berminyak (seboroik). Kadang tumbuh
pembuluh darah ke dalam kornea, menyebabkan mata silau. Pada laki-laki kulit
buah zakar mengalami peradangan (Kristanti, 2010).
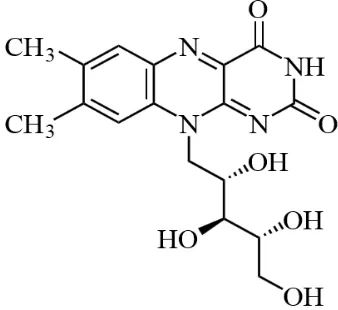
Menurut Dirjen POM (1995), sifat fisika dan kimia riboflavin adalah
sebagai berikut:
Gambar 2.1. Struktur Riboflavin Rumus molekul : C17H2ON4O6
Berat molekul : 376,37
Pemerian : Serbuk hablur, kuning hingga kuning jingga; bau lemah.
Melebur pada suhu lebih kurang 280º. Larutan jernihnya
netral terhadap lakmus. Jika kering tidak begitu
13
cahaya sangat cepat menyebabkan peruraian, terutama jika
ada alkali.
Kelarutan : Sangat sukar larut dalam air, dalam etanol dan dalam
larutan natrium klorida 0,9%; sangat mudah larut dalam
larutan alkali encer; tidak larut dalam eter dan dalam
kloroform.
Baku pembanding : Riboflavin BPFI; lakukan pengeringan pada suhu 105º
sebelum digunakan.
Identifikasi : Larutan 1 mg dalam 100 ml air dilihat dengan cahaya
yang ditransmisikan larutan berwarna kuning pucat
kehijauan, berfluoresensi hijau kekuningan intensif, yang
dengan penambahan asam mineral atau alkali, fluoresensi
hilang.
Susut pengeringan : Tidak lebih dari 1,5%, lakukam pengeringan pada suhu
105º selama 2 jam, menggunakan 500 mg.
Syarat kadar : Riboflavin mengandung tidak kurang dari 98,0% dan
tidak lebih dari 102,0% C17H2ON4O6, dihitung terhadap zat
yang telah dikeringkan.
Perhitungan penetapan kadar dapat dilakukan dengan menggunakan rumus
sebagai berikut :
C
�
��14 Keterangan :
C : Kadar Riboflavin BPFI dalam µg per ml
Iu : Serapan Larutan Uji
Is : Serapan Larutan Baku
2.5.1 Indikasi
Penggunaanya yang utama adalah untuk pencegahan dan terapi defisiensi
vitamin B2 yang sering menyertai pelagra atau defisiensi vitamin B kompleks
lainnya, sehingga riboflavin sering diberikan bersama vitamin lain. Dosis untuk
pengobatan adalah 5-10 mg/hari (Setiabudy, 2007).
Kebutuhan riboflavin per hari untuk bayi sekitar 0,6 mg; anak-anak dan
orang dewasa sekitar 0,9-2,5 mg, sedangkan untuk ibu-ibu selama hamil dan
menyusui sekitar 3 mg. Defisiensi riboflavin dapat menyebabkan luka-luka khas
pada bibir (cheilocis), radang pada lidah (glossitis), dan radang pada selaput mata
(conjunctivis) (Sumardjo, 2009).
2.5.2 Farmakologi
Defisiensi riboflavin ditandai dengan gejala sakit tenggorok dan radang di
sudut mulut (stomatitis angularis), keilosis, glositis, lidah berwarna merah dan
licin. Timbul dermatitis seboroik di muka, anggota gerak dan seluruh badan.
Gejala-gejala pada mata adalah fotofobia, lakrimasi, gatal dan panas (Setiabudy,
15
2.6 Metode Analisis Vitamin B2 (Riboflavin) 2.6.1 Metode Spektrofotometri
Larutan riboflavin dalam dapar pH 4,0 menunjukkan absorbansi
maksimum (λ maks) pada 444 nm dengan �1�� 1%
320. Cara ini digunakan untuk
menetapkan kemurnian riboflavin atau untuk penetapan riboflavin dengan kadar
lebih besar dari 90%. Penetapan riboflavin dilakukan dengan cara terlindung dari
cahaya (Rohman, 2008).
Cara penetapan riboflavin tunggal secara spektrofotometri: lebih kurang
100 mg riboflavin yang ditimbang saksama dilarutkan dengan pemanasan dalam
campuran 2 mL asam asetat glasial dan 150 mL air. Larutan selanjutnya
diencerkan dengan air, didinginkan, ditambah air secukupnya hingga 1000 mL.
Pada 10,0 mL larutan ditambah 3,5 mL natrium asetat 0,1 M kemudian ditambah
air secukupnya hingga 100 mL. Larutan akhir diukur absorbansinya dengan kuvet
1 cm pada panjang gelombang 444 nm. Kadar riboflavin dihitung dengan
menggunakan riboflavin baku sebagai pembanding (Rohman, 2008).
2.7 Spektrofotometer
2.7.1 Spektrofotometer UV-Vis
Spektrofotometer sesuai dengan namanya adalah alat yang terdiri dari
spektrometer dan fotometer. Spektrofotometer menghasilkan sinar dari spektrum
dengan panjang gelombang tertentu dan fotometer adalah alat pengukur intensitas
cahaya yang ditransmisikan atau yang diabsorpsi. Jadi, spektrofotometer
16
ditransmisikan, direfleksikan, atau diemisikan sebagai fungsi panjang gelombang
(Khopkar, 2008).
Spektrofotometer yang sesuai untuk pengukuran di daerah spektrum
ultraviolet dan sinar tampak terdiri atas suatu sistem optik dengan kemampuan
menghasilkan sinar monokromatis dalam jangkauan panjang gelombang 200-800
nm (Rohman, 2007).
Spektrofotometer UV-Vis adalah pengukuran panjang gelombang dan
intensitas sinar ultraviolet dan cahaya tampak yang diabsorpsi oleh sampel. Sinar
ultraviolet dan cahaya tampak memiliki energi yang cukup untuk mempromosikan
elektron pada kulit terluar ke tingkat energi yang lebih tinggi. Spektroskopi
UV-Vis biasanya digunakan untuk molekul dan ion anorganik atau kompleks di dalam
larutan. Spektrum UV-Vis mempunyai bentuk yang lebar dan hanya sedikit
informasi tentang struktur yang bisa didapatkan dari spektrum ini. Tetapi
spektrum ini sangat berguna untuk pengukuran secara kuantitatif. Konsentrasi dari
analit di dalam larutan bisa ditentukan dengan mengukur absorban pada panjang
gelombang tertentu dengan menggunakan hukum Lambert-Beer. Sinar ultraviolet
berada pada panjang gelombang 200-400 nm sedangkan sinar tampak berada pada
panjang gelombang 400-800 nm (Dachriyanus, 2004).
2.7.2 Instrumentasi Spektrofotometer UV-Vis
Instrumen yang digunakan untuk mempelajari serapan atau emisi radiasi
elektromagnetik sebagai fungsi dari panjang gelombang disebut ”spektrometer”
atau spektrofotometer. Komponen-komponen pokok dari spektrofotometer
lensa-17
lensa, cermin, celah-celah, dan lain-lain, (3) monokromator untuk mengubah
radiasi menjadi komponen-komponen panjang gelombang tunggal, (4) tempat
cuplikan yang transparan, dan (5) detektor radiasi yang dihubungkan dengan
sistem meter atau pencatat (Sastrohamidjojo, 1991).
Komponen-komponen pokok dari spektrofotometer meliputi:
a. Sumber tenaga radiasi
Sumber radiasi ultraviolet. Sumber-sumber radiasi ultraviolet yang
kebanyakan digunakan adalah lampu hidrogen dan lampu deuterium. Mereka
terdiri dari sepasang elektroda yang terselubung dalam tabung gelas dan diisi
dengan gas hidrogen atau deuterium pada tekanan yang rendah. Bila tegangan
yang tinggi dikenakan pada elektroda-elektroda, maka akan dihasilkan
elektron-elektron yang mengeksitasikan elektron-elektron-elektron-elektron lain dalam molekul gas ke
tingkatan tenaga yang tinggi. Bila elektron-elektron kembali ke tingkat dasar
mereka melepaskan radiasi yang kontinyu dalam daerah sekitar 180 dan 350 nm.
Sumber radiasi ultraviolet yang lain adalah lampu xenon, tetapi ia tidak se stabil
lampu hidrogen (Sastrohamidjojo, 1991).
b. Monokromator
Seperti kita ketahui bahwa sumber radiasi yang umum digunakan
menghasilkan radiasi kontinu dalam kisaran panjang gelombang yang lebar.
Dalam spektrometer, radiasi yang polikromatik ini harus diubah menjadi radiasi
monokromatik. Ada dua jenis alat yang digunakan untuk mengurai radiasi
polikromatik menjadi monokromatik yaitu penyaring dan monokromator.
18
panjang gelombang tertentu dan menyerap radiasi dari panjang gelombang yang
lain. Monokromator merupakan serangkaian alat optik yang menguraikan radiasi
polikromatik menjadi jalur-jalur yang efektif/panjang gelombang-gelombang
tunggalnya dan memisahkan panjang gelombang-gelombang tersebut menjadi
jalur-jalur yang sangat sempit (Sastrohamidjojo, 1991).
c. Tempat cuplikan
Cuplikan yang akan dipelajari pada daerah ultraviolet atau terlihat yang
biasanya berupa gas atau larutan ditempatkan dalam sel atau cuvet. Untuk daerah
ultraviolet biasanya digunakan Quartz atau sel dari silika yang dilebur, sedangkan
untuk daerah terlihat digunakan gelas biasa atau quartz (Sastrohamidjojo, 1991).
d. Detektor
Setiap detektor menyerap tenaga foton yang mengenainya dan mengubah
tenaga tersebut untuk dapat diukur secara kuantitatif seperti sebagai arus listrik
atau perubahan-perubahan panas. Kebanyakan detektor menghasilkan sinyal
listrik yang dapat mengaktifkan meter atau pencatat. Setiap pencatat harus
menghasilkan sinyal yang secara kuantitatif berkaitan dengan tenaga cahaya yang
mengenainya. Persyaratan-persyaratan penting detektor meliputi: (1) sensitivitas
tinggi hingga dapat mendeteksi tenaga cahaya yang mempunyai tingkatan rendah
sekalipun, (2) waktu respon yang pendek, (3) stabilitas yang panjang/lama untuk
menjamin respon secara kuantitatif, dan (4) sinyal elektronik yang mudah
19 BAB III METODOLOGI 3.1 Tempat
Uji mutu bahan baku riboflavin ini dilakukan di Laboratorium yang
terdapat di PT. Kimia Farma (Persero) Tbk. Plant Medan yang beralamat di Jl.
Sisingamangaraja Km.9 No. 59 Medan.
3.2 Alat-alat
Alat-alat yang digunakan adalah Moisture Analyzer merk Mettler Toledo
type HB43–S Halogen, Melting Point Merk Buchi type B-545, Spektrofotometer
UV-Vis merk Agilent type 8453 E, Ultrasonic Digital, Digital balance merk
Satorius type ep 224 5, kertas perkarmen, spatuladan alat-alat gelas (beaker gelas,
corong, gelas ukur, labu tentukur dan pipet volume).
3.3 Bahan-bahan
Bahan-bahan yang digunakan adalah Riboflavin Baku Pembanding
Farmakope Indonesia (BPFI), dan Sampel yang diuji bahan baku riboflavin
dengan No. Batch RIB1497FP, Asam Asetat Glasial (p), dan Aquadem.
3.4 Prosedur Pemeriksaan 3.4.1 Pemerian
Dapat di amati secara visual.
3.4.2 Kelarutan
Diambil sampel lalu dilarutkan dalam 30 ml aquadem dan diambil lagi
20 3.4.3 Susut Pengeringan
a. Ditimbang dengan teliti 500 mg sampel, lakukan pengeringan pada suhu
105º C selama 2 jam.
b. Tekan tombol “Power” untuk menghidupkan printer. Hubungkan steaker
alat dengan stop kontak, tekan tombol “On/Off” hingga muncul tampilan
dasar pada display.
c. Tekan tombol “Menu” kemudian pilih metode, ”Method A” atau ”Method
B”. kemudian tekan “Sel” lalu dipilih data produk yang akan diuji.
d. Untuk mengubah parameter data produk, tekan “Edit”, lalu pilih “Name”
lalu “Edit” isi nama produk yang akan diuji. Gunakan “A” untuk huruf
kapital atau “abc” untuk huruf kecil.
e. Tekan “ → “ untuk pengetikan karakter kedua dan gunakan ”^” atau ”v” untuk memilih huruf, bila telah selesai tekan “ ← ”.
f. Tekan “v” untuk memilih parameter selanjutnya “Target weight” isi
dengan bobot sampel yang akan diuji, gunakan ”_” atau “+” untuk
menambah atau mengurangi bobot kemudian tekan “ ← “.
g. Parameter selanjutnya “Drying program” tekan “Edit” kemudian pilih
“STD”.
h. Tekan “v” untuk memilih parameter selanjutnya “Temperature” isi dengan
syarat suhu pemanasan sesuai dengan sampel yang diuji. Gunakan “_” atau
“+” untuk menambah atau mengurangi suhu lalu tekan “ ← ”.
i. Tekan “v” untuk memilih parameter selanjutnya “Switch of mode” lalu
21
yang bisa digunakan untuk semua sampel, lalu tekan “ ← ” . Gunakan “v” untuk memilih tingkat pemanasan yang lain.
j. Setelah semua parameter diisi lalu tekan “Exit” 2x kemudian “Yes”.
k. Tekan tombol “A” atau “B” untuk menampilkan sampel yang akan diuji.
l. Kemudian buka penutupnya dan tutup kembali, bila alat digunakan
pertama kalinya. Namun bila alat sudah digunakan buka penutup sekali
saja.
m. Kemudian masukkan sampel sesuai dengan bobot maksimum dan
minimum pada display, lalu angkat pan piringan dan ratakan sampel.
n. Tutup kembali penutupnya, dan biarkan proses berjalan hingga hasil di
proleh.
3.4.4 Suhu Lebur
a. Hubungkan steaker alat dengan stop kontak.
b. Hidupkan alat dan printer dengan menekan switch power ke arah “On”.
c. Masukkan zat yang diperiksa pada tabung khusus dan masukkan tabung
tersebut pada lubang khusus yang terdapat pada bagian atas dari alat.
d. Tekan menu, atur set point, gradient, dan max point sesuai temperature
±10ºC, tekan enter.
e. Tekan menu, ketikkan nama zat yang diperiksa tekan enter.
f. Tekan menu, pada layar display muncul recall, store, clear dan print.
g. Tekan next 3 kali, kemudian tekan tombol start.
h. Tunggu beberapa menit sampai selesai pemeriksaan dan hasil pemeriksaan
22
i. Tekan stop dan biarkan beberapa menit sampai alat dingin.
3.4.5 Pembuatan Larutan Baku
a. Ditimbang seksama sejumlah Riboflavin BPFI sebanyak 10 mg.
b. Dimasukkan ke dalam labu tentukur 250 ml.
c. Ditambahkan 2 ml Asam Asetat Glasial (p).
d. Ditambahkan 20 ml Aquadem.
e. Dilarutkan dengan menggunakan alat Ultrasonic digital selama 15 menit.
f. Dicukupkan aquadem sampai garis tanda.
g. Dihomogenkan (larutan A).
3.4.6 Pembuatan Larutan Uji
a. Ditimbang seksama 10 mg zat uji.
b. Dimasukkan kedalam labu tentukur 250 ml.
c. Ditambahkan 2 ml Asam Asetat Glasial (p).
d. Ditambahkan 20 ml Aquadem.
e. Dilarutkan dengan menggunakan alat Ultrasonic digital selama 15 menit.
f. Dicukupkan aquadem sampai garis tanda.
g. Dihomogenkan (larutan B).
3.4.7 Penetapan Kadar Secara Spektrofotometer UV-Vis
Tahapan kerja penetapan kadar yang dilakukan adalah sebagai berikut:
a. Hidupkan seperangkat alat spektofotometer ultra violet (UV).
b. Klik program spektofotometer ultra violet (UV) yang terdapat di
23
c. Klik menu Quantification, masukkan panjang gelombang maksimum (444
nm) serta jarak batas atas dan batas bawah panjang gelombang (400 nm
dan 500 nm).
d. Tunggu selama 1 jam sampai mesin stabil.
e. Masukkan aquadem (blanko) ke dalam kuvet.
f. Letakkan kuvet di tempat pengukuran.
g. Klik blank, lalu spektrum keluar.
h. Masukkan larutan A (Larutan baku pembanding/BPFI) ke dalam kuvet.
i. Letakkan kuvet di tempat pengukuran.
j. Klik standard, lalu Procosed spectrum standard and calibration curve
keluar serta enam buah absorbansi keluar di dalam tabel. Dalam
perhitungan kadar yang digunakan adalah nilai rata-rata dari keenam
absorbansi.
k. Masukkan larutan B (Larutan uji) ke dalam kuvet.
l. Letakkan kuvet di tempat pengukuran.
m. Klik sampel, lalu Overhaid sampel spectra keluar. Serta 2 buah absorbansi
keluar di dalam tabel, dalam perhitungan kadar yang digunakan adalah
nilai rata-rata dari kedua absorbansi untuk masing-masing larutan B.
n. Catat absorban sampel yang diuji.
3.4.8 Perhitungan
Perhitungan penetapan kadar bahan baku riboflavin dapat dilakukan
24 � =�������
������� �������
Keterangan :
C : Kadar Riboflavinum (%)
Abs Uji : Absorban Larutan Uji
Abs Std : Absorban Larutan Baku
25 BAB IV
HASIL DAN PEMBAHASAN 4.1 Hasil
Berdasarkan uji mutu bahan baku riboflavin yang dilakukan, diperoleh
sebagai berikut:
Tabel 4.1. Data Hasil Pemeriksaan Bahan Baku
Pemeriksaan Persyaratan Hasil
Pemerian Serbuk hablur kuning
atau orange kuning
Serbuk hablur kuning
atau orange kuning
Kelarutan Sangat sukar larut dalam
air praktis tidak larut
dalam etanol 96%
Sangat sukar larut dalam
air praktis tidak larut
26 4.2 Pembahasan
Dari hasil uji mutu bahan baku riboflavin yang dilakukan bahwa pengujian
pemerian memenuhi syarat Farmakope Indonesia Edisi IV, yaitu serbuk hablur
kuning atau orange kuning. Kelarutannya sangat sukar larut dalam air, praktis
tidak larut dalam etanol 96%, memenuhi persyaratan. Susut pengeringan yang
dilakukan diperoleh 1,36%, 1,50%, 1,45%, dan 1,35% dengan persyaratan maks
1,5%, memenuhi persyaratan. Suhu lebur yang dilakukan diperoleh 286,3ºC
dengan persyaratan ± 280ºC, memenuhi persyaratan. Pada penetapan kadar
menggunakan spektrofotometri UV, diperoleh kadar sebesar 100,07% dengan
persyaratan 98,00-102,00%, kadar ini memenuhi persyaratan yang telah
ditetapkan. Dari data diatas dinyatakan bahwa bahan baku riboflavin yang
diproduksi oleh PT. Kimia Farma (Persero) Tbk. Plant Medan memenuhi
27 BAB V
KESIMPULAN DAN SARAN 5.1. Kesimpulan
Dari hasil pemeriksaan uji mutu bahan baku riboflavin yang nantinya akan
digunakan menjadi bahan berkhasiat dalam formulasi pembuatan sediaan tablet
Vitamin B Kompleks oleh PT. Kimia Farma (Persero) Tbk. Plant Medan, telah
memenuhi persyaratan uji pemeriksaan, yaitu mulai dari pemerian, kelarutan,
susut pengeringan, suhu lebur, dan penetapan kadar telah sesuai dengan
persyaratan yang ditetapkan oleh Farmakope Indonesia edisi ke-IV dan monografi
lainnya yang berpedoman pada Cara Pembuatan Obat yang Baik (CPOB).
5.2 Saran
Pada saat sebelum melakukan pemeriksaan uji mutu bahan baku
riboflavin, sebaiknya harus memahami metode serta prosedur yang dilakukan
mulai dari pemerian, kelarutan, susut pengeringan, suhu lebur, dan penetapan
kadar sehingga uji mutu bahan baku riboflavin diketahui sebanyak mungkin
kadarnya dan mutu sediaan tablet Vitamin B Kompleks yang beredar
dimasyarakat terjamin kadarnya karena menggunakan bahan baku berkhasiat
riboflavin yang sebelum digunakan dalam formulasi telah memenuhi persyaratan
28
DAFTAR PUSTAKA
Almatsier, S. (2009). Prinsip Dasar Ilmu Gizi. Jakarta: PT. Gramedia Pustaka Utama. Hal. 151, 152, 153, 194.
Anief, M. (2007). Apa Yang Perlu Diketahui Tentang Obat. Cetakan Kelima. Yogyakarta: Gadjah Mada University Press. Hal. 3.
Ansel, H.C. (1989). Pengantar Bentuk Sediaan Farmasi. Cetakan Pertama. Jakarta: Penerbit Universitas Indonesia (UI-Press). Hal. 50.
Budiyanto, K.A. (2009). Dasar-dasar Ilmu Gizi. Malang: UMM Press. Hal. 76.
Dachriyanus. (2004). Analisis Struktur Senyawa Organik Secara Spektroskopi. Padang: Andalas University Press. Hal. 1.
Dirjen POM. (2012). Pedoman Cara Pembuatan Obat Yang Baik. Jakarta: Badan POM. Hal. 282.
Ditjen POM. (1984). Farmakope Indonesia. Edisi III. Jakarta: Departemen Kesehatan RI. Hal. XXX, XXXIII, 768, 772, 773.
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan RI. Hal. 741, 742, 1032, 1043.
Khopkar, S.M. (2008). Konsep Dasar Kimia Analitik. Jakarta: UI Press. Hal. 226.
Kristanti, H. (2010). Penyakit Akibat Kelebihan dan Kekurangan Vitamin Mineral dan Elektrolit. Yogyakarta: Citra Pustaka. Hal. 10, 11, 63, 64.
Kusharto, C.M., dan Suhardjo. (1992). Prinsip-prinsip Ilmu Gizi. Yogyakarta: Kanisius. Hal. 235, 236.
Lachman, L., Lieberman, H.A., dan Kanig, J.L. (1994). Teori dan Praktek Farmasi Industri II. Edisi III. Jakarta: Penerbit Universitas Indonesia (UI-Press). Hal. 1603.
Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar. Hal. 245, 246, 261, 262.
Rohman, A., dan Sudjadi. (2008). Analisis Kuantitatif Obat. Yogyakarta: Gadjah Mada University Press. Hal. 200, 203.
Sastrohamidjojo, H. (1991). Spektroskopi. Yogyakarta: Liberty Yogyakarta. Hal. 39, 40, 41, 42.
29
Setiabudy, R. (2007). Farmakologi dan Terapi. Edisi V. Jakarta: Penerbit FKUI. Hal. 772, 773, 774, 779.
Siregar, C.J.P. (2010). Teknologi Farmasi Sediaan Tablet. Dasar-Dasar Praktis. Jakarta: Penerbit Buku Kedokteran EGC. Hal 84 – 86, 90, 96.
Sumardjo, D. (2009). Pengantar Kimia. Jakarta: Penerbit Buku Kedokteran EGC. Hal. 351, 352, 368, 370.
Syamsuni, A.H. (2007). Ilmu Resep. Jakarta: Penerbit Buku Kedokteran EGC. Hal. 61.
30
Lampiran 1. Perhitungan Penetapan Kadar Bahan Baku Riboflavin
Kadar Riboflavin dihitung dengan rumus sebagai berikut :
� =�������
St BPFI : Kadar Standar Baku Pembanding Farmakope Indonesia
Data bahan baku ini adalah data pengujian pada tanggal 9 Februari 2015, dengan
keterangan pemasoknya PT. Global Chemindo Megatrading ; Nomor Batch
31 Kadar Sampel II : �1,24730
1,25978� X 100,97 % = 99,97%
Kadar Sampel III : �1,24850
1,25978� X 100,97 % = 100,07%
Kadar Sampel IV : �1,23500
35
Lampiran 5. Gambar Alat Digital Semi Micro Balance
Lampiran 6. Gambar Alat Melting Point Analyzer
36
Lampiran 7. Gambar Alat Moisture Analyzer