LAPORAN PRAKTEK KERJA PROFESI
FARMASI INDUSTRI
di
PT. KIMIA FARMA (Persero) Tbk.
Plant Medan
Disusun oleh:
Aynul Qolby Nasution, S.Farm
103202068
PROGRAM PENDIDIKAN PROFESI APOTEKER
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
Lembar Pengesahan
LAPORAN PRAKTEK KERJA PROFESI
FARMASI INDUSTRI
di
PT. KIMIA FARMA (Persero) Tbk.
Plant Medan
Laporan ini disusun untuk melengkapi salah satu syarat untuk
memperoleh gelar Apoteker pada Fakultas Farmasi Universitas
Sumatera Utara Medan
Disusun oleh:
Aynul Qolby Nasution, S.Farm
103202068
P.T. Kimia Farma (Persero) Tbk. Plant Medan
Medan
Pembimbing,
Asisten Manager Pengelolaan Mutu
Heru Khoerudin, S.Si., Apt.
Fakultas Farmasi
Universitas Sumatera Utara
Dekan,
KATA PENGANTAR
Puji syukur kehadirat Tuhan Yang Maha Esa yang telah melimpahkan
rahmat dan hidayah-Nya sehingga penulis dapat menyelesaikan Praktek Kerja
Profesi Apoteker (PKPA) di P.T. Kimia Farma (Persero) Tbk. Plant Medan.
Laporan ini ditulis berdasarkan materi yang disampaikan oleh pihak P.T. Kimia
Farma (Persero) Tbk. PlantMedan dan tinjauan langsung ke lapangan.
Selama melaksanakan Praktek Kerja Profesi Apoteker (PKPA) ini penulis
banyak mendapatkan bantuan dari berbagai pihak baik berupa arahan, bimbingan
dan masukan. Oleh karena itu penulis ingin mengucapkan terima kasih yang
sebesar-besarnya kepada:
1. Bapak Drs. Beben Budiman, Apt. selaku Plant Manager P.T. Kimia Farma
(Persero) Tbk. Plant Medan, yang telah memberikan kesempatan kepada
penulis untuk melaksanakan Praktek Kerja Profesi Apoteker (PKPA).
2. Bapak Heru Khoerudin, S.Si., Apt. selaku Asisten Manager Pengelolaan
Mutu P.T. Kimia Farma (Persero) Tbk. Plant Medan, yang telah
memberikan bimbingan dan pengarahan kepada kami selama melaksanakan
Praktek Kerja Profesi Apoteker (PKPA).
3. Bapak Drs. Zulfadli., Apt selaku Asisten Manager Produksi P.T. Kimia
Farma (Persero) Tbk. Plant Medan, yang telah memberikan bimbingan dan
pengarahan kepada kami selama melaksanakan Praktek Kerja Profesi
Apoteker (PKPA).
4. Bapak, Prof. Dr. Sumadio Hadisahputra., Apt selaku Dekan Fakultas
5. Bapak, Drs, Wiryanto, M.S., Apt selaku Koordinator Program Pendidikan
Profesi Apoteker Fakultas Farmasi USU Medan.
6. Seluruh staf dan karyawan P.T. Kimia Farma (Persero) Tbk. Plant Medan
atas bantuan dan kerjasama yang diberikan selama Praktek Kerja Profesi
Apoteker (PKPA) di PT P.T. Kimia Farma (Persero) Tbk. Plant Medan.
7. Orangtua dan seluruh keluarga serta teman-teman atas semangat, bantuan moril
dan materil yang tak ternilai.
Semoga Tuhan Yang Maha Esa membalas budi baik Bapak dan Ibu dengan
balasan yang berlipat ganda, dan penulis berharap semoga tulisan ini dapat
memberikan manfaat bagi kita semua.
DAFTAR ISI
LEMBAR JUDUL……… i
LEMBAR PENGESAHAN………. ii
KATA PENGANTAR………. iii
DAFTAR ISI……… v
DAFTAR GAMBAR………... ix
DAFTAR LAMPIRAN……… x
DAFTAR TABEL ………... xi
RINGKASAN………... xii
BAB I PENDAHULUAN ……….. 1
1.1 Latar Belakang ……….. 1
1.2. Tujuan ………. 2
1.3 Mamfaat ... 2
BAB II TINJAUAN UMUM ………...………… 3
2.1. Tinjauan PT. Kimia Farma ( Persero) Tbk …….……... 3
2.1.1 Sejarah Perusahaan ……… 3
2.1.2. Visi dan Misi Perusahaan ………. 5
2.1.2.1. Visi Perusahaan ………. 5
2.1.2.2 Misi Perusahaan ……… 5
2.1.3. Lokasi dan Sarana Produksi Plant Medan………... 6
2.1.4. Cara Pembuatan obat yang baik (CPOB) ... … 7
2.1.4.2. Personalia ………. 9
2.1.4.3. Bangunan ……….….. 11
2.1.4.4. Peralatan ………..….. 13
2.1.4.5. Sanitasi dan Higiene ………...….. 14
2.1.4.5.1. Personalia ………. ... 14
2.1.4.5.2. Bangunan ……… 15
2.1.4.5.3. Peralatan ………...…. 15
2.1.4.6. Produksi ……… 16
2.1.4.6.1. Bahan Awal ……… 16
2.1.4.6.2. Validasi Prosedur ………….. 17
2.1.4.6.3. Pencemaran ……….. 17
2.1.4.6.4. Sistem Penomoran Batch & Lot. 18 2.1.4.6.5. Penimbangan & Penyerahan …. 18 2.1.4.6.6. Pengolahan ……….. 18
2.1.4.6.7. Pengawasan Selama Proses … 19 2.1.4.6.8. Pengemasan ………. 19
2.1.4.6.9. Penyiapan Bahan Awal,Produk Antara, Produk Ruahan & Obat Jadi ………... 20
2.1.4.7. Pengawasan Mutu ………... 21
2.1.4.8. Inspeksi Diri ……….... 23
2.1.4.9. Penaganan Keluhan & Penarikan Kembali Obat Yang Beredar ………….... 24
2.1.4.11. Prosedur dan catatan penanganan
Keluhan ……….. 25
2.1.4.12. Prosedur dan Catatan Penanganan Obat Kembalian ………. 26
2.1.4.13. Prosedur dan Catatan Penarikan Kembalian Obat Jadi ………. 26
2.1.4.14. Prosedur dan Catatan Pemusnahan Bahan dan Produk yang Ditolak …….. 26
2.1.5. Kualifikasi dan Validasi ………... 27
2.1.5.1. Kualifikasi .... ………... 27
2.1.5.2. Validasi ... ………. 29
2.1.5.2.1. Validasi Prosedur Analitik ... 30
2.1.5.2.2. Validasi Berkala ... 30
2.1.5.2.3 Langkah-langkah Pelaksanaan Validasi ... 30
BAB III KEGIATAN DI INDUSTRI FARMASI ………. 32
3.1. Aspek Personalia ……… 32
3.2. Struktur Organisasi ……….. 32
3.3. Sediaan-sediaan obat yang diproduksi PT. Kimia Farma (Persero) Tbk Plant Medan ……….. 32
3.4. Kegiatan Industri PT. Kimia Farma (Persero) Tbk Plant Medan ……….. 33
3.4.1. Perencanaan Produksi Dan Pengendalian Inventori (PPPI) ………. 33
3.4.3. Pengawasan Mutu ………. 43
3.4.3.1. Pemeriksaan Mutu Bahan Baku dan Bahan Pengemas ……….. 44
3.4.3.2. Pengawasan Selama Proses (In Process Control/IPC) ………. 44
3.4.3.3. Pengawasan dalam Proses Pengemasan .. 45
3.4.4. Gudang ……… 45
3.4.5. Penerimaan Barang ……… 46
3.4.6. Pengeluaran Barang ……… 46
3.4.7. Pengelohan Limbah ……… 47
3.4.7.1. Pengolahan Limbah Cair ……… 47
3.4.7.2. Pengolahan Limbah Padat ……….. 49
3.4.8. Administrasi dan Keuangan ……….. 49
BAB IV PEMBAHASAN……… 51
4.1. Aspek Personalia ………. 51
4.2. Aspek Bangunan ………. 51
4.3. Aspek Produksi ………. 52
4.4. Aspek Pengawasan Mutu ………. 53
4.5. Aspek Pengolahan Limbah ……….. 54
BAB V KESIMPULAN DAN SARAN ……….. 55
5.1. Kesimpulan ……… 55
5.2. Saran ……….. 55
DAFTAR PUSTAKA ……….. 56
DAFTAR GAMBAR
Gambar 1. Pengolahan Limbah Cair PT.Kimia Farma (Persero)
DAFTAR LAMPIRAN
Lampiran 1. Bagan Proses Pembuatan Krim………... 57
Lampiran 2. Bagan Proses Pembuatan Tablet………...….. 58
DAFTAR TABEL
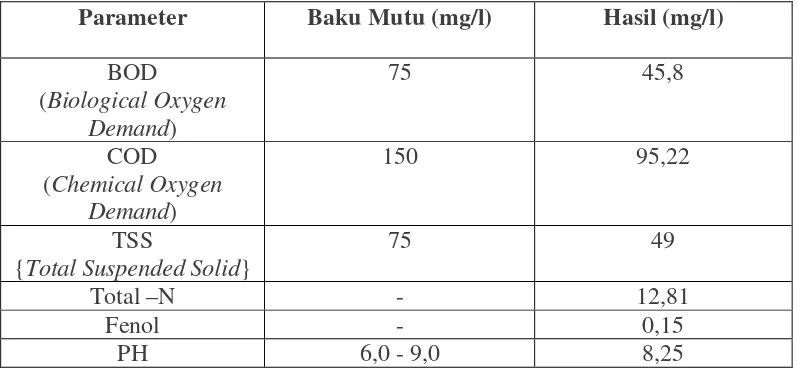
Tabel 1. Tabel Hasil Analisis Limbah Cair PT.Kimia Farma (Persero)
RINGKASAN
Telah dilakukan Praktek Kerja Profesi (PKP) di Industri Farmasi PT.
Kimia Farma (Persero) Tbk. Plant Medan yang merupakan salah satu program
dalam pendidikan profesi apoteker, yang bertujuan agar calon apoteker
mengetahui dan memahami tugas dan fungsi apoteker dalam industri farmasi,
yang diharapkan sebagai bekal untuk menghadapi dunia kerja yang sesungguhnya.
Mahasiswa juga diharuskan memperoleh wawasan dan pengetahuan yang lebih
luas, memahami penerapan CPOB di PT. Kimia Farma (Persero) Tbk. Plant
Medan, serta mengetahui gambaran tentang situasi dan kondisi kerja di PT. Kimia
Farma (Persero) Tbk. Plant Medan.
PKP di Industri Farmasi PT. Kimia Farma (Persero) Tbk. Plant Medan
dilaksanakan pada tanggal 05 April 2010 hingga 30 April 2010 dengan jumlah
jam efektif 160 jam. Kegiatan yang dilakukan selama PKP di Industri antara lain
membuat catatan kegiatan harian yang berisi absensi, pengamatan kegiatan
produksi, Laboratorium Quality Control (QC), Gudang Bahan Baku, Gudang
Bahan Kemasan, Gudang Obat Jadi, Sistem Pengolahan Air untuk Produksi,
RINGKASAN
Telah dilakukan Praktek Kerja Profesi (PKP) di Industri Farmasi PT.
Kimia Farma (Persero) Tbk. Plant Medan yang merupakan salah satu program
dalam pendidikan profesi apoteker, yang bertujuan agar calon apoteker
mengetahui dan memahami tugas dan fungsi apoteker dalam industri farmasi,
yang diharapkan sebagai bekal untuk menghadapi dunia kerja yang sesungguhnya.
Mahasiswa juga diharuskan memperoleh wawasan dan pengetahuan yang lebih
luas, memahami penerapan CPOB di PT. Kimia Farma (Persero) Tbk. Plant
Medan, serta mengetahui gambaran tentang situasi dan kondisi kerja di PT. Kimia
Farma (Persero) Tbk. Plant Medan.
PKP di Industri Farmasi PT. Kimia Farma (Persero) Tbk. Plant Medan
dilaksanakan pada tanggal 05 April 2010 hingga 30 April 2010 dengan jumlah
jam efektif 160 jam. Kegiatan yang dilakukan selama PKP di Industri antara lain
membuat catatan kegiatan harian yang berisi absensi, pengamatan kegiatan
produksi, Laboratorium Quality Control (QC), Gudang Bahan Baku, Gudang
Bahan Kemasan, Gudang Obat Jadi, Sistem Pengolahan Air untuk Produksi,
BAB I
PENDAHULUAN
1.1 Latar Belakang
Obat adalah suatu zat yang dimaksudkan untuk dipakai dalam diagnosis,
mengurangi rasa sakit, serta mengobati atau mencegah penyakit. Salah satu upaya
yang dilakukan pemerintah untuk menjamin tersedianya obat yang bermutu, aman
dan berkhasiat yaitu dengan mengharuskan setiap industri farmasi untuk
menerapkan Cara Pembuatan Obat yang Baik (CPOB).
Cara Pembuatan Obat yang baik (CPOB) adalah pedoman pembuatan obat
bagi industri farmasi di Indonesia yang bertujuan untuk menjamin mutu obat yang
dihasilkan senantiasa memenuhi persyaratan mutu yang telah ditentukan dan
sesuai dengan tujuan penggunaannya. Mutu suatu obat tidak dapat ditentukan
berdasarkan pemeriksaan produk akhir saja, melainkan harus dibentuk kedalam
produk selama keseluruhan proses pembuatan. CPOB mencakup seluruh aspek
produksi mulai dari personalia, dokumentasi, bangunan, peralatan, manajemen
mutu, produksi, sanitasi dan higiene, pengawasan mutu, penanganan keluhan,
penarikan obat dan obat kembalian, validasi dan kualifikasi serta analisis kontrak.
Personalia, yang salah satunya adalah Apoteker dalam industri farmasi
memegang peranan penting untuk menjamin mutu obat yang dihasilkan.
Kedudukan apoteker juga diatur dalam CPOB, yaitu sebagai penanggung jawab
produksi, pengawasan mutu dan pemastian mutu. Sehingga, dibutuhkan apoteker
yang memiliki wawasan, pengetahuan, keterampilan, dan kemampuan dalam
kenyataan di lapangan industri. Dengan demikian, apoteker harus mendapatkan
bekal pengetahuan dan pengalaman praktis yang cukup, yang salah satunya dapat
diperoleh melalui kegiatan Praktek Kerja Profesi di industri farmasi. Dalam
pelaksanaan Praktek Kerja Profesi di Industri, Fakultas Farmasi bekerja sama
dengan PT. Kimia Farma (Persero) Tbk. Plant Medan yang berlokasi di Jalan
Tanjung Morawa Km 9 Medan sebagai salah satu industri farmasi di Indonesia.
1.2Tujuan
Melalui Latihan Kerja Profesi di Industri Farmasi ini diharapkan calon
apoteker mengetahui tugas dan fungsi apoteker di industri farmasi, yakni bidang
pemastian mutu, pengawasan mutu dan bagian produksi serta penerapan CPOB
sehingga setelah Praktek Kerja Profesi ini para calon apoteker mampu mengelola
industri farmasi sesuai CPOB.
1.3 Manfaat
Praktek Kerja Profesi di industri farmasi ini diharapkan dapat memberikan
pengetahuan praktis kepada calon apoteker tentang pekerjaan kefarmasian di
BAB II
TINJAUAN UMUM INDUSTRI FARMASI
2.1. Tinjauan PT. Kimia Farma (Persero) Tbk.
2.1.1. Sejarah Perusahaan.
PT.Kimia Farma (Persero) Tbk sebagai Badan Usaha Milik Negara
(BUMN) dibentuk sebagai Perusahaan Perseroan pada tanggal 16 Agustus 1971.
Sejak berdirinya hingga sekarang ini PT. Kimia Farma (Persero) Tbk telah
mengalami beberapa perubahan, yaitu:
Periode I (1957-1959)
Periode ini adalah periode dimana pemerintah melaksanakan nasionalisasi
perusahaan farmasi milik bangsa Belanda yang ada di Indonesia. Program
nasionalisasi ini dikoordinasi oleh Badan Pengambil alihan Perusahaan Farmasi
(BAPPHAR). Adapun perusahaan farmasi milik Belanda tersebut yaitu :
1. NV. Rathkamp dan NV Bavosta di Jakarta
2. NV. Bandoengsche Kinine Febriek di Bandung
3. NV. Ordeneming Iodium Watadakon di Mojokerto
4. NV. Industri Tella di Surabaya
5. CV. Apotek Malang di Malang
6. Drogistry Van Belem dan NV. Sari Delle di Yogyakarta
Periode II (1960-1968)
Periode ini adalah periode pembentukan Perusahaan Negara Farmasi
(PNF) dan perusahaan-perusahaan farmasi milik Belanda yang telah
Perusahaan-perusahaan yang didirikan adalah :
1. PNF. Radja Farma (ex. Rathkamp) di Jakarta
2. PNF. Nurani Farma (ex. Van Gorkom) di Jakarta
3. PNF. Nakula Farma (ex. Bavosta) di Jakarta
4. PNF. Bhinneka Kina Farma di Bandung
5. PNF. Sari Husada (ex. Sari Delle) di Yogyakarta
6. PNF. Kasa Husada (ex. Varbanstaffen)
7. PNF. Biofarma (ex. Pasteur Institute) di Bandung
Periode III (1969-1970)
Untuk meningkatkan efisiensi setiap BUMN, dikeluarkan Intruksi
Presiden No. 17/1967 sehingga Departemen Kesehatan melebur
perusahaan-perusahaan milik Negara tersebut kedalam perusahaan-perusahaan Negara Farmasi dan
alat-alat Kesehatan Bhinneka Kimia Farma dan PNF Kasa Husada di Surabaya dirubah
menjadi Perusahaan Umum dan Perusahaan Daerah, kemudian PN Sari Husada di
Yogyakarta berdiri sendiri sebagai anak perusahaan.
Periode IV (1971-2001)
Periode IV dimulai tahun 1971 ditandai dengan dikeluarkannya PP No.116
tahun 1971 yang berlaku sejak tanggal 19 maret 1971. Perusahaan Negara
Farmasi dan Alat-alat Kesehatan Bhinneka Kimia Farma setelah melalui proses
audit dinyatakan lulus untuk menjadi Perseroan Terbatas (PT) yang selanjutnya
disahkan pada tanggal 16 Agustus 1971 sebagai PT. Kimia Farma (Persero)
Periode V (2001-sekarang)
Pada periode ini tepatnya tanggal 28 juni 2001 PT. Kimia Farma (Persero)
menjadi Perusahaan Terbuka (Tbk) dengan nama PT. Kimia Farma (Persero) Tbk
dimana untuk privatisasi tahap I saham yang lepas adalah sebanyak 9% dengan
rincian 3% untuk program Kepemilikan Saham Karyawan dan Manajemen
(KSKM) PT. Kimia Farma, dan sebanyak 6% untuk masyarakat umum.
Pada tanggal 4 januari 2003 PT. Kimia Farma membentuk 2 anak
perusahaan yaitu :
1. PT. Kimia Farma Health & Care
2. PT. Kimia Farma Trading & Distribution
Sedangkan pabrik sebagai Holding Company
2.1.2. Visi dan Misi Perusahaan
2.1.2.1. Visi Perusahaan
Komitmen pada peningkatan kualitas kehidupan, kesehatan dan
lingkungan.
2.1.2.2. Misi Perusahaan
PT. Kimia Farma (Persero) Tbk mempunyai misi :
1. Mengembangkan industri kimia dan farmasi dengan melakukan penelitian
dan pengembangan produk yang inovatif.
2. Mengembangkan bisnis pelayanan kesehatan terpadu yang berbasis
jaringan distribusi dan jaringan apotek.
3. Meningkatkan sumber daya manusia dan mengembangkan sistem
Misi ini diwujudkan melalui strategi corporate:
1. Meningkatkan sinergis antar unit usaha dengan menggunakan salah satu
unit usaha yang kuat untuk menarik unit usaha lain.
2. Meningkatkan efektifitas pemasaran dengan penyusunan program
pemasaran yang lebih fokus dan perluasan cakupan daerah pemasaran
yang ada.
3. Memperkuat struktur bisnis distribusi dengan melakukan intensifikasi dan
ekstensifikasi kegiatan distribusi.
4. Melakukan difersifikasi dan pengembangan produk baik yang berasal dari
pengembangan sendiri maupun kerja sama dengan pihak luar.
5. Melakukan pengembangan usaha yang terkait dengan pelayanan kesehatan
yang dilakukan sendiri, kerja sama dengan pihak luar ataupun melalui
akuisisi.
6. Mengembangkan sumber daya manusia untuk memperoleh sumber daya
manusia yang mempunyai komitmen-komitmen tinggi, melalui pelatihan
dan pendidikan yang terencana dan berkesinambungan.
7. Mengembangkan sistem dan prosedur operasi ditunjang dengan sistem
ilmu teknologi yang memadai untuk peningkatan efisiensi dan menuju
operasional excellence.
2.1.3. Lokasi dan Sarana Produksi Plant Medan
PT. Kimia Farma (Persero) Tbk. Plant Medan terletak di jalan Tanjung
Morawa km 9 dengan luas 20.269 m2
1. Ruang perkantoran
yang terdiri dari :
3. Ruang produksi tablet
4. Ruang produksi kapsul
5. Ruang produksi krim/salep
6. Ruang penimbangan sentral
7. Ruang sampling
8. Gudang bahan baku
9. Gudang bahan pengemas
10.Gudang etiket
11.Gudang obat jadi
12.Bangunan penunjang seperti tempat pencucian, dapur, mushola, dan
tempat olah raga.
Kontruksi bangunan PT. Kimia Farma (Persero) Tbk. Plant Medan telah
dibuat sesuai dengan persyaratan CPOB dimana dinding dan langit-langit
memiliki permukaan licin dan tidak terdapat sambungan. Lantai dan dinding di
dalam ruangan produksi dilapisi dengan epoksi, ruang produksi untuk
masing-masing bentuk sediaan terletak terpisah. Sistem pengaturan udara pada ruang
produksi menggunakan Air Handling Unit (AHU) dengan Air Conditioner (AC)
sentral.
2.1.4. Cara Pembuatan Obat Yang Baik (CPOB)
Cara Pembuatan Obat yang Baik (CPOB) bertujuan untuk menjamin obat
dibuat secara konsisten memenuhi persyaratan yang ditetapkan dan sesuai dengan
tujuan penggunaannya. CPOB mencakup seluruh aspek produksi dan
2.1.4.1. Manajemen Mutu (Pemastian Mutu)
Pemastian mutu merupakan suatu konsep luas yang mencakup semua hal
baik secara tersendiri maupun secara kolektif yang akan mempengaruhi mutu dari
obat yang dihasilkan. Pemastian mutu adalah totalitas semua pengaturan yang
dibuat dengan tujuan untuk memastikan bahwa obat dihasilkan dengan mutu yang
sesuai dengan tujuan pemakaiannya, karena itu pemastian mutu mencakup CPOB
ditambah dengan faktor lain diluar pedoman ini seperti desain dan pengembangan
produk. Sistem pemastian mutu yang benar dan tepat bagi industri farmasi
hendaklah memastikan bahwa:
• Desain dan pengembangan obat dilakukan dengan memperhatikan
persyaratan CPOB dan semua langkah produksi dan pengendalian
diuraikan secara jelas.
• Tanggung jawab manajerial diuraikan dengan jelas dalam uraian jabatan.
• Pengaturan disiapkan untuk pembuatan pasokan dan penggunaan bahan
awal dan pengemas yang benar.
• Semua pengawasan terhadap produk antara dan pengawasan selama
proses (in proses control) lain serta validasi yang diperlukan.
• Pengkajian terhadap semua dokumen yang terkait dengan proses
pengemasan dan pengujian bets dilakukan sebelum memberikan
pengesahan pelulusan untuk distribusi penilaian hendaklah meliputi
semua faktor yang relevan termasuk kondisi pembuatan, hasil dan
pengawasan selama proses, pengkajian dokumen produksi termasuk
ditetapkan, pemenuhan persyaratan dari spesifikasi produk jadi dan
pemeriksaan produk dalam kemasan akhir.
• Obat tidak dijual atau dipasok sebelum kepala bagian manajemen mutu
(pemastian mutu) menyatakan bahwa tiap bets produksi dibuat dan
dikendalikan sesuai dengan persyaratan yang tercantum dalam izin edar
dan peraturan lain yang berkaitan dengan aspek produksi, pengawasan
mutu dan pelulusan produk.
• Tersedia pengaturan yang memadai untuk memastikan bahwa sedapat
mungkin produk disimpan, didistribusikan dan selanjutnya ditangani
sedemikian rupa agar mutu tetap dijaga selama masa edar/ simpan obat.
• Tersedia prosedur inspeksi diri dan audit mutu yang secara berkala
mengevaluasi efektivitas dan penerapan sistem pemastian mutu.
• Pemasok bahan awal dan pengemas dievaluasi dan disetujui untuk
memenuhi spesifikasi mutu yang telah ditentukan oleh perusahaan.
• Penyimpangan dilaporkan, diselidiki dan dicatat.
• Tersedia sistem persetujuan terhadap perubahan yang berdampak pada
mutu produk.
• Prosedur pengolahan ulang dievaluasi dan disetujui.
• Evaluasi mutu produk berkala dilakukan untuk verifikasi konsistensi
proses dan memastikan perbaikan proses yang berkesinambungan.
2.1.4.2. Personalia
Struktur organisasi perusahaan hendaklah sedemikian rupa sehingga
bagian produksi dan pengawasan mutu dipimpin oleh apoteker yang berlainan dan
manajer pengawasan mutu membawahi beberapa supervisor yang terlatih dan
memiliki ketrampilan teknis serta pengalaman dalam bidang yang berkaitan
dengan bidangnya.
Manejer produksi dan pengawasan mutu haruslah seorang apoteker yang
cakap, terlatih, memiliki pengalaman praktis yang memadai untuk melaksanakan
tugasnya secara professional. Manajer produksi dan Manajer pengawasan mutu
memiliki wewenang dan tanggung jawab penuh dalam mutu obat yang dihasilkan.
Manajer produksi memiliki wewenang dan tanggung jawab penuh untuk
mengelola produksi obat. Manajer pengawasan mutu memiliki wewenang dan
tanggung jawab dalam seluruh tugas pengawasan mutu. Manajer produksi dan
pengawasan mutu bersama-sama bertanggung jawab dalam penyusunan dan
pengesahan prosedur-prosedur tertulis, pemantauan kebersihan lingkungan pabrik,
validasi proses produksi, pemberian persetujuan pada pemasok bahan,
pengamanan bahan dan produk terhadap kerusakan dan kemunduran mutu,
penyimpanan dokumen serta memastikan bahwa tugas dan tanggung jawab yang
diberikan kepada seluruh karyawan jelas dan dapat dipahami dengan baik.
Setiap karyawan yang langsung ikut serta dalam kegiatan pembuatan obat
dan yang karena tugasnya harus memasuki daerah pembuatan obat, hendaklah
diberikan pelatihan yang sesuai dengan tugasnya maupun pelatihan CPOB.
Pelatihan hendaknya dilaksanakan secara berkesinambungan dengan program
tertulis yang disetujui oleh manajer produksi dan manajer pengawasan mutu.
Pelatihan khusus diberikan kepada karyawan yang bekerja didaerah steril,
didaerah bersih, atau bagi mereka yang bekerja menggunakan bahan yang
diberikan oleh orang yang cakap. Dokumen pelatihan harus disimpan dengan baik
dan efektifitas program pelatihan hendaknya dinilai secara berkala.
2.1.4.3. Bangunan
Bangunan untuk pembuatan obat hendaklah memiliki ukuran, rancangan
kontruksi serta letak yang memadai agar memudahkan dalam melaksanakan kerja,
pembersihan dan pemeliharaan yang baik. Tiap sarana kerja hendaklah memadai,
sehingga setiap resiko terjadinya kekeliruan, pencemaran silang dan berbagai
kesalahan lain yang dapat menurunkan mutu obat, dapat dihindarkan.
Lokasi bangunan hendaklah sedemikian rupa untuk mencegah terjadinya
pencemaran dari lingkungan sekelilingnya, seperti pencemaran dari udara, tanah
dan air maupun dari kegiatan di dekatnya. Apabila bangunan itu terletak pada
tempat yang tidak sesuai, tindakan yang efektif hendaklah diambil untuk
mencegah pencemarannya.
Dalam menentukan rancang bangun dan penataan gedung hendaklah
dipertimbangkan hal-hal berikut :
1. Kesesuaian dengan kegiatan lain, yang mungkin dilakukan dalam sarana
yang sama atau dalam sarana yang berdampingan.
2. Luasnya ruang kerja, yang memungkinkan penempatan peralatan dan
bahan-bahan secara teratur dan logis serta memungkinkan terlaksananya
kegiatan, kelancaran arus kerja, komunikasi dan pengawasan yang efektif
maupun untuk mencegah kesesakan dan ketidakteraturan.
3. Pencegahan terjadinya penggunaan kawasan produksi sebagai lalu lintas
umum bagi karyawan atau bahan-bahan ataupun sebagai tempat
Rancang bangun dan penataan gedung hendaklah memenuhi
persyaratan-persyaratan berikut:
1. Mencegah resiko tercampur baurnya obat atau komponen obat yang
berbeda, kemungkinan terjadinya pencemaran silang oleh obat atau
bahan-bahan lain serta resiko terlewatnya salah satu langkah dalam proses
produksi.
2. Kegiatan pengolahan bahan bagi produk bukan obat dipisahkan dari ruang
produksi obat.
3. Disedikan ruang terpisah untuk membersihkan alat yang dapat
dipindah-pindahkan dan ruangan untuk menyimpan alat pembersih.
4. Kamar ganti-simpan pakaian berhubungan langsung dengan daerah
pengolahan tetapi letaknya terpisah.
5. Toilet tidak terbuka langsung kedaerah produksi dan dilengkapi dengan
ventilasi yang baik.
Untuk kegiatan-kegiatan berikut diperlukan daerah tertentu yaitu:
1. Penerimaan bahan
2. Karantina barang masuk
3. Ruang sampling
4. Penyimpanan bahan awal
5. Penimbangan dan penyerahan
6. Pengolahan
7. Penyimpanan produk ruahan
8. Pengemasan
10.Penyimpanan obat jadi
11.Pengiriman barang
12.Laboratorium
13.Pencucian peralatan
Bangunan hendaklah mendapatkan penerangan yang efektif dan
mempunyai ventilasi dengan fasilitas pengendali udara (termasuk suhu,
kelembaban dan penyaring) yang sesuai untuk kegiatan dalam bangunan maupun
dengan lingkungan sekitarnya.
2.1.4.4. Peralatan
Peralatan yang digunakan dalam pembuatan obat hendaklah memiliki
rancang bangun dan kontruksi yang tepat. Permukaan peralatan yang bersentuhan
langsung dengan bahan atau produk tidak boleh bereaksi karena dapat merubah
identitas, mutu dan kemurnian produk yang dihasilkan, tidak boleh mencemari
produk, harus mudah dibersihkan baik bagian dalam maupun bagian luar
mesin/alat tersebut. Peralatan yang digunakan untuk menimbang, mengukur, dan
menguji harus diperiksa ketelitiannya secara teratur serta dikalibrasi menurut
program dan prosedur yang tepat.
Pemasangan dan penempatan alat harus dapat mencegah terjadinya
kontaminasi silang dan cukup renggang untuk memberikan keleluasaan kerja.
Saluran air, uap, udara bertekanan atau hampa udara harus dipasang dengan baik
sehingga mudah dicapai selama kegiatan berlangsung.
Peralatan hendaknya dirawat menurut jadwal agar tetap berfungsi dengan
baik dan mencegah pencemaran terhadap produk. Catatan mengenai pelaksanaan,
buku catatan harian yang menunjukkan tanggal, waktu, kekuatan dan nomor batch
atau lot produk yang diolah dengan peralatan tersebut serta pelaksana pembersih.
2.1.4.5. Sanitasi dan Higiene
Tingkat sanitasi dan higiene yang tinggi hendaklah diterapkan pada setiap
aspek pembuatan obat. Ruang lingkup sanitasi dan higiene meliputi personil,
bangunan, peralatan dan perlengkapan, bahan produksi serta wadahnya dan segala
sesuatu yang dapat merupakan sumber pencemaran produk.
2.1.4.5.1. Personalia
1. Semua karyawan hendaklah menjalani pemeriksaan kesehatan, baik pada
waktu diterima bekerja maupun selama bekerja.
2. Setiap karyawan hendaklah menetapkan higiene pribadi yang baik.
3. Karyawan yang menderita suatu penyakit atau mempunyai luka terbuka,
yang dapat merugikan kualitas produk, hendaklah dilarang untuk
menangani bahan dan produk sampai dia sembuh kembali.
4. Semua karyawan hendaklah didorong untuk melaporkan keadaan
kesehatannya yang dapat merugikan kualitas produk kepada atasannya.
5. Dihindarkan persentuhan langsung antara tangan dengan bahan baku,
produk antara dan produk ruahan.
6. Karyawan hendaklah mengenakan pakaian pelindung badan yang bersih
termasuk penutup rambut, hidung, dan mulut sesuai dengan tempat kerja
karyawan tersebut untuk mencegah kontak langsung antara badan dengan
produk.
7. Karyawan harus mencuci tangan terlebih dahulu sebelum memasuki
8. Merokok, makan, minum, menguyah, meletakkan tanaman, menyimpan
makanan dan minuman hanya diperbolehkan ditempat-tempat tertentu
saja.
9. Peraturan higiene perorangan hendaklah diberlakukan bagi setiap orang
yang memasuki daerah produksi.
2.1.4.5.2. Bangunan
1. Rancang bangun gedung harus memudahkan untuk pelaksanaan
sanitasinya.
2. Tersedianya toilet dalam jumlah yang cukup dengan ventilasi yang baik.
3. Tersedia tempat penyimpanan barang milik pribadi yang memadai.
4. Fasilitas penyiapan makanan dibatasi daerah khusus, harus terpelihara dan
bersih.
5. Harus tersedia tempat sampah yang cukup yang terletak diluar bangunan
produksi, jangan biarkan sampah menumpuk dimana-mana.
6. Rodentisida, insektisida, bahan fumigasi dan bahan pembersih lain yang
digunakan pada sanitasi tidak boleh mencemari peralatan, bahan baku,
bahan pengemas, produk dalam proses dan produk jadi.
7. Harus mempunyai prosedur tetap sanitasi, meliputi cara-cara sanitasi,
jadwal pelaksanaan sanitasi dan penanggung jawab pelaksanaan sanitasi.
2.1.4.5.3. Peralatan
1. Setelah peralatan digunakan harus segera dibersihkan baik bagian dalam
maupun luarnya sesuai prosedur yang telah ditetapkan.
2. Hindari penggunaan sikat dan udara bertekanan, gunakan vakum atau cara
3. Pembersihan peralatan yang dapat dipindah-pindahkan hendaklah
dilakukan diruang terpisah dari ruang produksi.
4. Prosedur tetap cara pembersihan alat harus ditaati.
2.1.4.6. Produksi
Produksi obat hendaklah dilaksanakan mengikuti prosedur yang telah
ditetapkan agar selalu diperoleh obat jadi yang memenuhi spesifikasi yang
ditentukan. Prosedur produksi hendaklah dibuat oleh penanggung jawab produksi
bersama-sama dengan penanggung jawab pengawasan mutu. Setiap
penyimpangan prosedur yang telah ditetapkan hendaknya dicatat pada catatan
batch dan bila perlu proses produksi setiap batch sebelumnya dievaluasi kembali.
2.1.4.6.1. Bahan awal
1. Setiap pemasukan, pengeluaran dan sisa bahan harus dilakukan
pencatatan.
2. Pada saat diterima harus diperiksa keutuhan kemasan dan kebenaran label
dari bahan tersebut.
3. Setiap bahan awal, sebelum dinyatakan lulus untuk digunakan hendaklah
memenuhi spesifikasi bahan awal yang sudah ditetapkan yang diberi label
dengan nama yang dinyatakan dalam spesifikasi.
4. Bahan awal yang mengalami kerusakan oleh suhu disimpan ditempat yang
suhu udaranya diatur.
5. Bahan awal yang mudah terurai atau menurun potensinya harus dinyatakan
batas waktu penggunaannya.
6. Penyimpanan hendaklah dilakukan dalam ruangan atau tempat yang suhu
7. Persediaan bahan awal diperiksa dalam selang waktu tertentu untuk
menyakinkan bahwa wadahnya tertutup rapat, bertanda yang benar dan
dalam kondisi yang baik pemeriksaan laboratorium kembali dilakukan
sesuai prosedur yang ditentukan.
8. Semua bahan awal yang tidak memenuhi syarat ditandai dengan jelas,
ditempatkan terpisah dan secepatnya dikembalikan kepemasok atau
dimusnahkan.
2.1.4.6.2. Validasi Prosedur
Semua prosedur produksi hendaklah divalidasi dengan tepat. Validasi
dilaksanakan menurut prosedur yang telah ditentukan dan catatan hasilnya harus
disimpan. Program dan dokumentasi validasi hendaklah membuktikan kecocokan
bahan yang dipakai, keandalan peralatan dan sistem serta kemampuan petugas
pelaksana.
Perubahan penting dalam proses, peralatan atau bahan hendaklah disertai
dengan validasi ulang, untuk menjamin bahwa perubahan tersebut akan tetap
menghasilkan produk yang memenuhi spesifikasi yang telah ditentukan.
2.1.4.6.3. Pencemaran
Pencemaran kimiawi atau mikroba terhadap suatu obat yang dapat
merugikan kesehatan atau mengurangi daya terapeutik atau mempengaruhi
kualitas suatu produk, tidak dapat diterima. Perhatian khusus hendaklah diberikan
pada masalah pencemaran silang, karena sekalipun sifat dan tingkatannya tidak
berpengaruh langsung pada kesehatan, hal ini menunjukkan pelaksanaan
pembuatan obat yang tidak sesuai dengan CPOB. Tindakan pencegahan terhadap
dengan pemeriksaan rutin pada saringan udara, pemeriksaan lingkungan, dan
pemeriksaan perbedaan tekanan antar ruang terutama ruang penyangga.
2.1.4.6.4. Sistem penomoran batch dan lot.
Penomoran batch dan lot diperlukan secara rinci untuk memastikan bahwa
produk antara, produk ruahan, dan produk jadi dapat dikenali dengan nomor batch
atau lot tertentu. Sistem penomoran ini hendaknya menjamin bahwa nomor batch
dan lot yang sama tidak digunakan secara berulang. Tidak diperkenankan
memakai nomor bets atau nomor lot yang sama selama periode tertentu yaitu
paling sedikit 10 tahun. Untuk bets yang diolah ulang hendaklah diberikan kode
tambahan terhadap nomor bets tersebut.
2.1.4.6.5. Penimbangan dan penyerahan
Penimbangan dan penyerahan bahan awal, produk antara, produk ruahan
dan produk jadi harus dilakukan dan didokumentasikan sesuai dengan prosedur
yang telah ditetapkan. Sebelum dilakukan penimbangan harus dilakukan
pemeriksaan kebenaraan penandaan termasuk hasil pemeriksaan laboratorium.
Untuk menghindari terjadinya kontaminasi silang, dan hilangnya identitas maka
bahan awal, produk antara, dan produk ruahan yang ada didaerah penyerahan
hanya boleh untuk satu batch saja.
2.1.4.6.6. Pengolahan
Semua bahan yang digunakan dalam pengolahan harus diperiksa lebih
dahulu. Hendaklah tidak memasukkan bahan lain selain bahan untuk bets yang
sedang diolah tersebut. Pemantauan kondisi area pengolahan dan langkah yang
harus dilakukan sebelum memulai proses pengolahan sebaiknya menggunakan
dipantau dan dikendalikan sesuai persyaratan yang telah ditetapkan, peralatan
harus dinyatakan bersih secara tertulis sebelum digunakan. Kegiatan pengolahan
harus mengikuti prosedur tetap, dan tiap penyimpangan harus segera dilaporkan
kepada supervisor dan di dokumentasikan di dalam catatan pengolahan batch.
2.1.4.6.7. Pengawasan Selama Proses
Prosedur pengawasan selama proses harus dipatuhi seperti pengambilan
contoh, frekuensi pengambilan contoh, dan jumlah yang diambil untuk
pemeriksaan. Hasil pengujian pengawasan selama proses harus dicatat dan di
dokumentasikan.
Pengawasan mutu selama proses produksi (IPC) dilakukan untuk :
1. Sediaan padat meliputi: pemeriksaan kadar zat aktif, pemeriksaan
keseragaman bobot untuk tablet dan kapsul, dilakukan beberapa kali
selama proses produksi, pemeriksaan waktu hancur, kekerasan tablet
(kadar air), sample diambil pada waktu permulaan, pertengahan, dan akhir
pencetakan tablet.
2. Sediaan setengah padat meliputi: keseragaman dan homogenitas obat,
pemeriksaan ukuran partikel, pemeriksaan tampilan, viskositas, berat
jenis, pemeriksaan berat, pemeriksaan kebocoran tube (wadah).
2.1.4.6.8. Pengemasan
Kegiatan pengemasan berfungsi membagi-bagi dan mengemas produk
ruahan menjadi produk jadi. Proses pengemasan hendaklah dilaksanakan dibawah
pengawasan ketat untuk menjaga identitas, keutuhan, dan kualitas barang yang
sudah dikemas. Sebelum kegiatan pengemasan dimulai hendaklah dilakukan
bersih dan bebas dari produk dan sisa produk lain atau dokumen yang tidak
diperlukan untuk kegiatan yang dilakukan.
Sebelum menempatkan bahan pengemas pada jalur pengemasan hendaklah
diadakan pemeriksaan kesiapan jalur pengemasan yang bersangkutan oleh petugas
yang ditunjuk sesuai dengan prosedur tertulis yang ditentukan.
Pada penyelesaian proses pengemasan produk yang sudah dikemas
hendaklah diperiksa dengan teliti untuk memastikan bahwa produk obat tersebut
sesuai dengan persyaratan dalam prosedur pengemasan induk. Hanya obat jadi
yang berasal dari satu batch pengemasan saja yang boleh ditempatkan pada satu
plat. Bila ada karton yang tidak penuh maka jumlah yang ada didalamnya
hendaklah dituliskan pada karton tersebut.
Produk dalam status karantina hendaklah diberi label “karantina” dan
disimpan dalam rak khusus untuk karantina atau ditempat yang diberi tanda
khusus sehingga mudah dibedakan dengan produk yang telah diluluskan.
2.1.4.6.9. Penyimpanan Bahan Awal, Produk Antara, Produk Ruahan,dan
Obat Jadi
Semua bahan hendaklah disimpan secara rapi dan teratur untuk mencegah
resiko tercampur-baur atau pencemaran serta memudahkan pemeriksaan dan
pemeliharaan. Semua bahan ini disimpan dengan jarak yang cukup terhadap bahan
lainnya maupun terhadap dinding, tidak diletakkan dilantai, dan dalam kondisi
lingkungan yang sesuai. Penyimpanan diluar gudang diperbolehkan bagi bahan
yang dikemas dalam wadah kedap yang mutunya tidak terpengaruh oleh suhu,
kelembaban dan faktor lainnya. Bahan yang mudah terbakar hendaklah disimpan
Setiap bahan awal, produk antara, produk ruahan, dan obat jadi yang
disimpan hendaklah mempunyai kartu persediaan yang senantiasa direkonsiliasi
dan jika terdapat penyimpangan hendaklah dicatat disertai penjelasan.
2.1.4.7. Pengawasan Mutu
Pengawasan mutu adalah bagian yang penting dari cara pembuatan obat
yang baik agar tiap obat yang dibuat memenuhi persyaratan mutu yang sesuai
dengan tujuan penggunaannya. Rasa keterikatan dan tanggung jawab semua unsur
dalam semua rangkaian pembuatan adalah mutlak untuk menghasilkan obat yang
bermutu mulai dari saat obat dibuat sampai pada distribusi obat jadi. Untuk
keperluan tersebut harus ada suatu bagian pengawasan mutu yang berdiri sendiri.
Sistem pengawasan mutu hendaklah dirancang dengan tepat untuk
menjamin bahwa tiap obat mengandung bahan dengan mutu yamg benar dan
jumlah yang ditetapkan dan dibuat pada kondisi yang tepat dan mengikuti
prosedur standar sehingga obat tersebut senantiasa memenuhi spesifikasi yang
telah ditetapkan mengenai identitas, kadar, kemurnian mutu, dan keamanannya.
Pengawasan mutu meliputi semua fungsi analisa yang dilakukan
laboratorium termasuk pengambilan contoh, pemeriksaan dan pengujian bahan
awal, produk antara, produk ruahan, dan obat jadi. Pengawasan mutu juga
meliputi program uji stabilitas, pemantauan lingkungan kerja, validasi,
dokumentasi suatu batch, program penyimpanan contoh dan penyusunan serta
penyimpanan spesifikasi yang berlaku dari tiap bahan dan produk termasuk
Bagian pengawasan mutu melaksanakan tugas pokok sebagai berikut :
a. Menyusun dan merevisi prosedur pengawasan dan spesifikasi.
b. Menyiapkan intruksi tertulis yang rinci untuk tiap pemeriksaan dan
pengujian.
c. Menyusun rencana dan prosedur tertulis mengenai pengambilan contoh
untuk pemeriksaan.
d. Menyimpan contoh pertinggal untuk rujukan dimasa mendatang.
e. Meluluskan atau menolak tiap batch bahan awal, produk antara, produk
ruahan, dan obat jadi serta hal-hal lain yang telah ditentukan,
f. Meneliti catatan yang berhubungan dengan pengolahan, pengemasan, dan
pengujian obat jadi batch yang bersangkutan sebelum meluluskannya
untuk didistribusikan.
g. Mengevaluasi stabilitas semua obat jadi secara berlanjut, bahan awal jika
diperlukan, dan menyiapkan intruksi mengenai cara penyimpanan bahan
awal dan obat jadi dipabrik berdasarkan data stabilitas yang ada.
h. Menetapkan tanggal kadarluarsa dan batas waktu penggunaan bahan awal
dan obat jadi berdasarkan data stabilitas dan kondisi penyimpanannya.
i. Mengevaluasi dan menyetujui prosedur pengolahan ulang suatu produk.
j. Menyetujui penunjukkan pemasok bahan baku dan bahan pengemas yang
diketahui dapat dipercayai mampu atau dapat diandalkan untuk memasok
bahan awal yang memenuhi spesifikasi mutu yang telah ditetapkan.
k. Mengambil bagian atau memberikan bantuan dalam pelaksanaan program
l. Mengevaluasi semua keluhan yang diterima atau kekurangan yang
ditemukan mengenai suatu batch, dan bila perlu bekerjasama dengan
bagian lain untuk mengambil tindakan perbaikan yang diperlukan.
m. Menyediakan baku pembanding sekunder sesuai spesifikasi yang terdapat
pada prosedur pengujian yang berlaku dan menyimpan baku pembanding
ini pada kondisi yang tepat.
n. Menyimpan catatan pemeriksaan dan pengujian semua contoh yang
diambil.
o. Mengevaluasi obat yang dikembalikan dan menetapkan apakah obat
tersebut dapat digunakan langsung atau diproses ulang atau harus
dimusnahkan.
p. Ikut serta dalam program inspeksi diri bersama bagian lain dalam
perusahaan.
q. Memberikan rekomendasi untuk pembuatan obat oleh pihak lain atas dasar
kontrak setelah diadakan evaluasi terhadap kontraktor yang bersangkutan
di nilai mampu membuat obat yang memenuhi standart mutu yang
ditetapkan.
2.1.4.8. Inspeksi Diri
Tujuan inspeksi diri adalah untuk melakukan penilaian apakah seluruh
aspek produksi dan pengendaliaan mutu senantiasa memenuhi persyaratan CPOB.
Program inspeksi diri hendaklah dirancang untuk mencari kelemahan dalam
pelaksanaan CPOB dan untuk menetapkan tindakan perbaikannya. Inspeksi diri
ini hendaklah dilaksanakan secara teratur. Tindakan perbaikan yang disarankan
yang mampu menilai secara objektif pelaksanaan CPOB. Prosedur dan catatan
mengenai inspeksi diri hendaklah dibuat.
Untuk mendapatkan standar inspeksi diri yang minimal dan seragam maka
disusun daftar pemeriksaan selengkap mungkin. Daftar pemeriksaan hendaklah
meliputi pertanyaan mengenai hal-hal berikut :
1. Karyawan
2. Bangunan termasuk fasilitas untuk karyawan
3. Penyimpanan bahan awal dan bahan jadi
4. Peralatan
5. Produksi
6. Pengawasan mutu
7. Dokumentasi
8. Pemeliharaan gedung dan peralatan
Tim inspeksi diri ditunjuk oleh pimpinan perusahaan terdiri dari
sekurang-kurangnya tiga orang yang ahli dibidang yang berlainan dan paham
mengenai CPOB. Anggota tim dapat berasal dari lingkungan perusahaan atau dari
luar lingkungan perusahaan. Tiap anggota tim hendaklah bebas dalam
memberikan penilaian atas hasil inspeksi.
2.1.4.9. Penanganan Keluhan dan Penarikan Kembali Obat Yang Beredar
Keluhan dan laporan dapat menyangkut kualitas, efek samping yang
merugikan atau masalah medis lainnya. Semua keluhan dan laporan hendaklah
diselidiki dan dievaluasi serta diambil tindak lanjut yang sesuai.
Penarikan kembali obat jadi dapat berupa penarikan kembali satu atau
Penarikan kembali dilakukan apabila ditemukan adanya produk yang tidak
memenuhi persyaratan kualitas atau atas dasar pertimbangan adanya efek samping
yang tidak diperhitungkan yang merugikan kesehatan. Penarikan kembali seluruh
obat jadi tertentu dapat merupakan tindak lanjut penghentian pembuatan satu jenis
obat jadi yang bersangkutan.
2.1.4.10. Dokumentasi
Dokumentasi pembuatan obat merupakan bagian dari sistem informasi
manajemen yang meliputi spesifikasi, prosedur, metode dan instruksi, catatan dan
laporan serta jenis dokumentasi lain yang diperlukan dalam perencanaan,
pelaksanaan, pengendalian, serta evaluasi seluruh rangkaian kegiatan pembuatan
obat. Sistem dokumentasi hendaklah menggambarkan riwayat lengkap dari setiap
batch atau lot suatu produk sehingga memungkinkan penyelidikan serta
penelusuran terhadap batch atau lot produk yang bersangkutan. Sistem
dokumentasi diperlukan pula dalam pemantauan dan pengendalian, misalnya
kondisi lingkungan, perlengkapan dan personalia.
2.1.4.11. Prosedur dan Catatan Penanganan Keluhan
Hendaklah dibuat prosedur penanganan keluhan dan laporan mengenai
reaksi yang merugikan dari obat jadi, yang mencakup definisi tentang keluhan dan
reaksi merugikan, jenis keluhan dan laporan, cara penanganan keluhan dan
laporan mengenai reaksi yang merugikan dari obat jadi, yang mencakup definisi
tentang keluhan dan reaksi merugikan, jenis keluhan dan laporan, cara
penanganan dan evaluasi. Juga dibuat catatan untuk tiap keluhan dan laporan yang
memuat nama produk dan nomor batch. Jenis keluhan dan laporan, tempat asal
keluhan atau laporan, hasil penyelidikan, evaluasi, tanggapan dan tindak lanjut
terhadap keluhan atau laporan.
2.1.4.12. Prosedur dan Catatan Penanganan Obat Kembalian
Hendaklah dibuat prosedur penanganan obat yang dikembalikan yang
mencakup pedoman mengenai obat jadi yang dapat diselamatkan, diolah kembali
dan dimusnakan. Hasil penanganan obat kembalian haruslah dicatat.
2.1.4.13. Prosedur dan Catatan Penarikan Kembalian Obat Jadi
Hendaklah dibuat prosedur penarikan kembali obat jadi suatu batch atau
lot atau seluruh obat jadi dari peredaran dan juga dibuat catatan tindakan
penarikan kembali yang mencakup nama produk, nomor batch dan ukuran batch
tanggal dimulai dan selesainya penarikan, alasan penarikan kembali, jumlah sisa
dan jumlah yang telah didistribusikan, jumlah produk yang dikembalikan, tempat
asal produk dikembalikan, evaluasi, tindak lanjut, dan laporan penanganan
penarikan kembali termasuk laporan kepada pemerintah jika diperlukan.
2.1.4.14. Prosedur dan Catatan Pemusnahan Bahan dan Produk yang
Ditolak
Dibuat prosedur pemusnahan bahan atau produk yang ditolak yang
mencakup tindakan pencegahan lingkungan dan kemungkinan jatuhnya produk
tersebut ketangan orang yang tidak berwenang. Juga harus dibuat catatan
pemusnahan bahan atau produk yang ditolak yang berisi antara lain nama bahan,
nomor batch dan jumlah, asal bahan atau produk, cara pemusnahan, nama petugas
2.1.5 Kualifikasi dan Validasi
2.1.5.1 Kualifikasi
Validasi untuk mesin, peralatan produksi dan sarana penunjang disebut
dengan kualifikasi. Jadi, kualifikasi adalah istilah yang digunakan untuk validasi
mesin, peralatan produksi maupun sarana penunjang. Kualifikasi mesin, peralatan
produksi maupun sarana penunjang merupakan langkah pertama (first step) dalam
pelaksanakan validasi di industri farmasi.
Kualifikasi adalah “kegiatan pembuktian” bahwa perlengkapan fasilitas
atau sistem yang digunakan dalam suatu proses/ sistem akan selalu bekerja sesuai
dengan kriteria yang diinginkan dan konsisten. Kualifikasi peralatan merupakan
identitas sifat suatu peralatan yang berkaitan dengan kinerja dan fungsinya serta
pemberian batasan nilai tertentu terhadap sifat tersebut.
Validasi/ kualifikasi mesin, peralatan produksi dan sarana penunjang terdiri dari 4
tingkatan, yaitu:
1. Kualifikasi Desain
Tujuan dari kualifikasi desain adalah untuk menjamin dan
mendokumentasikan bahwa sistem atau peralatan atau bangunan yang
akan dipasang atau dibangun (rancang bangunan) sesuai dengan ketentuan
atau spesifikasi yang diatur dalam ketentuan CPOB yang berlaku. Jadi
kualifikasi desain dilaksanakan sebelum mesin, peralatan produksi atau
sarana penunjang (termasuk bangunan untuk industri farmasi) tersebut
2. Kualifikasi Instalasi
Tujuan kualifikasi instalasi adalah untuk menjamin dan
mendokumentasikan bahwa sistem atau peralatan yang diinstalasi sesuai
dengan spesifikasi yang tertera pada dokumen pembelian, manual alat
yang bersangkutan dan pemasangannya dilakukan memenuhi spesifikasi
yang telah ditetapkan. Jadi kualifikasi instalasi dilaksanakan pada saat
pemasangan atau instalasi peralatan produksi atau sarana penunjang.
3. Kualifikasi Operasional
Tujuan dari kualifikasi operasional adalah untuk menjamin &
mendokumentasikan bahwa sistem atau peralatan yang telah diinstalasi
bekerja (beroperasi) sesuai dengan spesifikasi yang diinginkan. Jadi
kualifikasi operasional dilaksanakan setelah pemasangan atau instalasi
mesin atau peralatan produksi atau sarana penunjang dan digunakan
sebagai tes mesin/ peralatan.
4. Kualifikasi Kinerja
Tujuan dari kualifikasi kinerja adalah untuk menjamin &
mendokumentasikan bahwa sistem atau peralatan yang telah diinstalasi
bekerja (beroperasi) sesuai dengan spesifikasi yang diinginkan dengan
cara menjalankan sistem sesuai dengan tujuan penggunaan
Masing-masing pelaksanaan kualifikasi harus dilakukan secara berurutan
dan berkesinambungan. Artinya, dalam pelaksanaan kualifikasi dimulai dari
Kualifikasi Desain, kemudian Kualifikasi Instalasi, Kualifikasi Operasional dan
2.1.5.2 Validasi
Validasi adalah tindakan pembuktian yang didokumentasi dengan
cara-cara yang sesuai bahwa tiap bahan, prosedur, kegiatan, sistem, dan perlengkapan
yang digunakan dalam produksi dan pengawasan mutu akan senantiasa mencapai
hasil yang diinginkan.
Cara-cara pelaksanaan validasi terbagi empat yaitu :
1. Validasi Prospektive
Adalah validasi berdasarkan pada perolehan data pertama sesuai protokol
validasi yang direncanakan. Validasi ini berlaku untuk produk yang belum
beredar.
2. Validasi Concurrent
Adalah validasi yang berdasarkan data otentik yang diperoleh dan
dikumpulkan dari proses yang sedang dilaksanakan. Validasi ini berlaku
pada produk yang sedang beredar.
3. Validasi Retrospektive
Adalah validasi yang berdasarkan data otentik yang diperoleh dan
dikumpulkan dari proses yang sudah dilaksanakan dan dinilai menurut
prinsip statistik. Validasi ini berlaku pada produk yang sudah beredar.
4. Validasi Ulang
Adalah validasi yang dilakukan bila ada perubahan bahan baku, proses
2.1.5.2.1 Validasi Prosedur Analitik
Validasi prosedur analitik merupakan proses yang dilakukan melalui
penelitian laboratorium untuk membuktikan bahwa karakteristik kinerja prosedur
itu memenuhi persyaratan aplikasi analitik yang dimaksudkan. Jenis prosedur
analitik yang harus divalidasi pada umumnya adalah uji identifikasi, uji kuantitatif
komponen terpilih lainnya dalam suatu produk obat, uji kuantitatif kandungan
cemaran, dan uji batas untuk mengendalikan jumlah cemaran.
2.1.5.2.2 Validasi Berkala
Bagian pengawasan mutu hendaklah memberikan bantuan yang diperlukan
atau mengambil bagian dalam pelaksanaan validasi berkala oleh bagian lain,
khususnya bagian produksi untuk menjamin bahwa setiap produk yang dihasilkan
senantiasa memenuhi spesifikasi yang telah ditetapkan.
2.1.5.2.3 Langkah-langkah Pelaksanaan Validasi
Begitu luasnya cakupan validasi, terkadang membingungkan kalangan
praktisi di industri farmasi untuk melaksanakannya. Food and Drug
Administration (FDA) dalam “Guideline on General Principles of Process
Validation” memberikan langkah-langkah dalam pelaksanaan validasi, yang
tertuang dalam “validation life cyle” berikut ini, yaitu:
1. Membentuk Validation Comitee (Komite Validasi), yang bertanggung
jawab terhadap pelaksanaan validasi di industri farmsai bersangkutan.
2. Menyusun Validation Master Plan (Rencana Induk Validasi), yaitu
dokumen yang menguraikan (secara garis besar) pedoman pelaksaan
3. Membuat Dokumen Validasi, yaitu protap (prosedur tetap), protokol serta
laporan validasi.
4. Pelaksanaan Validasi.
5. Melaksanakan Peninjauan Periodik, Change Control dan Validasi ulang
BAB III
KEGIATAN DI INDUSTRI FARMASI
3.1. Aspek Personalia
PT. Kimia Farma (Persero) Tbk Plant Medan memiliki personalia
sebanyak 70 orang dengan berbagai pendidikan, ketrampilan, dan kemampuan
sesuai dengan bidangnya masing-masing.
3.2. Struktur Organisasi
PT. Kimia Farma (Persero) Tbk Plant Medan dipimpin oleh seorang Plant
Manager yang membawahi :
1. Bagian Perencanaan Produksi dan Pengendalian Inventori.
2. Bagian Produksi dengan 2 supervisor.
- Supervisor Produksi
- Supervisor Pengemasan
3. Bagian Pemastian Mutu.
4. Supervisor Teknik dan Pemeliharaan.
5. Supervisor Umum dan Personalia.
6. Supervisor Keuangan.
7. Supervisor Akuntansi.
8. Supervisor Penyimpanan.
3.3. Sediaan-sediaan obat yang diproduksi PT. Kimia Farma (Persero) Tbk.
Plant Medan
1. Antalgin tablet 500 mg botol 1000
3. Betason-N krim
4. Parasetamol tablet 500 mg botol 1000
5. Parasetamol tablet 500 mg strip 10 x 10
6. Betason krim
7. Calcium tablet 500 mg botol 1000
8. Dexocort 0,2% krim
9. Ekstrak belladone tablet 10 mg
10.Fitocassol krim
11.Fungoral krim
12.Gentamisin 0,1% salep
13.Hidrocortison 2,5% krim
14.Undecyl salep
15.Vitamin B komplek tablet botol 1000
3.4. Kegiatan Industri PT Kimia Farma (Persero) Tbk. Plant Medan
Adapun kegiatan di industri PT Kimia Farma (Persero) Tbk. Plant Medan
adalah:
3.4.1. Perencanaan Produksi Dan Pengendalian Inventori (PPPI)
Tugas dan fungsi dari PPPI yaitu:
1. Merencanakan kebutuhan bahan produksi
2. Mengontrol jalannya pembuatan obat
3. Merencanakan pengiriman obat jadi
Dasar perencanaan adalah pesanan pemasaran yang berasal dari direktorat
pemasaran di Jakarta per triwulan. Dari jumlah pesanan tersebut di konversikan
per batch karena tiap produk memiliki ukuran batch yang berbeda.
Untuk pemesanan bahan, PPPI memperhatikan stok bahan baku yang ada
digudang, stok produk ruahan atau setengah jadi dan stok produk jadi di gudang,
sehingga dapat diketahui beberapa bahan yang akan dipesan.
Setelah semua jumlah bahan yang diperlukan untuk produksi dihitung,
maka PPPI mengeluarkan Surat Permintaan Pembelian Bahan (SPPB) ditujukan
kepada bagian pembelian. Pembelian ada dua cara yaitu: secara terpusat di Jakarta
dan secara lokal di Medan. Bagian pembelian ini akan memilih pemasok yang
paling murah tetapi memenuhi spesifikasi bahan yang diminta, kemudian bagian
pembelian menerbitkan surat pemesanan (Purchase Order/ PO) dan
ditandatangani pimpinan. Dibuat tembusan satu lembar arsip pesanan ke bagian
gudang agar disiapkan tempatnya.
Bahan pesanan yang datang diterima oleh bagian gudang dimana bagian
gudang akan memeriksa kecocokan nomor pesanan, jumlah, spesifikasi bahan
yang diminta pada arsip pesanan dengan bahan yang akan diantarkan. Bahan
tersebut akan dikarantina dan diberi label kuning sementara bagian gudang
membuat surat permohonan periksa ke bagian pengawasan mutu untuk melakukan
sampling dan pemeriksaan terhadap bahan tersebut. Bila bahan memenuhi syarat
akan diberi label hijau disertai Hasil Pemeriksaan Laboratorium (HPL), Jika tidak
memenuhi syarat yang akan diberi label merah dan HPL serta dikembalikan ke
Setelah semua bahan yang dipesan lengkap, maka PPPI membuat Surat
Perintah Kerja (SPK) ke bagian produksi yang ditandatangani pimpinan. Pada
SPK tersebut ditulis No.SPK, nama sediaan, No Batch, dan kapan obat tersebut
diharapkan siap diproduksi. SPK dari PPPI yang dikirim kebagian produksi
dilampiri catatan pengolahan batch, catatan pengemasan batch, Surat Perintah
Pengeluran Bahan Baku (SPPBB) dan bahan pengemasan (SPPBK). SPK dibuat
rangkap 4 dengan distribusi ke produksi, gudang, laboratorium dan arsip.
Obat jadi yang telah siap diproduksi dan dikemas kemudian dikirim ke
gudang penyimpanan obat jadi. Setelah dilakukan finished pack analysis oleh
petugas pengawasan mutu. Obat jadi tersebut akan dikirimkan oleh PPPI ke Unit
Logistik Sentral (ULS) Jakarta, maka PPPI membuat surat kebagian gudang untuk
menyiapkan obat jadi tersebut untuk dikirimkan ke Jakarta dan dilakukan stock
opname. Pada bahan yang telah di stock opname akan diberi label stock opname
yang dituliskan tanggal dilakukan stock opname, nama bahan dan jumlahnya.
3.4.2. Produksi
Produksi adalah semua kegiatan pembuatan mulai dari penerimaan bahan
awal, pengolahan sampai dengan menghasilkan obat jadi. Kegiatan produksi ini
dilakukan di grey area, tertutup dan tidak berhubungan langsung dengan bagian
gudang ataupun perkantoran.
Tugas dari bagian produksi PT Kimia Farma (Persero) Tbk. Plant Medan:
1. Melaksanakan pembuatan obat sesuai dengan surat perintah kerja (SPK)
dari bagian PPPI, mulai dari permintaan bahan baku ke gudang,
gudang obat jadi sesuai dengan prosedur tertulis yang telah ditetapkan
(Protap).
2. Melaksanakan dokumentasi atas semua tindakan yang dilakukan selama
proses pengolahan dan pengemasan dengan berpedoman pada protap.
Sebelum dimulainya kegiatan produksi, petugas yang terlibat dalam
kegiatan produksi ataupun yang memasuki area produksi harus memakai pakaian
bersih, masker, penutup kepala, dan mendesinfeksi tangan dengan desinfektan
yang tersedia sebelum memakai sarung tangan.
Hal-hal yang harus diperhatikan sebelum memulai kegiatan produksi:
1. Ruang produksi harus tetap terjaga kebersihan, dimana kegiatan
pembersihan dilakukan tiap pagi sebelum dimulai kegiatan produksi dan
sore hari sesudah selesai kegiatan produksi.
2. Temperatur dan kelembaban tiap ruangan produksi diatur sedemikan rupa
menggunakan Air Handling System (AHS) yaitu AC sentral.
3. Peralatan yang digunakan harus dipastikan selalu dalam keadaan bersih
sebelum dan sesudah dilakukan kegiatan produksi.
4. Ruangan Produksi harus mendapat penerangan dan pertukaran udara yang
cukup agar kegiatan produksi berjalan lancar.
Produksi dilaksanakan setelah adanya SPK dari bagian PPPI ke bagian
produksi, dan dilakukan produksi sesuai dengan protap yang telah ditetapkan serta
mendokumentasi setiap tindakan yang dilakukan selama produksi.
Setelah adanya perintah produksi dari PPPI, bagian produksi untuk
meminta bahan baku ke bagian gudang dengan surat perintah pengeluaran bahan
penyerahan bahan sesuai dengan yang ditulis pada SPPBB/SPPBK tersebut.
Selama produksi berlangsung, dibuat laporan proses produksi mulai dari
penimbangan bahan sampai pengemasan yang bertujuan untuk dokumentasi.
Sehingga bila terjadi kekeliruan ataupun kesalahan pada proses produksi, dapat
segera diketahui pada proses dimana kesalahan tersebut terjadi dan diambil
tindakan untuk mengatasi permasalahan tersebut.
Laporan proses produksi membuat sediaan, No batch, besar batch, tahapan
proses, operator, tanggal, jam, hasil, pengawasan yang berguna untuk mengetahui
berapa lama waktu yang dibutuhkan untuk menghasilkan suatu batch sediaan.
Laporan proses produksi ini diisi oleh petugas yang melakukan suatu tahapan
proses produksi dan diketahui oleh supervisor produksi.
Selama proses produksi berlangsung dilakukan pengawasan dalam proses
(In Process Control/ IPC). IPC yang dilakukan ada 2 macam, yaitu misalnya pada
produksi sediaan tablet:
1. Dilakukan oleh pihak produksi, yaitu setiap 15 menit sekali dilakukan
pemeriksaan keseragaman bobot tablet.
2. Dilakukan oleh pihak pengawasan mutu, antara lain: uji kadar air
granul, dan pada tablet dilakukan: uji kekerasan, waktu hancur, disolusi,
friabilitas, keseragaman bobot dan kadar zat berkhasiat.
Obat yang telah selesai di produksi akan dilakukan pengemasan primer
dibagian produksi yang selanjutnya diserahkan kebagian pengemasan sekunder
melalui pass box untuk dilakukan pengemasan sekunder sampai dihasilkan obat
jadi. Obat jadi yang telah selesai dikemas, ditimbang dan dicatat, diberi label
untuk dilakukan finished pack analysis. Obat jadi yang lulus pemeriksaan diberi
label hijau selanjutnya diserahkan ke gudang penyimpanan obat jadi.
Bagian Produksi pada PT Kimia Farma (Persero) Tbk. Plant Medan terdiri
dari:
1. Jalur Produksi Krim
Jalur pembuatan krim terpisah dari jalur produksi yang lain dimana pada
jalur produksi ini terdiri dari beberapa ruangan yang telah diatur suhu,
kelembaban dan tekanan udaranya dengan AHU. Adapun ruangan pada jalur
produksi krim terdiri dari:
a. Ruangan penimbangan
Pada ruangan ini dilengkapi dengan beberapa alat timbangan digital,
lemari asam, dust collector, Air Handling System (AHS). Bahan – bahan
yang telah ditimbang akan ditempatkan pada staging area untuk kemudian
diambil oleh petugas produksi lain untuk dilakukan proses produksi
selanjutnya. Ruangan dipakai untuk menimbang bahan sediaan krim,
tablet, dan kapsul.
b. Ruangan pencampuran
Pada ruangan ini dilengkapi dengan 2 unit double jacket tank untuk
memanaskan fase air dan fase minyak, ultraturrax untuk mencampur
bahan aktif dengan bahan dasar krim, mixer untuk pengadukan sehingga
diperoleh produk ruahan. Alat-alat tersebut dibersihkan setiap pagi hari
sebelum digunakan dan sore hari sesudah selesai digunakan. Bila tidak ada
proses produksi dilakukan pemeriksaan IPC oleh bagian pengawasan
mutu.
c. Ruangan pengisian
Ruangan untuk melakukan pengisian sediaan krim ada 2 yaitu:
• Ruangan pengisian I
Dilengkapi dengan mesin pengisian krim Elemech dengan kapasitas
2400 tube/jam dan neraca digital untuk pemeriksaan IPC oleh operator.
• Ruang pengisian II
Dilengkapi dengan mesin pengisian krim pharmech dengan kapasitas
900-200 tube/ jam dan neraca digital untuk pemeriksaan IPC oleh
operator.
Sebelum pengisian krim , tube kosong yang telah dibersihkan dibagian
pengemasan dimasukkan ke pass box, dibawa oleh petugas produksi ke
ruang pengisian dan disusun ke mesin pengisian yang telah diisi massa
krim, kemudian dilakukan pengisian. Setiap 15 menit dilakukan
pemeriksaan bobot oleh operator dan pada awal dan akhir pengisian
dilakukan pemeriksaan oleh bagian pengawasan mutu.
d. Ruangan karantina
Pada ruangan ini disimpan produk ruahan untuk menunggu hasil
pemeriksaan laboratorium. Produk ruahan yang telah selesai diperiksa,
kemudian dilakukan pengemasan primer di grey area dan pengemasan
2. Jalur Produksi tablet
Jalur produksi tablet terletak terpisah dari jalur produksi krim untuk
menghindari terjadinya kontaminasi silang. Pada unit tablet juga terdapat
beberapa ruangan yang telah diatur suhu, kelembaban dan tekanan udaranya
dengan AHS. Juga dilengkapi dengan dust collector sentral. Adapun ruangan pada
jalur produksi tablet terdiri dari :
a. Ruangan penimbangan
Pada ruangan ini dilengkapi dengan beberapa alat timbangan digital,
lemari asam, dust collector, dan Air Handling System (AHS).
b. Ruangan pencampuran
Semua bahan tambahan dan bahan aktif dimasukkan kedalam super mixer
dan dicampur hingga homogen, pengecualian untuk bahan pelicin dan
bahan pencampur luar. Massa di atas digranulasi dengan menggunakan
alat rotary wet granulator sehingga didapat granul basah. Selanjutnya
granul basah tersebut dipindahkan ke ruang pengeringan.
c. Ruang pengeringan
Granul basah yang dihasilkan dikeringkan di dalam oven dengan suhu
50-60o
d. Ruang granulasi
C selama 10 jam (tergantung pada bahan yang akan dikeringkan).
Kapasitas oven tersebut 450 kg/hari. Setelah kering dilakukan pemeriksaan
kadar air granul (LOD) di ruangan IPC dan selanjutnya dipindahkan ke
ruangan granulasi untuk pengayakan.
Massa granul yang telah dikeringkan, digranulasi dengan alat communiting
e. Ruang pencampuran akhir
Massa yang telah digranulasi dimasukkan ke dalam alat v-mixer dan
ditambahkan dengan bahan pelicin dan bahan penghancur luar, kemudian
dilakukan pemeriksaan IPC. Massa disimpan diruang karantina menunggu
hasil pemeriksaan.
f. Ruang pencetakan
Ruang untuk pencetakan ada 5, masing-masing terdapat 1 mesin cetak dan
juga terdapat dust collector, neraca digital, dan AHS. Pencetakan
dilakukan misalnya dengan menggunakan mesin cetak tablet merek
Rimek, dengan kecepatan mesin 50 ribu tablet/jam. Setiap 15 menit
operator harus memeriksa keseragaman bobot tablet. Bagian pengawasan
mutu di dalam ruang produksi melakukan pemeriksaan/ pengujian
terhadap produk ruahan yang meliputi: Pemerian, friabilitas, waktu hancur,
kekerasan tablet, disolusi, kadar zat berkhasiat dan keseragaman bobot.
g. Ruang sortir
Tablet yang dihasilkan disortir oleh petugas dari debu dan juga untuk
bentuk tablet yang tidak bagus/ pecah kemudian dipindahkan ke ruangan
pengemasan primer.
h. Ruang pengemasan
Tablet yang telah diluluskan oleh bagian pengawasan mutu dibawa ke
ruang pengemasan primer dan dikemas dalam kantong plastik. Tiap
kantong berisi 1000 tablet dengan menggunakan mesin penghitung dan
diberi silika gel. Atau dikemas dengan penyetripan menggunakan mesin
ruangan pengemasan sekunder melalui pass box untuk dilakukan
pengemasan sekunder.
3. Jalur Produksi kapsul
Sediaan kapsul yang diproduksi oleh PT. Kimia Farma (Persero) Tbk.
Plant Medan adalah kloramfenikol kapsul. Seperti jalur produksi krim dan tablet,
jalur produksi kapsul juga terletak terpisah untuk menghindari terjadinya mix up.
Pada jalur produksi kapsul juga terdapat beberapa ruangan dimana setiap ruangan
tersebut diatur suhu, kelembaban dan tekanan dengan AHS, juga dilengkapi dust
collector sentral.
Adapun ruangan pada unit kapsul terdiri dari :
a. Ruang pengeringan
Bahan pengisi (Avicel) dikeringkan terlebih dahulu didalam oven selama
±12 jam pada suhu 85o
b. Ruang pencampuran
C. Setelah itu semua bahan dipindahkan keruang
pencampuran.
Pada ruang ini dilakukan pencampuran bahan aktif, bahan pengisi dan
bahan tambahan lainnya dengan menggunakan alat V-mixer selama 15
menit. Setelah homogen, massa disimpan diruang karantina menunggu
pemeriksaan oleh bagian pengawasan mutu dan kemudian dipindahkan
keruang pengisian kapsul.
c. Ruang pengisian kapsul
Massa yang telah homogen dimasukkan ke mesin pengisian kapsul
(Kwang Dah). Pada awal dan akhir pengisian dilakukan pemeriksaan