ANALISIS KOMPOSISI ASAM LEMAK UDANG WINDU
(
Penaeus monodon)
DARI PERAIRAN LAUT DAN
TAMBAK BUDIDAYADAERAH PERCUT
SEI TUAN DELI SERDANGDENGAN
METODE GC-MS
TESIS
Oleh
ROBBY RUDIANSEN PURBA 117006127/KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
ANALISIS KOMPOSISI ASAM LEMAK UDANG WINDU
(
Penaeus monodon)
DARI PERAIRAN LAUT DAN
TAMBAK BUDIDAYADAERAH PERCUT
SEI TUAN DELI SERDANGDENGAN
METODE GC-MS
TESIS
Diajukan sebagai salah satu syarat untuk memperoleh gelar Magister Sains Dalam Program Studi Ilmu Kimia pada Fakultas Matematika dan Ilmu
Pengetahuan Alam Universitas Sumatera Utara
ROBBY RUDIANSEN PURBA 117006127/KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAMUNIVERSITAS SUMATERA UTARA
Judul Tesis :ANALISIS KOMPOSISI ASAM LEMAK UDANG WINDU(Penaeus monodon) DARIPERAIRAN LAUT DAN TAMBAK BUDIDAYA DAERAH PERCUT SEI
TUAN DELI SERDANG DENGAN METODE GC-MS Nama Mahasiswa : Robby Rudiansen Purba
Nomor Pokok : 117006127/KIM Program Studi : Ilmu Kimia
Menyetujui Komisi Pembimbing
(Prof.Dr. Tonel Barus)
Ketua Anggota
(Lamek Marpaung. M.Phil, Ph.D)
Ketua Program Studi Dekan
(Prof. Basuki Wirjosentono, MS, Ph.D) ( Dr. Sutarman, M. Sc)
PERNYATAAN ORISINALITAS
ANALISIS KOMPOSISI ASAM LEMAK UDANG WINDU (Penaeus monodon)
DARI PERAIRAN LAUT DAN TAMBAK BUDIDAYA DAERAH PERCUT SEI TUAN DELI SERDANG
DENGAN METODE GC-MS
TESIS
Dengan ini saya menyatakan bahwa tesis dalam tesis ini tidak terdapat karya yangpernah diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggidan sepanjang sepengetahuan saya tidak terdapat karya atau pendapat yang pernahditulis atau diterbitkan oleh orang lain kecuali secara tertulis diacu dalam
naskahdan disebut sumbernya dalam daftar pustaka
Medan, April 2013
(Robby Rudiansen Purba NIM. 117006127
PERNYATAAN PERSETUJUAN PUBLIKASI
Sebagai sivitas academia Universitas Sumatera Utara saya yang bertanda tangan dibawah ini :
Nama : Robby Rudiansen Purba
NIM : 117006027
Program Studi : Magister Ilmu Kimia
Jenis Karya Ilmiah : Tesis
Demi pengembangan ilmu pengetahuan, menyetujui untuk memberikan kepada Universitas Sumatera Utara Hak Bebas Royalty Non-Ekslusif ( No-Exclusive Royalty Free Righ) atas Tesis saya yang berjudul :
Analisis Komposisi Asam Lemak Udang Windu (Penaeus monodon) dari Perairan Laut dan Tambak Budidaya Daerah Percut Sei Tuan Deli Serdang Dengan Metode GC-MS
Beserta perangkat yang ada (jika diperlukan). Dengan Hak Bebas Royalty Non-Ekslusif ini, Universitas Sumatera Utara berhak menyimpan, mengalih media, memformat, mengelola dalam bentuk data- base, merawat dan mempublikasikan Tesis saya tanpa meminta ijin dari saya selama tetap mencantumkan nama saya sebagai penulis dan pemegang dan atau sebagai pemilik hak cipta.
Demikian pernyataan ini saya perbuat dengan sebenarnya.
Medan, 30 April 2013
Telah diuji pada
Tanggal : 26 April 2013
PANITIA PENGUJI TESIS
Ketua : Prof.Dr. Tonel Barus
Anggota : 1.Lamek Marpaung, M.Phil, Ph.D 2.Dr. Hamonangan Nainggolan, MSc. 3.Prof.Dr. Jamaran Kaban, MSc. 4.Dr. Mimpin Ginting, MS
RIWAYAT HIDUP
Nama : ROBBY RUDIANSEN PURBA
Tempat/ Tanggal lahir : M.Pematang, 19 Juli 1971
Riwayat Pendidikan : Tahun 1983 tamat dari SD inpres No 102003 Gunung
Meriah, Tahun 1986 tamat dari SMP Swasta Masehi
Gunung Meriah, Tahun 1989 tamat dari SMA Negeri
1 Bangun Purba, Tahun 1995 tamat dari IKIP Negeri
Medan dan mengikuti Sekolah Pascasarjana di
Universitas Sumatera Utara Tahun 2011 dan tamat
Tahun 2013.
Nama Istri : Dra.Desevita Simanjuntak
Nama Anak : Yolanda Septifanny Purba
David Criston Hamonangan Purba
Nigel Hiskia Purba
Nama Ayah : J. Purba
Nama Ibu : H. Br Sembiring
KATA PENGANTAR
Segala puji dan syukur saya panjatkan kepada Tuhan Yang Maha Kuasa
karena berkat dan anugerahnya lah saya dapat menyelesaikan penulisan Tesis ini
sebagai tugas akhir dalam jenjang Magister.
Saya menyadari bahwa tesis ini masih banyak kekurangan, baik dalam
penulisan kata mungkin juga bobot ilmiahnya.Kritik dan saran dari pembaca diterima
dengan senang hati untuk kesempurnaan tesis ini.
Selesainya penulisan tesis ini, bukanlah semata-mata karena kemampuan saya
sendiri, tetapi berkat saran, bimbingan dan dorongan dari berbagai pihak, untuk itu
saya ucapkan terima kasih kepada :
1. Universitas Sumatera Utara, karena telah memberi wadah pendidikan kepada
saya untuk melanjutkan pendidikan.
2. Bapak Prof.Dr.dr.Syahril Pasaribu,DTM&H, M.Sc (CTM),Sp.A(K) sebagai
Rektor Universitas Sumatera Utara yang telah memberi kesempatan dan fasilitas
kepada penulis untuk menyelesaikan pendidikan Magister Kimia.
3. Bapak Prof.Dr.Ir.Rahim Matondang,MSIE, selaku Direktur Sekolah Pascasarjana
Universitas Sumareta Utara yang telah memberikan kesempatan dan fasilitas
kepada penulis untuk menyelesaikan pendidikan Magister Kimia.
4. Pemerintah provinsi Sumatera Utara yang telah memfasilitasi saya untuk
mendapatkan beasiswa pendidikan dari BAPEDA.
5. Seluruh staf dosen yang memberi kuliah di Program Magister Kimia maupun
pegawai yang telah banyak membantu.
6. Bapak Prof.Dr.Tonel Barus dan Lamek Marpaung, M.Phil,Ph.D., sebagai
pembimbing saya, dan juga Bapak Prof.Basuki Wirjosentono,MS,Ph.D. (Ketua
Program), Prof.Dr.Jamaran Kaban,MSc., Dr.Mimpin Ginting, MS,
Dr.Hamonangan Nainggolan, MSc. Serta Prof. Dr. Yunazar Manjang sebagai
dosen penguji yang telah banyak memberi saran dan masukan.
7. Sembah sujud kepada almarhum kedua orang tua saya J.Purba dan
H.br.sembiring yang telah membiayai pendidikan saya sampai meraih gelar
Sarjana Pendidikan dari IKIP Negeri Medan.
8. Istri tercinta D.Br.Simanjuntak, S.Pd. dan anak-anakku Yolanda Septifany Purba,
David Christon H.Purba, Nigel Hiskia Purba yang telah banyak memberi
semangat dan dorongan.
9. Pihak-pihak yang tidak dapat saya tuliskan satu per satu tetapi begitu banyak
bantuannya selama saya mengerjakan tesis ini.
Medan, 30 April 2013
Hormat saya,
Robby Rudiansen Purba
ANALISIS KOMPOSISI ASAM LEMAK UDANG WINDU (Penaeus monodon) DARI PERAIRAN LAUT DAN TAMBAK BUDIDAYADAERAH
PERCUT SEI TUAN DELI SERDANG DENGAN METODE GC-MS
ABSTRAK
Penelitian ini dilakukan dengan skala laboratorium. Sebagai objek (bahan) dalam penelitian ini adalah Udang Windu (Penaeus monodon) dari perairan laut dan
tambak budidaya. Perlakuan yang diperlakukan yaitu memisahkan lemak dari Udang
Windu dengan cara maserasi menggunakan pelarut n-heksana, kemudian lemak yang diperoleh dimetanolisissebelum dianalisis komponen asam lemaknya dengan Kromatografi Gas –Spektrometri Massa. Data GC-MS memberikan informasi kromatogram terhadap metil ester asam lemak udang windu dari habitat tambak sebanyak 9 jenis asam lemak yaitu :asam iso caproat (1,30 %), asam miristat (1,26 %), asam pentadekanoat (5,83%), asam palmitat (0,93%),asam heptadekanoat (4,01%), asam stearate (0,38%), asam palmitoleat (21,10%), asam oleat(3,42%), asam linoleat (11,30%), dan asam lemak dari udang windu habitat laut teridentifikasi 8 jenis asam lemak yaitu : asam miristat (1,32%), asam pentadekanoat (1,41%), asam palmitat (18,77%), asam heptadekanoat (4,40%), asam stearate (15,19%), asam palmitoleat (5,41%), asam oleat (10,0%), asam linoleat (2,07%),
Kata kunci : Minyak udang windu, metanolisis, metil ester asam lemak, GC-MS
THE ANALYSISCOMPOSITION OF FATTY ACID ON WINDU SHRIMP (Penaeus monodon) FROM THE SEA WATERS ANDFISHPOND
ON PERCUT SEI TUAN DELI SERDANG WITH GC-MS METHOD
ABSTRACT
This study adapted a laboratory scale. The object involved the Windu Shrimp (Penaeus monodon) from sea waters and taken from fishpond. In research, the treatment was to separate its fat from the windu shrimp by airing them used n-hexane solvent, then the fat as oftained provided in metanolisis before analyzing its fatty acid component with a Gas Chromatography- Mass Spektrometry. The data by GC-MS present information abaut chromatogram over metyl ester af fatty acid in windu shrimp as taken from fishpond habitat totally 9 items fatty acid such as : iso hexanoat acid (1,30%), miristat acid (1,26%),pentadecanoat acid (5,83%), palmitat acid (0,93%), heptadecanoat acid (4,01%), stearate acid(0,38%), palmitoleat acid ( 21,10%), oktadecanoat acid (3,42%), linoleat acid (11,30%), and fatty acids from windu shrimp in sea habitat was identified 8 sorts fatty acid namely : miristat acid (1,32%), pentadecanoat acid (1,41%), palmitat acid (18,77%), heptadecanoat acid (4,40%), stearate acid (15,19%), palmitoleat acid (5,41%),oktadecanoat acid (10,0%) and linoleat acid (2,07%).
Keyword : shrimp oil, metanolisis, fatty acid methyl ester, GC-MS
DAFTAR ISI
Halaman
KATA PENGANTAR ii
ABSTRAK iv
1.2.Perumusan Masalah 2
1.3.Pembatasan Masalah 2
1.4.Tujuan Penelitian 3
1.5.Manfaat Penelitian 3
1.6.Tempat Penelitian 3
BAB 2.TINJAUAN PUSTAKA
2.1.Udang Windu (Penaeus monodon) 4
2.1.1.Deskripsi 4
2.1.2.Habitat 7
2.1.3.Komposisi Nilai Gizi 8
2.1.4.Pakan Udang Windu 9
2.2.Minyak dan Lemak 13
2.3.Pengaruh Lingkungan Terhadap Kandungan Lemak Ikan 16
2.4.Ester Asam Lemak 17
2.4.Kromatografi Gas- Spektrometri Massa 19
BAB 3.METODOLOGI PENELITIAN
3.1.Tempat Penelitian 28
3.2.Bahan-bahan 28
3.3.Peralatan 28
3.4.Rancangan penelitian 28
3.5.Diagram Alur Penelitian 31
BAB 4. HASIL DAN PEMBAHASAN
4.1.Hasil Penelitian 33
4.2.Pembahasan 37
4.3.Variasi Asam Lemak 67
BAB 5.KESIMPULAN DAN SARAN
5.1.Kesimpulan 71
5.2. Saran 71
DAFTAR PUSTAKA 72
LAMPIRAN 78
DAFTAR TABEL
Nomor Judul Halaman
2.1 Komposisi kimia dan zat gizi udang windu 8
4.1 Kadar lemak daging udang windu 33
4.2 Kromatogram GC-MS udang windu tambak 34
4.3 Kromatogram GC-MS udang windu laut 36
4.4 Kandungan PUFA dari udang windu 68
4.5 Kandungan MUFA dari udang windu 69
4.6 Kandungan SAFA dari udang windu 69
DAFTAR GAMBAR
Nomor Judul Halaman
2.1 Reaksi pembentukan trigliserida 14
3.1 Diagram alur penelitian 31
4.1 Kromatogram GCMS asam lemak udang windu tambak 34
4.2 Kromatogram GCMS asam lemak udang windu laut 36
4.3 Reaksi metanolisis trigliserida membentuk metil ester asam lemak 38
4.4 Spektrum metil iso hexanoat udang windu tambak 39
4.5 Fragmentasi metil iso hexanoat udang windu tambak 40
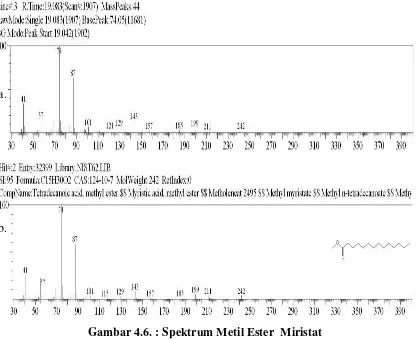
4.6 Spektrum metil myristat udang windu tambak 41
4.7 Fragmentasi metil miristat udang windu tambak 42
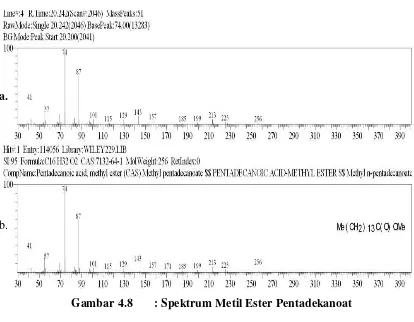
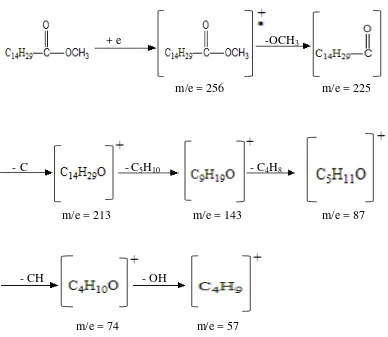
4.8 Spektrum metil pentadekanoat udang windu tambak 43
4.9 Fragmentasi metil pentadekanoat udang windu tambak 44
4.10 Spektrum metil palmitoleat udang windu tambak 45
4.11 Fragmentasi metil palmitoleat udang windu tambak 46
4.12 Spektrum metil hexadekanoat udang windu tambak 46
4.13 Fragmentasi metil hexadekanoat udang windu tambak 47
4.14 Spektrum metil heptadekanoat udang windu tambak 48
4.15 Fragmentasi metil heptadekanoat udang windu tambak 49
4.16 Spektrum metil linoleat udang windu tambak 50
4.17 Fragmentasi metil linoleat udang windu tambak 50
4.18 Spektrum metil 9-oktadekanoat udang windu tambak 51
4.18 Fragmentasi metil 9-oktadekaviinoat udang windu tambak 52
4.19 Spektrum metil stearat udang windu tambak 53
4.20 Fragmentasi metil stearat udang windu tambak 53
4.21 Spektrum metil miristat udang windu laut 54
4.22 Fragmentasi metil miristat udang windu laut 55
4.23. Spektra metil pentadekanoat udang windu laut 56
4,24 Fragmentasimetil pentadekanoat udang windu laut 67
4,25 Spektrum metil palmitoleat udang windu laut 58
4,26 Fragmentasi metil palmitoleat udang windu laut 59
4.27 Spektrum metil palmitat udang windu laut 60
4.28 Fragmentasi metil palmitatudang windu laut 61
4.29 Spektrum metil heptadekanoat udang windu laut 71
4.30 Fragmentasi metil heptadekanoat udang windu laut 63
4.31 Spektrum metil linoleat udang windu laut 63
4.32 Fragmentasi metil linoleat udang windu laut 64
4.33 Spektrum metil 11-oktadekanoatudang windu laut 65
4.34 Fragmentasimetil 11-oktadekanoatudang windu laut 65
4.35 Spektrum metil stearatudang windu laut 66
4.36 Fragmentasi metil stearatudang windu laut 67
DAFTAR LAMPIRAN
Nomor Judul Halaman
1. Pengelompokan asam lemak udang windu 76
2. Kromatogram GC-MS metil ester asam lemak udang windu tbk 77
3. Spektrum MS metil iso hexanoat udang windu tambak 78
4. Spektrum MS metil miristat udang windu tambak 79
5. Spektrum MS metil pentadekanoat udang windu tambak 80
6. Spektrum MS metil pelmitoleat udang windu tambak 81
7. Spektrum MS metil palmitat udang windu tambak 82
8. Spektrum MS metil heptadekanoat udang windu tambak 83
9. Spektrum MS metil linoleat udang windu tambak 84
10. Spektrum MS metil oleat udang windu tambak 85
11. Spektrum MS metil stearate udang windu tambak 86
12. Kromatogram GC-MS metil ester asam lemak udang windu laut 87
13. Spektrum MS metil miristat udang windu laut 88
14. Spektrum MS metil pentadekanoat udang windu laut 89
15. Spektrum MS metil palmitoleat udang windu laut 90
16. Spektrum MS metil palmitat udang windu laut 91
17. Spektrum MS metil heptadekanoat udang windu laut 92
18. Spektrum MS metil linoleat udang windu laut 93
19. Spektrum MS metil oktadekanoat udang windu laut 94
20. Spektrum MS metil stearate udang windu laut 95
21. Gambar udang windu laut dan tambak 96
22. Proses Maserasi lemak udang windu 97
23. Filtrat lemak hasil maserasi udang windu 98
24. Seperangkat alat Rotary epaporator 99
25. Ekstrak pekat lemak udang windu 100
ANALISIS KOMPOSISI ASAM LEMAK UDANG WINDU (Penaeus monodon) DARI PERAIRAN LAUT DAN TAMBAK BUDIDAYADAERAH
PERCUT SEI TUAN DELI SERDANG DENGAN METODE GC-MS
ABSTRAK
Penelitian ini dilakukan dengan skala laboratorium. Sebagai objek (bahan) dalam penelitian ini adalah Udang Windu (Penaeus monodon) dari perairan laut dan
tambak budidaya. Perlakuan yang diperlakukan yaitu memisahkan lemak dari Udang
Windu dengan cara maserasi menggunakan pelarut n-heksana, kemudian lemak yang diperoleh dimetanolisissebelum dianalisis komponen asam lemaknya dengan Kromatografi Gas –Spektrometri Massa. Data GC-MS memberikan informasi kromatogram terhadap metil ester asam lemak udang windu dari habitat tambak sebanyak 9 jenis asam lemak yaitu :asam iso caproat (1,30 %), asam miristat (1,26 %), asam pentadekanoat (5,83%), asam palmitat (0,93%),asam heptadekanoat (4,01%), asam stearate (0,38%), asam palmitoleat (21,10%), asam oleat(3,42%), asam linoleat (11,30%), dan asam lemak dari udang windu habitat laut teridentifikasi 8 jenis asam lemak yaitu : asam miristat (1,32%), asam pentadekanoat (1,41%), asam palmitat (18,77%), asam heptadekanoat (4,40%), asam stearate (15,19%), asam palmitoleat (5,41%), asam oleat (10,0%), asam linoleat (2,07%),
Kata kunci : Minyak udang windu, metanolisis, metil ester asam lemak, GC-MS
THE ANALYSISCOMPOSITION OF FATTY ACID ON WINDU SHRIMP (Penaeus monodon) FROM THE SEA WATERS ANDFISHPOND
ON PERCUT SEI TUAN DELI SERDANG WITH GC-MS METHOD
ABSTRACT
This study adapted a laboratory scale. The object involved the Windu Shrimp (Penaeus monodon) from sea waters and taken from fishpond. In research, the treatment was to separate its fat from the windu shrimp by airing them used n-hexane solvent, then the fat as oftained provided in metanolisis before analyzing its fatty acid component with a Gas Chromatography- Mass Spektrometry. The data by GC-MS present information abaut chromatogram over metyl ester af fatty acid in windu shrimp as taken from fishpond habitat totally 9 items fatty acid such as : iso hexanoat acid (1,30%), miristat acid (1,26%),pentadecanoat acid (5,83%), palmitat acid (0,93%), heptadecanoat acid (4,01%), stearate acid(0,38%), palmitoleat acid ( 21,10%), oktadecanoat acid (3,42%), linoleat acid (11,30%), and fatty acids from windu shrimp in sea habitat was identified 8 sorts fatty acid namely : miristat acid (1,32%), pentadecanoat acid (1,41%), palmitat acid (18,77%), heptadecanoat acid (4,40%), stearate acid (15,19%), palmitoleat acid (5,41%),oktadecanoat acid (10,0%) and linoleat acid (2,07%).
Keyword : shrimp oil, metanolisis, fatty acid methyl ester, GC-MS
BAB 1 PENDAHULUAN 1.1.Latar Belakang Masalah
Udang merupakan salah satu primadona ekspor perikanan Indonesia, yang telah
memberikan pemasukan devisa yang cukup besar bagi negara. Indonesia merupakan
salah satu negara pengekspor udang terpenting didunia disamping Cina, Thailand,
India,Vietnam dan beberapa negara di Amerika Latin. Pada tahun 2004 produksi
udang Indonesiaberada di urutan ke-6 dunia . Negara tujuan ekspor terpenting bagi
Indonesia adalah Amerika Serikat dan Jepang.Indonesia merupakan pengekspor
produk udang beku nomor dua terbesar bagi Jepang, sedangkan untuk Amerika
Serikat, Indonesia berada ditempat ketiga (Rangkuti 2007).
Kondisi geografis Indonesia dengan 2/3 dari wilayahnya adalah perairan
telah memberikan keuntungan tersendiri, yaitu tersedianya sumber daya perairan
yang telah memberi manfaat secara nyata diantaranya adalah udang.Karena
permintaan pasarnya yang cukup besar, udang saat ini tidak hanya ditangkap dari
alam tetapi juga telah berkembang menjadi industri budi daya.
Tingginya permintaan akankomoditas udang baik dipasar lokal maupun
dipasar dunia, dikarenakan udang mempunyai banyak kelebihan dibandingkan hasil
perikanan lainnya. Salah satu keistimewaan udang diantaranya memiliki aroma yang
spesifik, tekstur udang yang keras dan mempunyai nilai gizi yang tinggi.
Aspek gizi dan hasil perikanan yang telah diakui banyak manfaatnya adalah
tingginya kandungan asam lemak disamping protein dan mineral. Mengingat udang
hidup dilingkungan yang bersuhu relatif rendah , maka lemak udang lebih banyak
mengandung asam lemak tidak jenuh ganda (poly unsaturated fatty acid) seperti
linoleat, linolenat, arakhidonat, eikosapentaenoat (EPA) dan decosaheksaenoat
(DHA), merupakan asam lemak essensial bagi tubuh untuk dapat mempertahankan
Menurut data propil daerah Kabupaten Deli Serdang, komoditas unggulan
dari budidaya tambak produksi udang windu tahun 2012 sebesar 3473,1 ton dan
udang vaname sebesar 1185,3 ton. Kecamatan Percut Sei Tuan merupakan salah satu
daerah di Deli Serdang yang mempunyai wilayah pantai perairan laut Belawan,
dimana banyak terdapat tambak budi daya udang windu.
Tingginya kandungan asam lemak tak jenuh ganda dan rendahnya kadar
kolesterol pada ikan telah diakui, sehingga ikan merupakan makanan sehat yang
dianjurkan untuk dikonsumsi. Beberapa hasil penelitian menunjukkan bahwa ikan
tidak dapat memproduksi semua asam lemak yang diperlukannya, dan sintesis asam
lemak pada hewan tersebut sangatlah rendah.Tingginya kandungan asam lemak pada
ikan diduga berasal dari pakan, khususnya fitoplanton seperti chlorella, diatomae dan
dinoflagellata.Pada organisme tersebut sintesa asam lemak berlangsung sangat
efisien, mengingat rantai makanannya yang pendek.
Dari uraian diatas maka penulis tertarik untuk menganalisis kandungan asam
lemak pada udang windu(Penaeus monodon) dari perairan laut dan tambak budidaya
dari daerah Percut Sei Tuan Deli Serdang.
1.2.Perumusan Masalah
Adapun rumusan masalah dalam penelitian ini adalah :
Bagaimana komposisi asam lemak yang terdapat pada udang windu yang berasal dari
perairan laut dan tambak budi daya di daerah Percut Sei Tuan Deli Serdang.
1.3.Pembatasan Masalah
Dalam penelitian ini peneliti hanya menganalisis komposisi asam lemak yang
terdapat pada udang windu dari perairan laut dan tambak budi daya yang berasal
dari daerah Percut Sei Tuan Deli Serdang Sumatera Utara. Untuk mendapatkan
senyawa asam lemak dari udang windu, maka terlebih dahulu daging udang
diekstraksi dengan pelarut n-heksan melalui perendaman (maserasi) selama 3 hari
dengan maksud untuk memisahkan lemak dari udang, selanjutnya lemak yang telah
Kemudian metil ester asam lemak yang diperoleh dianalisis kandungan komposisinya
menggunakan GC-MS.
1.4.Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah :
Untuk mengetahui komposisi asam lemak yang terdapat pada udang windu yang
berasal dari perairan laut dan tambak budi daya di daerah Percut Sei Tuan Deli
Serdang.
1.5.Manfaat Penelitian
1. Hasil penelitian ini dapat dijadikan sebagai informasi komposisi kandungan asam
lemak dalam udang windu dari perairan laut dan tambak budi daya yang berasal
dari daerah Percut Sei Tuan Deli Serdang.
2. Memberikan informasi komposisi asam lemak jenuh dan tak jenuh pada udang
windu dari laut dan tambak budidaya yang berasal dari daerah Percut Sei Tuan
Deli Serdang.
1.6.Tempat Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Organik Bahan Alam FMIPA USU
Medan dan untuk analisis asam lemak dari ekstrak lemak hasil maserasi dilakukan
BAB 2
TINJAUAN PUSTAKA 2.1.Udang Windu (Penaeus monodon)
2.1.1.Deskripsi
Udang Windu (Penaeus monodon) diklasifikasikan Suwignyo (1989) sebagai berikut:
Phylum :Arthropoda
Udang windu (Penaeus monodon)yang dikenal dengan sebutan black tiger
shrimp adalah spesies udang laut yang dapat mencapai ukuran besar, dialam bebas
dapat mencapai 35 cm dan berat sekitar 260 gram, sedangkan yang dipelihara
ditambak, panjang tubuhnya hanya mencapai 20 cm dan berat sekitar 140 gram
(Mujiman dan Suyanto,1989).
Udang windu memiliki kulit tubuh yang keras, berwarna hijau kebiruan dan
berloreng-loreng besar.Namun udang dewasa yang hidup dilaut memiliki warna kulit
merah muda kekuningan dengan ujung kaki renang yang berwarna merah.Sedangkan
udang muda memiliki kulit dengan ciri khas totol-totol hijau.
Pada dasarnya badan udang dibagi menjadi dua bagian, yaitu bagian
cephalathorax, dan abdomen. Caphalathorax merupakan gabungan dari kepala dan
didalamnya terkandung sebagian besar daging yang dapat dimakan dan bagian ekor
(telson).Bagian kepala udang terdiri dari 6 ruas, tiga ruas pertama merupakan
penyangga mata dan perangkat mulut, sedangkan pada tiga ruas terakhir dilengkapi
dengan anggota badan yang berfungsi sebagai pembantu mulut yang disebut rostum
(cucuk kepala).Gigi rostum bagian atas biasanya 7 buah dan bagian bawah 3 buah,
sehingga sering ditulis gigi rostrum 7/3 (M.Ghufran, 2010).
Bagian dada udang terdiri atas 8 ruas yang tiap ruasnya memiliki sepasang
anggota badan (tracopoda). Tracopoda pada ruas pertama sasmpai ketiga (maxipila)
berperan sebagai pelengkap mulut dalam memegang makanan.sedangkan tracopoda
keempat sampai kedelapan (periopoda) berperan sebagai kaki jalan (M.Ghufran,
2010).
Bagian abdomen udang terdiri atas 6 ruas.Ruas pertama sampai kelima
mempunyai sepasang anggota badan pendek sebagai kaki renang (pleopoda).
Pleopoda pada ruas keenam (inopoda) berubah menjadi pipih melebar yang bersama
dengan telson berfungsi sebagai kemudi renang (M.Ghufran, 2010).
Habitat udang windu adalah laut dan dikenal sebagai penghuni dasar
laut.namun hanya udang windu dewasa yang mencari tempat yang dalam di tengah
laut. Saat muda, udang windu berada diperairan yang dangkal di tepi pantai, bahkan
ada yang memasuki muara sungai dan tambak berair payau.Udang termasuk hewan
euryhaline (dapat mentolelir kisaran salinitas yang luas).Udang windu dapat hidup
pada salinitas 3-35 ppt. bahkan kini udang windu telah dipelihara dikolam air tawar di
Gresik.Penelitian yang dilakukan oleh Harianto (2002) menunjukkan bahwa ternyata
udang windu dapat diadaptasi ke air tawar (salinitas 0 ppt) secara bertahap.
Selain bersifat euryhaline, udang windu juga bersifat eurythermal yaitu hewan
yang dapat mentolelir perubahan suhu yang luas. Goncangan suhu yang besar
dimedia kultur, terutama ditambak pada musim kemarau, yaitu pada siang hari suhu
ditolelir oleh udang, walaupun pada kondisi demikian, udang sensitif terhadap
serangan penyakit.
Udang windu dikenal sebagi hewan yang rakus. Hal ini erat kaitannya dengan
system pencernaannya, dimana udang memiliki usus yang tidak panjang sehingga
proses pencernaan makanan cepat sekali berlangsung dan perut cepat menjadi
kosong. Sifat udang yang demikian perlu diketahui agar dalam kulturnya perlu
diusahakan ketersediaan makanan secara terus-menerus, baik dalam jumlah maupun
mutunya.
Berdasarkan kebiasaan makan, udang windu dapat dikelompokkan dalam
golongan hewan pemakan segala (omnivore), baik hewan maupun tumbuhan.Pada
awal fase kehidupannya, yaitu disaat kuning telur habis, udang mulai mencari
makanan alami berupa plankton nabati seperti skeletoma, amphora, navicula,
tetraselmis dan sebagainya.
Pada tingkat Mysis, udang mulai memakan plankton hewan seperti protozoa,
rotifer, anak teritip, kutu air dan lain-lain. Setelah burayak mencapai tingkat post
larva dan juga setelah menjadi udang muda (juvenile), selain memakan makan
tersebut udang muda juga memakan diatomae dan cyanophyceae yang tumbuh
didasar perairan, anak tiram, anak teritip, anak udang-udangan, cacing annelida dan
juga detritus (sisa hewan dan tumbuhan yang membusuk di dasar perairan).
Sedangkan pada udang yang telah mencapai ukuran dewasa memakan berbagai
daging hewan lunak seperti Mollusca (kerang, tiram, siput), cacing annelida,
udang-udangan, anak-anak seranga dan sebagainya. Udang yang dipelihara ditambak
memakan makanan alami yang tumbuh ditambak seperti plankton,klekap, lumut dan
2.1.2.Habitat
Udang pada umumnya bersifat bentik, yaitu hidup dipermukaan dasar
perairan.Kondisi habitat laut yang disukai adalah dasar perairan laut yang lumer (saft)
yang biasanya terdiri dari campuran lumpur dan pasir.Perairan berbentuk teluk
dengan aliran sungai yang besar merupakan habitat yang baik bagi udang. Sedangkan
khusus untuk udang windu lebih menyukai kondisi tekstur dasar perairan lempung
berdebu atau lumpur pasir (M.Ghufran, 2010)
Udang windu pada perkembangannya mempunyai beberapa bentuk stadia
yaitu stadia nauplius (enam substadia), stadia zoea (tiga sub stadia), stadia mysis (tiga
sub stadia), stadia pasca larva dan stadia dewasa (Villaluz et al, yang dikutif
M.Ghufran, 2010)..
Selama daur hidupnya udang windu mempunyai pase hidup dilaut dan pase
hidup diperairan muara sungai dan pantai.Udang berada dilaut pada stadia menuju
dewasa, telur, nauplius, zoea, mysis dan pasca larva.Stadia awal pasca larva yang
bersifat planktonic terbawa arua kepase hidup perairan muara sungai dan pantai,
selanjutnya mengalami perkembangan pasca larva yang bersifatbentik di dasar
perairan hingga juvenile (M.Ghufran, 2010).
Udang pada umumnya bersifat omnivora, juga pemakan detritus dan sisa –sisa
bahan organik lainnya baik hewani maupun nabati.Dari kenyataan bahwa udang
mempunyai pergerakan yang hanya terbatas dalam mencari makanan, tampaknya
udang mempunyai sifat yang dapat menyesuaikan diri dengan makanan yang tersedia
dilingkungannya dan tidak bersifat terlalu memilih-milih (M.Ghufran, 2010).
Pada tingkat mysis, makanan udang windu terdiri dari campuran diatomae,
zooplankton yang terdiri dari Trochopora, Calanus, Veliger, Copepoda dan Larva
dewasa udang sering memakan molusca kecil (seperti kerang, tiram dan
siput),Crustaceae, cacing dan anak serangga (Mujiman dan Suyanto, 1989).
2.1.3.Komposisi Nilai Gizi
Komposisi daging udang sangat berpariasi, tergantung pada jenis, tingkat umur,
musim, habitat dan pakan tersebut. Menurut Chanmugan et.el, 1983, jumlah
kandungan lemak udang laut tidak berbeda nyata dengan udang dari air tawar, yaitu
1,0 – 1,1 gram dalam 100 gram daging, sedangkan kadar kolesterol dapat mencapai
125 mg pada 100 gram daging yang dapat dimakan (Mahmud dan Hermana, 1987).
Disamping kadar proteinnya yang tinggi, udang juga mempunyai kandungan
asam amino yang lengkap baik asam amino essensial maupun non essensial. Udang
merupakan hasil perikanan yang mempunyai nilai ekonomis yang tinggi.Komposisi
kimia dari jenis udang sangat penting artinya, dilihat dari segi manfaatnya sangat
memenuhi kebutuhan gizi manusia seperti kandungan protein, vitamin dan mineral
lainnya (Hadiwiyoto, 1993.
Komposisi kimia dan nilai gizi daging udang windu selengkapnya tersaji pada
Tabel 2.1.Komposisi kimia dan nilai gizi daging udang windu (penaeus spp)
Kalsium 145-320 mili gram/gram
Magnesium 40-105 milli gram/gram
Fosfor 170-250 mili gram/gram
Besi 1,6 mili gram/gram
Natrium 140 mili gram/gram
Kalium 220 mili gram/gram
Senyawa nitrogen non
Protein 0,80 %
Sumber : J.A. Shelf and J.M. Jay, 1971 (dalam Hadiwiyoto, 1993)
2.1.4.Pakan Udang Windu
Pakan yang baik dan sesuai akan memacu pertumbuhan udang windu dan
menghasilkan udang windu yang sehat. Pakan merupakan bagian yang penting dalam
agribisnis udang windu karena menempati 40-50 % dari total biaya produksi yang
dikeluarkan. Pakan yang lengkap mempunyai kandungan protein, karbohidrat, lemak
dan mineral yang diperlukan untuk pertumbuhan dan kesehatan udang windu.
(M.Ghufran,2010). Pakan terdiri atas pakan alami dan pakan buatan.Pakan alami
udang windu banyak terdapat didalam tambak.Yang tergolong pakan alami adalah
plankton dan bentos, sedangkan pakan buatan adalah pakan tambahan yang bibuat
Dalam budi daya udang, pakan merupakan salah satu faktor penting dalam
menentukan keberhasilan usaha.Karena itu pengelolaan pakan, yang terdiri atas
pemilihan jenis pakan, penyimpanan, pemberian dan sebagainya harus dilakukan
sesuai dengan kebutuhan udang budi daya dan target produksi.
2,1.4.1.Pakan Alami
Keberhasilan agribisnis udang windu ditentukan oleh tersedianya pakan yang
memadai, baik kuantitas maupun kualitasnya.Pakan merupakan unsur utama dalam
pertumbuhan udang.Penyediaan pakan sering menjadi kendala karena harganya yang
tinggi, serta biaya pembuatannya yang cukup mahal.
Keberadan plankton dalam media pemeliharaan udang, khususnya
phytoplankton yang menguntungkan, sangat dibutuhkan baik dari keanekaragaman
maupun melimpahnya pakan.Fungsi plankton pada media pemeliharaan, diantaranya
sebagai pakan alami untuk pertumbuhan organisme yang dipelihara, penyangga atau
buffer intensitas cahaya matahari dan bioindikator kestabilan lingkungan media
pemeliharaan.
2.1.4.2.Pakan Buatan
Dalam budi daya udang, ketersediaan pakan buatan berkualitas dan secara kontinu
adalah hal yang penting.Pakan buatan adalah pakan yang diramu dari bahan-bahan
sesuai dengan kebutuhan udang budi daya.Pakan buatan dapat diperoleh dari toko
atau diproduksi sendiri.Pakan buatan harus memenuhi standar kebutuhan nutrisi
udang budi daya. Apabila pakan yang diberikan kepada udang peliharaan mempunyai
kandungan nutrisi yang cukup tinggi, maka hal ini tidak saja akan menjamin hidup
dan aktifitas udang, tetapi juga akan mempercepat pertumbuhannya.
Udang yang kekurangan gizi juga merupakan sumber dan penyebab penyakit.
Pakan yang kandungan proteinnya rendah atau tidak sesuai dengan kebutuhan akan
dapat menyebabkan udang menjadi mudah terserang penyakit.Selain kandungan
nutrisinya lengkap, dalam artian seluruh zat gizi telah dikandung oleh pakan,
komposisi pakan juga harus berimbang. Menurut M.Ghufran ,beberapa komponen
nutrisi yang penting dan harus tersedia dalam pakan udang antara lain : protein,
lemak, karbohidrat, vitamin dan mineral.
1.Protein
Protein sangat penting bagi tubuh karena zat ini mempunyai fungsi sebagai
bahan-bahan dalam tubuh serta sebagai zat pembangun, zat pengatur dan zat
pembakar.Sebagai zat pembangun, protein berfungsi membentuk berbagai jaringan
baru untuk pertumbuhan, mengganti jaringan yang rusak, maupun yang bereproduksi.
Sedangkan sebagai zat pengatur, protein berperan dalam pembentukan enzim dan
hormon penjaga dan pengatur berbagai proses metabolisme didalam tubuh udang.
Dan sebagai zat pembakar, adalah karena unsur karbon yang terkandung didalamnya
dapat difungsikan sebagai sumber energi pada saat kebutuhan energi tidak terpenuhi
oleh karbohidrat dan lemak.
2.Lemak
Lemak berfungsi sebagai sumber energi yang paling besar diantara protein dan
karbohidrat.Pada udang, asam lemak mempunyai peranan penting baik sebagai
sumber energi maupun sebagai zat yang essensial untuk udang. Satu gram lemak
dapat menghasilkan 9 kkal per gram, sedangkan karbohidrat dan protein hanya
menghasilkan 4 kkal per gram. Lemak juga menjadi sumber asam lemak , posfolipid,
kolesterol dan sebagai pelarut pada proses penyerapan vitamin A, D, E, K. selain itu ,
lemak juga berfungsi membantu proses metabolisme, osmoregulasi dan menjaga
keseimbangan organisme dalam air serta untuk memelihara bentuk dan fungsi
membran atau jaringan. Kelebihan lemak dapat disimpan sebagai cadangan energi
dalam jangka panjang selama melakukan aktifitas atau selama periode tanpa
Lemak mengandung asam lemak yang diklasifikasikan sebagai asam lemak
jenuh dan asam lemak tak jenuh. Asam lemak tak jenuh ditandai dengan adanya
ikatan rangkap atau rantai jamak (polyunsaturated fatty acid = PUFA) yang lebih
banyak seri omega-3 dari pada seri omega-6 nya. Asam lemak jenuh ditandai dengan
tidak adanya ikatan rangkap. Sebagaimana pada protein yang telah diketahui adanya
asam amino non essensial, pada lemakpun terdapat asam amino essensial, seperti
pada linoleat, linolenat, eikosapentaenoat /EPA, decosaheksaenoat /DHA dan asam
arakidonat yang merupakan asam lemak penting untuk pertumbuhan dan
kelangsungan hidup udang.
3.Karbohidrat
Karbohidrat merupakan senyawa organik yang terdiri atas serat kasar dan bahan
bebas tanpa nitrogen. Unsur-unsur karbohidrat terdiri atas : karbon, hydrogen, dan
oksigen dalam perbandingan yang berbeda-beda. Karbohidrat dalam bentuk yang
sederhana umumnya lebih mudah larut dalam air dari pada lemak dan protein.
Pada pakan udang, dasar perhitungan penggunaan energi masih sulit
dilakukan. Hal ini disebabkan udang mempunyai system pencernaan yang masih
sederhana. Pada hewan lain terdapat organ hati dan pankreas. Pada udang windu
(penaeus monodon) umur diatar 3 bulan perlu waktu sekitar 2 jam 30 menit untuk
proses mencerna. Ini mulai proses pakan masuk ke mulut sampai menjadi tinja.
4.Vitamin
Vitamin adalah zat organik yang diperlukan tubuh udang dalam jumlah yang sedikit,
tetapi sangat penting untuk mempertahankan pertumbuhan dan pemeliharaan kondisi
tubuh. Pada umumnya vitamin tidak dapat disintesis dalam tubuh udang sehingga
harus tersedia dalam pakan. Ditinjau dari sifat-sifat fisiknya, vitamin dibagi kedalam
dua golongan, yaitu vitamin yang larut dalam air dan vitamin yang larut dalam
(B2), asam pentotenat (B6), biotin dan kobalamin (B12), vitamin C dan lain-lain.
Sedangkan vitamin yang larut dalam lemak antara lain retinola (vitamin A),
kolekalsiferol atau elgoklasiferol (vitamin), alfa tokoferol (vitamin E) dan menadion
(vitamin K).
Fungsi utama vitamin secara umum adalah :
1) Sebagai bagian dari enzim atau ko-enzim sehingga dapat mengatur berbagai
proses metabolism.
2) Mempertahankan fungsi berbagai jaringan tubuh
3) Mempengaruhi pertumbuhan dan pembentukan sel-sel baru
4) Membantu dalam pembuatan zat-zat tertentu dalam tubuh.
5.Mineral
Mineral merupakan bahan anorganik yang dibutuhkan udang dan ikan dalam jumlah
yang sedikit, tetapi mempunyai fungsi yang sangat penting. Beberapa proses didalam
tubuh memerlukan zat-zat mineral. Fungsi utama mineral adalah sebagai komponen
utama dalam struktur gigi dan tulang eksoskeleton, menjaga keseimbangan asam
basa, menjaga keseimbangan tekanan osmosis dengan lingkungan perairan, struktur
dari jaringan dan sebagai penerus dalam system syaraf dan kontraksi otot, fungsi
metabolisme, sebagai komponen utama dari enzim, vitamin, hormone, pigmen, dan
sebagai enzim aktivator.
Menurut fungsinya, mineral dibagi menjadi 3 kelompok besar yaitu fungsi
struktural, pernapasan dan metabolisme umum. Fungsi struktural adalah fungsi
mineral untuk pembentukan struktur tubuh seperti tulang, gigi dan sisik untuk ikan.
Mineral yang paling banyak berperan dalam fungsi ini adalah Ca, P, F, dan Mg. yang
membantu pernapasan adalah Fe, Cu, dan Co. sedangkan mineral yang membentu
proses metabolism adalah semua mineral essensial baik makro maupun mikro,
keseimbangan cairan tubuh dan beberapa fungsi lainnya. Kekurangan mineral dapat
berpengaruh pada pertumbuhan.
2.2. Minyak dan Lemak
Minyak dan lemak termasuk salah satu dari anggota golongan lipid yaitu merupakan
lipida netral. Lipida itu sendiri dapat di klasifikasikan menjadi 4 kelas yaitu : lipid
netral, fosfolipida, sfingolipid dan glikolipid. Semua jenis lipid ini banyak terdapat di
alam. Minyak dan lemak telah dipisahkan dari jaringan asalnya mengandung
sejumlah komponen selain trigliserida yaitu : lipid kompleks (lesitin, cephalin,
fosfatida lainnya serta glikolipid), sterol berada dalam keadaan bebas atau terikat
dengan asam lemak, asam lemak bebas, lilin, pigmen yang larut dalam lemak dan
hidrokarbon. Minyak merupakan trigliserida yang berwujud cairan pada suhu kamar
dan umumnya diperoleh dari sumber nabati.Sedangkan lemak merupakan trigliserida
yang pada suhu kamar berwujud padatan dan pada umumnya berasal dari hewani.
Minyak dan lemak adalah merupakan trigliserida yang merupakan bagian
terbesar dari kelompok lipida. Pembentukan trigliserida dihasilkan dari proses
esterifikasi satu molekul gliserol dengan tiga molekul asam lemak dapat sama atau
berbeda ( Gambar :2.1 ), membentuk satu molekul trigliserida dan tiga molekul air.
+ + 3H2O
Gliserol Asam Lemak Trigliserida Air
Gambar :2.1. Reaksi pembentukan terigliserida dari gliserol dan asam lemak. Jika R1 = R2 = R3, maka trigliserida yang terbentuk adalah trigliserida
gliserol hanya mengikat satu molekul asam lemak maka hasilnya disebut
monogliserida dan apabila dua molekul asam lemak disebut digliserida.
Modifikasii dari lemak dapat dilakukan dengan mengubah komposisi dari
pada asam lemak sebagai trigliserida untuk membentuk lemak baru misalnya lemak
dengan titik lebur yang tinggi atau titik lebur yang rendah.
Menurut Lehnigerlipid diklasifikasikan atas 2 kelompok, yaitu :
1. Lipid kompleks (yang bias mengalami safonifikasi) contoh: trigliserida.
2. Lipid sederhana (yang tidak bisa mengalami safonifikasi karena tidak mengandung
gliserol).
Sedangkan menurut Bloor, lipid diklasifikasikan atas 3 kelompok, yaitu :
1. Lipid sederhana : ester asam lemak dengan berbagai alkohol.
a.Lemak : ester asam lemak dengan gliserol
b.Malam/ Wax : ester asam lemak dengan alkohol mono hidrad berat molekul
tinggi.
2. Lipid komplek : ester asam lemak yang mengandung gugus lain disamping alkohol
dan asam lemak.
a.Fosfolipid : mengandung residu asam fospat, contoh gliserofosfolipid, sfingosin.
b.Glukolipid : mengandung karbohidrat, contoh sfingosin,
c. Lipid komplek lainnya, contoh : Sulfolipid, amino lipid, lipoprotein.
3. Derivat lipid / precursor lipid.
Bentuk ini mencakup asam lemak, gliserol, aldehid lemak, benda-benda keton,
vitamin larut lemak dan hormon..
Lemak atau lipid adalah senyawa organik berminyak atau berlemak yang
tidak larut dalam air, dapat diekstrak dari sel atau jaringan oleh pelarut non polar,
seperti kloroform, eter atau n-heksan. Jenis lipid yang paling banyak adalah lemak
Lemak didefinisikan sebagai komponen makanan yang tidak larut dalam
pelarut organik. Defenisi lain dari lemak adalah suatu molekul yang disintesis oleh
system biologis yang memiliki rantai alifatik hidrokarbon yang panjang sebagai
struktur utamanya, dapat bercabang atau tidak bercabang dapat membentuk cincin
karboksilat yang dapat mengandung rantai tak jenuh. yang paling tinggi
menghasilkan 9 kkal untuk tiap gramnya, yaitu 2,5 kali energi yang dihasilkan oleh
karbohidrat dan protein dalam jumlah yang sama (Almatsier 2000). Satu molekul
lemak tersusun atas satu hingga tiga asam lemak dan satu gliserol.Gliserol adalah
alkohol terhidrat, yaitu mempunyai tiga gugus hidroksil.
Asam lemak dibedakan menjadi asam lemak jenuh dan asam lemak tak jenuh.
Asam lemak jenuh memiliki titik cair lebih tinggi dari pada asam lemak tak jenuh dan
merupakan dasar dalam menentukansifat fisik lemak dan minyak. Lemak yang
tersusun oleh asam lemak tak jenuh akan bersifat cair pada suhu kamar, sedangkan
lemak yang tersusun oleh asam lemak jenuh akan berbentuk padat. Asam lemak tak
jenuh yang mengandung satu ikatan rangkap disebut asam lemak tak jenuh tunggal
(monounsaturated fatty acid /MUPA).Asam lemak yang mengandung dua atau lebih
ikatan rangkap disebut asam lemak tak jenuh majemuk (polyunsaturated fatty acid /
PUFA). (. Muchtadi et al.1993). semakin panjang rantai karbon dan semakin banyak
jumlah ikatan rangkapnya , maka semakin besar kecendrungan untuk menurunkan
kadar kolesterol dalam darah.
2.3.Pengaruh lingkungan Terhadap Kandungan Lemak Ikan
Komposisi lemak dan asam lemak pada ikan sangat bervariasi, banyak faktor yang
mempengaruhi kandungan lemak pada ikan,yaitu sfesies ikan, jenis kelamin, ukuran,
tingkat kematangan atau umur, siklus bertelur, lokasi geografis, jenis makanan dan
musim.
Komposisi lemak ikanlaut lebih kompleks bila dibandingkan dengan lemak
ikan air tawar. Hal ini terlihat dari kandungan asam lemak ikan laut yang lebih
banyak. Asam lemak tidak jenuh tidak jenuh berantai panjang pada lemak ikan laut
terdiri dari asam lemak rantai C18, C20 dan C22. Biasanya kandungan asam lemak C20
dan C22 lebih banyak dari pada C16 dan C18 (Herold dan Kinsella, 1986).sedangkan
hasil penelitian Nair dan Gopakumar (1978), menunjukkan bahwa ikan iar tawar
mengandung asam lemak C16 dan C18 lebih tinggi dari pada asam lemak C20 dan C22.
Perbedaan ini lebih disebabkan oleh komposisi jenis lemak yang dikonsumsi dari
lingkungan tempat hidupnya.
Hasil penelitian Suwerya (1993) menunjukkan bahwa kelompok asam lemak
linoleat (n=6) dan asam lemak omega 3 penting peranannya bagi pertumbuhan udang
windu. Pakan buatan yang baik untuk udang windu yang dibudi dayakan adalah
mengandung 1,75 % asam lemak omega-6 dan 1,86 % asam lemak omega-3. Asam –
asam lemak essensial yang banyak dibutuhkan udang windu adalah asam linoleat,
asam linolenat, EPA, dan DHA.Asam-asam lemak tersebut hanya dapat dipenuhi dari
pakannya saja.
2.4.Ester Asam Lemak
Ester asam lemak dialam terdapat dalam bentuk ester antara gliserol dengan
asam lemak ataupun dengan phospat seperti phospholipid. Ester asam lemak sering
dimodifikasi baik untuk bahan makanan maupun untuk surfaktan, aditif, detergen
danlain sebagainya (Endo, dkk, 1997). Senyawa ester dapat dibentuk dengan
beberapa cara, yaitu :
c. Alkoholisis
Ketiga reaksi yang terahir diatas dikelompokkan menjadi reaksi trans
esterifikasi (Gandhi, 1997).
Esterifikasi adalah suatu reaksi ionic yang merupakan reaksi addisi dan reaksi
penataan ulang eleminasi (Davidek, 1990).
ester
Esterifikasi juga dapat didefinisikan sebagai reaksi antara asam karboksilat
dan alkohol (Gandhi, 1997).Esterifikasi dapat di lakukan dengan menggunakan
katalis enzim (lipase) dan asam anorganik (asam sulfat dan asam klorida) dengan
berbagai variasi alkohol, biasanya methanol, etanol, 1-propanol dan lain sebagainya.
Jika dianggap oksigen dari karbonil yang diprotonasi maka mekanisme
+ H2O
Interesterifikasi merupakan reaksi pertukaran atau penataan ulang
(rearrangement) gugus asil antara dua buah ester. Interesterifikasi lemak sudah
menjadi perhatian pada saat ini untuk dapat menggantikan proses hidrogenasi lemak
oleh karena pada proses ini dapat terbentuk lemaktrans yang dapat membahayakan
kesehatan. Pada minyak atau lemak jika reaksi pertukaran gugus asil berlangsung
antara molekul trigliserida yang berbeda disebut sebagai intererterifikasi.
Interesterifikasi menyebabkan penataan ulang atau randomisasi residu asil
melalui pertukaran grup asil diantara ester-ester dalam trigliserol dan menghasilkan
lemak atau minyak dengan sifat-sifat baru.
Interesterifikasi dapat terjadi dengan batuan katalis kimia atau denganadanya
biokatalis enzim. Selama interesterifikasi akan terjadi redistribusi yang mengubah
komposisi asam lemak dalam trigliserol sehingga mempunyai karakter fisik minyak
dan lemak, seperti sifat pelelehan dan kristalisasi (Hilda, 2010).
Interesterifikasi memanfaatkan pengaruh suhu terhadap titik leleh komponen,
sehingga mengahsilkan reaksi pembentukan kembali komponen lemak untuk
mencapai kestabilan pada strukturnya.Reaksi interesterifikasi dapat disebabkan oleh
beberapa reaksi, yaitu reaksi alkoholisis, asidolisis, dan transesterifikasi (Gupta,
2.5.Kromatografi Gas – Spektrometri Massa (GC-MS)
GC-MS adalah metoda analisa dimana sampel dipisahkan secara fisik menjadi bentuk
molekul-molekul yang lebih kecil (hasil pemisahan dapat dilihat pada kromatogram).
Sedangkan spektroskopi massa adalah metode analisis dimana sampel yang dianalisis
akan diubah menjadi ion-ion gas dan ion-ion tersebut dapat diukur berdasarkan hasil
deteksi berupa spektrum massa.
Pada GC hanya terjadi pemisahan untuk mendapatkan komponen yang
diinginkan sedangkan bila dilengkapi dengan MS (berfungsi sebagai detektor) akan
dapat mengidentifikasi komponen tersebut karena bisa membaca spektrum bobot
molekul pada suatu komponen karena dilengkapi refrensi yang ada pada software,
secara instrument MS adalah detektor GC.
Pemisahan komponen senyawa dalam GC terjadi dalam kolom (kapiler)
dengan melibatkan dua fasa yaitu fasa diam dan fasa gerak. Fasa diam adalah zat
yang ada dalam kapiler, sedangkan fasa gerak adalah gas pembawa (He atau H2)
dengan kemurnian tinggi yaitu 99,95%. Proses pemisahan dapat terjadi karena
kecepatan alir dari tiap molekul dalam kolom. Perbedaan tersebut disebabkan oleh
perbedan affinitas antar molekul dengan fasa diam yang ada dalam kolom.
Spektrometer massa menembaki bahan yang sedang diteliti dengan berkas
elektron dan secara kuantitatif mencatat hasilnya sebagai suatu spektrum fragmen ion
positif.
Catatan ini disebut spektrum massa. Terpisahnya fragmen-fragmen ion positif
didasarkan pada massanya.
2.4.1.Kromatografi Gas
Kromatografi gas adalah metode kromatografi pertama yang dikembangkan
pada zaman instrument dan elektrokimia yang telah merefolusikan keilmuan selama
lebih dari tiga puluh tahun.
Kromatografi gas dapat dipakai untuk setiap campuran yang setiap campuran
yang sebagian komponennya atau akan lebih baik lagi jika semua komponennya
Tekanan uap atau keatsirian akan memungkinkan komponen menguap dan bergerak
bersama-sama dengan fase gerak yang berupa gas. Waktu yang diperlukan untuk
memisahkan campuran sangat beragam, tergantung banyaknya komponen dalam
suatu campuran, semakin banyak komponen yang terdapat dalam campuran maka
waktu yang diperlukan semakin lama.Komponen campuran dapat diidentifikasi
berdasarkan waktu tambat (waktu retensi) yang khas pada kondisi yang tepat. Waktu
tambat adalah waktu yang menunjukkan berapa lama suatu senyawa tertahan dalam
kolom.
a.Memilih Sistem
Dalam kromatografi gas terdapat empat peubah utama yaitu gas pembawa, jenis
kolom dan fase diam dan suhu untuk pemisahan.
Gas Pembawa.Faktor yang mempengaruhi suatu senyawa bergerak melalui kolom kromatografi gas ialah keatsirian yang merupakan sifat senyawa itu dan aliran gas
melalui kolom. Nitrogen, helium,argon, hydrogen dan karbon dioksida merupakan
gas yang sering digunakan sebagai gas pembawa karena tidak reaktif serta dapat
dibeli dalam keadaan murni dan kering dalam tangki bervolume besar dan bertekanan
tinggi.
Detektor. Detektor pilihan pertama untuk kromatografi gas adalah Detector Ionisasi Nyala (DIN) yang memiliki kepekaan yang tinggi untuk beberapa jenis senyawa.
Fase Cair Diam. Dua segi fase harus diketahui, pertama bagaimana cairan ditahan dalam kolom yaitu cairan itu disaputkan pada permukaan serbuk padat dalam kolam,
dan yang kedua yaitu sifat kimia dari cairan itu.
b.Sistem
Suhu Kolom. Kromatografi gas didasarkan pada dua sifat senyawa yang dipisahkan, kelarutan senyawa itu dalam cairan tertentu dan tekanan uapnya atau keatsiriannya.
Karena tekanan uap bergantung langsung pada suhu, maka suhu merupakan faktor
utama dalam kromatografi gas. Suhu kolom berkisar – 100oC-4000C tergantung sifat
patokan dapat dipakai bahwa setiap kenaikan suhu 30oC waktu tambat menjadi
setengahnya.
Gas Pembawa.Laju aliran gas tergantung pada diameter kolom.Aliran berbanding lurus dengan penampang kolom dan penampang bergantung jari-jari pangkat dua
(��2). Misalnya jika pemisahan yang baik dengan kolom 2 mm pada aliran 20
ml/menit, maka untuk menghasilkan hasil yang sama dengan kolom 4 mm diperlukan
aliran 80 ml/menit. Untuk mendapatkan system kolom yang optimal yaitu dengan
cara mengatur laju aliran gas dan menghasilkan tingkat puncak yang maksimum.
Kolom.Ada dua kolom dalam kromatografi gas yaitu : kolom kemas, terdiri atas fase cair berdiameter 1-3 mm dan panjangnya 2 m, kolom kapiler : berdiameter 0,02- 0,2
mm dan panjangnya 15-25 m, yang berfungsi sebagai penyangga lembam untuk fase
diam cair.
Detector.Detector adalah gawai yang ditempatkan pada ujung kolom kromatografi gas yang menganalisis aliran gas yang keluar dan memberikan data kepada perekam
data yang menyajikan hasil kromatogram secara grafis.
DHB (Detector Hantar Bahang) : didasarkan pada bahang dipindahkan dari
benda panas dengan laju yang bergantung pada susunan gas yang mengelilingi benda
panas. Daya hantar ini merupakan fungsi dari laju pergerakan molekul gas.Gas yang
mempunyai bobot molekul yang rendah mempunyai daya hantar paling tinggi.
Detector Ionisasi Nyala (DIN), pendeteksian DIN ialah jika dibakar, senyawa
organik terurai membentuk pecahan sederhana bermuatan positif, biasanya trediri atas
satu karbon. Pecahan ini meninggikan daya hantar tempat lingkungan nyala, dan
peningkatan daya hantar ini dapat diukur dengan mudah dan direkam.
Penanganan Sinyal
Data Kualitatif.Data kromatografi gas biasanya terdiri atas waktu tambat berbagai komponen campuran.Waktu tambat diukur mulai dari titik penyuntikan sampai ketitik
maksimum puncak dan sangat khas untuk senyawa tertentu dan pada kondisi tertentu.
tersedia senyawa murninya. Senyawa murni ditambahkan kedalam cuplikan yang
diduga mengandung senyawa itu dan cuplikan kromatografi.
Data Kuantitatif.Pengukuran sebenarnya yang dilakukan pada kertas grafik ialah pengukuran luas puncak.Jika puncak itu simetris atau berupa kurva gauss tinggi
puncak dapat dipakai untuk mengukur luas puncak.
2.4.2.Spektrum Massa
Spektrum massa biasa diambil pada energi berkas elektron sebesar 70 elektron volt.
Kejadian tersederhana ialah tercampaknya satu elektron dari satu molekul dalam fase
gas oleh sebuah elektron dalam berkas elektron dan membentuk suatu ion molekul
yang merupakan suatu kation radikal (M+).
Suatu spektrum massa menyatakan massa-massa sibir-sibir bermuatan positif
terhadap (konsentrasi) nisbinya. Puncak paling kuat (tinggi) pada spektrum disebut
puncak dasar (base peak), dinyatakan dengan nilai 100 % dan kekuatan (tinggi x
factor kepekaan) puncak-puncak lain, termasuk puncak ion molekulnya, dinyatakan
sebagai persentase puncak dasar tersebut.
Puncak ion molekul biasanya merupakan puncak-puncak dengan bilangan
massa tertinggi, kecuali jika terdapat puncak-puncak isotop. Puncak-puncak
isotopnya yang biasa.
a.Penentuan Rumus Molekul
Penentuan rumus molekul yang mungkin dari kekuatan puncak isotop hanya dapat
dilakukan jika puncak ion olekul termaksud cukup kuat hingga puncak tersebut dapat
diukur dengan cermat sekali.
Misalnya suatu senyawa mengandung satu atom karbon, maka untuk tiap 100
molekul yang mengandung satu atom 12C, sekitar 1,08 % molekul mengandung satu
atom 13C. Karenanya molekul-molekul ini akan menghasilkan sebuah puncak M + 1
yang besarnya 1,08 % kuat puncak ion molekulnya, sedangkan atom-atom 2H yang
akan memberikan sumbangan tambahan yang amat lemah pada puncak M + 1 itu.
Jika suatu senyawa mengandung sebuah atom sulfur, puncak M + 2 akan menjadi 4,4
b.Pengenalan Puncak Ion Molekul
Ada dua hal yang menyulitkan pengidentifikasian puncak ion molekul yaitu :
1. Ion molekul tidak nampak atau amat lemah. Cara penanggulanganya adalah
mengambil spektrum pada kepekaan maksimum, jika belum diketahui dengan jelas
dapat juga dilihat berdasarkan pola pecahnya.
2. Ion molekul nampak tetapi cukup membingungkan karena terdapatnya beberapa
puncak yang sama atau lebih menonjol. Dalam keadaan demikian, pertama-tama
soal kemurnian harus dipertanyakan. Jika senyawa memang sudah murni, masalah
yang lajim ialah membedakan puncak ion molekul dari puncak M-1 yang lebih
menonjol. Satu cara yang bagus ialah dengan mengurang energi berkas elektron
penembak mendekati puncak penampilan.
Kuat puncak ion molekul tergantung pada kemantapan ion molekul.Ion-ion
molekul paling mantap adalah dari sisten aromatik murni. Secara umum golongan
senyawa-senyawa berikut ini akan memberikan puncak –puncak ion menonjol :
senyawa aromatik, (alkane terkonjugasi), senyawa lingkar sulfida organik (alkane
normal, pendek), merkaptan. Ion molekul biasanya tidak nampak pada alkohol
alifatik, nitrit, nitrat, senyawa nitro, nitril dan pada senyawa-senyawa
bercabang.Puncak-puncak dalam arah M-3 sampai M-14 menunjukkan
kemungkinan adanya kontaminasi (Silverstein, dkk, 1981).
a. Kaidah Umum untuk Mengenali Puncak-Puncak dalam Spektra
Sejumlah kaidah umum untuk mengenali puncak-puncak menonjol dalam spektra
dampak elektron dapat ditulis dan dipahami dengan konsep-konsep buku kimia
organikfisik :
1. Tinggi nisbi puncak ion molekul terbesar bagi senyawa rantai lurus dan akan
menurun jika derajat percabangan bertambah.
2. Tinggi nisbi puncak ion molekul biasanya makin kecil dengan bertambahnya
bobot molekul deret homolog, kecuali untuk ester lemak.
3. Pemecahan/ pemutusan cenderung terjadi pada karbon terganti gugus alkil :
mantapnya karboksasi tersier dari pada sekunder yang lebih mantap dari pada
yang primer.
4. Adanya ikatan rangkap, stuktur lingkar dan terlebih-lebih cincin aromatik
(heteroatom) memantapkan ion molekul hingga meningkatkan pembentukannya.
5. Ikatan rangkap mendukung pemecahan alil dan menghasilkan ion karbonion alil.
6. Cincin jenuh cenderung melepas rantai samping pada ikatan-α. Hal ini tidak lain
dari pada kejadian khusus percabangan. Muatan positif cenderung menyertai
sibir cincin. Cincin tak jenuh dapat mengalami reaksi Retro-Diels-Alder.
7. Dalam senyawa aromatik terganti gugus alkil, pemecahan paling mungkin terjadi
pada ikatan beta terhadap cincin menghasilkan ion benzyl taluunan termantapkan
atau iontropilium.
8. Ikatan C-C yang bersebelahan dengan heteroatom cenderung terpecah,
meninggalkan muatan pada sibiran yang mengandung heteroatom yang elektron
tak-ikatannya menciptakan kemantapan talunan.
9. Pemecahan sering berkaitan dengan penyingkiran molekul netral mantap yang
kecil, misalnya karbon monoksida, olefin, ammonia, hydrogen sulfida, hydrogen
sianida, merkaptan, ketene, atau alkohol. (Silverstein,dkk, 1981).
Kaidah-kaidah penyibiran diatas berlaku untuk spektrometri Dampak Elektron
(DE).
2.4.3.Spektra Massa Beberapa Golongan Senyawa Kimia a.Hidrokarbon.
Hidrokarbon Jenuh.Puncak ion molekul (M) hidrokarbon jenuh berantai lurus selalu ada kendati puncaknya rendah untuk senyawa-senyawa rantai panjang. Pola
penyibiran (fragmentasi) ditandai oleh kumpulan atau kluster puncak dan puncak
yang bersangkutan pada tiap kluster terpisah oleh 14 (CH2) satuan massa. Puncak
terbesar pada tiap kluster ini mewakili sibiran CnH2n+1 ; disertai juga sibiran CnH2n
dan CnH2n-1. Sibiran terbanyak terdapat pada daerah C3 dan C4 dan kelimpahan sibiran
itu menurun teratur sampai M-C2H5 ; puncak M-CH3 biasanya lenyap sama sekali.
molekul dan mendukung pemecahan ikatan yang menghubungkan cincin dengan
bagian molekul lainnya. Penyibiran atas cincin biasanya oleh lepasnya dua atom
sebagai C2H4 dan C2H5.
b.Eter
Eter Alifatik. Penyibiran eter alifatik berlangsung dengan 2 cara :
1. Pemutusan ikatan C-C bersebelahan atom oksigen :
RCH2-CH2-CH-O+-CH2-CH3 RCH2CH2CH=O+-CH2-CH3
2. Pemutusan ikatan C-O dengan muatan tetap berada pada sibir alkil,
R – O+ - R’ R+
c.Ester
Pola fragmentasi pada senyawa ester terdapat pada pemutusan ke karbon karbonil.
Hilangnya gugus alkoksi adalah yang paling penting dari fragmentasi ini, seperti yang
Gambar :2.2. Fragmentasi senyawa golongan ester
Penataan ulang Mc Lafferti dapat berlangsung untuk ester di bagian alkil. Lihat
gambar :2.3
BAB 3
METODE PENELITIAN
3.1.Tempat Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Organik Bahan Alam, Fakultas
Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara dan uji analisis
asam lemak dilakukan di Laboratorium Kimia Organik Universitas Gajah Mada
Yokyakarta.
3.2. Bahan-bahan
Bahan yang digunakan adalah udang windu yang diambil secara acak dari Tempat
Pelelangan Ikan di Daerah Percut Sei Tuan, Deli Serdang, n-Heksana, Metanol,
LarutanNaCl jenuh, BF3 – Metanol 14%, Larutan NaOH 0,5 N dalam metanol, gas
Helium.
3.3. Peralatan
Peralatan yang digunakan dalam penelitian ini meliputi : toples kaca, erlenmeyer,
neraca analitik, desikator, blender, beaker gelas, rotari evaporator, corong kaca, kertas
saring, pipet tetes, water bath, botol vial, GC-MS, thermometer, kertas whatman 42.
Gas Chromatography – Mass Spectroscopy (GC-MS) model Shimadzu QP 2010 pada
kondisi sebagai berikut :
Temperature oven kolom 80 oC, temperature injeksi 310 oC, tekanan 16,5 kPa, total
aliran 40,0 mL/ menit, aliran kolom 0,50 mL/ menit dan kecepatan aliran 26,1 cm/
detik.
3.4.Rancangan Penelitian
1. Mengambil udang windu secara acak dari hasil tangkapan nelayan di tempat
pelelangan ikan bagan Percut Sei Tuan, serta dari tambak udang yang terdapat di
daerah Percut Sei Tuan sebagai sampel.
2. Udang windu dibersihkan kulitnya
3. Daging udang windu dihaluskan dengan menggunakan blender
4. Mengeringkan daging udang windu dengan menggunakan sinar matahari sampai
tampak kering
5. Daging udang windu setelah kering karna berbentuk lembaran, maka dihaluskan
lagi dengan menggunakan blender.
6. 200 gram daging udang windu dimaserasi dengan pelarut n-heksan selama 3 hari.
7. Menyaring hasil maserasi dengan mengambil filtratnya/ ekstraknya yang
berwarna kuning keemasan.
8. Ekstrtrak hasil maserasi diuapkan pelarutnya menggunakan rotary evaporator.
9. Ekstrak pekat hasil rotary evaporator dimasukkan dalam gelas vial, selanjutnya
diuapkan lari pelarut yang masih terkandung dengan menggunakan waterbath.
10. Lemak yang diperoleh ditimbang dengan neraca analitik.
3.4.2.Tahap Metanolisis lemak hasil maserasi.
1. Sebanyak 1,0 gram lemak hasil maserasi dari masing-masing sampel dimasukkan
dalam tabung reaksi .
2. Ditambahkan 8 mL larutan NaOH 0,5 N dalam metanol lalu dikocok hingga
sampel larut.
3. Kemudian dipanaskan dalam water bath selama 5 menit pada temperature 65 oC,
kocok dan letakkan lagi pada pemanas selama 10 menit.
4. Setelah didinginkan selama 5 menit tambahkan 10 mL larutan BF3-Metanol 14 %..
5. Panaskan kembali dalam water bath selama 10 menit dengan temperature 65 oC.
tambahkan larutan NaCl jenuh sebanyak 10 mL dan kocok denga kuat selama 30
detik.
7. Diamkan selama 5 menit dan terbentuk 2 lapisan larutan.
8. Fraksi metil ester (lapisan atas) dipisahkan dan disaring dengan mikro filter dan
siap dianalisa dengan GC-MS.
3.4.3.Analisis komposisi asam lemak dengan GC-MS.
1. Sebanyak 1 µ L sampel yang telah dimetanolisis diinjeksikan kedalam kolom
GC-MS dengan menggunakan auto sampler
2. Pemisahan dilakukan dalam kolom RTX-MS Restech
3. Hasil analisa berupa spectrum MS dibandingkan dengan library (refrence) Willey
147 dan N1ST47 yang terdapat pada GC-MS untuk mengetahui komposisi asam
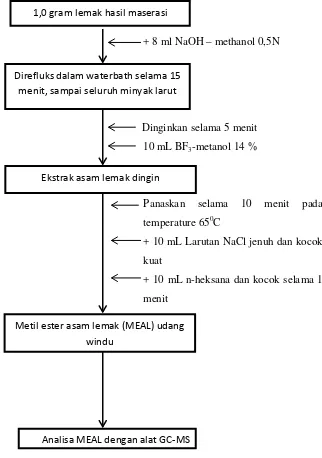
3.5.Diagram Alur Penelitian
Tahap Maserasi udang windu
- Dibersihkan dan dibuang kulit dan kepala
- Dihaluskan dengan blender - Dikeringkan di sinar matahari
- Dimasukkan dalam toples kaca - 1000 mL n-heksana dimaserasi 3
hari
- Disaring untuk memisahkan ampasnya
- Di uapkan pelarutnya dengan rotavapor
- Pemanasan dalam waterbath untuk memastikan semua pelarut tak tersisa
- Ditimbang dengan neraca analitik 200 gram sampel
Udang Windu
Filtrat berwarna kuning
Tahap metanolisis asam lemak
+ 8 ml NaOH – methanol 0,5N
Dinginkan selama 5 menit 10 mL BF3-metanol 14 %
-
Panaskan selama 10 menit pada temperature 650C
+ 10 mL Larutan NaCl jenuh dan kocok kuat
+ 10 mL n-heksana dan kocok selama 1 menit
Analisa MEAL dengan alat GC-MS
Gambar 3.1. : Diagram alur penelitian 1,0 gram lemak hasil maserasi
Ekstrak asam lemak dingin Direfluks dalam waterbath selama 15
menit, sampai seluruh minyak larut
BAB 4
HASIL DAN PEMBAHASAN 4.1. Hasil Penelitian
4.1.1.Metode Penentuan Kadar Lemak Daging Udang Windu
Kadar lemak udang windu(Penaeus monodon) dari tambak budi daya diperoleh 1,26 %, sedangkan udang windu dari laut sebesar 1,57 %, berarti kadar lemak nya tidak berbeda jauh (table 4.1).
Tabel.4.1 : Kadar lemak total dari daging udang windu
Habitat Berat daging Berat lemak Kadar lemak
4.1.2.Hasil Analisis dengan GC-MS
Lemak daging udang windu hasil maserasi yang sudah dimetilasi, kemudian dianalisis dengan Gas Cromatography-Mass Spectroscopy (GC-MS).
Analisis dengan GC-MS dilakukan dengan kondisi sebagai berikut :
Liniear Velocity : 26,1cm/sec
Purge Flow : 3,0 mL/min
Split Ratio : 73,0
High Pressure Injection : OFF
Carrier Gas Saver : OFF
Oven Temp.Program
Rate Temperatur (oC) Hold Time (min)
80,0 5,00
10,0 305,0 7,50
4.1.3.Data Kromatogram GC-MS
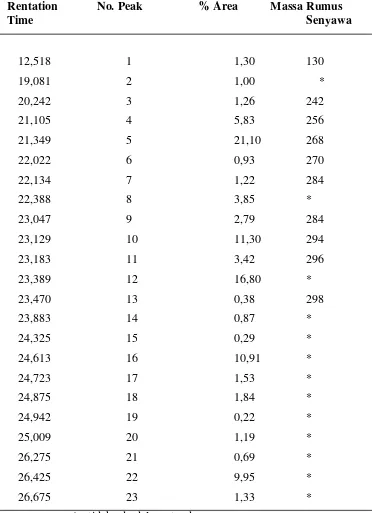
Hasil analisis melalui pemeriksaan GC-MS terhadap metil ester asam lemak
dari daging udang windu tambak budi daya diperoleh kromatogram dengan
memberikan puncak sebanyak 23 jenis senyawa seperti pada gambar 4.1
Gambar4.1 :Kromatogram metil ester asam lemak udang windu Tambak
Tabel.4.2. : Hasil analisisGC-MS metil ester asam lemak udang windu
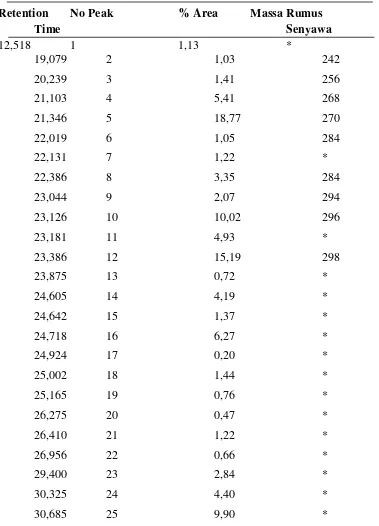
Pemeriksaan (analisis) dengan GC-MS metil ester asam lemak udang windu laut menhasilkan spectrum dengan 25 peak (puncak) seperti pada gambar 4.2
Gambar4.2 : Kromatogram metil ester asam lemak udang windu laut
4.2. Pembahasan
4.2.1. Pembuatan Metil Ester Asam Lemak Udang Windu
Untuk analisis komposisi asam lemak masing-masing udang windu yang berasal dari tambak maupun laut, terlebih dahulu dilakukan metanolisis. Metanolisis dalam hal ini untuk analisis dilakukan menggunakan katalis BF3 dengan reaksi (Gambar 4.3)
Metil ester asam lemak Gambar :4.3 Reaksi Metanolisis trigliserida membentuk metil ester asam lemak
4.2.2. Analisis GC-MS Metil Ester Asam Lemak Udang Windu Tambak
Untuk menentukan komposisi asam lemak yang terdapat pada udang windu
dari tambak maka hasil spektrum massa dari masing-masing puncak unknown
dibandingkan dengan spektrum massa senyawa yang ada pada daftar library GC-MS.
Dari sebanyak 23 jenis senyawa yang dapat teridentifikasi,dilakukan fragmentasi
terhadap 9 jenis senyawa yang massa rumus senyawa dapat disesuaikan dengan
spektrum standard dari library.
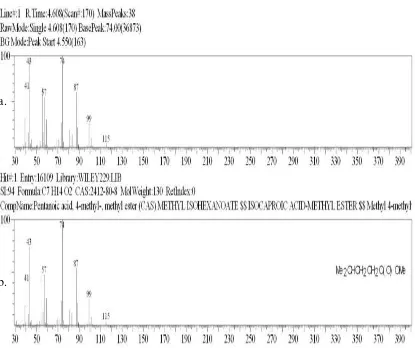
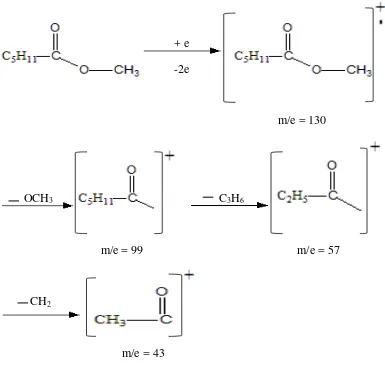
A.Puncak (peak) 1 dengan Rt 12,581 (1,13 %)
Data spektrum massa menunjukkan ion molekul m/e 130.Dengan membandingkan
data spektrum unknown dengan spektrum massa yang diperoleh dengan dataspektrum
pada standar, yang lebih mendekati adalah asam iso hexanoat atau metil ester,
4-metil pentanoat (Gambar4.4.)
a.
.
b.
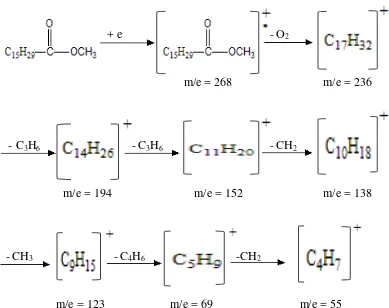
Dimana spektrum massa memberikan puncak ion molekul pada m/e 130 yang
merupakan berat molekul dari metil iso hexanoat atau metil ester 4-metil pentanoat.
Selanjutnya diikuti fragmen m/e = 99 (130-31) sebagai hasil terlepasnya radikal
OCH3, fragmen m/e = 57 (99 – 42) sebagai hasil terlepasnya C3H6 , dan fragmen m/e
= 43 (57 – 12) sebagai hasil terlepasnya CH2.
+ e
-2e
m/e = 130
OCH3 C3H6
m/e = 99 m/e = 57
CH2
m/e = 43