EFEK ANTIBAKTERI EKSTRAK ETANOL PEGAGAN
(
Centella asiatica
(L.) Urban) SEBAGAI ALTERNATIF
MEDIKAMEN SALURAN AKAR TERHADAP
Fusobacterium nucleatum
(SECARA
In-Vitro
)
SKRIPSI
Diajukan untuk memenuhi tugas dan melengkapi syarat guna memperoleh gelar Sarjana Kedokteran Gigi
OLEH :
MERY NIM : 080600075
FAKULTAS KEDOKTERAN GIGI
UNIVERSITAS SUMATERA UTARA
Fakultas Kedokteran Gigi
Departemen Ilmu Konservasi Gigi Tahun 2012
Mery
Efek Antibakteri Ekstrak Etanol Pegagan (Centella asiatica (L.) Urban)
sebagai Alternatif Medikamen Saluran Akar terhadap Fusobacterium nucleatum
(Secara In-Vitro) Xi + 58 halaman
Fusobacterium nucleatum merupakan salah satu bakteri yang paling banyak ditemukan pada infeksi saluran akar dengan insiden 48% dan sering ditemukan pada
kasus flare-up endodontik. Fusobacterium nucleatum juga resisten terhadap pemberian medikamen saluran akar sehingga perlu dikembangkan alternatif bahan
medikamen saluran akar yang dapat mengeliminasi bakteri ini. Salah satu bahan yang mungkin dapat dikembangkan ialah pegagan. Penelitian ini bertujuan untuk mengetahui efek antibakteri pegagan terhadap Fusobacterium nucleatum dengan
mencari nilai Kadar Hambat Minimum (KHM) dan Kadar Bunuh Minimum (KBM). Penelitian dimulai dengan pembuatan ekstrak pegagan, menggunakan 3 kg
pegagan yang dikeringkan dan dihaluskan menjadi 390 gram serbuk simplisia, dilarutkan dengan pelarut etanol 12 liter, kemudian diuapkan dengan rotavapor
diperoleh konsentrasi 100%, 50%, 25%, 12,5%, 6,25%, dan 3,125%, tiap konsentrasi
ditambahkan 1 ml suspensi bakteri, dicampur menggunakan vorteks dan diinkubasi 37°C selama 24 jam pada inkubator CO2. Amati kekeruhan dan bandingkan dengan
kontrol untuk menentukan KHM. Kemudian tiap kelompok dicampur menggunakan vorteks dan diambil 50µl diteteskan ke Mueller Hinton Agar, direplikasi 4 petri dan diinkubasi. Dilakukan penghitungan jumlah koloni bakteri untuk menentukan nilai
KBM.
Hasil pengujian dari konsentrasi 100% - 6,25%, tidak dijumpai pertumbuhan
koloni bakteri (0 CFU/ml). Konsentrasi 3,125% dijumpai rata - rata pertumbuhan koloni bakteri sebesar 1,1.102 CFU/ml.
Pada penelitian ini dapat disimpulkan bahwa ekstrak etanol pegagan memiliki efek antibakteri terhadap Fusobacterium nucleatum dengan nilai KBM 6,25%. Pada pengujian KHM, kekeruhan tidak bisa dibedakan sehingga tidak didapat nilainya.
Kata kunci: pegagan, medikamen saluran akar, Fusobacterium nucleatum
LEMBAR PENGESAHAN
SKRIPSI INI TELAH DISETUJUI UNTUK DISEMINARKAN PADA TANGGAL 8 MEI 2012
Oleh :
Pembimbing I
Nevi Yanti, drg., M.Kes NIP: 19631127 199203 2 004
Pembimbing II
Widi Prasetia, drg NIP : 19800213 200912 1 004
Mengetahui
Ketua Departemen Ilmu Konservasi Gigi Fakultas Kedokteran Gigi
Universitas Sumatera Utara
PERNYATAAN PERSETUJUAN Skripsi berjudul
EFEK ANTIBAKTERI EKSTRAK ETANOL PEGAGAN (Centella asiatica (L.) Urban) SEBAGAI ALTERNATIF MEDIKAMEN SALURAN AKAR
TERHADAP Fusobacterium nucleatum (SECARA In-Vitro) Yang dipersiapkan dan disusun oleh:
MERY NIM: 080600075
Telah dipertahankan di depan tim penguji Pada tanggal 8 Mei 2012
Dan dinyatakan telah memenuhi syarat untuk diterima
Susunan Tim Penguji Skripsi Ketua Penguji
Nevi Yanti, drg., M.Kes NIP: 19631127 199203 2 004
Anggota tim penguji lain
Prof. Dr.Rasinta Tarigan,drg.,Sp.KG (K) Prof.Trimurni Abidin,drg.,M.Kes,Sp.KG(K) NIP: 19450702 197802 1 001 NIP: 19631127 199203 2 004
Widi Prasetia, drg NIP : 19800213 200912 1 004
Medan, 11 Mei 2012 Fakultas Kedoketran Gigi Departemen Ilmu Konservasi Gigi
Ketua,
KATA PENGANTAR
Puji dan syukur penulis ucapkan kepada Tuhan Yang Maha Esa atas segala
berkat, rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan skripsi ini sebagai salah satu syarat untuk memperoleh gelar Sarjana Kedokteran Gigi pada Fakultas Kedokteran Gigi Universitas Sumatera Utara.
Pada kesempatan ini, penulis ingin menyampaikan terima kasih kepada orangtua tercinta, Papa (Tho Hong Liang) dan Mama (Herliana) atas segala kasih
sayang, nasehat, doa dan dukungan baik berupa moril dan materil selama ini. Tidak lupa penulis ucapkan terima kasih kepada abang (Hermantho), kakak (Arianty), dan
adik (Arianto) yang selalu memberi dukungan kepada penulis.
Dalam pelaksanaan penelitian dan penulisan skripsi ini, penulis banyak mendapatkan bantuan dan bimbingan dari berbagai pihak. Oleh karena itu, dengan
segala kerendahan hati penulis juga mengucapkan terima kasih kepada:
1. Prof. H. Nazruddin, drg., C.Ort., Ph.D., Sp.Ort, selaku Dekan Fakultas Kedokteran Gigi Universitas Sumatera Utara.
2. Cut Nurliza, drg., M.Kes, selaku Ketua Departemen Ilmu Konservasi Gigi Fakultas Kedokteran Gigi Universitas Sumatera Utara.
3. Nevi Yanti, drg., M.Kes, selaku pembimbing I penulis yang telah banyak meluangkan waktu, memberikan ide, dan bersedia membimbing penulis sehingga skripsi ini dapat diselesaikan.
5. Seluruh staf pengajar Departemen Ilmu Konservasi Gigi Fakultas Kedokteran
Gigi Universitas Sumatera Utara.
6. Prof. H. Ismet Danial Nasution, drg., Ph.D., Sp.Prost (K) selaku penasehat
akademik yang telah membimbing penulis selama menyelesaikan program akademik.
7. Drs. Awaluddin Saragih, M.Si., Apt selaku kepala Laboratorium Obat
Tradisional Fakultas Farmasi USU; Abang Bagus dan Abang Ari yang telah banyak membantu dalam kegiatan ekstraksi.
8. Wahyu Hidayahtiningsih, S.Si., M.Kes selaku peneliti di Laboratorium Pusat Penyakit Tropis UNAIR yang membantu dalam kegiatan di laboratorium.
9. Drs. Abdul Jalil A.A, M.Kes selaku pembantu dekan III FKM USU, dan Ibu Maya Fitria, SKM, M.Kes yang membantu dalam konsultasi statistika.
10. Teman-teman penulis angkatan 2008, Denis, Thilages, Liang Jie, serta teman
seperjuangan skripsi di bagian Konservasi Gigi (Kakak Laila, Imel, Tika). 11. Semua pihak yang telah banyak membantu dalam penulisan skripsi yang tidak
dapat saya sebutkan satu-persatu.
Penulis memohon maaf apabila ada kesalahan selama melakukan penelitian dan penyusunan skripsi ini dan berharap semoga skripsi ini dapat memberikan
sumbangan pikiran yang berguna bagi fakultas, pengembangan ilmu dan masyarakat. Medan, 24 April 2012 Penulis
DAFTAR ISI
Halaman
HALAMAN JUDUL.……….
HALAMAN PENGESAHAN JUDUL.………...
HALAMAN PERSETUJUAN.……….
KATA PENGANTAR... 2.1 Penggunaan Medikamen Saluran Akar.………...…... 6
2.2 Fusobacterium nucleatum Sebagai Salah Satu Bakteri Pada Infeksi Saluran Akar.……….…….... 10
2.3 Pegagan (Centella asiatica(L.) Urban).………..……. 14
BAB 3 KERANGKA KONSEP PENELITIAN 3.1 Kerangka Konsep……….………….…… 18
3.2 Hipotesis Penelitian………..………. 20
BAB 4 METODE PENELITIAN 4.1 Rancangan Penelitian……… 21
4.2 Populasi, Sampel dan Besar Sampel………. 21
4.3 Variabel Penelitian……… 24
4.5 Bahan dan Alat Penelitian……….. 28
4.6 Tempat dan Waktu Penelitian………. 29
4.7 Prosedur Pengambilan dan Pengumpulan Data……….. 29
BAB 5 HASIL PENELITIAN 5.1 Ekstraksi Pegagan (Centella asiatica(L.) Urban )…………..…….. 36
5.2 Uji Efektifitas Antibakteri………. 36
BAB 6 PEMBAHASAN……….. 39
BAB 7 KESIMPULAN DAN SARAN 7.1 Kesimpulan……… 45
7.2 Saran……….. 45
DAFTAR PUSTAKA... 47
DAFTAR TABEL
Tabel Halaman
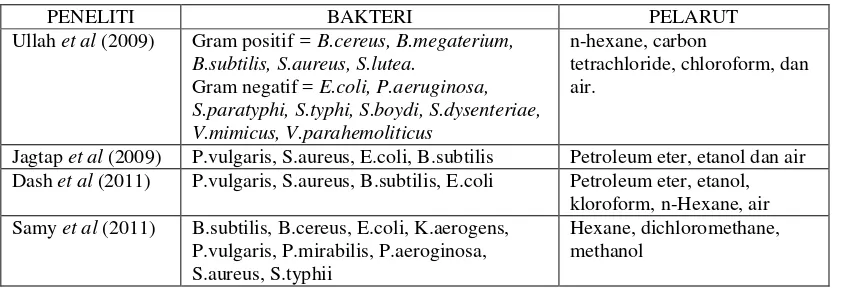
1. Bakteri yang diisolasi dari saluran akar gigi dengan lesi apikal ………….. 12 2. Daya antibakteri ekstrak pegagandengan pelarut yang berbeda………..… 16
3. Hasil perhitungan jumlah bakteri Fusobacterium nucleatum setelah
perlakuan……… 38
4. Kandungan senyawa dari bahan alam sebagai alternatif medikamen saluran
DAFTAR GAMBAR
Gambar Halaman
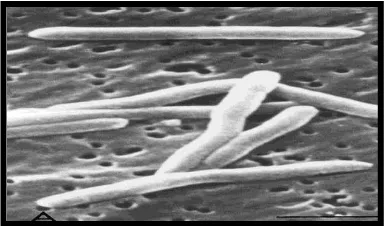
1. Koloni F.nucleatum dibawah Scanning Electron Microscopy (SEM) ….. 10
2. F.nucleatum dibawah mikroskop elektron Outer membrane (OM), Periplasmic space (P) dan Cell membrane (CM) ………..………. 11
3. Gambaran SEM dari Sel F.nucleatum yang berkoagregasi dengan P.gingivalis………...…….... 13
4. Pegagan yang terdapat di Desa Durian, Kec. Labuhan Batu, Kab. Deli Serdang ……….………....………... 15
5. Pegagan dengan panjang 10-80 cm, bentuk ginjal, tepi bergerigi ……….…….... 15
6. Pegagan ditimbang dan dikeringkan dalam lemari pengering ……… 30
7. Pegagan dihaluskan menjadi serbuk dan disimpan dalam plastik tertutup….. 30
8. Pegagan dilakukan perendaman, perkolasi dan evaporasi ………... 30
9. Ekstrak kental pegagan ………..……… 31
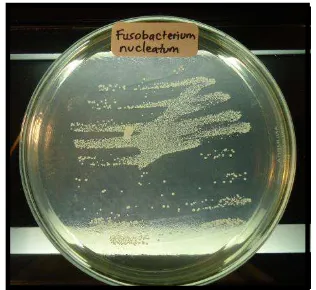
10.Koloni bakteri Fusobacterium nucleatum pada media Mueller Hinton Agar………..…….. 32
11.Mikropipet dan tips, vorteks, inkubator CO2……… 33
12.Kaca pembesar ……….. 34
13.Bentuk koloni pada media padat ……….. 34
15.Media Mueller Hinton Broth sebelum diberi perlakuan dan suspensi
bakteri setelah diberi perlakuan ………... 37 16.Koloni bakteri pada Mueller Hinton Agar………..………... 37
DAFTAR LAMPIRAN
Lampiran Halaman
1. Skema Alur Pikir………...………. 52
2. Skema Alur Penelitian……… 54 3. Data Hasil Uji Antibakteri Estrak Etanol Pegagan terhadap
Fusobacterium nucleatum……… 57
BAB 1 PENDAHULUAN
1.1 Latar Belakang
Bakteri memegang peranan penting dalam perkembangan penyakit pulpa dan jaringan periapikal. Tujuan utama dari perawatan saluran akar adalah menghilangkan bakteri sebanyak mungkin dari saluran akar dan kemudian menciptakan lingkungan
dimana organisme yang tersisa tidak dapat bertahan hidup. Mengingat anatomi pulpa yang begitu kompleks dan bakteri yang masuk jauh ke tubulus dentin, dan pada
kasus-kasus tertentu seperti kasus pulpa nekrosis atau periodontitis apikalis, maka tindakan preparasi saluran akar disertai irigasi tidak dapat membebaskan saluran akar
dari bakteri sehingga diperlukan medikamen intrakanal.1,2
Medikamen intrakanal bertujuan untuk mengeliminasi semua bakteri yang tersisa di saluran akar, mengurangi inflamasi periradikuler dan mengurangi nyeri,
mencegah resorpsi akar serta mencegah re-infeksi.1 Medikamen yang digunakan dalam perawatan endodontik dapat dibagi atas beberapa kelompok besar yaitu golongan fenol, aldehid / formaldehida, halida / halogen, steroid, kalsium hidroksida,
antibiotik dan kombinasi.3 Kalsium hidroksida (Ca(OH)2) adalah bahan medikamen intrakanal yang saat ini paling sering digunakan.1 Ca(OH)2 mempunyai efek
antimikroba terutama karena pH-nya yang tinggi sekitar 12,5 dan bekerja dengan merusak dinding sel bakteri dan struktur protein. Namun Ca(OH)2 juga memiliki beberapa kelemahan yaitu memiliki efek merusak jaringan periodontal ketika
penyembuhan jaringan lunak marginal dan menghambat perlekatan sel – sel fibroblas
gingiva.4 Secara teori, Ca(OH)2 bukan merupakan bahan biokompatibel yang bila terpapar ke pembuluh darah akan mengakibatkan kristalisasi yang disebabkan oleh
nilai pH yg berbeda. Sharma S, dkk (2008) melaporkan Ca(OH)2 dapat mengakibatkan nekrosis pada jaringan bila masuk ke pembuluh darah dan secara langsung menyebabkan toksisitas jaringan.5 Pemakaian Ca(OH)2 sebagai medikamen
intrakanal tidak berpengaruh pada pencegahan atau pengendalian nyeri.3 Penggunaan Ca(OH)2 dilaporkan tidak sama efektifnya untuk semua bakteri, Ca(OH)2 resisten
terhadap bakteri Enterococcus faecalis, Candida albicans,1 Lactococcus garvieae,
dan Fusobacterium nucleatum.6
Menurut Sundqvist (1994), bakteri Fusobacterium nucleatum (F.nucleatum) paling banyak ditemukan pada infeksi saluran akar yaitu 48%. Lipopolisakarida yang dikenal sebagai zat endotoksin dihubungkan dengan terjadinya inflamasi periapikal
dan aktivasi komplemen.7 Asam butirat yang dihasilkan dapat mengiritasi jaringan serta menyebabkan resorbsi tulang.7,8 Keberadaan F.nucleatum telah dihubungkan dengan rasa sakit yang parah disertai dengan pembengkakan. Adanya kombinasi dari
F.nucleatum, Prevotella spp, dan Porphyromonas spp dapat menjadi faktor resiko terjadinya flare-up endodontik.9
Mengingat bakteri F.nucleatum sering dijumpai pada infeksi saluran akar dan dengan kelemahan yang dimiliki Ca(OH)2 maka diperlukan suatu bahan medikamen saluran akar yang baru. Untuk itu, perlu dikembangkan bahan alami yang
pengembangan obat bahan alam, pemerintah saat ini telah menetapkan kebijakan
Program Nasional Pengembangan Obat Bahan Alam dengan menjadikan Indonesia sebagai produsen nomor satu di dunia dalam industri obat berbasis bahan alami
(world first class herbal medicine country) pada tahun 2020.10
Beberapa penelitian yang telah dilakukan di Indonesia mengenai pengembangan bahan alam sebagai alternatif bahan medikamen intrakanal,
diantaranya Aloe vera, buah mahkota dewa dan minyak atsiri kayu manis.11-13 Penelitian yang dilakukan oleh Rahma (2009) mengenai ekstrak etanol Aloe vera
didapat nilai KBM untuk F.nucleatum yaitu pada konsentrasi 50%.11 Penelitian yang dilakukan oleh Kere (2011) mengenai ekstrak etanol buah mahkota dewa terhadap
F.nucleatum dengan nilai KBM 3,125%.12
Salah satu bahan alam yang juga dapat dikembangkan sebagai bahan medikamen intrakanal adalah pegagan (Centella asiatica (L.) Urban) karena memiliki
khasiat yang cukup banyak. Masyarakat juga menggunakan pegagan sebagai obat sakit gigi, namun sampai saat ini belum ada penelitian atau data klinis yang mendukung.14 Tanaman ini rasanya manis, sifatnya sejuk, memiliki kemampuan
sebagai antibakteri, anti nyeri, anti inflamasi, dan tidak toksik. Pegagan juga dapat mempercepat penyembuhan luka, antidepresan, antiepileptik, antipiretik,
hipoglikemik.15
Komponen aktif sebagai antibakteri dari tanaman ini adalah saponin, alkaloid, flavonoid, dan tanin.16-18 Hasil penelitian Oryza (2010), menunjukkan bahwa
kandungan flavonoid, tanin dan saponin aktif dari pegagan dapat menghambat bakteri
memiliki aktivitas antimikroba yang lebih tinggi daripada petroleum ether dan water
extract. Hasil penelitiannya menunjukkan bahwa ekstrak etanol pegagan terhadap bakteri P.vulgaris, S.aureus, E.coli, jamur A.niger, C.albicans didapat nilai Kadar
Hambat Minimum (KHM) 125 µg/ml dan pada bakteri B.subtilis, jamur A.flavus nilai KHM 62,5 µg/ml.18
Pada penelitian ini temperatur dan waktu yang optimum untuk pertumbuhan
bakteri adalah 37°C dengan waktu 24 jam.19,20 Pelarut etanol digunakan karena etanol dapat melarutkan senyawa yang bersifat polar, sedikit semi polar dan non-polar.
Etanol juga relatif aman dibandingkan dengan metanol yang bersifat lebih toksik.21 Untuk memenuhi syarat sebagai bahan medikamen saluran akar, maka perlu
dilakukan uji antibakteri pegagan terhadap F.nucleatum. Konsentrasi ekstrak yang digunakan berdasarkan metode dilusi (pengenceran ganda) yang besarnya setengah dari konsentrasi awal yaitu 100%, 50%, 25%, 12,5%, 6,25%, dan 3,125%. Dalam
penelitian ini yang dicari adalah Kadar Hambat Minimum (KHM) dan Kadar Bunuh Minimum (KBM).
1.2 Rumusan Masalah
Berdasarkan uraian di atas, maka timbul permasalahan yaitu:
Apakah ada efek antibakteri ekstrak etanol pegagan terhadap F.nucleatum?
1.3 Tujuan Penelitian
Tujuan dari penelitian ini adalah untuk mengetahui efek antibakteri ekstrak
1.4 Manfaat Penelitian
Adapun manfaat dari penelitian ini adalah:
1. Sebagai dasar untuk penelitian lebih lanjut pengembangan ekstrak pegagan
sebagai bahan medikamen saluran akar.
2. Meningkatkan pelayanan kesehatan gigi pada masyarakat dengan menggunakan bahan alami yang bersifat biokompatibel dan mudah didapat
dengan harga terjangkau.
3. Sebagai informasi bagi dokter gigi tentang manfaat dan efek antibakteri dari
ekstrak pegagan.
4. Meningkatkan pendapatan masyarakat dengan membudidayakan bahan alam
BAB 2
TINJAUAN PUSTAKA
Pemberian medikamen saluran akar bertujuan untuk mengeliminasi bakteri yang tidak dapat dihancurkan dengan proses instrumentasi dan irigasi.1 Tetapi pada
beberapa kasus, setelah pemberian bahan medikamen Ca(OH)2, Fusobacterium
nucleatum masih ditemukan dalam saluran akar.6 Untuk mengeliminasi
Fusobacterium nucleatum maka diharapkan pegagan dapat dikembangkan sebagai alternatif bahan medikamen saluran akar.
2.1 Penggunaan medikamen saluran akar
Pada kasus-kasus tertentu seperti pulpa nekrosis atau periodontitis apikalis, dan pada waktu yang tidak cukup, maka pemberian medikamen intrakanal sangat
diperlukan untuk memperoleh saluran akar yang steril, sedangkan pada pulpa gigi yang masih vital atau pulpitis irreversibel, tidak memerlukan medikamen intrakanal karena lebih menekankan pada tindakan preparasi dan irigasi, sehingga dapat
diselesaikan dalam satu kali kunjungan.2
Medikamen digunakan untuk membantu meningkatkan keberhasilan
perawatan endodontik. Medikamen tersebut diharapkan dapat berpenetrasi ke dalam tubulus dentin dan membunuh bakteri. 1 Sehingga syarat dari medikamen saluran akar yaitu harus memiliki aktivitas antibakteri, menetralisir sisa-sisa debris di saluran akar,
atau paper point ke dalam saluran akar, sehingga efek antimikrobanya terjadi melalui
penguapan dari bahan medikamen tersebut.1
Medikamen yang digunakan dalam perawatan endodontik dapat dibagi atas
beberapa kelompok besar yaitu golongan fenol, aldehid / formaldehida, halida / halogen, steroid, kalsium hidroksida, antibiotik dan kombinasi. Golongan fenol meliputi eugenol, camphorated monoparachlorophenol (CMCP), parachlorofenol
(PCP), camphorated parachlorofenol (CPC), metacresyl acetate (kresatin), kresol, kreosote (beechwood), dan timol. Aldehid/formaldehida meliputi formokresol dan
glutaraldehid. Sementara halida / halogen meliputi natrium hipoklorit (NaOCl) dan iodin-kalium-iodida.3
Golongan fenol dan aldehid pada umumnya merupakan pembunuh sel yang poten, namun efek samping yang terjadi pada penggunaannya adalah alergenisitas sehingga dapat membahayakan jaringan pulpa dan periapeks. Golongan fenol
memiliki bau yang menyengat, rasa yang tidak enak, dan akan kehilangan daya aktifnya dalam waktu 24 jam. Pemakaian golongan aldehid pada jaringan yang nekrotik, pada kenyataannya akan membuat jaringan itu lebih toksik. Golongan fenol
dan formokresol menunjukkan bahwa medikamen ini tidak berpengaruh pada pencegahan nyeri, sedangkan golongan steroid dapat menurunkan nyeri pasca rawat,
tetapi tidak akan menurunkan insiden flare-up (nyeri parah).3
Kalsium hidroksida atau Ca(OH)2 adalah bahan medikamen yang saat ini paling sering digunakan. Pertama kali diperkenalkan oleh Herman 1920, Ca(OH)2
periapeks,3 merangsang penyembuhan periapikal dan dapat membunuh bakteri
dengan efek pH yaitu melalui pelepasan dan difusi dari ion hidroksil (OH) dengan menciptakan lingkungan yang bersifat alkaline yang tidak kondusif bagi
kelangsungan mikroorganisme.1
Efek bunuh dari kalsium hidroksida berkaitan dengan beberapa mekanisme, yaitu secara mekanis dan secara fisik. Aksi mekanis berlangsung melalui cara
merusak membran sitoplasma mikroba dengan aksi langsung ion hidroksil, menekan aktivitas enzim dan mengganggu metabolisme seluler, dan menghambat replikasi
DNA dengan memisahkan DNA. Sedangkan secara fisik melalui bertindak sebagai
barrier yang mengisi rongga dalam kanal dan mencegah masuknya bakteri ke dalam
sistem saluran akar dan membunuh mikroorganisme yang tersisa dengan menahan substrat untuk pertumbuhan dan membatasi tempat untuk multiplikasi.1
Ca(OH)2 juga memiliki kemampuan menginaktifkan Lipopolisakarida (LPS).4
Safavi dan Nichols, 1993 cit Estrela et al., mempelajari efek kalsium hidroksida terhadap LPS bakteri, dapat disimpulkan bahwa kalsium hidroksida menghidrolisis lapisan lipid dari LPS bakteri menghasilkan asam lemak hidroksil dalam jumlah yang
banyak dan menonaktifkan enzim dalam membran bakteri serta mengganggu mekanisme transportasi yang mengakibatkan sel keracunan.22
Namun terdapat juga beberapa kelemahan dari Ca(OH)2 yaitu memiliki efek merusak jaringan periodontal ketika digunakan sebagai medikamen intrakanal, dengan mempengaruhi proses penyembuhan jaringan lunak marginal dan
mengakibatkan kristalisasi yang disebabkan oleh nilai pH yg berbeda. Sharma S, dkk
(2008) melaporkan Ca(OH)2 dapat mengakibatkan nekrosis pada jaringan bila masuk ke pembuluh darah dan secara langsung menyebabkan toksisitas jaringan.5
Pemakaian Ca(OH)2 sebagai medikamen intrakanal tidak berpengaruh pada pencegahan atau pengendalian nyeri.3 Penggunaan Ca(OH)2 dilaporkan tidak sama efektifnya untuk semua bakteri, Ca(OH)2 resisten terhadap bakteri Enterococcus
faecalis, Candida albicans.1 Penelitian Siqueira et al (2007), menunjukkan dari sebelas saluran akar dengan lesi periodontitis apikalis, setelah penggunaan bahan
dressing antar kunjungan dengan menggunakan Ca(OH)2 selama satu minggu, ditemukan dua kasus bakteri postmedikamen, dengan satu takson per kasus, yaitu
bakteri F.nucleatum dan Lactococcus garvieae. F.nucleatum ditemukan persisten setelah pemberian medikamen.6
Bakteri dapat bertahan hidup setelah pemberian medikamen saluran akar karena
strain bakteri dalam infeksi saluran akar secara intrinsik resisten terhadap medikamen, sel bakteri tertutup oleh variasi anatomi gigi sehingga tidak dapat dimasuki oleh medikamen, medikamen dinetralkan oleh komponen jaringan dan sel
bakteri atau produknya sehingga kehilangan efek antibakterinya, medikamen saluran akar tidak cukup untuk menjangkau dan membunuh sel bakteri, serta bakteri dapat
mengubah pola ekspresi gen mereka untuk bertahan hidup di lingkungan yang tidak menguntungkan.23
Penelitian Peters et al (2002), menyatakan bakteri dalam saluran akar
endodontik.24 Gomez et al (2002) menyatakan walaupun Ca(OH)2 direkomendasikan
sebagai bahan medikamen intrakanal pada perawatan periodontitis apikalis, bukan berarti dapat digunakan secara universal karena Ca(OH)2 tidak menunjukkan
kemampuan yang sama terhadap seluruh bakteri.25
2.2 Fusobacterium nucleatum sebagai salah satu bakteri pada infeksi saluran akar
Berdasarkan taksonominya, Fusobacterium nucleatum (F. nucleatum)
diklasifikasikan atas:
Kingdom : Bacteria Filum : Fusobacteria
Famili : Bacteroidaceae Genus : Fusobacterium
Spesies : Fusobacterium nucleatum.8
Secara morfologi F.nucleatum merupakan bakteri berbentuk batang yang ujungnya tajam (Gambar 1), panjangnya 5-10µm, dikelompokkan ke dalam bakteri gram negatif, tidak bergerak, dan bersifat obligat anaerob. F.nucleatum memerlukan
media untuk tumbuh, biasanya tumbuh pada media yang mengandung trypticase, pepton, atau ekstrak ragi. 8
Membran luar bakteri ini mempunyai karakteristik bakteri gram negatif. Sel
bakteri dilindungi oleh membran luar dan membran dalam yang dipisahkan oleh ruang periplasmik yang mengandung lapisan peptidoglikan (Gambar 2). Pada
umumnya, membran dalam bakteri gram negatif merupakan dua lapisan fosfolipid yang simetris dimana perbandingan fosfolipid dan protein sama besar. Membran luar berfungsi sebagai penyaring molekul dan merupakan membran asimetrik yang terdiri
dari lapisan fosfolipid, lipopolisakarida, lipoprotein dan protein.8
Gambar 2. F.nucleatum dibawah mikroskop elektron Outer membrane (OM), Periplasmic space (P) dan Cell membrane (CM)8
Bakteri F.nucleatum banyak ditemukan pada kasus penyakit periodontal dan
kasus lesi apikal. Menurut Sundqvist (1994), F.nucleatum paling banyak ditemukan melalui kultur bakteri saluran akar dengan lesi apikal yaitu 48% (Tabel 1).7 Dari hasil penelitian Siqueira dan Rocas (2009), pada kasus abses apikalis akut didapat bahwa
bakteri F.nucleatum merupakan prevalensi terbesar sekitar 64% yaitu 27 kasus yang diambil dari 42 individu.26
asam amino seperti aspartat, glutamat, histidin, dan lisin untuk menyediakan
energinya. F.nucleatum menghasilkan asam butirat dan mengubah treonin menjadi asam propionat. Butirat, propionat dan ion amonium merupakan produk hasil
metabolisme F.nucleatum yang dapat menghambat proliferasi sel fibroblas pada gingiva. Kejadian ini memberikan jalan bagi F.nucleatum untuk melakukan penetrasi ke epitel gingiva. Asam butirat yang dihasilkan juga dapat mengiritasi jaringan.8
Asam butirat telah terbukti sebagai inhibisi terbesar dari T-sel blastogenesis dan menstimulasi produksi interleukin-1, ini dikaitkan dengan resorpsi tulang.7
Tabel 1. BAKTERI YANG DIISOLASI DARI SALURAN AKAR GIGI DENGAN LESI
dan resorpsi tulang. Lipopolisakarida memegang peranan penting dalam proses
perlekatannya dan mampu larut dalam saliva. Lipopolisakarida yang diproduksi oleh
F.nucleatum memungkinkan bakteri ini melekat pada struktur hidroksiapatit, serum
dan sementum. Hal ini menunjukkan bahwa lipopolisakarida dari F.nucleatum
memegang peranan penting dalam proses perlekatannya, bukan hanya pada epitel, tetapi juga permukaan gigi.7,8
F.nucleatum bertindak sebagai bridge diantara kolonisasi awal (bakteri gram positif) dan akhir (bakteri gram negatif). Bakteri ini memiliki kemampuan untuk
berkoagregasi dengan bakteri lain di rongga mulut, seperti Porphyromonas gingivalis
(Gambar 3), F.nucleatum berkoagregasi dengan P.gingivalis melalui karbohidrat
yaitu galaktosa pada P.gingivalis dan membran luar dari F.nucleatum. F.nucleatum juga dapat berkoaggresi dengan Candida albicans melalui ikatan protein permukaan sel bakteri dan residu karbohidrat pada permukaan Candida albicans.8,27 Kombinasi
dari F.nucleatum, Prevotella spp, dan Porphyromonas spp dapat menjadi faktor resiko terjadinya flare-up endodontik dengan bersinergi untuk meningkatkan intensitas reaksi inflamasi periapikal.9
2.3 Pegagan (Centella asiatica (L.)Urban)
Berdasarkan taksonominya, pegagan dapat diklasifikasikan atas: Kingdom : Plantae
Divisi : Magnoliophyta
Kelas : Magnoliopsida (Dicotyledonae) Ordo : Umbilales
Famili : Umbilaferae (Apiaceaea) Genus : Centella
Species : Centella asiatica (L.) Urban.16
Pegagan (Centella asiatica (L.) Urban) merupakan tanaman tahunan yang
tumbuh menjalar dan tidak berbatang. Biasanya tumbuh di tempat yang agak lembab, cukup sinar matahari dan perkembangbiakannya menggunakan stolon dan biji. Tanaman ini tumbuh liar dan mudah dibedakan dengan tanaman lainnya (Gambar 4)
yaitu dengan ciri-ciri panjang tanaman ini berkisar 10-80 cm. Daun tunggal, bertangkai panjang, jumlahnya 2-10 helai, berbentuk ginjal, tepi bergerigi dengan diameter 1-7 cm (Gambar 5). Bentuk bunga seperti payung. Buahnya kecil, berbentuk
lonjong, pipih, panjang 2-2,5 mm, wangi, pahit, lebar sekitar 7 mm, warna kuning kecoklatan. Bagian tanaman yang digunakan adalah herba yakni seluruh bagian
Gambar 4. Pegagan yang terdapat di Desa Gambar 5. Pegagan dengan panjang Durian, Kec. Labuhan Batu, 10-80 cm, Bentuk ginjal, Kab.Deli Serdang tepi bergerigi
Tanaman ini tersebar diseluruh Indonesia, dapat dibuktikan dengan namanya
di setiap daerah. Nama lain dari pegagan ialah Pegaga (Aceh), pegago (Minangkabau), daun kaki kuda (melayu), pegagan (Jakarta); antanan gede, antanan
rambat (Sunda), gagan-gagan, gagaga, kerok batok, panegowang, rendeng, calingan rambut (Jawa), kos tekosan, gan gagan (Madura), taidah (Bali); belele (Sasak, Nusa Tenggara); kelai lere (Sawo, Nusa Tenggara); wisu-wisu, pagaga (Makasar); daun
tungketungke, cipubalawo (Bugis); hisu-hisu (Aselayar, Sulawesi); Saraswati, korikori (halmahera); kolotidi manora (Ternate); dogauke, gogauke, sandanan (Irian).
Broken copper coin, button gas, small-leaved horsehoof grass, Indian pennywort,
asya sutasi, brahmi, marsh penny, white rot, buabok (Inggris); indische waternavel, paardevoet (Belanda), gotu kalo (India), ji xue cao (Cina).28
Rajakumar et al (2010), melakukan penelitian terhadap beberapa tanaman herbal yang digunakan sebagai obat-obatan di Sagar Taluk, Distrik Shimoga,
Karnataka, India dan menemukan pegagan digunakan sebagai obat sakit gigi dengan cara penggunaaan pasta dari daun tersebut digunakan pada daerah yang sakit, sehari
sekali sampai sembuh.29 Pegagan termasuk salah satu tanaman utama dalam khasanah
pengobatan india kuno (ayurveda) karena khasiatnya yang cukup banyak yaitu sebagai antibakteri (Tabel 2). Penelitian Dash et al (2011), menyatakan bahwa
aktivitas antibakteri pegagan pada berbagai pelarut didapat pelarut etanol yang paling besar zona hambatnya dibandingkan dengan pelarut petroleum eter, kloroform, n-hexane dan aqueous.30 Penelitian Somchit et al (2004), menyatakan ekstrak air dari
pegagan juga memiliki efek anti nyeri dan anti inflamasi pada mencit.31 Disamping itu, juga berkhasiat sebagai hemostatis, antipiretik, sedatif, diuretik, dan mempercepat
penyembuhan luka.15,28 Berdasarkan penelitian Sulastry (2009), menyatakan penggunaan ekstrak pegagan secara oral pada mencit dengan dosis 2000 mg/kgBB
telah terbukti praktis tidak toksik.32
Tabel 2. DAYA ANTIBAKTERI EKSTRAK PEGAGAN DENGAN PELARUT YANG BERBEDA
18,30,33,34
PENELITI BAKTERI PELARUT
Ullah et al (2009) Gram positif = B.cereus, B.megaterium, B.subtilis, S.aureus, S.lutea.
Gram negatif = E.coli, P.aeruginosa, S.paratyphi, S.typhi, S.boydi, S.dysenteriae, V.mimicus, V.parahemoliticus
n-hexane, carbon
tetrachloride, chloroform, dan air.
Jagtap et al (2009) P.vulgaris, S.aureus, E.coli, B.subtilis Petroleum eter, etanol dan air
Dash et al (2011) P.vulgaris, S.aureus, B.subtilis, E.coli Petroleum eter, etanol,
kloroform, n-Hexane, air Samy et al (2011) B.subtilis, B.cereus, E.coli, K.aerogens,
P.vulgaris, P.mirabilis, P.aeroginosa, S.aureus, S.typhii
Hexane, dichloromethane, methanol
Kandungan kimia pegagan ialah asiaticoside, thankunside, isothankunside, madecassoside, brahmoside, brahminoside, asam brahmat, asam madasiatic, hidrocotyline, mesoinositol, centallose, karoten, garam mineral (seperti K, Na, Ca,
atsiri.15,17,28 Komponen aktif sebagai antibakteri adalah saponin, alkaloid, flavonoid,
dan tanin.16,17 Hasil penelitian Oryza (2010), menunjukkan bahwa kandungan flavonoid, tanin dan saponin aktif dapat menghambat bakteri Staphylococcus
aureus.16
Triterpen terdiri dari asam asiatat, asiatikosida, madecassoside, dan asam madekasat adalah kandungan yang sering dijumpai pada pegagan.35 Norzaharaini et
al (2011) menyatakan Asam Asiatat (AA) memiliki efek antibakteri pada bakteri
Helicobacter pylori, Escherichia coli, Staphilococcus aureus, dan Streptococcus
penumonia.36 Krishnamurthy et al (2009) menguji efek neuroprotektif asam asiatat pada model mencit iskemia serebral permanen dan melaporkan asam asiatat memiliki
efek neuroprotektif yang dimediasi penurunan permeabilitas barier darah otak dan mereduksi kerusakan mitokondria.34 Menurut Taemchuay et al (2008), pada ekstrak air pegagan terdapat senyawa aktif Asiatikosida triterpen yang mempunyai aktivitas
antibakteri terhadap bakteri S.aureus.37 Asiatikosida memiliki efek penyembuh luka dengan meningkatkan pembentukan kolagen dan angiogenesis.17 Asiatikosida juga dilaporkan mengurangi jaringan fibrosis pada luka sehingga mencegah pembentukan
scar (bekas luka), mekanismenya yaitu dengan meningkatkan sintesis kolagen dan asam mukopolisakarida, dan dengan menghambat fase hipertrofi scar dan keloid.14
Senyawa lain yang banyak dijumpai adalah madecassoside. Liu et al, Efek farmakologis dari madecassoside menunjukkan sifat anti inflamasi pada tikus, madecassoside dapat meningkatkan kolagen tipe II melalui imunitas humoral dan
Kerangka di atas menunjukkan mekanisme antibakteri ekstrak pegagan100%,
50%, 25%, 12,5%, 6,25%, dan 3,125% yang digunakan sebagai medikamen saluran akar yang dapat menyebabkan kematian sel dari bakteri Fusobacterium nucleatum.
Ekstrak pegagan mengandung alkaloid, saponin, tanin dan flavonoid yang masing-masing mempunyai mekanisme yang berbeda dalam membunuh bakteri.18 Mekanisme kerja dari alkaloid yaitu dengan cara mengganggu komponen penyusun
peptidoglikan pada sel bakteri, sehingga lapisan dinding sel tidak terbentuk secara utuh dan menyebabkan kematian sel tersebut.38 Asiatikosida dan asam asiatat
termasuk ke dalam golongan saponin.17 Saponin bekerja sebagai deterjen atau sabun yang membuat senyawa ini terkonsentrasi pada permukaan sel. Saponin yang
berperan sebagai deterjen alam atau fitonutrien memiliki molekul ampifatik (mengandung bagian hidrofilik dan hidrofobik) yang dapat melarutkan protein membran. Ujung hidrofobik saponin berikatan pada regio hidrofobik protein
membran sel dengan menggeser sebagian besar unsur lipid yang terikat. Ujung hidrofilik saponin yang akan membawa protein ke dalam larutan sebagai kompleks saponin sehingga sel bakteri menjadi lisis dan mati.39 Tanin memiliki aktivitas
antibakteri, secara garis besar mekanisme yang diperkirakan adalah sebagai berikut: toksisitas tanin dapat merusak membran sel bakteri, senyawa astringent tanin dapat
menginduksi pembentukan kompleks senyawa ikatan terhadap enzim atau substrat mikroba dan pembentukan suatu kompleks ikatan tanin terhadap ion logam yang dapat menambah daya toksisitas tanin itu sendiri. Tanin diduga dapat mengkerutkan
sehingga pertumbuhannya terhambat atau bahkan mati. Tanin juga mempunyai daya
antibakteri dengan cara mempresipitasi protein karena tanin mempunyai efek yang sama dengan senyawa fenolik. Efek antibakteri tanin antara lain melalui reaksi
dengan membran sel, inaktivasi enzim, dan desktruksi atau inaktivasi fungsi materi genetik. Flavonoid membentuk senyawa kompleks terhadap protein ekstraseluler sehingga mengganggu integritas membran sel bakteri.38
3.2Hipotesis penelitian
Dari uraian di atas, maka hipotesa penelitian ini adalah:
Ada efek antibakteri ekstrak etanol pegagan terhadap Fusobacterium
BAB 4
METODE PENELITIAN
4.1 Rancangan Penelitian : Posttest Only Control Group Design
Jenis penelitian : Eksperimental Laboratorium
4.2 Populasi, Sampel dan Besar Sampel Penelitian 4.2.1 Populasi : Bakteri F.nucleatum
4.2.2 Sampel penelitian : Koloni F.nucleatum ATCC 25586 yang telah diisolasi dan dibiakkan dengan media Mueller Hinton Agar (MHA).
4.2.3 Besar Sampel
Penentuan besar sampel dilakukan berdasarkan SOP (Standard Operational Procedure) yang ada di Laboratorium Pusat Penyakit Tropis, Universitas Airlangga.
Jumlah pengulangan yang dilakukan pada penelitian ini menggunakan rumus Federer (1995):
(t-1) (r-1) ≥ 15 (6-1) x (r-1) ≥ 15 5 x (r-1) ≥ 15
5r – 5 ≥ 15 5r ≥ 20
r ≥ 4
Jumlah perlakuan ulang (r) yang digunakan dalam penelitian ini adalah 4 kali perulangan.
Keterangan:
t : jumlah perlakuan dalam penelitian
a. Penentuan nilai Kadar Hambat Minimum (KHM)
Bahan coba dibagi dalam enam kelompok dan kontrol bahan coba dua kelompok, yaitu:
Kelompok I : ekstrak dengan konsentrasi 100% = 4 sampel
Kelompok II : ekstrak dengan konsentrasi 50 % = 4 sampel
Kelompok III : ekstrak dengan konsentrasi 25 % = 4 sampel
Kelompok IV : ekstrak dengan konsentrasi 12,5 % = 4 sampel
Kelompok V : ekstrak dengan konsentrasi 6,25 % = 4 sampel
Kelompok VI : ekstrak dengan konsentrasi 3,125 % = 4 sampel
Kelompok VII : kontrol Mc Farland = 1 sampel
Kelompok VIII : kontrol negatif (ekstrak daun pegagan tanpa suspensi
F.nucleatum) = 1 sampel
Jumlah sampel = 26 sampel
Dari masing-masing konsentrasi dilakukan dilusi (pengenceran) untuk mendapatkan konsentrasi minimal yang dapat menghambat pertumbuhan bakteri.
b. Penentuan nilai Kadar Bunuh Minimum (KBM)
Dari hasil penentuan nilai KHM diperoleh beberapa kelompok yang dilanjutkan perhitungan jumlah koloni bakteri dengan metode Drop Plate Miles Misra.
Kelompok I : ekstrak dengan konsentrasi 100% = 4 sampel
Kelompok II : ekstrak dengan konsentrasi 50 % = 4 sampel
Kelompok IV : ekstrak dengan konsentrasi 12,5 % = 4 sampel
Kelompok V : ekstrak dengan konsentrasi 6,25 % = 4 sampel
Kelompok VI : ekstrak dengan konsentrasi 3,125 % = 4 sampel
Kelompok VII : kontrol Mc Farland = 1 sampel
Kelompok VIII : kontrol negatif (ekstrak daun pegagan tanpa suspensi
F.nucleatum) = 1 sampel
4.3 Variabel Penelitian
F.nucleatum pada media MHA
dengan penentuan nilai KHM dan KBM
Variabel terkendali
a. Jenis dan asal tumbuhan pegagan (Centella asiatica (L) Urban, Desa Durian, Kec. Pantai Labu, Deli Serdang) b. Berat pegagan sebelum pengeringan (3
kg)
c. Lama penyimpanan pegagan sampai proses ekstraksi (1 minggu)
d. Waktu dan suhu pengeringan pegagan (3 hari, 40°C)
e. Berat pegagan setelah pengeringan (390 gram)
f. Jenis etanol yang digunakan (etanol 96%) g. Jumlah etanol yang digunakan (12 L) h. Waktu dan suhu perendaman (1 jam,
25°C)
i. Waktu pada saat maserasi (24 jam)
j. Nomor kertas saring yang digunakan (Whatman no.42)
k. Jumlah kertas saring saat perkolasi (3 lapis)
l. Kecepatan tetes cairan dalam perkolator (20 tetes/menit)
m. Suhu penguapan dengan rotavapor (46°C) n. Waktu penguapan rotavapor (20jam) o. Media pertumbuhan bakteri yaitu MHA
dan MHB
p. Sterilisasi alat, bahan coba dan media
q. F.nucleatum ATCC 25586
r. Jumlah bahan coba yang diteteskan ke MHA dan MHB (MHA=50 µl, MHB=1 ml)
s. Suhu inkubasi (370 C)
t. Teknik pembiakan F.nucleatum
u. Waktu pembiakan F.nucleatum (24 jam)
Variabel tidak terkendali a. Lingkungan (kondisi tanah dan
iklim) tempat tumbuh pegagan. b. Perlakuan terhadap pegagan
selama tumbuh.
c. Suhu penyimpanan pegagan sebelum dilakukan ekstraksi. d. Waktu dan suhu saat pengiriman
bahan coba sampai ke
4.3.1 Variabel bebas
Ekstrak etanol pegagan 100%, 50%, 25%, 12,5%, 6,25%, dan 3,125%.
4.3.2 Variabel tergantung
Pertumbuhan bakteri F.nucleatum pada media MHAdengan penentuan nilai KHM dan KBM.
4.3.3 Variabel terkendali
a. Jenis dan asal tumbuhan pegagan (Centella asiatica (L) Urban, Desa Durian, Kec. Pantai Labu Deli Serdang)
b. Berat pegagan sebelum pengeringan (3 kg)
c. Lama penyimpanan pegagan sampai proses ekstraksi (1 minggu)
d. Waktu dan suhu pengeringan pegagan (3 hari, 40°C) e. Berat pegagan setelah pengeringan (390 gram) f. Jenis etanol yang digunakan (etanol 96%)
g. Jumlah etanol yang digunakan (12 L) h. Waktu dan suhu perendaman (1 jam, 25°C) i. Waktu pada saat maserasi (24 jam)
j. Nomor kertas saring yang digunakan (Whatman no.42) k. Jumlah kertas saring saat perkolasi (3 lapis)
l. Kecepatan tetes cairan dalam perkolator (20 tetes/menit) m. Suhu penguapan dengan rotavapor (46°C)
n. Waktu penguapan rotavapor (20jam)
p. Sterilisasi alat, bahan coba dan media
q. F.nucleatum ATCC 25586
r. Jumlah bahan coba yang diteteskan ke MHA dan MHB (MHA=50 µl,
MHB=1 ml)
s. Suhu inkubasi (370 C)
t. Teknik pembiakan F.nucleatum
u. Waktu pembiakan F.nucleatum (24 jam) v. Waktu pengamatan (24 jam)
w. Keterampilan operator
4.3.4 Variabel tidak terkendali
a. Lingkungan (kondisi tanah dan iklim) tempat tumbuh pegagan.
b. Perlakuan terhadap pegagan selama tumbuh.
c. Suhu penyimpanan pegagan sebelum dilakukan ekstraksi.
4.4Defenisi Operasional
NO VARIABEL DEFINISI OPERASIONAL CARA UKUR SKALA
UKUR kental pegagan dalam 1 ml media MHB
NO VARIABEL DEFINISI OPERASIONAL HASIL
4.5 Bahan dan Alat Penelitianpegagan 4.5.1 Bahan Penelitian
Pegagan 3 kg (Desa Durian, Kecamatan Labuhan Batu, Deli Serdang)
Etanol 96% 12 liter (Kimia Farma, Indonesia)
Aquadest 1 liter (Kimia Farma, Indonesia)
F.nucleatum ATCC 25586 (MediMark®Europe, France)
Media Mueller Hinton Agar (Difco, USA)
NaCl 0,9% 1 liter (Kimia Farma, Indonesia)
4.5.2 Alat Penelitian
Vaccum Rotary Evaporator (Heidolph VV 2000, Germany)
Autoklaf (Tomy, Japan)
Blender (Panasonic, Japan)
Electronic Balance (Ohyo JP2 6000, Japan)
Vortex (Iwaki model TM-100, Japan)
Perkolator
Kertas saring (Whatman no.42, England)
Inkubator CO2 (Sanyo, Japan)
Kapas 250 gr (Bio Panca, Indonesia)
Pipet mikro dan tips (Gilson, France)
Aluminium foil 1 gulung (Total Wrap, Indonesia)
Kertas perkamen 3 kajang
Ose dan Spiritus
Piring petri (Pyrex, Japan)
Kaca pembesar (Ootsuka ENV-CL, Japan)
4.6 Tempat dan Waktu Penelitian
4.6.1 Tempat penelitian: 1. Laboratorium Obat Tradisional Farmasi USU 2. Laboratorium Pusat Penyakit Tropis UNAIR
4.6.2 Waktu penelitian : 6 bulan
4.7 Prosedur Pengambilan dan Pengumpulan Data 4.7.1 Prosedur pembuatan ekstrak pegagan
Pegagan yang dipakai adalah daun yang segar, berwarna hijau. Bahan baku berupa pegagan sebanyak 5 kg dibersihkan dari kotoran, dibuang akar dan stolon,
dicuci bersih, ditimbang 3 kg. Dikeringkan di lemari pengering yang dialaskan kertas perkamen selama 3 hari pada suhu 40°C (Gambar 6). Tanaman dikatakan kering apabila bagian tanaman hancur ketika diremas. Sampel yang telah kering dihaluskan
dengan blender dan didapat serbuk simplisia 390 gr lalu disimpan dalam plastik tertutup (Gambar 7). Pada wadah dimasukkan serbuk simplisia dan tambahkan etanol
96% sebanyak 1,5 liter untuk perendaman, lalu ditutup, diamkan selama satu jam dengan suhu 25°C. Pada bagian dasar perkolator diberi kapas dan dilapisi dengan kertas saring 2 lembar, kemudian massa dipindahkan sedikit demi sedikit ke dalam
dibiarkan menetes dengan kecepatan ±20 tetes/menit, etanol 96% ditambahkan
berulang-ulang secukupnya hingga terdapat selapis cairan penyari diatas simplisia (Depkes RI,2000). Jumlah keseluruhan etanol yang digunakan 12 liter, menghasilkan
ekstrak cair 10 liter. Ekstrak cair diuapkan dengan alat vacuum rotavapor pada suhu 46ºC, 5 jam/hari untuk 20 jam selama 4 hari (Gambar 8) hingga diperoleh ekstrak kental hijau kehitaman 98 gram. Ekstrak kental pegagan dimasukkan ke dalam botol
kaca tertutup, disimpan di tempat yang sejuk (Gambar 9).
Gambar 7. Pegagan dihaluskan menjadi serbuk dan disimpan dalam plastik tertutup
Gambar 8. Pegagan dilakukan (a) perendaman, (b) perkolasi dan (c) evaporasi Gambar 6. Pegagan ditimbang dan dikeringkan dalam lemari pengering
4.7.2 Pengenceran bahan coba
Ekstrak pegagan ditimbang memakai electronic balance dan massanya disesuaikan dengan konsentrasi yang diinginkan dengan cara dilarutkan dengan
media Mueller Hinton Broth (MHB). Sediakan 6 buah tabung, pada masing – masing tabung berisi 1 ml MHB. Pada tabung pertama diisi 1 gram ekstrak kental pegagan
kemudian dicampur dengan menggunakan vorteks. Dari tabung pertama diambil setengahnya yaitu 1 ml campuran diisi ke tabung-2, dari tabung-2 diambil lagi setengahnya yaitu 1 ml campuran ke tabung-3, dan seterusnya sampai tabung-6
sehingga dihasilkan konsentrasi 100%, 50%, 25%, 12,5%, 6,25%, dan 3,125%. Masing-masing konsentrasi diberi label.
4.7.3 Penyiapan suspensi bakteri a. Pembuatan media bakteri
Sebelum spesimen dibiakkan, dibuat media MHA sebanyak 12 gram
dilarutkan kedalam 240 ml aquadest untuk 40 petri, lalu dipanaskan diatas tungku pemanas magnetik sampai mendidih. Kemudian media yang telah masak, disterilkan
disterilkan, media disimpan didalam lemari pendingin. Jika akan digunakan kembali,
media dipanaskan kembali hingga mendidih lalu dituangkan kedalam masing - masing petri (20 ml/petri) dan dibiarkan hingga dingin.
b. Pembiakan spesimen
Kegiatan pembiakan spesimen dilakukan dalam suasana anaerob pada inkubator CO2. F.nucleatum yang digunakan adalah spesimen stem-cell F.nucleatum
ATCC 25586 yang telah dibiakkan secara murni pada media MHA (Gambar 10) yang telah disiapkan pada prosedur sebelumnya dalam suasana anaerob. Sebanyak 1-2 ose
dari biakan murni bakteri uji yang telah dikultur dan tumbuh dengan subur disuspensikan dengan menggunakan larutan NaCl 0,9% sampai diperoleh kekeruhan sesuai standar 0,5 Mc Farland atau sebanding dengan jumlah bakteri 1 x 108
CFU/mL.
Gambar 10. Koloni bakteri F.nucleatum pada MHA
4.7.4 Penentuan KHM dan KBM bahan coba a. Penentuan KHM bahan coba
dipersiapkan sebelumnya dengan menggunakan mikropipet (Gambar 11a) lalu
dimasukkan ke dalam masing-masing tabung bahan coba kemudian dicampur menggunakan vorteks (Gambar 11b). Lalu tabung-tabung tersebut diinkubasi pada
suhu 37ºC selama 24 jam pada inkubator CO2 (Gambar 11c) dan diamati kekeruhan yang terjadi dengan bantuan spektrofotometer, lalu bandingkan tabung-tabung tersebut dengan kontrol Mc Farland untuk menentukan nilai KHM dari
masing-masing bahan coba. Tabung dengan kekeruhan yang mulai tampak jernih untuk setiap kelompok perlakuan merupakan KHM yaitu konsentrasi minimal ekstrak atau bahan
uji apapun yang mampu menghambat pertumbuhan F.nucleatum dalam media perbenihan setelah diinkubasi 24 jam dan secara visual dapat diamati.
Gambar 11. (a) Mikropipet dan tips (b) vorteks (c) inkubator CO2
b. Penentuan KBMbahan coba
Hasil pengujian penentuan nilai KHM tidak terlihat larutan yang mulai tampak jernih sehingga semua kelompok larutan dilanjutkan dengan perhitungan
jumlah koloni bakteri, yaitu pada konsentrasi 100%, 50%, 25%, 12,5%, 6,25%, dan 3,125% dengan metode Drop Plate Miles Misra. Setelah itu, bahan coba dengan konsentrasi diatas dicampur menggunakan vorteks dan diambil 50 µl untuk tiap
konsentrasi lalu diteteskan ke dalam media padat Mueller Hinton Agar, direplikasi 4
petri, diamkan selama 15-20 menit sampai mengering dan diinkubasi dalam inkubator CO2 dengan suhu 37ºC selama 24 jam. Dilakukan perhitungan jumlah koloni bakteri
untuk mendapatkan nilai KBM dengan bantuan kaca pembesar.
Jumlah koloni bakteri dihitung dengan prinsip satu sel bakteri hidup bila
dibiakkan pada media padat akan tumbuh menjadi 1 koloni bakteri. Yang dimaksud dengan koloni adalah sel bakteri yang membentuk suatu populasi.Gambar 13 adalah berbagai bentuk koloni untuk dihitung, dengan syarat yaitu (a) satu koloni dihitung
satu koloni, (b) dua koloni yang bertumpuk dihitung satu koloni, (c) beberapa koloni yang berhubungan dihitung satu koloni, (d) dua koloni yang berhimpitan dan masih dapat dibedakan dihitung dua koloni, (e) koloni yang terlalu besar (lebih besar dari
setengah luas cawan) tidak dihitung, (f) koloni yang besarnya kurang dari setengah luas cawan dihitung satu koloni.
a
b
c
d
Gambar 13. Bentuk koloni pada media padat Gambar 12. Kaca pembesar
e
Satuan yang dipakai adalah Colony Forming Unit (CFU)/ml cairan (suspensi).
Setelah dihitung jumlah koloni bakteri pada masing-masing tetesan, kemudian dibuat jumlah rata-ratanya dan dikalikan dengan faktor pengenceran dan faktor pangali.
Oleh karena itu, karena pada penelitian konsentrasi yang dilakukan perhitungan jumlah koloni bakteri merupakan konsentrasi awal (sebelum dilakukan dilusi) maka faktor pengenceran x 1, selain itu karena pada penetesan suspensi bahan coba dan
bakteri pada media padat sebanyak 50 µl, maka hasil perhitungan harus dikali dengan faktor pengali 20 untuk mendapatkan hasil sesuai satuan standard (CFU/ml).
Contoh cara perhitungan koloni pada semua kelompok metode Drop Plate Miles Misra adalah :
Pada media padat ditetesi dengan bahan coba 50 µl dan diinkubasi 24 jam.
Dilakukan perhitungan jumlah koloni dengan bantuan kaca pembesar. Jika pada tetesan berjumlah 5 koloni.
Maka jumlah kuman pada sampel cair tersebut adalah :
5 x 1 (faktor pengenceran) x 20 (faktor pengali) = 100 CFU / ml
4.7.5. Analisis Data
Data hasil pengujian antibakteri dianalisis dengan memakai uji statistik sebagai berikut:
1. Uji analisis varian satu arah (ANOVA), untuk melihat perbedaan efek antibakteri ekstrak etanol pegagan terhadap pertumbuhan F.nucleatum.
2. Uji Least Significant Difference (LSD), untuk melihat perbedaan efek
BAB 5
HASIL PENELITIAN
5.1 Ekstraksi Pegagan (Centella asiatica (L.) Urban)
Ekstak etanol pegagan berasal dari 390 gram serbuk simplisia yang dilarutkan dengan pelarut etanol 96% kemudian diuapkan dengan vaccum rotary evaporator
sehingga diperoleh ekstrak kental berwarna hijau kehitaman sebanyak 98 gram.
Ekstrak kental dimasukkan ke dalam botol kaca tertutup dan disimpan dalam lemari pendingin.
Gambar 14. Ekstrak kental pegagan 98 gram
5.2 Uji Efektifitas Antibakteri
Pada penentuan KHM yang dilihat adalah tabung perlakuan yang mulai
tampak jernih bila dibandingkan dengan kontrol. Dari hasil pengujian antibakteri ekstrak pegagan terhadap F.nucleatum setelah dicampur menggunakan vorteks dan diinkubasi selama 24 jam, didapat bahwa tidak ada larutan yang mulai tampak jernih,
dibandingkan dengan kontrol Mc Farland, sehingga nilai KHM dalam penelitian ini
tidak dapat ditentukan.
Pada penentuan KBM, yang dicari adalah konsentrasi minimal yang dapat membunuh bakteri pada media MHA (steril). Hasil pada uji antibakteri juga didapat
pada konsentrasi 100% - 6,25% (Gambar 16a) memperlihatkan zona bening yang tidak dijumpai pertumbuhan koloni bakteri atau senilai 0 CFU/ml yang menunjukkan
bahwa pada konsentrasi ini sudah mampu memberikan efek antibakteri, sedangkan pada konsentrasi 3,125% dijumpai adanya pertumbuhan bakteri (Gambar 16b-e) dengan rata-rata pertumbuhan bakteri sebesar 110 CFU/ml (Tabel 3).
Gambar 16. Koloni bakteri pada media MHA dengan konsentrasi (a) 100%-6,25%. Konsentrasi 3,125% (b) replikasi I (c) replikasi II (d) replikasi III (e) replikasi IV
Gambar 15. (a) Media MHB sebelum diberi perlakuan (b) Suspensi bakteri setelah diberi perlakuan
b
a b
e d
a
Tabel 3 menunjukkan pada pengujian antibakteri dengan menghitung jumlah
koloni F.nucleatum, konsentrasi terkecil yang mampu membunuh bakteri 99,9% adalah pada konsentrasi 6,25% dengan jumlah bakteri 0 CFU/ml (steril).
Tabel 3. HASIL PERHITUNGAN JUMLAH BAKTERI FUSOBACTERIUM NUCLEATUM SETELAH PERLAKUAN
Dapat disimpulkan bahwa KBM dari bahan coba ekstrak pegagan terhadap
F.nucleatum adalah 6,25%. Data hasil pengujian antibakteri tidak dapat dilakukan uji statistik ANOVA dan LSD karena nilai perhitungan koloni bakteri adalah 0 CFU/ml
yang artinya tidak dijumpai pertumbuhan bakteri dalam media perbenihan atau bakteri yang berkontak dengan bahan coba 100% mengalami kematian.
Bahan Uji Repli
BAB 6 PEMBAHASAN
Penelitian ini menggunakan pegagan 3 kg karena setiap bahan alam yang telah
dikeringkan akan didapat berat kering 10% - 12% dari berat awal sebelum dikeringkan. Pegagan 3 kg setelah pengeringan menjadi 300 – 400 gram, berat ini cukup untuk ditampung oleh perkolator dan juga untuk mendapatkan ekstrak yang
cukup untuk dilakukan pengujian aktivitas antibakteri. Pelarut etanol 96% digunakan karena relatif lebih aman (tidak bersifat toksik) dan sifatnya yang universal, dapat
melarutkan hampir seluruh bahan aktif yang terkandung dalam suatu bahan alami.22 Pada pengujian aktivitas antibakteri ekstrak etanol pegagan terhadap
F.nucleatum, ada dua metode untuk menentukan aktivitas antibakteri, yaitu diffusion
test dan dilution test. Pada metode difusi, digunakan paper disk yang diberi antibiotik dan diletakkan diatas agar media yang telah ditanam bakteri, agen antimikroba
tersebut akan berdifusi sehingga zona hambat akan terbentuk disekitar disk dan diukur zona hambatnya. Metode ini tergantung pada kelarutan dan difusi bahan coba sehingga kurang efektif untuk menghambat mikroorganisme. Disamping itu, metode
ini tidak mampu memberikan data yang tepat mengenai tingkat resisten atau kerentanan dari mikroorganisme.20
Metode dilusi dilakukan dengan pengenceran ganda dari konsentrasi awal, sehingga konsentrasi yang didapat adalah setengah dari konsentrasi awal sebelumnya.
metode dilusi untuk menguji daya antibakteri ekstrak etanol pegagan. Pada metode
dilusi ini, digunakan media Mueller Hinton karena merupakan media standar yang digunakan untuk menguji bakteri secara dilusi.20 Kandungan dari Mueller Hinton
adalah pepton (6 g), kasein (17,5 g), pati (1,5 g) dan agar (10 g). Kandungan ini diperlukan oleh F.nucleatum untuk tumbuh karena biasanya F.nucleatum tumbuh pada media yang mengandung pepton atau ekstrak ragi, trypticase.8
Hasil pengujian antibakteri dalam berbagai konsentrasi, bahwa nilai KHM tidak dapat ditentukan karena masih terjadi kekeruhan atau tidak ada tabung hasil
biakan yang mulai tampak jernih. Kekeruhan ini kemungkinan terjadi karena ekstrak pegagan yang memiliki warna hijau kehitaman dan setelah disuspensikan dengan
bakteri akan menjadi hijau keruh karena terdapatnya bakteri sehingga sulit untuk menentukan konsentrasi yang mulai tampak jernih. Selain itu, pegagan mengandung senyawa zat aktif steroid yang tidak larut dalam pelarut polar (bersifat non polar)
yang bila diencerkan dengan Mueller Hinton Broth (bersifat polar) maka akan terjadi kekeruhan yang dikarenakan adanya pemisahan dari zat aktif steroid dengan MHB.40 Dengan adanya kekeruhan ini maka nilai KHM tidak dapat diketahui, sehingga
diperlukan penelitian dengan metode lain untuk mendapatkan nilai KHM yaitu metode difusi dengan mengukur zona hambat.
Konsentrasi 100% (sangat kental) akan secara langsung membunuh bakteri
F.nucleatum karena tingginya konsentrasi antibakteri yang terkandung didalamnya. Begitu juga yang terjadi pada konsentrasi 50%, 25%, 12,5%, 6,25% tidak dijumpai
yang dilakukan akhirnya mampu mengurangi daya hambat bahan uji terhadap
pertumbuhan bakteri sehingga terlihat adanya pembentukan koloni bakteri 6.101 CFU/ml pada replikasi 1. Maka hipotesa pertama yaitu ada efek antibakteri ekstrak
etanol pegagan terhadap F.nucleatum diterima, hal ini terbukti dengan diperolehnya nilai KBM yaitu pada konsentrasi 6,25%. Dari data hasil penelitian tidak dapat dilakukan uji statistik dengan ANOVA dan LSD karena nilai perhitungan koloni
bakteri pada konsentrasi 100% - 6,25% adalah 0 CFU/ml, yang artinya tidak dijumpai pertumbuhan bakteri dalam media perbenihan atau bakteri yang berkontak dengan
bahan coba 100% mengalami kematian.
Efek antibakteri dari ekstrak pegagan dikarenakan banyaknya senyawa aktif
yang terkandung didalamnya yaitu alkaloid, saponin, tanin dan flavonoid yang berperan dengan mengganggu fungsi membran atau dinding sel bakteri F.nucleatum. Alkaloid mengganggu komponen penyusun peptidoglikan pada sel bakteri, sehingga
lapisan dinding sel tidak terbentuk secara utuh dan menyebabkan kematian sel.38 Asiatikosida dan asam asiatat termasuk ke dalam golongan saponin.17 Mekanisme saponin ini yaitu dengan membentuk senyawa kompleks dengan membran sel melalui
ikatan hidrogen sehingga mengganggu integritas membran sel dan akhirnya bakteri akan mengalami kematian.39 Mekanisme tanin diperkirakan adalah sebagai berikut:
toksisitas tanin dapat merusak membran sel bakteri, senyawa astringent tanin dapat menginduksi pembentukan kompleks senyawa ikatan terhadap enzim atau substrat mikroba dan pembentukan suatu kompleks ikatan tanin terhadap ion logam yang
itu sendiri. Akibatnya sel tidak dapat melakukan aktivitas hidup sehingga
pertumbuhannya terhambat atau bahkan mati. Flavonoid akan mengganggu integritas membran sel bakteri dengan membentuk senyawa kompleks terhadap protein
ekstraseluler.38
Bahan alam yang juga diteliti sebagai bahan medikamen diantaranya adalah
Aloe vera dan buah mahkota dewa.11,12 Penelitian yang dilakukan oleh Rahma (2009)
mengenai ekstrak etanol Aloe vera didapat nilai KBM untuk F.nucleatum yaitu pada konsentrasi 50%.11 Penelitian yang dilakukan oleh Kere CM (2011) mengenai ekstrak
etanol buah mahkota dewa terhadap F.nucleatum dengan nilai KBM 3,125%.12 Nilai KBM yang diperoleh berbeda, hal ini dikarenakan setiap bahan alam memiliki
kandungan senyawa aktif yang berbeda (Tabel 4).
Tabel 4. KANDUNGAN SENYAWA DARI BAHAN ALAM SEBAGAI ALTERNATIF MEDIKAMEN SALURAN AKAR11,12
Bahan alam sebagai alternatif medikamen saluran akar
Aloe vera Buah mahkota dewa Pegagan
KBM
terhadap F.nucleatum 50 % 3,125 % 6,25 %
Kandungan senyawa Tanin, antrakuinon
dan saponin
Polifenol, saponin, alkaloid, tanin
alkaloid, saponin, tanin dan flavonoid
Ekstrak pegagan memiliki aktifitas antimikroba yang juga dibuktikan oleh
Jagtap et al (2009) dengan menggunakan metode difusi yaitu pengukuran zona hambat, dengan nilai KHM 125 µg/ml terhadap bakteri P.vulgaris, S.aureus, E.coli;
dan pada bakteri B.subtilis dengan nilai KHM 62,5 µg/ml. Pada penelitian Jagtap,
mm, sedangkan E.coli mempunyai efek antibakteri paling lemah dengan zona hambat
6 mm.18
Nilai yang diperoleh peneliti berbeda dengan Jagtap, hal ini terjadi karena
metode yang digunakan berbeda, Jagtap menggunakan metode difusi, yaitu dengan mengukur zona hambat yang terbentuk disekitar disk dan didapat nilai KHM, sedangkan pada penelitian ini menggunakan metode dilusi dengan mencari nilai
KHM dan KBM. Metode ini dianggap lebih baik daripada metode difusi karena pada metode dilusi bahan coba langsung berinteraksi dengan bakteri tanpa dipengaruhi
oleh media padat (disk). Pada metode difusi, bahan uji tidak mudah berdifusi melewati disk oleh karena kekentalannya sehingga akan berpengaruh pada daya
hambat bakteri.
Perbedaan daerah dan keadaan geografis tanah juga berpengaruh, pada penelitian Jagtap tanaman pegagan berasal dari Amravati (India), sedangkan pada
penelitian ini pegagan yang digunakan berasal dari Desa Durian, Kec. Pantai Labu, Deli Serdang (Indonesia). Adanya perbedaan daerah dan keadaan geografis tanah akan memberikan pengaruh pada kandungan senyawa aktif yang terdapat dalam
Centella asiatica.35
Bakteri yang diuji berbeda, Jagtap meneliti bakteri lain, sedangkan pada
penelitian ini meneliti bakteri F.nucleatum yang tidak diteliti oleh Jagtap. Bakteri
B.subtilis adalah bakteri gram positif sedangkan bakteri F.nucleatum dan E.coli
merupakan bakteri gram negatif. Adanya perbedaan struktur dinding sel bakteri yaitu
dibandingkan dengan bakteri gram positif (Gambar 17) sehingga kemungkinan
kandungan senyawa pegagan akan sulit untuk menghambat bakteri gram negatif. Bakteri gram positif, memiliki selubung sel yang lebih sederhana yaitu lapisan
membran sitoplasma, peptidoglikan, dan lapisan S atau kapsul. Komponen dinding sel gram positif terdiri dari teichoic, teichuronic acid dan polisakarida. Pada bakteri gram negatif memiliki selubung sel yang lebih kompleks yaitu lapisan membran
sitoplasma, ruang periplasma, membran luar dan lapisan S atau kapsul. Komponen dinding sel gram negatif terdiri dari ruang periplasma, membran luar, lipoprotein dan
lipopolisakarida (LPS). 19,41
Penelitian ini membuktikan bahwa ekstrak etanol pegagan memiliki efek
antibakteri secara in-vitro. Hal ini kemungkinan akan berbeda hasilnya dalam saluran akar karena bakteri yang terdapat dalam infeksi saluran akar ialah polimikrobial maka kedepannya perlu dilakukan penelitian lebih lanjut sehingga pegagan dapat digunakan
sebagai bahan medikamen saluran akar secara klinis.
Gambar 17. Struktur sel bakteri: (A) gram positif dan (B) gram negatif 41 B
BAB 7
KESIMPULAN DAN SARAN
7.1Kesimpulan
Berdasarkan hasil penelitian efek antibakteri ekstrak etanol pegagan terhadap
F.nucleatum (secara in-vitro) dapat disimpulkan bahwa ekstrak etanol pegagan mempunyai efek antibakteri terhadap F.nucleatum dengan nilai KBM 6,25% jumlah
koloni 0 CFU/ml, dan nilai KHM tidak dapat ditentukan dalam penelitian ini karena tidak dapat dibedakan kekeruhannya.
7.2 Saran
1. Perlu dilakukan pengujian ekstrak etanol 96% pegagan dengan metode lain untuk mendapatkan nilai KHM.
2. Perlu dilakukan penelitian untuk mengetahui nilai KBM yang benar-benar minimal terhadap bakteri F.nucleatum antara range 6,25% - 3,125% dalam
membunuh bakteri 99,9%.
3. Perlu dilakukan uji fitokimia pada ekstrak etanol pegagan untuk mengetahui senyawa zat aktif mana yang memiliki aktifitas antibakteri paling besar.
4. Perlu dilakukan penelitian dengan menguji efek antimikrobial pegagan terhadap mikroba lain yang patogen dalam saluran akar.
5. Perlu dilakukan penelitian dengan membandingkan konsentrasi senyawa aktif berdasarkan daerah asal dan geografis tanah tempat tumbuhnya pegagan.
6. Dilakukan penelitian lebih lanjut untuk mengetahui efek pegagan secara
ekstrak pegagan dapat dikembangkan sebagai alternatif medikamen saluran akar dari
DAFTAR PUSTAKA
1. Athanassiadis B, Abbot PV, Walsh LJ. The use of calcium hydroxide, antibiotics and biocides as antimicrobial medicaments on endodontics. Aust
Dent J 2007; 52(1): 864-82.
2. Ingle, Bakland, Baumgartner. Ingle Endodontics 6. India : BC Decker, 2008:
992-1011.
3. Walton RE, Torabinejad M, eds Sumawiranata N, Juwono L. Prinsip dan Praktik Ilmu Endodonsia. Edisi 3. Jakarta: EGC, 2008: 259-61.
4. Hauman CHJ, Love RM. Biocompatibility of dental materials used in contemporary endodontic therapy: a review. Part 1. Intracanal drugs and
substances. Int Endod J 2003; 36: 75-85.
5. Sharma S, Webb R, Macpherson D, Wilson A. Severe tissue necrosis following intra-arterial injection of endodontic calcium hydroxide: a case series. Oral
Surg Oral Med Oral Pathol Oral Radiol Endod 2008; 105: 666-9.
6. Siqueira JF, Pinto TG, dan Rocas IN. Effect of Chemomechanical Preparation
with 2.5% Sodium Hypochlorite and Intracanal Medication with Calcium
Hydroxide on Cultivable Bacteria in Infected Root Canals. J.Endod 2007;
33(7): 800-5.
7. Ingle, Bakland. Endodontics. Edisi 5. USA: BC Decker, 2002: 63-7.
8. Bolstad Al, Jensen HB, Bakken V. Taxonomy, Biology, and Periodontal aspect