PENGARUH LOGAM BERAT
TERHADAP PERTUMBUHAN MIKROORGANISME PENDEGRADASI MINYAK DIESEL
Oleh
RATNA MAHMUDAH KURNIASARI F34101044
2005
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
PENGARUH LOGAM BERAT
TERHADAP PERTUMBUHAN MIKROORGANISME PENDEGRADASI MINYAK DIESEL
SKRIPSI
Sebagai Salah Satu Syarat Untuk Meraih Gelar SARJANA TEKNOLOGI PERTANIAN Pada DepartemenTeknologi Industri Pertanian
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh
RATNA MAHMUDAH KURNIASARI F34101044
Dilahirkan pada tanggal 8 September 1983 Di Ambarawa
Tanggal Lulus : 14 Oktober 2005
Disetujui,
Bogor, November 2005
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
PENGARUH LOGAM BERAT
TERHADAP PERTUMBUHAN MIKROORGANISME PENDEGRADASI MINYAK DIESEL
SKRIPSI
Sebagai Salah Satu Syarat Untuk Meraih Gelar SARJANA TEKNOLOGI PERTANIAN Pada DepartemenTeknologi Industri Pertanian
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh
RATNA MAHMUDAH KURNIASARI F34101044
2005
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
Surat Pernyataan
Saya menyatakan dengan sebenar-benarnya bahwa skripsi dengan judul:
“PENGARUH LOGAM BERAT TERHADAP PERTUMBUHAN
MIKROORGANISME PENDEGRADASI MINYAK DIESEL”
adalah karya asli saya sendiri dengan arahan dosen pembimbing akademik, kecuali yang dengan jelas ditunjukkan rujukannya.
Bogor,
Yang membuat pernyataan
RATNA MAHMUDAH KURNIASARI. F34101044. Pengaruh Logam Berat Terhadap Pertumbuhan Mikroorganisme Pendegradasi Minyak Diesel. Dibawah bimbingan Mohamad Yani. 2005.
RINGKASAN
Bahan bakar minyak merupakan sumber energi utama yang digunakan dalam rumah tangga, industri dan transportasi. Pencemaran minyak bumi dapat terjadi akibat penanganan yang tidak terkontrol, sehingga akan menjadi limbah yang berbahaya. Pencemaran minyak bumi ini sering diikuti dengan pencemaran logam berat. Pencemaran logam berat masuk ke atmosfer, tanah dan perairan melebihi kemampuan alamiah untuk memprosesnya. Bioremediasi merupakan salah satu proses pengolahan limbah B3 (Bahan Berbahaya dan Beracun) dengan menggunakan mikroorganisme.
Pseudomonas pseudomallei (PP) dan Enterobacter agglomerans (EA) merupakan mikroorganisme yang mampu mendegradasi hidrokarbon minyak diesel, namun belum diketahui kemampuannya terhadap kehadiran logam berat. Penelitian ini bertujuan untuk mengukur pengaruh konsentrasi logam berat terhadap pertumbuhan kedua isolat tersebut pada media dengan sumber karbon minyak diesel.
Logam berat yang ditambahkan meliputi logam seng (Zn), timbal (Pb), besi (Fe) dan merkuri (Hg). Konsentrasi logam ditambahkan secara bertahap hingga isolat tidak mampu tumbuh lagi. Kecepatan proses degradasi minyak diesel dapat dilihat secara visual dengan terbentuknya butiran-butiran antara minyak diesel dengan air. Pengaruh interaksi antara dua logam berat, yaitu logam Zn dengan Pb, dilakukan pada kombinasi isolat PPEA dengan mengukur optical density (OD), jumlah sel, biomassa kering, kinetika pertumbuhan dan nilai pH.
Pseudomonas pseudomallei dan Enterobacter agglomerans biasanya tumbuh hingga 1011 - 1012 cfu/ml pada media dengan penambahan minyak diesel 10%. Pada media dengan penambahan logam Zn 2000 ppm, logam Pb 3000 ppm, logam Fe 4000 ppm dan logam Hg 50 ppm, rata-rata jumlah sel yang mampu tumbuh mencapai 106 - 107 cfu/ml. Pada media yang mengandung logam Zn, Pb, Fe 8000 ppm dan logam Hg 150 ppm, isolat hanya mampu tumbuh 102 cfu/ml. Logam Hg merupakan logam yang paling toksik bagi pertumbuhan isolat, karena pada konsentrasi 200 ppm, isolat tidak mampu tumbuh. Pertumbuhan spesifik maksimal (µx-maks) cenderung menurun dengan kenaikan konsentrasi logam
berat.
RATNA MAHMUDAH KURNIASARI. F34101044. Effect of Heavy Metals to Growth of Diesel Oil Degradating Microorganism. Supervised by Mohamad Yani. 2005.
SUMMARY
Peoples need oil as energy source for household, transportation and industries. In out of control situation, oil pollution can occur and may cause environmental contamination. Oil contamination often followed by heavy metals contamination. Heavy metals contamination release to atmosphere, territorial water and land. Bioremediation is the application of biological process to the treatment of ground water, soil and sludge contaminated with hazardous waste.
Pseudomonas pseudomallei (PP) and Enterobacter agglomerans (EA) known as diesel oil degradating microorganism. The research objective is to assess the effect of heavy metals to both of these inoculant on medium with diesel oil as a carbon source.
Zinc, plumbum, iron and mercury as heavy metals were tested. These metals concentration have been tested step by step untill the inoculant unable to grow anymore. Degradation of diesel oil ca n be observed visually by globular forms between diesel oil and water. Effect of interaction between two heavy metal, zinc (Zn) and plumbum (Pb), have been observed using combination of PPEA by measuring optical density (OD), the number of cells, dried biomass, growth kinetics and pH value.
Pseudomonas pseudomallei and Enterobacter agglomerans usually grow about 101 1-101 2 cfu/ml in media containing 10% diesel oil. If media containing 2000 ppm of Zn, 3000 ppm of Pb, 4000 ppm of Fe and 50 ppm of Hg, they can grow about 106-107 cfu/ml. If media containing 8000 ppm of Zn, Pb, Fe and 150 ppm of Hg, they can grow about 102 cfu/ml. The Hg is the most toxic metal for inoculant growth, because at 200 ppm concentration, the inoculant can not grow anymore. Maximum specific growth ( ìx-maks) tend to decrease with the increasing of heavy metals concentration in media.
RIWAYAT HIDUP
Penulis dilahirkan pada tanggal 8 September 1983 di sebuah kota kecil Ambarawa. Pada tahun 1995, penulis menyelesaikan pendidikan Sekolah Dasar dari SD Negeri Salatiga 06, kemudian melanjutkan pendidikan ke SMP Negeri 1 Salatiga. Penulis menyelesaikan pendidikan Sekolah Menengah Pertama pada tahun 1998.
Pada tahun yang sama, melanjutkan pendidikan ke SMU Negeri 1 Salatiga dan lulus pada tahun 2001. Penulis diterima di Institut Pertanian Bogor pada Departemen Teknologi Industri Pertanian pada tahun 2001 melalui jalur USMI. Selama di IPB, penulis aktif dalam kegiatan kemahasiswaan terutama pada Himpunan Mahasiswa Teknologi Industri (Himalogin ). Tahun 2002, penulis menjadi pengurus Himalogin pada Departemen Agroindustri dan pada tahun 2003, penulis diberi amanah sebagai ketua Departemen Kewirausahaan. Selain itu, penulis juga aktif dalam kepengurusan Unit Kegiatan Mahasiswa (UKM) Zingiber (Komunitas Peduli Tanaman Obat) pada Departemen Public Relation. Pada tahun 2004 dan 2005, penulis me mperoleh pendanaan dalam Program Kreativitas Mahasiswa (PKM) yang diselenggarakan oleh DIKTI. Penulis juga pernah mengikuti lomba Inovasi Bisnis Pemuda yang diselenggarakan oleh DIKTI pada yahun 2003 dan 2004, mengikuti lomba penulisan karya ilmiah tentang pengelolaan lingkungan, yang diselenggaran oleh Bayer (2004), BRI (2004) dan Panasonic (2005). Selama tahun 2003 dan 2004 memperoleh beasiswa supersemar.
KATA PENGANTAR
Tiada kata yang terucap selain rasa syukur kepada Allah, dengan ucapan alhamdulillah, karena penulis yakin hanya dengan ijin Allah, penulis dapat menyelesaikan skripsi yang disusun berdasarkan hasil penelitian laboratorium mengenai pengaruh logam berat terhadap pe rtumbuha n mikroorganisme. Skripsi ini berjudul “Pengaruh Logam Berat Terhadap Pertumbuhan Mikroorganisme Pendegradasi Minyak Diesel”.
Dapat diselesaikannya skripsi ini berkat bimbingan, dorongan, dan bantuan dari berbagai pihak, oleh karena itu penulis mengucapka n terima kasih yang tulus kepada
1. Dr. Ir. Mohamad Yani, M.Eng selaku pembimbing akademik yang telah memberikan arahan dan bimbingan dengan bijak.
2. Dr. Ir. Nastiti Siswi Indrasti dan Drs. Purwoko M.Si selaku dosen penguji, yang telah memberikan arahan, bimbin gan dan saran.
3. Seluruh staf laboratorium Tekonologi Industri Pertanian yang telah banyak membantu dengan sabar.
4. Bapak dan Ibu beserta seluruh keluarga atas doa dan dorongannya. 5. Semua teman-teman yang telah banyak membantu dalam pelaksanaan
penelitian, terutama teman-teman di laboratorium bioindustri.
6. Teman-teman ‘TIN 38’, terima kasih untuk hari-hari yang telah kita lalui bersama, suka dan duka.
Ibarat pepatah, tiada gading yang tak retak, penulis menyadari bahwa masih terdapat kekurangan dalam penyusunan dan penulisan skripsi ini. Oleh karena itu, penulis mengharapkan masukan, kritik dan saran yang bersifat membangun untuk sempurnanya laporan skripsi ini. Namun terlepas dari semua itu, penulis berharap semoga skripsi ini dapat bermanfaat bagi semua pihak ya ng membutuhkan.
Bogor, Oktober 2005
Penulis
DAFTAR ISI
KATA PENGANTAR ……… vii
DAFTAR TABEL ... x
DAFTAR GAMBAR ... xi
DAFTAR LAMPIRAN ………. xii
I. PENDAHULUAN A. LATAR BELAKANG... 1
B. TUJUAN ... 3
II. TINJAUAN PUSTAKA A. LOGAM BERAT... 4
1. Toksisitas Logam Berat … ... 5
2. Akumulasi Logam Berat Pada Mikroorganisme ... 6
B. MINYAK BUMI ... 7
1. Jenis Hidr okarbon Dalam Minyak Bumi . ... 8
2. Minyak Diesel . ... 9
C. BIOREMEDIASI ……… 10
1. Faktor Fisiko Kimia Dalam Bioremediasi ……….. 12
a. Kadar air ……….. 13
b. Temperatur ……….. 13
c. Oksigen ……… 13
d. Nutrien ………. …………14
e. Surfaktan ………. ………….14
f. pH ………. …………15
2. Degradasi Minyak Diesel ………... 15
D. MIKROORGANISME ……….. …………16
III. METODOLOGI A. BAHAN DAN ALAT ……… 17
B. METODOLOGI PENELITIAN ……… 17
2...
Penambahan Logam Berat Dalam Berbagai Konsentrasi ...18
3... Pengaruh Interaksi Logam Antara Zn-Pb ...19
4... Pola Akumulasi Logam Berat ...20
IV HASIL DAN PEMBAHASAN A. PEMELIHARAAN ISOLAT DAN DEGRADASI MINYAK DIESEL .22 B. PENGARUH LOGAM BERAT PADA PERTUMBUHAN BAKTERI .25 1. Pengaruh Logam Berat Seng (Zn) ... 27
2. Pengaruh Logam Berat Timbal (Pb) ... 28
3. Pengaruh Logam Besi (Fe) ...29
4. Pengaruh Logam Merkuri (Hg) ... 31
C. INTERAKSI ANTARA LOGAM SENG (Zn) DAN TIMBAL (Pb) ...33
1. Pertumbuhan Kombinasi Isolat PPEA ...33
2. Kinetika Pertumbuhan Sel ...34
3. Perubahan pH Media Selama Inkubasi ... 35
4. Akumulasi Logam Berat Pada Interaksi Zn-Pb ... 36
V. KESIMPULAN DAN SARAN A. KESIMPULAN ... 38
B. SARAN ... 38
DAFTAR PUSTAKA...39
PENGARUH LOGAM BERAT
TERHADAP PERTUMBUHAN MIKROORGANISME PENDEGRADASI MINYAK DIESEL
Oleh
RATNA MAHMUDAH KURNIASARI F34101044
2005
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
PENGARUH LOGAM BERAT
TERHADAP PERTUMBUHAN MIKROORGANISME PENDEGRADASI MINYAK DIESEL
SKRIPSI
Sebagai Salah Satu Syarat Untuk Meraih Gelar SARJANA TEKNOLOGI PERTANIAN Pada DepartemenTeknologi Industri Pertanian
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh
RATNA MAHMUDAH KURNIASARI F34101044
Dilahirkan pada tanggal 8 September 1983 Di Ambarawa
Tanggal Lulus : 14 Oktober 2005
Disetujui,
Bogor, November 2005
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
PENGARUH LOGAM BERAT
TERHADAP PERTUMBUHAN MIKROORGANISME PENDEGRADASI MINYAK DIESEL
SKRIPSI
Sebagai Salah Satu Syarat Untuk Meraih Gelar SARJANA TEKNOLOGI PERTANIAN Pada DepartemenTeknologi Industri Pertanian
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh
RATNA MAHMUDAH KURNIASARI F34101044
2005
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
Surat Pernyataan
Saya menyatakan dengan sebenar-benarnya bahwa skripsi dengan judul:
“PENGARUH LOGAM BERAT TERHADAP PERTUMBUHAN
MIKROORGANISME PENDEGRADASI MINYAK DIESEL”
adalah karya asli saya sendiri dengan arahan dosen pembimbing akademik, kecuali yang dengan jelas ditunjukkan rujukannya.
Bogor,
Yang membuat pernyataan
RATNA MAHMUDAH KURNIASARI. F34101044. Pengaruh Logam Berat Terhadap Pertumbuhan Mikroorganisme Pendegradasi Minyak Diesel. Dibawah bimbingan Mohamad Yani. 2005.
RINGKASAN
Bahan bakar minyak merupakan sumber energi utama yang digunakan dalam rumah tangga, industri dan transportasi. Pencemaran minyak bumi dapat terjadi akibat penanganan yang tidak terkontrol, sehingga akan menjadi limbah yang berbahaya. Pencemaran minyak bumi ini sering diikuti dengan pencemaran logam berat. Pencemaran logam berat masuk ke atmosfer, tanah dan perairan melebihi kemampuan alamiah untuk memprosesnya. Bioremediasi merupakan salah satu proses pengolahan limbah B3 (Bahan Berbahaya dan Beracun) dengan menggunakan mikroorganisme.
Pseudomonas pseudomallei (PP) dan Enterobacter agglomerans (EA) merupakan mikroorganisme yang mampu mendegradasi hidrokarbon minyak diesel, namun belum diketahui kemampuannya terhadap kehadiran logam berat. Penelitian ini bertujuan untuk mengukur pengaruh konsentrasi logam berat terhadap pertumbuhan kedua isolat tersebut pada media dengan sumber karbon minyak diesel.
Logam berat yang ditambahkan meliputi logam seng (Zn), timbal (Pb), besi (Fe) dan merkuri (Hg). Konsentrasi logam ditambahkan secara bertahap hingga isolat tidak mampu tumbuh lagi. Kecepatan proses degradasi minyak diesel dapat dilihat secara visual dengan terbentuknya butiran-butiran antara minyak diesel dengan air. Pengaruh interaksi antara dua logam berat, yaitu logam Zn dengan Pb, dilakukan pada kombinasi isolat PPEA dengan mengukur optical density (OD), jumlah sel, biomassa kering, kinetika pertumbuhan dan nilai pH.
Pseudomonas pseudomallei dan Enterobacter agglomerans biasanya tumbuh hingga 1011 - 1012 cfu/ml pada media dengan penambahan minyak diesel 10%. Pada media dengan penambahan logam Zn 2000 ppm, logam Pb 3000 ppm, logam Fe 4000 ppm dan logam Hg 50 ppm, rata-rata jumlah sel yang mampu tumbuh mencapai 106 - 107 cfu/ml. Pada media yang mengandung logam Zn, Pb, Fe 8000 ppm dan logam Hg 150 ppm, isolat hanya mampu tumbuh 102 cfu/ml. Logam Hg merupakan logam yang paling toksik bagi pertumbuhan isolat, karena pada konsentrasi 200 ppm, isolat tidak mampu tumbuh. Pertumbuhan spesifik maksimal (µx-maks) cenderung menurun dengan kenaikan konsentrasi logam
berat.
RATNA MAHMUDAH KURNIASARI. F34101044. Effect of Heavy Metals to Growth of Diesel Oil Degradating Microorganism. Supervised by Mohamad Yani. 2005.
SUMMARY
Peoples need oil as energy source for household, transportation and industries. In out of control situation, oil pollution can occur and may cause environmental contamination. Oil contamination often followed by heavy metals contamination. Heavy metals contamination release to atmosphere, territorial water and land. Bioremediation is the application of biological process to the treatment of ground water, soil and sludge contaminated with hazardous waste.
Pseudomonas pseudomallei (PP) and Enterobacter agglomerans (EA) known as diesel oil degradating microorganism. The research objective is to assess the effect of heavy metals to both of these inoculant on medium with diesel oil as a carbon source.
Zinc, plumbum, iron and mercury as heavy metals were tested. These metals concentration have been tested step by step untill the inoculant unable to grow anymore. Degradation of diesel oil ca n be observed visually by globular forms between diesel oil and water. Effect of interaction between two heavy metal, zinc (Zn) and plumbum (Pb), have been observed using combination of PPEA by measuring optical density (OD), the number of cells, dried biomass, growth kinetics and pH value.
Pseudomonas pseudomallei and Enterobacter agglomerans usually grow about 101 1-101 2 cfu/ml in media containing 10% diesel oil. If media containing 2000 ppm of Zn, 3000 ppm of Pb, 4000 ppm of Fe and 50 ppm of Hg, they can grow about 106-107 cfu/ml. If media containing 8000 ppm of Zn, Pb, Fe and 150 ppm of Hg, they can grow about 102 cfu/ml. The Hg is the most toxic metal for inoculant growth, because at 200 ppm concentration, the inoculant can not grow anymore. Maximum specific growth ( ìx-maks) tend to decrease with the increasing of heavy metals concentration in media.
RIWAYAT HIDUP
Penulis dilahirkan pada tanggal 8 September 1983 di sebuah kota kecil Ambarawa. Pada tahun 1995, penulis menyelesaikan pendidikan Sekolah Dasar dari SD Negeri Salatiga 06, kemudian melanjutkan pendidikan ke SMP Negeri 1 Salatiga. Penulis menyelesaikan pendidikan Sekolah Menengah Pertama pada tahun 1998.
Pada tahun yang sama, melanjutkan pendidikan ke SMU Negeri 1 Salatiga dan lulus pada tahun 2001. Penulis diterima di Institut Pertanian Bogor pada Departemen Teknologi Industri Pertanian pada tahun 2001 melalui jalur USMI. Selama di IPB, penulis aktif dalam kegiatan kemahasiswaan terutama pada Himpunan Mahasiswa Teknologi Industri (Himalogin ). Tahun 2002, penulis menjadi pengurus Himalogin pada Departemen Agroindustri dan pada tahun 2003, penulis diberi amanah sebagai ketua Departemen Kewirausahaan. Selain itu, penulis juga aktif dalam kepengurusan Unit Kegiatan Mahasiswa (UKM) Zingiber (Komunitas Peduli Tanaman Obat) pada Departemen Public Relation. Pada tahun 2004 dan 2005, penulis me mperoleh pendanaan dalam Program Kreativitas Mahasiswa (PKM) yang diselenggarakan oleh DIKTI. Penulis juga pernah mengikuti lomba Inovasi Bisnis Pemuda yang diselenggarakan oleh DIKTI pada yahun 2003 dan 2004, mengikuti lomba penulisan karya ilmiah tentang pengelolaan lingkungan, yang diselenggaran oleh Bayer (2004), BRI (2004) dan Panasonic (2005). Selama tahun 2003 dan 2004 memperoleh beasiswa supersemar.
KATA PENGANTAR
Tiada kata yang terucap selain rasa syukur kepada Allah, dengan ucapan alhamdulillah, karena penulis yakin hanya dengan ijin Allah, penulis dapat menyelesaikan skripsi yang disusun berdasarkan hasil penelitian laboratorium mengenai pengaruh logam berat terhadap pe rtumbuha n mikroorganisme. Skripsi ini berjudul “Pengaruh Logam Berat Terhadap Pertumbuhan Mikroorganisme Pendegradasi Minyak Diesel”.
Dapat diselesaikannya skripsi ini berkat bimbingan, dorongan, dan bantuan dari berbagai pihak, oleh karena itu penulis mengucapka n terima kasih yang tulus kepada
1. Dr. Ir. Mohamad Yani, M.Eng selaku pembimbing akademik yang telah memberikan arahan dan bimbingan dengan bijak.
2. Dr. Ir. Nastiti Siswi Indrasti dan Drs. Purwoko M.Si selaku dosen penguji, yang telah memberikan arahan, bimbin gan dan saran.
3. Seluruh staf laboratorium Tekonologi Industri Pertanian yang telah banyak membantu dengan sabar.
4. Bapak dan Ibu beserta seluruh keluarga atas doa dan dorongannya. 5. Semua teman-teman yang telah banyak membantu dalam pelaksanaan
penelitian, terutama teman-teman di laboratorium bioindustri.
6. Teman-teman ‘TIN 38’, terima kasih untuk hari-hari yang telah kita lalui bersama, suka dan duka.
Ibarat pepatah, tiada gading yang tak retak, penulis menyadari bahwa masih terdapat kekurangan dalam penyusunan dan penulisan skripsi ini. Oleh karena itu, penulis mengharapkan masukan, kritik dan saran yang bersifat membangun untuk sempurnanya laporan skripsi ini. Namun terlepas dari semua itu, penulis berharap semoga skripsi ini dapat bermanfaat bagi semua pihak ya ng membutuhkan.
Bogor, Oktober 2005
Penulis
DAFTAR ISI
KATA PENGANTAR ……… vii
DAFTAR TABEL ... x
DAFTAR GAMBAR ... xi
DAFTAR LAMPIRAN ………. xii
I. PENDAHULUAN A. LATAR BELAKANG... 1
B. TUJUAN ... 3
II. TINJAUAN PUSTAKA A. LOGAM BERAT... 4
1. Toksisitas Logam Berat … ... 5
2. Akumulasi Logam Berat Pada Mikroorganisme ... 6
B. MINYAK BUMI ... 7
1. Jenis Hidr okarbon Dalam Minyak Bumi . ... 8
2. Minyak Diesel . ... 9
C. BIOREMEDIASI ……… 10
1. Faktor Fisiko Kimia Dalam Bioremediasi ……….. 12
a. Kadar air ……….. 13
b. Temperatur ……….. 13
c. Oksigen ……… 13
d. Nutrien ………. …………14
e. Surfaktan ………. ………….14
f. pH ………. …………15
2. Degradasi Minyak Diesel ………... 15
D. MIKROORGANISME ……….. …………16
III. METODOLOGI A. BAHAN DAN ALAT ……… 17
B. METODOLOGI PENELITIAN ……… 17
2...
Penambahan Logam Berat Dalam Berbagai Konsentrasi ...18
3... Pengaruh Interaksi Logam Antara Zn-Pb ...19
4... Pola Akumulasi Logam Berat ...20
IV HASIL DAN PEMBAHASAN A. PEMELIHARAAN ISOLAT DAN DEGRADASI MINYAK DIESEL .22 B. PENGARUH LOGAM BERAT PADA PERTUMBUHAN BAKTERI .25 1. Pengaruh Logam Berat Seng (Zn) ... 27
2. Pengaruh Logam Berat Timbal (Pb) ... 28
3. Pengaruh Logam Besi (Fe) ...29
4. Pengaruh Logam Merkuri (Hg) ... 31
C. INTERAKSI ANTARA LOGAM SENG (Zn) DAN TIMBAL (Pb) ...33
1. Pertumbuhan Kombinasi Isolat PPEA ...33
2. Kinetika Pertumbuhan Sel ...34
3. Perubahan pH Media Selama Inkubasi ... 35
4. Akumulasi Logam Berat Pada Interaksi Zn-Pb ... 36
V. KESIMPULAN DAN SARAN A. KESIMPULAN ... 38
B. SARAN ... 38
DAFTAR PUSTAKA...39
DAFTAR TABEL
Halaman Tabel 1. Parameter Kandungan Logam dalam Air
Menurut PP No.82/2001 ……….. 1
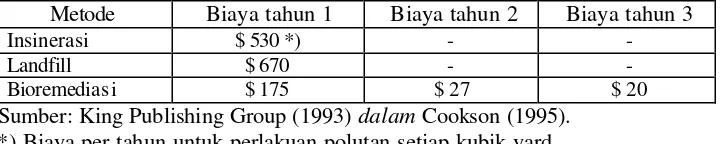
Tabel 2. Perbandingan Biaya Aplikasi Bioremediasi dengan Insenerasi dan Landfill ... 2
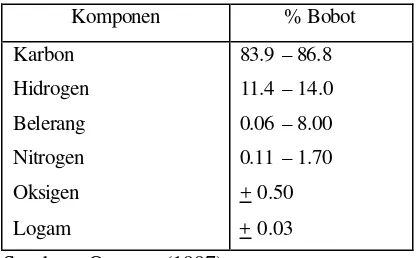
Tabel 3. Komposisi Minyak Bumi ... 7
Tabel 4. Kandungan As, Cd, Pb, dan Hg dalam Batu Bara dan Minyak Mentah (ug/g) ... 8
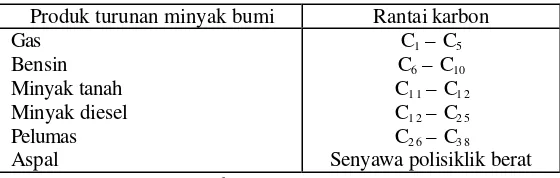
Tabel 5. Minyak bumi dan Turunannya ... 9
Tabel 6. Komposisi Media Luria Bertani ... 17
Tabel 7. Komposisi Media CMSC ... 18
Tabel 8. Kinetika Pertumbuhan PPEA Pada Logam Zn . ... 27
Tabel 9. Kinetika Pertumbuhan PPEA Pada Logam Pb ... 29
Tabel 10. Kinetika Pertumbuhan PPEA Pada Logam Fe ... 30
Tabel 11. Kinetika Pertumbuhan PPEA Pada Logam Hg . ... 32
Tabel 12. Hasil Perhitungan Kinetika Pertumbuhan Sel ... 34
DAFTAR GAMBAR
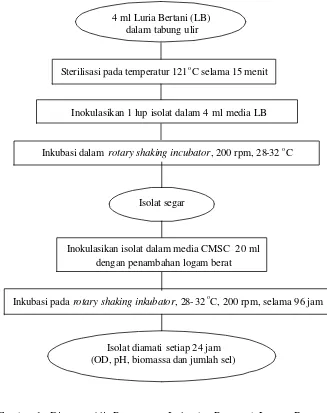
Halaman Gambar 1. Diagram Alir Penyegaran Isolat dan Pengaruh Logam Berat
Terhadap Pertumbuhan Isolat ………..………. 19 Gambar 2. Titik Uji Interaksi Logam Zn-Pb ... 20 Gambar 3. Diagram Alir Pe ngujian Konsentrasi Logam dengan Metode
AAS ... 21 Gambar 4. Grafik Pertumbuhan Bakteri PP, EA dan PPEA Pada
Konsentrasi 10 % Minyak Diesel ... 23 Gambar 5. Foto Pertumbuhan (1) PPEA (2) PP (3) (EA) pada Media CMSC
dengan Penambahan 10% Minyak Diesel ... 24 Gambar 6. Grafik Pertumbuhan PPEA pada Berbagai Konsentrasi Logam
(a) Zn, (b) Pb, (c) Fe dan (d) Hg dengan Penambahan
10% Minyak Diesel ... 26 Gambar 7. Grafik Penurunan Nilai ì-maks pada Kenaikan Konsentrasi
Logam Zn, Pb, Fe dan Hg . ... 32 Gambar 8. Grafik Tiga Dimensi (a) dan Kontur (b) Interaksi Zn-Pb
Terhadap Nilai Log CFU . ... 33 Gambar 9. Perubahan Nilai pH Pada Pengaruh Interaksi Logam Zn-Pb
DAFTAR LAMPIRAN
Halaman Lampiran 1. Prosedur analisis Kekeruhan (Optical Density)
dan Total Plate Count (jumlah mikroba) ... 42 Lampiran 2. Hasil perhitungan jumlah sel pada media kontrol ... 45 Lampiran 2a. Kekeruhan media yang diberi berbagai macam bakteri ... 45 Lampiran 2b. Bau asam yang terbentuk selama inkubasi ... 45 Lampiran 3. Pertumbuhan Pseudomonas pseudomallei pada
berbagai konsentrasi logam Zn ... 46 Lampiran 3a. Pertumbuhan Enterobacter agglomerans pada
berbagai konsentrasi logam Zn ... 46 Lampiran 3b. Hasil perhitungan jumlah sel pada logam Zn ... 46 Lampiran 4. Pertumbuhan Pseudomonas pseudomallei pada
berbagai konsentrasi logam Pb ... 47 Lampiran 4a. Pertumbuhan Enterobacter agglomerans pada
berbagai konsentrasi logam Pb ... 47 Lampiran 4b. Hasil perhitungan jumlah sel pada logam Pb ... 47 Lampiran 5. Pertumbuhan Pseudomonas pseudomallei pada
berbagai konsentrasi logam Fe ... 48 Lampiran 5a. Pertumbuhan Enterobacter agglomerans pada
berbagai konsentrasi logam Fe ... 48 Lampiran 5b. Hasil perhitungan jumlah sel pada logam Fe ... 48 Lampiran 6. Pertumbuhan Pseudomonas pseudomallei pada
berbagai konsentrasi logam Hg ... 49 Lampiran 6a. Pertumbuhan Enterobacter agglomerans pada
Lampiran 10. Perubahan nilai pH selama inkubasi ... 53
I. PENDAHULUAN
A. LATAR BELAKANG
Minyak bumi merupakan sumber energi konvensional yang digunakan dalam kegiatan industri. Bila tumpah atau terbuang ke lingkungan, minyak tersebut akan menjadi pencemar yang berbahaya. Tumpahan atau buangan minyak bumi dapat terjadi selama kegiatan industri perminyakan, mulai dari eksplorasi, eksploitasi, pengolahan sampai pengangkutan (Udiharto, 1996). Limbah yang dihasilkan dari pengolahan minya k bumi mengandung logam-logam berat yang dapat mengkontaminasi lingkungan (Darmono,1995). Logam berat, seperti arsenik, timbal, kadmium, merkuri dan seng berbahaya bagi kesehatan manusia dan kelangsungan kehidupan di lingkungan.
Walaupun pada konsentrasi yang rendah, logam berat dapat berpengaruh langsung terhadap kehidupan mahluk hidup hingga terakumulasi pada rantai makanan.
logam berat sejenis Pb, Hg, Zn, Cu, Fe dan Cd yang terdapat di Laut Jawa berada dalam tahap ambang maksimal (Anonim, 2003).
Tabel 1. Parameter Kandungan Logam dalam Air Menurut PP No.82/2001 Parameter Baku mutu (mg/L)
Seng
Menurut Udiharto (1996) bahan-bahan yang tahan terhadap pengaruh kimia seperti minyak bumi, dapat diuraikan dengan mikroorganisme. Mikroorganisme diperlukan sebagai pengurai dan pendegradasi bahan organik komplek, menjadi bahan yang lebih sederhana yaitu CO2 dan H2O. Bioremediasi relatif memiliki biaya penanganan yang lebih murah dibandingkan dengan alternatif metode lainnya (Tabel 2).
Tabel 2. Perbandingan Biaya Aplikasi Bioremediasi dengan Insenerasi dan Landfill
Metode Biaya tahun 1 Biaya tahun 2 Biaya tahun 3
Insinerasi $ 530 *) - -
Landfill $ 670 - -
Bioremedias i $ 175 $ 27 $ 20
Sumber: King Publishing Group (1993) dalam Cookson (1995). *) Biaya per tahun untuk perlakuan polutan setiap kubik yard
(Dopson et al., 2003). Hal ini disebabkan karena mikroorganisme dapat mengikat, mengakumulasi atau mereduksi ion-ion logam. Bioremediasi merupakan salah satu alternatif yang lebih ekonomis daripada metode secara fisika maupun kimia seperti teknologi membran, ion exchange dan insenerasi.
Beberapa penelitian menunjukkan bahwa hidrokarbon minyak bumi dapat didegradasi oleh mikroorganisme (Udiharto, 1996; Oetomo, 1997; Anggraeni, 2003; Hikmatuloh, 2004). Menurut Yugiarti (1999), terdapat pengaruh logam berat terhadap proses degradasi minyak bumi. Pada penelitian sebelumnya oleh Anggraeni (2003) tela h didapatkan tiga jenis isolat Pseudomonas pseudomallei, Pseudomonas aeruginosa dan Enterobacter agglomerans yang mampu mendegradasi minyak diesel. Kemampuan ketiga isolat tersebut dalam mendegradasi minyak diesel juga telah dibuktikan oleh Hikmatulloh (2004) dan Zaky (2005). Kemampuan tersebut perlu didukung pula oleh ketahanan isolat terhadap kandungan logam berat dalam pencemaran minyak bumi, pada pengolahan dengan bioremediasi.
B. TUJUAN
II. TINJAUAN PUSTAKA
A. LOGAM BERAT
Logam berat biasanya didefinisikan berdasarkan sifat-sifat fisiknya dalam keadaan padat. Sifat-sifat fisik tersebut antara lain memiliki: 1) daya pantul cahaya yang tinggi, 2) daya hantar listrik yang tinggi dan 3) daya hantar panas (Darmono, 1995). Istilah logam berat menunjuk pada logam yang mempunyai berat jenis lebih tinggi dari 5 atau 6 g/cm3. Beberapa logam berat tersebut adalah As, Cd, Cr, Cu, Pb, Hg, Ni dan Zn (Wild, 1995). Beberapa logam berat seperti Cu, Zn, Fe, Ni, Mn dan Co merupakan logam yang diperlukan dalam konsentrasi rendah untuk proses metabolisme. Pada konsentrasi tinggi, logam berat bersifat toksik karena sukar terurai. Apabila logam berat masuk perairan, akan terakumulasi terutama dalam sedimen dan terikat sebagai senyawa organik dan anorganik (Gadd, 1990).
Kantor Menteri Negara Lingkungan Hidup telah mengelompokkan sifat toksisitas logam berat dalam tiga kelompok, yaitu (1) bersifat toksik tinggi yang terdiri unsur-unsur Hg, Pb, Cd, Cu dan Zn, (2) bersifat toksik menengah yang terdiri atas unsur -unsur Cr, Ni dan Co, dan (3) bersifat toksik sangat rendah yang terdiri atas unsur-unsur Mn dan Fe.
Kontaminasi logam berat di lingkungan merupakan masalah besar dunia saat ini. Persoalan keberadaan logam berat di lingkungan terutama karena akumulasinya hingga pada rantai makanan dan keberadaannya di alam, serta meningkatnya sejumlah logam berat yang menyebabkan keracunan terhadap tanah, udara dan air (Suhendrayatna, 2001).
1 Toksisitas Logam Berat
Berdasarkan sudut pandang toksikologi, logam berat terbagi ke dalam dua jenis yaitu: pertama logam berat esensial dimana keberadaanya dalam jumlah tertentu sangat dibutuhkan oleh setiap organisme hidup, seperti antara lain, seng (Zn), tembaga (Cu), besi (Fe), kobalt (Co) dan mangan (Mn), serta logam berat tidak esensial atau beracun, dimana keberadaan dalam tubuh organisme hidup hingga saat ini masih belum diketahui manfaatnya bahkan justru dapat bersifat racun, seperti merkuri (Hg), kadmium (Cd), timbal (Pb) dan kromium (Cr) (Nugroho, 2001).
Secara umum, logam-logam esensial diperlukan sebagai katalis enzim, transpor molekul, struktur protein dan mengontrol tekanan osmotik sel (Roane dan Pepper, 2000). Menurut Darmono (1995), urutan toksisitas teringgi sampai terendah dari logam berat bagi manusia adalah sebagai berikut: Hg2+>Cd2+>Ag2+>Ni2+>Pb2+>As2+>Cr2+>Sn2+>Zn2+.
Logam berat dapat menyebabkan toksik pada organisme hidup, karena dapat berkompetisi, mengganti atau menempati ion-ion logam-logam esensial metabolisme (Wong et al. 2002; Roane dan Pepper, 2000). Pada umumnya, mikroorganisme menggunakan jalur transpor yang spesifik untuk membawa logam-logam esensial masuk ke dalam sitoplasma dengan melintasi membran sel. Demikian juga logam-logam toksik dapat juga melintasi membran melalui difusi (Roane dan Pepper, 2000).
Merkuri (Hg) adalah unsur logam yang berbentuk cair pada suhu kamar dan mempunyai titik beku -39 0C, mempunyai kecenderungan menguap lebih besar, mudah dicampur dengan logam lain dan mudah mengalirkan arus listrik (Darmono, 1995). Merkuri banyak digunakan pada industri alat listrik, industri cat, industri farmasi dan pada bidang pertanian merkuri digunakan untuk membasmi jamur (fungisida) (Suhendrayatna , 2001).
industri baterai kendaraan bermotor, industri cat, pestisida dan bahan anti letup kendaraan bermotor (Ambarwati, 2002).
Elemen seng (Zn) dan besi (Fe) banyak digunakan pada pembuatan baja, produksi logam campuran dan pelapis logam. Seng biasanya dijumpai pada tanah dengan konsentrasi 10-300 ppm dan banyak terdapat pada limbah industri pertambangan logam (Suhendrayatna, 2001). Besi tersebar luas di alam dengan konsentrasi sekitar 50000 ppm (Darmono, 1995).
2. Akumulasi Logam Berat Pada Mikroorganisme
Logam berat dapat diakumulasikan oleh sel mikroba hidup dengan berbagai cara baik fisikokimia maupun biologi (Suhendrayatna, 2001; Gadd, 1992; Roane dan Pepper, 2000). Jika akumulasi ion-ion logam tersebut tergantung pada fenomena akumulasi sel maka direferensikan sebagai bioakumulasi. Sedangkan fenomena yang memanfaatkan adsorpsi sel permukaan sel disebut biosorpsi. Namun kadang-kadang kedua fenomena direferensikan sebagai akumulasi (Marwati, 2005).
Bioremoval didefinisikan sebagai terakumulasi dan terkonsentrasinya zat polusi dari suatu lingkungan oleh material biologi, selanjutnya material ini dapat dibuang sehingga ramah terhadap lingkungan. Berbagai jenis mikroorganisme dapat digunakan untuk tujuan ini. Proses bioremoval berpotensi tinggi dalam kontribusinya untuk mengurangi kadar logam berat (Suhendrayatna, 2001). Mekanisme utama dalam imobilisasi atau memindahkan logam dari larutan dapat melalui volatilisasi dan akumulasi atau terikat pada permukaan sel (Ford dan Mitchel, 1992).
(Roane dan Pepper, 2000). Metalothionein ini dapat ditemukan pada beberapa mikroorganisme, antara lain P. Aeruginosa (Qureshi et al., 2001) dan Saccharromyces cerevisiae (Gadd, 1990)
Bakteri umumnya dapat memproduksi ekstraseluler polimer yang sebagian besar komposisinya terdiri dari karbohidrat, polisakarida, asam nukleat dan asam lemak. Komponen ekstraselular tersebut dapat menangkap ion-ion logam toksik melalui berbagai reaksi kimia seperti kompleksasi, binding kovalen dan ion exchange (Gadd, 1990; Roane dan Pepper, 2000).
Menurut Atlas dan Bartha (1998), komponen-komponen ekstraseluler atau ligan-ligan yang terikat pada dinding sel dapat menangkap logam toksik dan masuk melewati dinding sel dengan lambat. Logam selanjutnya di lepas ke dalam sel dan bergabung dalam lintasan biokimia atau terperangkap dalam bentuk inaktif yang berikatan komplek dengan ligan-ligan afinitas tinggi.
B. MINYAK BUMI
Perkembangan industri minyak begitu pesat, produksi minyak bumi di dunia lebih dari tiga miliar ton per tahun. Wilayah perairan menjadi rawan timbulnya pencemaran minyak karena separuh dari seluruh produksi tersebut diangkut melalui laut oleh kapal tanker sehingga kecelakaan-kecelakaan yang mengakibatkan tercecernya minyak di la ut hampir tidak dapat dielakkan (Fahruddin, 2004).
Tabel 3. Komposisi Minyak Bumi
Minyak bumi maupun produknya merupakan campuran senyawa organik yang terdiri atas senyawa hidrokarbon dan nonhidrokarbon. Senyawa
hidrokarbon merupakan komponen terbesar dalam minyak bumi (lebih dari 90%) sedangkan sisanya berupa senyawa nonhidrokarbon. Senyawa hidrokarbon merupakan senyawa organik yang terdiri atas karbon dan hidrogen. Senyawa-senyawa non hidrokarbon misalnya nitrogen, belerang, oksigen dan logam (Cookson, 1995).
Batu bara dan minyak merupakan bahan bakar yang banyak digunakan dalam pembangkit tenaga listrik, bahan bakar kendaraan, bahan bakar untuk mesin di pabrik dan lain-lain. Akan tetapi limbah yang dihasilkan cukup berbahaya bagi mahluk hidup, karena biasanya mengandung logam-logam berat seperti arsen (As), kadmium (Cd), timah hitam (Pb) dan merkuri (Hg) (Darmono, 1995). Walaupun logam berbahaya tersebut kandungannya sangat kecil dalam bahan bakar minyak dan batu bara, tetapi kekuatan untuk menyebabkan keracunan sangat besar. Kandungan logam dalam batu bara dan minyak bumi, seperti terlihat pada Tabel 4.
Tabel 4. Kandungan As, Cd, Pb, dan Hg dalam Batu Bara dan Minyak Mentah (ug/g).
Logam Batu bara (ug/g) Minyak mentah (ug/g)
As
Sumber: Darmono (1995)
1. Jenis Hidr okarbon Dalam Minyak Bumi a. Hidrokarbon Alifatik
dan jumlah atom lebih dari 16 adalah bentuk padat atau semi padat. Terdiri dari alkana dengan rumus molekul CnH2n+2, alkena dengan rumus molekul CnH2n dan alkuna dengan rumus molekul CnH2 n-2 (Udiharto, 1996 dan Oetomo, 1997).
b. Hidrokarbon alisiklik
Hidrokarbon alisiklik atau disebut juga naftena adalah senyawa yang umumnya berbentuk cincin dan tidak mempunyai ikatan ganda. Hidrokarbon alisiklik terdiri atas sikloalkana dengan rumus molekul CnH2n, sikloalkena dengan rumus molekul CnH2n-2 dan sikoalkuna dengan rumus molekul CnH2 n-4 (Udiharto, 1996).
c. Hidrokarbon aromatik
Dalam minyak bumi senyawa hidrokarbon aromatik terdiri atas senyawa aromatik tanpa subtitusi, sebagai contoh benzena, te rdiri dari enam atom karbon yang berikatan ganda atau tunggal dan senyawa aromatik tersubtitusi seperti toluene, fenol dan xilen (Udiharto, 1996).
2. Minyak Diesel
Produk-produk turunan minyak bumi antara lain adalah sebagai berikut Tabel 5. Minyak bumi dan Turunannya
Produk turunan minyak bumi Rantai karbon Gas
Sumber : Crawford (1996).
sebesar 19% dan sisanya resin sebesar 2%. Minyak diesel juga mengandung sejumlah VOCs seperti benzena, toluena, etilbenzena dan xilena.
Merujuk pada Udiharto (1996) mengenai jenis produk minyak bumi dan komposisinya, maka yang digolongkan sebagai minyak diesel adalah produk minyak bumi dengan jumlah rantai karbon antara 12-25. Minyak diesel dengan rantai karbon antara 12-18 disebut minyak diesel ringan, sedangkan untuk rantai karbon yang lebih panjang disebut minyak diesel berat yang juga digunakan sebagai minyak lumas ringan.
Minyak diesel terdiri atas komponen minyak dan bahan aditif. Komponen minyak dari bahan ini sebagian besar merupakan hidrokarbon, yaitu normal alkana atau n-parafin, isoalkana atau isoparafin, sikloalkana atau naftalena, olefin dan campuran aromat dengan olefin. Senyawa hidrokarbon merupakan komponen terbesar dari produk minyak bumi (lebih dari 90%), sedangkan komponen sisanya berupa senyawa non-hidrokarbon yaitu senyawa organik yang mengandung belerang, nitrogen dan oksigen (Udiharto, 1996). Beberapa senyawa polutan hasil pembakaran minyak diesel adalah hidrokarbon, oksida nitrogen, partikulat, benzena dan karbon monooksida. Hidrokarbon minyak diesel sebagian besar berupa n-alkana sederhana tidak bercabang, dengan kandungan senyawa poliaromatik kurang dari 4%.
C. BIOREMEDIASI
Bioremediasi menurut Citroreksoko (1996) diartikan sebagai proses pendegradasian bahan organik berbahaya secara biologis menjadi senyawa lain seperti CO2, metan dan air. Proses ini didasarkan pada siklus karbon di mana bentuk senyawa organik dan anorganik didaur ulang melalui reaksi reduksi dan oksidasi. Menurut Crawford dan Crawford (1996) bioremediasi merujuk pada penggunaan secara produktif proses biodegradatif untuk menghilangkan atau mendetoksifikasi polutan yang mencemari lingkungan dan mengancam kesehatan masyarakat.
senyawa xenobiotik (asing di alam) dan bersifat rekalsitran (sulit terdegradasi).
Reaksi oksidasi dan reduksi pada senyawa polutan bisa berlangsung dengan adanya katalis berupa enzim-enzim mikrobial yang disekresi oleh mikroorganisme pendegradasian alami. Pada mulanya, mikroorganisme pendegradasi tidak memiliki kemampuan dala m mendegradasi senyawa -senyawa polutan yang belum dikenal sebelumnya karena tidak memiliki enzim pendegradasi yang dibutuhkan. Sa’id dan Fauzi (1996) menjelaskan bahwa dalam evolusi kehidupannya mikroorganisme tersebut akan mengalami proses diagenesis, yaitu proses perubahan kimiawi, biokimia dan fisika sehingga lambat laun mikroorganisme-mikrooganisme tersebut dapat beradaptasi dan melakukan pendegradasian.
Mikroorganisme aerob dan reaksi aerob terjadi pada suatu lingkungan tersedia cukup oksigen yang bertindak sebagai akseptor elektron. Reaksi tersebut dikenal sebagai respirasi. Hasil akhir yang diperoleh merupakan campuran dari produk yang lebih teroksidasi atau lebih tereduksi dibandingkan substrat awalnya. Tergantung pada jenis mikroorganismenya, produk akhir tersebut berupa asam, alkohol, keton dan gas-gas (Cookson, 1995).
Menurut Cookson (1995) kebutuhan dasar dari proses biologis yaitu : a. Kehadiran mikroorganisme dengan kemampuan untuk mendegradasi
senyawa atau senyawa target.
b. Keberadaan substrat yang dikenali dan dapat digunakan sebagai sumber energi dan karbon.
c. Kondisi lingkungan yang sesuai untuk reaksi dan pH yang mendukung. d. Ketersediaan nutrien untuk mendukung pertumbuhan sel mikrobial dan
produksi enzim.
e. Suhu yang mendukung aktivitas mikrobial.
f. Ketiadaan bahan atau substansi beracun terhadap mikroorganisme tersebut.
tersebut dengan cara menurunkan energi aktivasi, yaitu energi yang dibutuhkan untuk memulai suatu reaksi. Produksi enzim dipicu oleh kehadiran substrat yang berfungsi sebagai sumber energi. Substrat tersebut bisa jadi merupakan senyawa polutan atau pun bukan polutan. Supaya mikroorganisme bisa memperoleh energi dari substrat tersebut, maka bahan tersebut harus masuk ke dalam membran sel dan melewati serangkaian transpor elektron selama respirasi seluler berlangsung. Bila substrat potensial terlalu besar untuk bisa menembus membran sel maka sel akan mengekskresi eksoenzim dan mencerna substrat di luar sel. Tingkat produksi enzim-enzim ektraseluler ini relatif rendah, sehingga degradasi makromolekul membutuhkan waktu aklimatisasi yang relatif lama dengan tingkat degradasi yang rendah (Cookson, 1995).
Terdapat beberapa mekanisme penghambatan enzim. Salah satunya, yang membuat produksi enzim terhenti adalah represi katabolit. Mekanisme ini terjadi bila metabolit dari degradasi menghambat produksi enzim atau tetap mempertahankan ikatan kompleknya dengan enzim. Mekanisme lain adalah penghambatan kompetitif, yang terjadi bila terdapat substrat lain yang lebih mudah dimetabolisme oleh sel (Cookson, 1995).
Kometabolisme merupakan proses transformasi senyawa secara tidak langsung yang berupa interaksi antara beberapa galur mikroorganisme di lingkungannya dalam mengoptimalkan aktivitas mikroorganisme untuk bioremediasi. Proses ini bisa berlangsung karena enzim yang dihasilkan mikroorganisme untuk mendegradasi substrat tertentu ternyata juga bisa bermanfaat bagi proses degradasi senyawa lain yang tidak ada hubungannya dengan proses produksi energi, asimilasi karbon, maupun proses lain yang berkaitan dengan pertumbuhan sel mikroorganisme tersebut. Proses ini hanya bisa berlangsung bila tersedia substrat lain yang bertindak sebagai sumber karbon bagi metabolisme mikroorganisme (Cookson, 1995).
1. Faktor Fisiko Kimia Dalam Bioremediasi
pendegradasi hidrokarbon, perlu dioptimalkan aktivitasnya dengan pengaturan kondisi dan penambahan suplemen yang sesuai. Perlu diperhatikan faktor -faktor lingkungan yang meliputi kadar air, pH, temperatur, oksigen, dan nutrien yang tersedia.
a. Kadar air
Kadar air merupakan salah satu faktor penting dalam proses bioremediasi. Mikroorganisme membutuhkan air untuk tumbuh dan berkembang biak. Kandungan air sangat penting untuk aktivitas metabolik mikroorgansime. Tanpa air mikroorganisme tidak dapat hidup dalam limbah minyak, karena mikroorganisme tumbuh aktif pada antar muka minyak dan air (Udiharto, 1996).
b. Temperatur
Dalam suatu proses degradasi, temperatur akan berpengaruh terhadap sifat fisik dan kimia komponen-komponen kimia, kecepatan degradasi oleh mikroorganisme dan komposisi komunitas mikroorganisme. Temperatur yang optimal untuk degradasi hidrokarbon adalah 30-40oC. Pada temperatur rendah, viskositas minyak akan meningkat mengakibatkan volatilitas alkana rantai pendek yang bersifat toksik menurun dan kelarutannya di air akan meningkat sehingga proses biodegradasi akan terhambat. Efek penghambatan tersebut juga disebabkan oleh penurunan aktivitas enzim mikrobial (Leahy dan Colwell, 1990).
c. Oksigen
respirasi aerob. Jika transpor oksigen tidak dipelihara, keberadaan oksigen dapat menjadi komponen pembatas (Oetomo, 1997).
d. Nutrien
Mikroorganisme memerlukan nutrisi sebagai sumber karbon, energi, dan keseimbangan metabolisme sel. Hidrokarbon minyak bumi akan dikonsumsi oleh mikroorganisme sebagai sumber karbon. Proses biodegradasi minyak bumi oleh mikroorganisme akan berlangsung lebih cepat dan pertumbuhannya lebih meningkat dengan penambahan nitrogen dan fosfor (Leahy dan Colwell, 1990).
Rosenberg dan Ron (1988) menyatakan bahwa secara teoritis jumlah nitrogen dan fosfor yang harus ditambahkan untuk mengkonversi 1 gram hidrokarbon menjadi material sel adalah 150 mg untuk nitrogen dan 30 mg untuk fosfat. Kebutuhan nitrogen dan fosfor untuk menghasilkan pertumbuhan yang maksimum dari mikroorganisme pendegradasi hidrokarbon bisa dipenuhi dari penambahan kedua nutrien tadi dalam bentuk campurannya dengan garam lain seperti amonium sulfat, amonium nitrat, amonium klorida dan kalsium fosfat. Penggunaan garam amonia dari asam kuat akan mengakibatkan penurunan pH larutan, untuk menghindari hal tersebut maka sebagai sumber nitrogen bisa digunakan urea.
e. Surfaktan
Zat yang dapat menyatukan beberapa zat yang berbeda jauh kepolarannya sehingga apabila dilihat dari sifat zat-zat tersebut sebenarnya tidak dapat disatukan disebut surfaktan atau emulsifier. Menurut Karanth et al. (2005), surfaktan memiliki gugus polar dan gugus non polar sekaligus dalam satu molekulnya sehingga pada satu sisi ia akan mengikat minyak yang bersifat non polar dan di sisi lain ia juga akan mengikat air yang bersifat polar.
kelebihan antara lain mudah didegradasi dan kandungan polutan rendah sehingga tidak mencemari lingkungan (Karanth et al., 2005).
e. pH
Tingkat keasaman adalah salah satu faktor yang mempengaruhi laju pertumbuhan mikroorganisme. Sebagian besar bakteri mampu tumbuh dengan baik pada kisaran pH netral antara 6,5-7,5 dan mampu bertahan pada kisaran pH 4-9 (Pelczar dan Chan, 1986). pH dapat berubah selama pertumbuhan mikroorganisme. Penurunan pH terjadi akibat terbentuknya asam-asam organik, sedangkan peningkatan pH terja di jika ada proses reduksi nitrat membentuk ammonia.
2. Degradasi Minyak Diesel
Rosenberg dan Ron (1996) mengemukakan bahwa degradasi hidrokarbon minyak diesel terjadi bila mikroorganisme menempel di permukaan butiran-butiran minyak karena enzim oksidase yang dibutuhkan untuk memecah rantai karbon yang sifatnya terikat pada membran sel. Dengan demikian degradasi minyak diesel dipengaruhi oleh bioavailabilitas komponen-komponennya di lingkungan.
Penghambatan degradasi bisa terjadi karena tumpahan minyak akan membentuk lapisan film di permukaan air yang menghambat difusi oksigen ke dalam air (Karanth et al., 2005). Untuk meningkatkan kontak antara bakteri dengan minyak yang tidak terlarut di dalam air dilakukan dengan dua cara, yaitu mekanisme adhesi atau adsorbsi spesifik serta dengan mengemulsi minyak.
terutama bila tersedia mikroorganisme pendegradasi yang melakukan kometabolisme terhadap komponen-komponennya.
D. MIKROORGANISME
Karakteristik isolat Pseudomonas pseudomallei dan Enterobacter agglomerans adalah sebagai berikut
1. Enterobacter agglomerans, merupakan bakteri gram negatif, tidak membentuk spora, fakultatif anarobik, memiliki ukuran lebar 0.6-1 um dan panjang 1.2-3.0 um. Sel bersifat motil, dapat tumbuh pada suhu antara 20-30 0C, bundar bewarna putih kekuningan.
(http://icarus.cc.uic.edu/~kliu4/bios351/bacteria/EnteroAmycoba.htm) 2.Pseudomonas pseudomallei, merupakan bakteri aerobik gram negatif,
bersifat motil oleh pergerakan flagella berbentuk batang dan memiliki ukuran lebar 0.5-1.0 um dan panjang 1.5-5.0 um (Holt et al.,1994).
Pseudomonas memegang peranan penting di lingkungan karena kemampuannya dalam memetabolisme senyawa-senyawa organik. Beberapa diantara senyawa-senyawa tersebut merupakan polutan misalnya benzen, toluen, silen, etil benzen, stirena dan klorobenzoat. Enterobacter agglomerans telah diketahui kemampuannya dalam mengkonversi gliserol menjadi 1,3-propanadiol (PPD) sebagai produk utama dan juga asam asetat, format, laktat, suksinat dan etanol sebagai produk sampingan.
III. METODOLOGI
A. BAHAN DAN ALAT
Bahan-bahan yang digunakan dalam penelitian ini adalah nutrien agar, alkohol 96 %, spirtus, media CMSC (Carbon Minimal Salts Culture), media Luria Bertani, logam berat (Fe, Zn, Pb dan Hg), minyak diesel, aquades, kertas saring, kapas, alumuniu m foil, garam fisiologis dan aquades.
Peralatan yang digunakan meliputi petridisk, tabung reaksi, tabung ulir, tabung serum, tabung film, tabung eppendorf, jarum ose, kertas pH, spektrofotometer, mikropipet berbagai ukuran, tip pipet berbagai ukuran, gelas ukur, gelas piala, labu erlenmeyer, lemari pendingin, inkubator, rotary shaking incubator, oven, autoclave, clean bench dan atomic absorption spectrophotometry (AAS).
Sumber mikroorganisme yang digunakan dalam penelitian ini adalah mikroorganisme yang telah teridentifikasi hasil isolasi dari kotoran hewan, yaitu Pseudomonas pseudomallei dan Enterobacter agglomerans (Anggraeni, 2003).
B. METODOLOGI PENELITIAN 1. Penyegaran Isolat
Stok isolat dalam gliserol, disegarkan dalam tabung ulir yang berisi 4 ml media Luria Bertani (Tabel 6). Sebanyak 0.1 ml isolat diambil dengan menggunakan pipet mikro untuk ditumbuhkan pada media LB diinkubasikan pada suhu kamar selama 96 jam, dilihat kekeruhan yang terjadi. Jika pada tabung ulir tersebut terjadi kekeruhan, maka isolat tersebut mengalami pertumbuhan.
Tabel 6. Komposisi Media Luria Bertani
Nilai kekeruhan yang terjadi diukur dengan menggunakan spektrofotometer setiap 24 jam. Kemudian dihitung jumlah sel dengan metode total plate count (TPC).
2. Penambahan Logam Berat Dalam Berbagai Konsentrasi
Untuk mengetahui pengaruh logam berat terhadap pertumbuhan mikroorganisme dilakukan penambahan logam berat (Fe, Zn, Pb dan Hg) dalam media CMSC (Tabel 7) dengan penambahan minyak diesel 10% . Isolat murni Pseudomonas pseudomallei dan Enterobacter agglomerans serta kombinasi keduanya yang berasal dari biakan yang telah disegarkan, ditumbuhkan di dalam 20 ml media tersebut. Penambahan logam berat dalam berbagai konsentrasi dilakukan secara bertahap dalam interval tertentu.
Tabel 7. Komposisi Media CMSC
Bahan Kimia Komposisi (g/L) K2HPO4
*) Tambahkan setelah media selesai diautoklaf dan suhunya mencapai suhu ruang.
Kultur diinkubasikan pada suhu ruang dan digoyang dengan kecepatan 200 rpm. Setiap 24 jam, diambil sampel untuk melihat pertumbuhan selnya dengan metode turbidimetri menggunakan spektrofotometer pada panjang gelombang 600 nm, pengukuran biomassa kering dan dilakukan juga pengukuran pH. Pengukuran dilakukan hingga jam ke 96 (hari ke 4). Dari hasil pengukuran secara turbidimetri tersebut, dilakukan penghitungan jumlah sel dengan metode Total Plate Count (TPC) (Lampiran 1), pada jam dimana nilai absorbansinya mencapai maksimal.
4 ml Luria Bertani (LB) dalam tabung ulir
Sterilisasi pada temperatur 121oC selama 15 menit
Inokulasikan 1 lup isolat dalam 4 ml media LB
Inkubasi dalam rotary shaking incubator, 200 rpm, 28-32 oC
Isolat segar
Inkubasi pada rotary shaking inkubator, 28- 32 oC, 200 rpm, selama 96 jam
Isolat diamati setiap 24 jam (OD, pH, biomassa dan jumlah sel)
Gambar 1. Diagram Alir Penyegaran Isolat dan Pengaruh Logam Berat Terhadap Pertumbuhan Isolat
3. Pengaruh Interaksi Logam Antara Zn-Pb
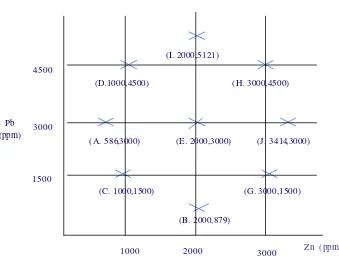
Interaksi antara logam Zn-Pb, dilakukan dengan mengambil 10 titik awal sebagai titik acuan untuk mengetahui pengaruhnya terhadap pertumbuhan mikroorganisme (Gambar 2). Nilai-nilai tersebut diperoleh dari hasil penelitian pendahuluan tentang pengaruh masing- masing logam Zn dan Pb terhadap nilai optical density (OD) dan nilai total plate count (TPC). Respon yang diukur meliputi jumlah sel berdasarkan metode Total Plate Count (TPC), berat biomass kering dan pH.
(J. 3414,3000) (I. 2000,5121)
(H. 3000,4500) (D.1000,4500)
(E. 2000,3000) (A. 586,3000)
(C. 1000,1500)
(B. 2000,879)
(G. 3000,1500)
Gambar 2. Titik Uji Interaksi Logam Zn-Pb
Respon yang diperoleh kemudian akan diplotkan dalam bentuk grafik tiga dimensi dengan menggunakan software Statistica 6.0
4. Pola Akumulasi Logam Berat
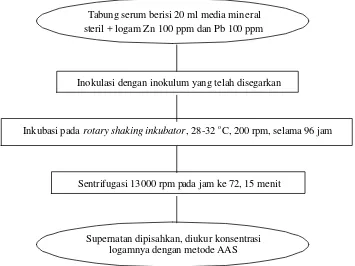
Pola akumulasi digunakan untuk mengetahui distribusi logam dalam supernatan dan dalam biomass sel. Pengujian ini dilakukan dengan menghitung penurunan konsentrasi logam berat dalam supernatan dengan konsentrasi awal 100 ppm Zn dan 100 ppm Pb. Pengujian ini dilakukan pada saat nilai OD maksimum (jam ke 72) dengan melakukan sentrifugasi dingin pada kecepatan 13000 rpm selama 15 menit. Supernatan dipisahkan, untuk kemudian diukur konsentrasi logam beratnya dengan menggunakan metode atomic absorption spectrophotometry (AAS). Biomassa dalam tabung ependorf yang telah dipisahkan dengan supernatannya dimasukkan pada oven bersuhu 100 oC hingga diperoleh berat kering yang konstan.
1000 2000 3000
Pb (ppm)
1500 3000 4500
Tabung serum berisi 20 ml media mineral steril + logam Zn 100 ppm dan Pb 100 ppm
Inokulasi dengan inokulum yang telah disegarkan
Inkubasi pada rotary shaking inkubator, 28-32 oC, 200 rpm, selama 96 jam
Sentrifugasi 13000 rpm pada jam ke 72, 15 menit
Supernatan dipisahkan, diukur konsentrasi logamnya dengan metode AAS
IV. HASIL DAN PEMBAHASAN
A. PEMELIHARAAN ISOLAT DAN DEGRADASI MINYAK DIESEL
Beberapa jenis mikroorgansime mempunyai toleransi yang tinggi terhadap logam dan mampu mengakumulasi logam berat melalui berbagai macam mekanisme (Nugroho, 2001). Beberapa macam mikroorganisme yang mempunyai toleransi terhadap logam antara lain Pseudomo nas, Bacillus, Acinetobacter, Flavobacterium dan Desulvovibrio.
Pseudomonas pseudomallei (PP), Pseudomonas aeruginosa (PA) dan Enterobacter agglomerans (EA) merupakan isolat hasil isolasi kotoran hewan yang mampu tumbuh pada konsentrasi 10% minyak diesel (Anggraeni, 2003). Menurut Hikmatulloh (2004), dibandingkan dengan isolat tunggalnya, kombinasi isolat Pseudomonas pseudomallei + Enterobacter agglomerans (PPEA) dan Pseudomonas aeruginosa + Enterobacter agglomerans (PAEA) lebih mampu mendegradasi hidrokarbon minyak diesel, sedangkan menurut Zaky (2005), degradasi hidrokarbon oleh isolat PPEA menunjukkan hasil yang lebih baik dibandingkan isolat PAEA.
Penelitian ini melakukan pengujian pengaruh logam berat Hg, Pb, Zn dan Fe terhadap pertumbuhan bakteri Pseudomonas pseudomallei, Enterobacter agglomerans dan kombinasi isolat Pseudomonas pseudomallei+Enterobacter agglomerans (PPEA) pada media CMSC (Carbon Minimal Salts Culture) dengan penambahan minyak diesel 10%.
Pemeliharaan isolat bakteri PP, EA dan PPEA dilakukan terhadap stok isolat yang disimpan di dalam tabung ependorf berisikan larutan gliserol pada suhu sekitar -40 oC. Isolat ditumbuhkan kembali pada media CMSC dengan penambahan 10% minyak diesel.
dilakukan penghitungan jumlah sel dengan menggunakan metode Total Plate Count (TPC), pada saat nilai kekeruhan sel (optical density) mencapai puncaknya pada jam ke 72, dengan melakukan pengenceran hingga 10-1 3 secara aseptis.
Gambar 4. Grafik Pertumbuhan Bakteri PP, EA dan PPEA pada Konsentrasi 10 % Minyak Diesel
Berdasarkan grafik diatas, ketiga isolat mampu tumbuh dalam media yang telah ditambahkan 10% minyak diesel sebagai sumber karbon. Hal tersebut disebabkan karena bakteri mempunyai kemampuan untuk meningkatkan kontak dengan minyak melalui mekanisme adhesi atau adsorpsi, yaitu meningkatkan interaksi antara permukaan membran luar sel yang bersifat hidrophobik dengan minyak. Setelah mengadhesi permukaan minyak, bakteri melakukan pembelahan sel. Ketika permukaan minyak menjadi jenuh oleh bakteri, maka pertumbuhan bakteri dibatasi oleh ketersediaan minyak. Jika bakteri mampu memisahkan lapisan butiran minyak (emulsifikasi), maka permukaan untuk pertumbuhan sel akan terbentuk (Rosenberg dan Ron, 1998). Berdasarkan penghitungan jumlah sel, isolat Pseudomonas pseudomallei (PP) mampu tumbuh hingga 1012 cfu/ml, Enterobacter agglomerans (EA) mampu tumbuh hingga 101 2 cfu/ml dankombinasi isolat Pseudomonas pseudomallei+Enterobacter agglomerans (PPEA) mampu tumbuh hingga 1013 cfu/ml (data disajikan pada Lampiran 2).
Kehadiran senyawa -senyawa toksik dalam minyak diesel seperti hidrokarbon rantai pendek (Citroreksoko, 1996) dan BTEX (benzen, toluen, etilbenzen, xilen) (Rosenberg dan Ron, 1998) mengakibatkan isolat
membutuhkan waktu relatif lama untuk bisa beradaptasi dengan kondisi lingkungan di sekitarnya. Menurut Oetomo (1997), untuk bisa beradaptasi dengan kondisi lingkungannya, mikroorganisme memerlukan waktu untuk: (1) pertumbuhan awal populasi yang mendegradasi sampai menjadi ukuran yang cukup besar untuk mempengaruhi degradasi; (2) aktivitas enzim mikrobial yang dibutuhkan; (3) perubahan gene tik dalam populasi yang mendegradasi; dan (4) penggunaan substrat pengganti oleh mikroorganisme yang mendegradasi.
Gambar 5. Foto Pertumbuhan (1) PPEA (2) PP (3) (EA) pada Media CMSC dengan Penambahan 10% Minyak Diesel.
Pengamatan secara visual dilakukan selama satu minggu telah menunjukkan adanya perubahan pada media yang semakin lama berubah menjadi keruh (data disajikan pada Lampiran 2a). Minyak diesel yang semula menyatu dan membentuk lapisan tersendiri pada permukaan media akan terpecah menjadi butiran-butiran seperti gelembung dalam jumlah yang cukup banyak. Terbentuknya butiran-butiran minyak tersebut disebabkan oleh produksi biosurfaktan oleh bakteri. Menurut Karanth et al. (2005) beberapa bakteri yang mampu menghasilkan biosurfaktan untuk mengemulsi substrat hidrokarbon antara lain rhamnolipid yang diproduksi oleh Pseudomonas sp. dan trehalose nonionik yang diproduksi oleh Enterobacter sp. Biosurfaktan dapat melarutkan senyawa hidrophobik pada struktur sel yang dapat meningkatkan daya larut antara minyak dan media, sehingga akan menurunkan tegangan permukaan pada minyak.
Berdasarkan pengamatan selama proses degradasi, tercium bau asam ketika tabung serum tersebut dibuka (data disajikan pada Lampiran 2b). Hal ini menunjukkan bahwa terjadi pembentukan asam-asam lemak, CH4, CO2 dan H2O sebagai hasil biodegradasi minyak diesel. Pembentukan gas CO2 dihasilkan melalui proses aerobik yang dilakukan oleh bakteri aerob yaitu Pseudomonas pseudomallei. Menurut Cookson (1995), Enterobacter agglomerans merupakan bakteri anaerobik fakultatif yang dalam kondisi aerob akan mempergunakan asam asetat sebagai sustratnya untuk menghasilkan gas CH4.
Pada degradasi minyak diesel yang 90% komponennya tersusun atas hidrokarbon, maka enzim yang berperan adalah enzim-enzim oksigenase. Monooksigenase berperan dalam degradasi hidrokarbon alifatik, sedangkan dioksigenase pada hidrokarbon asiklik. Pada n-alkana insersi molekul oksigen ke dalam struktur hidrokarbon terjadi pada gugus metil terminal maupun subterminal. N-alkana dioksigenasi menjadi alkohol kemudian menjadi asam karboksilat, yang selanjutnya akan dilakukan pemisahan dua unit karbon secara berkesinambungan dan dikenal dengan sekuen beta oksidasi (Cookson, 1995). Rantai panjang dari asam lemak akan dikonversi oleh acyl coenzyme A membentuk asetil-CoA dan rantai pendek asam lemak yang telah berkurang dua unit gugus karbonnya sebagai CO2 melaui siklus tricarboxylic acid (TCA) secara berulang-ulang (Atlas dan Bartha, 1998; Bailey dan Ollis, 1988).
B. PENGARUH LOGAM BERAT PADA PERTUMBUHAN BAKTERI
0
1. Pengaruh Logam Berat Seng (Zn)
Berdasarkan Gambar 6a, pada konsentrasi 100 ppm Zn kombinasi PPEA memiliki tingkat kekeruhan tertinggi sebesar 0.410 dengan jumlah sel mencapai 9.8x1010 cfu/ml, isolat tunggal PP memiliki tingkat kekeruhan 0.400 dengan jumlah sel mencapai 4.6 x 1010 cfu/ml dan EA memiliki tingkat kekeruhan 0.380 dengan jumlah sel mencapai 3.1 x 1010 cfu/ml (data disajikan pada Lampiran 3). Hal tersebut menunjukkan bahwa kedua isolat mampu tumbuh dan mempunyai toleransi terhadap kehadiran logam Zn.
Dibandingkan dengan kontrol, pada konsentrasi antara 1000 ppm hingga 2000 ppm, pertumbuhan kedua isolat ini hanya mencapai 50 % dibandingkan dengan kontrol. Rata-rata jumlah sel yang mampu tumbuh hanya sebesar 106 - 107 cfu/ml. Pada konsentrasi Zn 4000 ppm, pertumbuhan kedua isolat mengalami penghambatan secara signifikan dengan jumlah sel turun mencapai 5.6x105 cfu/ml untuk PP, 5.0x105 cfu/ml untuk EA dan 6.7 x 105 cfu/ml untuk kombinasi PPEA. Menurut Trindade et al. (2004), jumlah sel optimum dalam melakukan degradasi minyak bumi sebesar 108 cfu/ml dan jumlah sel sebesar 106 cfu/ml, masih memungkinkan untuk mendegradasi senyawa hidrokarbon.
Umumnya pertumbuhan mikroorganisme akan terhambat dengan kenaikan konsentrasi logam. Pada konsentrasi Zn diatas 4000 ppm yang ditambahkan ke dalam media, kedua isolat mengalami penghambatan pertumbuhan dengan jumlah sel kurang dar 106 cfu/ml, bahkan tidak mampu tumbuh sama sekali pada konsentrasi 10000 ppm Zn.
serius karena mempunyai afinitas yang tinggi dengan gugus fosfat seperti ADP dan ATP (Roane dan Pepper, 2000).
Tabel 8. Kinetika Pertumbuhan PPEA Pada Logam Zn
Konsentrasi Zn (ppm) Parameter
100 500 1000 2000 4000 6000 8000
X maks. (mg/ml) 7.8 7.1 6.0 5.4 5.0 4.3 3.3
µx-maks (hari -1
) 0.589 0.563 0.458 0.426 0.411 0.292 0.159
2. Pengaruh Logam Berat Timbal (Pb)
Gambar 6b menunjukkan bahwa kombinasi isolat PPEA mampu tumbuh dan mempunyai toleransi terhadap kehadiran logam Pb. Pada konsentrasi 100 ppm Pb, PPEA memiliki tingkat kekeruhan tertinggi sebesar 0.450 dengan jumlah sel mencapai 8.1x1010 cfu/ml. Sedangkan PP memiliki tingkat kekeruhan 0.430 dengan jumlah sel mencapai 6.8 x 1010 cfu/ml dan EA memiliki tingkat kekeruhan 0.410 dengan jumlah sel mencapai 5.6 x 101 0 cfu/ml (data disajikan pada Lampiran 4).
Pertumbuhan kedua isolat ini hanya mencapai 50 % pada konsentrasi antara 1000 ppm hingga 3000 ppm, dibandingkan dengan kontrol. Rata-rata jumlah sel yang mampu tumbuh hanya sebesar 106 - 107 cfu/ml. Pada konsentrasi Pb 5000 ppm, pertumbuhan kedua isolat mengalami penghambatan secara signifikan dengan jumlah sel turun mencapai 4.3 x 105 cfu/ml untuk PP, 5.0 x 105 sel/ml untuk EA dan 7.4 x 105 cfu/ml untuk kombinasi PPEA. Pertumbuhan mikroorganisme akan terhambat dengan kenaikan konsentrasi logam.
Tabel 9. Kinetika Pertumbuhan PPEA Pada Logam Pb
Konsentrasi Pb (ppm)
Parameter 100 500 1000 2000 3000 5000 8000
X maks. (mg/ml) 5.6 5.6 5.1 4.8 4.6 4.0 3.2
µx-maks (hari- 1) 0.445 0.467 0.444 0.367 0.304 0.255 0.165
Menurut Teitzel dan Parsek (2003), Pseudomonas aeroginosa akan terhambat pertumbuhan saat konsentrasi Pb mencapai 3100 ppm. Shi et al. (2002) telah mengisolasi sejumlah mikroorganisme yang berasal dari tanah terkontaminasi logam Cr, Pb dan hidrokarbon. Pada konsentrasi 400 ppm Pb, dapat menyebabkan turunnya aktivitas bakteri tersebut hingga mencapai 50 %. Logam Pb dapat menyebabkan toksik pada mikroorganisme, karena mampu menempati ion-ion logam esensial yang digunakan untuk metabolisme sel. Logam Pb dapat berikatan dengan gugus sulfidril (-SH), dan mengakibatkan kerusakan pada protein (Wong et al., 2002).
3. Pengaruh Logam Besi (Fe)
Berdasarkan Gambar 6c diatas, kombinasi isolat PPEA mampu tumbuh dan mempunyai toleransi yang lebih baik terhadap kehadiran logam Fe dibandingkan terhadap logam Zn dan logam Pb. Menurut Kementerian Negara Lingkungan Hidup, logam Fe termasuk dalam kategori logam yang bersifat toksik rendah. Pada konsentrasi 100 ppm Fe, kombinasi PPEA memiliki tingkat kekeruhan tertinggi sebesar 0.460 dengan jumlah sel mencapai 4.1x101 1 cfu/ml dibandingkan dengan isolat tunggalnya. Sedangkan PP memiliki tingkat kekeruhan 0.420 dengan jumlah sel mencapai 8.3 x 101 0 cfu/ml dan EA memiliki tingkat kekeruhan 0.430 dengan jumlah sel mencapai 9.6 x 1010 cfu/ml (data disajikan pada Lampiran 5).
6000 ppm, pertumbuhan kedua isolat mengalami penghambatan secara dengan jumlah sel turun mencapai 8.3 x 104 cfu/ml untuk PP, 9.0 x 104 cfu/ml untuk EA dan 3.4 x 105 cfu/ml untuk kombinasi PPEA.
Konsentrasi maksimum hingga kedua isolat tersebut tidak mampu tumbuh dicapai pada 10000 ppm Fe. Menurut Dopson et al. (2003), Acidimicrobium ferrooxidans akan mengalami lisis ketika ditambahkan logam Fe sebesar 20000 ppm, sedangkan L. ferrooxidans dan Acidimicrobium cryptum tahan terhadap logam Fe hingga konsentrasi 28000 ppm. Pengujian ini dilakukan dengan penambahan besi (II) atau Fe2+ sebagai ion yang dapat larut dan umum ditemukan dalam air tanah dibandingkan dengan besi (III).
Tabel 10. Kinetika Pertumbuhan PPEA Pada Logam Fe
Konsentrasi Fe (ppm) Parameter
100 200 1000 2000 4000 6000 8000
X maks. (mg/ml) 7.9 7.3 6.2 5.6 5.1 4.6 3.4
µx-maks (hari- 1) 0.639 0.556 0.454 0.467 0.376 0.346 0.153
Menurut Brock dan Madigan (1991), Fe2+ akan dioksidasi menjadi Fe3+ dan digunakan oleh bakteri dalam menghasilkan energi. Bakteri mengkonsumsi O2, H+ dan Fe2+ untuk menghasilkan Fe3+ dan H2O berdasarkan reaksi berikut ini
2 Fe2+ 2 Fe3+ + 2e 2e + 0.5 O2 + 2H+ H2O 2 Fe2+ + 0.5 O
2 + 2H+ 2 Fe3+ + H2O
dengan membentuk pengkelat. Pseudomonas sp. merupakan salah satu bakteri yang memiliki siderophorus.
Logam besi (Fe) diperlukan untuk mela kukan proses metabolisme dalam konsentrasi yang rendah. Besi (Fe) diperlukan juga dalam proses oksidasi bahan organik dalam media mikroorganisme anaerob untuk menghasilkan energi (Saeni, 1989).
4. Pengaruh Logam Merkuri (Hg)
Logam Hg termasuk logam berat dengan tingkat toksisitas tinggi. Tingkat bahaya Hg yang tinggi dapat diketahui dari banyaknya korban pada penduduk di teluk Minamata yang mengkonsumsi ikan tercemar merkuri.
Berdasarkan Gambar 6d, logam Hg merupakan logam yang paling toksik terhadap pertumbuhan kombinasi isolat PPEA. Pada konsentrasi antara 20 ppm hingga 50 ppm Hg, kombinasi PPEA hanya memiliki tingkat kekeruhan sebesar 0.280 hingga 0.300, dengan jumlah sel antara 107 - 108 cfu/ml. Sedangkan PP memiliki tingkat kekeruhan sekitar 0.260 hingga 0.280, dengan jumlah sel 107 - 108 cfu/ml dan EA memiliki tingkat kekeruhan 0.270 hingga 0.280, dengan jumlah sel mencapai 106-107 cfu/ml (data disajikan pada Lampiran 6). Dibandingkan dengan kontrol, pertumbuhan kedua isolat ini mengalami penur unan.
Pada konsentrasi Hg 100 ppm, pertumbuhan kedua isolat mengalami penghambatan secara signifikan dengan jumlah sel turun mencapai 6.3 x 104 cfu/ml untuk PP, 3.4 x 105 cfu/ml untuk EA dan 7.2 x 105 cfu/ml untuk kombinasi PPEA. Konsentrasi Hg 150 ppm, isolat PP, EA dan kombinasi isolat PPEA hanya mampu tumbuh sebesar 101-102 cfu/ml.
0
mereduksi logam Hg sebesar 94.7% hingga 97.8% pada konsentrasi logam Hg awal sebesar 120 ppm.
Tabel 11. Kinetika Pertumbuhan PPEA Pada Logam Hg
Bakteri yang toleran terhadap Hg merupakan akseptor elektron dan dapat memanfaatkan merkuri dalam metabolisme. Bakteri resisten Hg menghasilkan enzim lyase organomerkuri yang dapat memutuskan ikatan C-Hg dan enzim merkuri reduktase yang mereduksi Hg2+ yang bersifat toksik menjadi Hg0 yang bersifat lebih tidak toksik dan volatil (Gadd, 1990). Hg mudah membentuk ikatan kovalen dengan sulfur. Apabila sulfur terdapat dalam bentuk sulfidril (-SH), maka Hg divalen menggantikan ion hidrogen membentuk merkaptida (Hg-SR). Akibatnya aktivitas gugus sulfidril pada pembentukan protein terhambat, sehingga metabolisme dan fungsi sel terganggu.
10
0 1000 2000 3000 4000 5000 6000 7000
Zn
C. INTERAKSI ANTARA LOGAM SENG (Zn) DAN TIMBAL (Pb)
Titik-titik pengujian ditentukan berdasarkan nilai hasil pengujian OD dan TPC pengaruh logam Zn dan logam Pb terhadap pertumbuhan PPEA. Titik tengah merupakan titik dimana pertumbuhan sel hanya mampu mencapai 50% atau isolat telah mengalami penghambatan dalam pertumbuhannya. Pengujian ini dilakukan untuk mengetahui kemampuan pertumbuhan PPEA pada media dengan penambahan logam Zn - Pb.
1. Pertumbuhan Kombinasi Isolat PPEA
Gambar 8. Grafik Tiga Dimensi (a) dan Kontur (b) Interaksi Zn-Pb Terhadap Nilai Log CFU
Metode Total Plate Count (TPC) merupakan salah satu cara pengukuran pertumbuhan mikroorganisme menggunakan cawan-cawan petri berisi agar yang mengandung medium tumbuh yang tepat. Metode ini hanya mengukur
(a)
(b)
Log sel (cfu/ml)
sel yang mampu hidup. Pertumbuhan sel dengan metode TPC ini diukur saat sel mencapai puncak pertumbuhannya.
Pertumbuhan isolat PPEA dapat digambarkan dengan jelas melalui grafik tiga dimensi dan grafik konturnya. Berdasarkan gambar diatas, pertumbuhan PPEA menuju nilai maksimum ke arah sudut kiri bawah dengan pertumbuhan maksimumnya mencapai 1010 cfu/ml. Gambar kontur bewarna hijau kekuningan menunjukkan bahwa pertumbuhan PPEA turun hingga mencapai 106 cfu/ml. dan warna merah menunjukkan tidak ada lagi pertumbuhan yang terjadi akibat interaksi antara Zn-Pb.
2. Kinetika Pertumbuhan Sel
Kinetika pertumbuhan sel merupakan parameter penting untuk menentukan laju pertumbuhan mikroorganisme. Pertumbuhan mikroorganisme dicirikan dengan waktu yang digunakan untuk menggandakan sel dan konversi substrat menjadi biomassa.
Tabel 12. Hasil Perhitungan Kinetika Pertumbuhan Sel
Interaksi Zn-Pb Dalam Media
Parameter A B C D E F G H I J X maks.
(mg/ml)
4.9 4.7 5.3 4.3 4.5 4.5 4.4 3.9 4.1 3.8 Log TPC maks. 8.903 7.845 9.255 7.204 7.230 7.176 7.301 4.301 7.176 6.255
µx-maks (hari-1) 0.423 0.357 0.376 0.313 0.314 0.301 0.347 0.286 0.268 0.229