Escherichia coli
DARI Bacillus sp.
ASAL TAMBAK UDANG
ISRAMILDA
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa tesis yang berjudul Karakterisasi Zat Antimikrob Penghambat Pertumbuhan Vibrio harveyi dan Escherichia coli dari
Bacillus sp. Asal Tambak Udang adalah benar hasil karya saya sendiri dengan arahan dari komisi pembimbing dan belum pernah dipublikasikan kepada perguruan tinggi manapun. Sumber data dan informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, September 2007
Isramilda
ISRAMILDA. Karakterisasi Zat Antimikrob Penghambat Pertumbuhan Vibrio harveyi dan Escherichia coli dari Bacillus sp. Asal Tambak Udang. Dibimbing oleh IMAN RUSMANA dan NISA RACHMANIA MUBARIK.
Penyakit udang merupakan masalah umum yang terjadi di tambak. Salah satu bakteri patogen penting ialah Vibrio harveyi. Aplikasi bakteri probiotik dapat dijadikan sebagai kontrol untuk menanggulangi pertumbuhan bakteri patogen ditambak. Bacillus sp. merupakan suatu kelompok bakteri yang secara luas digunakan sebagai probiotik di akuakultur. Bakteri ini dapat menghasilkan zat antimikrob polipeptida sebagai bakteriosin dalam menghambat pertumbuhan bakteri lain. Objek dari studi ini untuk menyeleksi isolat Bacillus sp. dari tambak udang dan mengkarakterisasi zat antimikrob polipeptida yang dihasilkan oleh
Bacillus sp. Tiga isolat Bacillus sp. diuji aktivitas antimikrobnya terhadap V. harveyi dan E. coli. Dari hasil menunjukkan bahwa Bacillus sp. Lts 40 mempunyai aktivitas antimikrob paling besar. Uji kompetisi juga menunjukkan isolat Bacillus sp. Lts 40 dapat menghambat pertumbuhan V. harveyi 81,8% dan
E. coli 85,5%. Zat antimikrob ini diproduksi selama fase pertumbuhan dan produksi optimum setelah 3 hari inkubasi. Zat antimikrob polipeptida yang dihasilkan Bacillus sp. Lts 40 stabil pada kisaran pH 3-11 dan zat antimikrob ini juga stabil setelah diperlakukan dengan panas sampai 100 0C selama 20 menit. Hasil purifikasi dengan kromatografi filtrasi gel bahwa fraksi no 21 efektif dalam menghambat pertumbuhan V. harveyi dengan berat molekul 47,3 kDa dan fraksi no 29 efektif dalam menghambat pertumbuhan E. coli dengan berat molekul 34,83 kDa.
ISRAMILDA. Characterization of Antimicrobial Substance Inhibiting Vibrio harveyi and Escherichia coli Growth Produced by Bacillus sp. Isolated from Shrimp Pond. Under the direction of IMAN RUSMANA and NISA RACHMANIA MUBARIK.
Shrimp diseases are the mayor problem in shrimp culture. One of the important bacterial pathogen in shrimp culture is Vibrio harveyi. Application of bacterial probiotic is an alternative solution to control the growth of bacterial pathogen in shrimp culture. Bacillus sp. is one group of bacteria that has been used widely as a probiotic in aquaculture. This bacteria can produce antimicrobial polipeptides such as bacteriocins that can inhibit growth of other bacteria. The objectives of this study were to screen Bacillus sp. isolated from shrimp pond and to characterize their antimicrobial polipeptides produced by the isolates. Three isolates of Bacillus sp. were examined their antimicrobial activity againt V. harveyi and E. coli. The result showed that Bacillus sp Lts 40 had the biggest antimicrobial activity. Competition assay showed that Bacillus sp Lts 40 isolate could inhibit the growth of V. harveyi and E. coli up to 81,8% and 85,5% respectively. This substance was produced during the growth and optimum production was found after 3 days of incubation. Antimicrobial polipeptides produced by Bacillus sp. Lts 40 was stable in the range of pH 3 up to pH 11 and this antimicrobial substance was remain stable after heating at 100 0C for 20 minutes. Based on purification result using chromatografi filtration technique showed that fraction number 21 was effective to inhibit V. harveyi growth and its molecular weight was 47,3 kDa and fraction number 29 was effective to inhibit E. coli growth and its molecular weight was 34,83 kDa.
ISRAMILDA. Karakterisasi Zat Antimikrob Penghambat Pertumbuhan Vibrio harveyi dan Escherichia coli dari Bacillus sp. Asal Tambak Udang. Dibimbing oleh IMAN RUSMANA dan NISA RACHMANIA MUBARIK.
Penyakit merupakan masalah yang umum terjadi di tambak udang, salah satunya disebabkan oleh bakteri. Bakteri yang menyebabkan penyakit pada udang ialah Vibrio harveyi. Bakteri ini dapat menyebabkan kematian massal pada udang sehingga akan menyebabkan produksi dari udang itu mengalami penurunan. Sedangkan tantangan yang harus dihadapi dalam pasar dunia bagi komoditas perikanan budidaya udang tidak hanya masalah kuantitas saja tetapi juga kualitas atau mutu udang. Mutu dan keamanan makanan seperti residu antibiotik, bakteri patogen juga harus mendapat perhatian yang serius, bakteri indikator uji mutu kualitas dan makanan salah satunya adalah Escherichia coli. Peraturan pemerintah juga melarang menggunakan antibiotik karena dapat menimbulkan masalah baru yaitu terakumulasinya antibiotik pada lingkungan dan timbulnya resistensi dari mikrob patogen. Maka dilakukan alternatif dalam pengendalian penyakit ini dengan memamfaatkan bakteri probiotik, salah satunya ialah Bacillus. Bacillus sp. memiliki kemampuan dalam menghasilkan zat antimikrob.
Tujuan penelitian ini untuk menyeleksi dan mengkarakterisasi zat antimikrob isolat bakteri Bacillus sp. dari tambak udang yang potensial digunakan sebagai probiotik yang dapat menghambat pertumbuhan V. harveyi dan E. coli.
Penelitian ini menggunakan tiga isolat bakteri Bacillus sp. dan bakteri indikator ialah V. harveyi dan E. coli. Tahap-tahap yang dilakukan: (1) seleksi isolat penghasil zat antimikrob dengan menggunakan double layer method dan
cross streak method, (2) kompetisi dalam media cair, (3) penentuan waktu optimum produksi zat antimikrob, dan (4) karakterisasi zat antimikrob yang meliputi: pemurnian zat antimikrob, stabilitas terhadap pH dan suhu.
Dari tiga isolat Bacillus sp. yang diseleksi, Bacillus sp. Lts 40 yang memiliki aktivitas penghambatan paling besar terhadap E. coli dan V. harveyi dengan indeks penghambatan masing-masing 3 dan 7. Berdasarkan zona hambat yang terbentuk bahwa V. harveyi memiliki sensitivitas lebih tinggi dari E. coli terhadap zat antimikrob yang dihasilakan Bacillus sp. Lts 40. Pada uji kompetisi, persentase penghambatan dengan rasio inokulum 1:1 sudah cukup bagi Bacillus
sp. Lts 40 menghambat pertumbuhan V. harveyi (81,8%) dan terhadap E. coli
E. coli 12 mm dan pada V. harveyi 11 mm. Tahap selanjutnya pemurnian zat antimikrob yang meliputi pengendapan dengan amonium sulfat, dialisis dan dilanjutkan dengan kromatografi filtrasi gel. Pada pengendapan dengan amonium sulfat, aktivitas penghambatan paling tinggi terdapat pada pengendapan 30-40% terhadap E. coli dan 60-70% terhadap V. harveyi. Setelah itu didialisis selama semalam dan kemudian dilanjutkan dengan kromatografi filtrasi gel.
Hasil fraksinasi dengan menggunakan kromatografi filtrasi gel, zat antimikrob yang dihasilkan oleh Bacillus sp. Lts 40 merupakan polipeptida dengan berat molekul terhadap V. harveyi 47,38 kDa dan pada E. coli 34,83 kDa yang selanjutnya dinyatakan sebagai bakteriosin. Zat antimikrob Bacillus sp. Lts 40 juga bersifat stabil pada kisaran pH 3-11 dan juga tahan terhadap perlakuan panas sampai 100 0C selama 20 menit.
© Hak cipta milik Institut Pertanian Bogor, tahun 2007
Hak cipta dilindungi Undang-undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumber
a. pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah.
b. pengutipan tidak merugikan kepentingan yang wajar IPB. 2. Dilarang mengumumkan dan memperbanyak sebagian atau seluruh
Escherichia coli
DARI Bacillus sp.
ASAL TAMBAK UDANG
ISRAMILDA
Tesis
Sebagai salah satu syarat memperoleh gelar Magister Sains pada
Programstudi Biologi
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Nama : Isramilda
NIM : G351050081
Disetujui
Komisi Pembimbing
Dr. Ir. Iman Rusmana, M.Si Dr. Nisa Rachmania Mubarik, M.Si Ketua Anggota
Diketahui
Ketua Program Studi Biologi Dekan Sekolah Pascasarjana
Dr. Ir. Dedy duryadi DEA Prof. Dr. Ir. Khairil A. Notodiputro, MS
Escherichia coli
DARI Bacillus sp.
ASAL TAMBAK UDANG
ISRAMILDA
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa tesis yang berjudul Karakterisasi Zat Antimikrob Penghambat Pertumbuhan Vibrio harveyi dan Escherichia coli dari
Bacillus sp. Asal Tambak Udang adalah benar hasil karya saya sendiri dengan arahan dari komisi pembimbing dan belum pernah dipublikasikan kepada perguruan tinggi manapun. Sumber data dan informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, September 2007
Isramilda
ISRAMILDA. Karakterisasi Zat Antimikrob Penghambat Pertumbuhan Vibrio harveyi dan Escherichia coli dari Bacillus sp. Asal Tambak Udang. Dibimbing oleh IMAN RUSMANA dan NISA RACHMANIA MUBARIK.
Penyakit udang merupakan masalah umum yang terjadi di tambak. Salah satu bakteri patogen penting ialah Vibrio harveyi. Aplikasi bakteri probiotik dapat dijadikan sebagai kontrol untuk menanggulangi pertumbuhan bakteri patogen ditambak. Bacillus sp. merupakan suatu kelompok bakteri yang secara luas digunakan sebagai probiotik di akuakultur. Bakteri ini dapat menghasilkan zat antimikrob polipeptida sebagai bakteriosin dalam menghambat pertumbuhan bakteri lain. Objek dari studi ini untuk menyeleksi isolat Bacillus sp. dari tambak udang dan mengkarakterisasi zat antimikrob polipeptida yang dihasilkan oleh
Bacillus sp. Tiga isolat Bacillus sp. diuji aktivitas antimikrobnya terhadap V. harveyi dan E. coli. Dari hasil menunjukkan bahwa Bacillus sp. Lts 40 mempunyai aktivitas antimikrob paling besar. Uji kompetisi juga menunjukkan isolat Bacillus sp. Lts 40 dapat menghambat pertumbuhan V. harveyi 81,8% dan
E. coli 85,5%. Zat antimikrob ini diproduksi selama fase pertumbuhan dan produksi optimum setelah 3 hari inkubasi. Zat antimikrob polipeptida yang dihasilkan Bacillus sp. Lts 40 stabil pada kisaran pH 3-11 dan zat antimikrob ini juga stabil setelah diperlakukan dengan panas sampai 100 0C selama 20 menit. Hasil purifikasi dengan kromatografi filtrasi gel bahwa fraksi no 21 efektif dalam menghambat pertumbuhan V. harveyi dengan berat molekul 47,3 kDa dan fraksi no 29 efektif dalam menghambat pertumbuhan E. coli dengan berat molekul 34,83 kDa.
ISRAMILDA. Characterization of Antimicrobial Substance Inhibiting Vibrio harveyi and Escherichia coli Growth Produced by Bacillus sp. Isolated from Shrimp Pond. Under the direction of IMAN RUSMANA and NISA RACHMANIA MUBARIK.
Shrimp diseases are the mayor problem in shrimp culture. One of the important bacterial pathogen in shrimp culture is Vibrio harveyi. Application of bacterial probiotic is an alternative solution to control the growth of bacterial pathogen in shrimp culture. Bacillus sp. is one group of bacteria that has been used widely as a probiotic in aquaculture. This bacteria can produce antimicrobial polipeptides such as bacteriocins that can inhibit growth of other bacteria. The objectives of this study were to screen Bacillus sp. isolated from shrimp pond and to characterize their antimicrobial polipeptides produced by the isolates. Three isolates of Bacillus sp. were examined their antimicrobial activity againt V. harveyi and E. coli. The result showed that Bacillus sp Lts 40 had the biggest antimicrobial activity. Competition assay showed that Bacillus sp Lts 40 isolate could inhibit the growth of V. harveyi and E. coli up to 81,8% and 85,5% respectively. This substance was produced during the growth and optimum production was found after 3 days of incubation. Antimicrobial polipeptides produced by Bacillus sp. Lts 40 was stable in the range of pH 3 up to pH 11 and this antimicrobial substance was remain stable after heating at 100 0C for 20 minutes. Based on purification result using chromatografi filtration technique showed that fraction number 21 was effective to inhibit V. harveyi growth and its molecular weight was 47,3 kDa and fraction number 29 was effective to inhibit E. coli growth and its molecular weight was 34,83 kDa.
ISRAMILDA. Karakterisasi Zat Antimikrob Penghambat Pertumbuhan Vibrio harveyi dan Escherichia coli dari Bacillus sp. Asal Tambak Udang. Dibimbing oleh IMAN RUSMANA dan NISA RACHMANIA MUBARIK.
Penyakit merupakan masalah yang umum terjadi di tambak udang, salah satunya disebabkan oleh bakteri. Bakteri yang menyebabkan penyakit pada udang ialah Vibrio harveyi. Bakteri ini dapat menyebabkan kematian massal pada udang sehingga akan menyebabkan produksi dari udang itu mengalami penurunan. Sedangkan tantangan yang harus dihadapi dalam pasar dunia bagi komoditas perikanan budidaya udang tidak hanya masalah kuantitas saja tetapi juga kualitas atau mutu udang. Mutu dan keamanan makanan seperti residu antibiotik, bakteri patogen juga harus mendapat perhatian yang serius, bakteri indikator uji mutu kualitas dan makanan salah satunya adalah Escherichia coli. Peraturan pemerintah juga melarang menggunakan antibiotik karena dapat menimbulkan masalah baru yaitu terakumulasinya antibiotik pada lingkungan dan timbulnya resistensi dari mikrob patogen. Maka dilakukan alternatif dalam pengendalian penyakit ini dengan memamfaatkan bakteri probiotik, salah satunya ialah Bacillus. Bacillus sp. memiliki kemampuan dalam menghasilkan zat antimikrob.
Tujuan penelitian ini untuk menyeleksi dan mengkarakterisasi zat antimikrob isolat bakteri Bacillus sp. dari tambak udang yang potensial digunakan sebagai probiotik yang dapat menghambat pertumbuhan V. harveyi dan E. coli.
Penelitian ini menggunakan tiga isolat bakteri Bacillus sp. dan bakteri indikator ialah V. harveyi dan E. coli. Tahap-tahap yang dilakukan: (1) seleksi isolat penghasil zat antimikrob dengan menggunakan double layer method dan
cross streak method, (2) kompetisi dalam media cair, (3) penentuan waktu optimum produksi zat antimikrob, dan (4) karakterisasi zat antimikrob yang meliputi: pemurnian zat antimikrob, stabilitas terhadap pH dan suhu.
Dari tiga isolat Bacillus sp. yang diseleksi, Bacillus sp. Lts 40 yang memiliki aktivitas penghambatan paling besar terhadap E. coli dan V. harveyi dengan indeks penghambatan masing-masing 3 dan 7. Berdasarkan zona hambat yang terbentuk bahwa V. harveyi memiliki sensitivitas lebih tinggi dari E. coli terhadap zat antimikrob yang dihasilakan Bacillus sp. Lts 40. Pada uji kompetisi, persentase penghambatan dengan rasio inokulum 1:1 sudah cukup bagi Bacillus
sp. Lts 40 menghambat pertumbuhan V. harveyi (81,8%) dan terhadap E. coli
E. coli 12 mm dan pada V. harveyi 11 mm. Tahap selanjutnya pemurnian zat antimikrob yang meliputi pengendapan dengan amonium sulfat, dialisis dan dilanjutkan dengan kromatografi filtrasi gel. Pada pengendapan dengan amonium sulfat, aktivitas penghambatan paling tinggi terdapat pada pengendapan 30-40% terhadap E. coli dan 60-70% terhadap V. harveyi. Setelah itu didialisis selama semalam dan kemudian dilanjutkan dengan kromatografi filtrasi gel.
Hasil fraksinasi dengan menggunakan kromatografi filtrasi gel, zat antimikrob yang dihasilkan oleh Bacillus sp. Lts 40 merupakan polipeptida dengan berat molekul terhadap V. harveyi 47,38 kDa dan pada E. coli 34,83 kDa yang selanjutnya dinyatakan sebagai bakteriosin. Zat antimikrob Bacillus sp. Lts 40 juga bersifat stabil pada kisaran pH 3-11 dan juga tahan terhadap perlakuan panas sampai 100 0C selama 20 menit.
© Hak cipta milik Institut Pertanian Bogor, tahun 2007
Hak cipta dilindungi Undang-undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumber
a. pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah.
b. pengutipan tidak merugikan kepentingan yang wajar IPB. 2. Dilarang mengumumkan dan memperbanyak sebagian atau seluruh
Escherichia coli
DARI Bacillus sp.
ASAL TAMBAK UDANG
ISRAMILDA
Tesis
Sebagai salah satu syarat memperoleh gelar Magister Sains pada
Programstudi Biologi
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Nama : Isramilda
NIM : G351050081
Disetujui
Komisi Pembimbing
Dr. Ir. Iman Rusmana, M.Si Dr. Nisa Rachmania Mubarik, M.Si Ketua Anggota
Diketahui
Ketua Program Studi Biologi Dekan Sekolah Pascasarjana
Dr. Ir. Dedy duryadi DEA Prof. Dr. Ir. Khairil A. Notodiputro, MS
melimpahkan rahmat dan karunia-Nya sehingga tesis ini dapat diselesaikan. Tesis
yang berjudul “ Karakterisasi Zat Antimikrob Penghambat Pertumbuhan Vibrio harveyi dan Escherichia coli dari Bacillus sp. Asal Tambak Udang”.
Pada kesempatan kali ini, terima kasih dan penghargaan setinggi-tingginya
ingin penulis sampaikan kepada mereka yang telah berperan serta:
1. Dr. Ir. Iman Rusmana, M.Si, Dr. Nisa Rachmania Mubarik, M.Si selaku
dosen pembimbing yang telah meluangkan banyak waktu dan dengan
sabar memberikan bimbingan, arahan serta saran selama tesis ini
dirampungkan. Dr. Munti Yuhana SPi M.Si. selaku dosen penguji luar
komisi atas saran dan masukannya.
2. Orang-orang terkasih dalam hidup ini: Papa dan Mama serta adik-adik,
terimakasih untuk kehangatan cinta, dukungan, pengorbanan dan doa tiada
henti.
3. Rekan-rekan Lab Mikrobiologi (Bu‘It, Bu’ Tati, mbak Niken, Rina, mas Asrul, Irul, Ria, mbak dini, Rika dan adik-adik S1 Ika, Ima, Bibah, Rio,
Novan, Andri, Tri, Wahyu, Besti, Sarah, Muthe, Irni serta Teknisi lab
Mikrobiologi, mbak Heni, Bu’ Kokoy, pak Jaka dan pak Ndang), terimakasih atas persahabatan dan kerjasamanya selama ini. Juga penulis
menyampaikan ucapan terima kasih kepada Ibu Alina di Balitbiogen.
4. Teman-teman Wisma Vaillya (Oja, Bu ‘ Agnest, kak Diana dan Ela), terima kasih untuk persaudaraan yang telah terbina.
5. Seluruh rekan-rekan Bio (Vil, mas Sigit, Handay, mas Ratman, Dewi, kak
Meri, Bu‘ zubaidah, pak Krey dan rekan lainnya), terima kasih atas persahabatan selama ini.
Akhir kata penulis mengharapkan semoga tesis ini dan apa yang telah
dihasilkan dapat bermanfaat bagi pengembangan ilmu pengetahuan, bagi pembaca
pada umumnya dan penulis pada khususnya.
Bogor, September 2007
Penulis dilahirkan di Buo, 21 Mei 1982 merupakan putri sulung dari tiga
bersaudara pasangan Ayahanda Syawaluddin dan Ibunda Sustiar.
Pendidikan dasar diselesaikan di SD Negeri 09 Buo pada tahun 1994,
dilanjutkan ke Sekolah Madrasah Tsanawiyah Negeri Lintau Kab. Tanah Datar
dan menyelesaikannya pada tahun 1997. Sekolah lanjutan tingkat atas di
selesaikan di Madrasah Aliyah Negeri (MAN/MAKN) Koto Baru Padang Panjang
pada tahun 2000. Pada tahun yang sama melalui jalur PMDK, penulis diterima di
Program Studi Biologi Fakultas Matematika Ilmu Pengeta huan Alam Universitas
Negeri Padang dan lulus tahun 2005, kemudian penulis melanjutkan pendidikan
DAFTAR GAMBAR ... xii
Probiotik di Akuakultur... 3
Bacillus sp. sebagai Probiotik di Akuakultur ... 4 Biosintesis Bakteriosin . ... 6 Kemampuan Penghambatan Bacillus sp. Lts 40 terhadap V. harveyi
dan E. coli pada Kultur Campur Media Cair... 20 Waktu optimum Produksi Zat Antimikrob ... 21 Karakteristik Zat Antimikrob ... 22 Pemurnian Zat Antimikrob dengan Kromatografi. ... 23 Stabilitas Aktivitas Penghambatan Bacillus sp. Lts 40 terhadap
pH dan Suhu. ... 25
1 Efek biokimia bakteriosin bakteri Gram positif terhadap sel sensitif ... 8
2 Indeks penghambatan isolat Bacillus sp. penghasil antimikrob terhadap
V. harveyi dan E. coli dengan double layer method ... ... 19
3 Jarak penghambatan Bacillus sp. terhadap V. harveyi dan E. coli dengan
cross streak method ... ... 19
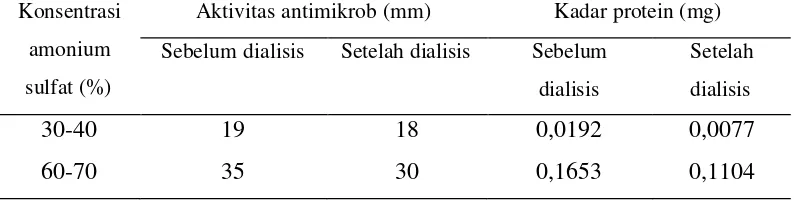
4 Aktivitas antimikrob pada proses dialisis... 23
5 Pengaruh suhu terhadap aktivitas antimikrob dari hasil dialisis ... 26
1 Model hipotesis biosintesis molekul pediosin AcH (Jack et al. 1995) ... 7
2 Mekanisme kerja molekul bakteriosin menembus membran sel
(Bibiana 1999 dalam Suarsana 2000)... 9
3 Penampakan hasil uji penghambatan dengan cross streak method ... 20 4 Persentase penghambatan Bacillus sp. Lts 40 terhadap (a) V. harveyi,
dan (b) E. coli ... ... 20 5 Jumlah sel Bacillus sp. Lts 40 dengan rasio inokulum Bacillus sp.
Lts 40 terhadap (a) V. harveyi dan (b) E. coli ... ... 21 6 (a) Kurva pertumbuhan Bacillus sp. Lts 40 pada media SWC, dan
(b) aktivitas penghambatan Bacillus sp. Lts 40 terhadap V. harveyi
dan E. coli... 21 7 Aktivitas penghambatan Bacillus sp. Lts 40 terhadap (a) E. coli,
(b) V. harveyi setelah penambahan amonium sulfat, dan (c) konsentrasi
protein ... 22
8 Penampakan aktivitas penghambatan pada (a) pengendapan 60-70%
terhadap V. harveyi, dan (b) pengendapan 30-40% terhadap E. coli ... 23 9 (a) Kromatogram dari hasl filtrasi gel, dan (b) aktivitas penghambatan
fraksi kromatografi filtrasi gel Bacillus sp. Lts 40.terhadap V. harveyi dan
E. coli ... 24
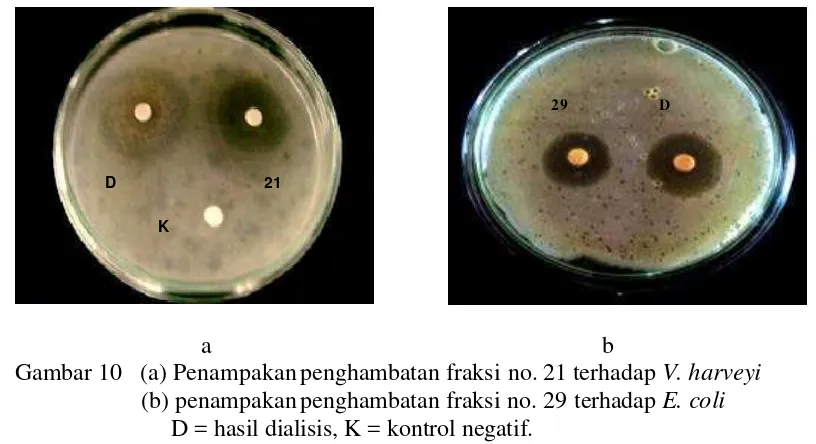
10 (a) Penampakan penghambatan fraksi no. 21 terhadap V. harveyi, dan
(b) penampakan penghambatan fraksi no. 29 terhadap E. coli ... 24
11 Aktivitas penghambatan Bacillus sp. Lts 40 terhadap V. harveyi
dan E. coli pada pH 3-11 hasil dialisis ... 25 12 Penampakan aktivitas antimikrob Bacillus sp. Lts 40 pada pH
1 Komposisi media ya ng digunakan ... 40
2 Komposisi reagen Bradford (Bradford 1976) ... 40 3 Jumlah amonium sulfat yang ditambahkan per 1 liter larutan
(Scopes 1987) .. ... 41
3 Kurva standar protein hasil pengendapan amonium sulfat, dialisis... 42
4 Penentuan kadar protein fraksi filtrasi gel dengan metode Bradford
(1976)... 43
PENDAHULUAN
Latar Belakang
Dalam usaha menunjang peningkatan devisa nonmigas melalui peningkatan
ekspor hasil perikanan, pemerintah menetapkan udang sebagai komoditas andalan
utama. Peluang dalam mengembangkan perikanan budidaya udang guna
memenuhi pasar dunia masih sangat besar. Produktivitas tambak udang
mengalami penurunan antara lain disebabkan oleh munculnya berbagai macam
penyakit. Tantangan-tantangan lain yang harus dihadapi dalam pasar dunia bagi
komoditi ekspor perikanan budidaya tidak hanya kuantitas saja, akan tetapi juga
kualitas atau mutu udang yang siap ekspor. Mutu dan keamanan makanan seperti
residu antibiotik, bakteri patogen, racun hayati laut (biotoksin) dan residu
pestisida juga harus mendapatkan perhatian yang serius, bakteri indikator uji mutu
kualitas dan makanan salah satunya ialah Escherichia coli (Djazuli 2002). Peraturan pemerintah untuk budidaya udang melarang penggunaan antibiotik.
Menurut Verschuere et al. (2000) penggunaan antibiotik untuk mencegah dan mengobati penyakit dapat menimbulkan masalah baru, yaitu terakumulasinya
antibiotik pada lingkungan dan spesies yang dibudidaya serta timbulnya resistensi
mikrob patogen. Resistensi terhadap antibiotik semakin meningkat karena
resistensi dapat ditransfer dari satu mikrob ke mikrob lainnya. Lightner (1993)
melaporkan beberapa kelompok bakteri penyebab penyakit udang yaitu : Vibrio,
Aeromonas, Pseudomonas dan Flavobacterium.
Bakteri patogen penting pada udang adalah Vibrio harveyi. Bakteri ini merupakan bakteri penyebab utama serangan penyakit pada udang yang dapat
terjadi mulai pada tingkat larva. Populasi V. harveyi sangat penting diperhatikan dalam budidaya udang, karena bakteri ini penyebab serangan penyakit vibriosis
yang berpendar. Serangan bakteri ini pada stadia larva dapat menyebabkan
kematian massal (Zafran & Roza 1993).
Alternatif pengendalian penyakit udang yang disebabkan bakteri patogen di
tambak udang ialah dengan memanfaatkan bakteri probiotik. Istilah probiotik
didefinisikan sebagai mikrob hidup yang memberikan pengaruh menguntungkan
inang, memperbaiki nilai nutrisi, memperbaiki respon inang terhadap penyakit,
atau memperbaiki lingkungan kualitas ambangnya (Verschuere et al. 2000). Bakteri probiotik menghasilkan senyawa metabolit yang memiliki efek
bakterisida atau bakteriostatik untuk menghambat pertumbuhan bakteri patogen
atau bakteri yang dapat menurunkan kualitas udang selama budidaya udang. Salah
satu bakteri yang umum digunakan dan menghasilkan zat antimikrob tersebut
ialah Bacillus sp. Bakteri kelompok ini umumnya ditemukan pada sedimen dan saluran pencernaan udang (Verschuere et al. 2000). Bacillus sp. dapat memproduksi zat antimikrob berupa bakteriosin (Irina et al. 2001).
Tujuan Penelitian
Penelitian ini bertujuan untuk menyeleksi dan mengkarakterisasi zat
antimikrob isolat bakteri Bacillus sp. dari tambak udang yang potensial digunakan sebagai probiotik yang dapat menghambat pertumbuhan Vibrio harveyi dan
TINJAUAN PUSTAKA
Probiotik di Akuakultur
Definisi probiotik pada akuakultur adalah mikrob hidup yang memiliki efek
menguntungkan pada inang dengan cara memodifikasi asosiasi inang atau ambang
batas komunitas mikrob dengan meningkatkan penggunaan pakan atau nilai
nutrisi, meningkatkan ketahanan inang terhadap penyakit atau meningkatkan
kualitas lingkungan. Berdasarkan definisi tersebut, maka probiotik termasuk juga
mikrob yang mencegah proliferasi patogen dalam saluran pencernaan, pada
permukaan tubuh ina ng, dan pada lingkungan, mikrob yang dapat meningkatkan
penggunaan pakan dengan meningkatkan daya cerna pakan, meningkatkan sistem
imun inang dan meningkatkan kualitas air (Verschuere et al. 2000).
Menurut Gomez-Gil et al. (2000) biokontrol ialah penggunaan musuh alami untuk mengurangi kerusakan yang ditimbulkan oleh organisme yang berbahaya
atau pengaturan populasi penyakit oleh musuh alamiahnya. Selanjutnya
ditambahkan bahwa komunitas mikrob di dalam saluran pencernaan hewan
sampai batas tertentu dapat me mberikan ketahanan terhadap penyakit.
Probiotik dalam akuakultur sering digunakan karena kemampuannya
memproduksi senyawa antimikrob. Probiotik yang berada di saluran pencernaan
dapat menghambat kerja bakteri patogen yang merusak melalui saluran
pencernaan. Interaksi antara mikrob dengan inang tidak terbatas pada saluran
pencernaan, bakteri probiotik dapat juga aktif pada insang, kulit tubuh inang atau
lingkungan sekitarnya. Interaksi yang intensif antara mikrob dan inang dalam
akukultur menjadikan sejumlah probiotik tidak hanya berhasil diisolasi dari
saluran pencernaan tetapi dapat juga diisolasi di lingkungan budidaya (Irianto
2003).
Mikrob probiotik unggul dapat diperoleh melalui eksplorasi dan seleksi
aktivitasnya. Mikrob probiotik dapat diisolasi dari inang dan habitat dimana
organisme tersebut akan diaplikasikan atau dari habitat yang berbeda (Verschuere
et al. 2000).
Penggunaan probiotik sebagai agen biokontrol dalam penanggulangan
pemakaiannya. Pemakaian antibiotik yang terus menerus pada dosis subletal dapat
menyebabkan timbulnya mikrob resisten terhadap antibiotik. Resistensi gen pada
bakteri patogen dapat ditransfer ke bakteri lain yang belum berkontak dengan
antibiotik (Verschuere et al. 2000).
Bacillus sp. sebagai Probiotik di Akuakultur
Dewasa ini penelitian mikrob menguntungkan bagi akuakultur mulai dicoba
pada mikrob yang diisolasi dari air laut, sedimen ataupun organ hewan yang
mampu menghasilkan senyawa antimikrob yang dapat menghambat pertumbuhan
bakteri patogen secara in vitro (Rengpipat et al. 1998). Secara umum probiotik untuk budidaya perairan diseleksi berdasarkan kemampuannya dalam
memproduksi senyawa antimikrob (Vine et al. 2004).
Menurut Verschuere et al. (2000) mekanisme kerja bakteri probiotik dapat dibagi menjadi beberapa cara yaitu: (1) produksi senyawa inhibitor, (2) kompetisi
terhadap senyawa kimia atau sumber energi, (3) kompetisi terhadap tempat
pelekatan, (4) peningkatan respon immun, (5) perbaikan kualitas air, dan (6)
interaksi dengan fitoplankton.
Sumber mikrob yang digunakan untuk probiotik dapat berasal dari inangnya
yang secara alami ada pada organ organisme tersebut atau dari habitatnya (air atau
sedimen). Mikrob yang digunakan sebagai probiotik harus mempunyai sifat
apatogen, tidak beracun, bersifat alami dan umum digunakan (Lopez 2000).
Beberapa probiotik yang telah digunakan dalam aquakultur adalah kelompok
bakteri asam laktat seperti Lactobacillus dan Carnobacteruium, genus Vibrio (V. alginolyticus), genus Bacillus, atau genus Pseudomonas. Irina et al. (2001) melaporkan bahwa bakteri dari genus Bacillus sp. bisa memproduksi zat antimikrob berupa bakteriosin. Bakteriosin merupakan zat antimikrob yang
merupakan polipeptida, protein atau senyawa yang mirip protein. Bakteriosin
disintesis di ribosom oleh bakteri selama masa pertumbuhannya dan umumnya
hanya menghambat galur-galur bakteri yang berkerabat dekat dengan bakteri
penghasil bakteriosin (Jack et al. 1995, Kone & Fung 1992). Kriteria yang merupakan ciri-ciri bakteriosin adalah (1) memiliki spektra aktivitas yang lebih
bakterisida, (4) mempunyai reseptor spesifik pada sel sasaran, dan (5) gen
determinan terdapat pada plasmid, plasmid rekombinan atau episom, kromosom
atau transposon yang berperan pada produksi dan imunitas (Tagg et al. 1976). Beberapa peneliti telah berhasil mengisolasi dan memurnikan bakteriosin
yang diproduksi oleh Bacillus sp. Gram positif di antaranya Subtilin dihasilkan oleh B. subtilis (Klein et al. 1993), Megacin oleh B. megaterium (Tagg et al. 1976), Coagulin oleh B. coagulans I4 (Hyronimus 1998), Cerein oleh B. cereus
(Oscariz & Pisabarro 2000), dan Tochicin oleh B. thuringiensis (Paik et al. 1997). Bakteriosin yang dihasilkan oleh bakteri Gram positif biasanya merupakan
polipeptida bermuatan positif yang dapat menembus membran sel dan tersusun
kurang dari 60 residu asam amino. Berdasarkan struktur asam aminonya
bakteriosin dapat diklasifikasikan ke dalam dua kelompok yaitu:
1. Kelompok lantibiotik: yaitu kelompok bakteriosin yang dikarakterisasi
oleh adanya jemb atan sulfur intra rantai dan me ngandung asam amino
yang tidak lazim yaitu dehidrolanin, lantionin dan ß-metil lantionin,
misalnya pada nisin yang dihasilkan oleh Lactococcus lactis (Hurst 1981) dan variacin (Pridmore et al. 1996).
2. Kelompok nonlantibiotik yang dapat dibagi dua berdasarkan bobot
molekulnya yaitu:
a. bakteriosin dengan berat molekul relatif kecil sekitar 2-6 kDa (Lozano
et al. 1992), misalnya Pediocin AcH yang dihasilkan oleh Pediococcus acidilactici.
b. bakteriosin dengan berat molekul relatif besar biasanya di atas 30 kDa
(Benoit et al. 1994), contohnya helveticine J yang dihasilkan oleh
Biosintesis Bakteriosin
Bakteriosin dapat dibedakan dari antibiotik atau antibakteri dari proses
biosintesisnya. Menurut Williams et al. (1996) bakteriosin disintesis melalui jalur ribosom sedangkan antibiotik disintesis melalui jalur di luar ribosom dengan
melibatkan multienzim. Kebanyakan bakteriosin disintesis dalam bentuk protein
yang tidak aktif yang memiliki N-terminal leader sequence dan C-terminal prepeptida.
Jack et al. (1995) menyatakan bahwa gen penyandi produksi bakteriosin terdapat di plasmid (contoh: Colicin dan bakteriosin yang dihasilkan oleh banyak bakteri Gram positif), plasmid rekombinan atau episom (contoh: Lactocin F), kromosom (contoh: Subtilin) atau transposon (contoh: Nisin).
Gen penyandi produksi bakteriosin dari golongan non lantionin pada
umumnya terdapat di plasmid kecuali lactacin F yang gen penyandinya terletak di episom (Muriana & Kleenhammer 1991), plantarin A yang gen penyandinya
terletak di kromosom (Dzung et al. 1993).
Gen penyandi bakteriosin dalam keadaan normal berada dalam keadaan
represif. Bila terjadi mutasi atau kompetisi untuk nutrisi esensial gen represif
tereduksi dan berakibat terbentuknya senyawa antibakteri (DeGroat & Oudega
1986). Biosintesis bakteriosin meningkat bila ada SOS-inducing agents yaitu senyawa yang dapat mengakibatkan kerusakan sel seperti radiasi sinar ultra violet
(Jack et al. 1995).
Karakterisasi gen plasmid yang mengkode produksi dan imunitas
bakteriosin telah banyak dilakukan (Muriana & Kleenhammer 1991; Hasting et al. 1991). Salah satunya mentransfer gen plasmid (Bac+) Lactococcus lactis subsp
Biosintesis bakteriosin dengan berat molekul rendah yang dihasilkan oleh
bakteri Gram positif diawali dengan pembentukan prepeptida yaitu bakteriosin
yang belum aktif, dengan ujung N penuntun (N-terminal leader sequence) yang pendek. Ujung ini terpisah pada saat pematangan dengan bantuan endopeptidase
(de Vos et al. 1991). Pada lantibiotik pemisahan terjadi pada asam amino prolin, sedangkan pada non lantibiotik terjadi pada asam amino glisin. Pemisahan ini
untuk mempermudah prepeptida bergandengan dengan peptida lain yang tepat.
Ujung penuntun N ini berperan penting untuk mengarahkan proses pematangan
berupa penggandengan prepeptida dengan peptida lain untuk membentuk
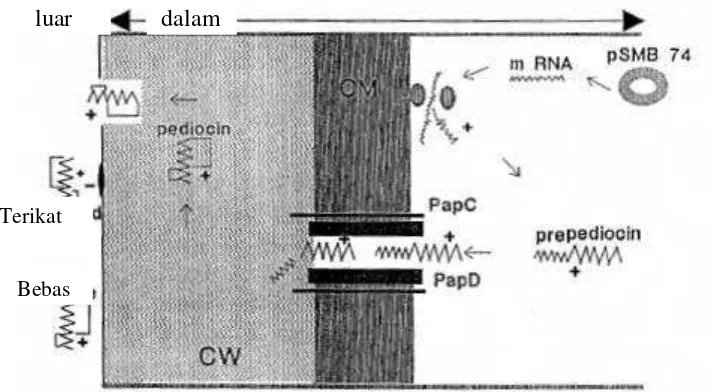
bakteriosin aktif (Jack et al. 1995). Penglepasan bakteriosin aktif ke ekstraseluler dari model hipotesis biosintesis pediocin AcH yang tergolong ke dalam non lantibiotik bergantung pada pH lingkungan molekul pediocinAcH yang berbentuk bebas atau terikat pada dinding sel (Gambar 1).
Gambar 1 Model hipotesis biosintesis molekul pediocin AcH (Jack et al. 1995). CW = dinding sel, OM = membran luar
luar dalam
Terikat
Mekanisme Kerja Bakteriosin
Mekanisme kerja bakteriosin diketahui bergantung pada konsentrasi
bakteriosin, kemampuan ionisasi, suhu, pH dan fase pertumbuhan sel target (Sahl
& Brandis 1982, Tabel 1).
Tabel 1 Efek biokimia bakteriosin bakteri Gram positif terhadap sel sensitif
Bakteriosin Menghambat síntesis Efek lainnya DNA RNA Protein
Megacin A-216 TU TU TU Kebocoran pada bahan penyerap UV dan lisisnya protoplas transpor ion aktif, bergabungnya glukosa ke dalam bahan yang terendapkan oleh asam dan asam amino.
Staphylococcin A-FF22
Adsorpsi molekul bakteriosin oleh dinding sel yang sensitif menyebabkan
dinding sel lebih permeabel terhadap bakteriosin. Sedangkan adsorpsi bakteriosin
oleh dinding sel bakteri yang resisten, tidak diikuti oleh perubahan permeabilitas
dinding sel (Gambar 2).
Gambar 2 Mekanisme kerja molekul bakteriosin menembus membran sel (Bibiana 1999 dalam Suarsana 2000).
Komponen lipid membran sel terdiri atas dua lapis fosfolipid dengan gugus
polar di bagian permukaan dan gugus nonpolar di bagian dalam membran.
Komponen non polar sangat efisien dalam menahan ion-ion kecil seperti K+ atau Na+.
Bakteriosin yang terabsorpsi akan masuk ke dalam lapisan fosfolipid
membran sel membentuk agregat yang melintang dari satu sisi membran kesisi
lain. Pada pengamatan secara fisik terlihat bakteriosin membentuk struktur heliks
dalam lingkungan nonpolar dan struktur heliks tersebut bersatu membentuk
saluran (ionophore). Saluran ini dapat menjadi lintasan ke luar ion-ion esensial
Mekanisme kerja bakteriosin acidocin J1132 yang dihasilkan oleh
Lactobacillus acidophilus JCM 1132 bersifat bakteriosida yang dapat menyebabkan sel bakteri lisis. Acidocin menyebabkan bakteri menjadi sensitif karena hilangnya gaya gerak proton, menghambat transpor asam amino dan
menyebabkan ke luarnya senyawa esensial oleh pembentukan pori didalam
membran sitoplasmik (Tahara et al. 1996).
Bhunia et al. (1991) melaporkan mekanisme kerja bakteriosin pediocin AcH
dari bakteri Pediococcus acidilactici melalui uji absorbsi dengan beberapa bakteri penguji. Hasil penelitiannya menunjukkan mekanisme kerja pediocin sebagai berikut: (1) awalnya pediocin AcH berikatan dengan reseptor nonspesifik, dalam hal ini kemungkinan oleh lipoteichoid acid, (2) apabila reseptor nonspesifik telah jenuh, molekul pediocin AcH berikatan dengan reseptor spesifik dan menyebabkan perubahan integritas membran, (3) molekul pediocin AcH kemudian menyebabkan gangguan fungsional membran sehingga sel kehilangan ion K, serta
kehilangan kemampuan untuk berkembang biak, (4) pada beberapa galur,
membran selnya juga kehilangan integritas struktur dan menyebabkan lisis, (5)
pada bakteri Gram positif yang resisten tidak dijumpai adanya reseptor spesifik
sehingga bakteri tersebut tidak mampu mengabsorbsi molekul pediocin AcH, dan (6) pada bakteri gram negatif tidak dijumpai reseptor spesifik maupun nonspesifik
untuk molekul pediocin AcH.
Pemurnian Bakteriosin
Pemurnian bakteriosin telah banyak dilakukan meskipun proses
purifikasinya berbeda, namun pada prinsipnya mengikuti pola purifikasi protein
(Aymerich et al. 1996; Pridmore et al. 1996). Ekstrak bakteriosin mula-mula dipekatkan dengan fraksi presipitasi yaitu dengan asam, garam, etanol dan
berbagai pelarut campuran. Proses pengendapan protein dengan menggunakan
garam mineral umum dilakukan untuk meningkatkan konsentrasi protein dan
awal proses pemur nian. Adapun garam mineral yang paling umum digunakan
ialah amonium sulfat karena solubilitas dalam air sangat tinggi, tidak mengandung
bertindak sebagai penstabil bagi protein itu sendiri (Booth & Hames 1990, Darwis
& Sukara 1990).
Setelah protein dipisahkan, dilakukanlah fraksinasi untuk memisahkan
protein berdasarkan berat molekulnya. Salah satu cara fraksinasi ialah dengan
filtrasi gel. Pada teknik ini protein dilarutkan dalam bufer yang sesuai kemudian
dibiarkan mengalir ke bawah berdasarkan gaya gravitasi melalui kolom yang
berisikan gel dari bahan polimer, misalnya Sephadex, Sephacril dan Bio-gel.
Protein dengan ukuran molekul besar tidak dapat merembes melewati pori
sehingga akan dibasuh ke luar, mengalir turun sepanjang kolom dengan cepat.
Sedangkan protein dengan ukuran molekul yang lebih kecil akan masuk ke pori
sehingga aliran tertahan dan lambat sekali. Martirani et al. (2002) telah melakukan pemurnian bakteriosin dari B. licheniformis dengan menggunakan filtrasi gel atau pemisahan fraksi berdasarkan berat molekul dengan kolom Sephadex G-75 dan
berat molekul yang diperoleh seki tar 2 kDa.
Vibrio harveyi
Bakteri Vibrio sp. merupakan bakteri Gram negatif, bersifat motil, oksidase positif, berbentuk sel tunggal, batang pendek bengkok atau lurus, berukuran
panjang 1,4-5,0 µm dan lebar 0,3-1,3 µm, fermentatif terhadap glukosa, berpendar
dan mempunyai flagela di salah satu kutubnya, tidak membentuk asam dari
glukosa dan dapat menggunakan sukrosa sebagai sumber energinya
(Lavilla-Pitogo et al. 1990).
Vibrio ditemukan di hampir seluruh habitat, seperti air tawar, estuaria, air laut, tanah dan merupakan agen penyebab penyakit pada manusia, ikan dan
crustase (Singleton 1992). Masuknya Vibrio patogen dalam usaha budidaya udang di tambak dapat berasal dari air laut dan benar yang di gunakan. Boer et al. (1993) melaporkan bahwa induk udang yang berasal dari air laut positif membawa
bakteri berpendar sehingga dapat menularkan pada benur (larva) dan akhirnya
terbawa masuk ke tambak.
Kehadiran Vibrio sp. pada pemeliharaan udang tidak selalu menyebabkan kematian, bakteri ini bersifat oportunistik. Tingkat kepadatan tertentu serta
patogen dan menginfeksi udang (Chanratchakool et al. 1998 & Rukyani 1993) Beberapa bakteri Vibrio yang sering menyebabkan kematian pada benih udang ialah Vibrio vulvinicus, V. alginolyticus, V. fluvialis, V. anguillarus dan V. harveyi
(Boer & Zafran 1992). Jenis yang sering menimbulkan masalah serius dalam
budidaya ialah Vibrio harveyi, larva yang terinfeksi terlihat bercahaya pada kondisi gelap sehingga penyakit yang ditimbulkan penyakit ini sering disebut
penyakit kunang-kunang atau luminescent vibriosis (Lightner 1996). Luminescence terjadi karena bakteri memiliki enzim luciferase yang dapat
mengkatalis reaksi yang memancarkan cahaya dengan menggunakan subtrat
berupa senyawa aldehid yang disebut luciferin (Meighen 1991).
Menurut Liu et al. (1996, diacu dalam Zhang & Austin 2000) protease, phospolipase, haemolisin atau exotosin merupakan piranti patogenitas penting
untuk Vibrio harveyi. Bakteri penghasil cahaya ini sangat patogen dan akut sehingga dapat menyebabkan kematian larva udang sampai 100% dalam waktu
1-2 hari. Larva udang yang terserang dapat mati, tidak berbangkai dan hancur
(Rukyani 1992). Vibrio harveyi akan bersifat patogen pada larva udang apabila kepadatannya dalam air mencapai 104 cfu/ml (Zafran & Roza 1993). Tingkat patogenitas Vibrio bercahaya juga telah diketahui dimana pada tingkat kepadatan 104 sel/ml air pemeliharaan sudah dapat menyebabkan kematian massal larva udang dalam waktu 24 jam (Zafran 1992)
Escherichia coli
Escherichia coli termasuk dalam Escherichiae dan merupakan bagian dari famili Enterobacteriaceae. Bakteri ini bersifat oksidase negatif, termasuk dalam
golongan bakteri Gram negatif, berbentuk batang dengan ukuran 1.1-1.5 µm x 2-6
µm, bersifat motil karena adanya flagela (Willshaw et al. 2000). Bakteri ini mempunyai kisaran suhu pertumbuhan yang sangat luas yaitu 15-45 0C dengan suhu optimum 37 0C. Bakteri ini resisten pada pemanasan suhu 55 0C selama 60 menit atau pada suhu 60 0C selama 15 menit. Menurut Pelczar & Chan (1993) Struktur dinding sel bakteri Escherichia coli berlapis-lapis terdiri atas lipopolisakarida, peptidoglikan, dan protein. Lipopolisakarida ini mengandung
Keberadaan lapisan ini menyebabkan dinding sel tidak mudah dipisahkan dari sel
bakteri oleh enzim pengurai. Selain itu Escherichia coli bersifat Gram negatif yang tahan hidup dalam media yang kekurangan gizi.
Holt et al. (1986) ciri biokimia dari bakteri ini adalah memiliki kemampuan memfermentasi laktosa, reaksi indol positif, metil positif, uji VP
(Voges-Proskauer) negatif dan tidak dapat menggunakan sitrat sebagai sumber karbon
satu-satunya. Pada media EMB (eosin metilen blue) bakteri ini menunjukan warna
hijau metalik. Bakteri ini merupakan mikroflora normal yang terdapat pada usus
besar manusia dan hewan berdarah panas lainnya yang dalam keadaan tertentu
dapat bersifat sebagai patogen.
Kemampuan suatu bakteri patogen untuk menyebabkan infeksi dipengaruhi
oleh faktor virulensi yang dimilikinya. Faktor virulensi merupakan kemampuan
yang dimiliki oleh bakteri untuk dapat bertindak sebagai bakteri patogen (Inglis
1996). Faktor virulensi diklasifikasikan menjadi dua yaitu faktor virulensi yang
memungkinkan bakteri untuk berkolonisasi seperti fili, flagella, motilitas dan
kemotaksis, protease ekstraseluler serta faktor virulensi yang mengakibatkan
BAHAN DAN METODE
Tempat dan Waktu Penelitian
Penelitian ini di lakukan di Laboratorium Mikrobiologi Institut Pertanian
Bogor, Laboratorium Biokimia, Balai Besar Penelitian dan Pengembangan
Bioteknologi dan Sumberdaya Genetika Pertanian, Bogor. Waktu penelitian
dilakukan pada bulan Oktober 2006 sampai dengan Juli 2007.
Alat dan Bahan
Alat-alat yang digunakan pada penelitian ini adalah inkubator bergoyang
(Eberbach, USA), sentrifuse (JOUAN CR 3, Francis), vortex (NS-80, USA),
timbangan analitik (EB-280, Shimadzu, Jepang), lemari pendingin (SHARP,
Jepang), laminar air flow (MSC 12, JOUAN, Francis), autoklaf (ISO LAB, Jerman), spektrofotometer, penangas air (TZ4ST, Autonics, USA), pH meter
(HANNA, Japan), pipet mikro, kantung dialisis (Sigma, USA), kolom
kromatografi filtrasi gel.
Bahan yang digunakan dalam penelitian ini ialah isolat bakteri Bacillus sp. asal tambak udang di Karawang, Jawa Barat (Koleksi Laboratorium Mikrobiologi
Institut Pertanian Bogor). Bakteri indikator yang digunakan ialah Escherichia coli
(E. coli) dan Vibrio harveyi (V. harveyi). Media yang digunakan ialah sea water complete (SWC), bahan kimia yang digunakan untuk pengendapan protein dan fraksinasi protein.
Metode Penelitian Seleksi Isolat Bakteri Penghasil Zat Antimikrob
Tiga isolat Bacillus sp. (Lts 36, Lts 40 dan Ltw 54), bakteri target V. harveyi
dan E. coli diremajakan pada media SWC, kemudian diinkubasi selama ± 2 hari. Untuk mengetahui kemampuan isolat bakteri Bacillus sp. Lts 40, Lts 36 dan Ltw 54 yang telah dikumpulkan dalam menghasilkan zat antimikrob, dilakukan uji
SWC padat dan didiamkan beberapa saat hingga beku. Selanjutnya isolat bakteri
Bacillus sp. yang berumur dua hari diinokulasikan pada agar dengan menggunakan jarum ose dan diinkubasi pada suhu ± 28 0C selama 24 jam. Bakteri yang memiliki kemampuan dalam menghasilkan senyawa antimikrob menunjukan
adanya zona bening (zona hamb atan) di sekitar koloni dihitung Indek
penghambatannya dengan menggunakan rumus:
Indeks Penghambatan = ø zona(mm) - ø koloni (mm)
ø koloni (mm)
Uji Penghambatan dengan Cross Streak Method
Bacillus sp. umur 24 jam dalam media cair SWC digores pada media padat SWC yang menyerupai lembaran pita melalui diameter media. Setelah diinkubasi
selama 24 jam pada suhu ± 28 0C, dua bakteri target yaitu V. harveyi dan E. coli
digores tegak lurus terhadap goresan pita Bacillus sp. menggunakan jarum ose. Kemudian diinkubasi selama 24 jam pada suhu ± 28 0C. Panjang zona hambat berupa garis lurus diukur pada masing-masing tempat bakteri target ditumbuhkan
(Chythanya et al. 2002).
Uji Kompetisi Bacillus sp. terhadap V. harveyi dan E. coli
Perlakuan pada masing-masing bakteri ialah dengan inokulasi bakteri uji dan
isolat Bacillus sp. terpilih dengan rasio 1:1, 1:2, 1:4, 1:10. Lima erlemeyer yang berisi 50 ml media cair sea water complete (SWC) dimasukkan 100 µl bakteri uji dengan jumlah sel 108 CFU/ml. Pada erlenmeyer 11, 111, 1V dan V ditambahkan
Bacillus sp. terpilih dengan volume 100 µl, 200 µl, 400 µl dan 1000 µl, satu erlenmeyer digunakan sebagai kontrol negatif bakteri uji dan diinkubasi di atas
mesin pengocok. Inkubasi dilakukan selama 24 jam dan untuk menentukan
jumlah sel dilakukan dengan menggunakan metode cawan sebar pada media SWC
padat. Tentukan penentuan persentase penghambatan terhadap V. harveyi dan E. coli dengan menggunakan rumus:
Penentuan Waktu Optimum Produksi Zat Antimikrob
Sebanyak 2 ml kultur Bacillus sp. dengan kepadatan sel 108 CFU/ml diinokulasikan ke dalam media cair SWC 200 ml dan diinkubasi di atas mesin
pengocok. Pengambilan sampel dilakukan setiap 6 jam dengan mengambil 5 ml
kultur dan dimasukkan ke dalam tabung mikro. Suspensi bakteri tersebut
selanjutnya disentrifugasi dengan kecepatan 4500 g selama 15 menit. Supernatan
bebas sel dari media produksi dari setiap pengambilan sampel diuji aktivitas
antimikrobnya terhadap V. harveyi dan E. coli (sel 108 CFU/ml) dengan menggunakan disk difusion method (Lisboa et al. 2006).
Karakterisasi Zat Antimikrob Pengendapan dengan Amonium sulfat
Suspensi yang telah diinkubasi selama waktu optimum disentrifugasi dengan
kecepatan 4500 g selama 15 menit pada suhu 4 0C. Supernatan yang diperoleh dipisahkan dengan metode salting out dengan menambahkan amonium sulfat. Sebanyak 150 ml filtrat kultur diendapkan secara bertahap dengan menambahkan
amonium sulfat mulai dari konsentrasi awal 0-10 % sampai konsentrasi akhir
70-80% pada suhu 4 0C. (Tingkat kejenuhan fraksinasi dengan amonium sulfat dapat dilihat dalam Lampiran 3). Penambahan dilakukan sedikit demi sedikit sambil
diaduk dengan menggunakan pengaduk magnet dengan kecepatan lambat.
Endapan protein dipisahkan dari cairannya dengan menggunakan sentrifugasi
4500 g selama 15 menit pada suhu 4 0C. Endapan yang diperoleh dilarutkan dalam 0.1 M bufer fosfat pH 7 dengan volume ± 10 ml, kemudian masing-masing diuji
aktivitas penghambatan pada bakteri uji untuk menentukan persentase kejenuhan
amonium sulfat yang optimal dengan menggunakan disk difusion method.
Aktivitas yang paling besar dari tingkat kejenuhan ini digunakan untuk
pengendapan pada tahap selanjutnya. Hasil dari pengendapan diukur juga kadar
Pengukuran Konsentrasi Protein
Konsentrasi protein filtrat kultur Bacillus sp. diukur dengan menggunakan metode Bradford (1976). Sebanyak 400 µl filtrat kultur direaksikan dengan 4 ml
pereaksi Coomassie Briliant Blue G-250, dikocok dan didiamkan selama 15 menit. Sebagai blanko digunakan 400 µl akuades yang direaksikan dengan
pereaksi yang sama, sedangkan sebagai standar protein digunakan Bovine Serum Albumin (BSA) dengan seri konsentrasi 0.02-0.1 mg/ml dari stok BSA 2 mg/ml.
Dialisis
Untuk memisahkan garam yang tersisa dari proses pengendapan maka
dilakukan dialisis. Sebelum digunakan membran dialisis direbus dulu dengan
menggunakan Na karbonat 2% dan EDTA 0.005 % selama 10 menit. Larutan
diganti dengan aquades dan kembali direbus selama 10 menit. Perlakuan ini
diulang dua kali. Kantong disimpan dalam larutan bufer yang akan digunakan
pada suhu 4 0C.
Pada saat akan digunakan, salah satu ujung kantong diikat dengan benang
jahit lalu dimasukkan 3 ml protein hasil pengendapan amonium sulfat. Pengisian
kantong sebaiknya tidak terlalu penuh, setelah terisi ujung lain dari kantong dapat
diikat. Kantong dimasukkan ke dalam wadah yang berisi bufer fosfat 0.01 M pH 7
(volume total 100x volume sampel di dalam membran) sambil diaduk pelan
dengan menggunakan pengaduk magnet. Bufer fosfat yang di luar membran (0.01
M pH 7) diganti setiap 2 jam inkubasi dengan bufer yang baru dan volume yang
Kromatografi Filtrasi Gel
Pemurnian protein dilakukan dengan teknik kromatografi menggunakan
kolom Hi Prep 16/60 Sephacryl S-200 High Resolution (HR), dengan sistem
AKTApurifier Swedia. Matriks Sephacryl S-200 dimasukkan secara perlahan ke dalam kolom kromatografi yang berdiameter 1 cm dan tinggi 60 cm, bagian dasar
kolom diberi glasswool (Merck, Darmstadt, Jerman) sebagai penahan. Sebanyak 2 ml protein hasil dialisis diaplikasikan ke dalam kolom dan elusi dilakukan dengan
menggunakan larutan bufer fosfat 0.1 M pH 7 dengan kecepatan alir 0.5 ml/menit.
Proses elusi diamati dengan detektor pada ? 280 nm. Fraksi hasil elusi ditampung
sebanyak 3 ml dalam tabung dan diukur pada ? 280 nm. Fraksi yang diperoleh
dikelompokkan berdasarkan waktu retensinya dalam kolom. Hasil dari fraksi ini
diuji aktivitas penghambata nnya terhadap bakteri uji dengan disk difusion method. Sephacril S-200 dapat digunakan untuk menentukan berat molekul (BM) yang belum diketahui dengan cara membuat kurva yang menghubungkan volume elusi
(ml) protein standar terhadap log BM dan tentukan BM nya dari kurva standar
(Lampiran 6).
Pengaruh pH terhadap Stabilitas Aktivitas Antimikrob
Fraksi dari hasil dialisis diatur pH nya dari 3, 5, 7, 9, 11, untuk mendapatkan
pH asam ditambahkan HCl 1 M sedangkan untuk mendapatkan pH basa
ditambahkan NaOH 1 M. Kemudian diinkubasi pada suhu ruang ± 28 0C selama 2 jam kemudian uji aktivitas antimikrobnya terhadap bakteri V. harveyi dan E. coli
dengan disk difusion method (Joshi et al. 2006)
Pengaruh Panas terhadap Stabilitas Aktivitas Antimikrob
Fraksi dari hasil dialisis dipanaskan pada suhu 50 dan 100 0C selama 10 menit dan 20 menit. Setelah dipanaskan didinginkan pada suhu kamar kemudian
HASIL
Aktivitas Penghambatan Zat Antimikrob dari Bacillus sp.
Tiga isolat Bacillus sp. penghasil antimikrob dari tambak udang di uji aktivitas penghambatannya terhadap V. harveyi dan E. coli (sel 108 CFU/ml) dengan menggunakan double layer method. Besarnya aktivitas penghambatan
Bacillus sp. Lts 40, Ltw 54 dan Lts 36 terhadap V. harveyi dan E. coli ditunjukkan pada Tabel 2. Indeks penghambatan isolat Bacillus sp. yang diuji pada E. coli
antara 0,7-3,0 sedangkan pada V. harveyi antara 3,6-7,0.
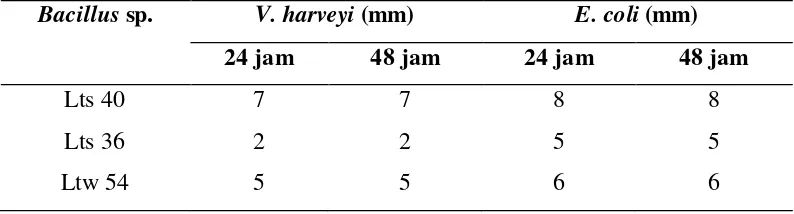
Tabel 2 Indeks penghambatan isolat Bacillus sp. penghasil antimikrob terhadap V.
harveyi dan E. coli dengan double layer method
Bacillus
Penghambatan Bacillus sp. dengan Cross Streak Method
Metode gores silang (cross streak method) bertujuan untuk melihat jarak penghambatan Bacillus sp. terhadap V. harveyi dan E. coli (Gambar 3) Jarak penghambatan Bacillus sp. terhadap V. harveyi berkisar antara 2-7 mm sedangkan pada E. coli 5-8 mm dan tidak ada peningkatan jarak penghambatan dari inkubasi 24 sampai 48 jam seperti yang tersaji pada Tabel 3.
80 85 90 95
1:1 1:2 1:4 1:10
Rasio inokulum
Persentase
penghambatan
E. coli
Gambar 3 Penampakan hasil uji penghambatan dengan cross streak method. Kemampuan Penghambatan Bacillus sp. Lts 40 terhadap V. harveyi dan E. coli pada Kultur Campur Media Cair
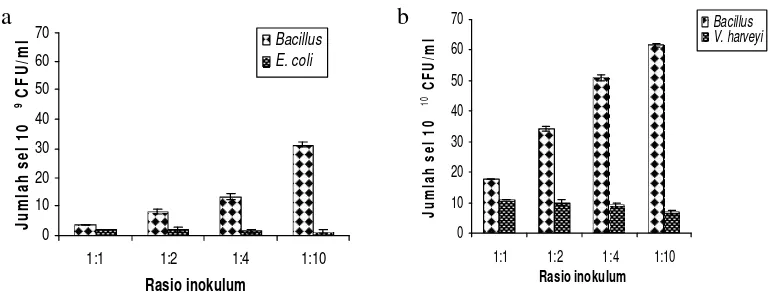
Hasil uji dari kultur campur media cair menunjukkan bahwa Bacillus sp. Lts 40 mempunyai kemampuan dalam menghambat pertumbuhan V. harveyi dan E. coli. Persentase penghambatan Bacillus sp. Lts 40 terhadap V. harveyi antara 81,8 - 88,7%, dengan jumlah sel Bacillus sp. Lts 40 antara 17,8-61,5 (1010) dan V. harveyi 10,9-6,8 (1010). Persentase penghambatan pada E. coli berkisar 85.5- 91,7% denga n jumlah sel Bacillus sp. Lts 40 ialah 3,9-31 (10 9), E. coli 21-2,1(109) (Gambar 4 & 5).
80 85 90 95
1:1 1:2 1:4 1:10
Rasio inokulum
Persentase penghambatan
V. harveyi
Gambar 4 Persentase penghambatan Bacillus sp. Lts 40 terhadap (a) V. harveyi
dan (b) E. coli.
0
Waktu Optimum Produksi Zat Antimikrob
Hasil uji aktivitas yang dilakukan pada kultur yang dipanen setiap 6 jam
menunjukkan bahwa kultur Bacillus sp. Lts 40 dalam media SWC pada umur 6 jam inkubasi yaitu pada fase pertumbuhan mulai menghasilkan antimikrob yang
mampu menghambat pertumbuhan bakteri V. harveyi dan E. coli (Gambar 6).
0 (b) aktivitas penghambatan Bacillus sp. Lts 40 terhadap V. harveyi
dan E. coli.
Karakteristik Zat Antimikrob
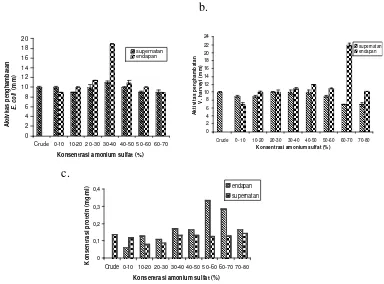
Tahap awal pemurnian zat antimikrob menggunakan metode pengendapan dengan ammonium sulfat yang dimulai dari konsentrasi 0-10% sampai 70-80 % (Gambar 7)
a. b.
c.
Gambar 7 Aktivitas penghambatan Bacillus sp. Lts 40 terhadap (a) E. coli, (b) V. harveyi setelah penambahan amonium sulfat, dan (c) Konsentrasi protein.
Setelah diperoleh hasil aktivitas penghambatan Bacillus sp. Lts 40 tertinggi dengan menggunakan amonium sulfat pada pemekatan 30-40% terhadap bakteri
indikator E. coli dan 60-70% terhadap V. harveyi (Gambar 7 & 8). Maka dilanjutkan dengan dialisis yang bertujuan untuk menghilangkan pengotor berupa
amonium sulfat dari protein yang akan dimurnikan. Hasil dialisis menunjukkan
sedikit penurunan nilai aktivitas antimikrob dan kadar protein (Tabel 4).
0
Crude 0-10 10-20 20-30 30-40 40-50 50-60 60-70
Konsentrasi amonium sulfat (%)
Crude 0-10 10-20 20-30 30-40 40-50 50-60 60-70 70-80
Konsentrasi amonium sulfat (%)
Crude 0-10 10-20 20-30 30-40 40-50 50-60 60-70 70-80
Konsentrasi amonium sulfat (%)
Konsentrasi protein (mg/ml)
Tabel 4 Aktivitas antimikrob pada proses dialisis
Konsentrasi amonium sulfat (%)
Aktivitas antimikrob (mm) Kadar protein (mg) Sebelum dialisis Setelah dialisis Sebelum
dialisis
Gambar 8 Penampakan aktivitas penghambatan pada (a) pengendapan 60-70 % terhadap V. harvey, (b) pengendapan 30-40 % terhadap E. coli
e = endapan, s = supernatan
Pemurnian Zat Antimikrob dengan Kromatografi
Pada penelitian ini tahap pemurnian dilakukan dengan cara presipitasi
dengan amonium sulfat sampai kadar akhir 60-70%, karena pengendapan 30-40%
sudah terendapkan terlebih dahulu sebelum pengendapan 60-70%. Selanjutnya di
dialisis semalam dan dilanjutkan dengan kromatografi filtrasi gel menggunakan
Sephacril S-200. Hasil dari kromatogram filtrasi gel, dari 50 fraksi yang ditamp ung, hanya 13 fraksi yang dipilih untuk mewakili puncak yang ada dan
diuji aktivitas antimikrobnya terhadap bakteri indikator E. coli dan V. harveyi. Fraksi yang menghasilkan aktivitas penghambatan paling besar terhadap V. harveyi ialah fraksi no. 21 denga n zona hambatan sebesar 30 mm, kadar protein 0,0167 mg dan berat molekul (BM) 47,38 kDa sedangkan pada E. coli terdapat pada fraksi no. 29 dengan zona hambatan sebesar 20 mm, kadar protein 0,0778
mg dan BM 34,83 kDa (Gambar 9 & 10).
e s
(a)
(b)
Gambar 9 (a) Kromatogram dari hasil filtrasi gel, dan (b) aktivitas penghambatan fraksi kromatografi filtrasi gel Bacillus sp. Lts 40 terhadap V. harveyi dan E. coli, K = hasil dari proses dialisis.
a b
Stabilitas Aktivitas Penghambatan Bacillus sp. Lts 40 terhadap pH dan Suhu
Peningkatan proses pemurnian menyebabkan kestabilan zat antimikrob
bakteriosin sering mengalami penurunan (Tagg et al. 1976). Maka perlu diteliti sifat zat antimikrob ini dari segi kestabilannya baik terhadap suhu maupun pH.
Hasil uji aktivitas penghambatan Bacillus sp. Lts 40 pada kisaran pH 3-11, mempunyai aktivitas hambatan optimum pada pH 5 dengan zona hambatan 22
mm terhadap bakteri V. harveyi sedangkan hambatan optimum pada E. coli
terdapat pada pH 7 dengan zona hambatan 24 mm. Hasil uji statistik pada kisaran
pH 3-11 dengan selang kepercayaan 95% tidak beda nyata, baik aktivitas
penghambatan terhadap V. harveyi maupun E. coli (Gambar 11).
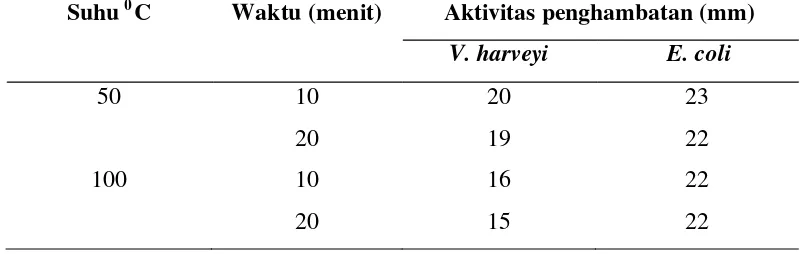
Hasil uji stabilitas aktivitas penghambatan terhadap perlakuan suhu setelah
dialisis menunjukkan Bacillus sp. Lts 40 bersifat tahan terhadap panas sampai suhu 100 0C selama 20 menit (Tabel 5), hal ini terlihat dari zona penghambatan oleh antimikrob tersebut terhadap bakteri indikator V. harveyi dan E. coli.
0 5 10 15 20 25 30
K 3 5 7 9 11
pH
Aktivitas penghambatan
(mm)
V. harveyi E. coli
Gambar 11 Aktivitas penghambatan Bacillus sp. Lts 40 terhadap
Tabel 5 Pengaruh suhu terhadap aktivitas antimikrob dari hasil dialisis
Suhu 0C Waktu (menit) Aktivitas penghambatan (mm) V. harveyi E. coli
50 10 20 23
20 19 22
100 10 16 22
20 15 22
a b
Gambar 12 Penampakan aktivitas antimikrob Bacillus sp. Lts 40 pada pH terhadap (a)V. harveyi, dan (b)E.coli
Keterangan : K = kontrol, 1 : pH 3. 2 : pH 5, 3 : pH 7, 4 : pH 9. 5 : pH 11.
5 k
1
2 3
4
1
2
3 4
5
PEMBAHASAN
Dari tiga isolat Bacillus sp. penghasil antimikrob yang diseleksi, isolat
Bacillus sp. Lts 40 memiliki aktivitas penghambatan paling besar terhadap E. coli
dan V. harveyi dengan indeks penghambatan masing-masing 3 dan 7. Berdasarkan zona hambatan yang terbentuk dapat diketahui bahwa V. harveyi memiliki sensitivitas lebih tinggi dari pada E. coli terhadap antimikrob yang dihasilkan
Bacillus sp. Lts 40. Irina et al. (2001) melaporkan Bacillus sp. memiliki kemampuan untuk menghasilkan zat antimikrob berupa bakteriosin, seperti Cerein
oleh B. cereus (Oscariz & Pisabarro 2000). Rachmaniar (1997) menyatakan bahwa faktor yang mempengaruhi besar kecilnya zona hambat zat antimikrob
antara lain adalah aktivitas zat antimikrob gugus fungsi dari substansi sendiri,
resistensi dari bakteri terhadap substansi zat antimikrob, kadar substansi aktif serta
jumlah inokulum bakteri atau kepadatan bakteri uji.
Pada cross streak method, Bacillus sp. Lts 40 juga memiliki jarak penghambatan lebih besar dibandingkan Bacillus sp. yang lain. Jarak penghambatan Bacillus sp. Lts 40 terhadap E. coli (8 mm) dan V. harveyi (7 mm), dilihat secara secara statistik jarak penghambatannya tidak berbeda nyata. Ketiga
Bacillus sp. yang diuji, aktivitas penghambatan pada masing-masing isolat berbeda nyata. Hasil uji ini menunjukkan bahwa dengan adanya perbedaan isolat
maka aktivitas penghambatannya juga akan berbeda dan pada metode ini Bacillus
sp. lebih dulu ditumbuhkan dari pada bakteri uji. Pada saat Bacillus sp. menghasilkan zat antimikrob, V. harveyi dan E. coli baru memasuki fase pertumbuhan. Beberapa faktor yang mempengaruhi aktivitas antimikrob itu ialah
1) jenis, jumlah, umur dan latar belakang kehidupan bakteri, 2) konsentrasi zat
antimikrob, 3) suhu dan waktu kontak dan 4) sifat fisiko-kimia substrat seperti
pH, kadar air dan tegangan permukaan (Frazier & Westhoff 1981). Isolat yang
mempunyai aktivitas penghambatan paling besarlah yang dipakai untuk uji
Dari uji kompetisi, persentase penghambatan dengan rasio inokulum 1:1
sudah cukup bagi Bacillus sp. Lts 40 untuk menghambat pertumbuhan V. harveyi
(81,8%) sedangkan persentase penghambatan terhadap E. coli (85,5%).
Zat antimikrob selain terdapat di dalam sel, juga merupakan komponen
permukaan sel yang dihasilkan pada kondisi tertentu dan dilepas dari sel ke dalam
lingkungan sekitarnya. Oleh karena itu sel bakteri yang telah ditumbuhkan di
dalam media cair akan melepaskan zat antimikrobnya ke dalam media. Fase cair
yang diperoleh setelah dipisahkan dari me dia sudah merupakan antimikrob
ekstraseluler. Bacillus sp. Lts 40 menghasilkan zat antimikrob selama fase pertumbuhan dan produksi optimum pada umur 3 hari dengan besar zona
penghambatan pada E. coli 12 mm dan pada V. harveyi 11 mm. Pada umumnya bakteriosin diproduksi pada fase pertumbuhan eksponensial dan disintesis di
ribosom dengan menghasilkan senyawa metabolit berupa protein atau polipeptida
(Ray & Daeschel 1992).
Pada inkubasi lebih dari 3 hari terlihat aktivitas antimikrobnya menurun.
Penyebab menurunnya aktivitas antimikrob pada inkubasi yang terlalu lama, hal
ini diduga karena pengaruh senyawa penghambat aktivitas antimikrob, enzim
pencernaan atau sifat reabsorbsi antimikrob oleh sel produsen (Dajani &
Wannamaker (1969), atau terbebasnya protease dari sel autolisis (Jo et al. 1996). Setelah mendapatkan ekstrak kasar dalam larutan yang bebas dari bentuk
sel, tahap selanjutnya adalah pemurnian. Preparasi ektrak kasar mula-mula
dipekatkan dengan fraksi presipitasi dengan amonium sulfat. Pada hasil
pengendapan amonium sulfat secara bertahap menunjukkan fraksi endapan
aktivitas penghambatan paling tinggi diperoleh pada pengendapan 30-40 %
terhadap bakteri indikator E.coli dengan zona penghambatannya meningkat dari 12 mm menjadi 19 mm sedangkan pada bakteri indikator V. harveyi diperoleh pada pengendapan 60-70 % dengan zona penghambatannya juga meningkat dari
11 mm menjadi 22 mm. Terjadinya peningkatan aktivitas penghambatan pada V. harveyi dan E. coli karena tujuan dari pengendapan ini ialah untuk meningkatkan konsentrasi protein dan untuk memperoleh zat antimikrob dalam jumlah yang