PENGARUH KONSENTRASI TAPIOKA DAN SORBITOL SEBAGAI ZAT PEMLASTIS DALAM PEMBUATAN EDIBLE COATING PADA
PENYIMPANAN BUAH MELON
LUTHFI HADI CHANDRA 050305033
DEPARTEMEN TEKNOLOGI PERTANIAN FAKULTAS PERTANIAN
PENGARUH KONSENTRASI TAPIOKA DAN SORBITOL SEBAGAI ZAT PEMLASTIS DALAM PEMBUATAN EDIBLE COATING PADA
PENYIMPANAN BUAH MELON
SKRIPSI
Oleh :
LUTHFI HADI CHANDRA 050305033
DEPARTEMEN TEKNOLOGI PERTANIAN FAKULTAS PERTANIAN
PENGARUH KONSENTRASI TAPIOKA DAN SORBITOL SEBAGAI ZAT PEMLASTIS DALAM PEMBUATAN EDIBLE COATING PADA
PENYIMPANAN BUAH MELON
SKRIPSI
Oleh :
LUTHFI HADI CHANDRA
050305033/ TEKNOLOGI HASIL PERTANIAN
Skripsi sebagai salah satu syarat untuk dapat memperoleh gelar sarjana teknologi pertanian di Fakultas Pertanian
Universitas Sumatera Utara
DEPARTEMEN TEKNOLOGI PERTANIAN FAKULTAS PERTANIAN
PENGARUH KONSENTRASI TAPIOKA DAN SORBITOL SEBAGAI ZAT PEMLASTIS DALAM PEMBUATAN EDIBLE COATING PADA
PENYIMPANAN BUAH MELON
SKRIPSI
Oleh :
LUTHFI HADI CHANDRA 050305033
Skripsi Sebagai Salah Satu Syarat untuk Dapat Memperoleh Gelar Sarjana Teknologi Pertanian di Fakultas Pertanian
Universitas Sumatera Utara Medan
Disetujui Oleh, Komisi Pembimbing :
Ir. Sentosa Ginting, MP
Ketua Anggota
Ir. Lasma Nora Limbong
DEPARTEMEN TEKNOLOGI PERTANIAN FAKULTAS PERTANIAN
Judu l Skripsi : Pengaruh konsentrasi tapioka dan sorbitol sebagai zat pemlastis dalam pembuatan edible coating pada penyimpanan buah melon
Nama : Luthfi Hadi Chandra NIM : 050305033
Departemen : Teknologi Pertanian Program Studi : Teknologi Hasil Pertanian
Disetujui Oleh, Komisi Pembimbing :
Ir. Sentosa Ginting, MP
Ketua Anggota
Ir. Lasma Nora Limbong
Mengetahui,
Ketua Departemen (Ir. Saipul Bahri Daulay, M.Si)
ABSTRAK
LUTHFI HADI CHANDRA : Pengaruh Konsentrasi Tapioka dan Sorbitol Sebagai Zat Pemlastis dalam Pembuatan Edible Coating pada Penyimpanan Buah Melon. Dibimbing oleh SENTOSA GINTING dan LASMA NORA LIMBONG.
Pelapisan buah dengan edible coating digunakan untuk memperlambat penurunan mutu, karena edible coating dapat berfungsi sebagai penahan difusi gas oksigen (O2) dan karbondioksida (CO2
Hasil penelitian menunjukkan bahwa konsentrasi tapioka memberikan pengaruh yang berbeda sangat nyata terhadap semua parameter kecuali total asam dan nilai organoleptik (rasa dan tekstur). Konsentrasi sorbitol memberikan pengaruh yang berbeda sangat nyata terhadap semua parameter. Interaksi kedua faktor memberikan pengaruh berbeda sangat nyata terhadap susut bobot dan total padatan terlarut. Konsentrasi tapioka 4 % w/v dan konsentrasi sorbitol 5 % w/v menghasilkan edible coating yang lebih baik untuk penyimpanan buah melon.
), difusi uap air serta komponen aroma. Penelitian ini dilakukan untuk menentukan konsentrasi tapioka dan konsentrasi sorbitol sebagai zat pemlastis yang terbaik dalam pembuatan edible coating pada penyimpanan buah melon.. Penelitian ini menggunakan metode rancangan acak lengkap dengan dua faktor, yaitu konsentrasi tapioka (P) : (4, 5, 6 dan 7 % w/v) dan konsentrasi sorbitol (S) : (5, 6, 7 dan 8 % w/v). Parameter yang dianalisa adalah kadar vitamin C, susut bobot, total asam, total padatan terlarut dan nilai organoleptik (rasa dan tekstur).
Kata kunci : melon, edible coating, tapioka, sorbitol.
ABSTRACT
LUTHFI HADI CHANDRA : The Influence of Tapioca Concentration and Sorbitol as Platicizer in the Making of Edible Coating for Melon Storage. Under the supervision of SENTOSA GINTING and LASMA NORA LIMBONG.
Coating a fruit with edible coating is used to delay the quality decrease because edible coating can be used as a barrier, for the diffusion of oxygen, carbondioxside and water vapor as well as vapor and flavor component. The aim of this research was to find the best tapioca concentration and sorbitol concentration as the plasticizer in the making of edible coating for melon storage. The research had been performed using factorial completely randomized design with two factors, i.e.: tapioca concentration (P) : 4, 5, 6 and 7 % w/v) and sorbitol concentration (S) : (5, 6, 7 and 8 % w/v). Parameter analyzed were vitamin C content, weight lost, total acid, total soluble solid and organoleptic values (taste and texture).
RIWAYAT HIDUP
Luthfi Hadi Chandra, lahir di Payakumbuh pada tanggal 17 September 1987. Anak ketiga dari empat bersaudara dari ayahanda H. Chandra Warman dan
ibunda Hj. Yusniar Hamid, S.Pd. Beragama Islam.
Pada tahun 2002 penulis memasuki jenjang pendidikan SMA di
SMA Negeri 2 Payakumbuh dan lulus pada tahun 2005. Penulis memasuki
Departemen Teknologi Pertanian dengan Program Studi Teknologi Hasil
Pertanian di Fakultas Pertanian Universitas Sumatera Utara melalui jalur PMP
pada tahun 2005.
Selama mengikuti perkuliahan, penulis aktif sebagai pengurus IMTHP
(Ikatan Mahasiswa Teknologi Hasil Pertanian) pada tahun 2007-2008. Penulis
pernah mengikuti Praktek Kerja Lapangan di PT. Multimas Nabati Asahan pada
KATA PENGANTAR
Puji dan syukur penulis ucapkan kehadirat Allah SWT karena atas rahmat
dan berkat-Nya penulis dapat menyelesaikan skripsi ini. Adapun judul skripsi ini
adalah ”Pengaruh Konsentrasi Tapioka Dan Sorbitol Sebagai Zat Pemlastis
Dalam Pembuatan Edible Coating Pada Penyimpanan Buah Melon”.
Terima kasih penulis ucapkan kepada Ir. Sentosa Ginting, MP, selaku
ketua komisi pembimbing dan Ir. Lasma Nora Limbong selaku anggota komisi
pembimbing atas arahan dan bimbingan yang diberikan selama penyusunan
skripsi ini.
Penulis juga menyampaikan terima kasih yang sebesar-besarnya kepada
yang tersayang Ayahanda Chandra, Ibunda Yusniar, Kakanda Artha dan Ratih
serta Adinda Wafi yang mendo’akan dengan tulus dan memberikan semangat
dalam menyelesaikan skripsi ini. Terima kasih yang terkhusus untuk
Nurizni Adinda, selanjutnya kepada rekan-rekan THP angkatan 2005
seperjuangan, asisten Laboratorium AKBP dan Mikrobiologi serta semua pihak
yang telah ikut menyukseskan pelaksanaan penelitian penulis.
Semoga skripsi ini bermanfaat bagi pihak yang membutuhkan.
Medan, September
DAFTAR ISI
HASIL DAN PEMBAHASAN Pengaruh Konsentrasi Tapioka terhadap Parameter yang Diamati .... 33
Pengaruh Konsentrasi Sorbitol terhadap Parameter yang Diamati ... 34
Kadar Vitamin C Pengaruh konsentrasi tapioka terhadap kadar vitamin C ... 35
Pengaruh konsentrasi sorbitol terhadap kadar vitamin C ... 37
Susut Bobot
Pengaruh konsentrasi tapioka terhadap susut bobot ... 39
Pengaruh konsentrasi sorbitol terhadap susut bobot ... 41
Pengaruh interaksi antara konsentrasi tapioka dan sorbitol terhadap susut bobot ... 42
Total Asam Pengaruh konsentrasi tapioka terhadap total asam ... 44
Pengaruh konsentrasi sorbitol terhadap total asam ... 44
Pengaruh interaksi antara konsentrasi tapioka dan sorbitol terhadap total asam ... 46
Total Padatan Terlarut Pengaruh konsentrasi tapioka terhadap total padatan terlarut 46
Pengaruh konsentrasi sorbitol terhadap total padatan terlarut ... 48
Pengaruh interaksi antara konsentrasi tapioka dan sorbitol terhadap total padatan terlarut ... 50
Organoleptik Rasa dan Tekstur Pengaruh konsentrasi tapioka terhadap organoleptik rasa dan tekstur ... 52
Pengaruh konsentrasi sorbitol terhadap organoleptik rasa dan tekstur ... 54
Pengaruh interaksi antara konsentrasi tapioka dan sorbitol terhadap organoleptik rasa dan tekstur ... 55
KESIMPULAN DAN SARAN Kesimpulan ... 56
Saran ... 57
DAFTAR PUSTAKA ... 58
DAFTAR TABEL
No. Hal
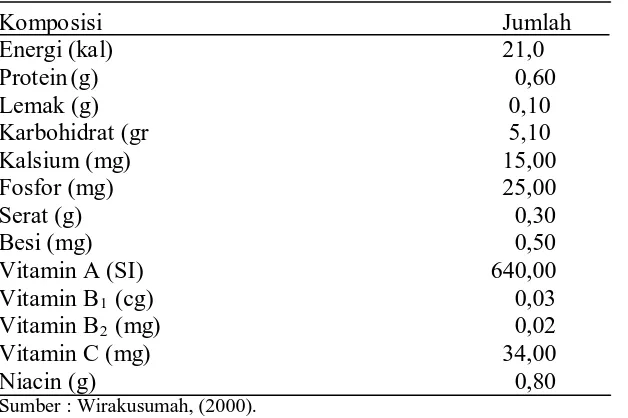
1. Komposisi kimia buah melon / 100 g bahan ... 20
2. Skala uji hedonik (Rasa) ... 29
3. Skala uji hedonik (Tekstur) ... 29
4. Pengaruh konsentrasi tapioka terhadap parameter yang diamati ... 33
5. Pengaruh konsentrasi sorbitol terhadap parameter yang diamati ... 34
6. Uji LSR efek utama pengaruh konsentrasi tapioka terhadap
9. Uji LSR efek utama pengaruh konsentrasi sorbitol terhadap susut bobot (%) ... 41
10. Uji LSR efek utama pengaruh interaksi konsentrsi tapioka dan sorbitol terhadap susut bobot (%) ... 43 dan sorbitol terhadap total padatan terlarut (0Brix) ... 50
15. Uji LSR efek utama pengaruh konsentrasi tapioka terhadap organoleptik rasa dan tekstur (Numerik) ... 52
DAFTAR GAMBAR
No. Hal
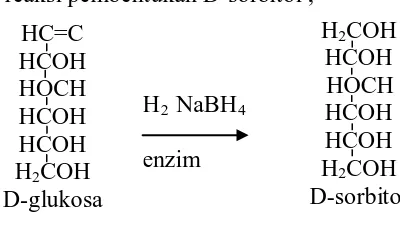
1. Reaksi pembentukan D-sorbitol ... 12
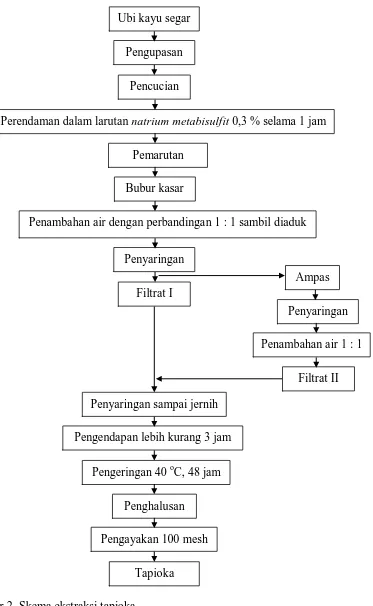
2. Skema ekstraksi tapioka ... 30
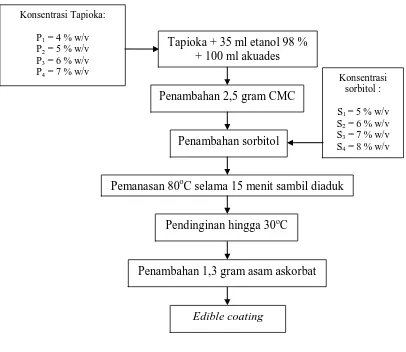
3. Skema pembuatan edible coating ... 31
4. Skema pencelupan buah melon pada edible coating ... 32
5. Grafik pengaruh konsentrasi tapioka terhadap kadar vitamin C ... 36
6. Grafik pengaruh konsentrasi sorbitol terhadap kadar vitamin C ... 38
7. Grafik pengaruh konsentrasi tapioka terhadap susut bobot ... 40
8. Grafik pengaruh konsentrasi sorbitol terhadap susut bobot ... 42
9. Grafik pengaruh interaksi antara konsentrasi tapioka dan sorbitol terhadap susut bobot ... 44
10. Grafik pengaruh konsentrasi sorbitol terhadap total asam ... 46
11. Grafik pengaruh konsentrasi tapioka terhadap total padatan terlarut ... 48
12. Grafik pengaruh konsentrasi sorbitol terhadap total padatan terlarut ... 49
13. Grafik pengaruh interaksi antara konsentrasi tapioka dan sorbitol terhadap total padatan terlarut ... 52
14. Grafik pengaruh konsentrasi tapioka terhadap organoleptik rasa dan tekstur ... 53
DAFTAR LAMPIRAN
No. Hal
1. Data pengamatan analisa kadar vitamin C (mg/ 100 g) ... 61
2. Data pengamatan analisa susut bobot (%) ... 62
3. Data pengamatan analisa total asam (%) ... 63
4. Data pengamatan analisa total padatan terlarut (0
5. Data pengamatan analisa organoleptik rasa dan tekstur ... 65 Brix) ... 64
6. Kandungan gizi buah melon sebelum perlakuan kontrol (Tanpa pencelupan) ... 66
7. Gambar buah melon yang dilapisi edible coating pada 0 hari... 67
ABSTRAK
LUTHFI HADI CHANDRA : Pengaruh Konsentrasi Tapioka dan Sorbitol Sebagai Zat Pemlastis dalam Pembuatan Edible Coating pada Penyimpanan Buah Melon. Dibimbing oleh SENTOSA GINTING dan LASMA NORA LIMBONG.
Pelapisan buah dengan edible coating digunakan untuk memperlambat penurunan mutu, karena edible coating dapat berfungsi sebagai penahan difusi gas oksigen (O2) dan karbondioksida (CO2
Hasil penelitian menunjukkan bahwa konsentrasi tapioka memberikan pengaruh yang berbeda sangat nyata terhadap semua parameter kecuali total asam dan nilai organoleptik (rasa dan tekstur). Konsentrasi sorbitol memberikan pengaruh yang berbeda sangat nyata terhadap semua parameter. Interaksi kedua faktor memberikan pengaruh berbeda sangat nyata terhadap susut bobot dan total padatan terlarut. Konsentrasi tapioka 4 % w/v dan konsentrasi sorbitol 5 % w/v menghasilkan edible coating yang lebih baik untuk penyimpanan buah melon.
), difusi uap air serta komponen aroma. Penelitian ini dilakukan untuk menentukan konsentrasi tapioka dan konsentrasi sorbitol sebagai zat pemlastis yang terbaik dalam pembuatan edible coating pada penyimpanan buah melon.. Penelitian ini menggunakan metode rancangan acak lengkap dengan dua faktor, yaitu konsentrasi tapioka (P) : (4, 5, 6 dan 7 % w/v) dan konsentrasi sorbitol (S) : (5, 6, 7 dan 8 % w/v). Parameter yang dianalisa adalah kadar vitamin C, susut bobot, total asam, total padatan terlarut dan nilai organoleptik (rasa dan tekstur).
Kata kunci : melon, edible coating, tapioka, sorbitol.
ABSTRACT
LUTHFI HADI CHANDRA : The Influence of Tapioca Concentration and Sorbitol as Platicizer in the Making of Edible Coating for Melon Storage. Under the supervision of SENTOSA GINTING and LASMA NORA LIMBONG.
Coating a fruit with edible coating is used to delay the quality decrease because edible coating can be used as a barrier, for the diffusion of oxygen, carbondioxside and water vapor as well as vapor and flavor component. The aim of this research was to find the best tapioca concentration and sorbitol concentration as the plasticizer in the making of edible coating for melon storage. The research had been performed using factorial completely randomized design with two factors, i.e.: tapioca concentration (P) : 4, 5, 6 and 7 % w/v) and sorbitol concentration (S) : (5, 6, 7 and 8 % w/v). Parameter analyzed were vitamin C content, weight lost, total acid, total soluble solid and organoleptic values (taste and texture).
PENDAHULUAN
Latar Belakang
Pelapisan buah dengan edible coating merupakan salah satu teknik yang
digunakan untuk memperlambat penurunan mutu, karena edible coating dapat
berfungsi sebagai penahan (barrier) difusi gas oksigen (O2), karbondioksida
(CO2
Komponen penyusun edible film mempengaruhi secara langsung bentuk
morfologi maupun karakteristik pengemas yang dihasilkan. Bahan-bahan
tambahan yang sering dijumpai dalam pembuatan edible film adalah antimikrobia,
antioksidan, flavour, pemlastis dan pewarna. Komponen pemlastis merupakan
bahan yang meningkatkan fleksibilitas dan ekstensibilitas film, menghindari film
dari keretakan, meningkatkan permeabilitas terhadap gas, uap air dan zat terlarut,
dan meningkatkan elastisitas film. Beberapa jenis plasticizer yang dapat
digunakan dalam pembuatan edible film adalah gliserol, lilin lebah, polivinil
alkohol dan sorbitol. Sedangkan komponen utama penyusun edible film
dikelompokkan menjadi tiga, yaitu hidrokoloid, lipida dan komposit. ) dan uap air serta komponen flavour.
Hidrokoloid yang cocok digunakan dalam edible coating diantaranya
adalah bersumber dari protein, derivat sellulosa, alginat, pektin, pati dan
polisakaridanya. Dalam hal ini tapioka mengandung pati yang baik digunakan
sebagai edible coating. Tapioka memiliki pati yang baik karena memiliki warna
yanng tidak coklat kehitaman. Pati merupakan bagian dari karbohidrat jenis
tekstur ini sulit dicerna tubuh namun memiliki serat-serat yang dapat
menstimulasi enzim-enzim pencernaan.
Kandungan serat dapat bersumber dari buah-buahan. Selain serat, di dalam
buah-buahan terkandung juga sumber nutrisi yang sangat diperlukan oleh tubuh
contohnya vitamin dan mineral. Banyak masalah kesehatan yang mungkin timbul
akibat kurang mengkonsumsi buahan. Oleh karena itu mengkonsumsi
buah-buahan adalah mutlak bagi tubuh dan kesehatan.
Dalam bentuk segar, tidak semua bagian dari buah itu yang dapat
dimakan. Sebagian besar buah-buahan mempunyai pelindung alami yang
melindungi bagian dalam buah-buahan itu sendiri, biasanya pelindung itu untuk
melindungi biji buah yang merupakan bakal tumbuhan yang baru, pelindung
biasanya disebut kulit. Pada sebagaian besar buah-buahan, kulitnya tidak dapat
dimakan dan terpaksa dibuang dan dipisahkan dari bagain yang dapat dimakan.
Misalnya kulit melon, pepaya dan durian.
Untuk dapat mengkonsumsi buah melon dalam bentuk segar, maka
terlebih dahulu dilakukan pengupasan kulit, memotong menjadi bagian-bagian
yang lebih kecil, kemudian biji yang berada di dalam buah itu dibuang. Mungkin
bagi orang yang mempunyai waktu yang cukup luang, mereka dapat melakukan
hal tersebut di atas sendirian, akan tetapi untuk sebagian masyarakat yang
mempunyai jadwal kegiatan yang padat, kegiatan yang dilakukan di atas akan
terasa menyita waktu dan dapat menikmati buah melon tersebut.
Kelemahan yang ditemui pada melon adalah singkatnya masa simpan yang
dimiliki. Kesegaran buah melon yang dapat dipertahankan apabila buah tersebut
Perubahan yang terjadi antara lain perubahan kadar air yang menyebabkan melon
akan terlihat keriput dan penampilannya menjadi kurang menarik, perubahan
kandungan gula dan juga perubahan kadar vitamin C.
Untuk mengatasi kerusakan diatas, maka dilakukan pengemasan sebagai
usaha untuk memperpanjang masa simpan buah tersebut. Sebelum menentukan
pilihan jenis dan cara pengemasan yang akan dilakukan maka perlu diketahui
persyaratan kemasan yang dibutuhkan yaitu penampilan, perlindungan, fungsi,
harga serta biaya penanganan limbah kemasan.
Oleh karena itu, penggunaan edible coating dapat dimanfaatkan sebagai
bahan pengemas dengan memperhatikan sifat fisik dan kimia. Sifat fisik dari
edible coating adalah permeabilitas terhadap uap air yang relatif kecil.
Penanganan produk buah dengan edible coating (bahan yang dapat dimakan)
merupakan salah satu alternatif yang aman bagi kesehatan konsumen serta ramah
lingkungan. Selain mampu menurunkan kecepatan respirasi, edible coating juga
dapat ditambah senyawa antioksidan yang dapat mencegah pencoklatan enzimatis
buah. Dalam rangka meningkatkan pemanfaatan edible coating dalam
penyimpanan buah melon, penulis tertarik untuk melakukan penelitian tentang
“Pengaruh Konsentrasi Tapioka dan Sorbitol sebagai Zat Pemlastis dalam Pembuatan Edible Coating pada Penyimpanan Buah Melon”.
Tujuan Penelitian
Untuk mengetahui pengaruh konsentrasi tapioka dan sorbitol sebagai zat
Kegunaan Penelitian
Sebagai sumber informasi tentang pengaruh edible coating pada
penyimpanan buah melon dan sebagai sumber data dalam penyusunan skripsi
sebagai salah satu syarat untuk memperoleh gelar sarjana Teknologi Pertanian di
Fakultas Pertanian Universitas Sumatera Utara.
Hipotesis Penelitian
Ada pengaruh konsentrasi tapioka dan sorbitol yang paling tepat untuk
menghasilkan edible coating yang tepat pada penyimpanan buah serta ada
TINJAUAN PUSTAKA
Edible Film
Edible film merupakan nama ilmiah bagi kemasan yang bisa dimakan. Saat
ini gencar dikembangkan bersamaan dengan kemasan yang gampang tururai atau
yang diberi nama biodegradable film. Edible film sudah sudah pasti tergolong
biodegradable film, namun tidak sebaliknya. Batasan makna kemasan bisa
dimakan bergantung pada proses peracikan, proses pengemasan dan segala
modifikasi perlakuan yang terkait. Jika bahan baku dan bahan racikannya adalah
bahan yang bisa dimakan dan hanya perubahan struktur bahan baku yang terjadi
selama proses pemasakan, perubahan pH atau modifikasi enzimatis, maka
kemasan tersebut digolongkan kemasan bisa dimakan (Bardant dan Dewi, 2007).
Pelapis edibel adalah lapisan tipis dan kontinu yang dibuat dari bahan
yang dapat dimakan, dibentuk di atas komponen makanan yang berfungsi sebagai
penghambat terhadap transfer massa (misalnya kelembapan, oksigen, lipid dan zat
terlarut), sebagai carrier bahan makanan (aditif) dan untuk meningkatkan
penanganan makanan (Krocha, 1994).
Beberapa makanan kadang-kadang dibungkus atau dilapisi dengan suatu
lapisan film yang dapat dimakan yang disebut edible film, misalnya permen dan
sosis. Lapisan film ini dapat melindungi makanan terhadap penguapan atau reaksi
dengan makanan lainnya. Beberapa bahan pelapis tersebut, misalnya gelatin dan
gum arab dapat dilapiskan pada makanan (Winarno, et al, 1980).
Prinsip pembentukan edible film adalah interaksi rantai polimer
secara spesifik dilakukan untuk mencari pengganti plastik pembungkus bumbu
kering, yang akan menjadi sampah. Dengan plastik biodegradable, bungkus ini
dapat langsung dimasak dan tidak menjadi sampah (Pikiran Rakyat, 2009).
Kondisi penyimpanan buah-buahan segar telah dikenal dengan teknologi
baru, misalnya penyimpanan buah apel di dalam kemasan film edibel yang
fleksibel. Dengan teknik ini buah-buahan dapat disimpan dalam kondisi yang
lebih baik untuk jangka waktu yang lebih lama. Kemasan film yang digunakan
mempunyai kecepatan transimisi uap air yang rendah, pertukaran oksigen yang
baik dan pertukaran karbondioksida yang rendah terhadap udara di dalam ruang
penyimpanan. Kecepatan respirasi yang terjadi di dalam kemasan film menjadi
berkurang yang menyebabkan kehilangan air menjadi sedikit (Desrosier, 1988).
Film-film tertentu
Komponen pelapis edibel dapat dibagi menjadi tiga golongan, yaitu
hidrokoloid, lipid dan komponen campurannya. Hidrokoloid yang cocok
diantaranya adalah protein, derivat sellulosa, alginat, pektin, pati dan
polisakaridanya. Lipid yang cocok adalah lilin, asilgliserol dan asam lemak.
Pelapis campuran dapat berbentuk bilayer, dimana lapisan yang satu hidrokoloid
bercampur dalam lapisan hidrofobik (Paramawati, 2001).
pada suhu rendah akan memiliki sifat permeabilitas
yang baik untuk hasil-hasil pertanian. Berdasarkan pengalaman diketahui bahwa
pada musim lain dengan buah yang berbeda, edible film mungkin tidak dapat
mempertahankan atmosfer yang menguntungkan. Penggunaan kemasan film yang
ditutup rapat pada suhu rendah akan memperlihatkan adanya variasi kegiatan
Pelapisan atau coating tidak hanya melapisi metal dari korosi, tetapi juga
mencegah kontak antara makanan dengan logam yang dapat menghasilkan warna
atau cita rasa yang tidak diinginkan. Sebagai contoh misalnya warna hitam yang
dihasilkan dari reaksi antara besi atau timah dengan sulfida pada makanan yang
berasam rendah atau pemucatan pigmen merah pada sayuran atau buah-buahan
misalnya bit atau anggur karena reaksi dengan baja, timah dan aluminium. Bahan
yang digunakan sebagai pelapis adalah oleoresin, zat penolik, polibutadiena, epon,
vinil dan malam (honey wax). Yang paling banyak digunakan adalah oleoresin
dan hampir semua pelapis dibuat dari pelapis buatan (sintetik)
(Winarno, et al, 1980).
Kelebihan edible film yang dibuat dari hidrokolid diantaranya memiliki
kemampuan yang baik untuk melindungi produk terhadap oksigen,
karbondiokasida dan lipid serta memiliki sifat mekanis yang diinginkan dan dapat
meningkatkan kesatuan struktural produk (Syamsir, 2008).
Pelapis yang dibuat dari hidrokoloid mempunyai beberapa kekurangannya
yaitu bungkus dari karbohidrat kurang bagus digunakan untuk mengatur migrasi
uap air dan bungkus protein biasanya sangat dipengaruhi oleh perubahan pH.
Pelapis edibel dari lipid mempunyai kelebihan yaitu baik digunakan untuk
melindungi produk konfeksioneri. Sedangkan kekurangannya yaitu kegunaannya
dalam bentuk murni sebagai pelapis terbatas, karena cukup banyak kekurangan
integritas dan ketahanannya (Paramawati, 2001).
Berbagai film yang mempunyai sifat larut air sangat cocok untuk jenis
makanan yang praktis atau dikenal dengan convenience foods. Sebagai contoh
serta kolagen. Amilosa film yan dibuat dari pati jagung yang banyak dimakan
banyak digunakan sebgai pembungkus permen. Kemasan yang dapat dimakan ini
dikenal dengan nama ediplex (Syarief dan Irawati, 1988).
Edible film diaplikasikan pada makanan dengan cara pembungkusan,
pencelupan, penyikatan dan penyemprotan. Bahan hidrokoloid dan lemak maupun
campuran keduanya dapat digunakan untuk membuat edible film. Hidrokoloid
yang dapat digunakan untuk membuat edible film adalah protein (gelatin, kasein,
protein kedelai, protein jagung dan glutein gandum) serta karbohidrat (pati,
alginat, pektin,, gum arab dan modifikasi lainnya), sedangkan lipid yang
digunakan adalah lilin, gliserol dan asam lemak (Syamsir, 2008).
Aplikasi dari pelapis edibel dapat dilakukan dengan pencelupan dan
penyemprotan untuk melapisi buah-buahan dan sayuran. Penelitian tentang
penggunaan pelapis edibel ini sudah dilakukan pada buah apel dan buah pir. Hasil
penelitian tersebut adalah diperoleh bahwa pelapis dari bahan carboxymethyl
cellulose ini dapat memperlambat perubahan warna dan menahan asam pada buah
(Krocha, et al, 1992).
Aplikasi dari edible film atau edible coating dapat dikelompokkan atas :
1. Sebagai kemasan primer dari produk pangan.
Contoh dari penggunaan edible film sebagai kemasan primer adalah pada
permen, sayur-sayuran dan buah-buahan segar, sosis, daging dan produk hasil
laut.
2. Sebagai barrier.
Penggunaan edible film sebagai barrier dapat dilihat dari contoh-contoh
Gellan gum yang direaksikan dengan garam mono atau bivalen yang
membentuk film, diperdagangkan dengan nama dagang Kelcoge merupakan
barrier yang baik untuk absorbsi minyak pada bahan pangan yang digoreng,
sehingga menghasilkan bahan dengan kandungan minyak yang rendah. Di Jepang
bahan ini digunakan untuk menggoreng tempura.
Edible coating yang terbuat dari zein (protein jagung) dengan nama
dagang Z`coat TM (Cozean) dari Zumbro Inc., Hayfielf, MN terdiri dari zein,
minyak sayuran, BHA, BHT dan eti lakohol, digunakan untuk produk-produk
konfiksionari seperti permen dan cokelat.
Fry Shield yang dipatenkan oleh Kerry Ingradient, Beloit, WI dan
Hercules, Wilmington, DE, terdiri dari pektin, remah-remahan roti dan kalsium,
digunakan untuk mengurangi lemak pada saat penggorengan, seperti pada
penggorengan french fries.
Film Zein dapat bersifat sebagai barrier untuk uap air dan gas pada
kacang-kacangan atau buah-buahan, diaplikasikan pada kismis untuk sereal dan
sarapan siap santap (ready to eat-breakfast cereal).
3. Sebagai pengikat (Binding).
Edible film juga dapat diaplikasikan pada snack atau crackers yang diberi
bumbu yaitu sebagai pengikat atau adesif dari bumbu yang diberikan agar dapat
lebih merekat pada produk. Pelapisan ini bergunak untuk mengurangi lemak pada
bahan yang dengan penambahan bumbu.
4. Sebagai Pelapis (Glaze).
Edible film dapat bersifat pelapis untuk meningkatkan penampilan dari
Keuntungan dari palapisan ini adalah dapat menghindari masuknya mikroba yang
dapat terjadi jika dilapisi dengan telur
(Julianti dan Nurminah, 2007).
Zat Pemlastis
Komponen penyusun edible film mempengaruhi secara langsung bentuk
morfologi maupun karakteristik pengemas yang dihasilkan. Komponen utama
penyusun edible film dikelompokkan menjadi tiga, yaitu hidrokoloid, lipida dan
komposit. Bahan-bahan tambahan yang sering dijumpai dalam pembuatan edible
film adalah antimikrobia, antioksidan, flavour dan pewarna. Komponen yang
meningkatkan fleksibilitas dan ekstensibilitas film, menghindari film dari
keretakan, meningkatkan permeabilitas terhadap gas, uap air dan zat terlarut, dan
meningkatkan elastisitas film. Beberapa jenis plasticizer yang dapat digunakan
dalam pembuatan edible film adalah gliserol, lilin lebah, polivinil alkohol dan
sorbitol (Julianti dan Nurminah, 2007).
Plasticizer didefinisikan sebagai bahan non volatil, bertitik didih tinggi
jika ditambahkan pada material lain sehingga dapat merubah sifat material
tersebut. Penambahan plasticizer dapat menurunkan kekuatan intermolekuler dan
meningkatkan fleksibilitas film dan menurunkan sifat barrier film. Gliserol dan
sorbitol merupakan plasticizer yang efektif karena memiliki kemampuan untuk
mengurangi ikatan hidrogen internal pada ikatan intermolekuler, plasticizer
ditambahkan pada pembuatan edible film untuk mengurangi kerapuhan,
meningkatkan fleksibilitas dan ketahanan film terutama jika disimpan pada suhu
Plasticizer adalah bahan organik dengan berat molekul rendah yang
ditambahkan dengan maksud untuk memperlemah kekakuan dari polimer,
sekaligus meningkatkan flesibilitas dan sekstensibilitas polimer. Plasticizer larut
dalam tiap-tiap rantai polimer sehingga akan mempermudah gerakan molekul
polimer dan bekerja menurunkan suhu transisi gelas (Tg), suhu kristalisasi atau
suhu pelelehan dari polimer. Pada daerah diatas Tg, bahan polimer menunjukkan
sifat fisik dalam keadaan lunak (soft) seperti karet, sebaliknya dibawah Tg
polimer dalam keadaan sangat stabil seperti gelas (Paramawati, 2001).
Rumus umum dari monosakarida sebagai CnH2nOn atau (CH2O)n
Menurut Sulaiman, (1995), aldosa juga dapat direduksi, misalnya dengan
memakai H
jika
dimulai dari n=3 maka terbentuklah deret, deret dengan gugus fungsi aldehid
disebut golongan aldosa dan deret dengan gugus fungsi keton disebut golongan
ketosa. Dari semua aldosa yang ada, yang perlu untuk diketahui adalah
gliseraldehid, eritrosa, treosa, ribosa, arabinosa, xilosa, liksosa, glukosa, manosa,
galaktosa, ribulosa, xilulosa dan fruktosa (Sulaiman, 1995).
2 atau NaBH4
Berikut reaksi pembentukan D-sorbitol ;
(Natrium borohidrida) atau dengan memakai enzim.
Dalam reaksi ini akan dihasilkan alkohol polihidroksida yang disebut dengan
alkohol gula (Sugar alkohol), misalnya D-sorbitol atau D-glusitol dari gluko sa,
manitol dari manosa dan sebagainya.
H2 NaBH4
enzim
Tapioka
Pati merupakan simpanan karbohidrat dalam tumbuh-tumbuhan dan
merupakan karbohidrat utama yang dimakan manusia di seluruh dunia. Komposisi
amilopektin dan amilosa berbeda dalam pati berbagai bahan makanan.
Amilopektin pada umumnya terdapat dalam jumlah lebih besar. Sebagian besar
pati mengandung antara 15% dan 35% amilosa. Dalam butiran pati, rantai-rantai
amilosa dan amilopektin tersusun dalam bentuk semi kristal, yang
menyebabkannya tidak larut dalam air dan memperlambat pencernaannya oleh
amilase di pankreas (Almatsier, 2004).
Pati adalah cadangan makanan utama pada tanaman. Senyawa ini
sebenarnya campuran dua polisakarida, yaitu amilosa yang terdiri dari 70 hingga
350 unit glukosa yang berikatan membentuk garis lurus dan amilopektin yang
terdiri hingga 100.000 unit glukosa yang berikatan membentuk struktur rantai
bercabang. Kira-kira 20% dari pati adalah amilosa. Pati berwarna putih, berbentuk
serbuk bukan kristal yang tidak larut dalam air dingin. Tidak seperti monosakarida
dan disakarida, pati dan polisakarida lain tidak mempunyai rasa manis. Hidrolisis
pati dapat dilakukan oleh asam atau enzim (Gaman dan Sherrington, 1992).
Pati merupakan bentuk karbohidrat yang ditimbun di dalam tanaman dan
sebagai sumber energi pada makanan. Pati terdiri dari rantai molekul-molekul
glukosa yang panjang dengan 2 jenis, yaitu amilosa dari rantai molekul glukosa
yang panjang dan lurus serta amilopektin yang terdiri dari rantai molekul glukosa
yang lebih pendek dan bercabang. Apabila pati dipanasi dengan panas basah atau
direbus, butir-butir pati tersebut akan menyerap air dan mengembang dan diniding
pencerna. Amilopektin mempunyai sifat koloidal sehingga jika dipanaskan,
campuran air dengan pati akan menjadi kental (thickening). (Purba, et al, 1984).
Pati dapat digolongkan berdasarkan sifat-sifat pasta yang dimasak. Pati
serealia (jagung, gandum, beras dan sorghum) membentuk pasta kental yang
mengandung bagian-bagian pendek dan pada pendinginan membentuk gel yang
buram. Pati akar dan umbi (kentang, ketela dan tapioka) membentuk pasta sangat
kental dan mengandung bagian-bagian panjang. Pasta ini biasanya jernih dan pada
pendinginan hanya membentuk gel lunak. (deMan, 1997).
Pati merupakan homopolimer glukosa dengan ikatan α-glikosidik.
Berbagai macam pati tidak sama sifatnya, tergantung dari panjang rantai C, serta
apakah lurus atau bercabang rantai molekulnya. Pati terdiri dari dua fraksi yang
dapat dipisahkan dengan air panas. Fraksi terlarut disebut amilosa dan fraksi yang
tidak terlarut dinamakan amilopektin. Amilosa memiliki struktur lurus dengan
ikatan α-(1,4)-D-glukosa sedangkan amilopektin mempunyai cabang dengan
ikatan α-(1,6)-D-glukosa sebanyak 4-5 dari berat total (Winarno, 1997).
Apabila pati mentah dimasukkan ke dalam air dingin, granula patinya akan
menyerap air dan membengkak. Namun demikian jumlah air yang terserap dan
pembengkakannya terbatas. Air yang terserap tersebut hanya dapat mencapai
30%. Peningkatan volume granula pati yang terjadi di dalam air pada suhu antara
550C sampai 650C merupakan pembengkakan yang sesungguhnya, dan setelah
pembengkakan ini granula pati dapat kembali pada kondisi semula. Granula pati
dapat dibuat membengkak luar biasa, tetapi bersifat tidak dapat kembali lagi pada
kondisi semula. Perubahan tersebut dinamakan gelatinisasi. Suhu gelatinisasi
lambat tercapai, sampai suhu tertentu kekentalan tidak bertambah, bahkan
kadang-kadang turun (Winarno, 1997).
Pada fraksinasi diketahui kandungan amilosa pati hanya sedikit,
perbadingan amilosa : amilopektin sekitar 1 : 3. beberapa varietas genetik dari
jagung, barley dan beras tidak mempunyai amilosa tetapi hanya amilopektin.
Namun lebih banyak jenis kacang polong, jagung dan barley yang mempunyai
karakteristik genotip dengan kandungan amilosa yang tinggi (60-80%)
(Whistler, et al, 1984).
Beberapa sifat pati adalah mempunyai rasa yang tidak manis, tidak larut
dalam air dingin tetapi di dalam air panas dapat membentuk gel atau sol yang
bersifat kental. Sifat kekentalannya ini dapat digunakan untuk mengatur tekstur
makanan dan sifat gelnya dapat diubah oleh gula atau asam. Penguraian tidak
sempurna dari pati dapat menghasilkan dekstrin yaitu suatu bentuk oligosakarida
(Winarno, et al, 1980).
Meskipun suatu gel adalah sistem dispersi koloid zat cair dalam zat padat
namun tidak berarti zat cair sebagai fase dispersinya harus lebih sedikit daripada
zat padat sebagai medium dispersi. Pada kenyataannya malah dijumpai bahwa
persentase zat padat pada hampir semua gel adalah jauh lebih kecil dari pada
persentase zat cairnya. Semua gel mempunyai konsistensi padat atau hampir padat
dengan harga plastisitas yang tinggi. Dan gel pati merupakan golongan gel elastis,
reversibel yang dapat kembali membentuk sol (Sulaiman, 1995).
Tapioka yang dibuat dari ubi kayu mempunyai banyak kegunaan, antara
lain sebagai bahan pembantu dalam berbagai industri. Dibandingkan dengan
baik sehingga mengurangi kerusakan tenun, juga digunakan sebagai bahan bantu
pewarna putih. Tapioka juga banyak digunakan sebagai bahan pengental, bahan
pengisi dan bahan pengikat dalam industri makanan seperti dalam pembuatan
puding, makanan bayi, es krim, pengolahan sosis daging dan industri farmasi
(Teknopangan dan Agroindustri, 2008).
Tapioka banyak digunakan dalam berbagai industri karena kandungan
patinya yang tinggi dan sifat patinya yang mudah membengkak dalam air panas
dengan membentuk kekentalan yang dikehendaki. Selain itu pemakaian tapioka
disukai karena memiliki larutan yang jernih, daya gel yang baik, rasa yang netral,
warna yang terang dan daya lekatnya yang sangat baik (Somaatmadja, 1984).
Bahan yang Ditambahkan
Bahan baku yang ditambahkan dalam pembuatan edible film antara lain
antimikroba, antioksidan, flavour, pewarna dan plasticizer. Bahan antimikroba
yang umumnya sering digunakan adalah asam benzoat, asam askorbat, kalium
sorbat dan asam propionat. Antioksidan diperlukan untuk melindungi dari reaksi
oksidasi, degradasi dan pemudaran. Antioksidan yang sering digunakan berupa
senyawa asam dan senyawa fenolik. Senyawa asam yang digunakan antara lain
asam sitrat dan asam sorbat. Sedangkan senyawa fenolik yang dipakai adalah
BHA, BHT, propil galat, dan tokoferol. Plasticizer yang dipakai adalah sorbitol
(Mumtaaz, 2006).
Antioksidan adalah bahan yang digunakan untuk mencegah oksidasi
lemak, misalnya digunakan pada bahan pangan yang akan digoreng, makanan dari
biji-bijian dan makanan-makanan lain yang banyak mengandung lemak dan
(BHA), butylated hidroxy-toluena (BHT), propil galat dan nondihydrogualaretic
(NDGA). Sulfur dioksida selain berfungsi sebagai pengawet juga digunakan
sebagai antioksidan (Winarno, et al, 1980).
Asam askorbat adalah antioksidan yang sekarang telah dapat dihasilkan
secara sintetik. Asam askorbat atau vitamin C ini bisa ditambahkan kedalam
daging sebagai antioksidan, tetapi tidak akan menambah nilai vitaminnya karena
asam askorbat akan rusak oleh pemanasan (Winarno, et al, 1980).
Vitamin C memegang peranan penting dalam metabolisme lemak, protein,
asam amino, besi dan tembaga serta dalam fungsi sel darah merah. Dalam bentuk
kimia aslinya, jika kering vitamin C adalah betul-betul stabil, akan tetapi jika
dalam bentuk larutan seperti halnya dengan vitamin C dalam bahan pangan, bahan
tersebut adalah yang paling tidak stabil. Vitamin C mudah rusak jika dibiarkan
terkena udara, panas, tembaga atau alkali (Suhardjo, et al, 1982).
Asam askorbat berwarna putih, membentuk kristal putih dan sangat larut
dalam air. Dalam semua vitamin, asam askorbat adalah yang paling mudah rusak.
Asam askorbat sangat larut dalam air dan oleh karena itu terlarutkan ke dalam air
masakan. Asam askorbat juga mudah teroksidasi. Oksidasinya sangat cepat
apabila kondisinya alkalis, pada suhu tinggi dan terkena sinar serta logam-
logam berkadar sangat rendah seperti seng, besi dan terutama tembaga
(Gaman dan Sherrington, 1992).
Bahan-bahan yang termasuk kedalam bahan pengental diantaranya adalah
gum, pati, dekstrin, turunan-turunan dari protein dan bahan-bahan lainnya yang
dapat menstabilkan, memekatkan atau mengentalkan makanan yang dicampur
misalnya saus selada, susu cokelat, jeli, puding dan lain-lainnya adalah makanan
yang mengandung bahan pengental misalnya gum arab, CMC (carboxymethyl
cellulose), karagenan, pektin, amilosa dan gelatin (Winarno, et al, 1980)
Karboksimetil selulosa (CMC) merupakan eter polimer linier dan berupa
senyawa anion yang bersifat biodegredable, tidak berbau, tidak berwarna, tidak
beracun, butiran atau bubuk yang larut dalam air, memiliki rentang pH sebesar
6,5-8,0 dan stabil pada rentang pH 2-10. Karboksimetil selulosa berasal dari
selulosa kayu dan kapas yang diperoleh dari reaksi antara selulosa dengan asam
monokloroasetat dengan katalis berupa senyawa alkali. Karboksimetil selulosa
juga merupakan senyawa serbaguna yang memiliki sifat penting seperti kalarutan,
reologi dan adsorpsi dipermukaan (Deviwings, 2008).
Turunan selulosa yang dikenal dengan carboxylmetyl cellulose (CMC)
sering dipakai dalam industri makanan untuk mendapatkan tekstur yang baik.
Misalnya pada pembuatan es krim. Pemakaian CMC akan memperbaiki tekstur
dan kristal laktosa yang terbentuk akan lebih halus. CMC juga sering dipakai
dalam bahan makanan untuk mencegah terjadinya retrogradasi. CMC memiliki
gugus karboksil, maka viskositasnya dipengaruhi oleh pH larutan, pH optimum
adalah 5 dan apabila pH terlalu rendah (<3) maka CMC akan mengendap
(Winarno, 1997).
Etanol adalah turunan dari etana dan tersusun dari induk hidrokarbon yang
mengandung dua atom karbon (C2H5-) dan satu gugus hidroksil (-OH). Rumus
dari etanol adalah C2H5OH. Etanol yang juga disebut etil alkohol adalah alkohol
yang terdapat dalam bir, anggur dan spiritus. Senyawa dihasilkan dengan proses
etanol dan karbondioksida. Metanol dan etanol adalah alkohol monohidrat yaitu
tiap molekul memiliki sebuah gugus hidroksil (Gaman dan Sherrington, 1992).
Tingkat polaritas aseton lebih tinggi dari etanol. Perbedaan tingkat
polaritas ini menyebabkan film zein dengan pelarut aseton lebih cepat terbentuk
daripada denga pelarut etanol. Namun hasil film dengan pelarut aseton
menunjukkan kemampuannya sebagai sekat lintas terhadap uap air lebih jelek
dibandingkan film zein dengan pelarut etanol (Paramawati, 2001).
Melon
Tanaman melon (Cucumis melo L.) termasuk famili Cucurbitaceae.
Tanaman melon berasal dari Turki dan India. Melon termasuk tanaman semusim
yang bersifat merambat. Melon memiliki akar tunggang dan akar cabang yang
menyebar pada kedalaman lapisan tanah antara 30 hingga 50 cm. Batang tanaman
biasanya mencapai ketinggian (panjang) antara 1,5 sampai 3 meter, berbentuk segi
lima, lunak, berbuku-buku sebagai tempat melekatnya tangkai daun. Helai daun
berbentuk bundar bersudut lima dan berlekuk, diameternya antara 9 sampai 15 cm
dan letak antara satu daun dengan daunnya saling berselang (Tjahjadi, 1995).
Buah melon sangat bervariasi, baik bentuk, warna kulit, warna daging
buah maupun bobotnya. Bentuk buah melon antara bulat, bulat oval sampai
lonjong atau selindris. Warna kulit buah antara, putih krem, hijau krem, hijau
kekuning-kuningan, hijau muda, kuning, kuning muda, hingga kombinasi dari
warna lainnya. Bahkan ada yang bergaris-garis, totol-totol, dan juga struktur kulit
Berdasarkan Prajnanta, (2003) secara lengkap dilihat dari segi taksonomi
tumbuhan, tanaman melon diklasifikasikan sebagai berikut :
Kingdom : Platae
Divisio : Spematophyta
Sub-divisio : Angiospremae
Kelas : Dikotil
Sub-kelas : Sympetalae
Ordo : Cucurbitales
Famili : Cucurbitaceae
Genus : Cucumis
Spesies : Cucumis melo L.
Adapun kandungan gizi buah melon/ 100 g bahan yang dapat dimakan
dapat dilihat pada Tabel 1 dibawah ini :
Tabel 1. Komposisi kimia buah melon/ 100 g bahan
Komposisi Jumlah
Energi (kal) 21,0
Sumber : Wirakusumah, (2000).
Total gula pada buah-buahan selalu meningkat karena terjadinya degradasi
dari karbohidrat dan menurun pada hari tertentu karena gula digunakan untuk
proses respirasi akan diubah menjadi senyawa lainnya. Total gula tersebut
selanjutnya digunakan untuk melakukan aktivitas seluruh sisa hidup dari buah
Pola penimbunan gula pada sebangsa semangka sangat penting untuk
menegakkan peraturan pemasaran. Gula total pada PMR 45 dan honneydew boleh
dikatakan tetap (4 sampai 6%) sampai 4 minggu setelah mekarnya bunga
kemudian meningkat cepat sampai 1% setelah 1 minggu. Bertambahnya jumlah
gula dengan cepat terutama disebabkan adanya peningkatan sintesis sukrosa.
Jumlah glukosa dan frukstosa berkurang dengan bertambahnya sukrosa
(Pantastico, 1997).
Menurut Samadi, (1995) vitamin dan mineral yang terkandung dalam buah
melon sangat baik untuk kesehatan tubuh manusia. Kandungan protein dan
karbohidrat yang terkandung dalam buah melon sangat penting bagi tubuh
manusia untuk pembentukan jaringan sel.
Sumber vitamin C sebagian besar berasal dari sayuran dan buah-buahan.
Buah yang masih mentah lebih banyak kandungan vitamin C-nya, makin tua buah
makin berkurang kandungannya (Winarno, 1997).
Kandungan vitamin C pada melon akan mencegah terjadinya sariawan dan
meningkatkan ketahanan tubuh terhadap penyakit. Buah melon mengandung
banyak zat gizi yang cukup beragam sehingga tidak mengherankan apabila melon
merupakan sumber gizi yang sangat baik (Prajnanta, 2003).
Buah melon bersifat cepat matang dan mudah masak, sehingga teknik
penyimpanan yang baik adalah diruang dingin, baik berupa cold storage maupun
lemari pendingin. Suhu pada ruang dingin biasanya mendekati ± 00
Salah satu faktor penyebab kerusakan bahan pangan adalah suhu, hal ini
dikarenakan suhu dapat mempengaruhi kelayuan dan laju kehilangan air, laju C, sehingga
respirasi dan kecepatan reaksi biokimia serta laju pertumbuhan mikroba
(Budaraga, 1998).
Penyimpanan pada suhu rendah atau penyimpanan dingin (chilling
storage) pada umumnya menggunakan suhu dibawah 15 0
Menurut Pantastico, (1997) agar keawetan dari buah yang disimpan pada
suhu dingin maksimum, maka perlu diusahakan agar respirasi aerobik
berlangsung pada laju yang rendah, sehingga proses yang berhubungan dengan
pemeliharaan kehidupan sel dapat tetap utuh. Demikian juga suhu rendah yang
cocok diusahakan tetap terjaga, sehingga reaksi-reaksi penyebab kerusakan dapat
dihambat.
C dan diatas titik beku.
Pada suhu tersebut penurunan mutu buah-buahan akan dapat dihambat, karena
terhambatnya laju respirasi, laju kehilangan air bahan dan reaksi biokimia serta
BAHAN DAN METODE
Bahan Penelitian
Bahan yang digunakan dalam penelitian ini adalah buah melon yang
diperoleh dari Deli Tua dan ubi kayu yang diperoleh dari Pasar Sore, Padang
Bulan, Medan. Bahan-bahan lain yang digunakan adalah sorbitol, CMC
(carboxylmetyl cellulose), asam askorbat, etanol 98 % dan akuades.
Waktu dan Tempat Penelitian
Penelitian dilaksanakan pada bulan Mei 2009 di Laboratorium
Mikrobiologi Departemen Teknologi Pertanian Fakultas Pertanian Universitas
Sumatera Utara, Medan.
Bahan Kimia
Adapun bahan kimia yang digunakan dalam penelitian ini adalah
NaOH 0,1 N, Pati 1 %, Indikator phenolpthalein 1 %, Iodine 0,01 % dan Natrium
metabisulfit 0,3 %
Alat Penelitian
Adapun alat penelitian yang digunakan dalam penelitian ini adalah Beaker
glass, Oven, Loyang, Erlemeyer , Styrofoam, Penjepit, Gelas ukur, Sendok,
Piring, Kertas saring, Ayakan 100 mesh, Corong, Pipet Tetes, Handrefraktometer,
Pipet skala, Desikator, Oven, Mortal, Alu, Talenan, Timbangan, Panci stainless
steel, Kain saring, Plastik Poliethylen, Pisau stainless steel, Aluminium foil dan
Metode Penelitian
Penelitian ini menggunakan metode Rancangan Acak Lengkap (RAL)
faktorial yang terdiri dari 2 faktor, yaitu :
Faktor I : Konsentrasi Tapioka (P) (bk)
P1
Faktor II : Konsentrasi Sorbitol (S) (bk) = 7 % w/v
Banyaknya kombinasi perlakuan (Tc) adalah 4 x 4 = 16, maka jumlah ulangan
Model Rancangan
Penelitian ini dilakukan dengan Rancangan Acak Lengkap (RAL) faktorial
dengan model :
: Hasil pengamatan dari faktor P pada taraf ke-i dan faktor S pada taraf ke-j
dengan ulangan ke-k
: Efek interaksi faktor P pada taraf ke-i dan faktor S pada taraf ke-j
ijk
Apabila diperoleh hasil yang berbeda nyata atau sangat nyata maka
dilanjutkan dengan uji LSR (Least Significant Range).
: Efek galat dari faktor P pada taraf ke-i dan faktor S pada taraf ke-j dalam
ulangan ke-k
Pelaksanaan Penelitian Ekstraksi tapioka
Umbi ubi kayu segar dikupas, dicuci sampai bersih kemudian direndam
dalam larutan natrium metabisulfit 0,3 % selama 1 jam. Diparut hingga menjadi
bubur kasar. Kemudian ditambah air (untuk mengekstrak patinya) dengan
perbandingan 1 : 1 lalu diaduk-aduk. Selanjutnya disaring dengan kain saring dan
hasilnya disebut filtrat I. Ampas yang diperoleh ditambah air dengan
perbandingan yang sama dengan perbandingan sebelumnya dan disaring kembali
Penyaringan dilakukan berulang-ulang sampai hasil saringannya tampak
jernih. Hasil saringan (filtrat I dan filtrat II) kemudian diendapkan kurang lebih 3
jam. Air yang sudah bening dibuang dan endapan patinya diambil dan dikeringkan
dalam oven pada suhu 40o
Pembuatan edible coating
C selama 48 jam. Endapan yang telah kering diblender
dan diayak dengan ayakan 100 mesh. Pati yang telah dihasilkan disimpan dalam
wadah tertutup.
Ekstraksi pati sesuai perlakuan dilarutkan dalam 35 ml etanol 98 % dan
100 ml akuades. Setelah itu ditambah 2,5 gram CMC dan zat pemlastis sesuai
perlakuan, yaitu sorbitol. Diaduk sampai semuanya tercampur. Setelah itu
dipanaskan sampai suhu 80OC sambil diaduk selama 15 menit, kemudian
didinginkan sampai suhu 30O
Pencelupan buah melon pada edible coating
C dan ditambah antioksidan asam askorbat sebanyak
1,3 gram.
Disiapkan buah melon yang masih segar, kemudian buah dipisahkan dari
kulit dengan cara dikupas dan dipotong membentuk kubus. Buah yang telah
dipotong kemudian dicuci menggunakan air yang telah dimasak sebelumnya, lalu
diangkat dan ditiriskan. Kemudian dicelupkan ke dalam larutan edible coating
tersebut hingga merata. Kemudian dimasukkan dalam styrofoam dan ditutup
dengan poliethylen. Lalu disimpan dalam refrigerator selama kurang lebih 1
Pengamatan dan Pengukuran Data
Pengamatan dan pengukuran data dilakukan dengan cara analisis terhadap
parameter :
1. Penentuan kadar vitamin C
2. Penentuan susut bobot
3. Penentuan total asam
4. Penentuan total padatan terlarut
5. Organoleptik rasa dan tekstur
Penentuan kadar vitamin C (Sudarmadji, dkk., 1984)
Kandungan vitamin C ditentukan dengan cara titrasi yaitu diambil
sebanyak 10 g contoh yang telah dihaluskan, dimasukkan ke dalam beaker glass
ukuran 100 ml dan ditambahkan aquadest hingga 50 ml kemudian diaduk hingga
merata dan disaring dengan kertas saring. Filtrat diambil sebanyak 10 ml dengan
menggunakan gelas ukur kemudian dimasukkan ke dalam erlenmeyer dan
ditambahkan 2-3 tetes larutan pati 1% lalu dititrasi dengan menggunakan larutan
iodine 0,01 N hingga terjadi perubahan warna biru sambil dicatat berapa ml iodine
yang terpakai.
Kadar vitamin C dapat dihitung dengan menggunakan rumus yaitu :
ml iodine 0,01 N x 0,88 x FP x 100 Kadar vitamin C (mg/ 100 g bahan) =
Berat contoh (g)
Penentuan susut bobot
Pengukuran susut bobot dapat dilakukan dengan cara menimbang bahan
sebelum penyimpanan dan sesudah penyimpanan. Kemudian dilakukan
perhitungan sebagai berikut :
X – Y % Susut Bobot = x 100 %
X
Dimana :
X = Berat bahan sebelum penyimpanan
Y = Berat bahan setelah penyimpanan
Penentuan total asam (Ranganna, 1978)
Ditimbang contoh sebanyak 10 g yang telah dihaluskan, dimasukkan ke
dalam beaker glass dan ditambahi aquadest sampai volume 100 ml. Diaduk
hingga merata dan disaring dengan kain saring. Diambil filtratnya sebanyak 10 ml
dan dimasukkan ke dalam erlenmeyer lalu ditambahkan indikator phenolpthalein
1% sebanyak 2-3 tetes kemudian dititrasi dengan menggunakan NaOH 0,1 N.
Titrasi dihentikan setelah timbul warna merah jambu yang stabil.
Total asam dapat dihitung dengan menggunakan rumus yaitu :
ml NaOH x N NaOH x BM Asam Dominan x FP
Total Asam = x 100 %
Berat Contoh x 1000 x Valensi
Dimana :
FP = Faktor Pengencer (10)
Asam Dominan = Asam Tartarat (C4H6O6
BM = 150 g/ Mr
)
Penentuan total padatan terlarut (AOAC, 1970)
Buah melon dihaluskan terlebih dahulu. Diambil setetes larutan dan
diletakkan pada lensa hand-refraktometer. Lalu dilihat batas terang dan gelap.
Angka yang tertera pada batas tersebut merupakan nilai total padatan terlarut.
o
dimana FP = Faktor Pengencer (10) Brix = Nilai yang tertera x FP
Organoleptik rasa dan tekstur (Soekarto, 1985)
Uji organoleptik digunakan dengan menggunakan panelis sebanyak 10
orang. Pengujian dilakukan secara inderawi (organoleptik) yang ditentukan
berdasarkan skala numerik. Untuk skala uji hedonik rasa adalah sebagai berikut :
Tabel 2. Skala uji hedonik (Rasa)
Skala hedonik Skala numerik
Sangat suka 4
Suka 3
Agak suka 2
Tidak suka 1
Untuk skala uji hedonik tekstur adalah sebagai berikut :
Tabel 3. Skala uji hedonik (Tekstur)
Skala hedonik Skala numerik
Sangat lembut 4
Lembut 3
Agak keras 2
Ubi kayu segar
Pengupasan
Pencucian
Perendaman dalam larutan natrium metabisulfit 0,3 % selama 1 jam
Pemarutan
Bubur kasar
Penambahan air dengan perbandingan 1 : 1 sambil diaduk
Penyaringan
Filtrat I
Penyaringan
Filtrat II Ampas
Penyaringan sampai jernih
Pengendapan lebih kurang 3 jam
Pengeringan 40 oC, 48 jam
Penambahan air 1 : 1
Penghalusan
Pengayakan 100 mesh
Tapioka
Konsentrasi Tapioka:
P1 = 4 % w/v
P2 = 5 % w/v
P3 = 6 % w/v
P4 = 7 % w/v
Tapioka + 35 ml etanol 98 % + 100 ml akuades
Konsentrasi sorbitol :
S1 = 5 % w/v
S2 = 6 % w/v
S3 = 7 % w/v
S4 = 8 % w/v
Penambahan 2,5 gram CMC
Penambahan sorbitol
Pemanasan 80oC selama 15 menit sambil diaduk
Pendinginan hingga 30oC
Penambahan 1,3 gram asam askorbat
Edible coating
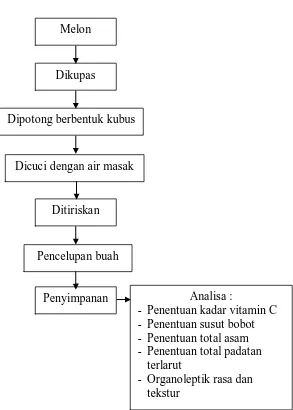
Analisa :
- Penentuan kadar vitamin C - Penentuan susut bobot - Penentuan total asam - Penentuan total padatan
terlarut
- Organoleptik rasa dan tekstur
Penyimpanan Melon
Dipotong berbentuk kubus Dikupas
Dicuci dengan air masak
Ditiriskan
Pencelupan buah
HASIL DAN PEMBAHASAN
Hasil penelitian menunjukkan bahwa konsentrasi tapioka dan konsentrasi
sorbitol memberikan pengaruh terhadap parameter yang diamati. Pengaruh
konsentrasi tapioka dan sorbitol terhadap parameter yang diamati dapat dijelaskan
di bawah ini.
Pengaruh Konsentrasi Tapioka terhadap Parameter yang Diamati
Hasil penelitian menunjukkan bahwa konsentrasi tapioka memberikan
pengaruh terhadap kadar vitamin C, susut bobot, total asam, total padatan terlarut
dan organoleptik warna dan tekstur dapat dilihat pada Tabel 4.
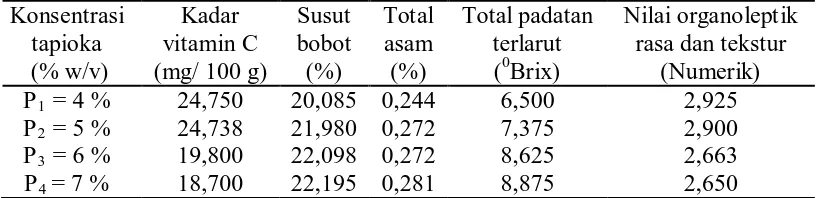
Tabel 4. Pengaruh konsentrasi tapioka terhadap parameter yang diamati
Konsentrasi
Dari Tabel dapat dilihat bahwa konsentrasi tapioka memberikan pengaruh
terhadap parameter yang diuji. Kadar vitamin C tertinggi terdapat pada perlakuan
konsentrasi tapioka 4 % w/v (P1) yaitu sebesar 24,750 mg/ 100 g bahan
dan terendah terdapat pada perlakuan konsentrasi tapioka 7 % w/v (P4) yaitu
sebesar 18,700 mg/ 100 g bahan. Susut bobot tertinggi terdapat pada perlakuan
konsentrasi tapioka 7 % w/v (P4) yaitu sebesar 22,195 % dan terendah terdapat
pada perlakuan konsentrasi tapioka 4 % w/v (P1) yaitu sebesar 20,085 %.
% w/v (P1) yaitu sebesar 0,244 %. Total padatan terlarut tertinggi terdapat pada
perlakuan konsentrasi tapioka 7 % w/v (P4) yaitu sebesar 8,875 0Brix dan
terendah terdapat pada perlakuan konsentrasi tapioka 4 % w/v (P1) yaitu sebesar
6,500 0Brix. Nilai organoleptik rasa dan tekstur tertinggi terdapat pada perlakuan
konsentrasi tapioka 4 % w/v (P1) yaitu sebesar 2,925 dan terendah terdapat pada
perlakuan konsentrasi tapioka 7 % w/v (P4) yaitu sebesar 2,650.
Pengaruh Konsentrasi Sorbitol terhadap Parameter yang Diamati
Hasil penelitian menunjukkan bahwa konsentrasi sorbitol memberikan
pengaruh terhadap kadar vitamin C, susut bobot, total asam, total padatan terlarut
dan organoleptik warna dan tekstur dapat dilihat pada Tabel 5.
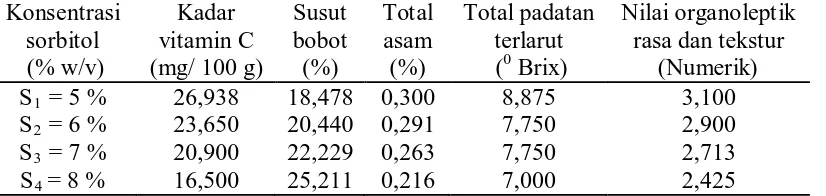
Tabel 5. Pengaruh konsentrasi sorbitol tehadap parameter yang diamati
Konsentrasi
Dari Tabel 5 dapat dilihat bahwa konsentrasi sorbitol memberikan
pengaruh terhadap parameter yang diuji. Kadar vitamin C tertinggi terdapat pada
perlakuan konsentrasi sorbitol 5 % w/v (S1) yaitu sebesar 26,938 mg/ 100 g bahan
dan terendah terdapat pada perlakuan konsentrasi sorbitol 8 % w/v (S4) yaitu
sebesar 16,500 mg/ 100 g bahan. Susut bobot tertinggi terdapat pada
perlakuan konsentrasi sorbitol 8 % w/v (S4) yaitu sebesar 25,211 % dan terendah
terdapat pada perlakuan konsentrasi sorbitol 5 % w/v (S1) yaitu sebesar 18,478 %.
Total asam tertinggi terdapat pada perlakuan konsentrasi sorbitol 5 % w/v (S1)
8 % w/v (S4) yaitu sebesar 0,216 %. Total padatan terlarut tertinggi terdapat pada
perlakuan konsentrasi sorbitol 5 % w/v (S1) yaitu sebesar 8,875 0Brix
dan terendah terdapat pada perlakuan konsentrasi sorbitol 8 % w/v (S4) yaitu
sebesar 7,000 0Brix. Nilai organoleptik rasa dan tekstur tertinggi terdapat pada
perlakuan konsentrasi sorbitol 5 % w/v (S1) yaitu sebesar 3,100 dan terendah
terdapat pada perlakuan konsentrasi sorbitol 8 % w/v (S4) yaitu sebesar 2,425.
Kadar Vitamin C
Pengaruh konsentrasi tapioka terhadap kadar vitamin C
Dari daftar analisis sidik ragam (Lampiran 1) dapat dilihat bahwa konsentrasi tapioka memberikan pengaruh berbeda sangat nyata (P<0,01)
terhadap kadar vitamin C. Hasil uji LSR pengaruh konsentrasi tapioka terhadap
kadar vitamin C dapat dilihat pada Tabel 6.
Tabel 6. Uji LSR efek utama pengaruh konsentrasi tapioka terhadap kadar vitamin C (mg/ 100 g)
Jarak LSR Konsentrasi Rataan Notasi
0,05 0,01 tapioka 0,05 0,01
- - - P1 = 4 % w/v 24,750 a A
2 2,327 3,203 P2 = 5 % w/v 24,738 a A
3 2,443 3,366 P3 = 6 % w/v 19,800 b B
4 2,505 3,452 P4 = 7 % w/v 18,700 b B
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% dan berbeda sangat nyata pada taraf 1%.
Dari Tabel 6 dapat dilihat bahwa perlakuan P1 berbeda tidak nyata dengan
perlakuan P2, namun berbeda sangat nyata dengan perlakuan P3 dan P4. Perlakuan
P2 berbeda sangat nyata dengan perlakuan P3 dan P4. Perlakuan P3 berbeda tidak
Kadar vitamin C tertinggi terdapat pada perlakuan konsentrasi tapioka 4 %
w/v (P1) yaitu sebesar 24,750 mg/ 100 g bahan dan yang terendah terdapat pada
perlakuan konsentrasi tapioka 7 % w/v (P4
Makin tinggi konsentrasi tapioka yang digunakan maka kadar vitamin C
dari bahan makin menurun dan tidak dapat dipertahankan. Penurunan ini
mengikuti garis regresi linier yang terlihat pada Gambar 5. Pantastico, (1997)
menyatakan bahwa apabila konsentrasi CO
) yaitu sebesar 18,700 mg/ 100 g bahan.
2
Pernyataan ini memperkuat dugaan bahwa makin tebalnya konsentrasi
tapioka yang digunakan, maka bahan akan mengalami proses respirasi anaerob
karena CO
yang dimiliki suatu bahan kemasan
tinggi, hal ini dapat mengakibatkan matinya sel-sel buah akibat terhambatnya
aktivitas enzim pada proses respirasi dan pembentukan asam organik.
2
Konsent rasi t apioka (% w/v)
K
yang dihasilkan dari proses respirasi menjadi terhambat
pengeluarannya akibat makin tebalnya lapisan film. Hal inilah yang membuat
kadar vitamin C bahan menjadi menurun. Hubungan antara konsentrasi tapioka
terhadap kadar vitamin C dapat dilihat pada Gambar 5.
Gambar 5. Grafik pengaruh konsentrasi tapioka terhadap kadar vitamin C
Pengaruh konsentrasi sorbitol terhadap kadar vitamin C
Dari daftar analisis sidik ragam (Lampiran 1) dapat dilihat bahwa
konsentrasi sorbitol memberikan pengaruh berbeda sangat nyata (P<0,01)
terhadap kadar vitamin C. Hasil uji LSR pengaruh konsentrasi sorbitol terhadap
kadar vitamin C yang dihasilkan dapat dilihat pada Tabel 7.
Tabel 7. Uji LSR efek utama pengaruh konsentrasi sorbitol terhadap kadar vitamin C (mg/ 100 g)
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% dan berbeda sangat nyata pada taraf 1%.
Dari Tabel 7 dapat dilihat bahwa perlakuan S1 berbeda nyata terhadap
perlakuan S2, berbeda sangat nyata dengan perlakuan S3 dan S4. Perlakuan S2
berbeda nyata dengan perlakuan S3 dan berbeda sangat nyata dengan perlakuan
S4. Perlakuan S3 berbeda sangat nyata dengan perlakuan S4
Kadar vitamin C tertinggi terdapat pada perlakuan konsentrasi tapioka 5 %
w/v (S
.
1) yaitu sebesar 26,938 mg/ 100 g bahan dan yang terendah terdapat pada
perlakuan konsentrasi tapioka 8 % w/v (S4
Makin tinggi konsentrasi sorbitol yang digunakan maka kadar vitamin C
dari bahan makin menurun. Penurunan ini mengikuti garis regresi linier yang
dapat dilihat pada Gambar 6. Hal diatas dapat terjadi karena ketebalan edible
coating dipengaruhi oleh konsentrasi sorbitol dimana makin tebal film, maka
bahan dapat mengalami respirasi anaerob karena CO
) yaitu sebesar 16,500 mg/ 100 g bahan.
2 yang dihasilkan dari proses
memperkuat dugaan diatas dimana apabila konsentrasi CO2
Hubungan antara konsentrasi sorbitol terhadap kadar vitamin C dapat
dilihat pada Gambar 6.
yang tinggi dalam
kemasan akan mengakibatkan matinya sel-sel buah akibat terhambatnya aktivitas
enzim pada proses respirasi dan pembentukan asam organik.
Ý = -3,4062S + 44,137
Konsent rasi sorbit ol (% w/v)
K Gambar 6. Grafik pengaruh konsentrasi sorbitol terhadap kadar vitamin C
Pengaruh interaksi antara konsentrasi tapioka dan sorbitol terhadap kadar vitamin C
Dari daftar analisis sidik ragam (Lampiran 1) menunjukkan bahwa
konsentrasi tapioka dan sorbitol memberikan pengaruh yang berbeda tidak nyata
(P>0,05) terhadap kadar vitamin C, sehingga uji LSR tidak dilanjutkan.
Susut Bobot
Pengaruh konsentrasi tapioka terhadap susut bobot
Dari daftar analisis sidik ragam (Lampiran 2) dapat dilihat bahwa
konsentrasi tapioka memberikan pengaruh berbeda sangat nyata (P<0,01)
terhadap susut bobot. Hasil uji LSR pengaruh konsentrasi tapioka terhadap susut
bobot yang dihasilkan dapat dilihat pada Tabel 8.
Tabel 8. Uji LSR efek utama pengaruh konsentrasi tapioka terhadap susut bobot (%)
Jarak LSR Konsentrasi Rataan Notasi
0,05 0,01 tapioka 0,05 0,01
- - - P1 = 4 % w/v 20,085 b B
2 0,715 0,985 P2 = 5 % w/v 21,980 a A
3 0,751 1,035 P3 = 6 % w/v 22,098 a A
4 0,770 1,061 P4 = 7 % w/v 22,195 a A
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% dan berbeda sangat nyata pada taraf 1%.
Dari Tabel 8 dapat dilihat bahwa perlakuan P1 berbeda sangat nyata
dengan perlakuan P2, P3 dan P4. Perlakuan P2 berbeda tidak nyata dengan
perlakuan P3 dan P4. Perlakuan P3 berbeda tidak nyata dengan perlakuan P4
Susut bobot tertinggi terdapat pada perlakuan konsentrasi tapioka 7 % w/v
(P
.
4) yaitu sebesar 22,195 % dan yang terendah terdapat pada konsentrasi tapioka
4 % w/v (P1
Makin tinggi konsentrasi tapioka maka susut susut bobot yang dihasilkan
menjadi makin meningkat. Hal ini disebabkan karena adanya perombakan gula
bahan melalui respirasi yang terjadi pada bahan. Dimana buah secara alami akan
mengalami proses respirasi setelah dipetik yang bertujuan untuk menghasilkan
energi yang akan dipakai dalam mempertahankan kehidupannya. ) yaitu sebesar 20,085 %.
Glukosa yang dirombak ini lambat laun akan habis dan buah mengalami
kebusukan akibat tidak adanya lagi kandungan gula yang dimiliki bahan sebagai
cadangan makanan. Proses inilah yang menjadi penyebab utama pengurangan
susut bobot yang dialami bahan. Pernyataan ini sesuai dengan pernyataan
Sjaifullah, (1996) yang menyatakan bahwa gula yang dihasilkan pada proses
Lama kelamaan buah akan kehabisan gula sebagai cadangan makanan, sehingga
berat buah berkurang akibat tidak adanya gula dan zat-zat penyusun buah tersebut.
Edible coating yang dibentuk dari tapioka mempunyai kelemahan dalam
menghambat atau mengatur migrasi uap air karena tapioka yang bersifat hidrofil
sehingga makin tinggi konsentrasi tapioka yang digunakan maka akan makin
banyak air yang hilang yang menyebabkan makin tingginya susut bobot bahan.
Hal ini sesuai dengan pernyataan Paramawati, (2001) yang mengungkapkan
bahwa pelapis yang dibuat dari hidrokoloid (tapioka) mempunyai beberapa
kekurangannya yaitu bungkus dari karbohidrat kurang bagus digunakan untuk
mengatur migrasi uap air. Hubungan antara konsentrasi tapioka terhadap susut
bobot dapat dilihat pada Gambar 7.
Ý = 0,6448P + 19,978
Konsent rasi t apioka (% w/v)
S
Gambar 7. Grafik pengaruh konsentrasi tapioka terhadap susut bobot
Pengaruh konsentrasi sorbitol terhadap susut bobot
Dari daftar analisis sidik ragam (Lampiran 2) dapat dilihat bahwa
konsentrasi sorbitol memberikan pengaruh berbeda sangat nyata (P<0,01)
terhadap susut bobot. Hasil uji LSR pengaruh konsentrasi sorbitol terhadap susut
bobot yang dihasilkan dapat dilihat pada Tabel 9.
Tabel 9. Uji LSR efek utama pengaruh konsentrasi sorbitol terhadap
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% dan berbeda sangat nyata pada taraf 1%.
Dari Tabel 9 dapat dilihat bahwa perlakuan S1 berbeda sangat nyata
dengan perlakuan S2, S3 dan S4. Perlakuan S2 berbeda sangat nyata dengan
perlakuan S3 dan S4. Perlakuan S3 berbeda sangat nyata dengan perlakuan S4
Susut bobot tertinggi terdapat pada perlakuan konsentrasi sorbitol 8 % w/v
(S
.
4) yaitu sebesar 25,211 % dan yang terendah terdapat pada konsentrasi sorbitol
5 % w/v (S1
Makin tinggi konsentrasi sorbitol yang digunakan maka susut bobot yang
dihasilkan menjadi makin tinggi. Peningkatan ini mengikuti garis regresi linier
seperti pada Gambar 8. Hal ini disebabkan sifat sorbitol yang menurunkan sifat
barrier film sehingga kemampuan migrasi uap air bahan menjadi meningkat.
Dimana Teknopangan dan Agroindustri, (2008) berpendapat bahwa penambahan
plasticizer dapat meningkatkan fleksibilitas film namun dapat menurunkan sifat
barrier film. Dengan makin rendahnya sifat barrier film, maka kemampuan
migrasi uap air film menjadi meningkat yang berpengaruh besar terhadap
Hubungan antara konsetrasi sorbitol terhadap susut bobot dapat dilihat
pada Gambar 8.
Ý = 2,199S + 16,092 r = 0,9927
16,000 18,000 20,000 22,000 24,000 26,000
4 5 6 7 8 9
Konsent rasi sorbit ol (% w/v)
S
us
ut
bobot
(
%
)
Gambar 8. Grafik pengaruh konsentrasi sorbitol terhadap susut bobot
Pengaruh interaksi antara konsentrasi tapioka dan sorbitol terhadap susut bobot
Dari daftar analisis sidik ragam (Lampiran 2) menunjukkan bahwa
konsentrasi tapioka dan sorbitol memberikan pengaruh yang berbeda sangat nyata
(P<0,01) terhadap susut bobot yang dihasilkan.
Hasil pengujian LSR pengaruh interaksi antara konsentrasi tapioka dan
sorbitol terhadap susut bobot yang dihasilkan dapat dilihat pada Tabel 10.
Tabel 10. Uji LSR efek utama pengaruh interaksi konsentrsi tapioka dan sorbitol terhadap susut bobot (%)
Keterangan : Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% dan berbeda sangat nyata pada taraf 1%.
Dari Tabel 10 dapat dilihat bahwa kombinasi perlakuan antara konsentrasi
tapioka dan sorbitol memberikan pengaruh berbeda sangat nyata terhadap susut
bobot. Susut bobot tertinggi terdapat pada perlakuan interaksi antara konsentrasi
tapioka 7 % w/v dan sorbitol 8 % w/v (P4S4) adalah sebesar 26,255 % dan
terendah terdapat pada perlakuan interaksi antara konsentrasi tapioka 4 % w/v dan
sorbitol 5 % w/v (P1S1
Makin tinggi konsentrasi tapioka dan sorbitol maka susut bobot yang
dihasilkan makin meningkat. Peningkatan ini mengikuti garis regresi linier seperti
Gambar 9. Hal ini disebabkan karena makin tinggi konsentrasi sorbitol maka sifat
barrier film makin menurun, yang kemudian diikuti dengan kemampuan migrasi
uap air film yang juga akan makin tinggi, sehingga pada akhirnya berpengaruh